DE112010001236B4 - Organische elektrolumineszenzvorrichtung - Google Patents
Organische elektrolumineszenzvorrichtung Download PDFInfo
- Publication number
- DE112010001236B4 DE112010001236B4 DE112010001236.9T DE112010001236T DE112010001236B4 DE 112010001236 B4 DE112010001236 B4 DE 112010001236B4 DE 112010001236 T DE112010001236 T DE 112010001236T DE 112010001236 B4 DE112010001236 B4 DE 112010001236B4
- Authority
- DE
- Germany
- Prior art keywords
- aromatic
- occurrence
- ring system
- radicals
- carbon atoms
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/321—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3]
- H10K85/322—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3] comprising boron
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/346—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising platinum
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/658—Organoboranes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/30—Highest occupied molecular orbital [HOMO], lowest unoccupied molecular orbital [LUMO] or Fermi energy values
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Inorganic Chemistry (AREA)
- Optics & Photonics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Organische Elektrolumineszenzvorrichtung, enthaltend Anode, Kathode und mindestens eine emittierende Schicht, welche mindestens eine phosphoreszierende Verbindung enthält, welche in eine Mischung aus zwei Materialien A und B eingebracht ist, wobei die Materialien A und B definierte niedermolekulare Verbindungen mit einer Molmasse von 2000 g/mol oder weniger sind, wobei das Material A ein elektronentransportierendes Material ist, welche ausgewählt ist aus der Gruppe bestehend aus aromatischen Ketonen, aromatischen Phosphinoxiden, aromatischen Sulfoxiden, aromatischen Sulfonen, Triazinderivaten, Zink-Komplexen und Aluminium-Komplexen, und wobei das Material B ein Material ist, welches nicht am Ladungstransport beteiligt ist, welches ein HOMO von -5,4 eV oder weniger und ein LUMO von -2,4 eV oder mehr aufweist, und welches eine Energielücke von mindestens 3,5 eV aufweist, und welches ausgewählt ist aus Verbindungen der Formeln (23), (24) und (25),wobeiAr ist bei jedem Auftreten gleich oder verschieden ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches jeweils mit einer oder mehreren Gruppen R1substituiert sein kann;R1ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, CHO, C(=O)Ar1, P(=O)(Ar1)2, S(=O)Ar1, S(=O)2Ar1, CR2=CR2Ar1, CN, NO2, Si(R2)3, B(OR2)2, B(R2)2, B(N(R2)2)2, OSO2R2, eine geradkettige Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 1 bis 40 C-Atomen oder eine geradkettige Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkenyl-, Alkinyl-, Alkoxy- oder Thioalkoxygruppe mit 3 bis 40 C-Atomen, die jeweils mit einem oder mehreren Resten R2substituiert sein kann, wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch R2C=CR2, C=C , Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S oder CONR2ersetzt sein können und wobei ein oder mehrere H-Atome durch F, Cl, Br, I, CN oder NO2ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R2substituiert sein kann, oder eine Aryloxy- oder Heteroaryloxygruppe mit 5 bis 60 aromatischen Ringatomen, die durch einen oder mehrere Reste R2substituiert sein kann, oder eine Kombination dieser Systeme; dabei können zwei oder mehrere benachbarte Substituenten R1auch miteinander ein mono- oder polycyclisches, aliphatisches oder aromatisches Ringsystem bilden;Ar1ist bei jedem Auftreten gleich oder verschieden ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 40 aromatischen Ringatomen, das mit einem oder mehreren Resten R2substituiert sein kann;R2ist bei jedem Auftreten gleich oder verschieden H, D, CN oder ein aliphatischer, aromatischer und/oder heteroaromatischer Kohlenwasserstoffrest mit 1 bis 20 C-Atomen, in dem auch H-Atome durch F ersetzt sein können; dabei können zwei oder mehrere benachbarte Substituenten R2auch miteinander ein mono- oder polycyclisches, aliphatisches oder aromatisches Ringsystem bilden;n ist gleich oder verschieden bei jedem Auftreten 0 oder 1;R3ist bei jedem Auftreten gleich oder verschieden eine geradkettige Alkylgruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkylgruppe mit 3 bis 20 C-Atomen, oder ein aromatisches Ringsystem mit 6 bis 60 aromatischen C-Atomen, welches keine nicht-aromatischen Gruppen ungleich Kohlenstoff oder Wasserstoff enthält und welches durch einen oder mehrere Reste R4substituiert sein kann; dabei können zwei oder mehrere Reste R3auch miteinander ein Ringsystem bilden;R4ist bei jedem Auftreten gleich oder verschieden eine geradkettige Alkylgruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkylgruppe mit 3 bis 20 C-Atomen; dabei können zwei oder mehrere Reste R4auch miteinander ein Ringsystem bilden;q ist 1, 2, 3 oder 4.
Description
- Die vorliegende Erfindung betrifft organische Elektrolumineszenzvorrichtungen, welche mindestens eine Schicht mit mindestens einem phosphoreszierenden Dotanden und mindestens zwei Matrixmaterialien enthalten.
- Der Aufbau organischer Elektrolumineszenzvorrichtungen (OLEDs), in denen organische Halbleiter als funktionelle Materialien eingesetzt werden, ist beispielsweise in
US 4 539 507 A ,US 5 151 629 A ,EP 0 676 461 A2 undWO 98/ 27 136 A1 - Allerdings gibt es bei phosphoreszierenden OLEDs noch Verbesserungsbedarf. Dies gilt insbesondere für die Effizienz und die Lebensdauer der Vorrichtung.
- Die der vorliegenden Erfindung zugrunde liegende technische Aufgabe besteht daher darin, eine phosphoreszierende organische Elektrolumineszenzvorrichtung bereitzustellen, welche eine verbesserte Lebensdauer aufweist. Eine weitere Aufgabe besteht darin, eine phosphoreszierende organische Elektrolumineszenzvorrichtung bereitzustellen, welche eine verbesserte Effizienz aufweist.
- Gemäß dem Stand der Technik werden elektronenleitende Materialien, unter anderem Ketone (z.B. gemäß
WO 2004/ 093 207 A2 DE 10 2008 033 943 A1 ) oder Triazinderivate (z. B. gemäßDE 10 2008 036 982 A1 ) als Matrixmaterialien für phosphoreszierende Emitter verwendet. Insbesondere mit Ketonen werden niedrige Betriebsspannungen und lange Lebensdauern erzielt, was diese Verbindungsklasse zu einem sehr interessanten Matrixmaterial macht. Allerdings besteht bei Verwendung dieser Matrixmaterialien ebenso wie bei anderen Matrixmaterialien noch Verbesserungsbedarf, insbesondere in Bezug auf die Effizienz und die Lebensdauer der Vorrichtung. - Aus dem Stand der Technik sind weiterhin organische Elektrolumineszenzvorrichtungen bekannt, welche einen phosphoreszierenden Emitter dotiert in eine Mischung aus zwei Matrixmaterialien enthalten.
- In der
US 2007 / 0 252 516 A1 US 2007 / 0 015 005 A1 US 2009 / 0 026 937 A1 - In der
US 2007 / 0 099 026 A1 - Überraschend wurde gefunden, dass sich sowohl die Effizienz wie auch die Lebensdauer einer phosphoreszierenden organischen Elektrolumineszenzvorrichtung auf Basis niedermolekularer Moleküle (so genannte Small Molecules) deutlich verbessert, wenn in der emittierenden Schicht als Matrix für den phosphoreszierenden Emitter eine Mischung aus mindestens zwei Matrixmaterialien verwendet wird, wobei eines der beiden Matrixmaterialien ein Material ist, welches in der Lage ist, Ladungen zu transportieren, hier ein Elektronentransportmaterial, und das andere der beiden Matrixmaterialien ein Material ist, welches so gewählt ist, dass es nicht am Ladungstransport beteiligt ist. Dies erreicht man durch Materialien, in denen die Lage des HOMO (höchstes besetztes Molekülorbital) und des LUMO (niedrigstes unbesetztes Molekülorbital) sowie die Energielücke (Bandgap) entsprechend gewählt wird. Mit derartigen Elektrolumineszenzvorrichtungen werden bessere Ergebnisse, insbesondere in Bezug auf Effizienz und Lebensdauer, erzielt als mit Elektrolumineszenzvorrichtungen, welche als Matrix für den phosphoreszierenden Emitter eine Mischung aus einem elektronentransportierenden und einem lochtransportierenden Material enthalten.
- Gegenstand der Erfindung ist somit eine organische Elektrolumineszenzvorrichtung, enthaltend Anode, Kathode und mindestens eine emittierende Schicht, welche mindestens eine phosphoreszierende Verbindung enthält, welche in eine Mischung aus zwei Materialien A und B eingebracht ist, wobei diese Materialien definierte niedermolekulare Verbindungen mit einer Molmasse von 2000 g/mol oder weniger sind, dadurch gekennzeichnet, dass das Material A ein elektronentransportierendes Material ist und dass das Material B ein Material ist, welches ein HOMO von -5.4 eV oder weniger und ein LUMO von -2.4 eV oder mehr aufweist, und welches eine Energielücke von mindestens 3.5 eV aufweist. Das Material B ist nicht am Ladungstransport beteiligt.
- Das Material A ist aus der Gruppe bestehend aus aromatischen Ketonen, aromatischen Phosphinoxiden, aromatischen Sulfoxiden, aromatischen Sulfonen, Triazinderivaten, Zink-Komplexen und Aluminium-Komplexen ausgewählt.
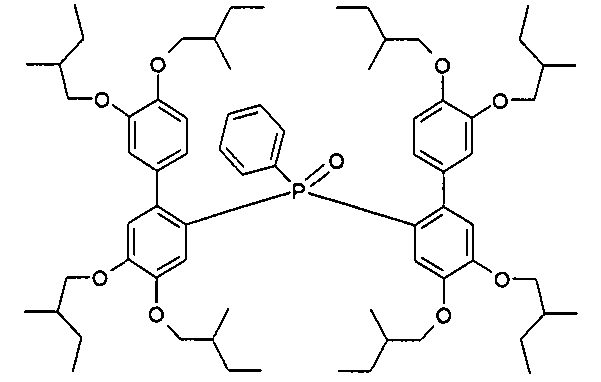
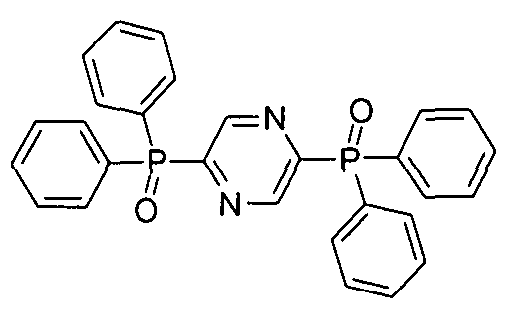
- Das Material B ist aus Verbindungen der Formeln (23), (24) und (25) ausgewählt:
Ar ist bei jedem Auftreten gleich oder verschieden ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches jeweils mit einer oder mehreren Gruppen R1 substituiert sein kann;
R1 ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, CHO, C(=O)Ar1, P(=O)(Ar1)2, S(=O)Ar1, S(=O)2Ar1, CR2=CR2Ar1, CN, NO2, Si(R2)3, B(OR2)2, B(R2)2, B(N(R2)2)2, OSO2R2, eine geradkettige Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 1 bis 40 C-Atomen oder eine geradkettige Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkenyl-, Alkinyl-, Alkoxy- oder Thioalkoxygruppe mit 3 bis 40 C-Atomen, die jeweils mit einem oder mehreren Resten R2 substituiert sein kann, wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch R2C=CR2, C=C , Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S oder CONR2 ersetzt sein können und wobei ein oder mehrere H-Atome durch F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R2 substituiert sein kann, oder eine Aryloxy- oder Heteroaryloxygruppe mit 5 bis 60 aromatischen Ringatomen, die durch einen oder mehrere Reste R2 substituiert sein kann, oder eine Kombination dieser Systeme; dabei können zwei oder mehrere benachbarte Substituenten R1 auch miteinander ein mono- oder polycyclisches, aliphatisches oder aromatisches Ringsystem bilden;
Ar1 ist bei jedem Auftreten gleich oder verschieden ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 40 aromatischen Ringatomen, das mit einem oder mehreren Resten R2 substituiert sein kann;
R2 ist bei jedem Auftreten gleich oder verschieden H, D, CN oder ein aliphatischer, aromatischer und/oder heteroaromatischer Kohlenwasserstoffrest mit 1 bis 20 C-Atomen, in dem auch H-Atome durch F ersetzt sein können; dabei können zwei oder mehrere benachbarte Substituenten R2 auch miteinander ein mono- oder polycyclisches, aliphatisches oder aromatisches Ringsystem bilden;
n ist gleich oder verschieden bei jedem Auftreten 0 oder 1;
R3 ist bei jedem Auftreten gleich oder verschieden eine geradkettige Alkylgruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkylgruppe mit 3 bis 20 C-Atomen, oder ein aromatisches Ringsystem mit 6 bis 60 aromatischen C-Atomen, welches keine nicht-aromatischen Gruppen ungleich Kohlenstoff oder Wasserstoff enthält und welches durch einen oder mehrere Reste R4 substituiert sein kann; dabei können zwei oder mehrere Reste R3 auch miteinander ein Ringsystem bilden;
R4 ist bei jedem Auftreten gleich oder verschieden eine geradkettige Alkylgruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkylgruppe mit 3 bis 20 C-Atomen; dabei können zwei oder mehrere Reste R4 auch miteinander ein Ringsystem bilden;
q ist 1, 2, 3 oder 4. - Die Materialien A und B sind dabei die Matrixmaterialien für die phosphoreszierende Verbindung und sind selber nicht an der Emission der Elektrolumineszenzvorrichtung beteiligt.
- Ein lochtransportierendes Material im Sinne dieser Anmeldung ist charakterisiert durch ein HOMO von mehr als -5.4 eV. Ein elektronentransportierendes Material im Sinne dieser Anmeldung ist charakterisiert durch ein LUMO von weniger als -2.4 eV. Dabei erfolgt die Bestimmung der HOMO- und LUMO-Lagen und der Energielücke so, wie im Beispielteil ausführlich allgemein beschrieben.
- Die erfindungsgemäße organische Elektrolumineszenzvorrichtung enthält, wie oben beschrieben, Anode, Kathode und mindestens eine emittierende Schicht, welche zwischen der Anode und der Kathode angeordnet ist. Dabei enthält die emittierende Schicht mindestens eine phosphoreszierende Verbindung und weiterhin mindestens ein Elektronentransportierendes Matrixmaterial und ein weiteres Matrixmaterial mit einem HOMO von -5.4 eV oder weniger, einem LUMO von -2.4 eV oder mehr und einer Energielücke von 3.5 eV oder mehr. Die organische Elektrolumineszenzvorrichtung muss nicht notwendigerweise nur Schichten enthalten, welche aus organischen oder metallorganischen Materialien aufgebaut sind. So ist es auch möglich, dass Anode, Kathode und/oder eine oder mehrere Schichten anorganische Materialien enthalten oder ganz aus anorganischen Materialien aufgebaut sind.
- Eine phosphoreszierende Verbindung im Sinne dieser Erfindung ist eine Verbindung, welche bei Raumtemperatur Lumineszenz aus einem angeregten Zustand mit höherer Spinmultiplizität zeigt, also einem Spinzustand > 1, insbesondere aus einem angeregten Triplettzustand. Im Sinne dieser Erfindung sollen alle lumineszierenden Übergangsmetallkomplexe, insbesondere alle lumineszierenden Iridium-, Platin- und Kupferverbindungen als phosphoreszierende Verbindungen angesehen werden.
- In einer bevorzugten Ausführungsform der Erfindung handelt es sich bei der phosphoreszierenden Verbindung um eine rot phosphoreszierende Verbindung oder um eine grün phosphoreszierende Verbindung.
- Bevorzugt weisen die Matrixmaterialien A und B eine Glasübergangstemperatur TG von größer als 70 °C auf, besonders bevorzugt größer als 90 °C, ganz besonders bevorzugt größer als 110 °C.
- Der Anteil der phosphoreszierenden Verbindung in der emittierenden Schicht beträgt bevorzugt 1 bis 50 Vol.-%, besonders bevorzugt 3 bis 30 Vol.-%, ganz besonders bevorzugt 5 bis 25 Vol.-%, insbesondere 10 bis 20 Vol.-%.
- Das Verhältnis zwischen dem Matrixmaterial A und dem Matrixmaterial B kann variieren. Insbesondere kann durch Variation dieses Verhältnisses die Ladungsbalance der OLED einfach und reproduzierbar eingestellt werden. Durch das Einstellen des Mischungsverhältnisses lässt sich somit leicht die Effizienz der OLED optimieren. Dabei beträgt das Mischungsverhältnis zwischen der dem Elektronentransportierenden Matrixmaterial A und dem Matrixmaterial B im Allgmeinen von 10:1 bis 1:10, bevorzugt von 7:1 bis 1:7, besonders bevorzugt von 4:1 bis 1:4, jeweils bezogen auf das Volumen.
- Im Folgenden werden bevorzugte Ausführungsformen für das Elektronentransportierende Matrixmaterial A und das Matrixmaterial B sowie für die phosphoreszierende Verbindung, welche erfindungsgemäß in der emitterenden Schicht vorhanden sind, ausgeführt.
- Unter einem aromatischen Keton im Sinne dieser Anmeldung wird eine Carbonylgruppe verstanden, an die zwei aromatische oder heteroaromatische Gruppen bzw. aromatische oder heteroaromatische Ringsysteme direkt gebunden sind. Aromatische Sulfone und Sulfoxide sind entsprechend definiert. Unter einem aromatischen Phosphinoxid im Sinne dieser Anmeldung wird eine Phosphinoxidgruppe verstanden, an die drei aromatische oder heteroaromatische Gruppen bzw. aromatische oder heteroaromatische Ringsysteme direkt gebunden sind.
-
- Eine Arylgruppe im Sinne dieser Erfindung enthält mindestens 6 C-Atome; eine Heteroarylgruppe im Sinne dieser Erfindung enthält mindestens 2 C-Atome und mindestens 1 Heteroatom, mit der Maßgabe, dass die Summe aus C-Atomen und Heteroatomen mindestens 5 ergibt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Dabei wird unter einer Arylgruppe bzw. Heteroarylgruppe entweder ein einfacher aromatischer Cyclus, also Benzol, bzw. ein einfacher heteroaromatischer Cyclus, beispielsweise Pyridin, Pyrimidin, Thiophen, etc., oder eine kondensierte Aryl- oder Heteroarylgruppe, beispielsweise Naphthalin, Anthracen, Pyren, Chinolin, Isochinolin, etc., verstanden.
- Ein aromatisches Ringsystem im Sinne dieser Erfindung enthält mindestens 6 C-Atome im Ringsystem. Ein heteroaromatisches Ringsystem im Sinne dieser Erfindung enthält mindestens 2 C-Atome und mindestens ein Heteroatom im Ringsystem, mit der Maßgabe, dass die Summe aus C-Atomen und Heteroatomen mindestens 5 ergibt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Unter einem aromatischen oder heteroaromatischen Ringsystem im Sinne dieser Erfindung soll ein System verstanden werden, das nicht notwendigerweise nur Aryl- oder Heteroarylgruppen enthält, sondern in dem auch mehrere Aryl- oder Heteroarylgruppen durch eine kurze, nicht-aromatische Einheit (bevorzugt weniger als 10 % der von H verschiedenen Atome), wie z. B. ein sp3-hybridisiertes C-, N- oder O-Atom oder eine Carbonylgruppe, unterbrochen sein können. So sollen beispielsweise auch Systeme wie 9,9'-Spirobifluoren, 9,9-Diarylfluoren, Triarylamin, Diarylether, Stilben, Benzophenon, etc. als aromatische Ringsysteme im Sinne dieser Erfindung verstanden werden. Ebenso werden unter einem aromatischen bzw. heteroaromatischen Ringsystem Systeme verstanden, in denen mehrere Aryl- bzw. Heteroarylgruppen durch Einfachbindungen miteinander verknüpft sind, beispielsweise Biphenyl, Terphenyl oder Bipyridin.
- Im Rahmen der vorliegenden Erfindung werden unter einer C1- bis C40-Alkylgruppe, in der auch einzelne H-Atome oder CH2-Gruppen durch die oben genannten Gruppen substituiert sein können, besonders bevorzugt die Reste Methyl, Ethyl, n-Propyl, i-Propyl, n-Butyl, i-Butyl, s-Butyl, t-Butyl, 2-Methylbutyl, n-Pentyl, s-Pentyl, t-Pentyl, 2-Pentyl, neo-Pentyl, Cyclopentyl, n-Hexyl, s-Hexyl, t-Hexyl, 2-Hexyl, 3-Hexyl, neo-Hexyl, Cyclohexyl, 2-Methylpentyl, n-Heptyl, 2-Heptyl, 3-Heptyl, 4-Heptyl, Cycloheptyl, 1-Methylcyclohexyl, n-Octyl, 2-Ethylhexyl, Cyclooctyl, 1-Bicyclo[2,2,2]octyl, 2-Bicyclo[2,2,2]octyl, 2-(2,6-Dimethyl)octyl, 3-(3,7-Dimethyl)octyl, Trifluormethyl, Pentafluorethyl und 2,2,2-Trifluorethyl verstanden. Unter einer unter einer C2- bis C40-Alkenylgruppe werden bevorzugt Ethenyl, Propenyl, Butenyl, Pentenyl, Cyclopentenyl, Hexenyl, Cyclohexenyl, Heptenyl, Cycloheptenyl, Octenyl und Cyclooctenyl verstanden. Unter einer unter einer C2- bis C40-Alkinylgruppe werden bevorzugt Ethinyl, Propinyl, Butinyl, Pentinyl, Hexinyl, Heptinyl und Octinyl verstanden. Unter einer C1- bis C40-Alkoxygruppe werden bevorzugt Methoxy, Trifluormethoxy, Ethoxy, n-Propoxy, i-Propoxy, n-Butoxy, i-Butoxy, s-Butoxy, t-Butoxy oder 2-Methylbutoxy verstanden. Unter einem aromatischen oder heteroaromatischen Ringsystem mit 5-60 aromatischen Ringatomen, welches noch jeweils mit den oben genannten Resten R substituiert sein kann und welches über beliebige Positionen am Aromaten bzw. Heteroaromaten verknüpft sein kann, werden insbesondere Gruppen verstanden, die abgeleitet sind von Benzol, Naphthalin, Anthracen, Phenanthren, Benzanthracen, Benzphenanthren, Pyren, Chrysen, Perylen, Fluoranthen, Benzfluoranthen, Naphthacen, Pentacen, Benzpyren, Biphenyl, Biphenylen, Terphenyl, Terphenylen, Fluoren, Benzofluoren, Dibenzofluoren, Spirobifluoren, Dihydrophenanthren, Dihydropyren, Tetrahydropyren, cis- oder trans-Indenofluoren, cis- oder trans-Monobenzoindenofluoren, cis- oder trans-Dibenzoindenofluoren, Truxen, Isotruxen, Spirotruxen, Spiroisotruxen, Furan, Benzofuran, Isobenzofuran, Dibenzofuran, Thiophen, Benzothiophen, Isobenzothiophen, Dibenzothiophen, Pyrrol, Indol, Isoindol, Carbazol, Pyridin, Chinolin, Isochinolin, Acridin, Phenanthridin, Benzo-5,6-chinolin, Benzo-6,7-chinolin, Benzo-7,8-chinolin, Phenothiazin, Phenoxazin, Pyrazol, Indazol, Imidazol, Benzimidazol, Naphthimidazol, Phenanthrimidazol, Pyridimidazol, Pyrazinimidazol, Chinoxalinimidazol, Oxazol, Benzoxazol, Naphthoxazol, Anthroxazol, Phenanthroxazol, Isoxazol, 1,2-Thiazol, 1,3-Thiazol, Benzothiazol, Pyridazin, Benzopyridazin, Pyrimidin, Benzpyrimidin, Chinoxalin, 1,5-Diazaanthracen, 2,7-Diazapyren, 2,3-Diazapyren, 1,6-Diazapyren, 1,8-Diazapyren, 4,5-Diazapyren, 4,5,9,10-Tetraazaperylen, Pyrazin, Phenazin, Phenoxazin, Phenothiazin, Fluorubin, Naphthyridin, Azacarbazol, Benzocarbolin, Phenanthrolin, 1,2,3-Triazol, 1,2,4-Triazol, Benzotriazol, 1,2,3-Oxadiazol, 1,2,4-Oxadiazol, 1,2,5-Oxadiazol, 1,3,4-Oxadiazol, 1,2,3-Thiadiazol, 1,2,4-Thiadiazol, 1,2,5-Thiadiazol, 1,3,4-Thiadiazol, 1,3,5-Triazin, 1,2,4-Triazin, 1,2,3-Triazin, Tetrazol, 1,2,4,5-Tetrazin, 1,2,3,4-Tetrazin, 1,2,3,5-Tetrazin, Purin, Pteridin, Indolizin und Benzothiadiazol.
- Geeignete Verbindungen gemäß Formel (1a) sind insbesondere die in
WO 2004/ 093 207 A2 DE 10 2008 033 943 A1 offenbarten Ketone und geeignete Verbindungen gemäß Formel (1b) sind die inWO 2005/ 003 253 A2 - Aus der Definition der Verbindung gemäß Formel (1a) und (1b) geht hervor, dass diese nicht nur eine Carbonyl- bzw. Phosphinoxidgruppe enthalten muss, sondern auch mehrere dieser Gruppen enthalten kann.
- Bevorzugt ist die Gruppe Ar in Verbindungen gemäß Formel (1a) und (1b) ein aromatisches Ringsystem mit 6 bis 40 aromatischen Ringatomen, d. h. sie enthält keine Heteroarylgruppen. Wie oben definiert, muss das aromatische Ringsystem nicht notwendigerweise nur aromatische Gruppen aufweisen, sondern es können auch zwei Arylgruppen durch eine nicht-aromatische Gruppe, beispielsweise durch eine weitere Carbonylgruppe bzw. Phosphinoxidgruppe unterbrochen sein.
- In einer weiteren bevorzugten Ausführungsform der Erfindung weist die Gruppe Ar nicht mehr als zwei kondensierte Ringe auf. Sie ist also bevorzugt nur aus Phenyl- und/oder Naphthylgruppen, besonders bevorzugt nur aus Phenylgruppen, aufgebaut, enthält aber keine größeren kondensierten Aromaten, wie beispielsweise Anthracen.
- Bevorzugte Gruppen Ar, die an die Carbonylgruppe gebunden sind, sind Phenyl, 2-, 3- oder 4-Tolyl, 3- oder 4-o-Xylyl, 2- oder 4-m-Xylyl, 2-p-Xylyl, o-, m- oder p-tert-Butylphenyl, o-, m- oder p-Fluorphenyl, Benzophenon, 1-, 2- oder 3-Phenylmethanon, 2-, 3- oder 4-Biphenyl, 2-, 3- oder 4-o-Terphenyl, 2-, 3- oder 4-m-Terphenyl, 2-, 3- oder 4-p-Terphenyl, 2'-p-Terphenyl, 2'-, 4'- oder 5'-m-Terphenyl, 3'- oder 4'-o-Terphenyl, p-, m,p-, o,p-, m,m-, o,m- oder o,o-Quaterphenyl, Quinquephenyl, Sexiphenyl, 1-, 2-, 3- oder 4-Fluorenyl, 2-, 3- oder 4-Spiro-9,9'-bifluorenyl, 1-, 2-, 3- oder 4-(9,10-Dihydro)phenanthrenyl, 1- oder 2-Naphthyl, 2-, 3-, 4-, 5-, 6-, 7- oder 8-Chinolinyl, 1-, 3-, 4-, 5-, 6-, 7- oder 8-iso-Chinolinyl, 1- oder 2-(4-Methylnaphthyl), 1- oder 2-(4-Phenylnaphthyl), 1- oder 2-(4-naphthyl-naphthyl), 1-, 2- oder 3-(4-naphthyl-phenyl), 2-, 3- oder 4-Pyridyl, 2-, 4- oder 5-Pyrimidinyl, 2- oder 3-Pyrazinyl, 3- oder 4-Pyridanzinyl, 2-(1,3,5-Triazin)yl-, 2-, 3- oder 4-(Phenylpyridyl), 3-, 4-, 5- oder 6-(2,2'-Bipyridyl), 2-, 4-, 5- oder 6-(3,3'-Bipyridyl), 2- oder 3-(4,4'-Bipyridyl) und Kombinationen eines oder mehrerer dieser Reste.
- Die Gruppen Ar können, wie oben beschrieben, durch einen oder mehrere Reste R1 substituiert sein. Diese Reste R1 sind bevorzugt gleich oder verschieden bei jedem Auftreten gewählt aus der Gruppe bestehend aus H, F, C(=O)Ar1, P(=O)(Ar1)2, S(=O)Ar1, S(=O)2Ar1, einer geradkettigen Alkylgruppe mit 1 bis 4 C-Atomen oder einer verzweigten oder cyclischen Alkylgruppe mit 3 bis 5 C-Atomen, die jeweils mit einem oder mehreren Resten R2 substituiert sein kann, wobei ein oder mehrere H-Atome durch F ersetzt sein können, oder einem aromatischen Ringsystem mit 6 bis 24 aromatischen Ringatomen, das durch einen oder mehrere Reste R2 substituiert sein kann, oder eine Kombination dieser Systeme; dabei können zwei oder mehrere benachbarte Substituenten R1 auch miteinander ein mono- oder polycyclisches, aliphatisches oder aromatisches Ringsystem bilden. Wenn die organische Elektrolumineszenzvorrichtung aus Lösung aufgebracht wird, sind auch geradkettige, verzweigte oder cyclische Alkylgruppen mit bis zu 10 C-Atomen als Substituenten R1 bevorzugt. Die Reste R1 sind besonders bevorzugt gleich oder verschieden bei jedem Auftreten gewählt aus der Gruppe bestehend aus H, C(=O)Ar1 oder einem aromatischen Ringsystem mit 6 bis 24 aromatischen Ringatomen, das durch einen oder mehrere Reste R2 substituiert sein kann, bevorzugt aber unsubstituiert ist.
- In nochmals einer bevorzugten Ausführungsform der Erfindung ist die Gruppe Ar1 gleich oder verschieden bei jedem Auftreten ein aromatisches Ringsystem mit 6 bis 24 aromatischen Ringatomen, das mit einem oder mehreren Resten R2 substituiert sein kann. Besonders bevorzugt ist Ar1 gleich oder verschieden bei jedem Auftreten ein aromatisches Ringsystem mit 6 bis 12 aromatischen Ringatomen.
- Besonders bevorzugte aromatische Ketone sind Benzophenon-Derivate, die jeweils an den 3,5,3',5'-Positionen durch ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 30 aromatischen Ringatomen substituiert sind, welche wiederum durch einen oder mehrere Reste R1 gemäß der obigen Definition substituiert sein kann. Weiterhin bevorzugt sind Ketone und Phosphinoxide, welche mit mindestens einer Spirobifluorengruppe substituiert sind.
-
- Z
- ist gleich oder verschieden bei jedem Auftreten CR1 oder N;
- n
- ist gleich oder verschieden bei jedem Auftreten 0 oder 1.
- Bevorzugt steht Ar in der oben genannten Formel (2), (4) und (5) für ein aromatisches oder heteroaromatisches Ringsystem mit 1 bis 30 aromatischen Ringatomen, welches mit einem oder mehreren Resten R1 substituiert sein kann. Besonders bevorzugt sind die oben genannten Gruppen Ar.
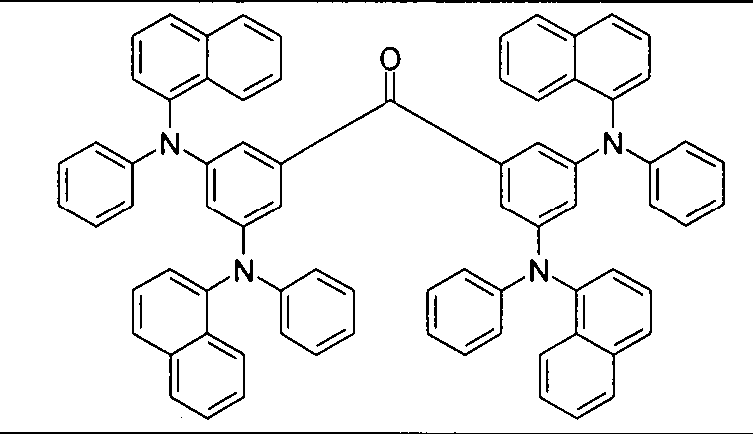
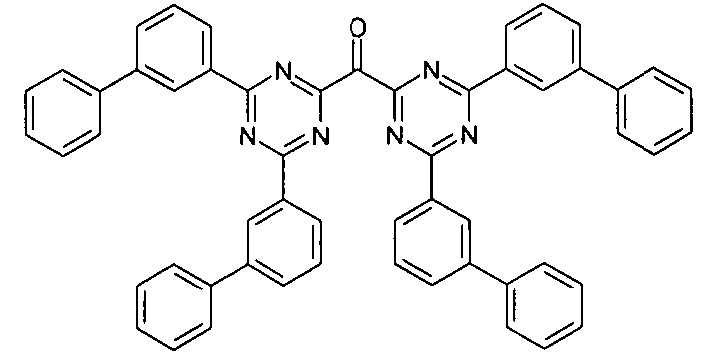
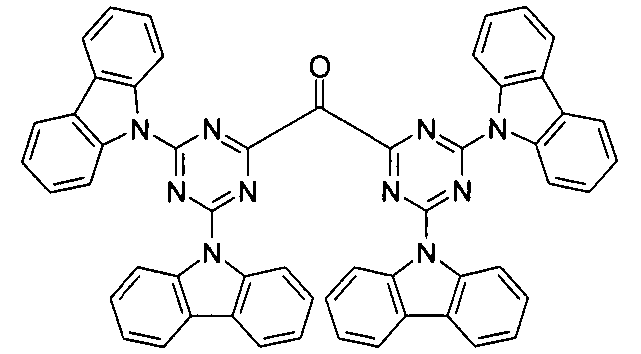
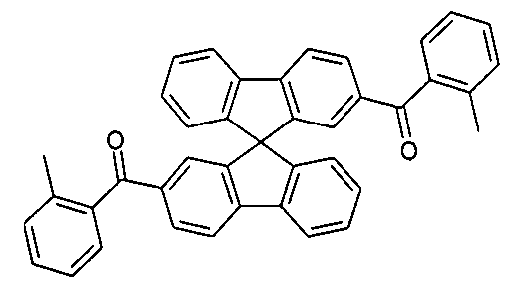
- Beispiele für geeignete Verbindungen gemäß Formel (1a) sind die im Folgenden abgebildeten Verbindungen (1) bis (59).
(1) (2) (3) (4) (5) (6) (7) (8) (9) (10) (11) (12) (13) (14) (15) (16) (17) (18) (19) (20) (21) (22) (23) (24) (25) (26) (27) (28) (29) (30) (31) (32) (33) (34) (35) (36) (37) (38) (39) (40) (41) (42) (43) (44) (45) (46) (47) (48) (49) (50) (51) (52) (53) (54) (55) (56) (57) (58) (59) -
- Geeignete Triazinderivate, die als Matrixmaterial A verwendet werden können, sind insbesondere 1,3,5-Triazine, welche mit mindestens einer, bevorzugt mindestens zwei, besonders bevorzugt mit drei aromatischen oder heteroaromatischen Ringsystemen substituiert sind. Besonders bevorzugt sind also Verbindungen der folgenden Formel (6) oder (7),
- Ar2
- ist gleich oder verschieden bei jedem Auftreten ein monovalentes aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches jeweils mit einem oder mehreren Resten R1 substituiert sein kann;
- Ar3
- ist ein bivalentes aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches mit einem oder mehreren Resten R1 substituiert sein kann.
- Bevorzugt ist in Verbindungen der Formel (6) und (7) mindestens eine Gruppe Ar2 gewählt aus den Gruppen der folgenden Formeln (8) bis (14), und die anderen Gruppen Ar2 haben die oben angegebene Bedeutung,
- X
- ist gleich oder verschieden bei jedem Auftreten eine bivalente Brücke, ausgewählt aus B(R1), C(R1)2, Si(R1)2, C=O, C=NR1, C=C(R1)2, O, S, S=O, SO2, N(R1), P(R1) und P(=O)R1;
- m
- ist bei jedem Auftreten gleich oder verschieden 0, 1, 2 oder 3;
- o
- ist bei jedem Auftreten gleich oder verschieden 0, 1, 2, 3 oder 4.
-
-
- Besonders bevorzugte Gruppen Ar3 sind gewählt aus den Gruppen der folgenden Formeln (15a) bis (21a),
- Bevorzugt sind weiterhin Verbindungen der oben aufgeführten Formel (7), in der die Gruppe Ar3 aus den oben aufgeführten Formeln (15) bis (21) ausgewählt ist und Ar2 gleich oder verschieden bei jedem Auftreten ausgewählt ist aus den oben aufgeführten Formeln (8) bis (14) oder Phenyl, 1- oder 2-Naphthyl, ortho-, meta- oder para-Biphenyl, welche durch einen oder mehrere Reste R1 substituiert sein können, jedoch bevorzugt unsubstituiert sind.
- Wie oben beschrieben, ist das Matrixmaterial B ein Material, welches ein HOMO von -5.4 eV oder weniger aufweist und welches ein LUMO von -2.4 eV oder mehr aufweist und welches weiterhin eine Energielücke von 3.5 eV oder mehr aufweist. In einer bevorzugten Ausführungsform der Erfindung weist das Matrixmaterial B ein HOMO von -5.7 eV oder weniger, besonders bevorzugt von -6.0 eV oder weniger auf. Weiterhin bevorzugt weist das Matrixmaterial B eine Energielücke von 3.7 eV oder mehr, besonders bevorzugt von 3.9 eV oder mehr auf. Durch die Wahl von Materialien mit den oben genannten Bedingungen für HOMO, LUMO und Energielücke wird gewährleistet, dass dieses Material nicht bzw. nicht in einem wesentlichen Anteil am Ladungstransport in der Schicht teilnimmt. Weiterhin bevorzugt weist das Matrixmaterial B ein LUMO von -2.2 eV oder mehr, besonders bevorzugt von -2.0 eV oder mehr auf.
-
- Als phosphoreszierende Verbindung eignen sich insbesondere Verbindungen, die bei geeigneter Anregung Licht, vorzugsweise im sichtbaren Bereich, emittieren und außerdem mindestens ein Atom der Ordnungszahl größer 20 enthalten. Bevorzugt werden als Phosphoreszenzemitter Verbindungen, die Kupfer, Molybdän, Wolfram, Rhenium, Ruthenium, Osmium, Rhodium, Iridium, Palladium, Platin, Silber, Gold oder Europium enthalten, verwendet, insbesondere Verbindungen, die Iridium, Platin oder Kupfer enthalten.
-
- DCy
- ist gleich oder verschieden bei jedem Auftreten eine cyclische Gruppe, die mindestens ein Donoratom, bevorzugt Stickstoff, Kohlenstoff in Form eines Carbens oder Phosphor, enthält, über welches die cyclische Gruppe an das Metall gebunden ist, und die wiederum einen oder mehrere Substituenten R1 tragen kann; die Gruppen DCy und CCy sind über eine kovalente Bindung miteinander verbunden;
- CCy
- ist gleich oder verschieden bei jedem Auftreten eine cyclische Gruppe, die ein Kohlenstoffatom enthält, über welches die cyclische Gruppe an das Metall gebunden ist und die wiederum einen oder mehrere Substituenten R1 tragen kann;
- A
- ist gleich oder verschieden bei jedem Auftreten ein mono- anionischer, zweizähnig chelatisierender Ligand, bevorzugt ein Diketonatligand.
- Dabei kann durch Bildung von Ringsystemen zwischen mehreren Resten R1 auch eine Brücke zwischen den Gruppen DCy und CCy vorliegen. Weiterhin kann durch Bildung von Ringsystemen zwischen mehreren Resten R1 auch eine Brücke zwischen zwei oder drei Liganden CCy-DCy bzw. zwischen ein oder zwei Liganden CCy-DCy und dem Liganden A vorliegen, so dass es sich um ein polydentates bzw. polypodales Ligandensystem handelt.
- Beispiele der oben beschriebenen Emitter können den Anmeldungen
WO 00/ 70 655 A2 WO 01/ 41 512 A1 WO 02/ 002 714 A2 WO 02/ 015 645 A1 EP 1 191 613 A2 ,EP 1 191 612 A2 ,EP 1 191 614 A2 ,WO 2004/ 081 017 A1 WO 2005/ 033 244 A1 WO 2005/ 042 550 A1 WO 2005/ 113 563 A1 WO 2006/ 008 069 A1 WO 2006/ 061 182 A1 WO 2006/ 081 973 A1 WO 2009/ 118 087 A1 WO 2009/ 1467 70A2 DE 10 2009 007 038 A1 entnommen werden. Generell eignen sich alle phosphoreszierenden Komplexe, wie sie gemäß dem Stand der Technik für phosphoreszierende OLEDs verwendet werden und wie sie dem Fachmann auf dem Gebiet der organischen Elektrolumineszenz bekannt sind, und der Fachmann kann ohne erfinderisches Zutun weitere phosphoreszierende Verbindungen verwenden. - Insbesondere ist dem Fachmann bekannt, welche phosphoreszierenden Komplexe in welcher Emissionsfarbe emittieren.
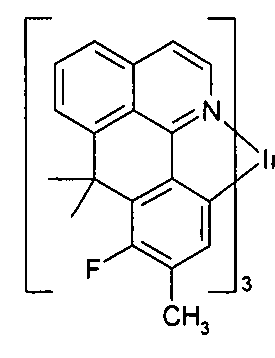
- Beispiele für geeignete phosphoreszierende Verbindungen sind die in der folgenden Tabelle aufgeführten Strukturen (1) bis (140).
(1) (2) (3) (4) (5) (6) (7) (8) (9) (10) (11) (12) (13) (14) (15) (16) (17) (18) (19) (20) (21) (22) (23) (24) (25) (26) (27) (28) (29) (30) (31) (32) (33) (34) (35) (36) (37) (38) (39) (40) (41) (42) (43) (44) (45) (46) (47) (48) (49) (50) (51) (52) (53) (54) (55) (56) (57) (58) (59) (60) (61) (62) (63) (64) (65) (66) (67) (68) (69) (70) (71) (72) (73) (74) (75) (76) (77) (78) (79) (80) (81) (82) (83) (84) (85) (86) (87) (88) (89) (90) (91) (92) (93) (94) (95) (96) (97) (98) (99) (100) (101) (102) (103) (104) (105) (106) (107) (108) (109) (110) (111) (112) (113) (114) (115) (116) (117) (118) (119) (120) (121) (122) (123) (124) (125) (126) (127) (128) (129) (130) (131) (132) (133) (134) (135) (136) (137) (138) (139) (140) - Außer Kathode, Anode und der mindestens einen emittierenden Schicht, die oben beschrieben wurde, kann die organische Elektrolumineszenzvorrichtung noch weitere Schichten enthalten. Diese sind beispielsweise gewählt aus jeweils einer oder mehreren Lochinjektionsschichten, Lochtransportschichten, Lochblockierschichten, Elektronentransportschichten, Elektroneninjektionsschichten, Elektronenblockierschichten, Exzitonenblockierschichten, Ladungserzeugungsschichten (Charge-Generation Layers) und/oder organischen oder anorganischen p/n-Übergängen. Außerdem können Interlayers vorhanden sein, welche beispielsweise die Ladungsbalance im Device steuern. Insbesondere können solche Interlayers als Zwischenschicht zwischen zwei emittierenden Schichten sinnvoll sein, insbesondere als Zwischenschicht zwischen einer fluoreszierenden und einer phosphoreszierenden Schicht. Weiterhin können die Schichten, insbesondere die Ladungstransportschichten, auch dotiert sein. Die Dotierung der Schichten kann für einen verbesserten Ladungstransport vorteilhaft sein. Es sei aber darauf hingewiesen, dass nicht notwendigerweise jede der oben genannten Schichten vorhanden sein muss und die Wahl der Schichten immer von den verwendeten Verbindungen abhängt. Die Verwendung derartiger Schichten ist dem Fachmann bekannt, und er kann hierfür ohne erfinderisches Zutun alle für derartige Schichten bekannten Materialien gemäß dem Stand der Technik verwenden.
- Weiterhin ist es möglich, mehr als eine emittierende Schicht zu verwenden, beispielsweise zwei oder drei emittierende Schichten, wobei diese bevorzugt unterschiedliche Emissionsfarben aufweisen. In einer besonders bevorzugten Auführungsform der Erfindung handelt es sich um eine weiß emittierende organische Elektrolumineszenzvorrichtung. Diese ist dadurch charakterisiert, dass sie Licht mit CIE-Farbkoordinaten im Bereich von 0.28/0.29 bis 0.45/0.41 emittiert. Der allgemeine Aufbau einer derartigen weiß emittierenden Elektrolumineszenzvorrichtung ist beispielsweise in
WO 2005/ 011 013 A1 - Als Kathode der erfindungsgemäßen Elektrolumineszenzvorrichtung sind Metalle mit geringer Austrittsarbeit, Metalllegierungen oder mehrlagige Strukturen aus verschiedenen Metallen bevorzugt, wie beispielsweise Erdalkalimetalle, Alkalimetalle, Hauptgruppenmetalle oder Lanthanoide (z. B. Ca, Ba, Mg, Al, In, Mg, Yb, Sm, etc.). Bei mehrlagigen Strukturen können auch zusätzlich zu den genannten Metallen weitere Metalle verwendet werden, die eine relativ hohe Austrittsarbeit aufweisen, wie z. B. Ag, wobei dann in der Regel Kombinationen der Metalle, wie beispielsweise Ca/Ag oder Ba/Ag verwendet werden. Ebenso bevorzugt sind Metalllegierungen, insbesondere Legierungen aus einem Alkalimetall oder Erdalkalimetall und Silber, besonders bevorzugt eine Legierung aus Mg und Ag. Es kann auch bevorzugt sein, zwischen einer metallischen Kathode und dem organischen Halbleiter eine dünne Zwischenschicht eines Materials mit einer hohen Dielektrizitätskonstante einzubringen. Hierfür kommen beispielsweise Alkalimetall- oder Erdalkalimetallfluoride, aber auch die entsprechenden Oxide oder Carbonate in Frage (z. B. LiF, Li2O, CsF, CS2CO3, BaF2, MgO, NaF, etc.). Die Schichtdicke dieser Schicht beträgt bevorzugt zwischen 0.5 und 5 nm.
- Als Anode der erfindungsgemäßen Elektrolumineszenzvorrichtung sind Materialien mit hoher Austrittsarbeit bevorzugt. Bevorzugt weist die Anode eine Austrittsarbeit größer 4.5 eV vs. Vakuum auf. Hierfür sind einerseits Metalle mit hohem Redoxpotential geeignet, wie beispielsweise Ag, Pt oder Au. Es können andererseits auch Metall/Metalloxid-Elektroden (z. B. Al/Ni/NiOx, Al/PtOx) bevorzugt sein. Dabei muss mindestens eine der Elektroden transparent sein, um die Auskopplung von Licht zu ermöglichen. Ein bevorzugter Aufbau verwendet eine transparente Anode. Bevorzugte Anodenmaterialien sind hier leitfähige gemischte Metalloxide. Besonders bevorzugt sind Indium-Zinn-Oxid (ITO) oder Indium-Zink Oxid (IZO). Bevorzugt sind weiterhin leitfähige, dotierte organische Materialien, insbesondere leitfähige dotierte Polymere.
- Die Vorrichtung wird entsprechend (je nach Anwendung) strukturiert, kontaktiert und schließlich hermetisch versiegelt, da sich die Lebensdauer derartiger Vorrichtungen bei Anwesenheit von Wasser und/oder Luft drastisch verkürzt.
- Es können generell alle weiteren Materialien, wie sie gemäß dem Stand der Technik in organischen Elektrolumineszenzvorrichtungen eingesetzt werden, in Kombination mit der erfindungsgemäßen emittierenden Schicht, welche mindestens einen phosphoreszierenden Emitter und die oben definierten Matrixmaterialien A und B enthält, eingesetzt werden.
- Geeignete Ladungstransportmaterialien, wie sie in der Lochinjektions- bzw. Lochtransportschicht oder in der Elektronentransportschicht der erfindungsgemäßen organischen Elektrolumineszenzvorrichtung verwendet werden können, sind beispielsweise die in Y. Shirota et al., Chem. Rev. 2007, 107(4), 953-1010 offenbarten Verbindungen oder andere Materialien, wie sie gemäß dem Stand der Technik in diesen Schichten eingesetzt werden.
- Beispiele für bevorzugte Lochtransportmaterialien, die in einer Lochtransport- oder Lochinjektionsschicht in der erfindungsgemäßen Elektrolumineszenzvorrichtung verwendet werden können, sind Indenofluorenamine und Derivate ( z. B. gemäß
WO 2006/ 122 630 A1 WO 2006/ 100 896 A1 EP 1 661 888 A1 offenbarten phenylenderivate (z. B. gemäßWO 01/ 49 806 A1 US 5 061 569 A ), die inWO 95/ 09 147 A1 WO 2008/006449 WO 2007/140847 JP 2001 226 331 A EP 0 676 461 A2 ,EP 650 955 A1 WO 01/ 49 806 A1 US 4 780 536 A ,WO 98/ 30 071 A1 EP 0 891 121 A1 ,EP 1 661 888 A1 ,JP 2006 253 445 A EP 0 650 955 A1 ,WO 2006/ 073 054 A1 US 5 061 569 A offenbart werden. -
- Geeignete Elektronentransport- oder Elektroneninjektionsmaterialien für die erfindungsgemäße Elektrolumineszenzvorrichtung sind beispielsweise die in der folgenden Tabelle aufgeführten Materialien. Weiterhin geeignete Elektronentransport- und Elektroneninjektionsmaterialien sind Derivate der oben abgebildeten Verbindungen, wie sie in
JP 2000 53 957 A WO 2003/ 060 956 A2 WO 2004/ 028 217 A1 WO 2004/ 080 975 A1 - Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit einem Sublimationsverfahren beschichtet werden. Dabei werden die Materialien in Vakuum-Sublimationsanlagen bei einem Anfangsdruck kleiner 10-5 mbar, bevorzugt kleiner 10-6 mbar aufgedampft. Es sei jedoch angemerkt, dass der Anfangsdruck auch noch geringer sein kann, beispielsweise kleiner 10-7 mbar.
- Bevorzugt ist ebenfalls eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit dem OVPD (Organic Vapour Phase Deposition) Verfahren oder mit Hilfe einer Trägergassublimation beschichtet werden. Dabei werden die Materialien bei einem Druck zwischen 10-5 mbar und 1 bar aufgebracht. Ein Spezialfall dieses Verfahrens ist das OVJP (Organic Vapour Jet Printing) Verfahren, bei dem die Materialien direkt durch eine Düse aufgebracht und so strukturiert werden (z. B. M. S. Arnold et al., Appl. Phys. Lett. 2008, 92, 053301).
- Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten aus Lösung, wie z. B. durch Spincoating, oder mit einem beliebigen Druckverfahren, wie z. B. Siebdruck, Flexodruck, Offsetdruck, LITI (Light Induced Thermal Imaging, Thermotransferdruck), Ink-Jet Druck (Tintenstrahldruck) oder Nozzle-Printing, hergestellt werden. Hierfür sind lösliche Verbindungen nötig. Hohe Löslichkeit lässt sich durch geeignete Substitution der Verbindungen erreichen. Dabei können nicht nur Lösungen aus einzelnen Materialien aufgebracht werden, sondern auch Lösungen, die mehrere Verbindungen enthalten, beispielsweise Matrixmaterialien und Dotanden.
- Die organische Elektrolumineszenzvorrichtung kann auch als Hybridsystem hergestellt werden, indem eine oder mehrere Schichten aus Lösung aufgebracht werden und eine oder mehrere weitere Schichten aufgedampft werden.
- Die organische Elektrolumineszenzvorrichtung kann für verschiedene Anwendungen verwendet werden, insbesondere für Display-Anwendungen oder als Lichtquelle, beispielsweise für Beleuchtungsanwendungen oder für medizinische Anwendungen.
- Diese Verfahren sind dem Fachmann generell bekannt und können von ihm ohne erfinderisches Zutun auf die erfindungsgemäßen organischen Elektrolumineszenzvorrichtungen angewandt werden.
- Die erfindungsgemäßen organischen Elektrolumineszenzvorrichtungen weisen folgende überraschende Vorteile gegenüber dem Stand der Technik auf:
- 1. Die erfindungsgemäße organische Elektrolumineszenzvorrichtung weist eine sehr hohe Effizienz auf. Dabei ist die Effizienz besser als bei Verwendung eines elektronentransportierenden Matrixmaterials in Kombination mit einem lochtransportierenden Matrixmaterial.
- 2. Die erfindungsgemäße organische Elektrolumineszenzvorrichtung weist gleichzeitig eine verbesserte Lebensdauer auf. Dabei ist die Lebensdauer höher als bei Verwendung eines elektronentransportierenden Matrixmaterials in Kombination mit einem lochtransportierenden Matrixmaterial.
- Die Erfindung wird durch die nachfolgenden Beispiele genauer beschrieben, ohne sie dadurch einschränken zu wollen. Der Fachmann kann, ohne erfinderisch tätig zu werden, weitere erfindungsgemäße organische Elektrolumineszenzvorrichtungen herstellen.
- Beispiele:
- Bestimmung von HOMO, LUMO und Energielücke aus Cyclovoltammetrie und Absortionsspektrum
- Die Bestimmung der HOMO- und LUMO-Werte sowie der Energielücke im Sinne der vorliegenden Erfindung erfolgt nach den im Folgenden beschriebenen allgemeinen Verfahren:
- Der HOMO-Wert ergibt sich aus dem Oxidationspotential, das mittels Cyclovoltammetrie (CV) bei Raumtemperatur gemessen wird. Als Messgerät hierzu wird ein ECO Autolab System mit Metrohm 663 VA Stand verwendet. Die Arbeitselektrode ist eine Goldelektrode, die Referenzelektrode Ag/AgCI, der Zwischenelektrolyt KCl (3 mol/l) und die Hilfselektrode Platin.
- Für die Messung wird zunächst eine 0.11 M Leitsalzlösung aus Tetrabutylammoniumhexafluorophosphat (NH4PF6) in Dichlormethan hergestellt, in die Messzelle eingefüllt und 5 min entgast. Anschließend werden zwei Messzyklen mit folgenden Parametern durchgeführt:
- Messtechnik: CV
- Initial purge time: 300 s
- Cleaning Potential: -1 V
- Cleaning Time: 10 s
- Deposition Potential: -0.2 V
- Deposition Time: 10 s
- Start Potential: -0.2 V
- End Potential: 1.6 V
- Voltage Step: 6 mV
- Sweep Rate: 50 mV/s
- Anschließend wird die Leitsalzlösung mit 1 ml der Probenlösung (10 mg der zu messenden Substanz in 1 ml Dichlormethan) versetzt und erneut 5 min entgast. Anschließend werden fünf weitere Messzyklen gefahren, von denen die letzten 3 zur Auswertung aufgezeichnet werden. Dabei werden dieselben Parameter eingestellt, wie oben beschrieben.
- Anschließend wird die Lösung mit 0.1 ml Ferrocenlösung (100 mg Ferrocen in 1 ml Dichlormethan) versetzt, 1 min entgast, und ein Messzyklus mit folgenden Parametern durchgeführt:
- Messtechnik: CV
- Initial purge time: 60 s
- Cleaning Potential: -1 V
- Cleaning Time: 10 s
- Deposition Potential: -0.2 V
- Deposition Time: 10 s
- Start Potential: -0.2 V
- End Potential: 1.6 V
- Voltage Step: 6 mV
- Sweep Rate: 50 mV/s
- Zur Auswertung wird für die Probenlösung und die mit Ferrocenlösung versetzte Lösung jeweils der Mittelwert aus den Spannungen des ersten Oxidationsmaximums aus den Hinkurven und des zugehörigen Reduktionsmaximums aus den Rückkurven genommen (VP und VF), wobei als Spannung jeweils die Spannung gegen Ferrocen verwendet wird. Der HOMO-Wert der zu untersuchenden Substanz EHOMO ergibt sich als EHOMO = -[e·(VP - VF) + 4.8 eV], wobei e die Elementarladung darstellt.
- Es ist zu beachten, dass im Einzelfall gegebenenfalls sinnvolle Abwandlungen der Messmethode vorgenommen werden müssen, z. B. wenn sich die zu untersuchende Substanz in Dichlormethan nicht lösen lässt oder wenn es zu Zersetzung der Substanz während der Messung kommt. Sollte eine sinnvolle Messung mittels CV mit der oben genannten Methode nicht möglich sein, wird die HOMO-Energie über Photoelektronen-Spektroskopie mittels Model AC-2 Photoelectron Spectrometer von Riken Keiki Co. Ltd. (http://www.rikenkeiki.com/pages/AC2.htm) bestimmt werden, wobei zu beachten ist, dass die erhaltenen Werte dabei typischerweise um 0.3 eV tiefer liegen, als die mit CV gemessenen. Unter dem HOMO-Wert im Sinne dieses Patents ist dann der Wert aus Riken AC2 + 0.3 eV zu verstehen.
- Weiterhin lassen sich sowohl mit der beschriebenen CV Methode wie auch mit der beschriebenen Photoelektronen-Spektroskopie HOMO-Werte, die tiefer als -6 eV liegen, nicht verlässlich messen. In diesem Fall werden die HOMO-Werte aus quantenchemischer Rechnung mittels Dichtefunktional-Theorie (DFT) ermittelt. Dies erfolgt über die kommerziell erhältliche Software Gaussian 03W (Gaussian Inc.) mit der Methode B3PW91 / 6-31G(d). Die Normierung der berechneten Werte auf CV-Werte wird über einen Abgleich mit aus CV messbaren Materialien erreicht. Hierzu werden die HOMO-Werte einer Reihe von Materialien mit der CV Methode gemessen und ebenso berechnet. Die berechneten Werte werden dann mittels der gemessenen kalibriert, dieser Kalibrierfaktor wird für alle weiteren Berechnungen verwendet. Auf diese Weise lassen sich HOMO-Werte berechnen, die sehr gut denen entsprechen, die man über CV messen würde. Sollte sich der HOMO-Wert einer bestimmten Substanz nicht über CV oder Riken AC2 wie oben beschrieben messen lassen, ist unter dem HOMO-Wert im Sinne dieses Patents daher der Wert zu verstehen, der entsprechend der Beschreibung durch eine auf CV kalibrierte DFT-Rechnung, wie oben beschrieben, erhalten wird. Beispiele für auf diese Weise berechnetete Werte einiger gäninger organischer Materialien sind: NPB = (HOMO -5.16 eV, LUMO -2.28 eV); TCTA (HOMO -5.33 eV, LUMO -2.20 eV); TPBI (HOMO -6.26 eV, LUMO -2.48 eV). Diese Werte können für die Kalibrierung der Rechenmethode verwendet werden.
- Die Energielücke wird bestimmt aus der Absorptionskante des Absorptionsspektrums gemessen an einem Film mit Schichtdicke 50 nm. Die Absorptionskante ist dabei definiert als die Wellenlänge, die man erhält, wenn man im Absorptionsspektrum an die langwelligste abfallende Flanke an ihrer steilsten Stelle eine Gerade anfittet und den Wert ermittelt, bei dem diese Gerade die Wellenlängeachse, d. h.den Absorptionswert = 0, schneidet
- Der LUMO Wert wird durch Addition der Energielücke auf den oben beschriebenen HOMO-Wert erhalten.
- Herstellung und Charakterisierung von organischen Elektrolumineszenzvorrichtungen gemäß der Erfindung Erfindungsgemäße Elektrolumineszenzvorrichtungen können, wie beispielsweise in
WO 2005/ 003 253 A2 - Diese noch nicht optimierten OLEDs werden standardmäßig charakterisiert; hierfür werden die Elektrolumineszenzspektren und Farbkoordinaten (gemäß CIE 1931), die Effizienz (gemessen in cd/A) in Abhängigkeit von der Helligkeit, die Betriebsspannung, berechnet aus Strom-Spannungs-Leuchtdichte-Kennlinien (IUL-Kennlinien), und die Lebensdauer bestimmt. Die erhaltenen Ergebnisse sind in Tabelle 2 zusammengefasst.
- Im Folgenden werden die Ergebnisse verschiedener OLEDs gegenübergestellt. Für die verwendeten Matrixmaterialien werden dabei folgende Werte für HOMO, LUMO und Energielücke mit der oben beschriebenen allgemeinen Methode bestimmt (Tabelle 1). Tabelle 1
Material HOMO LUMO Enerqielücke TMM1 -6.3 eV -2.75 eV 3.55 eV TMM2 -6.1 eV -2.8 eV 3.3 eV TMM3 -5.8 eV -1.8 eV 4.0 eV TMM4 -6.15 eV -2.0 eV 4.15 eV TMM5 -6.2 eV -2.2 eV 4.0 eV TMM6 -6.15 eV -2.25 eV 3.9 eV TMM7 -6.0 eV -2.5 eV 3.5 eV CBP -5.40 eV -2.0 eV 3.4 eV TCTA -5.30 eV -2.2 eV 3.1 eV - Dabei sind TMM1 und TMM2 elektronenleitende Matrixmaterialien, CBP und TCTA sind lochleitende Matrixmaterialien und TMM3 bis TMM6 sind weder elektronenleitende noch lochleitende Matrixmaterialien. TMM7 ist ein elektronenleitendes Matrixmaterial.
- Beispiel 1:
- Erfindungsgemäße Beispiele 1a und 1b werden durch folgenden Schichtaufbau realisiert:
- 20 nm HIM, 20 nm HTM, 30 nm Mischschicht TMM1:TMM4 im Verhältnis 2:1 (1a) bzw. 1:2 (1b) dotiert mit 10% TEG-1, 10 nm TMM1, 20 nm ETM, 1 nm LiF, 100 nm Al.
- TMM1 stellt hierbei gemäß Definition einen elektronenleitenden Host dar und TMM4 einen Neutralhost. Die erhaltenen OLEDs weisen grüne Emission mit hoher Effizienz, niedriger Betriebsspannung und einer langen Betriebslebensdauer auf.
- Beispiel 2:
- Erfindungsgemäßes Beispiel 2 wird durch den gleichen Schichtaufbau realisiert wie Beispiel 1a, wobei als Neutralhost anstelle von TMM4 das Material TMM3 verwendet wurde. Auch diese OLED weist ähnlich gute Emissionseigenschaften auf wie Beispiele 1a und 1b
- Beispiel 3:
- Erfindungsgemäßes Beispiel 3 wird durch den gleichen Schichtaufbau realisiert wie Beispiel 2, wobei als Neutralhost anstelle von TMM3 das Material TMM5 verwendet wurde. Auch diese OLED weist ähnlich gute Emissionseigenschaften auf wie Beispiel 2
- Beispiel 4 (Vergleich):
- Vergleichsbeispiel 4 wird durch den gleichen Schichtaufbau realisiert wie Beispiele 1, 2 und 3 allerdings wird hier auf eine Mischschicht verzichtet, die Emissionsschicht enthält TMM1 alleine, dotiert mit 10% TEG-1.
- Die Verwendung des elektronenleitenden Hosts ohne Beimischung eines Neutralmaterials ermöglich zwar etwas geringere Spannungen, dafür liegen aber Effizienz und Betriebslebensdauer deutlich unter den Daten der in Beispielen 1, 2 und 3 gezeigten OLEDs mit erfindungsgemäßer Mischschicht.
- Beispiel 5 (Vergleich):
- Vergleichsbeispiel 5 wird durch den gleichen Schichtaufbau realisiert wie Beispiel 4, allerdings wird hier der Neutralhost TMM4 als alleiniger Host für die Emissionsschicht verwendet, wieder dotiert mit 10% TEG-1.
- Es zeigt sich, dass dieses Material als alleiniger Host aufgrund seiner HOMO und LUMO Lagen ungeeignet ist, um eine brauchbare OLED Emissionscharakteristik zu erhalten. Schon alleine an der sehr hohen Betriebsspannung zeigt sich, dass dieses Material zu keinem guten Ladungstransport in der OLED führt.
- Beispiel 6 (Vergleich):
- Vergleichsbeispiele 6a und 6b enthalten wieder eine Mischschicht als Host, allerdings keine erfindungesgemäße, da sie entsprechend dem Stand der Technik neben dem elektronenleitenden Material TMM1 die lochleitenden Materialien CBP oder TCTA enthalten. Sie werden analog zu Beispiel 1a durch folgenden Schichtaufbau realisiert:
- 20 nm HIM, 20 nm HTM, 30 nm Mischschicht TMM1:CBP (6a) bzw.
- TMM1:TCTA (6b) im Verhältnis 2:1 dotiert mit 10% TEG-1, 10 nm TMM1, 20 nm ETM, 1 nm LiF, 100 nm Al. Es zeigt sich, dass die Spannung bei Verwendung von TCTA zwar etwas niedriger liegt als bei den erfindungsgemäßen Mischschichten in Beispielen 1 und 2. Die Effizienz und insbesondere die Betriebslebensdauer ist den erfindungsgemäßen Mischschichten aber deutlich unterlegen.
- Beispiel 7:
- Erfindungsgemäße Beispiele 7a und 7b werden durch folgenden Schichtaufbau realisiert:
- 20 nm HIM, 20 nm HTM, 30 nm Mischschicht TMM7:TMM4 im Verhältnis 2:1 (1a) bzw. 1:2 (1b) dotiert mit 10% TEG-1, 10 nm TMM1, 20 nm ETM, 1 nm LiF, 100 nm AI.
- TMM7 stellt hierbei gemäß Definition einen elektronenleitenden Host dar und TMM4 einen Neutralhost. Die erhaltenen OLEDs weisen grüne Emission mit hoher Effizienz, niedriger Betriebsspannung und einer längen Betriebslebensdauer als Vergleichsbeispiel 8 auf.
- Beispiel 8 (Vergleich):
- Vergleichsbeispiel 8 wird durch den gleichen Schichtaufbau realisiert wie Beispiel 7 allerdings wird hier auf eine Mischschicht verzichtet, die Emissionsschicht enthält TMM7 alleine, dotiert mit 10% TEG-1.
- Die Verwendung des elektronenleitenden Hosts ohne Beimischung eines Neutralmaterials ermöglich zwar etwas geringere Spannungen, dafür liegen aber Effizienz und Betriebslebensdauer aber unter den Daten der in Beispiel 7 gezeigten OLED mit erfindungsgemäßer Mischschicht.
- Beispiel 9:
- Erfindungsgemäßes Beispiel 9 wird durch folgenden Schichtaufbau realisiert:
- 20 nm HIM, 20 nm HTM, 30 nm Mischschicht TMM2:TMM4 im Verhältnis 1:1 dotiert mit 10% TEG-1, 10 nm TMM2, 25 nm ETM, 1 nm LiF, 100 nm Al.
- TMM2 stellt hierbei gemäß Definition einen elektronenleitenden Host dar und TMM4 einen Neutralhost. Die erhaltenen OLEDs weisen grüne Emission mit hoher Effizienz und insbesondere einer längeren Betriebslebensdauer als Vergleichsbeispiel 10 auf.
- Beispiel 10 (Vergleich):
- Vergleichsbeispiel 10 wird durch den gleichen Schichtaufbau realisiert wie Beispiel 9 allerdings wird hier auf eine Mischschicht verzichtet, die Emissionsschicht enthält TMM2 alleine, dotiert mit 10% TEG-1. Tabelle 2: Device-Eraebnisse
Bsp. Wirtsmaterial(ien) Dotand CIE x/y bei 1000 cd/m2 Effizienz bei 1000 cd/m2 Spannung bei 1000 cd/m2 Lebensdauer 50% bei 4000 cd/m2 1a TMM1 :TMM4 (2:1) TEG-1 10% 0.36/0.61 46 cd/A 4.0 V 2900 1b TMM1 :TMM4 (1:2) TEG-1 10% 0.36/0.61 45 cd/A 4.3 V 3100 2 TMM1 :TMM3 (2:1) TEG-1 10% 0.36/0.61 47 cd/A 4.1 V 2700 3 TMM1:TMM5 (2:1) TEG-1 10% 036/0.61 45 cd/A 4.1 V 2300 4 (Vgl.) TMM1 TEG-1 10% 0.37/0.60 42 cd/A 3.8 V 2000 5 (Vgl.) TMM4 TEG-1 10% 0.34/0.59 12 cd/A 8.7 V 140 6a(Vgl) TMM1:CBP (2:1) TEG-1 10% 0.36/0.61 44 cd/A 4.1 V 2000 6b(Vgl) TMM1:TCTA (2:1) TEG-1 10% 0.35/0.60 42 cd/A 3.9 V 1100 7a TMM7:TMM4 (2:1) TEG-1 10% 0.37/0.60 47 cd/A 3.9 V 2200 7b TMM7:TMM4 (1:2) TEG-1 10% 0.36/0.61 45 cd/A 42 V 2200 8 (Vgl) TMM7 TEG-1 10% 0.38/0.60 41 cd/A 3.9 V 1200 9 TMM2:TMM4 (1:1) TEG-1 10% 0.36/0.60 48 cd/A 4.9 V 3000 10(Vgl) TMM2 TEG-1 10% 0.37/0.60 45 cd/A 4.9 V 2000 - Herstellung und Charakterisierungen von organischen Elektrolumineszenzvorrichtungen aus Lösung
- Erfindungsgemäße Elektrolumineszenzvorrichtungen können auch aus Lösung hergestellt werden, was zu wesentlich einfacheren Devices mit dennoch guten Eigenschaften führt. Die Herstellung solcher Bauteile lehnt sich an die Herstellung polymerer Leuchtdioden (PLEDs) an, die in der Literatur bereits vielfach beschrieben ist ( z. B. in der
WO 2004/ 037 887 A2 1 zeigt den typischen Aufbau einer solchen Device. In der emittierenden Schicht liegen die gemeinsam gelösten Matrixmaterialien sowie der Emitter in Form einer amorphen Schicht vor. Strukturierte ITO-Substrate und das Material für die sogenannte Pufferschicht (PEDOT, eigentlich PEDOT:PSS) sind käuflich erhältlich (ITO von Technoprint und anderen, PEDOT:PPS als wässrige Dispersion Clevios P von H.C. Starck). Die verwendete Interlayer dient der Lochinjektion; in diesem Fall wurde HIL-012 von Merck verwendet. Die Emissionsschicht wird in einer Inertgasatmosphäre, im vorliegenden Fall Argon, aufgeschleudert und 10 min bei 160 °C bzw. 180 °C ausgeheizt. Zuletzt wird eine Kathode aus Barium und Aluminium im Vakuum aufgedampft. Zwischen der emittierenden Schicht und der Kathode können auch die in den vorgenannten Beispielen verwendeten Lochblockier- und/oder Elektronentransportschichten per Bedampfung aufgebracht werden, auch kann die Interlayer durch eine oder mehrere Schichten ersetzt werden, die lediglich die Bedingung erfüllen müssen, durch den nachgelagerten Prozessierungsschritt der Abscheidung der emittierenden aus Lösung nicht wieder abgelöst zu werden. Auch die lösungsprozessierten Devices werden standardmäßig charakterisiert, die genannten OLED-Beispiele sind noch nicht optimiert. - In Tabelle 3 werden die Deviceergebnisse gemäß dem Stand der Technik mit denen, die durch eine gemischte Schicht enthaltend die Matrixmaterialien A und B erhalten wurden, verglichen. Auch im Bereich löslich prozessierter Devices zeigt sich hier, dass die erfindungsgemäßen Materialien die Bauteile in Effizienz und Lebensdauer deutlich verbessern.
- Beispiel 11 (Vergleich):
- 30 mg TEG2 und 150 mg TMM1 werden gemeinsam in 10 ml trockenem und sauerstofffreiem Toluol gelöst. Auf der zuvor aufgebrachten HIL-012 Schicht werden in einer Argon-gefluteten Glovebox bei einer Spinrate von 1000 rpm 80 nm EML (emitting layer) abgeschieden. Die Schicht wird vor dem Aufdampfen der Kathode 10 min bei 120 °C ausgeheizt.
- Beispiel 12:
- 40 mg TEG2, 100 mg TMM1 und 100 mg TMM5 werden gemeinsam in 10 ml trockenem und sauerstofffreiem Toluol gelöst. Auf der zuvor aufgebrachten HIL-012 Schicht werden in einer Argon-gefluteten Glovebox bei einer Spinrate von 2110 rpm 80 nm EML abgeschieden. Die Schicht wird vor dem Aufdampfen der Kathode 10 min bei 120 °C ausgeheizt.
- Beispiel 13 (Vergleich):
- 40 mg TEG2 und 200 mg TMM2 werden gemeinsam in 10 ml trockenem und sauerstofffreiem Chlorbenzol gelöst. Auf der zuvor aufgebrachten HIL-012 Schicht werden in einer Argon-gefluteten Glovebox bei einer Spinrate von 1000 rpm 80 nm EML abgeschieden. Die Schicht wird vor dem Aufdampfen der Kathode 10 min bei 180 °C ausgeheizt.
- Beispiel 14:
- 40 mg TEG2, 100 mg TMM2 und 100 mg TMM4 werden gemeinsam in 10 ml trockenem und sauerstofffreiem Toluol gelöst. Auf der zuvor aufgebrachten HIL-012 Schicht werden in einer Argon-gefluteten Glovebox bei einer Spinrate von 3260 rpm 80 nm EML abgeschieden. Die Schicht wird vor dem Aufdampfen der Kathode 10 min bei 160 °C ausgeheizt.
- Beispiel 15:
- 40 mg TEG2, 100 mg TMM2 und 100 mg TMM6 werden gemeinsam in 10 ml trockenem und sauerstofffreiem Toluol gelöst. Auf der zuvor aufgebrachten HIL-012 Schicht werden in einer Argon-gefluteten Glovebox bei einer Spinrate von 2080 rpm 80 nm EML abgeschieden. Die Schicht wird vor dem Aufdampfen der Kathode 10 min bei 160 °C ausgeheizt. Tabelle 3: Device-Ergebnisse
Bsp. Wirtsmaterial(ien) Dotand CIE x/y bei 1000 cd/m2 Effizienz bei 1000 cd/m2 Spannung bei 1000 cd/m2 Lebensdauer 50% bei 1000 cd/m2 11 (Vgl.) TMM1 TEG-2 16.7 % 0.35/0.61 24 cd/A 6.4 V 2700 12 TMM1:TMM5 (1:1) TEG-2 16.7 % 0.33/0.63 32 cd/A 6.4 V 6600 13 (Vgl.) TMM2 TEG-2 16.7 % 0.36/0.61 11 cd/A 5.7 V 9400 14 TMM2:TMM4 (1:1) TEG-2 16.7 % 0.32/0.62 20 cd/A 4.6 V 13000 15 TMM2:TMM6(1:1) TEG-2 16.7 % 0.33/0.63 26 cd/A 4.7 V 20500
Claims (11)
- Organische Elektrolumineszenzvorrichtung, enthaltend Anode, Kathode und mindestens eine emittierende Schicht, welche mindestens eine phosphoreszierende Verbindung enthält, welche in eine Mischung aus zwei Materialien A und B eingebracht ist, wobei die Materialien A und B definierte niedermolekulare Verbindungen mit einer Molmasse von 2000 g/mol oder weniger sind, wobei das Material A ein elektronentransportierendes Material ist, welche ausgewählt ist aus der Gruppe bestehend aus aromatischen Ketonen, aromatischen Phosphinoxiden, aromatischen Sulfoxiden, aromatischen Sulfonen, Triazinderivaten, Zink-Komplexen und Aluminium-Komplexen, und wobei das Material B ein Material ist, welches nicht am Ladungstransport beteiligt ist, welches ein HOMO von -5,4 eV oder weniger und ein LUMO von -2,4 eV oder mehr aufweist, und welches eine Energielücke von mindestens 3,5 eV aufweist, und welches ausgewählt ist aus Verbindungen der Formeln (23), (24) und (25),
- Organische Elektrolumineszenzvorrichtung nach
Anspruch 1 , dadurch gekennzeichnet, dass der Anteil der phosphoreszierenden Verbindung in der emittierenden Schicht 1 bis 50 Vol.-% beträgt. - Organische Elektrolumineszenzvorrichtung nach
Anspruch 1 oder2 , dadurch gekennzeichnet, dass das Mischungsverhältnis zwischen dem Material A und dem Material B zwischen 10:1 und 1:10 liegt, jeweils bezogen auf das Volumen. - Organische Elektrolumineszenzvorrichtung nach
Anspruch 1 , dadurch gekennzeichnet, dass das aromatische Keton eine Verbindung der Formel (2), (3), (4) oder (5) ist,Anspruch 1 beschrieben, und weiterhin gilt: Z ist gleich oder verschieden bei jedem Auftreten CR1 oder N. - Organische Elektrolumineszenzvorrichtung nach
Anspruch 1 , dadurch gekennzeichnet, dass das Triazinderivat eine Verbindung der Formel (6) oder (7) ist,Anspruch 1 genannte Bedeutung hat und für die weiteren verwendeten Symbole gilt: Ar2 ist gleich oder verschieden bei jedem Auftreten ein monovalentes aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches jeweils mit einem oder mehreren Resten R1 substituiert sein kann; Ar3 ist ein bivalentes aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches mit einem oder mehreren Resten R1 substituiert sein kann. - Organische Elektrolumineszenzvorrichtung nach einem oder mehreren der
Ansprüche 1 bis6 , dadurch gekennzeichnet, dass das Material B ein HOMO von -5,7 eV oder weniger aufweist. - Organische Elektrolumineszenzvorrichtung nach einem oder mehreren der
Ansprüche 1 bis7 , dadurch gekennzeichnet, dass das Material B eine Energielücke von 3,7 eV oder mehr aufweist. - Organische Elektrolumineszenzvorrichtung nach einem oder mehreren der
Ansprüche 1 bis8 , dadurch gekennzeichnet, dass das Material B ein LUMO von -2,2 eV oder mehr aufweist. - Organische Elektrolumineszenzvorrichtung nach einem oder mehreren der
Ansprüche 1 bis9 , dadurch gekennzeichnet, dass die phosphoreszierende Verbindung eine Verbindung der Formeln (26) bis (29) ist,Anspruch 6 beschrieben, und für die weiteren verwendeten Symbole gilt: DCy ist gleich oder verschieden bei jedem Auftreten eine cyclische Gruppe, die mindestens ein Donoratom, bevorzugt Stickstoff, Kohlenstoff in Form eines Carbens oder Phosphor, enthält, über welches die cyclische Gruppe an das Metall gebunden ist, und die wiederum einen oder mehrere Substituenten R1 tragen kann; die Gruppen DCy und CCy sind über eine kovalente Bindung miteinander verbunden; CCy ist gleich oder verschieden bei jedem Auftreten eine cyclische Gruppe, die ein Kohlenstoffatom enthält, über welches die cyclische Gruppe an das Metall gebunden ist und die wiederum einen oder mehrere Substituenten R1 tragen kann; A ist gleich oder verschieden bei jedem Auftreten ein monoanionischer, zweizähnig chelatisierender Ligand, bevorzugt ein Diketonatligand. - Verfahren zur Herstellung einer organischen Elektrolumineszenzvorrichtung nach einem oder mehreren der
Ansprüche 1 bis10 , dadurch gekennzeichnet, dass eine oder mehrere Schichten mit einem Sublimationsverfahren beschichtet werden oder dass eine oder mehrere Schichten mit dem OVPD (Organic Vapour Phase Deposition) Verfahren oder mit Hilfe einer Trägergassublimation beschichtet werden oder dass eine oder mehrere Schichten aus Lösung oder mit einem Druckverfahren beschichtet werden.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102009014513A DE102009014513A1 (de) | 2009-03-23 | 2009-03-23 | Organische Elektrolumineszenzvorrichtung |
| DE102009014513.3 | 2009-03-23 | ||
| PCT/EP2010/001123 WO2010108579A1 (de) | 2009-03-23 | 2010-02-24 | Organische elektrolumineszenzvorrichtung |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE112010001236A5 DE112010001236A5 (de) | 2012-06-14 |
| DE112010001236B4 true DE112010001236B4 (de) | 2022-07-07 |
Family
ID=42170826
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE102009014513A Withdrawn DE102009014513A1 (de) | 2009-03-23 | 2009-03-23 | Organische Elektrolumineszenzvorrichtung |
| DE112010001236.9T Active DE112010001236B4 (de) | 2009-03-23 | 2010-02-24 | Organische elektrolumineszenzvorrichtung |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE102009014513A Withdrawn DE102009014513A1 (de) | 2009-03-23 | 2009-03-23 | Organische Elektrolumineszenzvorrichtung |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9444064B2 (de) |
| JP (1) | JP5670418B2 (de) |
| KR (1) | KR101704837B1 (de) |
| CN (1) | CN102362367B (de) |
| DE (2) | DE102009014513A1 (de) |
| TW (1) | TWI510596B (de) |
| WO (1) | WO2010108579A1 (de) |
Families Citing this family (350)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102009041289A1 (de) * | 2009-09-16 | 2011-03-17 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102009041414A1 (de) | 2009-09-16 | 2011-03-17 | Merck Patent Gmbh | Metallkomplexe |
| DE102009057167A1 (de) | 2009-12-05 | 2011-06-09 | Merck Patent Gmbh | Elektronische Vorrichtung enthaltend Metallkomplexe |
| CN102668152A (zh) * | 2009-12-23 | 2012-09-12 | 默克专利有限公司 | 包括聚合粘结剂的组合物 |
| USRE47654E1 (en) | 2010-01-15 | 2019-10-22 | Idemitsu Koasn Co., Ltd. | Organic electroluminescence device |
| DE102010004803A1 (de) | 2010-01-16 | 2011-07-21 | Merck Patent GmbH, 64293 | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010005697A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Verbindungen für elektronische Vorrichtungen |
| DE102010009903A1 (de) | 2010-03-02 | 2011-09-08 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| DE102010010481A1 (de) | 2010-03-06 | 2011-09-08 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102010014933A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010020567A1 (de) | 2010-05-14 | 2011-11-17 | Merck Patent Gmbh | Metallkomplexe |
| WO2011157339A1 (de) | 2010-06-15 | 2011-12-22 | Merck Patent Gmbh | Metallkomplexe |
| DE102010024335A1 (de) | 2010-06-18 | 2011-12-22 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| DE102010024542A1 (de) | 2010-06-22 | 2011-12-22 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010024897A1 (de) | 2010-06-24 | 2011-12-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010027218A1 (de) | 2010-07-15 | 2012-01-19 | Merck Patent Gmbh | Organische Komplexe enthaltend Metalle |
| DE102010027317A1 (de) | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Metallkomplexe |
| DE102010027319A1 (de) | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Metallkomplexe |
| DE102010027316A1 (de) | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Metallkomplexe |
| DE102010045405A1 (de) | 2010-09-15 | 2012-03-15 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010046512A1 (de) | 2010-09-24 | 2012-03-29 | Merck Patent Gmbh | Phosphorhaltige Metallkomplexe |
| WO2012048819A1 (en) * | 2010-10-11 | 2012-04-19 | Solvay (Societe Anonyme) | Novel spirobifluorene compounds |
| DE102010048497A1 (de) * | 2010-10-14 | 2012-04-19 | Merck Patent Gmbh | Formulierungen für organische Elektrolumineszenzvorrichtungen |
| DE102010048498A1 (de) * | 2010-10-14 | 2012-04-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| TW201240958A (en) * | 2010-12-08 | 2012-10-16 | Georgia Tech Res Inst | Bis (sulfonyl) biaryl derivatives as electron transporting and/or host materials |
| DE102011106849A1 (de) | 2010-12-15 | 2012-06-21 | Merck Patent Gmbh | Verfahren zur Synthese N-N verknüpfter und um die N-N Bindung rotationsgehinderter bis-N-heterocyclische Carbene und deren Einsatz als Liganden für Metallkomplexe |
| DE112012007377B4 (de) | 2011-02-16 | 2025-08-07 | Semiconductor Energy Laboratory Co., Ltd. | Licht emittierendes Element |
| KR20250026895A (ko) | 2011-02-16 | 2025-02-25 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 발광 엘리먼트 |
| DE102011011539A1 (de) | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| CN103443950B (zh) | 2011-03-23 | 2016-06-15 | 株式会社半导体能源研究所 | 发光元件 |
| JP5996628B2 (ja) | 2011-04-04 | 2016-09-21 | メルク パテント ゲーエムベーハー | 金属錯体 |
| CN103477462B (zh) * | 2011-04-05 | 2016-05-25 | 默克专利有限公司 | 有机电致发光器件 |
| EP2697226B1 (de) | 2011-04-13 | 2017-01-18 | Merck Patent GmbH | Verbindungen für elektronische vorrichtungen |
| WO2012139692A1 (de) | 2011-04-13 | 2012-10-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| JP6022541B2 (ja) | 2011-04-18 | 2016-11-09 | メルク パテント ゲーエムベーハー | 電子デバイスのための化合物 |
| WO2012149992A1 (de) | 2011-05-04 | 2012-11-08 | Merck Patent Gmbh | Vorrichtung zur aufbewahrung von frischwaren |
| KR101884496B1 (ko) | 2011-05-05 | 2018-08-01 | 메르크 파텐트 게엠베하 | 전자 소자용 화합물 |
| KR102014552B1 (ko) | 2011-05-05 | 2019-10-21 | 메르크 파텐트 게엠베하 | 전자 소자용 화합물 |
| US9142791B2 (en) | 2011-05-27 | 2015-09-22 | Universal Display Corporation | OLED having multi-component emissive layer |
| US10103340B2 (en) | 2011-06-03 | 2018-10-16 | Merck Patent Gmbh | Metal complexes |
| EP2726490B1 (de) | 2011-06-28 | 2015-04-29 | Merck Patent GmbH | Metallkomplexe |
| WO2013017189A1 (de) | 2011-07-29 | 2013-02-07 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2013020631A1 (de) | 2011-08-10 | 2013-02-14 | Merck Patent Gmbh | Metallkomplexe |
| DE102012016192A1 (de) | 2011-08-19 | 2013-02-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| KR102051790B1 (ko) | 2011-08-22 | 2019-12-04 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스 |
| EP2782975B1 (de) | 2011-10-27 | 2018-01-10 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| CN104011056B (zh) * | 2011-12-22 | 2017-05-10 | 默克专利有限公司 | 用于有机电致发光器件的化合物 |
| WO2013097920A1 (en) | 2011-12-27 | 2013-07-04 | Merck Patent Gmbh | Metal complexes comprising 1,2,3-triazoles |
| CN106986858B (zh) | 2012-01-16 | 2019-08-27 | 默克专利有限公司 | 有机金属络合物 |
| WO2013120577A1 (en) | 2012-02-14 | 2013-08-22 | Merck Patent Gmbh | Spirobifluorene compounds for organic electroluminescent devices |
| KR101358784B1 (ko) * | 2012-02-14 | 2014-02-10 | 삼성디스플레이 주식회사 | 개선된 효율 특성을 갖는 유기 발광 소자 및 이를 포함하는 유기 발광 표시 장치 |
| WO2013174471A1 (en) | 2012-05-24 | 2013-11-28 | Merck Patent Gmbh | Metal complexes comprising condensed heteroaromatic rings |
| DE102012011335A1 (de) | 2012-06-06 | 2013-12-12 | Merck Patent Gmbh | Verbindungen für Organische Elekronische Vorrichtungen |
| WO2014006913A1 (ja) * | 2012-07-06 | 2014-01-09 | 出光興産株式会社 | ベンゾジアザボロール化合物及びそれを用いた有機エレクトロルミネッセンス素子用材料と有機エレクトロルミネッセンス素子 |
| US9837622B2 (en) | 2012-07-13 | 2017-12-05 | Merck Patent Gmbh | Metal complexes |
| KR102583348B1 (ko) | 2012-07-23 | 2023-09-26 | 메르크 파텐트 게엠베하 | 화합물 및 유기 전계 발광 디바이스 |
| KR20150038193A (ko) | 2012-07-23 | 2015-04-08 | 메르크 파텐트 게엠베하 | 2-디아릴아미노플루오렌의 유도체 및 이를 함유하는 유기 전자 화합물 |
| KR102155492B1 (ko) | 2012-07-23 | 2020-09-14 | 메르크 파텐트 게엠베하 | 플루오렌 및 이를 함유하는 전자 소자 |
| WO2014023377A2 (de) | 2012-08-07 | 2014-02-13 | Merck Patent Gmbh | Metallkomplexe |
| CN107056718A (zh) | 2012-08-10 | 2017-08-18 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| DE112013004610A5 (de) | 2012-09-20 | 2015-06-03 | Merck Patent Gmbh | Metallkomplexe |
| DE102012020167A1 (de) | 2012-10-13 | 2014-04-17 | Eberhard Karls Universität Tübingen | Metallkomplexe |
| EP3806176B1 (de) | 2012-10-31 | 2025-06-25 | Merck Patent GmbH | Elektronische vorrichtung |
| DE102012021650A1 (de) | 2012-11-03 | 2014-05-08 | Eberhard Karls Universität Tübingen | Metallkomplexe |
| EP3378857B1 (de) | 2012-11-12 | 2021-03-24 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| CN104756273B (zh) | 2012-11-20 | 2017-10-24 | 默克专利有限公司 | 用于制造电子器件的高纯度溶剂中的制剂 |
| KR102173856B1 (ko) | 2012-11-30 | 2020-11-04 | 메르크 파텐트 게엠베하 | 전자 소자 |
| US8766531B1 (en) * | 2012-12-14 | 2014-07-01 | Universal Display Corporation | Wearable display |
| CN104871329B (zh) * | 2012-12-18 | 2017-10-24 | 默克专利有限公司 | 有机电致发光器件 |
| US20150340636A1 (en) * | 2013-01-03 | 2015-11-26 | Merck Patent Gmbh | Electronic Device |
| CN104884572B (zh) | 2013-01-03 | 2017-09-19 | 默克专利有限公司 | 用于电子器件的材料 |
| EP2941469A2 (de) | 2013-01-03 | 2015-11-11 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| DE102013008189A1 (de) | 2013-05-14 | 2014-12-04 | Eberhard Karls Universität Tübingen | Metallkomplexe |
| WO2015014434A1 (de) | 2013-07-30 | 2015-02-05 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP3712229A1 (de) | 2013-07-30 | 2020-09-23 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| DE102013013876A1 (de) | 2013-08-20 | 2015-03-12 | Merck Patent Gmbh | Metallkomplexe |
| CN105531347B (zh) * | 2013-09-11 | 2018-09-11 | 默克专利有限公司 | 金属络合物 |
| KR102310370B1 (ko) | 2013-10-02 | 2021-10-07 | 메르크 파텐트 게엠베하 | Oled 에서의 사용을 위한 붕소 함유 화합물 |
| US9390649B2 (en) | 2013-11-27 | 2016-07-12 | Universal Display Corporation | Ruggedized wearable display |
| EP3077382B1 (de) | 2013-12-06 | 2018-12-26 | Merck Patent GmbH | Substituierte oxepine |
| KR102445509B1 (ko) | 2013-12-06 | 2022-09-20 | 메르크 파텐트 게엠베하 | 화합물 및 유기 전자 소자 |
| JP6644688B2 (ja) | 2013-12-12 | 2020-02-12 | メルク パテント ゲーエムベーハー | 電子素子のための材料 |
| CN112851613A (zh) | 2013-12-19 | 2021-05-28 | 默克专利有限公司 | 杂环螺环化合物 |
| KR102434545B1 (ko) | 2014-04-30 | 2022-08-19 | 메르크 파텐트 게엠베하 | 전자 소자용 재료 |
| DE102015006708A1 (de) | 2014-06-12 | 2015-12-17 | Merck Patent Gmbh | Metallkomplexe |
| DE102014008722B4 (de) * | 2014-06-18 | 2024-08-22 | Merck Patent Gmbh | Zusammensetzungen für elektronische Vorrichtungen, Formulierung diese enthaltend, Verwendung der Zusammensetzung, Verwendung der Formulierung sowie organische elektronische Vorrichtung enthaltend die Zusammensetzung |
| US11107994B2 (en) | 2014-06-18 | 2021-08-31 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| KR102419246B1 (ko) | 2014-06-25 | 2022-07-08 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| US10903430B2 (en) | 2014-07-21 | 2021-01-26 | Merck Patent Gmbh | Materials for electronic devices |
| DE102014012818A1 (de) | 2014-08-28 | 2016-03-03 | Eberhard Karls Universität Tübingen | Metallkomplexe |
| CN106687563B (zh) | 2014-09-05 | 2023-03-14 | 默克专利有限公司 | 制剂和电子器件 |
| JP6946186B2 (ja) * | 2014-11-21 | 2021-10-06 | メルク パテント ゲーエムベーハー | ヘテロ環化合物 |
| EP3241248A1 (de) | 2014-12-30 | 2017-11-08 | Merck Patent GmbH | Formulierungen und elektronische vorrichtungen |
| CN107108578A (zh) | 2015-01-30 | 2017-08-29 | 默克专利有限公司 | 电子器件的材料 |
| JP6772188B2 (ja) | 2015-02-03 | 2020-10-21 | メルク、パテント、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングMerck Patent GmbH | 金属錯体 |
| CN107431139B (zh) | 2015-03-30 | 2020-12-01 | 默克专利有限公司 | 包含硅氧烷溶剂的有机功能材料的制剂 |
| JP2018525331A (ja) | 2015-06-10 | 2018-09-06 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| EP3581633B1 (de) | 2015-06-12 | 2021-01-27 | Merck Patent GmbH | Ester mit nichtaromatischen zyklen als lösungsmittel für oled-formulierungen |
| EP3326218B1 (de) | 2015-07-22 | 2021-02-17 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2017016632A1 (en) | 2015-07-29 | 2017-02-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CN107922359A (zh) | 2015-07-30 | 2018-04-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| US10696664B2 (en) | 2015-08-14 | 2020-06-30 | Merck Patent Gmbh | Phenoxazine derivatives for organic electroluminescent devices |
| JP2018527733A (ja) | 2015-08-28 | 2018-09-20 | メルク パテント ゲーエムベーハー | エポキシ基含有溶媒を含む有機機能性材料の調合物 |
| DE102015013381A1 (de) | 2015-10-14 | 2017-04-20 | Eberhard Karls Universität Tübingen | Metallkomplexe |
| CA3002752A1 (en) | 2015-10-26 | 2017-05-04 | Oti Lumionics Inc. | Method for patterning a coating on a surface and device including a patterned coating |
| KR102678422B1 (ko) | 2015-10-27 | 2024-06-25 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| DE102015016016A1 (de) | 2015-12-10 | 2017-06-14 | Eberhard Karls Universität Tübingen | Metallkomplexe |
| KR102721890B1 (ko) | 2015-12-10 | 2024-10-24 | 메르크 파텐트 게엠베하 | 비-방향족 사이클을 함유하는 케톤을 포함하는 제형 |
| CN108369997B (zh) | 2015-12-15 | 2020-03-24 | 默克专利有限公司 | 作为用于有机电子制剂的溶剂的含芳族基团的酯 |
| JP7438661B2 (ja) | 2015-12-16 | 2024-02-27 | メルク パテント ゲーエムベーハー | 固体溶媒を含む調合物 |
| US11407916B2 (en) | 2015-12-16 | 2022-08-09 | Merck Patent Gmbh | Formulations containing a mixture of at least two different solvents |
| WO2017133829A1 (de) | 2016-02-05 | 2017-08-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US10840448B2 (en) | 2016-02-17 | 2020-11-17 | Merck Patent Gmbh | Formulation of an organic functional material |
| DE102016003104A1 (de) | 2016-03-15 | 2017-09-21 | Merck Patent Gmbh | Behälter umfassend eine Formulierung enthaltend mindestens einen organischen Halbleiter |
| TWI745361B (zh) | 2016-03-17 | 2021-11-11 | 德商麥克專利有限公司 | 具有螺聯茀結構之化合物 |
| TWI805547B (zh) | 2016-04-11 | 2023-06-21 | 德商麥克專利有限公司 | 具有二苯并呋喃及/或二苯并噻吩結構之雜環化合物 |
| TWI731981B (zh) | 2016-06-03 | 2021-07-01 | 德商麥克專利有限公司 | 用於有機電激發光裝置之材料 |
| CN109153871A (zh) | 2016-06-16 | 2019-01-04 | 默克专利有限公司 | 有机功能材料的制剂 |
| JP2019523998A (ja) | 2016-06-17 | 2019-08-29 | メルク パテント ゲーエムベーハー | 有機機能材料の調合物 |
| TW201815998A (zh) | 2016-06-28 | 2018-05-01 | 德商麥克專利有限公司 | 有機功能材料之調配物 |
| KR102404836B1 (ko) | 2016-06-30 | 2022-06-02 | 메르크 파텐트 게엠베하 | 금속 착물로부터의 거울상이성질체 혼합물의 분리 방법 |
| KR102432968B1 (ko) | 2016-07-14 | 2022-08-16 | 메르크 파텐트 게엠베하 | 금속 착물 |
| WO2018019687A1 (de) | 2016-07-25 | 2018-02-01 | Merck Patent Gmbh | Di- und oligonukleare metallkomplexe mit tripodalen bidentaten teilliganden sowie deren verwendung in elektronischen vorrichtungen |
| CN109476691B (zh) | 2016-07-25 | 2023-09-12 | Udc爱尔兰有限公司 | 用作有机电致发光器件中的发光体的金属络合物 |
| CN109563402B (zh) | 2016-08-04 | 2022-07-15 | 默克专利有限公司 | 有机功能材料的制剂 |
| WO2018041769A1 (de) | 2016-08-30 | 2018-03-08 | Merck Patent Gmbh | Bl- und trinukleare metallkomplexe aufgebaut aus zwei miteinander verknüpften tripodalen hexadentaten liganden zur verwendung in elektrolumineszenzvorrichtungen |
| EP3512848B1 (de) | 2016-09-14 | 2020-11-18 | Merck Patent GmbH | Verbindungen mit carbazol-strukturen |
| US11447464B2 (en) | 2016-09-14 | 2022-09-20 | Merck Patent Gmbh | Compounds with spirobifluorene-structures |
| EP3515925B1 (de) | 2016-09-21 | 2020-10-21 | Merck Patent GmbH | Binukleare metallkomplexe für den einsatz als emitter in organischen elektrolumineszenzvorrichtungen |
| TWI766884B (zh) | 2016-09-30 | 2022-06-11 | 德商麥克專利有限公司 | 具有二氮雜二苯并呋喃或二氮雜二苯并噻吩結構的化合物、其製法及其用途 |
| KR20250028521A (ko) | 2016-09-30 | 2025-02-28 | 메르크 파텐트 게엠베하 | 디아자디벤조푸란 또는 디아자디벤조티오펜 구조를 갖는 카르바졸 |
| KR102522745B1 (ko) | 2016-10-12 | 2023-04-17 | 메르크 파텐트 게엠베하 | 이핵성 금속 착물 및 상기 금속 착물을 함유하는 전자 디바이스, 특히 유기 전계발광 디바이스 |
| JP7064487B2 (ja) | 2016-10-12 | 2022-05-10 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 金属錯体 |
| US11145828B2 (en) | 2016-10-13 | 2021-10-12 | Merck Patent Gmbh | Metal complexes |
| DE102017008794A1 (de) | 2016-10-17 | 2018-04-19 | Merck Patent Gmbh | Materialien zur Verwendung in elektronischen Vorrichtungen |
| CN109863157A (zh) | 2016-10-25 | 2019-06-07 | 默克专利有限公司 | 金属络合物 |
| CN109890939B (zh) | 2016-10-31 | 2023-07-11 | 默克专利有限公司 | 有机功能材料的制剂 |
| CN109863223B (zh) | 2016-10-31 | 2023-06-20 | 默克专利有限公司 | 有机功能材料的制剂 |
| US11302870B2 (en) | 2016-11-02 | 2022-04-12 | Merck Patent Gmbh | Materials for electronic devices |
| TWI756292B (zh) | 2016-11-14 | 2022-03-01 | 德商麥克專利有限公司 | 具有受體基團與供體基團之化合物 |
| TW201833118A (zh) | 2016-11-22 | 2018-09-16 | 德商麥克專利有限公司 | 用於電子裝置之材料 |
| WO2018095940A1 (en) | 2016-11-25 | 2018-05-31 | Merck Patent Gmbh | Bisbenzofuran-fused indeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (oled) |
| US11584753B2 (en) | 2016-11-25 | 2023-02-21 | Merck Patent Gmbh | Bisbenzofuran-fused 2,8-diaminoindeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (OLED) |
| US11713319B2 (en) | 2016-11-30 | 2023-08-01 | Merck Patent Gmbh | Compounds having valerolactam structures |
| CN118215324B (zh) | 2016-12-02 | 2025-08-15 | Oti照明公司 | 包括设置在发射区域上面的导电涂层的器件及其方法 |
| WO2018104194A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| TW201831468A (zh) | 2016-12-05 | 2018-09-01 | 德商麥克專利有限公司 | 含氮的雜環化合物 |
| KR20190086028A (ko) | 2016-12-05 | 2019-07-19 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| CN110036498B (zh) | 2016-12-06 | 2023-04-18 | 默克专利有限公司 | 电子器件的制备方法 |
| WO2018108760A1 (en) | 2016-12-13 | 2018-06-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018114883A1 (de) | 2016-12-22 | 2018-06-28 | Merck Patent Gmbh | Mischungen umfassend mindestens zwei organisch funktionelle verbindungen |
| CN110049986A (zh) | 2017-01-04 | 2019-07-23 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| CN110177855A (zh) | 2017-01-23 | 2019-08-27 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| CN110198936B (zh) | 2017-01-25 | 2024-03-12 | 默克专利有限公司 | 咔唑衍生物 |
| TWI791481B (zh) | 2017-01-30 | 2023-02-11 | 德商麥克專利有限公司 | 形成有機電致發光(el)元件之方法 |
| TWI763772B (zh) | 2017-01-30 | 2022-05-11 | 德商麥克專利有限公司 | 電子裝置之有機元件的形成方法 |
| KR102559144B1 (ko) | 2017-01-30 | 2023-07-24 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| US12503424B2 (en) | 2017-02-02 | 2025-12-23 | Merck Patent Gmbh | Materials for electronic devices |
| TW201835075A (zh) | 2017-02-14 | 2018-10-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| CN117440703A (zh) | 2017-03-01 | 2024-01-23 | 默克专利有限公司 | 有机电致发光器件 |
| KR102557516B1 (ko) | 2017-03-02 | 2023-07-20 | 메르크 파텐트 게엠베하 | 유기 전자 디바이스용 재료 |
| TW201843143A (zh) | 2017-03-13 | 2018-12-16 | 德商麥克專利有限公司 | 含有芳基胺結構之化合物 |
| TWI780134B (zh) | 2017-03-29 | 2022-10-11 | 德商麥克專利有限公司 | 芳族化合物 |
| WO2018178136A1 (en) | 2017-03-31 | 2018-10-04 | Merck Patent Gmbh | Printing method for an organic light emitting diode (oled) |
| KR102632027B1 (ko) | 2017-04-10 | 2024-01-31 | 메르크 파텐트 게엠베하 | 유기 기능성 재료의 제형 |
| KR102608491B1 (ko) | 2017-04-13 | 2023-11-30 | 메르크 파텐트 게엠베하 | 유기 전자 디바이스용 조성물 |
| WO2018197447A1 (de) | 2017-04-25 | 2018-11-01 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| CN116583131A (zh) | 2017-04-26 | 2023-08-11 | Oti照明公司 | 用于图案化表面上覆层的方法和包括图案化覆层的装置 |
| JP7330898B2 (ja) | 2017-05-03 | 2023-08-22 | メルク パテント ゲーエムベーハー | 有機機能材料の調合物 |
| WO2018211460A1 (en) | 2017-05-17 | 2018-11-22 | Oti Lumionics Inc. | Method for selectively depositing a conductive coating over a patterning coating and device including a conductive coating |
| EP3630764B1 (de) | 2017-05-22 | 2021-08-18 | Merck Patent GmbH | Hexazyklische heteroaromatische verbindungen für elektronische vorrichtungen |
| CN110770363A (zh) | 2017-06-26 | 2020-02-07 | 默克专利有限公司 | 均质混合物 |
| JP7317725B2 (ja) | 2017-06-28 | 2023-07-31 | メルク パテント ゲーエムベーハー | 電子デバイスのための材料 |
| EP3649213B1 (de) | 2017-07-05 | 2021-06-23 | Merck Patent GmbH | Zusammensetzung für organische elektronische vorrichtungen |
| EP4186898A1 (de) | 2017-07-05 | 2023-05-31 | Merck Patent GmbH | Zusammensetzung für organische elektronische verbindungen |
| KR102698061B1 (ko) | 2017-07-18 | 2024-08-22 | 메르크 파텐트 게엠베하 | 유기 기능성 재료의 제형 |
| TWI776926B (zh) | 2017-07-25 | 2022-09-11 | 德商麥克專利有限公司 | 金屬錯合物 |
| TWI779067B (zh) | 2017-07-28 | 2022-10-01 | 德商麥克專利有限公司 | 電子裝置用材料 |
| KR20250007655A (ko) | 2017-09-08 | 2025-01-14 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| CN108675975A (zh) | 2017-10-17 | 2018-10-19 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| WO2019081391A1 (de) | 2017-10-24 | 2019-05-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| TWI785142B (zh) | 2017-11-14 | 2022-12-01 | 德商麥克專利有限公司 | 用於有機電子裝置之組成物 |
| EP3714022B1 (de) | 2017-11-23 | 2023-06-07 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| TWI820057B (zh) | 2017-11-24 | 2023-11-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置的材料 |
| TWI838352B (zh) | 2017-11-24 | 2024-04-11 | 德商麥克專利有限公司 | 用於有機電致發光裝置的材料 |
| TWI637960B (zh) * | 2017-12-01 | 2018-10-11 | Yuan Ze University | 苯並二氮雜硼雜環戊二烯化合物以及有機發光二極體元件 |
| EP3724202B1 (de) | 2017-12-13 | 2022-08-17 | Merck Patent GmbH | Metallkomplexe |
| CN111418081B (zh) | 2017-12-15 | 2024-09-13 | 默克专利有限公司 | 有机功能材料的制剂 |
| KR20240109280A (ko) | 2017-12-15 | 2024-07-10 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 치환된 방향족 아민 |
| TW201938562A (zh) | 2017-12-19 | 2019-10-01 | 德商麥克專利有限公司 | 雜環化合物 |
| TWI811290B (zh) | 2018-01-25 | 2023-08-11 | 德商麥克專利有限公司 | 用於有機電致發光裝置的材料 |
| US11751415B2 (en) | 2018-02-02 | 2023-09-05 | Oti Lumionics Inc. | Materials for forming a nucleation-inhibiting coating and devices incorporating same |
| CN111699192B (zh) | 2018-02-13 | 2024-03-08 | Udc爱尔兰有限公司 | 金属络合物 |
| KR102710151B1 (ko) | 2018-02-26 | 2024-09-25 | 메르크 파텐트 게엠베하 | 유기 기능성 재료의 포뮬레이션 |
| TW201938761A (zh) | 2018-03-06 | 2019-10-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置的材料 |
| TWI802656B (zh) | 2018-03-06 | 2023-05-21 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| TWI828664B (zh) | 2018-03-19 | 2024-01-11 | 愛爾蘭商Udc愛爾蘭責任有限公司 | 金屬錯合物 |
| WO2019215591A1 (en) | 2018-05-07 | 2019-11-14 | Oti Lumionics Inc. | Method for providing an auxiliary electrode and device including an auxiliary electrode |
| US12595256B2 (en) | 2018-05-30 | 2026-04-07 | Merck Patent Gmbh | Composition for organic electronic devices |
| US12419192B2 (en) | 2018-06-07 | 2025-09-16 | Merck Patent Gmbh | Organic electroluminescence devices |
| EP3807367B1 (de) | 2018-06-15 | 2023-07-19 | Merck Patent GmbH | Formulierung aus einem organischen funktionalen material |
| WO2020011686A1 (de) | 2018-07-09 | 2020-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| KR102316066B1 (ko) * | 2018-07-27 | 2021-10-21 | 주식회사 엘지화학 | 잉크 조성물, 이를 이용한 유기 발광 소자 및 이의 제조방법 |
| TWI823993B (zh) | 2018-08-28 | 2023-12-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| WO2020043646A1 (en) | 2018-08-28 | 2020-03-05 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| TWI837167B (zh) | 2018-08-28 | 2024-04-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| EP3850055A1 (de) | 2018-09-12 | 2021-07-21 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| CN112740432B (zh) | 2018-09-24 | 2024-09-20 | 默克专利有限公司 | 用于生产粒状材料的方法 |
| KR20260019662A (ko) | 2018-09-27 | 2026-02-10 | 메르크 파텐트 게엠베하 | 유기 전자 디바이스에서 활성 화합물로 사용될 수 있는 화합물 |
| CN112771024A (zh) | 2018-09-27 | 2021-05-07 | 默克专利有限公司 | 用于制备空间位阻型含氮杂芳族化合物的方法 |
| WO2020089138A1 (en) | 2018-10-31 | 2020-05-07 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11917906B2 (en) | 2018-11-05 | 2024-02-27 | Merck Patent Gmbh | Compounds that can be used in an organic electronic device |
| CN112867709A (zh) | 2018-11-06 | 2021-05-28 | 默克专利有限公司 | 作为用于oled的有机电致发光材料的5,6-二苯基-5,6-二氢-二苯并[c,e][1,2]氮杂磷杂苯和6-苯基-6h-二苯并[c,e][1,2]噻嗪-5,5-二氧化物衍生物及类似化合物 |
| JP2022506510A (ja) | 2018-11-06 | 2022-01-17 | メルク パテント ゲーエムベーハー | 電子デバイスの有機素子を形成する方法 |
| KR20210091769A (ko) | 2018-11-14 | 2021-07-22 | 메르크 파텐트 게엠베하 | 유기 전자 디바이스의 제조에 사용될 수 있는 화합물 |
| KR102845628B1 (ko) | 2018-11-15 | 2025-08-13 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| JP2022508040A (ja) | 2018-11-23 | 2022-01-19 | オーティーアイ ルミオニクス インコーポレーテッド | 光透過領域を含むオプトエレクトロニクスデバイス |
| TW202039493A (zh) | 2018-12-19 | 2020-11-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| TW202035345A (zh) | 2019-01-17 | 2020-10-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| TWI850329B (zh) | 2019-02-11 | 2024-08-01 | 愛爾蘭商Udc愛爾蘭責任有限公司 | 金屬錯合物 |
| KR102803370B1 (ko) | 2019-02-18 | 2025-05-07 | 메르크 파텐트 게엠베하 | 유기 전자 디바이스용 조성물 |
| US20220127286A1 (en) | 2019-03-04 | 2022-04-28 | Merck Patent Gmbh | Ligands for nano-sized materials |
| KR20250160226A (ko) | 2019-03-07 | 2025-11-11 | 오티아이 루미오닉스 인크. | 핵생성 억제 코팅물 형성용 재료 및 이를 포함하는 디바이스 |
| EP3938367A1 (de) | 2019-03-12 | 2022-01-19 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20210141593A (ko) | 2019-03-20 | 2021-11-23 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 재료 |
| EP3947372A1 (de) | 2019-03-25 | 2022-02-09 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| CN113646317B (zh) | 2019-04-15 | 2024-10-18 | Udc爱尔兰有限公司 | 金属络合物 |
| CN113950630A (zh) | 2019-04-18 | 2022-01-18 | Oti照明公司 | 用于形成成核抑制涂层的材料和结合所述成核抑制涂层的装置 |
| US12069938B2 (en) | 2019-05-08 | 2024-08-20 | Oti Lumionics Inc. | Materials for forming a nucleation-inhibiting coating and devices incorporating same |
| JP7618938B2 (ja) * | 2019-05-21 | 2025-01-22 | ユニバーサル ディスプレイ コーポレイション | 有機エレクトロルミネセンス材料及びデバイス |
| KR20240134240A (ko) | 2019-06-26 | 2024-09-06 | 오티아이 루미오닉스 인크. | 광 회절 특성을 갖는 광 투과 영역을 포함하는 광전자 디바이스 |
| US11832473B2 (en) | 2019-06-26 | 2023-11-28 | Oti Lumionics Inc. | Optoelectronic device including light transmissive regions, with light diffraction characteristics |
| CN114342068A (zh) | 2019-08-09 | 2022-04-12 | Oti照明公司 | 包含辅助电极和分区的光电子装置 |
| EP4021903A1 (de) | 2019-08-26 | 2022-07-06 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20220056223A (ko) | 2019-09-02 | 2022-05-04 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| TW202122558A (zh) | 2019-09-03 | 2021-06-16 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| EP4031638B1 (de) | 2019-09-19 | 2026-01-14 | Merck Patent GmbH | Mischung von zwei hostmaterialien und organische elektrolumineszierende vorrichtung damit |
| CN114401945A (zh) | 2019-09-20 | 2022-04-26 | 默克专利有限公司 | 作为用于电子器件的材料的迫位缩合杂环化合物 |
| US20220416172A1 (en) | 2019-10-22 | 2022-12-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| EP4069709B1 (de) | 2019-12-04 | 2025-04-23 | UDC Ireland Limited | Metallkomplexe |
| TW202136471A (zh) | 2019-12-17 | 2021-10-01 | 德商麥克專利有限公司 | 有機電致發光裝置用的材料 |
| JP7620631B2 (ja) | 2019-12-18 | 2025-01-23 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子のための芳香族化合物 |
| US12552818B2 (en) | 2019-12-19 | 2026-02-17 | Merck Patent Gmbh | Polycyclic compounds for organic electroluminescent devices |
| KR102931641B1 (ko) | 2019-12-24 | 2026-02-26 | 오티아이 루미오닉스 인크. | 캡핑 층을 포함하는 발광 장치 및 그 제조방법 |
| KR102822247B1 (ko) * | 2019-12-26 | 2025-06-20 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 및 유기 전계 발광 소자용 다환 화합물 |
| EP4097090A1 (de) | 2020-01-29 | 2022-12-07 | Merck Patent GmbH | Benzimidazol-derivate |
| CN115135741A (zh) | 2020-02-25 | 2022-09-30 | 默克专利有限公司 | 杂环化合物在有机电子器件中的用途 |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| EP4121432A1 (de) | 2020-03-17 | 2023-01-25 | Merck Patent GmbH | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4122028B1 (de) | 2020-03-17 | 2024-10-16 | Merck Patent GmbH | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4126868A1 (de) | 2020-03-24 | 2023-02-08 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| KR20220158771A (ko) | 2020-03-26 | 2022-12-01 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 환형 화합물 |
| KR20220162156A (ko) | 2020-04-02 | 2022-12-07 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 재료 |
| EP4132939B1 (de) | 2020-04-06 | 2024-01-31 | Merck Patent GmbH | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| US20230151235A1 (en) | 2020-04-21 | 2023-05-18 | Merck Patent Gmbh | Formulation of an organic functional material |
| EP4168397B1 (de) | 2020-06-18 | 2025-08-20 | Merck Patent GmbH | Indenoazanaphthaline |
| KR102914927B1 (ko) | 2020-06-23 | 2026-01-19 | 메르크 파텐트 게엠베하 | 혼합물의 제조 방법 |
| KR20230028315A (ko) | 2020-06-29 | 2023-02-28 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 복소환 화합물 |
| KR20230029927A (ko) | 2020-06-29 | 2023-03-03 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 헤테로방향족 화합물 |
| EP4185574A1 (de) | 2020-07-22 | 2023-05-31 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| EP4192832A1 (de) | 2020-08-06 | 2023-06-14 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| CN116134113B (zh) | 2020-08-13 | 2025-12-26 | Udc爱尔兰有限公司 | 金属络合物 |
| EP4200294A1 (de) | 2020-08-18 | 2023-06-28 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| US20230295104A1 (en) | 2020-08-19 | 2023-09-21 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP4222155B1 (de) | 2020-09-29 | 2025-06-11 | UDC Ireland Limited | Mononukleare tripodale hexadentate iridium komplexe zur verwendung in oleds |
| TW202222748A (zh) | 2020-09-30 | 2022-06-16 | 德商麥克專利有限公司 | 用於結構化有機電致發光裝置的功能層之化合物 |
| TW202229215A (zh) | 2020-09-30 | 2022-08-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置功能層之結構化的化合物 |
| CN116406414A (zh) | 2020-10-16 | 2023-07-07 | 默克专利有限公司 | 用于有机电致发光器件的包含杂原子的化合物 |
| WO2022079068A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| TW202231838A (zh) | 2020-10-27 | 2022-08-16 | 德商麥克專利有限公司 | 有機電致發光裝置 |
| US20230422610A1 (en) | 2020-11-10 | 2023-12-28 | Merck Patent Gmbh | Sulfurous compounds for organic electroluminescent devices |
| CN116547286A (zh) | 2020-12-02 | 2023-08-04 | 默克专利有限公司 | 用于有机电致发光器件的杂环化合物 |
| US11985841B2 (en) | 2020-12-07 | 2024-05-14 | Oti Lumionics Inc. | Patterning a conductive deposited layer using a nucleation inhibiting coating and an underlying metallic coating |
| CN116635491A (zh) | 2020-12-08 | 2023-08-22 | 默克专利有限公司 | 油墨体系和用于喷墨印刷的方法 |
| KR20230118615A (ko) | 2020-12-10 | 2023-08-11 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| US20240114782A1 (en) | 2020-12-18 | 2024-04-04 | Merck Patent Gmbh | Indolo[3.2.1-jk]carbazole-6-carbonitrile derivatives as blue fluorescent emitters for use in oleds |
| US20240101560A1 (en) | 2020-12-18 | 2024-03-28 | Merck Patent Gmbh | Nitrogenous heteroaromatic compounds for organic electroluminescent devices |
| WO2022129114A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| KR20230129470A (ko) | 2021-01-05 | 2023-09-08 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| KR20230137375A (ko) | 2021-01-25 | 2023-10-04 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 질소 화합물 |
| KR20230154439A (ko) | 2021-03-02 | 2023-11-08 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 화합물 |
| EP4308664A1 (de) | 2021-03-18 | 2024-01-24 | Merck Patent GmbH | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022207678A1 (de) | 2021-03-30 | 2022-10-06 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| EP4079742B1 (de) | 2021-04-14 | 2026-04-01 | UDC Ireland Limited | Metallkomplexe |
| EP4326826A1 (de) | 2021-04-23 | 2024-02-28 | Merck Patent GmbH | Formulierung eines organischen funktionellen materials |
| EP4330240B1 (de) | 2021-04-29 | 2025-10-15 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20240005782A (ko) | 2021-04-29 | 2024-01-12 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 재료 |
| CN117425655A (zh) | 2021-04-30 | 2024-01-19 | 默克专利有限公司 | 用于有机电致发光器件的含氮杂环化合物 |
| DE112022003409A5 (de) | 2021-07-06 | 2024-05-23 | MERCK Patent Gesellschaft mit beschränkter Haftung | Materialien für organische elektrolumineszenzvorrichtungen |
| CN117980439A (zh) | 2021-09-14 | 2024-05-03 | 默克专利有限公司 | 用于有机电致发光器件的含硼杂环化合物 |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP4409620A1 (de) | 2021-09-28 | 2024-08-07 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| KR20240075872A (ko) | 2021-09-28 | 2024-05-29 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| EP4410071A1 (de) | 2021-09-28 | 2024-08-07 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| TW202349760A (zh) | 2021-10-05 | 2023-12-16 | 德商麥克專利有限公司 | 電子裝置之有機元件的形成方法 |
| KR20240091021A (ko) | 2021-10-27 | 2024-06-21 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 붕소 및 질소 복소환 화합물 |
| KR102549366B1 (ko) * | 2021-11-12 | 2023-07-03 | 삼성디스플레이 주식회사 | 발광 소자 및 이를 포함하는 전자 장치 |
| JP7757154B2 (ja) * | 2021-11-24 | 2025-10-21 | キヤノン株式会社 | 有機化合物及び有機発光素子 |
| WO2023094412A1 (de) | 2021-11-25 | 2023-06-01 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| CN118303151A (zh) | 2021-11-30 | 2024-07-05 | 默克专利有限公司 | 具有芴结构的化合物 |
| CN118401524A (zh) | 2021-12-13 | 2024-07-26 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| WO2023117836A1 (en) | 2021-12-21 | 2023-06-29 | Merck Patent Gmbh | Electronic devices |
| EP4452909A1 (de) | 2021-12-21 | 2024-10-30 | Merck Patent GmbH | Verfahren zur herstellung von deuterierten organischen verbindungen |
| EP4476215A1 (de) | 2022-02-09 | 2024-12-18 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| US20250160204A1 (en) | 2022-02-14 | 2025-05-15 | Merck Patent Gmbh | Materials for electronic devices |
| JP7834495B2 (ja) * | 2022-02-15 | 2026-03-24 | キヤノン株式会社 | 有機化合物及び有機発光素子 |
| EP4719022A3 (de) | 2022-02-23 | 2026-04-15 | UDC Ireland Limited | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| EP4482843A1 (de) | 2022-02-23 | 2025-01-01 | Merck Patent GmbH | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN119156435A (zh) | 2022-05-06 | 2024-12-17 | 默克专利有限公司 | 用于有机电致发光器件的环状化合物 |
| WO2023222559A1 (de) | 2022-05-18 | 2023-11-23 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| CN119325756A (zh) | 2022-06-20 | 2025-01-17 | 默克专利有限公司 | 用于光电器件的杂环化合物 |
| WO2023247338A1 (de) | 2022-06-20 | 2023-12-28 | Merck Patent Gmbh | Organische heterocyclen für photoelektrische vorrichtungen |
| CN119452060A (zh) | 2022-07-11 | 2025-02-14 | 默克专利有限公司 | 用于电子器件的材料 |
| EP4311849B1 (de) | 2022-07-27 | 2025-01-29 | UDC Ireland Limited | Metallkomplexe |
| KR20250075641A (ko) | 2022-09-22 | 2025-05-28 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 질소 함유 헤테로사이클 |
| WO2024061942A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024094592A2 (de) | 2022-11-01 | 2024-05-10 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| TW202440819A (zh) | 2022-12-16 | 2024-10-16 | 德商麥克專利有限公司 | 有機功能性材料之調配物 |
| CN120380877A (zh) | 2022-12-19 | 2025-07-25 | 默克专利有限公司 | 用于电子器件的材料 |
| KR20250126107A (ko) | 2022-12-20 | 2025-08-22 | 메르크 파텐트 게엠베하 | 중수소화 방향족 화합물을 제조하기 위한 방법 |
| WO2024149694A1 (de) | 2023-01-10 | 2024-07-18 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| KR20250131832A (ko) | 2023-01-17 | 2025-09-03 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 헤테로사이클 |
| EP4665715A1 (de) | 2023-02-17 | 2025-12-24 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| CN120787228A (zh) | 2023-03-07 | 2025-10-14 | 默克专利有限公司 | 用于有机电致发光器件的环状氮化合物 |
| EP4683925A1 (de) | 2023-03-20 | 2026-01-28 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2024218109A1 (de) | 2023-04-20 | 2024-10-24 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP4720070A1 (de) | 2023-05-25 | 2026-04-08 | Merck Patent GmbH | Tris[1,2,4]triazolo[1,5-a:1',5'-c:1'',5''-e][1,3,5]triazin-derivate zur verwendung in organischen elektrolumineszenzvorrichtungen |
| WO2025003084A1 (de) | 2023-06-28 | 2025-01-02 | Merck Patent Gmbh | Dicyanoarylverbindungen für organische elektrolumineszenzvorrichtungen |
| EP4486099B1 (de) | 2023-06-30 | 2026-04-29 | UDC Ireland Limited | Verbindungen für organische elektrolumineszenzvorrichtungen |
| CN121487940A (zh) | 2023-07-12 | 2026-02-06 | 默克专利有限公司 | 用于电子器件的材料 |
| KR20260044229A (ko) | 2023-07-27 | 2026-04-01 | 메르크 파텐트 게엠베하 | 유기 발광 디바이스 및 유기 센서를 위한 재료 |
| WO2025032039A1 (en) | 2023-08-07 | 2025-02-13 | Merck Patent Gmbh | Process for the preparation of an electronic device |
| WO2025045843A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| CN121753522A (zh) | 2023-08-30 | 2026-03-27 | 默克专利有限公司 | 用于有机发光器件的材料 |
| WO2025045851A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045935A1 (de) | 2023-08-31 | 2025-03-06 | Merck Patent Gmbh | Cyanogruppen-enthaltende aromaten für organische elektrolumineszenzvorrichtungen |
| WO2025109056A1 (de) | 2023-11-24 | 2025-05-30 | Merck Patent Gmbh | Sauerstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025119821A1 (en) | 2023-12-05 | 2025-06-12 | Merck Patent Gmbh | Material composition for organic electroluminescent devices |
| WO2025132547A1 (en) | 2023-12-21 | 2025-06-26 | Merck Patent Gmbh | Mechanochemical method for deuterating organic compounds |
| WO2025132551A1 (de) | 2023-12-22 | 2025-06-26 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2025181097A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025181044A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025181124A1 (de) | 2024-03-01 | 2025-09-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2025196145A1 (en) | 2024-03-22 | 2025-09-25 | Merck Patent Gmbh | Materials for organic light emitting devices |
| WO2025210013A1 (de) | 2024-04-04 | 2025-10-09 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen, insbesondere verbindungen für oleds |
| WO2026008710A1 (de) | 2024-07-05 | 2026-01-08 | Merck Patent Gmbh | Cyclische siliciumverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2026022016A1 (de) | 2024-07-22 | 2026-01-29 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2026041632A1 (de) | 2024-08-21 | 2026-02-26 | Merck Patent Gmbh | Heterocyclische materialien für organische lichtemittierende vorrichtungen |
| WO2026073855A1 (de) | 2024-10-01 | 2026-04-09 | Merck Patent Gmbh | Siliciumverbindungen für organische elektrolumineszenz-vorrichtungen |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070015005A1 (en) | 2005-07-07 | 2007-01-18 | Chi Mei Optoelectronics Corp. | Organic electroluminescent device and host material of luminescent and hole-blocking material thereof |
| US20070252516A1 (en) | 2006-04-27 | 2007-11-01 | Eastman Kodak Company | Electroluminescent devices including organic EIL layer |
| US20090026937A1 (en) | 2007-07-27 | 2009-01-29 | Masaru Kinoshita | Organic electroluminescent device |
Family Cites Families (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US4780536A (en) | 1986-09-05 | 1988-10-25 | The Ohio State University Research Foundation | Hexaazatriphenylene hexanitrile and its derivatives and their preparations |
| US5061569A (en) | 1990-07-26 | 1991-10-29 | Eastman Kodak Company | Electroluminescent device with organic electroluminescent medium |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| JP3295088B2 (ja) | 1993-09-29 | 2002-06-24 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| DE69412567T2 (de) | 1993-11-01 | 1999-02-04 | Hodogaya Chemical Co., Ltd., Tokio/Tokyo | Aminverbindung und sie enthaltende Elektrolumineszenzvorrichtung |
| DE59510315D1 (de) | 1994-04-07 | 2002-09-19 | Covion Organic Semiconductors | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| DE19652261A1 (de) | 1996-12-16 | 1998-06-18 | Hoechst Ag | Arylsubstituierte Poly(p-arylenvinylene), Verfahren zur Herstellung und deren Verwendung in Elektroluminszenzbauelementen |
| EP0891121B8 (de) | 1996-12-28 | 2013-01-02 | Futaba Corporation | Organische elektrolumineszente elementen |
| JP3302945B2 (ja) | 1998-06-23 | 2002-07-15 | ネースディスプレイ・カンパニー・リミテッド | 新規な有機金属発光物質およびそれを含む有機電気発光素子 |
| CN101312235B (zh) | 1999-05-13 | 2010-06-09 | 普林斯顿大学理事会 | 基于电致磷光的极高效有机发光器件 |
| JP4357781B2 (ja) | 1999-12-01 | 2009-11-04 | ザ、トラスティーズ オブ プリンストン ユニバーシティ | 有機led用燐光性ドーパントとしての式l2mxの錯体 |
| KR100377321B1 (ko) | 1999-12-31 | 2003-03-26 | 주식회사 엘지화학 | 피-형 반도체 성질을 갖는 유기 화합물을 포함하는 전기소자 |
| JP4220644B2 (ja) | 2000-02-14 | 2009-02-04 | 三井化学株式会社 | アミン化合物および該化合物を含有する有機電界発光素子 |
| US20020121638A1 (en) | 2000-06-30 | 2002-09-05 | Vladimir Grushin | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| JP5241053B2 (ja) | 2000-08-11 | 2013-07-17 | ザ、トラスティーズ オブ プリンストン ユニバーシティ | 有機金属化合物及び放射移行有機電気燐光体 |
| JP4154138B2 (ja) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | 発光素子、表示装置及び金属配位化合物 |
| JP4154140B2 (ja) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | 金属配位化合物 |
| JP4154139B2 (ja) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | 発光素子 |
| KR100691543B1 (ko) | 2002-01-18 | 2007-03-09 | 주식회사 엘지화학 | 새로운 전자 수송용 물질 및 이를 이용한 유기 발광 소자 |
| KR20050057518A (ko) | 2002-09-20 | 2005-06-16 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자 |
| DE10249723A1 (de) | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Arylamin-Einheiten enthaltende konjugierte Polymere, deren Darstellung und Verwendung |
| DE10310887A1 (de) | 2003-03-11 | 2004-09-30 | Covion Organic Semiconductors Gmbh | Matallkomplexe |
| JP4185097B2 (ja) | 2003-03-13 | 2008-11-19 | 出光興産株式会社 | 新規含窒素複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| EP1717291A3 (de) * | 2003-04-15 | 2007-03-21 | Merck Patent GmbH | Mischungen von organischen, zur Emission befähigten Halbleitern und Maxtrixmaterialien, deren Verwendung und diese Mischungen enthaltende Elektronikbauteile |
| US8592614B2 (en) | 2003-07-07 | 2013-11-26 | Merck Patent Gmbh | Mixtures of organic emissive semiconductors and matrix materials, their use and electronic components comprising said materials |
| DE10333232A1 (de) | 2003-07-21 | 2007-10-11 | Merck Patent Gmbh | Organisches Elektrolumineszenzelement |
| WO2005029923A1 (en) * | 2003-09-24 | 2005-03-31 | Fuji Photo Film Co., Ltd. | Electroluminescent device |
| DE10345572A1 (de) | 2003-09-29 | 2005-05-19 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| DE10350722A1 (de) | 2003-10-30 | 2005-05-25 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| KR100787425B1 (ko) | 2004-11-29 | 2007-12-26 | 삼성에스디아이 주식회사 | 페닐카바졸계 화합물 및 이를 이용한 유기 전계 발광 소자 |
| US7825249B2 (en) | 2004-05-19 | 2010-11-02 | Merck Patent Gmbh | Metal complexes |
| DE102004034517A1 (de) | 2004-07-16 | 2006-02-16 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| US7803468B2 (en) * | 2004-09-29 | 2010-09-28 | Fujifilm Corporation | Organic electroluminescent element |
| KR100669757B1 (ko) * | 2004-11-12 | 2007-01-16 | 삼성에스디아이 주식회사 | 유기 전계 발광 소자 |
| TW200634020A (en) | 2004-12-09 | 2006-10-01 | Merck Patent Gmbh | Metal complexes |
| EP1830320A4 (de) | 2004-12-24 | 2010-10-20 | Nat Univ Corp Yokohama Nat Uni | Bildverarbeiter |
| KR101239462B1 (ko) | 2005-01-05 | 2013-03-06 | 이데미쓰 고산 가부시키가이샤 | 방향족 아민 유도체 및 이를 이용한 유기 전기발광 소자 |
| KR20070100965A (ko) | 2005-02-03 | 2007-10-15 | 메르크 파텐트 게엠베하 | 금속 착물 |
| JP2006253445A (ja) | 2005-03-11 | 2006-09-21 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子 |
| JP4358884B2 (ja) | 2005-03-18 | 2009-11-04 | 出光興産株式会社 | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| DE102005023437A1 (de) | 2005-05-20 | 2006-11-30 | Merck Patent Gmbh | Verbindungen für organische elektronische Vorrichtungen |
| KR100713989B1 (ko) | 2005-07-15 | 2007-05-04 | 삼성에스디아이 주식회사 | 백색 유기 발광 소자 및 그의 제조방법 |
| US8206839B2 (en) * | 2005-10-04 | 2012-06-26 | Fujifilm Corporation | Organic electroluminescent element |
| DE102006025846A1 (de) | 2006-06-02 | 2007-12-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102006031990A1 (de) | 2006-07-11 | 2008-01-17 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| JP5300255B2 (ja) | 2007-02-07 | 2013-09-25 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子 |
| US20080187748A1 (en) * | 2007-02-07 | 2008-08-07 | Masayuki Mishima | Organic electroluminescence device |
| DE102008015526B4 (de) | 2008-03-25 | 2021-11-11 | Merck Patent Gmbh | Metallkomplexe |
| DE102008027005A1 (de) | 2008-06-05 | 2009-12-10 | Merck Patent Gmbh | Organische elektronische Vorrichtung enthaltend Metallkomplexe |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008036982A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102009007038A1 (de) | 2009-02-02 | 2010-08-05 | Merck Patent Gmbh | Metallkomplexe |
-
2009
- 2009-03-23 DE DE102009014513A patent/DE102009014513A1/de not_active Withdrawn
-
2010
- 2010-02-24 CN CN201080013018.5A patent/CN102362367B/zh active Active
- 2010-02-24 JP JP2012501154A patent/JP5670418B2/ja active Active
- 2010-02-24 US US13/258,214 patent/US9444064B2/en active Active
- 2010-02-24 DE DE112010001236.9T patent/DE112010001236B4/de active Active
- 2010-02-24 WO PCT/EP2010/001123 patent/WO2010108579A1/de not_active Ceased
- 2010-02-24 KR KR1020117024815A patent/KR101704837B1/ko active Active
- 2010-03-18 TW TW099108016A patent/TWI510596B/zh not_active IP Right Cessation
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070015005A1 (en) | 2005-07-07 | 2007-01-18 | Chi Mei Optoelectronics Corp. | Organic electroluminescent device and host material of luminescent and hole-blocking material thereof |
| US20070252516A1 (en) | 2006-04-27 | 2007-11-01 | Eastman Kodak Company | Electroluminescent devices including organic EIL layer |
| US20090026937A1 (en) | 2007-07-27 | 2009-01-29 | Masaru Kinoshita | Organic electroluminescent device |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2010108579A1 (de) | 2010-09-30 |
| DE102009014513A1 (de) | 2010-09-30 |
| DE112010001236A5 (de) | 2012-06-14 |
| CN102362367B (zh) | 2014-06-18 |
| KR20110135974A (ko) | 2011-12-20 |
| KR101704837B1 (ko) | 2017-02-08 |
| US9444064B2 (en) | 2016-09-13 |
| CN102362367A (zh) | 2012-02-22 |
| US20120056169A1 (en) | 2012-03-08 |
| TWI510596B (zh) | 2015-12-01 |
| JP5670418B2 (ja) | 2015-02-18 |
| JP2012521643A (ja) | 2012-09-13 |
| TW201105769A (en) | 2011-02-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE112010001236B4 (de) | Organische elektrolumineszenzvorrichtung | |
| DE112011102558B4 (de) | Organische Elektrolumineszenzvorrichtung | |
| EP2303815B1 (de) | Organische elektrolumineszenzvorrichtung | |
| EP2695213B1 (de) | Organische elektrolumineszenzvorrichtung | |
| DE112011101604B4 (de) | Organische Elektrolumineszenzvorrichtung | |
| DE102009012346B4 (de) | Organische Elektrolumineszenzvorrichtung und Verfahren zu deren Herstellung | |
| EP2826079B1 (de) | Elektronische vorrichtungen | |
| EP2984152B1 (de) | Organische elektrolumineszenzvorrichtung | |
| EP2907173B1 (de) | Elektronische vorrichtung | |
| DE102008063490B4 (de) | Organische Elektrolumineszenzvorrichtung und Verfahren zum Einstellen des Farbortes einer weiß emittierenden Elektrolumineszenzvorrichtung | |
| EP2764558B1 (de) | Organische elektrolumineszenzvorrichtung | |
| EP2984691B1 (de) | Organische lichtemittierende vorrichtung mit verzögerter fluoreszenz | |
| DE102010048497A1 (de) | Formulierungen für organische Elektrolumineszenzvorrichtungen | |
| DE102010010481A1 (de) | Organische Elektrolumineszenzvorrichtung | |
| WO2010069442A1 (de) | Organische elektrolumineszenzvorrichtung | |
| DE102009031021A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| WO2010115498A1 (de) | Organische elektrolumineszenzvorrichtung | |
| WO2021170886A2 (de) | Elektronische vorrichtung | |
| WO2021028513A1 (de) | Elektronische vorrichtung | |
| WO2011035835A1 (de) | Organische elektrolumineszenzvorrichtung |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| R012 | Request for examination validly filed | ||
| R079 | Amendment of ipc main class |
Free format text: PREVIOUS MAIN CLASS: H01L0051500000 Ipc: H01L0051540000 |
|
| R016 | Response to examination communication | ||
| R018 | Grant decision by examination section/examining division | ||
| R079 | Amendment of ipc main class |
Free format text: PREVIOUS MAIN CLASS: H01L0051540000 Ipc: H10K0085000000 |
|
| R020 | Patent grant now final |