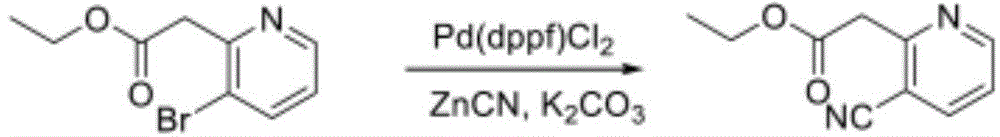CN115836063A - 作为运铁素(ferroportin)抑制剂的环烷基嘧啶 - Google Patents
作为运铁素(ferroportin)抑制剂的环烷基嘧啶 Download PDFInfo
- Publication number
- CN115836063A CN115836063A CN202180047289.0A CN202180047289A CN115836063A CN 115836063 A CN115836063 A CN 115836063A CN 202180047289 A CN202180047289 A CN 202180047289A CN 115836063 A CN115836063 A CN 115836063A
- Authority
- CN
- China
- Prior art keywords
- alkyl
- group
- membered
- pharmaceutically acceptable
- acceptable salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/444—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring heteroatom, e.g. amrinone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/517—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with carbocyclic ring systems, e.g. quinazoline, perimidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/553—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having at least one nitrogen and one oxygen as ring hetero atoms, e.g. loxapine, staurosporine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/70—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/048—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being five-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/056—Ortho-condensed systems with two or more oxygen atoms as ring hetero atoms in the oxygen-containing ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains two hetero rings
- C07D513/04—Ortho-condensed systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Obesity (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
本文所描述的主题针对式I或I'的运铁素抑制剂化合物及其药用盐、制备所述化合物的方法、包含所述化合物的药物组合物,以及施用所述化合物以预防和/或治疗由铁调素缺乏或铁代谢障碍、尤其铁超负荷状态引起的疾病,诸如地中海贫血、镰状细胞疾病及血红素沉着症以及肾损伤的方法。
Description
相关申请的交叉引用
本申请主张2020年4月28日申请的美国临时申请第63/016,891号及2020年12月18日申请的美国临时申请第63/127,774号的权益及优先权,其每一者的内容在此以全文引用的方式并入。
技术领域
本文所描述的主题针对运铁素抑制剂化合物、制备所述化合物的方法、其药物组合物以及其在预防和/或治疗由铁调素缺乏或铁代谢障碍、尤其铁超负荷状态引起的疾病,诸如地中海贫血、镰状细胞疾病及血红素沉着症以及肾损伤中的用途。
背景技术
在几乎所有生物体中,铁为必需微量元素。在人类中,铁为氧运输、氧摄取、诸如粒线体电子传输的细胞功能、认知功能及能量代谢的关键组分。铁以铁蛋白及血铁质形式存在于酶、血红素及肌血球素中。就血红素而言,大约所有铁的一半结合于红血球的血红素中而以血质铁形式存在。人体平均含有约4至5g铁。成年人的铁需求在0.5至1.5毫克/天之间,而婴儿及妊娠期女性每天需要2至5mg铁。
健康成年人的约1mg的正常每日铁损耗通常经由食物摄取补偿。铁平衡主要通过再循环及自衰老红血球的血红素进行铁回收以及以二价及三价铁离子形式进行膳食铁的十二指肠吸收来调控。
吸收是视铁需求及铁积存的多少而由生物体调控的。通常,Fe(III)化合物将在足够酸性的pH值下溶解于胃中并因此可用于吸收。铁的吸收在小肠上段通过黏膜细胞进行。三价非血质铁首先在肠细胞膜中例如通过三价铁还原酶(膜结合十二指肠细胞色素b)还原成Fe(II)以供吸收,使得其随后可借助于转运蛋白DMT1(二价金属转运体1)经转运至肠细胞中。相比之下,血质铁经由细胞膜进入肠上皮细胞而不发生任何变化。在肠上皮细胞中,铁作为积存铁储存于铁蛋白中,或通过转运蛋白运铁素而释放至血液中。通过运铁素转运至血液中的二价铁由氧化酶(血浆铜蓝蛋白,亚铁氧化酶(hephaestin))转化成三价铁。三价铁随后通过运铁蛋白(transferrin)转运至其在生物体中的目的地。(“Balancing acts:molecular control of mammalian iron metabolism”,M.W.Hentze,Cell,1:17,2004,285-297)。铁调素在此程序中起到中心作用,因为其为铁吸收的必需调控因子。铁调素-运铁素系统直接调控铁代谢。
铁吸收及储存通过铁调素调控。铁调素抗微生物肽(HAMP;也称为LEAP-1;还称作铁调素)为25个氨基酸的肽(Krause等人,FEBS Lett.480,147-150,2000)。铁调素具有发夹结构,其含有形成4个二硫桥键的8个半胱氨酸(Jordan等人,J Biol Chem.284,24155-24167,2009)。N端对于铁调控功能显得十分重要,因为前5个氨基酸的缺失导致生物活性完全丧失(Nemeth等人,Blood,107,328-333,2006)。铁调素产生于肝脏中且充当控制肠道铁吸收的主要铁调控激素,并调控其他器官中的铁储存(Ganz,Hematol.Am.Soc.Hematol.Educ.Program,29-35,507 2006;Hunter等人,J.Biol.Chem.277,37597-37603,2002;Park等人,J.Biol.Chem.276,7806-7810,2001)。铁调素通过结合于铁转运分子运铁素且使其降解来限制铁吸收(Sebastiani等人,Front.Pharmacol.7,160,2016)。
铁调素形成的调控与生物体的铁含量直接相关,亦即,若生物体经供应有充足铁及氧,则形成较多铁调素;若铁及氧含量低,或在红血球生成增加的情况下,则形成较少铁调素。在小肠黏膜细胞及巨噬细胞中,铁调素与转运蛋白运铁素结合,运铁素常规地将来自细胞内部的以吞噬方式再循环的铁转运至血液中。
运铁素为在调控体内铁吸收及分布且因此控制血液中的铁含量方面起到关键作用的铁转运体。转运蛋白运铁素为由571个氨基酸组成的跨膜蛋白,其形成于肝脏、脾脏、肾脏、心脏、肠道及胎盘中。详言之,运铁素位于肠上皮细胞的基底膜中。因此,以此方式结合的运铁素用以将铁输出至血液中。在此情况下,运铁素最可能转运呈Fe2+形式的铁。若铁调素结合于运铁素,则会将运铁素转运至细胞内,在其中进行分解,使得随后几乎完全阻断以吞噬方式再循环的铁自细胞的释放。若运铁素例如由铁调素进行不活化,使得其无法输出储存于黏膜细胞中的铁,则所储存的铁经由粪便随细胞的自然排出而损失。当运铁素例如由铁调素进行不活化或抑制时,肠道中的铁吸收因此降低。
铁调素降低使得活性运铁素增加,因此允许增强所储存铁的释放及增强例如自食物的铁吸收,导致血清铁含量增加,亦即,铁超负荷。铁超负荷引起许多疾病及非期望医学病况。铁超负荷可通过自体内移除铁来进行治疗。此治疗包括定期排程的静脉切开术(放血)。对于无法忍受常规抽血的患者,存在可供使用的螯合剂。通过螯合疗法治疗铁超负荷的缺点在于在铁超负荷已经发生时自体内移除螯合铁,而不是预防病症发生。
因此,本领域未有效解决的需求是具有所需功效及治疗潜力的起到运铁素抑制剂作用的化合物。此问题以及其他源于铁不平衡的问题由本文所描述的主题解决。
发明内容
在某些实施方案中,本文所描述的主题针对一种式I或式I'化合物或其药学上可接受的盐。
在某些实施方案中,本文所描述的主题针对一种药物组合物,其包含式I或式I'化合物或其药学上可接受的盐。
在某些实施方案中,本文所描述的主题针对抑制受试者中由运铁素介导的铁转运的方法,其包含向该受试者施用有效量的式I或式I'化合物其药学上可接受的盐,或包含式I或式I'化合物的药物组合物。
在某些实施方案中,本文所描述的主题针对制备式I或式I'化合物的方法。
亦描述其他实施方案。
具体实施方式
本文描述式I及式I'的运铁素抑制剂化合物、制备所述化合物的方法、包含所述化合物的药物组合物以及其在预防和/或治疗由铁调素缺乏或铁代谢障碍、尤其铁超负荷状态引起的疾病,诸如地中海贫血、镰状细胞疾病及血红素沉着症中的用途。运铁素为负责经由肠道吸收所释放的铁及其至血液循环中的转移的铁转运蛋白,铁最终在血液循环中被递送至适当组织及器官。运铁素的不活化或抑制减少或防止铁输出,从而减少肠道中的铁吸收且最终减少体内的铁量。这些化合物、组合物及方法可用于预防及治疗与铁含量增加相关的铁代谢障碍的有效疗法。期望提供展现极少副作用、具有极低毒性及良好生物可用性及兼容性的化合物、组合物及方法。
铁超负荷与各种疾病相关(Blanchette等人,Expert Rev.Hematol.9,169-186,2016)。遗传性血红素沉着症为欧洲最常见的遗传疾病,且由铁调素缺乏或不敏感性引起(Powell等人,The Lancet 388,706-716,2016)。血红素沉着症的临床表达为肝硬化、糖尿病及皮肤色素沉着(Powell等人,The Lancet 388,706-716,2016)。虽然此疾病可通过静脉切开术管控,但此方法可能繁琐且无法处理疾病的病因。
诸如β地中海贫血的铁负荷性贫血亦与铁调素含量降低相关(Origa等人,Haematologica 92,583-588,2007)。用铁调素模拟物治疗此疾病不仅可解决铁超负荷,而且亦显示改善此疾病中发生的无效红血球生成(Casu等人,Blood 128,265-276,2016)。此铁调素模拟物可能主要有益于可能较不依赖于输血的地中海贫血患者,输血可能造成这些患者的铁超负荷。
骨髓纤维化、骨髓发育不良综合征及镰状细胞疾病为特征亦在于无效红血球生成且可能需要频繁输血的疾病(Carreau等人,Blood Rev.30,349-356,2016;Temraz等人,Crit.Rev.Oncol.Hematol.91,64-73,2014;Walter等人,Acta Haematol.122,174-183,2009)。已描述一些这些患者的铁调素含量降低(Cui等人,Leuk.Res.38,545-550,2014;Santini等人,PLoS ONE 6,e23109,2011)。铁调素模拟物亦可有益于这些患者。
真性红血球增多症为特征在于红血球生成增加的疾病。动物模型中已显示,高剂量的铁调素模拟物可通过降低红血球生成而减轻此疾病(Casu等人,Blood 128,265-276,2016)。
铁吸收减少及由此的血清铁含量的降低甚至可有益于铁负荷正常的疾病,诸如肾病(Walker及Agarwal,Nephrol.36,62-70,2016)、铁依赖性细菌感染(Arezes等人,CellHost Microbe 17,47-57,2015)及多微生物败血症(Zeng等人,Anesthesiology,122,374-386,2015)。
铁调素自身作为药物的用途由于其要求复杂制造的复杂结构以及其有限体内作用持续时间而受到限制。已持续努力搜寻可用以增加铁调素含量的铁调素模拟物及化合物。
常见方法涉及小型铁调素来源或铁调素样肽,其可平价生产且可用以治疗铁调素相关疾病及病症,诸如本文所描述的那些疾病及病症。这些所谓的微铁调素为经合理设计的小型肽,其模拟铁调素活性且可适用于治疗铁超负荷以及铁超负荷相关疾病症状。
这些微铁调素肽描述于例如WO 2010/065815 A2及WO 2013/086143A1中。WO2015/157283 A1及对应US 9,315,545 B2描述铁调素模拟肽及其在铁调素相关病症,诸如铁超负荷、β地中海贫血、血红素沉着症等)中的用途,且涵盖Merganser Biotech公司的开发化合物M012,该化合物已在1期临床计划中作为用于包括β地中海贫血、低危骨髓发育不良及真性红血球增多症的多种血液病的有潜力变革疗法进行评估。
WO 2014/145561 A2及WO 2015/200916 A2描述其他小型铁调素肽类似物及其在治疗或预防包括铁超负荷疾病及铁负荷性贫血的各种铁调素相关疾病以及其他相关病症中的用途。此外,WO 2015/042515 A1涉及铁调素及其肽片段,其尤其旨在用于治疗肾缺血再灌注损伤或急性肾损伤。此外,例如Preza等人,J.Clin.Invest.,121(12),4880-4888,2011或CN 104 011 066及WO 2016/109363 A1中描述了微铁调素类似物。
需要亦具有诸如改良的溶解度、稳定性和/或效力的额外有益特性的运铁素抑制剂以及具有铁调素样活性的化合物。本文所描述的式I的运铁素抑制剂化合物的优势在于其可通过本文所公开的合成途径以足够的产率制备。
现将在下文中更充分描述本发明所公开的主题。然而,对于本发明公开主题所属领域的技术人员来说,受益于在前述描述中所呈现的教导的情况下,将想到本文所阐述的本发明所公开主题的许多修改及其他实施方案。因此,应理解,本发明所公开的主题不限于所公开的特定实施方案且那些修改及其他实施方案意欲包括于随附权利要求书的范畴内。换言之,本文所描述的主题涵盖所有替代方案、修饰及等效物。除非另有定义,否则本文所用的所有技术及科学术语皆具有与本领域普通技术人通常所理解相同的含义。本文所提及的所有公开案、专利申请案、专利及其他参考文献均以全文引用的方式并入本文中。在所并入的文献、专利及类似材料中之一或多者,包括但不限于所定义术语、术语用法、所描述的技术等与本申请案不同或矛盾的情况下,以本申请案为准。
I.定义
如本说明书中所用,以下单词、词组及符号一般意欲具有如在下文所阐述的含义,但使用其的上下文另有指示的情况除外。
不在两个字母或符号之间的短划线(“-”)用于指示取代基的连接点。举例而言,-C(O)NH2经由碳原子连接。在化学基团之前端或末端处的短划线为出于方便的目的;可在存在或不存在一个或多个短划线的情况下描绘化学基团而不会丢失其普通含义。在结构中穿过或垂直于线的末端绘制的波浪线或虚线指示基团的指定连接点。除非化学或结构上需要,否则不由化学基团所书写或提出的次序指示或暗示方向性或立体化学。
前缀“Cu-Cv”指示以下基团具有u至v个碳原子。举例而言,“C1-C6烷基”指示烷基具有1至6个碳原子。
本文中对“约”一个值或参数的提及包括(及描述)针对该值或参数本身的实施方案。在某些实施方案中,术语“约”包括指示量±50%。在某些其他实施方案中,术语“约”包括指示量±20%。在某些其他实施方案中,术语“约”包括指示量±10%。在其他实施方案中,术语“约”包括指示量±5%。在某些其他实施方案中,术语“约”包括指示量±1%。在某些其他实施方案中,术语“约”包括指示量±0.5%,且在某些其他实施方案中包括指示量±0.1%。这些变化适合于执行所公开的方法或采用所公开的组合物。此外,术语“约x”包括“x”的描述。此外,除非上下文另有明确规定,否则单数形式“一”及“该”包括复数个提及物。因此,例如对“化合物”的提及包括复数种此类化合物,且对“分析”的提及包括对本领域技术人员已知的一种或多种分析及其等效物的提及。
“烷基”是指非分支链或分支链饱和烃链。如本文所用,烷基具有1至20个碳原子(亦即C1-C20烷基)、1至12个碳原子(亦即C1-C12烷基)、1至8个碳原子(亦即C1-C8烷基)、1至6个碳原子(亦即C1-C6烷基)、1至4个碳原子(亦即C1-C4烷基)或1至3个碳原子(亦即C1-C3烷基)。烷基的例子包括例如甲基、乙基、丙基、异丙基、正丁基、仲丁基、异丁基、叔丁基、戊基、2-戊基、异戊基、新戊基、己基、2-己基、3-己基及3-甲基戊基。当具有特定碳数的烷基通过化学名称命名或通过分子式鉴别时,可涵盖具有该碳数的所有位置异构体;因此,举例而言,“丁基”包括正丁基(亦即-(CH2)3CH3)、仲丁基(亦即-CH(CH3)CH2CH3)、异丁基(亦即-CH2CH(CH3)2)及叔丁基(亦即-C(CH3)3);且“丙基”包括正丙基(亦即-(CH2)2CH3)及异丙基(亦即-CH(CH3)2)。
可使用某些常用替代性化学名称。举例而言,诸如二价“烷基”、二价“芳基”等的二价基团亦可分别称为“亚烷基(alkylene或alkylenyl)”、“亚芳基(arylene或arylenyl)”。此外,除非明确指示,否则当本文将基团的组合称为一个部分(例如芳基烷基或芳烷基)时,最后提及的基团含有该部分藉以连接至分子的其余部分的原子。
“烯基”是指含至少一个碳碳双键且具有2至20个碳原子(亦即C2-C20烯基)、2至8个碳原子(亦即C2-C8烯基)、2至6个碳原子(亦即C2-C6烯基)或2至4个碳原子(亦即C2-C4烯基)的烷基。烯基的例子包括例如乙烯基、丙烯基、丁二烯基(包括1,2-丁二烯基及1,3-丁二烯基)。
“炔基”是指含至少一个碳碳三键且具有2至20个碳原子(亦即C2-C20炔基)、2至8个碳原子(亦即C2-C8炔基)、2至6个碳原子(亦即C2-C6炔基)或2至4个碳原子(亦即C2-C4炔基)的烷基。术语“炔基”亦包括具有一个三键及一个双键的那些基团。
术语“亚烷基”本身或作为另一取代基的部分意谓衍生自烷烃的二价基团,诸如亚甲基-CH2-、亚乙基-CH2CH2-及其类似基团。作为一例,“羟基-亚甲基”是指HO-CH2-*,其中*为与分子的连接点。
“烷氧基”是指基团“烷基-O-”(例如C1-C3烷氧基或C1-C6烷氧基)。烷氧基的例子包括例如甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、叔丁氧基、仲丁氧基、正戊氧基、正己氧基及1,2-二甲基丁氧基。
“烷氧基-烷基”是指基团“-烷基-烷氧基”。术语“C1-C3烷氧基-C1-C3烷基”是指一至三个碳的烷基链,其中任一碳上的一个氢经具有一至三个碳的烷氧基置换,详言之,烷基链的一个碳上的一个氢经具有一至三个碳的烷氧基置换。术语“C1-C6烷氧基-C1-C3烷基”是指一至三个碳的烷基链,其中任一碳上的一个氢经具有一至六个碳的烷氧基置换,详言之,烷基链的一个碳上的一个氢经具有一至六个碳的烷氧基置换。烷氧基-烷基的非限制性实例为-CH2OCH3、-CH2OC(CH3)3及-C(CH3)2CH2OCH3。
“烷硫基”是指基团“烷基-S-”。“烷基硫烷基”是指基团-烷基-S-烷基,诸如-C1-C3烷基-S-C1-C3烷基。烷基硫烷基的非限制性实例为-CH2CH2SCH3。“烷基亚磺酰基”是指基团“烷基-S(O)-”。“烷基磺酰基”是指基团“烷基-S(O)2-”。“烷基磺酰烷基”是指-烷基-S(O)2-烷基。
“酰基”是指基团-C(O)Ry,其中Ry为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。酰基的例子包括例如甲酰基、乙酰基、环己基羰基、环己基甲基-羰基及苯甲酰基。
“酰胺基”是指“C-酰胺基”及“N-酰胺基”两者,“C-酰胺基”是指基团-C(O)NRyRz且“N-酰胺基”是指基团-NRyC(O)Rz,其中Ry及Rz独立地为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义,或Ry及Rz一起形成环烷基或杂环基;其中的每一者可任选经取代,如本文所定义。
“氨基”是指基团-NRyRz,其中Ry及Rz独立地为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。
“脒基”是指-C(NRy)(NRz 2),其中Ry及Rz独立地为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。
“芳基”是指具有单个环(例如单环)或多个环(例如双环或三环)的包括稠合系统的芳族碳环基。如本文所用,芳基具有6至20个环碳原子(亦即C6-C20芳基)、6至12个碳环原子(亦即C6-C12芳基)或6至10个碳环原子(亦即C6-C10芳基)。芳基的例子包括例如苯基、萘基、芴基及蒽基。然而,芳基不以任何方式涵盖下文所定义的杂芳基或与其重叠。若一个或多个芳基与杂芳基稠合,则所得环系统为杂芳基,无论连接点如何。若一个或多个芳基与杂环基稠合,则所得环系统为杂环基,无论连接点如何。
“芳基烷基”或“芳烷基”是指基团“芳基-烷基-”,诸如(C6-C10芳基)-C1-C3烷基。如本文所用,“(C6-C10芳基)-C1-C3烷基”是指一至三个碳的烷基链,其中任一碳上的氢原子中之一者经具有六至十个碳原子的芳基置换,详言之,烷基链的一个碳上的一个氢经具有六至十个碳原子的芳基置换。芳基烷基的非限制性实例为苯甲基。
“氨甲酰基”是指“O-氨甲酰基”及“N-氨甲酰基”,“O-氨甲酰基”是指基团-O-C(O)NRyRz且“N-氨甲酰基”是指基团-NRyC(O)ORz,其中Ry及Rz独立地为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。
“羧基酯”或“酯”是指-OC(O)Rx及-C(O)ORx两者,其中Rx为烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。
“环烷基”是指具有单个环或多个环的包括稠合、桥接及螺环系统的饱和或部分不饱和环烷基。术语“环烷基”包括环烯基(亦即,具有至少一个双键的环基)及具有至少一个sp3碳原子的碳环稠合环系统(亦即至少一个非芳族环)。如本文所用,环烷基具有3至20个环碳原子(亦即C3-C20环烷基)、3至12个环碳原子(亦即C3-C12环烷基)、3至10个环碳原子(亦即C3-C10环烷基)、3至8个环碳原子(亦即C3-C8环烷基)、3至7个环碳原子(亦即C3-C7环烷基)或3至6个环碳原子(亦即C3-C6环烷基)。单环基团包括例如环丙基、环丁基、环戊基、环己基、环庚基及环辛基。多环基团包括例如桥联和/或稠合环,诸如双环[2.2.1]庚烷基、双环[2.2.2]辛烷基、双环[1.1.1]戊-1-基、金刚烷基、降冰片基、十氢萘基、7,7-二甲基-双环[2.2.1]庚烷基及其类似基团。此外,术语环烷基意欲涵盖包含任何可与芳环稠合的非芳族烷基环的任何环或环系统,无论与分子的其余部分的连接如何。此外,当在同一碳原子上存在两个取代位时,环烷基亦包括“螺环烷基”,例如螺[2.5]辛烷基、螺[4.5]癸烷基或螺[5.5]十一烷基。
“环烷基烷基”是指基团“环烷基-烷基-”,诸如(C3-C6环烷基)-C1-C3烷基。如本文所用,“(C3-C6环烷基)-C1-C3烷基”是指一至三个碳的烷基链,其中任一碳上的氢原子中之一者经具有三至六个碳原子的环烷基置换,详言之,链的一个碳上的一个氢经具有三至六个碳原子的环烷基置换。
“环烷基-烷氧基”是指基团“-烷氧基-环烷基”(例如C3-C7环烷基-C1-C6烷氧基-或C3-C7环烷基-C1-C3烷氧基-),诸如-OCH2-环丙基。如本文所用,“C3-C7环烷基-C1-C6烷氧基”是指具有一至六个碳的烷基链的烷氧基,其中任一碳上的氢原子中之一者经具有三至七个碳原子的环烷基置换,详言之,该链的一个碳上的一个氢经具有三至七个碳原子的环烷基置换。如本文所用,“C3-C7环烷基-C1-C3烷氧基”是指具有一至三个碳的烷基链的烷氧基,其中任一碳上的氢原子中之一者经具有三至七个碳原子的环烷基置换,详言之,该链的一个碳上的一个氢经具有三至七个碳原子的环烷基置换。
“胍基”是指-NRyC(=NRz)(NRyRz),其中各Ry及Rz独立地为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。
“肼基”是指-NHNH2。
“亚氨基”是指基团-C(NRy)Rz,其中Ry及Rz各独立地为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。
“酰亚氨基”是指基团-C(O)NRyC(O)Rz,其中Ry及Rz各独立地为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。
“卤素”或“卤素”是指占据元素周期表的VIIA族的原子,诸如氟基(氟)、氯基(氯)、溴基(溴)或碘基(碘)。
“卤烷基”是指如上文所定义的非分支链或分支链烷基,其中一个或多个(例如1至6或1至3个)氢原子经卤素置换。举例而言,卤代-C1-C3烷基是指具有1至3个碳的烷基,其中至少一个氢原子经卤素置换。在残基经超过一个卤素取代的情况下,可通过使用对应于所连接的卤素部分的数目之前缀来提及。二卤烷基及三卤烷基是指经两个(“二”)或三个(“三”)卤素取代的烷基,所述卤素可为(但未必为)相同卤素。卤烷基的例子包括例如三氟甲基、二氟甲基、氟甲基、三氯甲基、2,2,2-三氟乙基、1,2-二氟乙基、3-溴-2-氟丙基、1,2-二溴乙基及其类似基团。
“卤烷氧基”是指如上文所定义的烷氧基,其中一个或多个(例如1至6或1至3个)氢原子经卤素置换。卤烷氧基的非限制性实例为-OCH2CF3、-OCF2H及-OCF3。
“羟烷基”是指如上文所定义的烷基,其中一个或多个(例如1至6或1至3个)氢原子经羟基置换(例如羟基-C1-C3烷基、羟基-C1-C6烷基)。术语“羟基-C1-C3烷基”是指一至三个碳的烷基链,其中任一碳上的一个或多个氢经羟基置换,详言之,该链的一个碳上的一个氢经羟基置换。术语“羟基-C1-C6烷基”是指一至六个碳的烷基链,其中任一碳上的一个或多个氢经羟基置换,详言之,该链的一个碳上的一个氢经羟基置换。羟烷基的非限制性实例包括-CH2OH、-CH2CH2OH及-C(CH3)2CH2OH。
“羟基烷氧基”是指基团“-烷氧基-羟基”(例如羟基-C1-C3烷氧基、羟基-C1-C6烷氧基)。术语“羟基-C1-C3烷氧基”是指含有一至三个碳的烷基链的烷氧基,其中任一碳上的一个或多个氢经羟基置换,详言之,该链的一个碳上的一个氢经羟基置换。术语“羟基-C1-C6烷氧基”是指含有一至六个碳的烷基链的烷氧基,其中任一碳上的一个或多个氢经羟基置换,详言之,该链的一个碳上的一个氢经羟基置换。羟基烷氧基的非限制性实例包括-OCH2CH2OH及-OCH2C(CH3)2OH。
“杂烷基”是指其中碳原子(及任何相关氢原子)中之一或多者各独立地经相同或不同杂原子基团置换的烷基,条件是与分子的其余部分的连接点经由碳原子。在某些实施方案中,杂烷基可具有1至3个碳原子(例如C1-C3杂烷基)或1至6个碳原子(例如C1-C6杂烷基)及一个或多个(例如1、2或3个)杂原子或杂原子基团。术语“杂烷基”包括具有碳及杂原子的非分支链或分支链饱和链。举例而言,“杂烷基”中的烷基的1、2或3个碳原子可独立地经相同或不同杂原子基团置换。杂原子基团包括但不限于:-NRy-、-O-、-S-、-S(O)-、-S(O)2-及其类似基团,其中Ry为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。杂烷基的例子包括例如醚基(例如-CH2OCH3、-CH(CH3)OCH3、-CH2CH2OCH3、-CH2CH2OCH2CH2OCH3等)、硫醚基(例如-CH2SCH3、-CH(CH3)SCH3、-CH2CH2SCH3、-CH2CH2SCH2CH2SCH3等)、砜基(例如-CH2S(O)2CH3、-CH(CH3)S(O)2CH3、-CH2CH2S(O)2CH3、-CH2CH2S(O)2CH2CH2OCH3等)及氨基(例如-CH2NRyCH3、-CH(CH3)NRyCH3、-CH2CH2NRyCH3、-CH2CH2NRyCH2CH2NRyCH3等,其中Ry为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义)。在某些实施方案中,杂烷基可具有1至20个碳原子、1至15个碳原子、1至12个碳原子、1至10个碳原子、1至8个碳原子或1至4个碳原子;以及1至3个杂原子、1至2个杂原子或1个杂原子。
“杂芳基”是指具有单个环、多个环或多个稠合环的芳族基,其中一个或多个环杂原子独立地选自氮、氧及硫。如本文所用,杂芳基包括1至20个环碳原子(亦即C1-C20杂芳基)、3至12个环碳原子(亦即C3-C12杂芳基)或3至8碳环原子(亦即C3-C8杂芳基),以及1至5个环杂原子、1至4个环杂原子、1至3个环杂原子、1至2个环杂原子或1个环杂原子,所述环杂原子独立地选自氮、氧及硫。在某些情况下,杂芳基包括9元至10元环系统(亦即9元至10元杂芳基)、5元至10元环系统(亦即5元至10元杂芳基)、5元至7元环系统(亦即5元至7元杂芳基)、5元至6元环系统(亦即5元至6元杂芳基)或4元至6元环系统(亦即4元至6元杂芳基),其各独立地具有独立地选自氮、氧及硫的1至4个环杂原子、1至3个环杂原子、1至2个环杂原子或1个环杂原子。杂芳基的例子包括例如吖啶基、苯并咪唑基、苯并噻唑基、苯并吲哚基、苯并呋喃基、苯并噻唑基、苯并噻二唑基、苯并萘并呋喃基、苯并噁唑基、苯并噻吩基(benzothienyl/benzothiophenyl)、苯并三唑基、苯并[4,6]咪唑并[1,2-a]吡啶基、咔唑基、噌啉基、二苯并呋喃基、二苯并噻吩基、呋喃基、异噻唑基、咪唑基、吲唑基、吲哚基、吲唑基、异吲哚基、异喹啉基、异噁唑基、萘啶基、噁二唑基、噁唑基、1-氧离子基吡啶基、1-氧离子基嘧啶基、1-氧离子基吡嗪基、1-氧离子基哒嗪基、吩嗪基、酞嗪基、喋啶基、嘌呤基、吡咯基、吡唑基、吡啶基、吡嗪基、嘧啶基、哒嗪基、喹唑啉基、喹噁啉基、喹啉基、奎宁基、异喹啉基、噻唑基、噻二唑基、三唑基、四唑基及三嗪基。稠合杂芳基环的例子包括但不限于苯并[d]噻唑基、喹啉基、异喹啉基、苯并[b]噻吩基、吲唑基、苯并[d]咪唑基、吡唑并[1,5-a]吡啶基及咪唑并[1,5-a]吡啶基,其中该杂芳基可经由稠合系统的任一环结合。具有单个或多个稠合环、含有至少一个杂原子的任何芳族环视为杂芳基,无论与分子的其余部分的连接如何(亦即,经由所述稠合环中的任一者)。杂芳基不涵盖如上文所定义的芳基或不与其重叠。
“杂芳基烷基”是指基团“杂芳基-烷基-”,诸如(5元至10元单环杂芳基)-C1-C3烷基。如本文所用,“(5元至10元单环杂芳基)-C1-C3烷基”是指一至三个碳的烷基链,其中任一碳上的一个或多个氢经具有5元至10元的单环杂芳基置换,详言之,该链的一个碳上的一个氢经5元至10元单环杂芳基置换。
“杂环基”是指具有一个或多个独立地选自氮、氧及硫的环杂原子的饱和或部分不饱和环烷基。术语“杂环基”包括杂环烯基(亦即具有至少一个双键的杂环基)、桥接杂环基、稠合杂环基及螺杂环基。杂环基可为单个环或多个环,其中多个环可经稠合、桥联或螺接。含有至少一个杂原子的任何非芳族环视为杂环基,无论连接如何(亦即,可经由碳原子或杂原子结合)。此外,术语杂环基意欲涵盖包含可与芳环或杂芳环稠合的含有至少一个杂原子的任何非芳族环的环或环系统,无论与分子的其余部分的连接如何。术语杂环基亦意欲涵盖包含与杂芳环稠合的环烷基环的环系统,无论与分子的其余部分的连接如何。另外,术语杂环基意欲涵盖包含与杂环基环稠合的环烷基环的环系统,无论与分子的其余部分的连接如何。如本文所用,杂环基具有2至20个环碳原子(亦即C2-C20杂环基)、2至12个环碳原子(亦即C2-C12杂环基)、2至10个环碳原子(亦即C2-C10杂环基)、2至8个环碳原子(亦即C2-C8杂环基)、3至12个环碳原子(亦即C3-C12杂环基)、3至8个环碳原子(亦即C3-C8杂环基)或3至6个环碳原子(亦即C3-C6杂环基);具有1至5个环杂原子、1至4个环杂原子、1至3个环杂原子、1至2个环杂原子或1个环杂原子,所述环杂原子独立地选自氮、硫或氧。当杂环基环含有4至6个环原子时,其在本文中亦称作4元至6元杂环基。本文亦公开分别具有5或6个环原子的5元或6元杂环基及具有5至10个环原子的5元至10元杂环基。杂环基的例子包括例如氮杂环丁烷基、氮杂卓基、苯并间二氧杂环戊烯基、苯并[b][1,4]二氧呯基、1,4-苯并二氧杂环己烷基、苯并吡喃基、苯并间二氧杂环己烯基、苯并吡喃酮基、苯并呋喃酮基、二氧戊环基、二氢吡喃基、氢吡喃基、噻吩基[1,3]二噻烷基、十氢异喹啉基、呋喃酮基、咪唑啉基、咪唑啶基、吲哚啉基、吲哚啉嗪基、异吲哚啉基、异噻唑啶基、异噁唑啶基、吗啉基、八氢吲哚基、八氢异吲哚基、2-氧代哌嗪基、2-氧代哌啶基、2-氧代吡咯烷基、噁唑啶基、环氧乙烷基、氧杂环丁烷基、吩噻嗪基、啡噁嗪基、哌啶基、哌嗪基、4-哌啶酮基、吡咯烷基、吡唑啶基、奎宁基、噻唑啶基、四氢呋喃基、四氢吡喃基、三噻烷基、四氢喹啉基、噻吩基(thiophenyl/thienyl)、四氢吡喃基、硫吗啉基、噻吗啉基、1-氧代-硫吗啉基及1,1-二氧代-硫吗啉基。在某些实施方案中,当同一碳原子上存在两个取代位时,术语“杂环基”可包括“螺杂环基”。螺杂环基环的例子包括例如双环及三环系统,诸如2-氧杂-7-氮螺[3.5]壬烷基、2-氧杂-6-氮螺[3.4]辛烷基及6-氧杂-1-氮螺[3.3]庚烷基。稠合杂环基环的例子包括但不限于:1,2,3,4-四氢异喹啉基、4,5,6,7-四氢噻吩并[2,3-c]吡啶基、吲哚啉基及异吲哚啉基,其中该杂环基可经由稠合系统的任一环结合。
“杂环基烷基”是指基团“杂环基-烷基-”。
“肟”是指基团-CRy(=NOH),其中Ry为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。
“氧代”是指基团(=O)。
“磺酰基”是指基团-S(O)2Ry,其中Ry为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。磺酰基的例子为甲磺酰基、乙磺酰基、苯磺酰基及甲苯磺酰基。
“亚磺酰基”是指基团-S(O)Ry,其中Ry为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。亚磺酰基的例子为甲基亚磺酰基、乙基亚磺酰基、苯亚磺酰基及甲苯亚磺酰基。
“磺酰胺基”是指基团-SO2NRyRz及-NRySO2Rz,其中Ry及Rz各独立地为氢、烷基、烯基、炔基、环烷基、杂环基、芳基、杂烷基或杂芳基;其中的每一者可任选经取代,如本文所定义。
术语“任选存在”或“任选”意谓随后所描述的事件或情形可发生或可不发生,且该描述包括该事件或情形发生的情况及该事件或情形不发生的情况。此外,术语“任选经取代”是指指定原子或基团上的任一个或多个(例如1至5、1至4或1至3个)氢原子可经或可不经除氢以外的部分置换。
本文所用的术语“经取代”意谓以上基团(亦即,烷基、烯基、炔基、亚烷基、烷氧基、卤烷基、卤烷氧基、环烷基、芳基、杂环基、杂芳基和/或杂烷基)中的任一者中至少一个(例如1至5、1至4或1至3个)氢原子经连至非氢原子之一键置换,该非氢原子诸如但不限于烷基、烯基、炔基、烷氧基、烷硫基、酰基、酰胺基、氨基、脒基、芳基、芳烷基、叠氮基、氨甲酰基、羧基、羧基酯、氰基、环烷基、环烷基烷基、胍基、卤素、卤烷基、卤烷氧基、羟烷基、杂烷基、杂芳基、杂芳基烷基、杂环基、杂环基烷基、-NHNH2、=NNH2、亚氨基、酰亚氨基、羟基、氧代、肟、硝基、磺酰基、亚磺酰基、烷基磺酰基、烷基亚磺酰基、硫氰酸酯基、-S(O)OH、-S(O)2OH、磺酰胺基、硫醇基、硫酮基、N-氧化物或-Si(Ry)3,其中各Ry独立地为氢、烷基、烯基、炔基、杂烷基、环烷基、芳基、杂芳基或杂环基。
在某些实施方案中,“经取代”包括以上烷基、烯基、炔基、环烷基、杂环基、芳基或杂芳基中的任一者中一个或多个(例如1至5、1至4或1至3个)氢原子独立地经氘、卤素、氰基、硝基、叠氮基、氧代、烷基、烯基、炔基、卤烷基、环烷基、杂环基、芳基、杂芳基、-NRgRh、-NRgC(=O)Rh、-NRgC(=O)NRgRh、-NRgC(=O)ORh、-NRgS(=O)1-2Rh、-C(=O)Rg、-C(=O)ORg、-OC(=O)ORg、-OC(=O)Rg、-C(=O)NRgRh、-OC(=O)NRgRh、-ORg、-SRg、-S(=O)Rg、-S(=O)2Rg、-OS(=O)1-2Rg、-S(=O)1-2ORg、-NRgS(=O)1-2NRgRh、=NSO2Rg、=NORg、-S(=O)1-2NRgRh、-SF5、-SCF3或-OCF3置换。在某些实施方案中,“经取代”亦意谓以上基团中的任一者中一个或多个(例如1至5、1至4或1至3个)氢原子经-C(=O)Rg、-C(=O)ORg、-C(=O)NRgRh、-CH2SO2Rg或-CH2SO2NRgRh置换。在前述内容中,Rg及Rh为相同或不同的且独立地为氢、烷基、烯基、炔基、烷氧基、硫烷基、芳基、芳烷基、环烷基、环烷基烷基、卤烷基、杂环基、杂环基烷基、杂芳基和/或杂芳基烷基。在某些实施方案中,“经取代”亦意谓以上基团中的任一者中一个或多个(例如1至5、1至4或1至3个)氢原子经连至以下之一键置换:氨基、氰基、羟基、亚氨基、硝基、氧代、硫酮基、卤素、烷基、烷氧基、烷氨基、硫烷基、芳基、芳烷基、环烷基、环烷基烷基、卤烷基、杂环基、N-杂环基、杂环基烷基、杂芳基和/或杂芳基烷基,或Rg及Rh以及Ri中的两者与其所连接的原子一起形成任选经氧代、卤素或烷基取代的杂环基环,该烷基任选经氧代、卤素、氨基、羟基或烷氧基取代。
本文不意欲包括通过用无限地附加的其他取代基(例如,具有经取代烷基的经取代芳基,该经取代烷基本身由经取代芳基取代,该经取代芳基进一步由经取代杂烷基取代等等)定义取代基所获得的聚合物或类似无限结构。除非另外指出,否则本文所描述的化合物中的连续取代的最大数目为三。举例而言,用两个其他经取代芳基连续取代经取代芳基受限于经(经(经取代芳基)取代的芳基)取代的芳基。类似地,以上定义不意欲包括不允许的取代模式(例如,经5个氟取代的甲基或具有两个邻接氧环原子的杂芳基)。此类不允许的取代模式为本领域技术人员所熟知的。当用于修饰化学基团时,术语“经取代”可描述本文中所定义的其他化学基团。
在某些实施方案中,如本文所用,词组“一个或多个”是指一至五个。在某些实施方案中,如本文所用,词组“一个或多个”是指一至四个。在某些实施方案中,如本文所用,词组“一个或多个”是指一至三个。
本文中所给出的任何化合物或结构意欲表示该化合物的未经标记的形式以及经同位素标记的形式(同位素物)。这些化合物形式亦可称作且包括“经同位素富集类似物”。经同位素标记的化合物具有本文中描绘的结构,但一个或多个原子经具有所选原子质量或质量数的原子置换除外。可并入所公开的化合物中的同位素的实例包括:氢、碳、氮、氧、磷、氟、氯及碘的同位素,分别诸如2H、3H、11C、13C、14C、13N、15N、15O、17O、18O、31P、32P、35S、18F、36Cl、123I及125I。经各种同位素标记的本发明化合物为例如其中并有诸如3H、13C及14C的放射性同位素的那些化合物。这些经同位素标记的化合物可适用于代谢研究;反应动力学研究;检测或成像技术,诸如正电子发射断层摄影术(PET)或单光子放射计算机断层摄影术(SPECT),包括药物或底物组织分布分析;或适用于患者的放射性治疗。
术语“经同位素富集类似物”包括本文所描述的化合物的“氘代类似物”,其中一个或多个氢,诸如碳原子上的氢经氘置换。此类化合物展现增加的代谢抗性,且因此当向哺乳动物(尤其人类)施用时,适用于增加任何化合物的半衰期。参见例如Foster,“DeuteriumIsotope Effects in Studies of Drug Metabolism”,Trends Pharmacol.Sci.5(12):524-527(1984)。此类化合物为通过本领域熟知的手段合成,例如通过采用其中一个或多个氢已由氘置换的起始物质。
本发明的经氘标记或取代的治疗性化合物可具有改良的DMPK(药物代谢及药物动力学)特性,所述特性与分布、代谢及排泄相关(ADME)。用较重同位素(诸如氘)取代可得到由更大代谢稳定性产生的某些治疗优势,例如增加的体内半衰期、降低的剂量需求和/或治疗指数的改良。经18F、3H、11C标记的化合物可适用于PET或SPECT或其他成像研究。本发明的经同位素标记的化合物及其前药一般可通过进行流程中或下文所描述的例子及制备中所公开的程序,通过用易于获得的经同位素标记的试剂取代非同位素标记的试剂来制备。应理解,在此上下文中,将氘视为本文所描述的化合物的取代基。
可通过同位素富集因子来界定此类较重同位素(尤其氘)的浓度。在本发明的化合物中,未明确指定为特定同位素的任何原子意在表示彼原子的任何稳定同位素。除非另有说明,否则当位置经明确指定为“H”或“氢”时,应理解该位置在其天然丰度同位素组成中具有氢。因此,在本发明的化合物中,明确指定为氘(D)的任何原子意在表示氘。此外,在一些实施方案中,提供对应氘代类似物。
在许多情况下,本发明的化合物能够借助于氨基和/或羧基或与其类似的基团的存在而形成酸盐和/或碱盐。
亦提供本文所描述的化合物的药学上可接受的盐、经同位素富集类似物、氘代类似物、异构体(诸如立体异构体)、异构体混合物(诸如立体异构体混合物)、前药及代谢物。
“药学上可接受”或“生理学上可接受”是指化合物、盐、组合物、剂型及其他物质适用于制备适合于兽医学或人类药物用途的药物组合物。
术语给定化合物的“药学上可接受的盐”是指保留所给定化合物的生物学有效性及特性且在生物学上或其他方面并非不合需要的盐。“药学上可接受的盐”或“生理学上可接受的盐”包括例如与无机酸所成的盐及与有机酸所成的盐。另外,若本文中所描述的化合物以酸加成盐形式获得,则可通过使酸盐溶液碱化来获得游离碱。反之,若产物为游离碱,则可根据由碱化合物制备酸加成盐的常规程序,通过将游离碱溶解于适合有机溶剂中且用酸处理溶液来产生加成盐,尤其药学上可接受的加成盐。本领域技术人员将认识到可用于制备无毒性药学上可接受的加成盐的各种合成方法。药学上可接受的酸加成盐可自无机酸及有机酸制备。衍生自无机酸的盐包括例如盐酸、氢溴酸、硫酸、硝酸、磷酸及其类似者的盐。衍生自有机酸的盐包括例如乙酸、丙酸、葡糖酸、乙醇酸、丙酮酸、草酸、苹果酸、丙二酸、丁二酸、顺丁烯二酸、反丁烯二酸、酒石酸、柠檬酸、苯甲酸、肉桂酸、杏仁酸、甲磺酸、乙磺酸、对甲苯磺酸、水杨酸及其类似物的盐。同样,药学上可接受的碱加成盐可由无机碱及有机碱制备。仅举例而言,衍生自无机碱的盐包括钠盐、钾盐、锂盐、铝盐、铵盐、钙盐及镁盐。衍生自有机碱的盐包括但不限于伯胺、仲胺及叔胺的盐,诸如烷基胺(亦即NH2(烷基))、二烷基胺(亦即HN(烷基)2)、三烷基胺(亦即N(烷基)3)、经取代的烷基胺(亦即NH2(经取代的烷基))、二(经取代的烷基)胺(亦即HN(经取代的烷基)2)、三(经取代的烷基)胺(亦即N(经取代的烷基)3)、烯基胺(亦即NH2(烯基))、二烯基胺(亦即HN(烯基)2)、三烯基胺(亦即N(烯基)3)、经取代的烯基胺(亦即NH2(经取代的烯基))、二(经取代的烯基)胺(亦即HN(经取代的烯基)2)、三(经取代的烯基)胺(亦即N(经取代的烯基)3)、单环烷基、二环烷基或三环烷基胺(亦即,NH2(环烷基)、HN(环烷基)2、N(环烷基)3)、单芳基、二芳基或三芳基胺(亦即,NH2(芳基)、HN(芳基)2、N(芳基)3)或混合胺等。仅举例而言,适合的胺的特定实施例包括异丙胺、三甲基胺、二乙基胺、三(异丙基)胺、三(正丙基)胺、乙醇胺、2-二甲氨基乙醇、哌嗪、哌啶、吗啉、N-乙基哌啶及其类似者。
术语“水合物”是指通过将本文所描述的化合物与水组合而形成的复合物。
术语“溶剂合物”是指一个或多个溶剂分子与本发明化合物的缔合物或复合物。形成溶剂合物的溶剂的例子包括但不限于水、异丙醇、乙醇、甲醇、二甲亚砜、乙酸乙酯、乙酸及乙醇胺。
一些化合物以互变异构体的形式存在。互变异构体彼此处于平衡。举例而言,含酰胺化合物可与亚氨酸互变异构体以平衡形式存在。无论展示何种互变异构体且无论互变异构体之间的平衡性质如何,一般本领域技术人员均将化合物理解为包含酰胺及亚氨酸互变异构体两者。因此,含酰胺化合物应理解为包括其亚氨酸互变异构体。同样,含亚氨酸化合物应理解为包括其酰胺互变异构体。
本发明的化合物或其药学上可接受的盐包括不对称中心,且因此可产生对映异构体、非对映异构体及其他立体异构形式,就绝对立体化学而言,其针对氨基酸可定义为(R)-或(S)-或者(D)-或(L)-。本发明意在包括所有此类可能异构体,以及其外消旋及光学纯形式。具光学活性的(+)及(-)、(R)-及(S)-或(D)-及(L)-异构体可使用手性合成子或手性试剂来制备,或使用常规技术(例如色谱及分步晶体)来解析。用于制备/分离个别对映异构体的常规技术包括自适合光学纯前驱体进行手性合成或使用例如手性高效液相色谱(HPLC)解析外消旋体(或盐或衍生物之外消旋体)。当本文所描述的化合物含有烯为双键或其他几何不对称中心时,且除非另有规定,否则化合物意欲包括E及Z几何异构体。
“立体异构体”是指由通过相同键键合的相同原子构成但具有不可互换的不同三维结构的化合物。本发明涵盖各种立体异构体及其混合物且包括“对映异构体”,对映异构体是指分子互为不可重叠镜像的两种立体异构体。
“非对映异构体”为具有至少两个不对称原子但不互为镜像的立体异构体。
本文所描绘的化合物的相对中心为使用“粗键”样式(粗体或并行线)以图形方式指示,且绝对立体化学为使用楔形键(粗体或并行线)描绘。
“前药”意谓在向哺乳动物受试者施用前药时根据本文所描述的结构而体内释放出活性母体药物的任何化合物。通过修饰本文所描述的化合物中存在的官能基,以此方式使得所述修饰可体内裂解以释放母体化合物来制备本文所描述的化合物之前药。可通过修饰化合物中存在的官能基,以此方式使得所述修饰在常规处理中或在体内裂解得到母体化合物来制备前药。前药包括本文所描述的化合物,其中本文所描述的化合物的羟基、氨基、羧基或硫氢基可结合至可体内裂解从而分别再生游离羟基、氨基或硫氢基的任何基团。前药的例子包括但不限于本文所描述的化合物中的羟基官能基的酯(例如乙酸酯、甲酸酯及苯甲酸酯衍生物)、酰胺、胍、氨基甲酸酯(例如N,N-二甲氨基羰基)及其类似物。前药的制备、选择及使用论述于T.Higuchi及V.Stella,“Pro-drugs as Novel Delivery Systems”,A.C.S.Symposium Series的第14卷;“Design of Prodrugs”,H.Bundgaard编,Elsevier,1985;及Bioreversible Carriers in Drug Design,Edward B.Roche编,AmericanPharmaceutical Association and Pergamon Press,1987中,所述文献中的每一者以全文引用的方式并入本文中。
如本文所用的术语“代谢物”是指当本文所公开的化合物代谢时形成的所得产物。如本文所用,术语“代谢”是指诸如本文所公开的化合物的特定物质被生物体改变的过程(包括但不限于水解反应及由酶催化的反应)的总和。举例而言,醛部分(-C(O)H)可体内还原成-CH2OH部分。
除非另有规定,否则本文使用的字语“抑制剂”或“抑制”适用于式I化合物或药学上可接受的盐对于运铁素的活性。本文中的“抑制”意谓相较于在不存在化合物的情况下的运铁素的活性,使运铁素的活性降低。在一些实施方案中,术语“抑制”意谓运铁素活性降低至少约5%、至少约10%、至少约20%、至少约25%、至少约50%、至少约60%、至少约70%、至少约80%、至少约90%或至少约95%。在其他实施方案中,抑制意谓运铁素活性降低约5%至约25%、约25%至约50%、约50%至约75%或约75%至100%。在一些实施方案中,抑制意谓运铁素活性降低约95%至100%,例如活性降低95%、96%、97%、98%、99%或100%。这些降低可使用本领域技术人员可识别的多种技术量测,包括体外分析。
如本文所用,术语“运铁素抑制剂”及类似者是指例如通过诱导运铁素的内化降低、抑制或以其他方式减弱运铁素的一种或多种生物活性的化合物。活性可降低统计学上显著的量,包括例如运铁素的活性相较于适当对照降低至少约5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、95%或100%。
“治疗”是用于获得有益或所需结果(包括临床结果)的途径。有益或所需临床结果可包括以下中之一或多者:a)抑制疾病或病况(例如,减少由疾病或病况产生的一种或多种症状,和/或减轻疾病或病况的程度);b)减缓或遏制与疾病或病况相关的一种或多种临床症状的发展(例如,稳定疾病或病况、预防或延迟疾病或病况的恶化或进展,和/或预防或延迟疾病或病况的扩散(例如转移));和/或c)减轻疾病,亦即,使临床症状消退(例如,改善疾病状态、提供疾病或病况的部分或完全缓解、增强另一药物的效应、延迟疾病进展、提高生活质量和/或延长存活期)。
“预防”意谓促使疾病或病况的临床症状不发展的对疾病或病况的任何治疗。在一些实施方案中,化合物可向处于该疾病或病况的风险下或具有该疾病或病况的家族史的受试者(包括人类)施用。
“受试者”是指已成为或将成为治疗、观察或实验的对象的动物,诸如哺乳动物(包括人类)。本文所描述的方法可适用于人类治疗和/或兽医学应用。在一些实施方案中,该受试者为哺乳动物。在一个实施方案中,该受试者为人类。
术语本文所描述的化合物或其药学上可接受的盐、互变异构体、立体异构体、立体异构体混合物、前药或氘代类似物的“治疗有效量”或“有效量”意谓当向受试者施用时足以实现治疗以提供治疗益处(诸如改善症状或减缓疾病进展)的量。举例而言,治疗有效量可为足以减少镰状细胞疾病的症状的量。治疗有效量可视待治疗的受试者及疾病或病况、受试者的体重及年龄、该疾病或病况的严重程度及施用方式而变化,其可容易地由本领域普通技术人员判定。
当在任何结构或式中出现一次以上任何变量或取代基时,其在每次出现时的定义独立于其在每一次其他出现时的定义。取代基和/或变量的组合是容许的,只要这些组合产生化学稳定化合物即可。应理解,关于本文所描述的化合物的取代基及取代模式可由一般本领域技术人员选择以提供化学稳定且可易于通过本领域已知的技术以及本文所阐述的那些方法合成的化合物。
下文亦可按需要提供额外定义。
II.化合物
在某些实施方案中,本文所描述的主题针对式I'化合物:
或其药学上可接受的盐;其中
Z为N或CH;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C10烷氧基、羟基-C1-C10烷基、氰基、-NRGRH、卤代-C1-C3烷氧基、-O-(C1-C6烷基)-Rbb、-O-Rbb、-(C1-C6烷基)-NRGIRHI、-S-C1-C3烷基、-S-C1-C3烷基-NRG1RH1、卤代-C1-C3烷基、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
羟基-C1-C10烷氧基或-O-(C1-C6烷基)-Rbb中的该烷基部分任选经氰基、羟基、羟基-C1-C3烷基、卤素或C1-C3烷氧基取代;
Rbb为4元至7元单环或桥联杂环基、C3-C7环烷基、5元或6元单环杂芳基、-SO2-C1-C3烷基、-S-C1-C3烷基、-C(O)NRG1RH1或-NRGRH;
Rcc为C1-C3烷基;且
Rdd为C1-C3烷基或6元杂芳基;
其中R6、Rbb或Rdd的该环烷基、杂环基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:羟基、卤素、卤代-C1-C3烷基、氧代、C1-C3烷氧基及C1-C3烷基;
RG1及RH1各独立地为氢或C1-C3烷基;
且
RG及RH各独立地为氢、-C(O)RGa或任选氘代的C1-C3烷基;其中
RGa为C1-C3烷基或氢;
或
两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元至6元单环杂芳基;其中
与环B稠合的该杂环基、苯基、环烷基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基;
n为0、1、2或3;
Y1、Y2、Y3及Y4各独立地选自由以下组成的组:CH、N、NH、O、S、SH、S-R6、N-R6及C-R6,条件是Y1、Y2、Y3及Y4中的1或2者可为N、N-R6、NH、O、SH或S-R6;
f为0或1;
p为1或2;
Rx在各情况下为卤素、C1-C6烷基、C1-C3烷氧基、羟基、氧代或氰基;
m为0、1或2;
R3选自由以下组成的组:氢、任选氘代的C1-C3烷基、羟基-C1-C3烷基、卤代-C1-C3烷基、环丙基及苯基;
R4选自由以下组成的组:
i.(5元至10元单环或稠合双环杂芳基)-C1-C3烷基或(6元或7元单环杂环基)-C1-C3烷基;其中
该杂芳基或杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C6-C10单环或稠合双环芳基、C3-C7环烷基、5元或6元杂芳基、-(C1-C3烷基)-T及5元至7元单环杂环基;
T选自由以下组成的组:C6-C10单环或稠合双环芳基、C3-C7环烷基、5元或6元杂芳基及5元至7元单环杂环基;且
其中R4的T或该芳基、环烷基、杂芳基或杂环基取代基任选经一个或两个各自个别地选自由C1-C3烷基、卤素及羟基组成的组的取代基取代;且
当p为1时,该(5元至10元单环或稠合双环杂芳基)-C1-C3烷基中的C1-C3烷基为直链的;
且
其中
R4a及R4g各独立地选自由以下组成的组:氢;C1-C10烷基;羟基-C1-C6烷基;卤代-C1-C3烷基;C1-C3烷氧基-C1-C6烷基;-C1-C6烷基-NRJ1RJ2;C3-C7环烷基;4元至10元单环、稠合双环、桥联双环或螺杂环基;C6-C10单环或稠合双环芳基;5元至10元单环或稠合双环杂芳基;(C6-C10单环或稠合双环芳基)-C1-C3烷基;及(5元至10元单环或稠合双环杂芳基)-C1-C3烷基;
RJ1及RJ2独立地为氢或C1-C3烷基;
其中R4a或R4g的该环烷基、杂环基、芳基、杂芳基、芳基-烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素;C1-C6烷基;卤代-C1-C3烷基;羟基;C1-C3烷氧基;卤代-C1-C3烷氧基;氧代;C3-C7环烷基;及5元至10元单环、稠合双环或螺杂环基;
R4b为氢或C1-C6烷基;或
R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基;或
R4b及R4c与其各自所连接的原子一起形成任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代的5元至7元单环杂环基:羟基、卤素及C1-C3烷基;或
R4c及R4d各独立地选自由以下组成的组:氢、C1-C3烷氧基、羟基、C1-C3烷基-硫基-C1-C3烷基、羟基-C1-C6烷基、C1-C6烷氧基-C1-C3烷基、C3-C7环烷基及C1-C3烷基;或
R4c及R4d与其各自所连接的原子一起形成C3-C7环烷基;
或当p为1时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个或两个杂原子的7元稠合双环杂环基、7元桥联双环杂环基或7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷氧基、氧代及-(CH2)sC(=O)NRkRl;其中
s为0、1、2或3;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、羟基、C1-C3烷基、C3-C7环烷基及C6-C10单环或稠合双环芳基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及-NRqRw;其中
Rq为氢或C1-C3烷基;且
Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;
或
iii.8元、9元、10元或11元稠合双环杂环基,或12元双环桥联及稠合杂环基,其中该8元、9元或11元杂环基含有一个杂原子且该10元或12元杂环基含有一个或两个杂原子;且其中该10元、11元或12元杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、C1-C3烷氧基及羟基;
或当p为2时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个杂原子的6元单环杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、羟基-(C1-C6烷基)、羟基、氧代及C1-C3烷氧基;或
ii.含有一个或两个杂原子的4元或7元单环杂环基,或含有一个、两个或三个杂原子的7元、8元、9元、10元或11元桥联双环、稠合双环或螺杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、氧代、氰基、C1-C3烷基、羟基、-NRGRH及-(CH2)sC(=O)NRkRl;
条件是当式(I)结构为
且
其中该式(I)化合物不为:
N-((1,4-二氧杂环己-2-基)甲基)-2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-胺;
4-(哌啶-1-基)-2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉;
4-(氮杂环庚-1-基)-2-(6-丙基吡啶-2-基)-5,6,7,8-四氢喹唑啉;
1-丙基-4-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,4-二氮杂环庚-2-酮;或
2-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,2-氧氮杂环庚烷;或其盐。
在某些实施方案中,本文所描述的主题针对式I'化合物:
或其药学上可接受的盐;其中
Z为N或CH;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C3烷基、氰基、-NRGRH、卤代-C1-C3烷氧基、-O-(CH2)u-Rbb、卤代-C1-C3烷基、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
u为0至6的整数;
Rbb为4元至7元单环杂环基、C3-C7环烷基或-NRGRH;
Rcc及Rdd各独立地为C1-C3烷基;
其中该环烷基、杂环基或杂芳基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代;
且
RG及RH各独立地为氢、-C(O)RGa或C1-C3烷基;其中
RGa为C1-C3烷基或氢;
或
两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元至6元单环杂芳基;其中
与环B稠合的该杂环基、苯基、环烷基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基;
n为0、1、2或3;
Y1、Y2、Y3及Y4各独立地选自由以下组成的组:CH、N、NH、O、S、SH、S-R6、N-R6及C-R6,条件是Y1、Y2、Y3及Y4中的1或2者可为N、N-R6、NH、O、SH或S-R6;
f为0或1;
p为1或2;
Rx在各情况下为卤素、C1-C6烷基、C1-C3烷氧基、羟基或氰基;
m为0、1或2;
R3选自由以下组成的组:氢、C1-C3烷基、羟基-C1-C3烷基、环丙基及苯基;
R4选自由以下组成的组:
i.分支链或直链(5元至10元单环或稠合双环杂芳基)-C1-C3烷基,或分支链或直链(6元或7元单环杂环基)-C1-C3烷基;其中
该杂芳基或杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C6-C10单环或稠合双环芳基、C3-C7环烷基、5元或6元杂芳基及5元至7元单环杂环基,且其中该芳基、环烷基、杂芳基或杂环基任选经一个或两个各自个别地选自由C1-C3烷基、卤素及羟基组成的组的取代基取代;且
当p为1时,该(5元至10元单环或稠合双环杂芳基)-C1-C3烷基中的C1-C3烷基为直链的;
且
其中
R4a及R4g各独立地选自由以下组成的组:氢;C1-C6烷基;羟基-C1-C6烷基;C1-C3烷氧基-C1-C6烷基;C3-C7环烷基;5元至10元单环、稠合双环、桥联双环或螺杂环基;C6-C10单环或稠合双环芳基;5元至10元单环或稠合双环杂芳基;(C6-C10单环或稠合双环芳基)-C1-C3烷基;及(5元至10元单环或稠合双环杂芳基)-C1-C3烷基;
其中R4a或R4g的该环烷基、杂环基、芳基、杂芳基、芳基-烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素;C1-C6烷基;卤代-C1-C3烷基;羟基;C1-C3烷氧基;卤代-C1-C3烷氧基;氧代;C3-C7环烷基;及5元至10元单环、稠合双环或螺杂环基;
R4b为氢或C1-C6烷基;或
R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基;或
R4b及R4c与其各自所连接的原子一起形成任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代的5元至7元单环杂环基:羟基、卤素及C1-C3烷基;或
R4c及R4d各独立地选自由以下组成的组:氢、C1-C3烷氧基、羟基、C1-C3烷基-硫基-C1-C3烷基、羟基-C1-C6烷基、C1-C6烷氧基-C1-C3烷基、C3-C7环烷基及C1-C3烷基;或
R4c及R4d与其各自所连接的原子一起形成C3-C7环烷基;
或当p为1时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个或两个杂原子的7元稠合双环杂环基、7元桥联双环杂环基或7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷氧基、氧代及-(CH2)sC(=O)NRkRl;其中
s为0、1、2或3;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、羟基、C1-C3烷基、C3-C7环烷基及C6-C10单环或稠合双环芳基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及-NRqRw;其中
Rq为氢或C1-C3烷基;且
Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;
或
iii.8元、9元、10元或11元稠合双环杂环基,或12元双环桥联及稠合杂环基,其中该8元、9元或11元杂环基含有一个杂原子且该10元或12元杂环基含有一个或两个杂原子;且其中该10元、11元或12元杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、C1-C3烷氧基及羟基;
或当p为2时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个杂原子的6元单环杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、羟基-(C1-C6烷基)、羟基、氧代及C1-C3烷氧基;或
ii.含有一个或两个杂原子的4元或7元单环杂环基,或含有一个、两个或三个杂原子的7元、8元、9元、10元或11元桥联双环、稠合双环或螺杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、氧代、氰基、C1-C3烷基、羟基、-NRGRH及-(CH2)sC(=O)NRkRl;
条件是当式(I)结构为
且
其中该式(I)化合物不为:
N-((1,4-二氧杂环己-2-基)甲基)-2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-胺;
4-(哌啶-1-基)-2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉;
4-(氮杂环庚-1-基)-2-(6-丙基吡啶-2-基)-5,6,7,8-四氢喹唑啉;
1-丙基-4-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,4-二氮杂环庚-2-酮;或
2-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,2-氧氮杂环庚烷;或其盐。
在某些实施方案中,本文所描述的主题针对式I化合物:
其中
Z为N或CH;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C3烷基、氰基、C3-C7环烷基-C1-C3烷氧基、NRGRH、卤代-C1-C3烷氧基及C3-C6环烷基;
其中RG及RH各独立地为氢或C1-C3烷基;
或其中两个R6基团与其各自所连接的原子一起形成5元或6元杂环基、C3-C7环烷基、C6-C10芳基或5元至10元杂芳基;
n为0、1、2或3;
Y1、Y2、Y3及Y4各独立地选自由以下组成的组:CH、N、NH、O、S、及C(当R6与其连接时),条件是Y1、Y2、Y3及Y4中的1或2者可为N、NH、O或S;
f为0或1;
p为1或2;
Rx在各情况下为卤素、C1-C6烷基、C1-C3烷氧基、羟基或氰基;
m为0、1或2;
R3选自由以下组成的组:氢、C1-C3烷基、羟基-C1-C3烷基、环丙基及苯基;
R4选自由以下组成的组:
i.分支链或直链(5元至10元单环或双环稠合杂芳基)-C1-C3烷基,或分支链或直链(6元或7元单环杂环基)-C1-C3烷基;
其中
当p为1时,(5元至10元单环或双环稠合杂芳基)-C1-C3烷基中的C1-C3烷基为直链的;
且
其中
R4a及R4g各独立地选自由以下组成的组:氢、C1-C6烷基、羟基-C1-C6烷基、C1-C3烷氧基-C1-C6烷基、C3-C7环烷基、5元至10元单环、双环稠合或螺杂环基、C6-C10芳基、5元至10元单环或双环稠合杂芳基、(C6-C10芳基)-C1-C3烷基及(5元至10元单环杂芳基)-C1-C3烷基;
其中R4a或R4g的环烷基、杂环基、芳基、杂芳基、芳基烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤烷基、羟基、C1-C3烷氧基、氧代、C3-C7环烷基及5元至10元单环、双环稠合或螺杂环基;
R4b为氢或C1-C6烷基;
或R4a及R4b与其各自所连接的原子一起形成5元至7元杂环基;
或R4b及R4c与其各自所连接的原子一起形成经一个、两个或三个各独立地选自由以下组成的组的取代基取代的5元至7元杂环基:羟基、卤素及C1-C3烷基;
R4c及R4d各独立地选自由以下组成的组:氢、C1-C3烷氧基、羟基、C1-C3烷基-硫基-C1-C3烷基、羟基-C1-C6烷基、C1-C6烷氧基-C1-C3烷基、C3-C7环烷基及C1-C3烷基;
或R4c及R4d与其各自所连接的原子一起形成C3-C7环烷基;
或当p为1时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个或两个杂原子的7元双环稠合杂环基、7元桥联杂环基或7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤烷基及C6-C10芳基;且其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷氧基、氧代及-(CH2)sC(=O)NRkRl;
其中s为0、1、2或3;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、羟基、C1-C3烷基、C3-C7环烷基及C6-C10芳基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及NRqRw;
其中Rq为氢或C1-C3烷基及Rw为C6-C10芳基或C3-C7环烷基,且其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;
iii.8元、9元、10元或11元双环稠合杂环基,或12元双环桥联稠合杂环基,其中该8元、9元或11元杂环基含有一个杂原子且该10元或12元杂环基含有一个或两个杂原子;且其中该10元、11元或12元杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、C1-C3烷氧基及羟基;
或当p为2时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个杂原子的6元单环杂环基,其任选具有一个或两个各独立地选自由以下组成的组的取代基:卤素、羟基-(C1-C6烷基)、羟基、氧代及C1-C3烷氧基;或
ii.含有一个或两个杂原子的4元或7元单环杂环基,或含有一个、两个或三个杂原子的7元、8元、9元、10元或11元双环桥联、稠合或螺杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、氧代、氰基、C1-C3烷基、羟基、NRGRH及-(CH2)sC(=O)NRkRl;
条件是当式(I)结构为
或其药学上可接受的盐;且
其中该式(I)化合物不为:
N-((1,4-二氧杂环己-2-基)甲基)-2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-胺;
4-(哌啶-1-基)-2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉;
4-(氮杂环庚-1-基)-2-(6-丙基吡啶-2-基)-5,6,7,8-四氢喹唑啉;
1-丙基-4-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,4-二氮杂环庚-2-酮;或
2-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,2-氧氮杂环庚烷;或其盐。
适用的式I'或I化合物包括其中p为1的那些化合物。
适用的式I'或I化合物包括其中Z为N的那些化合物。
每当式I'或I化合物含有变数C-R6、N-R6或S-R6时,整数n将减小一,且n的总数(C-R6、N-R6或S-R6的总数不可超过3)。
适用的式I'或I化合物包括其中Y1、Y2、Y3及Y4各为CH或C-R6的那些化合物。在某些实施方案中,适用的式I'或I化合物包括其中Y1为CH、Y2为C-R6且Y3及Y4各为CH的那些化合物。适用的式I'或I化合物包括其中Y3为N且Y1、Y2及Y4各为CH或C-R6的那些化合物。适用的式I'或I化合物包括其中Y2为N且Y1、Y3、Y4各为CH或C-R6的那些化合物。适用的式I'或I化合物包括其中Y1为N且Y2、Y3及Y4各为CH或C-R6的那些化合物。适用的式I'或I化合物包括其中Y1为CH、Y2为C-R6、Y3为CH且Y4为CH的那些化合物。
适用的式I'或I化合物包括如下的那些化合物,其中R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C3烷基、-O-(CH2)u-Rbb、卤代-C1-C3烷氧基、-O-Rcc-O-Rdd、卤代-C1-C3烷基、羟基-C1-C10烷基、-O-(C1-C6烷基)-Rbb、-O-Rbb、-S-C1-C3烷基、-S-C1-C3烷基-NRG1RH1及-NRGRH;其中羟基-C1-C10烷氧基或-O-(C1-C6烷基)-Rbb中的烷基部分任选经氰基、羟基、羟基-C1-C3烷基、卤素或C1-C3烷氧基取代;Rbb为-NRGRH;u为1至3的整数;RG及RH各独立地为氢或C1-C3烷基;且Rcc及Rdd各独立地为C1-C3烷基烷基。适用的式I'或I化合物包括如下的那些化合物,其中R6在各情况下选自由以下组成的组:甲氧基、乙氧基、甲基、氟、氯、乙基、-N(CH3)2、羟基、-OCH2CH2OH、-CH2OH、-CH2OCH3、-OCH2CH2NH2、-OCH2CH2N(CH3)2、-OCH2C(CH3)2OH、-OCH2CF3、-OCHF2、-OCF3、-OCH2CH2OCH3、-OCH2CH2F、-OC(CH3)2CH2OH、-OCH2CH(CH3)OH、-OCH2CH2NHC(O)CH3、-OC(CH3)2CH2N(CH3)2、-OCH(CH3)CH2OH、-OCH2CH(CH(CH3)2)OH、-OCH2CH(CH2CH3)OH、-OCH2C(CH2CH3)2OH、-OCH2CH2N(CH2CH3)2、-OCH(CH3)CH2N(CH3)2、-OCH2C(O)N(CH3)2、-OCH2C(CH3)2N(CH3)2、-OCH2CH(CH2OH)OH、-OCH2CH2NH(CH3)、-OCH2CH(CF3)OH、-OCH2C(CH3)(CH2CH3)OH、-OCH2CH(CH2OCH3)OH、-OCH2CH(CH2F)OH、-(CH2)3N(CH3)2、-(CH2)3N(CH3)H、-O(CH2)2S(O)2CH3、-O(CH2)2SCH3、-(CH2)2C(CH3)2OH及-CH2CH2OH。此外,适用的式I'或I化合物包括其中R6在各情况下为甲氧基、-OCH2CH2N(CH3)2、-OCH2CH2OH或-OCH2C(CH3)2OH的那些化合物。适用的式I'或I化合物包括如下的那些化合物,其中R6在各情况下选自由-O-(CH2)u-Rbb及C3-C6组成的组;其中u为0至3的整数;Rbb为4元至7元单环杂环基或C3-C7环烷基;且其中该环烷基或杂环基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代。适用的式I'或I化合物包括如下的那些化合物,其中R6在各情况下选自由环丙基及-O-(CH2)u-Rbb组成的组;其中u为0、1或2;且Rbb选自由以下组成的组:环丙基、环丁基、四氢呋喃基、氧杂环丁烷基及吡咯烷基,其各任选经羟基或甲基取代。适用的式I'或I化合物包括其中R6在各情况下选自由以下组成的组的那些化合物:
适用的式I'或I化合物包括如下的那些化合物,其中两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元或6元单环杂芳基,所述基团各任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基。适用的式I'或I化合物包括如下的那些化合物,其中两个R6基团与其各自所连接的原子一起形成与环B稠合的吡唑基、二氧杂环己烷基、吡啶基、嘧啶基、噻唑基、呋喃基、二氧杂环戊烷基或苯基环,其中该环任选经一个选自由以下组成的组的取代基取代:羟基、甲氧基、四氢吡喃基、-CH2OH及甲基。适用的式I'或I化合物包括如下的那些化合物,其中两个邻位R6基团与其各自所连接的原子一起形成与环B稠合的选自由以下组成的组的环:
,其中该对表示该环与环B的连接。适用的式I'或I化合物包括如下的那些化合物,其中两个邻位R6基团与其各自所连接的原子一起形成与环B稠合的选自由以下组成的组的环:适用的式I'或式I化合物包括如下的那些化合物,其中两个邻位R6基团与其各自所连接的原子一起形成与环B稠合的环,其中由环B及两个邻位R6基团形成的双环选自由以下组成的组:
适用的式I'或式I化合物包括其中f为1的那些化合物。适用的式I'或式I化合物包括其中f为0且环B为的那些化合物。适用的式I'或式I化合物包括如下的那些化合物,其中环B为其中n为0或1;且Y2及Y3各独立地选自由以下组成的组:CH、N、NH、NR6、S、O及CR6,条件是Y2及Y3中仅一者可为N、NH、NR6、S或O。适用的式I'或式I化合物包括其中环B选自由以下组成的组的那些化合物:适用的式I'或式I化合物包括其中R6在各情况下选自由C1-C3烷基及羟基-C1-C3烷基组成的组的那些化合物。适用的式I'或式I化合物包括其中R6在各情况下选自由甲基、乙基、正丙基、-CH2CH2OH及-CH2CH2CH2OH组成的组的那些化合物。
适用的式I'或式I化合物包括其中n为1的那些化合物。适用的式I'或式I化合物包括其中n为0的那些化合物。适用的式I'或式I化合物包括如下的那些化合物,其中n为2,其中一个R6选自由甲基及甲氧基组成的组,且另一R6选自由甲基、甲氧基、卤素及-OCH2CH2OH组成的组。
适用的式I'或式I化合物包括其中R3选自由氢、甲基、乙基、苯基及-CH2CH2OH组成的组的那些化合物。适用的式I'或式I化合物包括其中R3选自由氢、甲基、-CD3、乙基、苯基-CH2CF3及-CH2CH2OH组成的组的那些化合物。适用的式I'或式I化合物包括其中R3为甲基的那些化合物。
适用的式I'或式I化合物包括如下的那些化合物,其中R4为(5元至10元单环或稠合双环杂芳基)-甲基,其中该杂芳基任选经一个或两个各独立地选自由苯基、C3-C7环烷基及5元至7元单环杂环基组成的组的取代基取代,且其中该苯基、环烷基或杂环基任选经一个或两个各自个别地选自由C1-C3烷基、卤素及羟基组成的组的取代基取代。适用的式I'或式I化合物包括如下的那些化合物,其中R4为(6元杂芳基)-甲基,其中该6元杂芳基中在连接点的邻位的环原子中的至少一者为氮。适用的式I'或式I化合物包括如下的那些化合物,其中R4选自由以下组成的组:吡啶基-甲基、嘧啶基-甲基、苯并噁唑-甲基、噁唑基-甲基及三唑基-甲基,其各任选经苯基或苯甲基取代,且其中该苯基任选经一个选自由氟、甲基及氯组成的组的取代基取代。适用的式I'或式I化合物包括其中R4选自由以下组成的组的那些化合物:
适用的式I'或式I化合物包括其中R4为的那些化合物。适用的式I'或式I化合物包括如下的那些化合物,其中R4c选自由以下组成的组:氢、甲基、异丙基、-CH2OH、-CH2OC(CH3)3及-CH2CH2SCH3;且R4d选自由氢及甲基组成的组;或R4c及R4d与其各自所连接的原子一起形成环丙基环。适用的式I'或式I化合物包括其中R4c及R4d各为氢的那些化合物。适用的式I'或式I化合物包括其中R4b为氢的那些化合物。适用的式I'或式I化合物包括其中R4a为C1-C6烷基的那些化合物。适用的式I'或式I化合物包括其中R4a为叔丁基或异丙基的那些化合物。适用的式I'或式I化合物包括如下的那些化合物,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的苯基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环或稠合双环杂环基。适用的式I'或式I化合物包括如下的那些化合物,其中R4a为任选经一个选自由氟、氯、甲基及甲氧基组成的组的取代基取代的苯基。适用的式I'或式I化合物包括其中R4a选自由以下组成的组的那些化合物:
适用的式I'或式I化合物包括如下的那些化合物,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环或稠合双环杂芳基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、稠合双环或螺杂环基。适用的式I'或式I化合物包括如下的那些化合物,其中R4a为吡啶基、嘧啶基、吡唑基、异噻唑基、哒嗪基或喹啉基,其任选经一个选自由以下组成的组的取代基取代:氟、氯、甲氧基、氮杂环庚烷基、环丙基、-CF3、-OCF3或甲基。适用的式I'或式I化合物包括其中R4a选自由以下组成的组的那些化合物:
适用的式I'或式I化合物包括如下的那些化合物,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的C3-C7环烷基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环或稠合双环杂环基。适用的式I'或式I化合物包括如下的那些化合物,其中R4a选自由以下组成的组:环丙基、环丁基、环戊基、环己基及双环[1.1.1]戊-1-基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:甲基、-CF3、氟或羟基。适用的式I'或式I化合物包括其中R4a选自由以下组成的组的那些化合物:
适用的式I'或式I化合物包括如下的那些化合物,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的4元至10元单环或稠合双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、氧代、C3-C7环烷基及5元至10元单环或稠合双环杂环基。适用的式I'或式I化合物包括如下的那些化合物,其中R4a选自由以下组成的组:四氢呋喃基、吡咯烷基、苯并[d][1,3]间二氧杂环戊烯基、氧杂环丁烷基及四氢吡喃基,其任选经一个或两个各独立地选自由甲基、甲氧基及氧代组成的组的取代基取代。适用的式I'或式I化合物包括其中R4a选自由以下组成的组的那些化合物:
适用的式I'或式I化合物包括如下的那些化合物,其中R4a为(C6-C10单环或稠合双环芳基)-C1-C3烷基或(5元至10元单环或稠合双环杂芳基)-C1-C3烷基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、稠合双环杂环基。适用的式I'或式I化合物包括其中R4a选自由苯甲基、2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙基及吡啶基-甲基组成的组的那些化合物。适用的式I'或式I化合物包括其中R4a选自由以下组成的组的那些化合物:
适用的式I'或式I化合物包括其中R4a选自由-C(CH3)2CH2OH、-CH2CH2OH及-C(CH3)2CH2OCH3组成的组的那些化合物。适用的式I'或式I化合物包括如下的那些化合物,其中R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基。适用的式I'或式I化合物包括如下的那些化合物,其中R4a及R4b与其各自所连接的原子一起形成哌啶基、吗啉基、吡咯烷基、氮杂环庚烷基、吲哚啉基、氮双环[3.1.1]庚烷基或哌嗪基,所述基团任选经一个或两个各独立地选自由以下组成的组的取代基取代:甲基、氟、羟基及甲氧基。
适用的式I'或式I化合物包括如下的那些化合物,其中R4b及R4c与其各自所连接的原子一起形成任选经一个或两个各独立地选自C1-C3烷基的取代基取代的5元至7元单环杂环基。适用的式I'或式I化合物包括如下的那些化合物,其中R4b及R4c与其各自所连接的原子一起形成任选经甲基取代一次或两次的哌啶-2-酮或吡咯烷-2-酮。
适用的式I'或式I化合物包括如下的那些化合物,其中R4为其中R4g选自由C6-C10单环或稠合双环芳基及C1-C3烷基组成的组。适用的式I'或式I化合物包括其中R4a选自由苯基及甲基组成的组的那些化合物。
适用的式I'或式I化合物包括如下的那些化合物,其中R3及R4与其各自所连接的氮原子一起形成含有一个或两个杂原子的7元单环或桥联双环杂环基;其中当该7元杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且当该7元杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基。适用的式I'或式I化合物包括如下的那些化合物,其中R3及R4与其各自所连接的氮原子一起形成:含有一个杂原子的单环7元杂环基,其中该杂环基任选经甲基或氧代取代一次;或含有两个杂原子的7元单环或桥联双环杂环基,其中所述杂原子为N或O,且该杂环基任选经一个或两个各独立地选自由苯基、甲基及氧代组成的组的取代基取代,且其中该苯基任选经甲氧基取代。适用的式I'或式I化合物包括如下的那些化合物,其中R3及R4与其各自所连接的氮原子一起形成
适用的式I'或式I化合物包括如下的那些化合物,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的10元或11元稠合双环杂环基,或12元双环稠合及桥联杂环基,所述基团各任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、C1-C3烷氧基、羟基及卤素。适用的式I'或式I化合物包括如下的那些化合物,其中R3及R4与其各自所连接的氮原子一起形成
适用的式I'或式I化合物包括如下的那些化合物,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的4元或6元单环杂环基;其中该4元单环杂环基任选经-(CH2)sC(=O)NRkRl取代;其中s为0、1或2;Rk为氢或C1-C3烷基;且Rl选自由以下组成的组:氢、甲基、苯基、环戊基及环己基;且该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及-NRqRw;其中Rq为氢或C1-C3烷基;Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基。适用的式I'或式I化合物包括如下的那些化合物,其中R3及R4与其各自所连接的氮原子一起形成
适用的式I'或式I化合物包括其中Rx在各情况下为甲基的那些化合物。适用的式I'或式I化合物包括其中m为0的那些化合物。适用的式I'或式I化合物包括其中m为2的那些化合物。
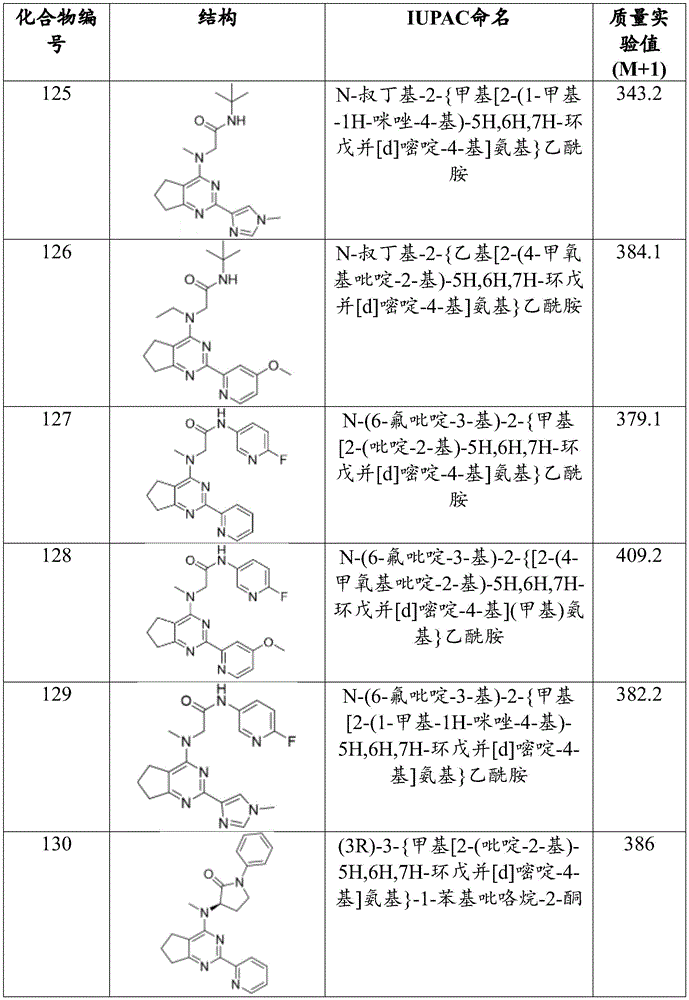
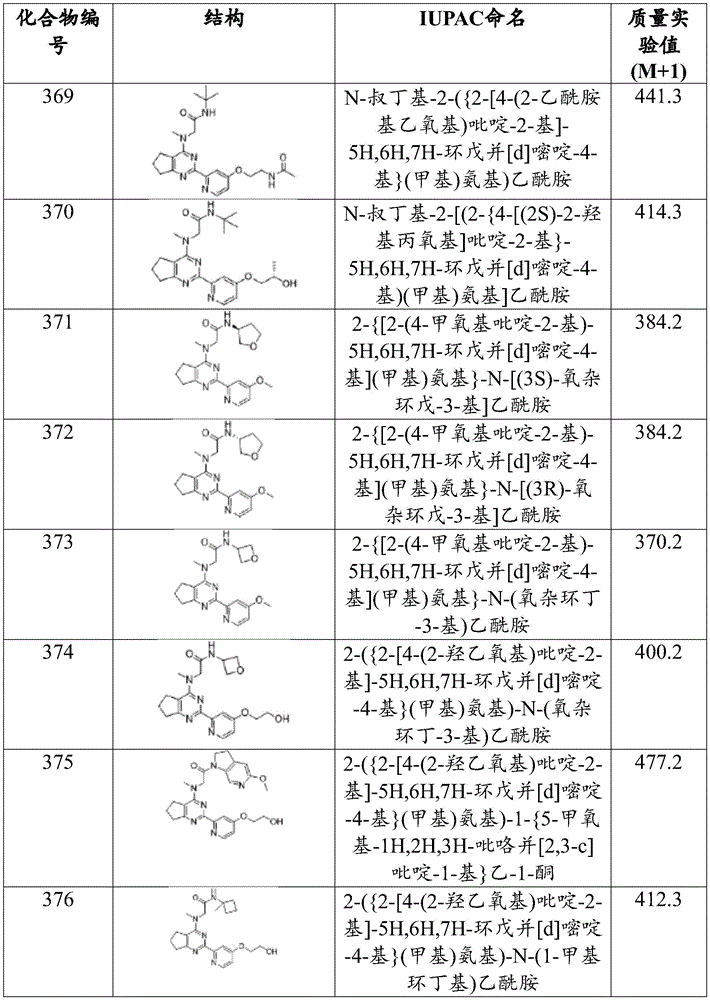
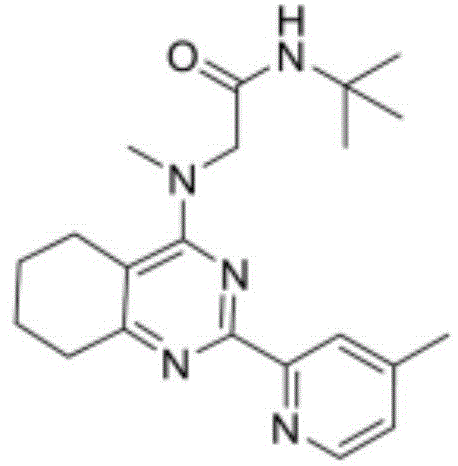
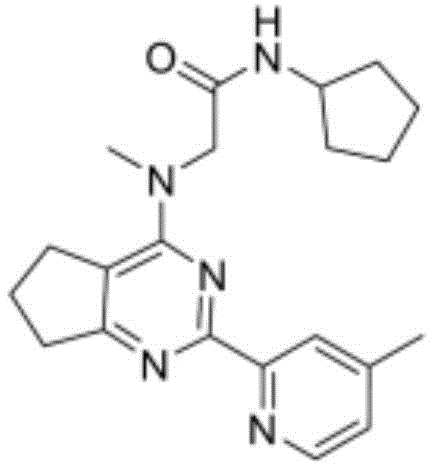
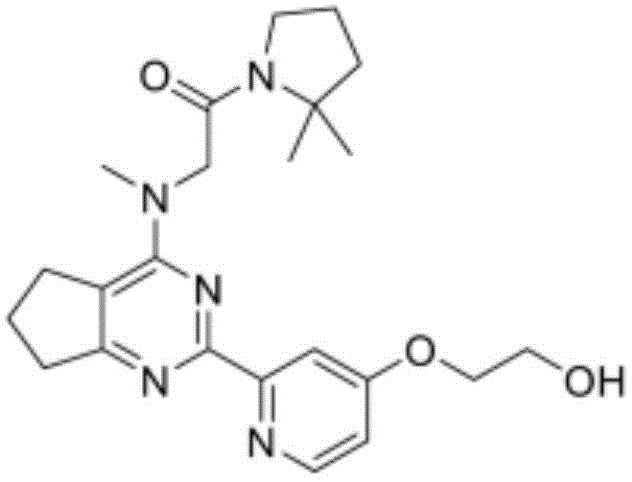
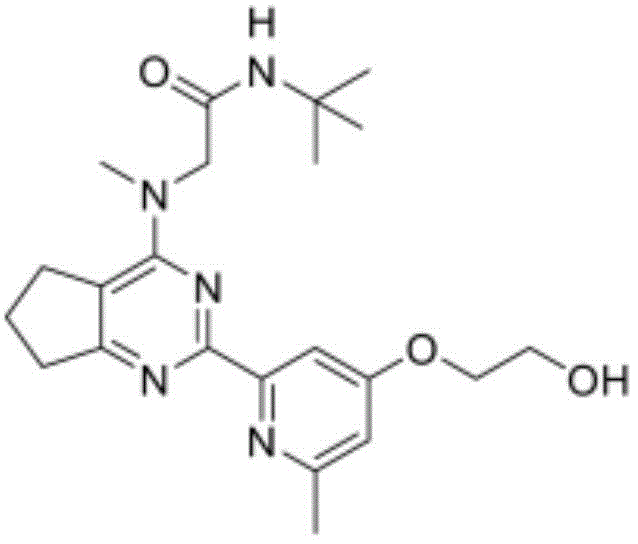
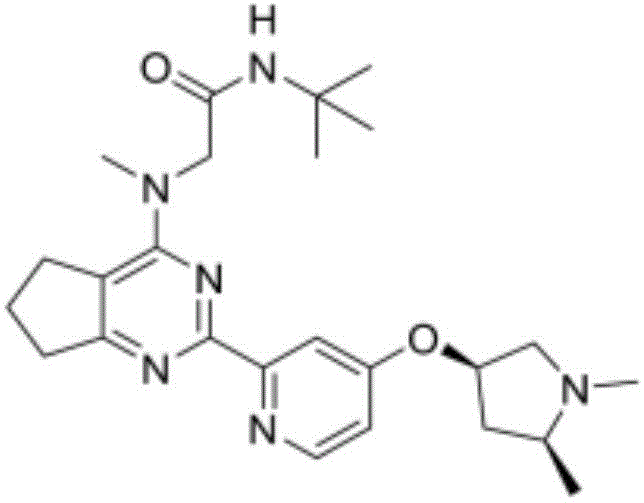
本文所描述的主题包括以下表1中的化合物或其药学上可接受的盐:
表1.在表1中未提供化合物的质量的情况下,化合物的质量可见于合成实施例中。
III.药物组合物及施用模式
本文所提供的化合物通常以药物组合物形式施用。因此,本文亦提供药物组合物,其包含本文所描述的化合物或其药学上可接受的盐、立体异构体或立体异构体混合物中之一或多者及一种或多种药学上可接受的媒剂,所述媒剂选自载剂、佐剂及赋形剂。适合的药学上可接受的媒剂可包括例如惰性固体稀释剂及填充剂、稀释剂(包括无菌水溶液及各种有机溶剂)、渗透增强剂、增溶剂及佐剂。此类组合物以药物技术中熟知的方式制备。参见例如Remington's Pharmaceutical Sciences,Mace Publishing Co.,Philadelphia,Pa.第17版(1985);及Modern Pharmaceutics,Marcel Dekker,Inc.第3版(G.S.Banker及C.T.Rhodes编)。
药物组合物可按单次或多次剂量形式施用。药物组合物可通过各种方法施用,包括例如经直肠、经颊、鼻内及经皮途径。在某些实施方案中,药物组合物可通过动脉内注射、静脉内、腹膜内、非经肠、肌肉内、皮下、经口、局部或以吸入剂形式施用。
一种施用模式为非经肠,例如通过注射。本文所描述的药物组合物可并入以供通过注射施用的形式包括例如水性或油性悬浮液或乳液,含芝麻油、玉米油、棉籽油或花生油以及酏剂、甘露糖醇、右旋糖或无菌水溶液及类似药物媒剂。
经口施用可为用于施用本文所描述的化合物的另一途径。可经由例如胶囊或包覆肠溶包衣片剂施用。在制备包括至少一种本文所描述的化合物或其药学上可接受的盐、立体异构体或立体异构体混合物的药物组合物时,通常通过赋形剂稀释活性成分和/或将活性成分密封于可呈胶囊、药囊、纸张或其他容器的形式的此类载剂内。当赋形剂充当稀释剂时,其可呈固体、半固体或液体材料形式,其充当活性成分的媒剂、载剂或介质。因此,所述组合物可呈以下形式:片剂、丸剂、粉剂、口含片、药囊、扁囊剂、酏剂、悬浮液、乳液、溶液、糖浆、气溶胶(呈固体形式或于液体介质中)、含有例如高达10重量%活性化合物的软膏、软明胶胶囊及硬明胶胶囊、无菌可注射溶液及无菌包装的粉剂。
适合的赋形剂的一些实施例包括乳糖、右旋糖、蔗糖、山梨糖醇、甘露糖醇、淀粉、阿拉伯胶、磷酸钙、海藻酸盐、黄蓍胶、明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、无菌水、糖浆及甲基纤维素。调配物可另外包括:润滑剂,诸如滑石、硬脂酸镁及矿物油;润湿剂;乳化剂及悬浮剂;防腐剂,诸如羟基苯甲酸甲酯及羟基苯甲酸丙酯;甜味剂;及调味剂。
包括至少一种本文所描述的化合物或其药学上可接受的盐、立体异构体或立体异构体混合物的组合物可经调配以便在通过采用本领域已知的程序向受试者施用之后提供活性成分的快速、持续或延迟释放。用于经口施用的控制释放药物递送系统包括含有包覆聚合物包衣的储集囊或药物-聚合物基质调配物的渗透泵系统及溶解系统。控制释放系统的例子在美国专利第3,845,770号、第4,326,525号、第4,902,514号及第5,616,345号中给出。另一种用于本文所公开的方法中的调配物采用经皮递送装置(“贴片”)。此类经皮贴片可用于以受控量提供本文所描述的化合物的连续或不连续输注。用于递送药物剂的经皮贴片的构造及用法为本领域所熟知。参见例如美国专利第5,023,252号、第4,992,445号及第5,001,139号。此类贴片可经构造以连续、脉冲式或按需递送药物剂。
对于制备固体组合物,诸如片剂而言,主要活性成分可与药物赋形剂混合以形成含有本文所描述的化合物或其药学上可接受的盐、立体异构体或立体异构体混合物的均质混合物的固体预调配组合物。当提及这些预调配组合物为均质的时,活性成分可均匀分散在整个组合物中,使得组合物可容易地再分成同等有效的单位剂型,诸如片剂、丸剂及胶囊。
本文所描述的化合物的片剂或丸剂可经包覆包衣或以其他方式混配以提供得到长期作用或免受胃的酸性条件影响的优势的剂型。举例而言,片剂或丸剂可包括内部剂量及外部剂量组分,后者呈前者上的包膜形式。两种组分可由肠溶层隔开,该肠溶层用以防止在胃中崩解且允许内部组分完整进入十二指肠或释放延迟。各种材料可用于此类肠溶层或肠溶衣,此类材料包括多种聚合酸及聚合酸与诸如虫胶、鲸蜡醇及乙酸纤维素的材料的混合物。
用于吸入或吹入的组合物可包括在药学上可接受的水性或有机溶剂或其混合物中的溶液及悬浮液以及粉剂。液体或固体组合物可含有如本文所描述的适合的药学上可接受的赋形剂。在一些实施方案中,通过经口或经鼻呼吸道途径施用组合物以达到局部或全身性作用。在其他实施方案中,含组合物的药学上可接受的溶剂可通过使用惰性气体进行雾化。雾化溶液可直接自雾化装置吸入或雾化装置可连接至面罩或间歇性正压呼吸机。可以适当方式自递送调配物的装置优选地经口或经鼻施用溶液、悬浮液或粉剂组合物。
本申请案的化合物用于任何特定受试者的具体剂量水平将视多种因素而定,包括经受治疗的受试者所采用特定化合物的活性、年龄、体重、总体健康状况、性别、膳食、施用时间、施用途径及排泄速率、药物组合及特定疾病的严重程度。举例而言,剂量可表述为每公斤受试者体重的本文所描述化合物的毫克数(mg/kg)。介于约0.1与150mg/kg之间的剂量可为适当的。在一些实施方案中,约0.1至100mg/kg可为适当的。在其他实施方案中,介于0.5与60mg/kg之间的剂量可为适当的。当在体型广泛不同的受试者之间调整剂量时,诸如当在儿童及成人两者中使用药物时或当将诸如犬的非人类受试者中的有效剂量转换成适合于人类受试者的剂量时所发生,根据受试者的体重标准化尤其适用。视药物动力学及药力学性质(包括特定化合物的吸收、分布、代谢及分泌)而定,剂量可一天一次(QID)、每天两次(BID)或更频繁地施用。此外,毒性因素可影响剂量及施用方案。在经口施用时,丸剂、胶囊或片剂可每天摄取或以较低频率摄取指定时段。方案可重复多个治疗循环。
IV.治疗方法
在某些实施方案中,本文所描述的主题针对一种抑制受试者中由运铁素介导的铁转运的方法,其包含向受试者施用有效量的式I或式I'化合物或其药学上可接受的盐。
在某些实施方案中,本文所描述的主题针对一种治疗罹患与以下有关或由以下引起的疾病的受试者的方法:铁调素含量降低、运铁素含量增加、运铁素对铁调素的敏感性降低、铁含量增加、铁吸收增加、铁超负荷、红血球生成增加、应激性红血球生成或无效红血球生成,该方法包含向受试者施用有效量的式I或式I'化合物。
在某些实施方案中,疾病与铁调素含量降低、运铁素对铁调素的敏感性降低、血红素异常或铁超负荷有关或由所述因素引起。
在某些实施方案中,疾病与铁调素含量降低或运铁素对铁调素的敏感性降低有关或由所述因素引起。
在某些实施方案中,疾病为血红素沉着症。
在某些实施方案中,疾病与血红素异常有关或由其引起。
在某些实施方案中,疾病为地中海贫血、血红素E型疾病、血红素H型疾病或镰状细胞疾病。
在某些实施方案中,疾病为镰状细胞疾病。
在某些实施方案中,镰状细胞疾病为镰状细胞贫血。
本文所描述的方法可应用于体内或离体细胞群体。“体内”意谓在活的个体内,如在动物或人类内。在此上下文中,可在个体中在治疗学上使用本文所描述的方法。“离体”意谓在活的个体外部。离体细胞群体的例子包括体外细胞培养物及生物样本,包括自个体获得的体液或组织样本。这些样本可通过本领域熟知的方法获得。例示性生物体液样本包括血液、脑脊髓液、尿液及唾液。在此上下文中,本文所描述的化合物及组合物可用于各种目的,包括治疗性及实验性目的。举例而言,可离体使用本文所描述的化合物及组合物以测定就给定适应症、细胞类型、个体及其他参数而言本发明化合物的最佳施用时程和/或剂量。自此类使用搜集的信息可用于实验性目的或临床中以设定体内治疗方案。本文所描述的化合物及组合物可能适合的其他离体使用描述于下文中或对本领域技术人员将变得显而易见。所选化合物可进一步经表征以检验在人类或非人类受试者中的安全性或耐受剂量。这些特性可使用本领域技术人员通常已知的方法检验。
式I或式I'化合物及其药学上可接受的盐的运铁素抑制活性提供尤其适合于用于抑制由运铁素介导的铁转运的方法。因而,式I或式I'化合物及其药学上可接受的盐适用于预防和/或治疗与以下有关或由以下引起的疾病:铁调素含量降低、运铁素含量增加、运铁素对铁调素的敏感性降低、铁含量增加、铁吸收增加、铁超负荷、红血球生成增加、应激性红血球生成或无效红血球生成。
此外,式I或式I'化合物适合于通过限制可用于病原微生物(例如嗜铁菌创伤弧菌(Vibrio vulnificus)及小肠大肠炎耶氏杆菌(Yersinia enterocolitica))及常见病原体(例如大肠杆菌(Escherichia coli))的铁量,从而预防或治疗由该病原微生物引起的感染、发炎、败血症及败血性休克而用于辅助疗法中。
在某些实施方案中,本文所描述的主题针对一种抑制受试者中由运铁素介导的铁转运的方法,其包含向受试者施用有效量的式I或式I'化合物或其药学上可接受的盐。
在某些实施方案中,本文所描述的主题针对一种治疗罹患与以下有关或由以下引起的疾病的受试者的方法:铁调素含量降低、运铁素含量增加、运铁素对铁调素的敏感性降低、血红素异常、铁含量增加、铁吸收增加、铁超负荷(例如归因于输血)、红血球生成增加、应激性红血球生成或无效红血球生成,该方法包含向受试者施用有效量的式I或式I'化合物或其药学上可接受的盐。在这些实施方案的方面中,治疗包含抑制受试者中由运铁素介导的铁转运。
在某些实施方案中,本文所描述的主题针对一种治疗罹患与以下有关或由以下引起的疾病的受试者的方法:铁调素含量降低、运铁素对铁调素的敏感性降低、血红素异常或铁超负荷。
在某些实施方案中,本文所描述的主题针对一种治疗罹患与铁调素含量降低或运铁素对铁调素的敏感性降低有关或由其引起的疾病的受试者的方法。在此实施方案的某些方面中,疾病为血红素沉着症。
在某些实施方案中,本文所描述的主题针对一种治疗罹患与血红素异常有关或由其引起的疾病的受试者的方法。在此实施方案的某些方面中,疾病为地中海贫血、血红素E型疾病、血红素H型疾病或镰状细胞疾病。在此实施方案的某些方面中,疾病为镰状细胞疾病。在此实施方案的某些方面中,疾病为镰状细胞贫血。
在某些实施方案中,与铁含量增加、铁吸收增加、铁超负荷(例如组织铁超负荷)或无效红血球生成相关、有关、由其引起或导致的疾病包含地中海贫血、血红素异常(诸如血红素E型疾病(HbE)、血红素H型疾病(HbH))、血红素沉着症、溶血性贫血(诸如镰状细胞贫血)及先天性红血球生成障碍性贫血。与铁含量增加、铁吸收增加、铁超负荷(例如组织铁超负荷)相关、有关、由其引起或导致的额外疾病包括神经退化性疾病,诸如阿尔茨海默氏症(Alzheimer's disease)、帕金森氏病(Parkinson's disease)、亨廷顿氏病(Huntington'sdisease)、多发性硬化症、威尔森氏症(Wilson's disease)、肌肉萎缩性侧索硬化(ALS)及弗里德希氏共济失调(Friedreich's Ataxia),其中认为化合物及方法有效限制组织或细胞中的铁沉积或增加;与由过量铁或铁超负荷引起的自由基、活性氧类(ROS)及氧化应激的形成相关的病况;由过量铁或铁超负荷引起的心脏、肝脏及内分泌损伤;由过量铁或铁超负荷触发的发炎;与无效红血球生成相关的疾病,诸如骨髓发育不良综合征(MDS,骨髓发育不良)、真性红血球增多症及先天性红血球生成障碍性贫血;包含由参与系统铁储存感测的基因(诸如铁调素/铁调素抗微生物肽(HAMP)、血红素沉着症蛋白(HFE)、铁调素调节蛋白(hemojuvelin;HJV)及运铁蛋白受体2(TFR2))的突变引起的铁超负荷的疾病、病症和/或疾病状况,诸如尤其与HFE及HJV基因突变有关的疾病;与运铁素突变有关的疾病;慢性溶血相关疾病;镰状细胞疾病(包括镰状细胞贫血(HbSS)以及血红素SC型疾病(HbSC)、血红素Sβ+地中海贫血(HbS/β+)及血红素Sβ0地中海贫血(HbS/β0));红血球细胞膜病症;葡萄糖-6-磷酸脱氢酶缺乏症(G6PD缺乏症);红血球生成性紫质症;弗里德希氏共济失调;以及铁超负荷的子群,诸如输注性铁超负荷、铁中毒、肺含铁血黄素沉积症、骨量减少、胰岛素抗性、非洲铁超负荷(African iron overload)、Hallervorden-Spatz二氏病、高铁蛋白血症(hyperferritinemia)、血浆铜蓝蛋白缺乏症、新生儿血红素沉着症及红血球异常,包含地中海贫血,包括α地中海贫血、β地中海贫血及δ地中海贫血、中间型地中海贫血、镰状细胞疾病及脊髓发育不良综合征;肝病(例如B型肝炎病毒感染、C型肝炎病毒感染、酒精性肝病、自体免疫性肝炎);其他病况,包括共济失调、弗里德希氏共济失调、老年性黄斑部病变、老年性白内障、老年性视网膜疾病及神经退化性疾病,诸如泛酸盐激酶相关的神经退化、不宁腿综合征及亨廷顿氏病。在某些实施方案中,疾病为镰状细胞贫血。式I化合物及其药学上可接受的盐例如通过诱导运铁素内化实现的运铁素抑制活性可通过本文中描述的分析以及以全文引用的方式并入本文中的WO2018/192973中所描述的那些分析测定。
式I或式I'化合物在治疗镰状细胞贫血(镰状细胞疾病)中的活性可通过使用小鼠模型测定,诸如由Yulin Zhao等人在“MEK1/2inhibitors reverse acute vascularocclusion in mouse models of sickle cell disease”;The FASEB杂志第30卷,第3期,第1171-1186页,2016描述的小鼠模型。该小鼠模型可适用于测定式I或式I'化合物在治疗镰状细胞贫血中的活性。在某些实施方案中,疾病由铁调素缺乏或铁代谢障碍、尤其铁超负荷状态引起,诸如地中海贫血、镰状细胞疾病及血红素沉着症。在某些实施方案中,疾病与铁调素含量降低、铁含量增加、铁吸收增加、铁超负荷、红血球生成增加、应激性红血球生成或无效红血球生成有关或由其引起。在某些实施方案中,疾病选自由以下组成的组:地中海贫血、血红素异常、血红素E型疾病、血红素H型疾病、血红素沉着症及溶血性贫血。
在某些实施方案中,本文所描述的施用及治疗方法进一步包含共同施用或与输血组合施用一种或多种额外药学活性化合物。
在组合疗法中,药学活性化合物可在同一调配物中同时施用或在不同时间施用。这些组合疗法包含共同施用式I或式I'化合物或其药学上可接受的盐与至少一种额外药物活性化合物。固定剂量组合疗法中的组合疗法包含在固定剂量调配物中共同施用式I或式I'化合物或其药学上可接受的盐与至少一种额外药物活性化合物。自由剂量组合疗法中的组合疗法包含通过同时施用个别化合物或通过在一段时间内依序使用个别化合物而以各别化合物的自由剂量共同施用式I或式I'化合物或其药学上可接受的盐与至少一种额外药物活性化合物。
详言之,额外药物活性化合物包括用于减少铁超负荷的药物(例如Tmprss6-ASO或siRNA)或铁螯合剂,详言之姜黄素、SSP-004184、去铁蛋白(Deferitrin)、地拉罗司(deferasirox)去铁胺(deferoxamine)和/或去铁酮(deferiprone);或抗氧化剂,诸如N-乙酰半胱氨酸;抗糖尿病剂,诸如GLP-1受体激动剂;抗生素,诸如青霉素、万古霉素(Van)或托普霉素;抗真菌药物;抗病毒药,诸如干扰素-a或利巴韦林(ribavirin);用于治疗疟疾的药物;抗癌剂;用于治疗神经退化性疾病(诸如阿尔茨海默氏症及帕金森氏病)的药物(例如多巴胺激动剂,诸如左旋多巴(Levodopa));或免疫抑制剂(环孢素A或环孢素A衍生物);铁补充剂;维生素补充剂;红血球产生刺激剂(例如红血球生成素,Epo);抗炎剂;抗溶血栓剂;斯他汀类;血管加压剂;及心肌收缩化合物。本发明的另一目标涉及以上组合用于预防和/或治疗由铁调素缺乏或铁代谢障碍(尤其诸如铁超负荷状态)引起的疾病(详言之,诸如地中海贫血、镰状细胞疾病及血红素沉着症)及本申请案中所描述的其他病症的用途。
在某些实施方案中,本文所描述的主题针对一种治疗受试者的β地中海贫血(beta-thalassemia/β-thalassemia)的方法,其包含向受试者施用有效量的式I化合物或其药学上可接受的盐。如本文所定义的式I化合物充当运铁素抑制剂且可用于治疗重型β地中海贫血,诸如输血依赖性β地中海贫血,详言之,包括重度β地中海贫血及血红素Eβ地中海贫血及与其相关的症状病理病况,详言之,诸如缺陷性骨髓红血球产生、无效红血球生成、低血红素含量/贫血、多器官功能障碍、铁超负荷、肝脏铁负荷及心脏铁超负荷、苍白、疲乏、黄疸及脾肿大。
详言之,重型β地中海贫血为输血依赖性β地中海贫血(TDT),详言之,包括重度β地中海贫血及重型血红素Eβ地中海贫血。重型β-地中海贫血及血红素Eβ地中海贫血需要罹患所述疾病的患者进行定期输血/红血球输注(RBC输注)。因此,这些重型β地中海贫血亦被归纳为输血依赖性β地中海贫血(TDT)。因此,治疗重型β地中海贫血(详言之,诸如输血依赖性β地中海贫血(TDT))的方法尤其包括通过向有需要的受试者施用如本文所描述的式I化合物中之一或多者治疗重度β地中海贫血及重症血红素Eβ地中海贫血。
受试者可:患有β地中海贫血或血红素Eβ地中海贫血且需要定期输血;患有重度β地中海贫血和/或重型血红素Eβ地中海贫血,更特别是患者患有重度β地中海贫血。
治疗β地中海贫血的方法会使得:受试者的NTBI含量降低;受试者的LPI含量降低、受试者的α血球蛋白聚集体含量降低;受试者的RBC中的ROS含量降低;受试者的肝脏铁浓度降低;受试者的心肌铁浓度降低;受试者的参数Hct、MCV、MCH、ROW及网状红血球数目中的至少一者提高;包含受试者的输注负荷降低的红血球为反应;受试者的输注负荷相较于使用方法治疗之前的输注负荷的降低;实现输血依赖性β地中海贫血受试者不再需要输注;受试者的血清铁蛋白含量降低;与一种或多种输血依赖性β地中海贫血临床并发症相关的症状的减少。输血依赖性β地中海贫血症状的非限制性实例包括生长迟滞、脸色苍白、黄疸、肌肉组织不良、膝外翻、肝脾肿大、小腿溃疡、骨髓外造血肿块形成、骨髓扩增导致的骨骼变化及长期红血球输注的临床并发症(诸如B型肝炎病毒感染、C型肝炎病毒感染及人类免疫缺陷病毒感染)、同种异体免疫以及归因于铁超负荷的器官损伤,诸如肝损伤、心脏损伤及内分泌腺损伤。尽管预期式(I)化合物不会直接影响生长分化因子11(GDF11),但髓外红血球生成减少亦可使得骨骼畸形减少。
可测定以下参数以评估本发明的化合物在新医疗用途中的功效:血清铁、NTBI含量、LPI(不稳定血浆铁)含量、红血球生成素、TSAT(运铁蛋白饱和)、Hb(血红素)、Hct(血细胞比容)、MCV(平均红细胞体积)、MCH(平均细胞血红素)、RDW(红血球分布宽度)及网状红血球数目、全血细胞计数、脾脏及肝脏重量、脾脏及骨髓的红血球生成、脾脏及肝脏铁含量以及RBC膜中的α血球蛋白聚集体。可使用此项技术的常规方法,详言之通过下文更详细描述的那些方法进行判定。本发明的化合物(I)适合于改良这些参数中的至少一者。
方法可在输血之前或伴随输血进行,以预防或至少减缓输注引起的病理病况的发生。
在某些实施方案中,本文所描述的主题针对一种预防及治疗受试者的肾损伤的方法,其包含向受试者施用有效量的式I化合物或其药学上可接受的盐。在这些实施方案的某些方面中,式I化合物可与另一药物活性化合物一起共同施用。在这些实施方案的某些方面中,肾损伤为由催化性游离铁诱发的那些损伤。在这些实施方案的某些方面中,肾损伤选自肾缺血再灌注损伤(IRI)、缺血性损伤及急性肾损伤。在另一方面中,肾损伤选自急性肾损伤(AKI)、肾缺血再灌注损伤(IRI)、缺血性损伤及由缺血性损伤引起的AKI、手术或手术干预后(详言之,诸如在最常使用涉及心肺绕通的程序的心脏手术、其他大型胸部或腹部手术之后)的AKI以及与RBC输注相关的肾损伤。
术语“预防”及类似者包括例如通过在缺血事件、RBC输注或手术干预之前或同时或之后不久施用化合物来防止缺血性肾损伤、避免发生AKI或至少减轻缺血性损伤、RBC输注或手术干预后AKI的严重程度,以预防或至少减缓由催化性游离铁诱发的肾损伤的发生。
游离催化性铁或不稳定铁或NTBI被认为是肾损伤的主要诱因,诸如尤其由局部缺血触发的AKI。施用如本文所描述的式(I)的运铁素抑制剂化合物可防止催化性游离铁的损害作用。在不受理论束缚的情况下,本文所描述的运铁素抑制剂可通过肝脏及脾脏的巨噬细胞中的螯合铁减少或预防催化性游离铁或NTBI的形成,由此降低其在血浆中的含量且降低ROS形成的风险。本文所描述的式I化合物充当运铁素抑制剂,且具有螯合巨噬细胞中的铁的潜能,由此中断催化性游离铁的自持释放循环。式I化合物适合于通过限制活性氧类(ROS)以避免肾组织损伤来预防及治疗本文所描述的肾损伤。除催化性游离铁以外,NTBI及LPI(不稳定血浆铁)可导致肾损伤。NTBI涵盖不与运铁蛋白紧密相关且在化学及功能上异质的所有形式的血清铁。LPI表示能够渗透至器官中并诱发组织铁超负荷的氧还活性及可螯合NTBI组分。
可测定以下参数以评估化合物治疗肾损伤的功效:血浆肌酐、肾小球滤过率(包括估算肾小球滤过率eGFR)、尿白蛋白排泄率、尿嗜中性球明胶酶相关的脂质运载蛋白(NGAL)、NTBI、LPI、RBC溶血、血尿素氮(BUN)、血浆血红素(Hb)、总血浆铁、血浆铁调素、肾嗜中性球浸润、血清IL-6、脾脏、肾脏和/或肝脏铁含量、肾运铁素、作为血液及尿液中肾损伤的急性标记的KIM-1(肾损伤分子-1)以及H铁蛋白。另外或替代地,可经由肾小管损伤评分测定本发明的化合物的功效,诸如如下文更详细描述的用于检测急性小管损伤的CSA-NGAL评分(心脏手术相关NGAL评分)、下文更详细地描述的KDIGO评分或包含内皮细胞、肾小球、小管及间质(EGTI)组分的用以评估组织学的EGTI评分(例如由Khalid等人『Kidneyischaemia reperfusion injury in the rat the EGTI scoring system as a validand reliable tool for histological assessment』Journal of Histology&Histopatholoy,第3卷,2016描述)。
治疗或预防肾损伤的方法可使得受试者的血清肌酐(sCr)减少。治疗或预防肾损伤的方法可校正(降低)受试者的尿白蛋白排泄率。治疗或预防肾损伤的方法可使得受试者的血尿素氮(BUN)减少。治疗或预防肾损伤的方法可使得受试者的总血浆铁减少。治疗或预防肾损伤的方法可使得受试者的介白素-6(IL-6)含量降低。治疗或预防肾损伤的方法可使得受试者的KIM-1含量降低。治疗或预防肾损伤的方法可使得受试者的脾脏和/或肝脏铁浓度提高。治疗或预防肾损伤的方法可使得受试者的肾脏铁浓度降低。治疗或预防肾损伤的方法可使得NTBI含量降低。治疗或预防肾损伤的方法可使得受试者的LPI含量降低。治疗或预防肾损伤的方法可抑制小管损伤,诸如小管坏死。治疗或预防肾损伤的方法可抑制细胞凋亡。治疗或预防肾损伤的方法可使得IRI诱导的肾嗜中性球浸润减少。治疗或预防肾损伤的方法可使得受试者的肾组织中的ROS含量降低。治疗或预防肾损伤的方法可校正(提高)受试者的肾脏H铁蛋白含量。详言之,治疗或预防肾损伤的方法可减少AKI、肾缺血再灌注损伤及由缺血性损伤引起的AKI、手术或手术干预后(详言之,诸如在最常使用涉及心肺绕通的程序的心脏手术、其他大型胸部或腹部手术之后)的AKI以及与RBC输注相关的肾损伤的发生。治疗或预防肾损伤的方法可包含a)减少血清肌酐、加速血清肌酐的减少或预防血清肌酐的增加;和/或b)提高估算肾小球滤过率(eGFR)或预防其降低;和/或c)减少肾运铁素或预防其增加;和/或d)提高H铁蛋白含量或预防其降低;和/或e)减少肾嗜中性球浸润或预防其增加;和/或f)降低血清IL-6含量或预防其提高。
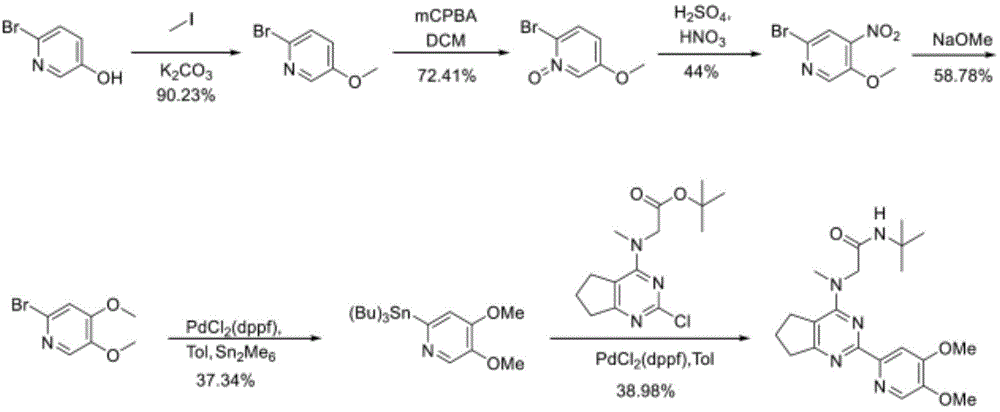
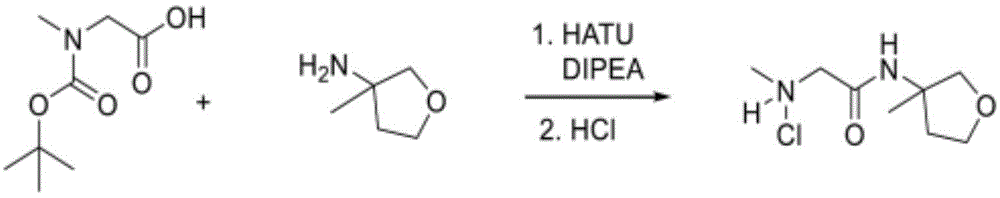
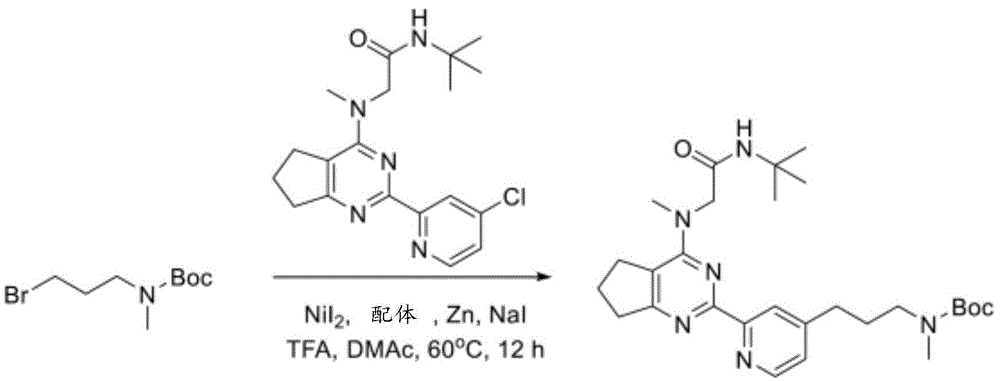
V.制备式I化合物及其药学上可接受的盐的方法
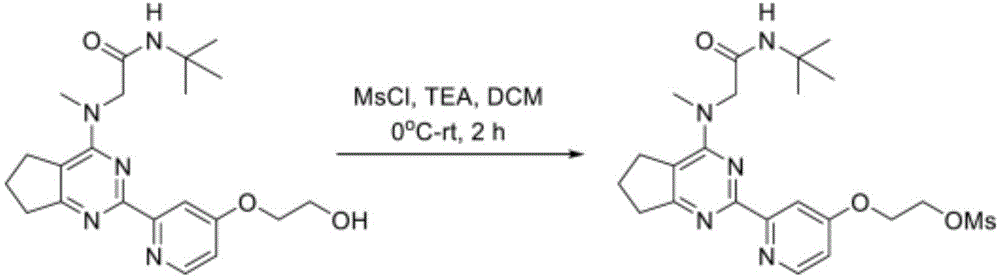
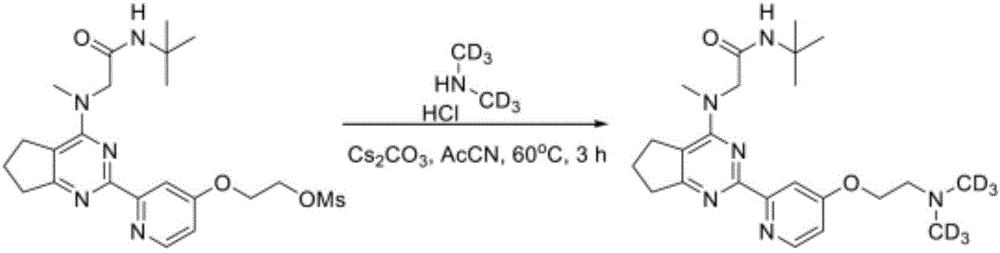
化合物可通过如下合成途径合成,所述合成途径包括类似于化学技术中熟知、尤其根据本文所含有的描述的方法及以下文献中所描述的用于其他杂环的方法:Comprehensive Heterocyclic Chemistry II,编辑Katritzky及Rees,Elsevier,1997,例如第3卷;Liebigs Annalen der Chemie,(9):1910-16,(1985);Helvetica Chimica Acta,41:1052-60,(1958);Arzneimittel-Forschung,40(12):1328-31,(1990),其中的每一者以引用的方式明确并入。起始物质一般购自诸如Aldrich Chemicals(Milwaukee,WI)的商业来源,或易于使用本领域技术人员熟知的方法制备(例如,通过以下文献中大体描述的方法制备:Louis F.Fieser及Mary Fieser Reagents for Organic Synthesis,第1-23卷,Wiley,N.Y.(1967-2006版),或Beilsteins Handbuch der organischen Chemie,4,Aufl.编,Springer-Verlag,Berlin,包括增刊(亦可经由Beilstein在线数据库获得))。DTT是指二硫苏糖醇。DHAA是指脱氢抗坏血酸。
适用于合成化合物及所需试剂以及中间体的合成化学转化及保护基法(添加保护基及去除保护基)为本领域已知,且包括例如以下文献中所描述的方法:R.Larock,Comprehensive Organic Transformations,VCH Publishers(1989);T.W.Greene及P.G.M.Wuts,Protective Groups in Organic Synthesis,第3版,John Wiley and Sons(1999);及L.Paquette编,Encyclopedia of Reagents for Organic Synthesis,JohnWiley and Sons(1995)及其后续版本。
化合物可单独制备或以包含至少2种,例如5至1,000种化合物或10至100种化合物的化合物库形式制备。式I化合物的库可通过组合的‘分离及混合’方法或通过多个平行合成使用溶液相或固相化学法,通过本领域技术人员已知的程序来制备。因此,根据另一方面,提供一种化合物库,其包含至少2种化合物或其药学上可接受的盐。
本文所描述的主题针对以下实施方案。
1A.一种式(I)化合物:
或其药学上可接受的盐;其中
Z为N或CH;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C3烷基、氰基、C3-C7环烷基-C1-C3烷氧基、NRGRH、卤代-C1-C3烷氧基及C3-C6环烷基;
其中RG及RH各独立地为氢或C1-C3烷基;或
两个R6基团与其各自所连接的原子一起形成5元或6元杂环基、C3-C7环烷基、C6-C10芳基或5元至10元杂芳基;
n为0、1、2或3;
Y1、Y2、Y3及Y4各独立地选自由以下组成的组:CH、N、NH、O、S、及C(当R6与其连接时),条件是Y1、Y2、Y3及Y4中的1或2者可为N、NH、O或S;
f为0或1;
p为1或2;
Rx在各情况下为卤素、C1-C6烷基、C1-C3烷氧基、羟基或氰基;
m为0、1或2;
R3选自由以下组成的组:氢、C1-C3烷基、羟基-C1-C3烷基、环丙基及苯基;
R4选自由以下组成的组:
i.分支链或直链(5元至10元单环或双环稠合杂芳基)-C1-C3烷基,或分支链或直链(6元或7元单环杂环基)-C1-C3烷基;
其中
当p为1时,该(5元至10元单环或双环稠合杂芳基)-C1-C3烷基中的C1-C3烷基为直链的;
且
其中
R4a及R4g各独立地选自由以下组成的组:氢、C1-C6烷基、羟基-C1-C6烷基、C1-C3烷氧基-C1-C6烷基、C3-C7环烷基、5元至10元单环、双环稠合或螺杂环基、C6-C10芳基、5元至10元单环或双环稠合杂芳基、(C6-C10芳基)-C1-C3烷基及(5元至10元单环杂芳基)-C1-C3烷基;
其中R4a或R4g的环烷基、杂环基、芳基、杂芳基、芳基烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤烷基、羟基、C1-C3烷氧基、氧代、C3-C7环烷基及5元至10元单环、双环稠合或螺杂环基;
R4b为氢或C1-C6烷基;或
R4a及R4b与其各自所连接的原子一起形成5元至7元杂环基;或
R4b及R4c与其各自所连接的原子一起形成经一个、两个或三个各独立地选自由以下组成的组的取代基取代的5元至7元杂环基:羟基、卤素及C1-C3烷基;或
R4c及R4d各独立地选自由以下组成的组:氢、C1-C3烷氧基、羟基、C1-C3烷基-硫基-C1-C3烷基、羟基-C1-C6烷基、C1-C6烷氧基-C1-C3烷基、C3-C7环烷基及C1-C3烷基;或
R4c及R4d与其各自所连接的原子一起形成C3-C7环烷基;
或当p为1时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个或两个杂原子的7元双环稠合杂环基、7元桥联杂环基或7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤烷基及C6-C10芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷氧基、氧代及-(CH2)sC(=O)NRkRl;
其中s为0、1、2或3;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、羟基、C1-C3烷基、C3-C7环烷基及C6-C10芳基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及NRqRw;
其中Rq为氢或C1-C3烷基及Rw为C6-C10芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;
或
iii.8元、9元、10元或11元双环稠合杂环基,或12元双环桥联稠合杂环基,其中该8元、9元或11元杂环基含有一个杂原子且该10元或12元杂环基含有一个或两个杂原子;且其中该10元、11元或12元杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、C1-C3烷氧基及羟基;
或当p为2时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个杂原子的6元单环杂环基,其任选具有一个或两个各独立地选自由以下组成的组的取代基:卤素、羟基-(C1-C6烷基)、羟基、氧代及C1-C3烷氧基;或
ii.含有一个或两个杂原子的4元或7元单环杂环基,或含有一个、两个或三个杂原子的7元、8元、9元、10元或11元双环桥联、稠合或螺杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、氧代、氰基、C1-C3烷基、羟基、NRGRH及-(CH2)sC(=O)NRkRl;
条件是当式(I)结构为
且
其中该式(I)化合物不为:
N-((1,4-二氧杂环己-2-基)甲基)-2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-胺;
4-(哌啶-1-基)-2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉;
4-(氮杂环庚-1-基)-2-(6-丙基吡啶-2-基)-5,6,7,8-四氢喹唑啉;
1-丙基-4-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,4-二氮杂环庚-2-酮;或
2-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,2-氧氮杂环庚烷;或其盐。
2A.如实施方案1A的化合物,
其中
Z为N;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C3烷基及NRGRH;
其中RG及RH各独立地为氢或C1-C3烷基;或
其中两个R6基团与其各自所连接的原子一起形成5元或6元杂环基、C6-C10芳基或5元至10元杂芳基;
n为0、1或2;
Y1、Y2、Y3及Y4各独立地选自由以下组成的组:CH、N、NH及C(当R6与其连接时),条件是Y1、Y2、Y3及Y4中的1或2者可为N或NH;
f为0或1;
p为1或2;
m为0;
R3选自由以下组成的组:氢、C1-C3烷基及羟基-C1-C3烷基;
R4选自由以下组成的组:
i.分支链或直链(5元至10元单环或双环稠合杂芳基)-C1-C3烷基;
其中
当p为1时,该(5元至10元单环或双环稠合杂芳基)-C1-C3烷基中的C1-C3烷基为直链的;
且
其中
R4a选自由以下组成的组:C1-C6烷基、羟基-C1-C6烷基、C1-C3烷氧基-C1-C6烷基、C3-C7环烷基、5元至10元单环杂环基、C6-C10芳基、5元至10元单环或双环稠合杂芳基、(C6-C10芳基)-C1-C3烷基及(5元至10元单环杂芳基)-C1-C3烷基;
其中R4a的环烷基、杂环基、芳基、杂芳基、芳基烷基或杂芳基-烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤烷基、羟基、C1-C3烷氧基、氧代、C3-C7环烷基及5元至10元单环、双环稠合或螺杂环基;
R4g选自由以下组成的组:C6-C10芳基及C1-C3烷基;
R4b为氢或C1-C6烷基;
或R4a及R4b与其各自所连接的原子一起形成5元至7元杂环基;
或R4b及R4c与其各自所连接的原子一起形成任选经一个或两个各独立地选自C1-C3烷基的取代基取代的5元至7元杂环基;
R4c及R4d各独立地为氢或C1-C3烷基;
或R4c及R4d与其各自所连接的原子一起形成C3-C5环烷基;
或
R3及R4与其各自所连接的氮原子一起形成:
i.含有一个或两个杂原子的7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤烷基及C6-C10芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经-(CH2)sC(=O)NRkRl取代;
其中s为0、1或2;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、甲基、苯基、环戊基及环己基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及NRqRw;
其中Rq为氢或C1-C3烷基及Rw为C6-C10芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;或
iii.含有一个杂原子的10元或11元双环稠合杂环基,其任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、C1-C3烷氧基、羟基及卤素。
3A.如实施方案1A或2A的化合物,其中Y1、Y2、Y3及Y4各为CH或C(R6与其结合)。
4A.如实施方案1A或2A的化合物,其中Y3为N且Y1、Y2及Y4各为CH或C(R6与其结合)。
5A.如实施方案1A或2A的化合物,其中Y2为N且Y1、Y3、Y4各为CH或C(R6与其结合)。
6A.如实施方案1A或2A的化合物,其中Y1为N且Y2、Y3及Y4各为CH或C(R6与其结合)。
7A.如实施方案1A至6A中任一项的化合物,其中R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C3烷氧基、羟基-C1-C3烷基及NRGRH;
其中RG及RH各独立地为氢或C1-C3烷基。
8A.如实施方案7A的化合物,其中R6在各情况下选自由以下组成的组:甲氧基、甲基、氟、氯、乙基、N(CH3)2、羟基、-OCH2CH2OH、-CH2OH、-CH2OCH3及-CH2CH2OH。
9A.如实施方案8A的化合物,其中R6在各情况下为甲氧基或甲基。
10A.如实施方案1A至6A中任一项的化合物,其中两个R6基团与其各自所连接的原子一起形成5元或6元杂环基、C6-C10芳基或5元至10元杂芳基。
11A.如实施方案10A的化合物,其中两个R6基团与其各自所连接的原子一起形成吡唑基、二氧杂环己烷基、吡啶基或苯基环。
12A.如实施方案1A至11A中任一项的化合物,其中n为1。
13A.如实施方案1A至11A中任一项的化合物,其中n为0。
14A.如实施方案1A至13A中任一项的化合物,其中f为1。
15A.如实施方案1A至13A中任一项的化合物,其中f为0。
16A.如实施方案1A至15A中任一项的化合物,其中R3选自由以下组成的组:氢、甲基及-CH2CH2OH。
17A.如实施方案16A的化合物,其中R3为甲基。
18A.如实施方案1A至17A中任一项的化合物,其中R4为(5元至10元单环或双环稠合杂芳基)-甲基。
19A.如实施方案18A的化合物,其中R4为(5元至10元单环或双环稠合杂芳基)-甲基,其中在连接点邻位的环原子中的至少一者为氮或氧。
20A.如实施方案18A或19A的化合物,其中R4选自由以下组成的组:吡啶基-甲基、嘧啶基-甲基及苯并噁唑-甲基。
22A.如实施方案21A的化合物,其中R4c及R4d各独立地为氢或甲基。
23A.如实施方案22A的化合物,其中R4c及R4d各为氢。
24A.如实施方案21A至23A中任一项的化合物,其中R4b为氢。
25A.如实施方案21A至24A中任一项的化合物,其中R4a为C1-C6烷基。
26A.如实施方案25A的化合物,其中R4a为叔丁基。
27A.如实施方案21A至24A中任一项的化合物,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的C6-C10芳基:卤素、C1-C6烷基、卤烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、双环稠合或螺杂环基。
28A.如实施方案27A的化合物,其中R4a为任选经氟或甲氧基取代的苯基。
29A.如实施方案21A至24A中任一项的化合物,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环或双环稠合杂芳基:卤素、C1-C6烷基、卤烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、双环稠合或螺杂环基。
30A.如实施方案29A的化合物,其中R4a为任选经氟、甲氧基或甲基取代的吡啶基或喹啉基。
31A.如实施方案21A至24A中任一项的化合物,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的C3-C7环烷基:卤素、C1-C6烷基、卤烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、双环稠合或螺杂环基。
32A.如实施方案31A的化合物,其中R4a为任选经甲基、三氟甲基、氟或羟基取代的环丙基、环丁基、环戊基或环己基。
33A.如实施方案21A至24A中任一项的化合物,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元或6元杂环基:卤素、C1-C6烷基、卤烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、双环稠合或螺杂环基。
34A.如实施方案33A的化合物,其中R4a选自由以下组成的组:任选经一个或两个各独立地选自由甲基及氧代组成的组的取代基取代的四氢呋喃基、吡咯烷基及四氢吡喃基。
35A.如实施方案21A至24A中任一项的化合物,其中R4a为(C6-C10芳基)-C1-C3烷基或(5元至10元单环杂芳基)-C1-C3烷基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤素、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、双环稠合或螺杂环基。
36A.如实施方案35A的化合物,其中R4a为苯基-甲基或吡啶基-甲基。
37A.如实施方案21A至23A中任一项的化合物,其中R4a及R4b与其各自所连接的原子一起形成5元至7元杂环基。
38A.如实施方案37A的化合物,其中R4a及R4b与其各自所连接的原子一起形成选自由以下组成的组的6元杂环基:哌啶基、吗啉基及哌嗪基。
39A.如实施方案21A或25A至36A中任一项的化合物,其中R4b及R4c与其各自所连接的原子一起形成任选经C1-C3烷基取代一次或两次的5元至7元杂环基。
40A.如实施方案39A的化合物,其中R4b及R4c与其各自所连接的原子一起形成任选经C1-C3烷基取代一次或两次的哌啶-2-酮或吡咯烷-2-酮。
42A.如实施方案41A的化合物,其中R4g为苯基或甲基。
43A.如实施方案1A至15A中任一项的化合物,其中R3及R4与其各自所连接的氮原子一起形成含有一个或两个杂原子的7元单环杂环基。
44A.如实施方案43A的化合物,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的7元单环杂环基,其中该杂环基任选经甲基或氧代取代一次。
45A.如实施方案43A的化合物,其中R3及R4与其各自所连接的氮原子一起形成含有两个杂原子的7元单环杂环基,其中所述杂原子为N或O,且该杂环基任选经苯基、甲基或氧代取代一次,且其中该苯基任选经甲氧基取代。
46A.如实施方案1A至15A中任一项的化合物,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的任选经甲氧基取代的11元双环稠合杂环基。
47A.如实施方案1A至46A中任一项的化合物,其中p为1。
1B.一种式(I')化合物:
或其药学上可接受的盐;其中
Z为N或CH;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C3烷基、氰基、-NRGRH、卤代-C1-C3烷氧基、-O-(CH2)u-Rbb、卤代-C1-C3烷基、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
u为0至6的整数;
Rbb为4元至7元单环杂环基、C3-C7环烷基或-NRGRH;
Rcc及Rdd各独立地为C1-C3烷基;
其中该环烷基、杂环基或杂芳基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代;
且
RG及RH各独立地为氢、-C(O)RGa或C1-C3烷基;其中
RGa为C1-C3烷基或氢;
或
两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元至6元单环杂芳基;其中
与环B稠合的该杂环基、苯基、环烷基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基;
n为0、1、2或3;
Y1、Y2、Y3及Y4各独立地选自由以下组成的组:CH、N、NH、O、S、SH、S-R6、N-R6及C-R6,条件是Y1、Y2、Y3及Y4中的1或2者可为N、N-R6、NH、O、SH或S-R6;
f为0或1;
p为1或2;
Rx在各情况下为卤素、C1-C6烷基、C1-C3烷氧基、羟基或氰基;
m为0、1或2;
R3选自由以下组成的组:氢、C1-C3烷基、羟基-C1-C3烷基、环丙基及苯基;
R4选自由以下组成的组:
i.分支链或直链(5元至10元单环或稠合双环杂芳基)-C1-C3烷基,或分支链或直链(6元或7元单环杂环基)-C1-C3烷基;其中
该杂芳基或杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C6-C10单环或稠合双环芳基、C3-C7环烷基、5元或6元杂芳基及5元至7元单环杂环基,且其中该芳基、环烷基、杂芳基或杂环基任选经一个或两个各自个别地选自由C1-C3烷基、卤素及羟基组成的组的取代基取代;且
当p为1时,该(5元至10元单环或稠合双环杂芳基)-C1-C3烷基中的C1-C3烷基为直链的;
且
其中
R4a及R4g各独立地选自由以下组成的组:氢;C1-C6烷基;羟基-C1-C6烷基;C1-C3烷氧基-C1-C6烷基;C3-C7环烷基;5元至10元单环、稠合双环、桥联双环或螺杂环基;C6-C10单环或稠合双环芳基;5元至10元单环或稠合双环杂芳基;(C6-C10单环或稠合双环芳基)-C1-C3烷基;及(5元至10元单环或稠合双环杂芳基)-C1-C3烷基;
其中R4a或R4g的该环烷基、杂环基、芳基、杂芳基、芳基-烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素;C1-C6烷基;卤代-C1-C3烷基;羟基;C1-C3烷氧基;卤代-C1-C3烷氧基;氧代;C3-C7环烷基;及5元至10元单环、稠合双环或螺杂环基;
R4b为氢或C1-C6烷基;或
R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基;或
R4b及R4c与其各自所连接的原子一起形成任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代的5元至7元单环杂环基:羟基、卤素及C1-C3烷基;或
R4c及R4d各独立地选自由以下组成的组:氢、C1-C3烷氧基、羟基、C1-C3烷基-硫基-C1-C3烷基、羟基-C1-C6烷基、C1-C6烷氧基-C1-C3烷基、C3-C7环烷基及C1-C3烷基;或
R4c及R4d与其各自所连接的原子一起形成C3-C7环烷基;
或当p为1时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个或两个杂原子的7元稠合双环杂环基、7元桥联双环杂环基或7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷氧基、氧代及-(CH2)sC(=O)NRkRl;其中
s为0、1、2或3;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、羟基、C1-C3烷基、C3-C7环烷基及C6-C10单环或稠合双环芳基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及-NRqRw;其中
Rq为氢或C1-C3烷基;且
Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;
或
iii.8元、9元、10元或11元稠合双环杂环基,或12元双环桥联及稠合杂环基,其中该8元、9元或11元杂环基含有一个杂原子且该10元或12元杂环基含有一个或两个杂原子;且其中该10元、11元或12元杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、C1-C3烷氧基及羟基;
或当p为2时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个杂原子的6元单环杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、羟基-(C1-C6烷基)、羟基、氧代及C1-C3烷氧基;或
ii.含有一个或两个杂原子的4元或7元单环杂环基,或含有一个、两个或三个杂原子的7元、8元、9元、10元或11元桥联双环、稠合双环或螺杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、氧代、氰基、C1-C3烷基、羟基、-NRGRH及-(CH2)sC(=O)NRkRl;
条件是当式(I)结构为
且
其中该式(I)化合物不为:
N-((1,4-二氧杂环己-2-基)甲基)-2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-胺;
4-(哌啶-1-基)-2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉;
4-(氮杂环庚-1-基)-2-(6-丙基吡啶-2-基)-5,6,7,8-四氢喹唑啉;
1-丙基-4-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,4-二氮杂环庚-2-酮;或
2-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,2-氧氮杂环庚烷;或其盐。
1C.一种式(I')化合物:
或其药学上可接受的盐;其中
Z为N或CH;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C10烷氧基、羟基-C1-C10烷基、氰基、-NRGRH、卤代-C1-C3烷氧基、-O-(C1-C6烷基)-Rbb、-O-Rbb、-(C1-C6烷基)-NRGIRHI、-S-C1-C3烷基、-S-C1-C3烷基-NRG1RH1、卤代-C1-C3烷基、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
羟基-C1-C10烷氧基或-O-(C1-C6烷基)-Rbb中的该烷基部分任选经氰基、羟基、羟基-C1-C3烷基、卤素或C1-C3烷氧基取代;
Rbb为4元至7元单环或桥联杂环基、C3-C7环烷基、5元或6元单环杂芳基、-SO2-C1-C3烷基、-S-C1-C3烷基、-C(O)NRG1RH1或-NRGRH;
Rcc为C1-C3烷基;且
Rdd为C1-C3烷基或6元杂芳基;
其中R6、Rbb或Rdd的该环烷基、杂环基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:羟基、卤素、卤代-C1-C3烷基、氧代、C1-C3烷氧基及C1-C3烷基;
RG1及RH1各独立地为氢或C1-C3烷基;
且
RG及RH各独立地为氢、-C(O)RGa或任选氘代的C1-C3烷基;其中
RGa为C1-C3烷基或氢;
或
两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元至6元单环杂芳基;其中
与环B稠合的该杂环基、苯基、环烷基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基;
n为0、1、2或3;
Y1、Y2、Y3及Y4各独立地选自由以下组成的组:CH、N、NH、O、S、SH、S-R6、N-R6及C-R6,条件是Y1、Y2、Y3及Y4中的1或2者可为N、N-R6、NH、O、SH或S-R6;
f为0或1;
p为1或2;
Rx在各情况下为卤素、C1-C6烷基、C1-C3烷氧基、羟基、氧代或氰基;
m为0、1或2;
R3选自由以下组成的组:氢、任选氘代的C1-C3烷基、羟基-C1-C3烷基、卤代-C1-C3烷基、环丙基及苯基;
R4选自由以下组成的组:
i.(5元至10元单环或稠合双环杂芳基)-C1-C3烷基或(6元或7元单环杂环基)-C1-C3烷基;其中
该杂芳基或杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C6-C10单环或稠合双环芳基、C3-C7环烷基、5元或6元杂芳基、-(C1-C3烷基)-T及5元至7元单环杂环基;
T选自由以下组成的组:C6-C10单环或稠合双环芳基、C3-C7环烷基、5元或6元杂芳基及5元至7元单环杂环基;且
其中R4的T或该芳基、环烷基、杂芳基或杂环基取代基任选经一个或两个各自个别地选自由C1-C3烷基、卤素及羟基组成的组的取代基取代;且
当p为1时,该(5元至10元单环或稠合双环杂芳基)-C1-C3烷基中的C1-C3烷基为直链的;
且
其中
R4a及R4g各独立地选自由以下组成的组:氢;C1-C10烷基;羟基-C1-C6烷基;卤代-C1-C3烷基;C1-C3烷氧基-C1-C6烷基;-C1-C6烷基-NRJ1RJ2;C3-C7环烷基;4元至10元单环、稠合双环、桥联双环或螺杂环基;C6-C10单环或稠合双环芳基;5元至10元单环或稠合双环杂芳基;(C6-C10单环或稠合双环芳基)-C1-C3烷基;及(5元至10元单环或稠合双环杂芳基)-C1-C3烷基;
RJ1及RJ2独立地为氢或C1-C3烷基;
其中R4a或R4g的该环烷基、杂环基、芳基、杂芳基、芳基-烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素;C1-C6烷基;卤代-C1-C3烷基;羟基;C1-C3烷氧基;卤代-C1-C3烷氧基;氧代;C3-C7环烷基;及5元至10元单环、稠合双环或螺杂环基;
R4b为氢或C1-C6烷基;或
R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基;或
R4b及R4c与其各自所连接的原子一起形成任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代的5元至7元单环杂环基:羟基、卤素及C1-C3烷基;或
R4c及R4d各独立地选自由以下组成的组:氢、C1-C3烷氧基、羟基、C1-C3烷基-硫基-C1-C3烷基、羟基-C1-C6烷基、C1-C6烷氧基-C1-C3烷基、C3-C7环烷基及C1-C3烷基;或
R4c及R4d与其各自所连接的原子一起形成C3-C7环烷基;
或当p为1时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个或两个杂原子的7元稠合双环杂环基、7元桥联双环杂环基或7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷氧基、氧代及-(CH2)sC(=O)NRkRl;其中
s为0、1、2或3;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、羟基、C1-C3烷基、C3-C7环烷基及C6-C10单环或稠合双环芳基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及-NRqRw;其中
Rq为氢或C1-C3烷基;且
Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;
或
iii.8元、9元、10元或11元稠合双环杂环基,或12元双环桥联及稠合杂环基,其中该8元、9元或11元杂环基含有一个杂原子且该10元或12元杂环基含有一个或两个杂原子;且其中该10元、11元或12元杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、C1-C3烷氧基及羟基;
或当p为2时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个杂原子的6元单环杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、羟基-(C1-C6烷基)、羟基、氧代及C1-C3烷氧基;或
ii.含有一个或两个杂原子的4元或7元单环杂环基,或含有一个、两个或三个杂原子的7元、8元、9元、10元或11元桥联双环、稠合双环或螺杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、氧代、氰基、C1-C3烷基、羟基、-NRGRH及-(CH2)sC(=O)NRkRl;
条件是当式(I)结构为
且
其中该式(I)化合物不为:
N-((1,4-二氧杂环己-2-基)甲基)-2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-胺;
4-(哌啶-1-基)-2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉;
4-(氮杂环庚-1-基)-2-(6-丙基吡啶-2-基)-5,6,7,8-四氢喹唑啉;
1-丙基-4-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,4-二氮杂环庚-2-酮;或
2-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,2-氧氮杂环庚烷;或其盐。
2B.如实施方案1B或1C的化合物或其药学上可接受的盐,其中p为1。
3B.如实施方案1B、2B或1C的化合物或其药学上可接受的盐,其中Z为N。
4B.如实施方案1B至3B或1C中任一项的化合物或其药学上可接受的盐,其中Y1、Y2、Y3及Y4各为CH或C-R6。
5C.如实施方案4B或1C的化合物或其药学上可接受的盐,其中Y1为CH,Y2为C-R6,Y3为CH,且Y4为CH。
5B.如实施方案1B至3B或1C中任一项的化合物或其药学上可接受的盐,其中Y3为N且Y1、Y2及Y4各为CH或C-R6。
6B.如实施方案1B至3B或1C中任一项的化合物或其药学上可接受的盐,其中Y2为N且Y1、Y3、Y4各为CH或C-R6。
7B.如实施方案1B至3B或1C中任一项的化合物或其药学上可接受的盐,其中Y1为N且Y2、Y3及Y4各为CH或C-R6。
8B.如实施方案1B至7B中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C3烷基、-O-(CH2)u-Rbb、卤代-C1-C3烷氧基、-O-Rcc-O-Rdd、卤代-C1-C3烷基及-NRGRH;其中
Rbb为-NRGRH;
u为1至3的整数;
RG及RH各独立地为氢或C1-C3烷基;且
Rcc及Rdd各独立地为C1-C3烷基。
9C.如实施方案1C、2B至8B或5C中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C10烷氧基、羟基-C1-C10烷基、-O-(C1-C6烷基)-Rbb、卤代-C1-C3烷氧基、-O-Rcc-O-Rdd、卤代-C1-C3烷基、-(C1-C6烷基)-NRGIRHI、-S-CH3、-S(CH2)2N(CH3)2及-NRGRH;其中
Rbb为-NRGRH、-C(O)N(CH3)2、-S(O)2CH3或-SCH3;
RG及RH各独立地为氢、任选氘代的C1-C3烷基或-C(O)RGa;其中RGa为C1-C3烷基;
RGI及RHI各独立地为氢或C1-C3烷基;
Rcc及Rdd各独立地为C1-C3烷基;且
其中羟基-C1-C10烷氧基中的该烷基部分任选经羟基、卤素或C1-C3烷氧基取代。
9B.如实施方案1B至8B、5C或9C中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:甲氧基、乙氧基、甲基、氟、氯、乙基、-N(CH3)2、羟基、-OCH2CH2OH、-CH2OH、-CH2OCH3、-OCH2CH2NH2、-OCH2CH2N(CH3)2、-OCH2C(CH3)2OH、-OCH2CF3、-OCHF2、-OCF3、-OCH2CH2OCH3、-OCH2CH2F、-OC(CH3)2CH2OH及-CH2CH2OH。
10C.如实施方案9C的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:甲氧基、乙氧基、甲基、氟、氯、乙基、-N(CH3)2、羟基、-OCH2CH2OH、-CH2OH、-CH2OCH3、-OCH2CH2NH2、-OCH2CH2N(CH3)2、-OCH2C(CH3)2OH、-OCH2CF3、-OCHF2、-OCF3、-OCH2CH2OCH3、-OCH2CH2F、-OC(CH3)2CH2OH、-OCH2CH(CH3)OH、-OCH2CH2NHC(O)CH3、-OC(CH3)2CH2N(CH3)2、-OCH(CH3)CH2OH、-OCH2CH(CH(CH3)2)OH、-OCH2CH(CH2CH3)OH、-OCH2C(CH2CH3)2OH、-OCH2CH2N(CH2CH3)2、-OCH(CH3)CH2N(CH3)2、-OCH2C(O)N(CH3)2、-OCH2C(CH3)2N(CH3)2、-OCH2CH(CH2OH)OH、-OCH2CH2NH(CH3)、-OCH2CH(CF3)OH、-OCH2C(CH3)(CH2CH3)OH、-OCH2CH(CH2OCH3)OH、-OCH2CH(CH2F)OH、-(CH2)3N(CH3)2、-(CH2)3N(CH3)H、-O(CH2)2S(O)2CH3、-O(CH2)2SCH3、-(CH2)2C(CH3)2OH、-OCH2CH2N(CD3)2及-CH2CH2OH。
10B.如实施方案9B、9C或10C的化合物或其药学上可接受的盐,其中R6在各情况下为甲氧基、-OCH2CH2OH或-OCH2C(CH3)2OH。
11C.如实施方案10C的化合物或其药学上可接受的盐,其中R6在各情况下为甲氧基、-OCH2CH2N(CH3)2、-OCH2CH2OH或-OCH2C(CH3)2OH。
12C.如实施方案11C的化合物或其药学上可接受的盐,其中R6在各情况下为-OCH2CH2N(CH3)2或-OCH2C(CH3)2OH。
11B.如实施方案1B至7B中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:-O-(CH2)u-Rbb及C3-C6;其中
u为0至3的整数;
Rbb为4元至7元单环杂环基或C3-C7环烷基;且
其中该环烷基或杂环基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代。
12B.如实施方案11B的化合物或其药学上可接受的盐,其中R6在各情况下选自由环丙基及-O-(CH2)u-Rbb组成的组;其中
u为0、1或2;且
Rbb选自由以下组成的组:各任选经羟基或甲基取代的环丙基、环丁基、四氢呋喃基、氧杂环丁烷基及吡咯烷基。
13C.如实施方案1C、2B至8B或5C中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:-O-(C1-C6烷基)-Rbb、-O-Rbb、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
Rcc为C1-C3烷基且Rdd为6元杂芳基;
Rbb为4元至7元单环或桥联杂环基、5元或6元单环杂芳基或C3-C7环烷基;且
其中R6、Rbb或Rdd的该环烷基、杂芳基或杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:羟基、卤素、C1-C3烷氧基、氧代、卤代-C1-C3烷基及C1-C3烷基。
14C.如实施方案13C的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:环丙基、-O-Rbb、-O-(CH2)-Rbb及-O-(CH2)2-Rbb、-O-(CH2)2-O-哒嗪基、任选经C1-C3烷基取代的咪唑基;其中
Rbb选自由以下组成的组:环丙基、环丁基、环戊基、环己基、四氢呋喃基、四氢吡喃醇、氧杂环丁烷基、二氧杂环戊烷基、氮杂环丁烷基、吗啉基、哌嗪基、2-氧杂-5-氮双环[2.2.1]庚烷、咪唑基、四唑基、哒嗪基、哌啶基、硫吗啉基及吡咯烷基,其各任选经羟基、氧代、氟、-CF3、-CH2CF3、-CH2CHF2、-CH2CH2F、甲氧基、乙基或甲基取代。
16C.如实施方案15C的化合物或其药学上可接受的盐,其中R6为
14B.如实施方案13B或13至16C的化合物或其药学上可接受的盐,其中R6为
15B.如实施方案1B至7B或1C中任一项的化合物或其药学上可接受的盐,其中两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元或6元单环杂芳基,所述基团各任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基。
16B.如实施方案1B至7B或1C中任一项的化合物或其药学上可接受的盐,其中两个R6基团与其各自所连接的原子一起形成与环B稠合的吡唑基、二氧杂环己烷基、吡啶基、嘧啶基、噻唑基、呋喃基、二氧杂环戊烷基或苯基环,其中该环任选经一个选自由以下组成的组的取代基取代:羟基、甲氧基、四氢吡喃基、-CH2OH及甲基。
17B.如实施方案16B的化合物或其药学上可接受的盐,其中两个R6基团与其各自所连接的原子一起形成选自由以下组成的组的环:与环B稠合的
18B.如实施方案17B的化合物或其药学上可接受的盐,其中两个R6基团与其各自所连接的原子一起形成选自由以下组成的组的环:与环B稠合的
18.bb如实施方案15B至18B中任一项的化合物,其中环B选自由以下组成的组:
19B.如实施方案1B至19B、1C、5C、9C、10C、11C、12C、13C、14C、15C或16C中任一项的化合物或其药学上可接受的盐,其中f为1。
n为0或1;且
Y2及Y3各独立地选自由以下组成的组:CH、N、NH、NR6、S、O及CR6,条件是Y2及Y3中仅一者可为N、NH、NR6、S或O。
23B.如实施方案20B至22B中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由C1-C3烷基及羟基-C1-C3烷基组成的组。
24B.如实施方案23B的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:甲基、乙基、正丙基、-CH2CH2OH及-CH2CH2CH2OH。
25B.如实施方案1B至24B、1C、5C、9C、10C、11C、12C、13C、14C、15C或16C中任一项的化合物或其药学上可接受的盐,其中n为1。
26B.如实施方案1B至24B、1C、5C、9C、10C、11C、12C、13C、14C、15C或16C中任一项的化合物或其药学上可接受的盐,其中n为0。
27B.如实施方案1B至14B、1C、5C、9C、10C、11C、12C、13C、14C、15C或16C中任一项的化合物或其药学上可接受的盐,其中n为2。
28B.如实施方案27B的化合物,其中一个R6选自由甲基及甲氧基组成的组,且另一R6选自由甲基、甲氧基、卤素及-OCH2CH2OH组成的组。
31C.如实施方案1至28B或1C、5C、9C、10C、11C、12C、13C、14C、15C或16C中任一项的化合物或其药学上可接受的盐,其中R3选自由以下组成的组:氢、甲基、乙基、苯基、-CD3、-CH2CF3及-CH2CH2OH。
29B.如实施方案1B至28B、1C、5C、9C、10C、11C、12C、13C、14C、15C、16C或31C中任一项的化合物或其药学上可接受的盐,其中R3选自由以下组成的组:氢、甲基、乙基、苯基及-CH2CH2OH。
30B.如实施方案29B或31C的化合物或其药学上可接受的盐,其中R3为甲基。
33C.如实施方案1B至30B或1C、5C、9C、10C、11C、12C、13C、14C、15C、16C或31C中任一项的化合物或其药学上可接受的盐,其中R4为(5元至10元单环或稠合双环杂芳基)-甲基,其中该杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:苯基、C3-C7环烷基、-(C1-C3烷基)-苯基及5元至7元单环杂环基,且其中单独的或-(C1-C3烷基)-苯基中的该苯基、环烷基或杂环基任选经一个或两个各自个别地选自由C1-C3烷基、卤素及羟基组成的组的取代基取代。
31B.如实施方案1B至30B或33C中任一项的化合物或其药学上可接受的盐,其中R4为(5元至10元单环或稠合双环杂芳基)-甲基,其中该杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:苯基、C3-C7环烷基及5元至7元单环杂环基,且其中该苯基、环烷基或杂环基任选经一个或两个各自个别地选自由C1-C3烷基、卤素及羟基组成的组的取代基取代。
32B.如实施方案31B或33C的化合物或其药学上可接受的盐,其中R4为(6元杂芳基)-甲基,其中该6元杂芳基中在连接点邻位的环原子中的至少一者为氮。
35C.如实施方案33C或32B的化合物或其药学上可接受的盐,其中R4选自由以下组成的组:吡啶基-甲基、嘧啶基-甲基、苯并噁唑-甲基、噁唑基-甲基及三唑基-甲基,其各任选经苯基或苯甲基取代,且其中该苯基任选经一个选自由氟、甲基及氯组成的组的取代基取代。
33B.如实施方案31B、32B或35C的化合物或其药学上可接受的盐,其中R4选自由以下组成的组:各任选经苯基取代的吡啶基-甲基、嘧啶基-甲基、苯并噁唑-甲基及三唑基-甲基,且其中该苯基任选经一个选自由氟、甲基及氯组成的组的取代基取代。
36B.如实施方案35B的化合物或其药学上可接受的盐,其中R4c选自由以下组成的组:氢、甲基、异丙基、-CH2OH、-CH2OC(CH3)3及-CH2CH2SCH3;且R4d选自由氢及甲基组成的组;或R4c及R4d与其各自所连接的原子一起形成环丙基环。
37B.如实施方案36B的化合物或其药学上可接受的盐,其中R4c及R4d各为氢。
37bb.如实施方案36B的化合物或其药学上可接受的盐,其中R4c为氢或甲基;且R4d为氢。
37bbb.如实施方案36B或37bb的化合物或其药学上可接受的盐,其中R4c为甲基;且R4d为氢。
38B.如实施方案35B至37B中任一项的化合物或其药学上可接受的盐,其中R4b为氢。
39B.如实施方案35B至38B中任一项的化合物或其药学上可接受的盐,其中R4a为C1-C6烷基。
42C.如实施方案39B的化合物或其药学上可接受的盐,其中R4a为甲基、乙基、异丙基、叔丁基或3-甲基戊-3-基。
43C.如实施方案39B或42C的化合物或其药学上可接受的盐,其中R4a为叔丁基或异丙基。
40B.如实施方案39B或42C的化合物或其药学上可接受的盐,其中R4a为叔丁基。
41B.如实施方案35B至38B中任一项的化合物或其药学上可接受的盐,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的苯基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环或稠合双环杂环基。
42B.如实施方案41B的化合物或其药学上可接受的盐,其中R4a为任选经一个选自由以下组成的组的取代基取代的苯基:氟、氯、甲基及甲氧基。
43B.如实施方案42B的化合物,其中R4a选自由以下组成的组:
44B.如实施方案35B至38B中任一项的化合物或其药学上可接受的盐,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环或稠合双环杂芳基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、稠合双环或螺杂环基。
45B.如实施方案44B的化合物或其药学上可接受的盐,其中R4a为吡啶基、嘧啶基、吡唑基、异噻唑基、哒嗪基或喹啉基,其任选经一个选自由以下组成的组的取代基取代:氟、氯、甲氧基、氮杂环庚烷基、环丙基、-CF3、-OCF3或甲基。
47B.如实施方案35B至38B中任一项的化合物或其药学上可接受的盐,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的C3-C7环烷基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环或稠合双环杂环基。
48B.如实施方案47B的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:环丙基、环丁基、环戊基、环己基及双环[1.1.1]戊-1-基,其任选经一个或两个各独立地选自由甲基、-CF3、氟或羟基组成的组的取代基取代。
52C.如实施方案48B的化合物,其中R4a选自由以下组成的组:
49B.如实施方案48B或52C的化合物,其中R4a选自由以下组成的组:
53C.如实施方案35B至38B中任一项的化合物或其药学上可接受的盐,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的4元至10元单环或稠合双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、氧代、C3-C7环烷基及5元至10元单环或稠合双环杂环基。
50B.如实施方案35B至38B或53C中任一项的化合物或其药学上可接受的盐,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环或稠合双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、氧代、C3-C7环烷基及5元至10元单环或稠合双环杂环基。
54C.如实施方案53C的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:四氢呋喃基、吡咯烷基、苯并[d][1,3]间二氧杂环戊烯基、氧杂环丁烷基及四氢吡喃基,其任选经一个或两个各独立地选自由甲基、甲氧基及氧代组成的组的取代基取代。
51B.如实施方案50B的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:四氢呋喃基、吡咯烷基、苯并[d][1,3]间二氧杂环戊烯基及四氢吡喃基,其任选经一个或两个各独立地选自由甲基、甲氧基及氧代组成的组的取代基取代。
55C.如实施方案54C的化合物,其中R4a选自由以下组成的组:
52B.如实施方案51B或55C的化合物,其中R4a选自由以下组成的组:
53B.如实施方案35B至38B中任一项的化合物或其药学上可接受的盐,其中R4a为(C6-C10单环或稠合双环芳基)-C1-C3烷基或(5元至10元单环或稠合双环杂芳基)-C1-C3烷基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、稠合双环杂环基。
54B.如实施方案53B的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:苯基-甲基、1-环丁基-2-乙基-5-甲基-1H-咪唑基及吡啶基-甲基。
57C.如实施方案53B的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:苯甲基、2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙基及吡啶基-甲基。
59C.如实施方案35B至38B中任一项的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:羟基-C1-C6烷基、卤代-C1-C3烷基、C1-C3烷氧基-C1-C6烷基及-C1-C6烷基-NRJ1RJ2,其中RJ1及RJ2各独立地为氢或C1-C3烷基。
60C.如实施方案59C的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:-C(CH3)2CH2OH、-CH2CH2OH、-C(CH3)2CH2OCH3、-CH(CH3)CH2OH、-CH2CH2N(CH3)2及-CH2CF3。
56B.如实施方案35B至38B中任一项的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:-C(CH3)2CH2OH、-CH2CH2OH及-C(CH3)2CH2OCH3。
61C.如实施方案59C、60C或56B的化合物或其药学上可接受的盐,其中R4a为-C(CH3)2CH2OH。
57B.如实施方案35B至38B中任一项的化合物或其药学上可接受的盐,其中R4a及R4b与其各自所连接的原子一起形成5元至10元单环、稠合双环或桥联双环杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基。
63C.如实施方案57B的化合物或其药学上可接受的盐,其中R4a及R4b与其各自所连接的原子一起形成哌啶基、吗啉基、吡咯烷基、氮杂环庚烷基、吲哚啉基、氮双环[3.1.1]庚烷基、2,3-二氢-1H-吡咯并[2,3-c]吡啶或哌嗪基,所述基团任选经一个或两个各独立地选自由羟基、甲基、氟及甲氧基组成的组的取代基取代。
58B.如实施方案57B或63C的化合物或其药学上可接受的盐,其中R4a及R4b与其各自所连接的原子一起形成哌啶基、吗啉基、吡咯烷基、氮杂环庚烷基、吲哚啉基、氮双环[3.1.1]庚烷基或哌嗪基,所述基团任选经一个或两个各独立地选自由甲基、氟及甲氧基组成的组的取代基取代。
60B.如实施方案35B、39B至56B、42C、43C、52C、53C、54C、55C、59C、60C或61C中任一项的化合物或其药学上可接受的盐,其中R4b及R4c与其各自所连接的原子一起形成任选经一个或两个各独立地选自C1-C3烷基的取代基取代的5元至7元单环杂环基。
61B.如实施方案60B的化合物或其药学上可接受的盐,其中R4b及R4c与其各自所连接的原子一起形成任选经甲基取代一次或两次的哌啶-2-酮或吡咯烷-2-酮。
62B.如实施方案1B至30B、1C、5C、9C、10C、11C、12C、13C、14C、15C、16C或31C中任一项的化合物或其药学上可接受的盐,其中R4为其中R4g选自由C6-C10单环或稠合双环芳基及C1-C3烷基组成的组。
63B.如实施方案62B的化合物或其药学上可接受的盐,其中R4g选自由苯基及甲基组成的组。
64B.如实施方案1B至28B、1C、5C、9C、10C、11C、12C、13C、14C、15C、16C或31C中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个或两个杂原子的7元单环或桥联双环杂环基;
其中当该7元杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基。
65B.如实施方案64B的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成:含有一个杂原子的7元杂环基,其中该杂环基任选经甲基或氧代取代一次;或含有两个杂原子的7元单环或桥联双环杂环基,其中所述杂原子为N或O,且该杂环基任选经一个或两个各独立地选自由苯基、甲基及氧代组成的组的取代基取代,且其中该苯基任选经甲氧基取代。
67B.如实施方案1B至28B、1C、5C、9C、10C、11C、12C、13C、14C、15C、16C或31C中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的10元或11元稠合双环杂环基,或12元双环稠合及桥联杂环基,所述基团各任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、C1-C3烷氧基、羟基及卤素。
69B.如实施方案1B至28B、1C、8C、9C、10C、11C、12C、13C、14C、15C、16C或31C中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的4元或6元单环杂环基;其中
该4元单环杂环基任选经-(CH2)sC(=O)NRkRl取代;其中
s为0、1或2;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、甲基、苯基、环戊基及环己基;
且
该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及-NRqRw;其中
Rq为氢或C1-C3烷基;
Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基,
其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基。
70B.如实施方案69B的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成
71B.如实施方案1B至70B、1C、5C、9C、10C、11C、12C、13C、14C、15C、16C、31C、33C、35C、36C、42C、52C、53C、54C、55C、61C、63C或64C中任一项的化合物或其药学上可接受的盐,其中Rx在各情况下为甲基。
72B.如实施方案1B至71B、1C、5C、9C、10C、11C、12C、13C、14C、15C、16C、31C、33C、35C、36C、42C、52C、53C、54C、55C、61C、63C或64C中任一项的化合物或其药学上可接受的盐,其中m为0。
73B.如实施方案1B至71B、1C、5C、9C、10C、11C、12C、13C、14C、15C、16C、31C、33C、35C、36C、42C、52C、53C、54C、55C、61C、63C或64C中任一项的化合物或其药学上可接受的盐,其中m为2。
79C.如实施方案1的化合物或其药学上可接受的盐,其中
Z为N;
p为1;
f为1;
Y1、Y2、Y3及Y4各独立地选自由CH、N及C-R6组成的组,条件是Y1、Y2、Y3及Y4中的1或2者可为N;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C10烷氧基、羟基-C1-C10烷基、氰基、-NRGRH、卤代-C1-C3烷氧基、-O-(C1-C6烷基)-Rbb、-O-Rbb、-(C1-C6烷基)-NRGIRHI、卤代-C1-C3烷基、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
羟基-C1-C10烷氧基或-O-(C1-C6烷基)-Rbb中的该烷基部分任选经羟基、羟基-C1-C3烷基、卤素或C1-C3烷氧基取代;
Rbb为4元至7元单环杂环基、C3-C7环烷基或-NRGRH;
Rcc及Rdd各独立地为C1-C3烷基;
其中R6或Rbb的该环烷基、杂环基或杂芳基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代;
且
RG1及RH1各独立地为氢或C1-C3烷基;
RG及RH各独立地为氢、-C(O)RGa或任选氘代的C1-C3烷基;其中
RGa为C1-C3烷基或氢;
或
两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元至6元单环杂芳基;其中
与环B稠合的该杂环基、苯基、环烷基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基;
n为0、1或2;
R3选自由以下组成的组:氢、苯基、-CH2CH2OH及任选氘代的甲基或乙基;
R4c选自由以下组成的组:氢、甲基、异丙基、-CH2OH、-CH2OC(CH3)3及-CH2CH2SCH3;
R4d选自由氢及甲基组成的组;
或
R4c及R4d与其各自所连接的原子一起形成环丙基环;
R4b为氢或甲基;
R4a选自由以下组成的组:氢;C1-C10烷基;羟基-C1-C6烷基;C1-C3烷氧基-C1-C6烷基;-C1-C6烷基-NRJ1RJ2;C3-C7环烷基;5元至10元单环、稠合双环或桥联双环杂环基;C6-C10单环或稠合双环芳基;4元至10元单环或稠合双环杂芳基;(C6-C10单环或稠合双环芳基)-C1-C3烷基;及(5元至10元单环或稠合双环杂芳基)-C1-C3烷基;其中R4a的该环烷基、杂环基、芳基、杂芳基、芳基烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、卤代-C1-C3烷氧基、氧代、C3-C7环烷基及5元至10元单环或稠合双环杂环基;
RJ1及RJ2独立地为氢或C1-C3烷基;
或
R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基;
Rx在各情况下为C1-C3烷基;且
m为0、1或2。
74B.如实施方案1B的化合物或其药学上可接受的盐,其中
Z为N;
p为1;
f为1;
Y1、Y2、Y3及Y4各独立地选自由CH、N及C-R6组成的组,条件是Y1、Y2、Y3及Y4中的1或2者可为N;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C3烷基、氰基、-NRGRH、卤代-C1-C3烷氧基、-O-(CH2)u-Rbb、卤代-C1-C3烷基、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
u为0至6的整数;
Rbb为4元至7元单环杂环基、C3-C7环烷基或-NRGRH;
Rcc及Rdd各独立地为C1-C3烷基;
其中该环烷基、杂环基或杂芳基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代;
且
RG及RH各独立地为氢、-C(O)RGa或C1-C3烷基;其中
RGa为C1-C3烷基或氢;
或
两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元至6元单环杂芳基;其中
与环B稠合的该杂环基、苯基、环烷基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基;
n为0、1或2;
R3选自由以下组成的组:氢、甲基、乙基、苯基及-CH2CH2OH;
R4c选自由以下组成的组:氢、甲基、异丙基、-CH2OH、-CH2OC(CH3)3及-CH2CH2SCH3;
R4d选自由氢及甲基组成的组;
或
R4c及R4d与其各自所连接的原子一起形成环丙基环;
R4b为氢或甲基;
R4a选自由以下组成的组:氢;C1-C6烷基;羟基-C1-C6烷基;C1-C3烷氧基-C1-C6烷基;C3-C7环烷基;5元至10元单环、稠合双环或桥联双环杂环基;C6-C10单环或稠合双环芳基;5元至10元单环或稠合双环杂芳基;(C6-C10单环或稠合双环芳基)-C1-C3烷基;及(5元至10元单环或稠合双环杂芳基)-C1-C3烷基;其中R4a的该环烷基、杂环基、芳基、杂芳基、芳基烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、卤代-C1-C3烷氧基、卤代-C1-C3烷基、氧代、C3-C7环烷基及5元至10元单环或稠合双环杂环基;
或
R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基;
Rx在各情况下为C1-C3烷基;且
m为0、1或2。
75B.如实施方案74B或79C的化合物或其药学上可接受的盐,其中m为0。
76B.如实施方案74B或79C的化合物或其药学上可接受的盐,其中m为2且Rx在各情况下为甲基。
77B.如实施方案74B至76B或79C中任一项的化合物或其药学上可接受的盐,其中Y1、Y2、Y3及Y4各为CH或C-R6;
Y3为N且Y1、Y2及Y4各为CH或C-R6;
Y2为N且Y1、Y3、Y4各为CH或C-R6;
或
Y1为N且Y2、Y3及Y4各为CH或C-R6。
77bb.如实施方案74B至77B或79C中任一项的化合物或其药学上可接受的盐,其中Y1为CH,Y2为C-R6,Y3为CH,且Y4为CH。
83C.如实施方案79C或75B至77bb中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C10烷基、-O-Rbb、-O-(C1-C6烷基)-Rbb、卤代-C1-C3烷氧基、-O-Rcc-O-Rdd、卤代-C1-C3烷基、C3-C6环烷基及-NRGRH;其中
Rbb为-NRGRH、4元至6元单环杂环基或C3-C7环烷基;
RG及RH各独立地为氢或C1-C3烷基;
Rcc及Rdd各独立地为C1-C3烷基;且其中
R6或Rbb的该环烷基或杂环基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代。
84C.如实施方案83C的化合物,其中Rbb选自由以下组成的组:环丙基、环丁基、四氢呋喃基、氧杂环丁烷基、吗啉基及吡咯烷基,其各任选经羟基或甲基取代;或Rbb为-N(CH3)2。
78B.如实施方案74B至77B中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C3烷基、-O-(CH2)u-Rbb、卤代-C1-C3烷氧基、-O-Rcc-O-Rdd、卤代-C1-C3烷基、C3-C6环烷基及-NRGRH;其中
Rbb为-NRGRH、4元或5元单环杂环基或C3-C7环烷基;
u为0至3的整数;
RG及RH各独立地为氢或C1-C3烷基;
Rcc及Rdd各独立地为C1-C3烷基;且其中
该环烷基或杂环基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代。
79B.如实施方案78B的化合物,其中Rbb选自由以下组成的组:环丙基、环丁基、四氢呋喃基、氧杂环丁烷基及吡咯烷基,其各任选经羟基或甲基取代。
85C.如实施方案79C、75B至77B或84C中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:甲氧基、乙氧基、甲基、氟、氯、乙基、-N(CH3)2、羟基、-OCH2CH(CH3)OH、-OCH2CH2N(CH2CH3)2、-OCH2C(CH3)(CH2CH3)OH、-OCH2CH(CH2OCH3)OH、-OCH2CH2OH、-CH2OH、-CH2OCH3、-OCH2CH2NH2、-OCH2CH2N(CH3)2、-OCH2C(CH3)2OH、-OCH2CF3、-OCHF2、-OCF3、-OCH2CH2OCH3、-OCH2CH2F、-OC(CH3)2CH2OH、-CH2CH2OH、
80B.如实施方案74B至79B中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:甲氧基、乙氧基、甲基、氟、氯、乙基、-N(CH3)2、羟基、-OCH2CH2OH、-CH2OH、-CH2OCH3、-OCH2CH2NH2、-OCH2CH2N(CH3)2、-OCH2C(CH3)2OH、-OCH2CF3、-OCHF2、-OCF3、-OCH2CH2OCH3、-OCH2CH2F、-OC(CH3)2CH2OH、-CH2CH2OH、
81B.如实施方案80B或86C的化合物或其药学上可接受的盐,其中R6在各情况下为甲氧基、-OCH2CH2OH、-OCH2CH2N(CH3)2、-OCH2C(CH3)2OH或
82B.如实施方案74B至77B中任一项的化合物或其药学上可接受的盐,其中两个R6基团与其各自所连接的原子一起形成与环B稠合的吡唑基、二氧杂环己烷基、吡啶基、嘧啶基、噻唑基、呋喃基、二氧杂环戊烷基或苯基环,其中该环任选经一个选自由以下组成的组的取代基取代:羟基、甲氧基、四氢吡喃基、-CH2OH及甲基。
83B.如实施方案74B至82B、79C、83C、84C、85C、86C或87C中任一项的化合物或其药学上可接受的盐,其中R3为甲基。
84B.如实施方案74B至82B、79C、83C、84C、85C、86C或87C中任一项的化合物或其药学上可接受的盐,其中n为1。
85B.如实施方案74B至84B、79C、83C、84C、85C、86C或87C中任一项的化合物或其药学上可接受的盐,其中R4b为氢。
92C.如实施方案79C、83C、84C、85C、86C或87C中任一项的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:
i.叔丁基或异丙基;
ii.苯基,其任选经一个选自由氟、氯、甲基及甲氧基组成的组的取代基取代;
iii.吡啶基、嘧啶基、吡唑基、异噻唑基、哒嗪基或喹啉基,其任选经一个选自由以下组成的组的取代基取代:氟、氯、甲氧基、氮杂环庚烷基、环丙基、-CF3、-OCF3及甲基;
iv.环丙基、环丁基、环戊基、环己基及双环[1.1.1]戊-1-基,其任选经一个或两个各独立地选自由甲基、-CF3、氟及羟基组成的组的取代基取代;
v.四氢呋喃基、吡咯烷基、苯并[d][1,3]间二氧杂环戊烯基及四氢吡喃基,其任选经一个或两个各独立地选自由甲基、甲氧基及氧代组成的组的取代基取代;
vi.苯甲基、2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙基及吡啶基-甲基;
及
vii.-C(CH3)2CH2OH、-CH2CH2OH及-C(CH3)2CH2OCH3。
86B.如实施方案74B至84B、79C、83C、84C、85C、86C或87C中任一项的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:
i.叔丁基;
ii.苯基,其任选经一个选自由氟、氯、甲基及甲氧基组成的组的取代基取代;
iii.吡啶基、嘧啶基、吡唑基、异噻唑基、哒嗪基或喹啉基,其任选经一个选自由以下组成的组的取代基取代:氟、氯、甲氧基、氮杂环庚烷基、环丙基、-CF3、-OCF3或甲基;
iv.环丙基、环丁基、环戊基、环己基及双环[1.1.1]戊-1-基,其任选经一个或两个各独立地选自由甲基、-CF3、氟或羟基组成的组的取代基取代;
v.四氢呋喃基、吡咯烷基、苯并[d][1,3]间二氧杂环戊烯基及四氢吡喃基,其任选经一个或两个各独立地选自由甲基、甲氧基及氧代组成的组的取代基取代;
vi.苯基-甲基、1-环丁基-2-乙基-5-甲基-1H-咪唑基及吡啶基-甲基;
及
vii.-C(CH3)2CH2OH、-CH2CH2OH及-C(CH3)2CH2OCH3。
87B.如实施方案74B至84B、79C、83C、84C、85C、86C或87C中任一项的化合物,其中R4a及R4b与其各自所连接的原子一起形成哌啶基、吗啉基、吡咯烷基、氮杂环庚烷基、吲哚啉基、氮双环[3.1.1]庚烷基或哌嗪基,所述基团任选经一个或两个各独立地选自由甲基、氟及甲氧基组成的组的取代基取代。
88B.如实施方案1B或1C的化合物或其药学上可接受的盐,其中
Z为N;
f为1;
R6在各情况下选自由以下组成的组:C1-C3烷基、-NRGRH、卤素及C1-C3烷氧基;
p为1
n为0或1
RG及RH各独立地为氢或C1-C3烷基;
Y1、Y2、Y3及Y4各独立地选自由CH、N及C-R6组成的组,条件是Y1、Y2、Y3及Y4中的1或2者可为N;
Rx在各情况下为卤素、C1-C6烷基、C1-C3烷氧基、羟基或氰基;
m为0;且
R3及R4与其各自所连接的氮原子一起形成:
i.含有一个或两个杂原子的7元稠合双环杂环基、7元桥联双环杂环基或7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷氧基、氧代及-(CH2)sC(=O)NRkRl;其中
s为0、1、2或3;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、羟基、C1-C3烷基、C3-C7环烷基及C6-C10单环或稠合双环芳基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及NRqRw;其中
Rq为氢或C1-C3烷基;且
Rw为C6-C10单环或双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;
或
iii.8元、9元、10元或11元稠合双环杂环基,或12元双环桥联稠合杂环基,其中该8元、9元或11元杂环基含有一个杂原子且该10元或12元杂环基含有一个或两个杂原子;且其中该10元、11元或12元杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、C1-C3烷氧基及羟基。
89B.如实施方案88B的化合物或其药学上可接受的盐,其中Y1、Y2、Y3及Y4各为CH或C-R6。
90B.如实施方案88B或89B的化合物或其药学上可接受的盐,其中R6若存在则选自由以下组成的组:-N(CH3)2、甲基、甲氧基、氟及氯。
91B.如实施方案88B至90B中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成:含有一个杂原子的7元杂环基,其中该杂环基任选经甲基或氧代取代一次;或含有两个杂原子的7元单环或桥联双环杂环基,其中所述杂原子为N或O,且该杂环基任选经一个或两个各独立地选自由苯基、甲基及氧代组成的组的取代基取代,且其中该苯基任选经甲氧基取代。
92B.如实施方案88B至90B中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的10元或11元稠合双环杂环基,或12元双环稠合桥联杂环基,所述基团各任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、C1-C3烷氧基、羟基及卤素。
93B.如实施方案88B至90B中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的4元或6元单环杂环基;其中
该4元单环杂环基任选经-(CH2)sC(=O)NRkRl取代;其中
s为0、1或2;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、甲基、苯基、环戊基及环己基;
且
该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及NRqRw;其中
Rq为氢或C1-C3烷基;
Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基。
94B.如实施方案1B、74B或1C的化合物或其药学上可接受的盐,其中
Z为N;
p为1;
f为1;
Y1、Y2、Y3及Y4各自独立地为CH或C-R6。
R6在各情况下选自由以下组成的组:C1-C3烷基、羟基、C1-C3烷氧基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C3烷基、羟基-C1-C6烷氧基、-O-(CH2)u-Rbb、卤代-C1-C3烷基、-O-Rcc-O-Rdd及C3-C6环烷基;;或R6在各情况下为-O-Rbb或-O-(C1-C6烷氧基)-Rbb,其中
u为0至6的整数;
Rbb为4元至7元单环杂环基、C3-C7环烷基或-NRGRH;
Rcc及Rdd各独立地为C1-C3烷基;
其中该环烷基或杂环基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代;
且
RG及RH各独立地为氢、-C(O)RGa或C1-C3烷基;其中
RGa为C1-C3烷基或氢;
n为0、1或2;
R3选自由以下组成的组:氢、甲基、乙基、苯基及-CH2CH2OH;
R4c选自由以下组成的组:氢、甲基、异丙基、-CH2OH及-CH2OC(CH3)3;
R4d选自由氢及甲基组成的组;
或
R4c及R4d与其各自所连接的原子一起形成环丙基环;
R4b为氢或甲基;
R4a选自由以下组成的组:氢;C1-C6烷基;羟基-C1-C6烷基;C1-C3烷氧基-C1-C6烷基;C3-C7环烷基;5元至10元单环、稠合双环或桥联双环杂环基;C6-C10单环或稠合双环芳基;5元至10元单环或稠合双环杂芳基;(C6-C10单环或稠合双环芳基)-C1-C3烷基;及(5元至10元单环或稠合双环杂芳基)-C1-C3烷基;其中R4a的该环烷基、杂环基、芳基、杂芳基、芳基烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、卤代-C1-C3烷氧基、卤代-C1-C3烷基、氧代、C3-C7环烷基及5元至10元单环或稠合双环杂环基;
或
R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基;
Rx在各情况下为C1-C3烷基;且
m为0、1或2。
95B.如实施方案94B的化合物或其药学上可接受的盐,其中Y1为CH,Y2为C-R6,Y3为CH,且Y4为CH。
96B.如实施方案94B或95B的化合物或其药学上可接受的盐,其中R6选自由羟基-C1-C6烷氧基及-O-(CH2)u-Rbb组成的组;其中
u为0至6的整数;
Rbb为4元至7元单环杂环基、C3-C7环烷基或-NRGRH;
其中该环烷基或杂环基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代;
且
RG及RH各独立地为氢或C1-C3烷基;且
n为0、1或2。
98B.如实施方案94B至97B中任一项的化合物或其药学上可接受的盐,其中:
R3为甲基;
R4c及R4d各为氢;
R4b为氢;且
R4a选自由以下组成的组:C1-C6烷基、C6-C10单环或稠合双环芳基及5元至10元单环或稠合双环杂芳基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基及卤代-C1-C3烷氧基。
99B.如实施方案98B的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:C1-C6烷基、苯基及吡啶基,其中该苯基或嘧啶基任选经C1-C3烷氧基取代。
101B.如实施方案1A、1B或1C的化合物或其药学上可接受的盐,该化合物选自表1。
102B.一种药物组合物,其包含如实施方案1B至101B、1A至47A、1C、5C、9C、10C、11C、12C、13C、14C、15C、16C、31C、33C、35C、36C、42C、52C、53C、54C、55C、61C、63C、64C、79C、83C、84C、85C、86C或87C中任一项的化合物或其药学上可接受的盐,及药学上可接受的赋形剂。
103B.一种抑制受试者中由运铁素介导的铁转运的方法,其包含向该受试者施用有效量的如实施方案1B至101B、1A至47A、1C、5C、9C、10C、11C、12C、13C、14C、15C、16C、31C、33C、35C、36C、42C、52C、53C、54C、55C、61C、63C、64C、79C、83C、84C、85C、86C或87C中任一项的化合物或如实施方案102B的药物组合物。
通用程序及实施例提供用于制备化合物的例示性方法。本领域技术人员应了解,其他合成途径可用于合成化合物。尽管流程、通用程序及实施例中描绘且论述了特定起始物质及试剂,但其他起始物质及试剂可容易地取而代之以提供各种衍生物和/或反应条件。另外,通过所描述方法制备的多种例示性化合物可根据本发明使用本领域技术人员熟知的常规化学法进一步改质。
通用合成流程
FPN1化合物1a及1b的通用合成方法。在某些实施方案中,可如流程1中所示合成化合物1a,核心中间体2a可经由方法A经各种经取代的胺3a置换,得到中间体4a,随后使其与各种有机金属试剂5a偶合,得到最终化合物1a。或者,可如流程2中所示合成最终化合物1a。中间体2a可经伯胺6a置换,得到中间体7a,与有机金属试剂5a偶合之后,所得中间体8a则可通过卤化物烷基化,得到化合物1a。可根据流程3合成最终化合物1b。中间体2a经甘氨酸酯9a置换,得到中间体10a,在与有机金属试剂5a偶合之后,皂化所得中间体11a。使对应甲酸中间体12a与各种胺偶合形成化合物1b。
可基于起始物质的可获得性及试剂、起始物质或中间体的合成兼容性而进行流程1至3的修改及变化。这对于本领域技术人员将是显而易见的。举例而言,R1及R2可为氢、卤素、简单烷基或可与环连接;R3可为氢或烷基;R4可为经氨基羰基、烷氧基取代的烷基;或R3及R4可连接在一起形成环胺。对于方法B,可使用另一可获得的杂芳族铃木(Suzuki)或施蒂勒(Stille)试剂,得到最终化合物1a。
流程1描绘一种使用方法A及方法B制备例示性化合物的方法。
流程1
流程2描绘一种使用方法A、方法B及方法C制备例示性化合物的方法。
流程2
流程3描绘一种使用方法A、方法B、方法D及方法E制备例示性化合物的方法。
流程3
以下实施例中提供用于方法A至E的条件及试剂。以下实施例为以说明而非限制的方式提供。
1.合成实施例
实施例1.1
方法A:使胺亲核偶合以得到中间体4a的通用合成方法
向100mL圆底烧瓶中放入二氯嘧啶中间体2a(1.00当量)、CH3CN、胺3a(1.10当量)及三乙胺(2.00当量)。在80℃下搅拌所得溶液3hr。真空浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚的硅胶柱上,得到中间体4a。
实施例1.2
方法B:用于金属介导的交叉偶合的通用合成方法
向用惰性氮气氛围吹扫及维持的100mL圆底烧瓶中放入中间体4a(1.00当量)、二噁烷、有机金属试剂5(2.0当量)及Pd(dppf)Cl2(0.05当量)。在100℃下搅拌所得溶液过夜。真空浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上或对其进行制备型HPLC纯化,得到化合物1a、8a或11a。
实施例1.3
方法C:用于使用卤化物烷基化以得到化合物1a的通用合成方法
将中间体8a(1.00当量)溶解于DMF中且冷却于冰浴中。分两份添加氢化钠(2.00当量)(60%)且搅拌反应物45min。缓慢添加卤化物(2.00当量)且再搅拌混合物1.5h。添加水(20mL)及乙酸乙酯(100mL),分离各相,且用更多乙酸乙酯萃取水相。将合并的有机相用一些水洗涤且经硫酸钠干燥。蒸发溶剂后,通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物。将纯化的洗脱份用1M HCl处理且冷冻干燥,得到化合物1a。
实施例1.4
方法D:用于皂化以得到化合物12a的通用合成方法
将中间体11a(1.00当量)溶解于THF及甲醇中。将氢氧化锂(5.00当量)溶解于水中且逐滴添加至溶液中。7h后,将混合物用6M HCl小心地酸化至pH 3且蒸发至干燥。使残余物与甲苯共蒸发且高真空干燥,得到12a。
实施例1.5
方法E:用于酰胺形成以得到化合物1b的通用合成方法
将中间体12a(1.00当量)悬浮于N,N-二甲基甲酰胺中,且随后添加N,N-二异丙基乙胺(2.50当量)、胺(1.35当量)及3-氧化六氟磷酸1-[双(二甲基氨基)亚甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓(HATU,1.35当量)。40h后,添加乙酸乙酯(50ml)及碳酸氢钠溶液(20ml),分离各相,且用乙酸乙酯(50ml)萃取水相。将合并的有机相用氯化钠溶液洗涤且经硫酸钠干燥。蒸发溶剂后,通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到化合物1b。
实施例1.6
常见中间体的实验性程序
流程4描绘一种制备中间体I的方法
流程4
步骤1
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(2.00g;10.58mmol;1.00当量)溶解于乙腈(36ml)中。缓慢添加氯化(2-乙氧基-2-氧代乙基)(甲基)铵(2.11g;13.75mmol;1.30当量,肌氨酸乙酯HCl),继的以N,N-二异丙基乙胺(4.6mL;26.45mmol;2.50当量)。将反应物在25℃下搅拌22h且随后在50℃下搅拌20h。蒸发溶剂且通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈固体的2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酸乙酯(2.18g,76%)。1H NMR(400MHz,氯仿-d)δ4.30-4.19(m,4H),3.31(s,3H),3.11(t,J=7.4Hz,2H),2.88(t,J=7.9Hz,2H),2.12-2.02(m,2H),1.30(t,J=7.2Hz,3H)。
步骤2
将2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酸乙酯(900.00mg;3.34mmol;1.00当量)溶解于1,4-二噁烷(9ml)中且用氩气吹扫。添加2-(三丁基锡烷基)吡啶(2.34mL;6.67mmol;2.00当量)及四(三苯基膦)钯(385.58mg;0.33mmol;0.10当量),将反应容器密封,且随后在热浴中于105℃下搅拌。16h后,蒸发溶剂且通过硅胶色谱(甲醇/二氯甲烷)纯化残余物,得到2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酸乙酯(0.72g,62%)。1H NMR(400MHz,氯仿-d)δ8.83(d,J=4.8Hz,1H),8.39-8.28(m,1H),7.86-7.77(m,1H),7.41-7.32(m,1H),4.37(s,2H),4.20(q,J=7.2,1.5Hz,2H),3.42(s,3H),3.23-3.12(m,4H),2.15-2.07(m,2H),1.27-1.23(m,3H)。MS(ES+):(M+H)+=269.9。
步骤3
将2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酸乙酯(0.72g;2.30mmol;1.00当量)溶解于THF(20ml)及甲醇(5ml)中。将溶解于水(8ml)中的氢氧化锂(0.28g;11.52mmol;5.00当量)逐滴添加至溶液中。7h后,将混合物用6M HCl小心地酸化至pH 3且蒸发至干燥。使残余物与甲苯共蒸发且高真空干燥,得到呈灰白色固体的2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酸盐酸盐(中间体I)。1H NMR(400MHz,DMSO-d6)δ8.84(d,J=4.7Hz,1H),8.41(d,J=7.9Hz,1H),8.21-8.12(m,1H),7.75(dd,J=7.8,4.8Hz,1H),3.28-3.27(m,2H),3.07-3.01(m,2H),2.15-2.05(m,2H)。MS(ES+):(M+H)+=284.9。
实施例1.7
流程5描绘一种制备中间体II的方法
流程5
步骤1
向1L 3颈圆底烧瓶中放入2-(苯甲氧基羰基氨基)乙酸(20.0g,95.6mmol,1.00当量)、DCM(500mL)、HOBt(15.5g,114.7mmol,1.20当量)、EDCI(22.0g,114.7mmol,1.20当量)及叔丁胺(21.0g,286.8mmol,3.00当量)。在室温下搅拌所得溶液过夜。浓缩所得混合物。将残余物施加至含PE/EA乙醚(0-50%)的硅胶柱上。由此产生25.1g(99%)呈白色固体的N-[(叔丁基氨甲酰基)甲基]-氨基甲酸苯甲酯。LCMS:(ES,m/z):[M+H]+265。
向250mL圆底烧瓶中放入N-[(叔丁基氨甲酰基)甲基]氨基甲酸苯甲酯(7.0g,26.48mmol,1.00当量)、MeOH(50mL)及Pd/C(10%)(0.70g,10%)。在室温下于H2(1atm)下搅拌所得溶液过夜。滤出固体。浓缩所得混合物。由此产生3.3g(95%)呈无色油状物的2-氨基-N-叔丁基乙酰胺。LCMS:(ES,m/z):[M+H]+:131。
向50mL圆底烧瓶中放入2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(0.80g,4.23mmol,1.00当量)、THF(20mL)、TEA(0.51g,5.04mmol,1.19当量)及2-氨基-N-叔丁基乙酰胺(0.58g,4.44mmol,1.05当量)。在室温下搅拌所得溶液过夜。浓缩所得混合物。将残余物施加至含乙酸乙酯/己烷(0-50%)的硅胶柱上。由此产生0.688g(57%)呈白色固体的N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基)乙酰胺。LCMS(ES,m/z):[M+H]+:283.1。
实施例1.8
合成1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷(化合物92)。
流程6描绘用于制备例示性化合物的合成途径。
流程6
步骤1
向100mL圆底烧瓶中放入2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(500.00mg,2.645mmol,1.00当量)、乙腈(20.00mL,0.487mmol,0.18当量)、氮杂环庚烷(314.78mg,3.174mmol,1.20当量)及TEA(321.17mg,3.174mmol,1.20当量)。在80℃下搅拌所得溶液2hr。真空浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:3)的硅胶柱上,得到600mg(90.10%)呈固体的1-[2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷。
步骤2
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入1-[2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷(300.00mg,1.192mmol,1.00当量)、二噁烷(20.00mL)、2-(三丁基锡烷基)吡啶(877.39mg,2.383mmol,2.0当量)及Pd(dppf)Cl2(43.60mg,0.060mmol,0.05当量)。于油浴中在100℃下搅拌所得溶液过夜。浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上。通过自EA(乙酸乙酯)再晶体来纯化粗产物。由此产生79mg(24.16%)呈白色固体的1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷。1H NMR(300MHz,DMSO-d6):δ8.66(d,J=4.5Hz,1H),8.25(d,J=7.8Hz,1H),7.882(t,J=7.8Hz,1H),7.42(dd,J=5.1Hz,6.0Hz,1H),3.78-3.64(m,4H),3.11-3.00(m,2H),2.83-2.78(m,2H),2.08-1.97(m,2H),1.76(s,4H),1.49(s,2H)。LCMS:(ES)[M+1]+m/z295.2。
实施例1.9
合成4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-氧氮杂环庚烷(化合物93)。
流程7描绘用于制备例示性化合物的合成途径。
流程7
步骤1
向100mL圆底烧瓶中放入2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(500.00mg,1.00当量)、CH3CN(10.00mL)、1,4-氧氮杂环庚烷盐酸盐(402.00mg,1.10当量)及TEA(534.00mg,2.00当量)。在80℃下搅拌所得溶液3hr。通过LCMS监测反应进程。真空浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:2)的硅胶柱上。由此产生600mg(89.28%)呈棕色固体的4-[2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-氧氮杂环庚烷。
步骤2
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入4-[2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-氧氮杂环庚烷(0.30g,1.18mmol,1.00当量)、二噁烷(20mL)、2-(三丁基锡烷基)吡啶(0.87g,2.36mmol,2.0当量)、Pd(dppf)Cl2(0.04g,0.035mmol,0.05当量)。于油浴中在100℃下搅拌所得溶液过夜。真空浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上。通过自EA再晶体来纯化粗产物。由此产生358.1mg(90%)呈淡棕色固体的4-[2-(吡啶-2-基)-5H,6H,7H-1-λ-4-环戊并[d]嘧啶-4-基]-1,4-氧氮杂环庚烷。1H NMR(300MHz,DMSO-d6):δ8.66(dd,J=0.9,0.9Hz,1H),8.25(d,J=7.8Hz,1H),7.91-7.86(m,1H),7.45-7.41(m,1H),3.97-3.87(m,4H),3.85-3.75(m,2H),3.66-3.62(m,2H),3.08(t,J=7.5Hz,2H),2.85-2.80(m,2H),2.06-1.96(m,4H)。LCMS(ES)[M+1]+m/z297.2。
实施例1.10
合成1-[2-(3-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷(化合物71)。
用4-氟-2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)吡啶,与化合物92类似地合成化合物71。1H NMR(400MHz,甲醇-d4)δ8.46(d,J=4.8Hz,1H),7.77-7.68(m,1H),7.54(dt,J=8.5,4.3Hz,1H),3.82(t,J=6.1Hz,4H),3.19(t,J=7.4Hz,2H),2.89(t,J=7.9Hz,2H),2.11(p,J=7.7Hz,2H),1.80(s,4H),1.59(p,J=2.8Hz,4H)。LCMS(ES)[M+1]+m/z312.4。
实施例1.11
合成5-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-2-氧杂-5-氮双环[2.2.1]庚烷(化合物72)。
用2-氧杂-5-氮双环[2.2.1]庚烷替换氮杂环庚烷,与化合物92类似地合成化合物72。LCMS(ES+):(M+H)+=295.0。1H NMR(400MHz,氯仿-d)δ8.85(d,J=4.8Hz,1H),8.40(d,J=7.9Hz,1H),7.89-7.79(m,1H),7.39(dd,J=7.5,4.9Hz,1H),5.33(s,1H),4.71(s,1H),4.00-3.94(m,2H),3.83-3.76(m,2H),3.20-2.96(m,4H),2.19-1.94(m,4H)。
实施例1.12
合成N-甲基-2-(吡啶-2-基)-N-[(吡啶-2-基)甲基]-5H,6H,7H-环戊并[d]嘧啶-4-胺(化合物73)
流程8描绘用于制备例示性化合物的合成途径。
流程8
步骤1
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(204.00mg;1.08mmol;1.00当量)溶解于乙腈(4ml)中。缓慢添加2-吡啶基甲胺(0.15mL;1.40mmol;1.30当量),继的以N,N-二异丙基乙胺(0.28mL;1.62mmol;1.50当量)。将反应物在25℃下搅拌18h,随后在50℃下搅拌6h。蒸发溶剂,且通过硅胶色谱(甲醇/二氯甲烷梯度)纯化残余物,得到呈白色固体的2-氯-N-(吡啶-2-基甲基)-5H,6H,7H-环戊并[d]嘧啶-4-胺(277mg,98%)。1H NMR(400MHz,氯仿-d)δ8.58(d,J=5.2Hz,1H),7.97-7.88(m,1H),7.59(d,J=7.8Hz,1H),7.45-7.38(m,1H),6.63(s,1H),4.86(d,J=5.3Hz,2H),2.87(t,J=7.8Hz,2H),2.79(t,J=7.5Hz,2H),2.19-2.09(m,2H)。
步骤2
将2-氯-N-(吡啶-2-基甲基)-5H,6H,7H-环戊并[d]嘧啶-4-胺(274.00mg;1.05mmol;1.00当量)悬浮于1,4-二噁烷(5ml)中且用氩气吹扫混合物。添加2-(三丁基锡烷基)吡啶(0.74mL;2.10mmol;2.00当量)及随后的四(三苯基膦)钯(121.44mg;0.11mmol;0.10当量)。密封反应容器,且在105℃下于热浴中搅拌内容物16h。蒸发溶剂且通过硅胶色谱(甲醇/二氯甲烷梯度)纯化残余物,得到呈白色固体的2-(吡啶-2-基)-N-(吡啶-2-基甲基)-5H,6H,7H-环戊并[d]嘧啶-4-胺(161mg,50%)。1H NMR(400MHz,氯仿-d)δ8.87(d,J=5.0Hz,1H),8.57(d,J=5.0Hz,1H),8.49(d,J=8.0Hz,1H),7.94-7.88(m,1H),7.80-7.73(m,1H),7.65(d,J=7.9Hz,1H),7.45(dd,J=7.4,4.9Hz,1H),7.30-7.26(m,1H),7.13(s,1H),5.07(d,J=5.1Hz,2H),3.11(t,J=7.8Hz,2H),2.95(t,J=7.5Hz,2H),2.24-2.16(m,2H)。MS(ES+):(M+H)+=304.0。
步骤3
将2-(吡啶-2-基)-N-(吡啶-2-基甲基)-5H,6H,7H-环戊并[d]嘧啶-4-胺(0.16g;0.53mmol;1.00当量)溶解于DMF(10ml)中且在冰浴中冷却。分两份添加氢化钠(42mg;1.05mmol;2.00当量)(60%)且搅拌反应物45m。缓慢添加碘甲烷(66μL;1.05mmol;2.00当量)且再搅拌混合物1.5h。添加水(20ml)及乙酸乙酯(100ml),分离各相,且用更多乙酸乙酯(3×75ml)及3:1氯仿:异丙醇(50ml)萃取水相。将合并的有机相用一些水(5ml)洗涤且经硫酸钠干燥。蒸发溶剂后,通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物。将纯化的洗脱份用1M HCl处理且冷冻干燥,得到呈白色固体的N-甲基-2-(吡啶-2-基)-N-[(吡啶-2-基)甲基]-5H,6H,7H-环戊并[d]嘧啶-4-胺盐酸盐(90mg,48%)。1H NMR(400MHz,氯仿-d)δ9.08(d,J=5.3Hz,1H),8.69(d,J=5.5Hz,1H),8.62(d,J=8.0Hz,1H),8.29-7.98(m,3H),7.75-7.68(m,1H),7.55-7.47(m,1H),5.68(s,2H),3.67(s,3H),3.52-3.37(m,2H),3.26-3.14(m,2H),2.23-2.12(m,2H)。MS(ES+):(M+H)+=317.9。
实施例1.13
合成N-(4-甲氧基苯基)-2-{甲基[2-(吡啶-2-基)嘧啶-4-基]氨基}乙酰胺(化合物75)。
流程9描绘用于制备例示性化合物的合成途径。
流程9
将氯化2-{4-[(羧甲基)(甲基)氨基]-5H,6H,7H-环戊并[d]嘧啶-2-基}吡啶-1-鎓(中间体I)(150.00mg;0.35mmol;1.00当量)悬浮于N,N-二甲基甲酰胺(3.5ml)中。添加N,N-二异丙基乙胺(0.15mL;0.87mmol;2.50当量)、4-甲氧基苯胺(57.5mg;0.47mmol;1.35当量)及随后的3-氧化六氟磷酸1-[双(二甲基氨基)亚甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓(HATU,177.6mg;0.47mmol;1.35当量)。40h后,添加乙酸乙酯(50ml)及碳酸氢钠溶液(20ml),分离各相,且用乙酸乙酯(50ml)萃取水相。将合并的有机相用氯化钠溶液洗涤且经硫酸钠干燥。蒸发溶剂后,通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈固体的N-(4-甲氧基苯基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(甲酸盐,46mg,34%)。1H NMR(400MHz,氯仿-d)δ10.18(s,1H),8.86(d,J=5.0Hz,1H),8.53(d,J=8.0Hz,1H),8.22(s,1H),8.04-7.93(m,1H),7.56-7.46(m,3H),6.76(d,J=8.6Hz,2H),4.56(s,2H),3.74(s,3H),3.50(s,3H),3.24(t,J=7.4Hz,2H),2.99(t,J=7.9Hz,2H),2.12(p,J=7.7Hz,2H)。MS(ES+):(M+H)+=390.1。
实施例1.14
合成N-(3-氟苯基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物74)。
用3-氟苯胺替换4-甲氧基苯胺,与化合物75类似地合成化合物74。LCMS(ES+):(M+H)+=379.0。1H NMR(400MHz,氯仿-d)δ10.80(s,1H),9.10-8.96(m,1H),8.67(d,J=7.9Hz,1H),8.21-8.09(m,1H),7.72-7.58(m,2H),7.40(d,J=8.2Hz,1H),7.21-7.11(m,1H),6.75-6.65(m,1H),4.71(s,2H),3.55(s,3H),3.29(t,J=7.4Hz,2H),2.97(t,J=7.9Hz,2H),2.14(p,J=7.7Hz,2H)。
实施例1.15
合成1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,2,3,4-四氢喹啉(化合物76)
流程10描绘用于制备例示性化合物的合成途径。
流程10
步骤1
向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(100.00mg;0.53mmol;1.00当量)于AcCN(2mL)中的溶液中添加1,2,3,4-四氢喹啉(73.98mg;0.56mmol;1.05当量),继的以休尼格氏碱(Hunig's base)(0.19mL;1.06mmol;2.00当量)。在75℃下加热混合物2h,将混合物冷却且浓缩,用水稀释残余物,通过过滤收集所得沉淀物,且真空干燥,得到1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}-1,2,3,4-四氢喹啉(25mg)。LCMS(ES+):(M+H)+=286.2,288.2。
步骤2
向1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}-1,2,3,4-四氢喹啉(25.00mg;0.09mmol;1.00当量)于甲苯(1.5mL)中的溶液中添加2-(三丁基锡烷基)吡啶(48.31mg;0.13mmol;1.50当量)及四(三苯基膦)钯(10.11mg;0.01mmol;0.10当量)。使混合物脱气且在110℃下加热15h。将混合物冷却且浓缩,用AcCN及水稀释,且通过制备型HPLC进行纯化,得到1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,2,3,4-四氢喹啉(36mg)。1HNMR(400MHz,甲醇-d4)δ8.73-8.67(m,1H),8.42(dt,J=8.0,1.2Hz,1H),7.96(td,J=7.8,1.8Hz,1H),7.50(ddd,J=7.5,4.9,1.3Hz,1H),7.17(q,J=7.5Hz,2H),7.03(td,J=7.5,1.3Hz,1H),6.77(d,J=7.9Hz,1H),4.10(t,J=6.5Hz,2H),2.97(t,J=7.7Hz,2H),2.82(t,J=6.6Hz,2H),2.31(t,J=7.3Hz,2H),2.02(dp,J=36.1,7.5,7.0Hz,4H)。LCMS(ES+):(M+H)+=329.1。
实施例1.16
合成2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-苯基乙酰胺(化合物77)
用苯胺替换4-甲氧基苯胺,与化合物75类似地合成化合物77。LC MS(ES+):(M+H)+=360.0。1H NMR(400MHz,氯仿-d)δ10.39(s,1H),8.98-8.87(m,1H),8.58(d,J=8.0Hz,1H),8.08-7.96(m,1H),7.62(d,J=8.0Hz,2H),7.59-7.51(m,1H),7.25-7.17(m,2H),7.01(t,J=7.4Hz,1H),4.61(s,2H),3.52(s,3H),3.26(t,J=7.4Hz,2H),2.98(t,J=7.9Hz,2H),2.18-2.07(m,2H)。
实施例1.17
合成N-环己基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物78)
用环己胺替换4-甲氧基苯胺,与化合物75类似地合成化合物78。1H NMR(400MHz,氯仿-d)δ9.07-8.93(m,1H),8.59(d,J=8.0Hz,1H),8.12-8.01(m,1H),7.83-7.64(m,1H),7.59(d,J=6.7Hz,1H),4.47(s,2H),3.78-3.68(m,1H),3.47(s,3H),3.24(t,J=7.4Hz,2H),3.00(t,J=7.9Hz,2H),2.17-2.07(m,2H),1.75(d,J=12.0Hz,2H),1.65-1.58(m,2H),1.56-1.49(m,1H),1.28-1.06(m,5H)。LCMS(ES+):(M+H)+=366.0。
实施例1.18
合成2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(氧杂环己-4-基)乙酰胺(化合物79)
用4-氨基四氢吡喃替换4-甲氧基苯胺,与化合物75类似地合成化合物79。LCMS(ES+):(M+H)+=368.1。1H NMR(400MHz,氯仿-d)δ9.32(s,1H),8.87(d,J=8.0Hz,1H),8.81-8.73(m,1H),8.45-8.35(m,1H),7.92-7.84(m,1H),4.76(s,2H),3.93-3.84(m,3H),3.58(s,3H),3.40-3.30(m,4H),2.96(t,J=7.9Hz,2H),2.16-2.11(m,2H),1.75-1.56(m,4H)。
实施例1.19
合成N-乙基-2-(吡啶-2-基)-N-[(嘧啶-2-基)甲基]-5H,6H,7H-环戊并[d]嘧啶-4-胺(化合物80)
用2-嘧啶基甲胺替换2-吡啶基甲胺且用碘乙烷替换碘甲烷,与化合物73类似地合成化合物80。LCMS(ES+):(M+H)+=333.0。1H NMR(400MHz,氯仿-d)δ8.96-8.82(m,3H),8.52(d,J=7.7Hz,1H),8.18-8.09(m,1H),7.75-7.68(m,1H),7.55(s,1H),5.43(s,2H),4.01(q,J=7.1Hz,2H),3.32-3.13(m,4H),2.28-2.17(m,2H),1.37(t,J=6.9Hz,3H)。
实施例1.20
合成N-甲基-2-(吡啶-2-基)-N-[(嘧啶-2-基)甲基]-5H,6H,7H-环戊并[d]嘧啶-4-胺(化合物81)
用2-嘧啶基甲胺替换2-吡啶基甲胺,与化合物73类似地合成化合物81。LCMS(ES+):(M+H)+=319.1。1H NMR(400MHz,氯仿-d)δ8.78-8.69(m,3H),8.33(s,1H),8.18(d,J=8.0Hz,1H),7.79-7.72(m,1H),7.38-7.31(m,1H),7.22-7.17(m,1H),5.14(s,2H),3.53(s,3H),3.21(t,J=7.4Hz,2H),3.15-3.10(m,2H),2.13-2.07(m,2H)。
实施例1.21
合成N-[(1,3-苯并噁唑-2-基)甲基]-N-甲基-2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-胺(化合物82)
用1,3-苯并噁唑-2-基甲胺替换2-吡啶基甲胺,与化合物73类似地合成化合物82。LCMS(ES+):(M+H)+=358.0。1H NMR(400MHz,氯仿-d)δ8.82(d,J=5.4Hz,1H),8.34(d,J=8.0Hz,1H),8.14(s,1H),7.86-7.77(m,1H),7.74-7.67(m,1H),7.54-7.47(m,1H),7.41-7.35(m,1H),7.35-7.29(m,2H),5.25(s,2H),3.54(s,3H),3.29(t,J=7.3Hz,2H),3.18-3.11(m,2H),2.16-2.12(m,2H)。
实施例1.22
合成3-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-2,3,4,5-四氢-1H-3-苯并氮杂卓(化合物83)
用2,3,4,5-四氢-1H-苯并[d]氮杂卓替换氮杂环庚烷,与化合物92类似地合成化合物83。LCMS(ES+):(M+H)+=343.0。1H NMR(400MHz,氯仿-d)δ8.81(d,J=4.8Hz,1H),8.41(d,J=7.9Hz,1H),7.89-7.80(m,1H),7.39(dd,J=7.5,4.9Hz,1H),7.15(s,4H),6.10(s,2H),4.08-3.99(m,4H),3.15-3.02(m,8H),2.19-2.08(m,2H)。
实施例1.23
合成N-(2-甲氧基乙基)-N-甲基-2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-胺(化合物84)
用N-(2-甲氧基乙基)-N-甲胺替换氮杂环庚烷,与化合物92类似地合成化合物84。LCMS(ES+):(M+H)+=285.0。1H NMR(400MHz,氯仿-d)δ8.81(dd,J=4.7,2.0Hz,1H),8.45(d,J=1.5Hz,1H),8.34(dd,J=8.2,1.5Hz,1H),7.89-7.80(m,1H),7.50-7.27(m,3H),3.97-3.90(m,2H),3.70-3.63(m,2H),3.41(s,3H),3.36(s,3H),3.23-3.14(m,4H),2.16-2.07(m,2H)。
实施例1.24
合成1-甲基-4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚烷(化合物85)
用1-甲基-1,4-二氮杂环庚烷替换氮杂环庚烷,与化合物92类似地合成化合物85。LCMS(ES+):(M+H)+=310.1。1H NMR(400MHz,氯仿-d)δ8.79(d,J=4.8Hz,1H),8.29-8.21(m,1H),7.86-7.76(m,1H),7.40-7.34(m,1H),4.36-4.22(m,2H),3.98(t,J=6.7Hz,2H),3.50-3.40(m,2H),3.28-3.18(m,2H),3.11(t,J=7.3Hz,2H),3.03(t,J=7.8Hz,2H),2.82(s,3H),2.56(s,2H),2.15-2.04(m,2H)。
实施例1.25
合成2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-1-(吗啉-4-基)乙-1-酮(化合物86)
用吗啉替换4-甲氧基苯胺,与化合物75类似地合成化合物86。LCMS(ES+):(M+H)+=354.0。1H NMR(400MHz,氯仿-d)δ8.96-8.86(m,1H),8.50-8.37(m,1H),8.21-8.15(m,1H),8.07-7.93(m,1H),7.60-7.48(m,1H),4.86-4.75(m,2H),3.81-3.74(m,2H),3.71-3.66(m,4H),3.62-3.58(m,2H),3.41(s,3H),3.29-3.25(m,2H),3.06-3.00(m,2H),2.17-2.05(m,2H)。
实施例1.26
合成N-甲基-N-(2-苯氧基乙基)-2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-胺(化合物87)
用N-甲基-N-(2-苯氧基乙基)胺替换氮杂环庚烷,与化合物92类似地合成化合物87。LCMS(ES+):(M+H)+=285.0。1H NMR(400MHz,氯仿-d)δ9.09(d,J=4.9Hz,1H),8.57(d,J=7.8Hz,1H),8.16-8.00(m,1H),7.69-7.63(m,1H),7.29-7.25(m,2H),6.98-6.91(m,1H),6.86(d,J=8.0Hz,2H),4.36(s,4H),3.61(s,3H),3.45(t,J=7.8Hz,2H),3.29(t,J=7.3Hz,2H),2.24-2.13(m,2H)。
实施例1.27
合成2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-1-(哌啶-1-基)乙-1-酮(化合物88)
用哌啶替换4-甲氧基苯胺,与化合物75类似地合成化合物88。LCMS(ES+):(M+H)+=352.1。1H NMR(400MHz,氯仿-d)δ9.03(d,J=5.1Hz,1H),8.69-8.55(m,1H),8.23-8.07(m,1H),7.74-7.64(m,1H),5.17-4.78(m,2H),3.64-3.56(m,2H),3.52(t,J=5.6Hz,2H),3.44(s,3H),3.33-3.20(m,4H),2.20-2.10(m,2H),1.73-1.62(m,4H),1.57-1.49(m,2H)。
实施例1.28
合成N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物89)。
用叔丁胺替换4-甲氧基苯胺,与化合物75类似地合成化合物89。1H NMR(400MHz,氯仿-d)δ9.33-9.18(m,1H),8.87(d,J=7.7Hz,1H),8.43-8.33(m,1H),8.28(s,1H),7.91-7.79(m,1H),4.71(s,2H),3.55(s,3H),3.29(t,J=7.3Hz,2H),3.00(t,J=7.9Hz,2H),2.17-2.07(m,2H),1.27(s,9H)。MS(ES+):(M+H)+=340.0。
实施例1.29
合成N-环己基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物91)
步骤1
将2-{[(叔丁氧基)羰基](甲基)氨基}丙酸(500mg;2.5mmol;1当量)溶解于DMF(6ml)中。添加N,N-二异丙基乙胺(1.1mL;6.15mmol;2.5当量)及随后的3-氧化六氟磷酸1-[双(二甲基氨基)亚甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓(HATU,1262mg;3.3mmol;1.35当量)。添加环己胺(0.38mL;3.3mmol;1.35当量)且在25℃下搅拌反应混合物。14h后,用乙酸乙酯(50ml)、水(15ml)及碳酸氢钠溶液(30ml)稀释反应物。分离各相,且用乙酸乙酯(50ml)萃取水相。将合并的有机物用氯化钠溶液(50ml)洗涤且经硫酸钠干燥。蒸发后,通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈白色晶体的N-[1-(环己基氨甲酰基)乙基]-N-甲基氨基甲酸叔丁酯(0.48g,68%)。LCMS(ES+):(M+H)+=285.0。
步骤2
将N-[1-(环己基氨甲酰基)乙基]-N-甲基氨基甲酸叔丁酯(0.48g;1.7mmol;1当量)溶解于二氯甲烷(12ml)中且于冰浴中冷却。缓慢添加三氟乙酸(6mL)且在20℃下搅拌反应物。1.6h后,将反应物蒸发成残余物且随后自甲苯(40ml)共蒸发。粗产物N-环己基-2-(甲基氨基)丙酰胺三氟乙酸盐直接用于下一步骤中。
步骤3
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(150mg;0.79mmol;1当量)溶解于含有N-环己基-2-(甲基氨基)丙烯酰胺三氟乙酸盐(355mg;1.19mmol;1.5当量)的乙腈(3ml)中。添加N,N-二异丙基乙胺(0.55mL;3.2mmol;4当量)且将反应物在50℃下搅拌14h,随后在60℃下搅拌6h且经18h达到30℃。蒸发后,通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈薄膜的2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-环己基丙酰胺(174mg,65%)。LCMS(ES+):(M+H)+=337.2。
步骤4
将2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-环己基丙酰胺(174mg;0.52mmol;1当量)溶解于1,4-二噁烷(4ml)中且用Ar气体吹扫溶液。添加2-(三丁基锡烷基)吡啶(0.39mL;1.03mmol;2当量),之后添加四(三苯基膦)钯(60mg;0.05mmol;0.1当量)。密封反应容器且在110℃下于热浴中搅拌15h。蒸发后,通过反相色谱(Waters XSelectCSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈灰白色固体的N-环己基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙烯酰胺(86mg,43%)。LCMS(ES+):(M+H)+=380.0。1H NMR(400MHz,DMSO-d6)δ8.69(d,J=4.8Hz,1H),8.34(d,J=7.9Hz,1H),8.19(d,J=8.3Hz,1H),7.96-7.84(m,1H),7.53-7.42(m,1H),5.16(q,J=7.0Hz,1H),3.63-3.49(m,1H),3.25-3.16(m,1H),3.14-3.06(m,4H),2.93-2.76(m,2H),1.74(s,1H),1.65(s,1H),1.59-1.44(m,3H),1.33(d,J=7.0Hz,3H),1.25-1.12(m,3H),1.07-0.93(m,2H)。
实施例1.30
合成N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物90)
用叔丁胺替换环己胺,与化合物91类似地合成化合物90。LCMS(ES+):(M+H)+=354.4。1H NMR(400MHz,DMSO-d6)δ8.80-8.74(m,1H),8.50(d,J=7.9Hz,1H),8.09-8.01(m,1H),7.81(s,1H),7.66-7.59(m,1H),5.14(q,J=7.0Hz,1H),3.26(s,3H),3.24-3.10(m,2H),3.05-2.88(m,2H),2.15-1.97(m,3H),1.40(d,J=7.1Hz,3H),1.21(s,9H)。
实施例1.31
合成10-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-10-氮三环[6.3.1.0^{2,7}]十二-2,4,6-三烯(化合物1)
用10-氮三环[6.3.1.02,7]十二-2(7),3,5-三烯替换氮杂环庚烷,与化合物92类似地合成化合物1。LCMS(ES+):(M+H)+=355.0。1H NMR(400MHz,氯仿-d)δ8.66(s,1H),8.45-8.12(m,1H),7.71(s,1H),7.26-6.87(m,5H),4.46-4.19(m,2H),3.52-3.10(m,4H),2.99-2.74(m,4H),2.34(s,1H),2.01-1.76(m,3H)。
实施例1.32
合成7-甲氧基-3-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-2,3,4,5-四氢-1H-3-苯并氮杂卓(化合物2)
用7-甲氧基-2,3,4,5-四氢-1H-3-苯并氮杂卓替换氮杂环庚烷,与化合物92类似地合成化合物2。LCMS(ES+):(M+H)+=373.1 1H NMR(400MHz,氯仿-d)δ8.90-8.70(m,1H),8.40(d,J=7.1Hz,2H),7.90-7.76(m,1H),7.43-7.31(m,1H),7.07(d,J=8.2Hz,1H),6.77-6.60(m,2H),4.10-3.91(m,4H),3.79(s,3H),3.15-2.91(m,8H),2.19-2.07(m,2H)。
实施例1.33
合成6-甲氧基-3-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-2,3,4,5-四氢-1H-3-苯并氮杂卓(化合物3)
用6-甲氧基-2,3,4,5-四氢-1H-3-苯并氮杂卓替换氮杂环庚烷,与化合物92类似地合成化合物3。LCMS(ES+):(M+H)+=373.0。1H NMR(400MHz,氯仿-d)δ8.81(dd,J=4.8,1.8Hz,1H),8.42(d,J=7.9Hz,1H),7.86-7.77(m,1H),7.39-7.31(m,1H),7.14-7.07(m,1H),6.79-6.74(m,2H),4.00(dt,J=25.4,4.9Hz,4H),3.81(s,3H),3.17-3.03(m,8H),2.15-2.06(m,2H)。
实施例1.34
合成1-(3-甲氧基苯基)-4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚烷(化合物4)
流程11描绘用于制备例示性化合物的合成途径。
流程11
步骤1
将4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚烷-1-甲酸叔丁酯(200mg;0.51mmol;1当量)溶解于二氯甲烷(5ml)中。缓慢添加三氟乙酸(2.5mL)且在25℃下搅拌反应物。1h后,蒸发反应物至干燥,且使残余物与甲苯共蒸发。LCMS(ES+):(M+H)+=296。
步骤2
将1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚烷(108mg;0.37mmol;1.15当量)及1-碘-3-甲氧基苯(75mg;0.32mmol;1当量)与1,4-二噁烷(1ml)及叔丁醇(0.5ml)混合。用Ar气体吹扫混合物。添加2-[2-(二环己基磷烷基)苯基]-N,N-二甲基苯胺(25mg;0.06mmol;0.20当量)、参(二苯亚甲基丙酮)二钯(0)(15mg;0.02mmol;0.05当量)及叔丁醇钠(46mg;0.48mmol;1.50当量),且密封反应容器并在100℃下搅拌。19h后,添加其他部分的试剂(碘化物、配体、钯催化剂及碱)以驱动产物形成。随后将反应混合物过滤、浓缩且通过反相色谱(Waters XSelect CSH C18柱,0-50%乙腈/0.1%甲酸水溶液梯度)纯化,得到呈黄色固体的1-(3-甲氧基苯基)-4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚烷(19mg,15%)。
MS(ES+):(M+H)+=402.1。1H NMR(400MHz,氯仿-d)δ8.94-8.87(m,1H),8.34(d,J=7.9Hz,1H),8.02-7.92(m,1H),7.62-7.53(m,1H),7.19-7.10(m,1H),6.41(d,J=8.3Hz,1H),6.35-6.28(m,2H),4.30-4.22(m,2H),3.92-3.86(m,2H),3.81-3.76(m,5H),3.64(t,J=6.2Hz,2H),3.36(t,J=8.0Hz,2H),3.18(t,J=7.4Hz,2H),2.27-2.15(m,4H)。
实施例1.35
合成N-(吡啶-2-基)-2-{[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物5)
流程12描绘用于制备例示性化合物的合成途径。
流程12
步骤1
向50mL 3颈圆底烧瓶中放入[(叔丁氧羰基)氨基]乙酸(2.0g,11.42mmol,1.0当量)、DMF(20.0mL)、2-氨基吡啶(1.29g,13.71mmol,1.2当量)及DIPEA(3.69g,28.54mmol,2.5当量)。之后在0℃下分数批添加HATU(5.21g,13.70mmol,1.2当量)。在室温下搅拌反应溶液2h。随后通过添加50mL H2O将反应物淬灭,过滤且在红外灯下干燥收集的固体。获得2.4g(产率84%)呈白色固体的N-[[(吡啶-2-基)氨甲酰基]甲基]氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z:252。
步骤2
向50mL圆底烧瓶中放入N-[[(吡啶-2-基)氨甲酰基]甲基]氨基甲酸叔丁酯(2.40g,9.55mmol,1.0当量)及DCM(20.0mL)。在0℃下向以上混合物中添加HCl(g)(2M于EA中)(19.0mL)。在室温下搅拌混合物2h。浓缩混合物以移除溶剂,获得呈白色固体的1.4g(产率78%)2-氨基-N-(吡啶-2-基)乙酰胺盐酸盐。LCMS(ES)[M-HCl+1]+m/z:152。
步骤3
向100mL圆底烧瓶中放入2-氨基-N-(吡啶-2-基)乙酰胺盐酸盐(1.40g,7.46mmol,1.0当量)、NMP(30.0mL)、2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(1.30g,6.88mmol,0.9当量)、DIEA(2.70g,20.89mmol,2.80当量)。于油浴中在60℃下搅拌混合物12h。冷却至室温后,将反应物用H2O(50mL)稀释且用3×40mL乙酸乙酯萃取。将合并的有机相用3×40ml盐水洗涤,经无水硫酸钠干燥,过滤,且减压浓缩滤液。通过含乙酸乙酯/石油醚(1:2)的硅胶柱纯化残余物。获得320mg(产率14%)呈白色固体的2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基)-N-(吡啶-2-基)乙酰胺。LCMS(ES)[M+1]+m/z:304。
步骤4
向50mL圆底烧瓶中放入2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基)-N-(吡啶-2-基)乙酰胺(320mg,1.05mmol,1.0当量)、二噁烷(20.0mL)、2-(三丁基锡烷基)吡啶(465mg,1.26mmol,1.2当量)及Pd(dppf)Cl2(86mg,0.11mmol,0.1当量)。在N2氛围下在110℃下于油浴中搅拌混合物12h。将反应混合物冷却至室温且浓缩以移除溶剂。通过含乙酸乙酯/石油醚(3:1)的硅胶柱纯化残余物。通过使用以下条件的急骤制备型HPLC进一步纯化粗产物:柱:HPH C18,50*3.0mm,2.6um,移动相A:水/0.05%NH3·H2O,移动相B:CH3CN,流动速率:1.2mL/min,梯度:1.1min内自5%B达至100%B,保持0.7min。获得78.9mg(产率22%)呈灰白色固体的N-(吡啶-2-基)-2-[[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1H-NMR(300MHz,DMSO-d6,ppm):δ10.60(s,1H),8.61(d,J=4.6Hz,1H),8.33(dd,J=4.9,1.1Hz,1H)8.23(d,J=8.1Hz,1H),8.03(d,J=8.4Hz,1H),7.78-7.69(m,2H),7.40-7.35(m,2H),7.09(ddd,J=7.3,4.8,1.0Hz,1H),4.31(d,J=5.8Hz,2H),2.86(t,J=7.7Hz,2H),2.79(t,J=7.4Hz,2H),2.09(p,J=7.5Hz,2H)。LCMS:(ES,m/z):[M+H]+:347.1。
实施例1.36
合成N-(2-氟苯基)-2-{[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物6)
流程13描绘用于制备例示性化合物的合成途径。
流程13
向50mL圆底烧瓶中放入[[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(160mg,0.59mmol,1.0当量)、DMF(3.0mL)、2-氟苯胺(98mg,0.88mmol,1.5当量)、DIEA(153mg,1.18mmol,2.0当量)及HATU(337mg,0.88mmol,1.5当量)。在室温下搅拌所得溶液2h。将反应溶液用5mL CH3CN稀释且过滤。通过使用以下条件的制备型HPLC(SHIMADZU(HPLC-01))纯化滤液:柱,Welch Xtimate C18,21.2*250mm,5um,移动相:水(10mmol/LNH4HCO3)及MeOH:CH3CN=1:1(15min内自25%相B达至65%),检测器,UV,254nm。此得到117.3mg呈淡黄色固体的N-(2-氟苯基)-2-[[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1H NMR(300MHz,DMSO-d6)δ10.03(br,1H),8.63-8.61(m,1H),8.31-8.28(m,1H),7.88-7.75(m,2H),7.50-7.37(m,2H),7.29-7.18(m,1H),7.18-7.08(m,2H),4.28(d,J=5.4Hz,2H),2.86(t,J=7.8Hz,2H),2.78(t,J=7.4Hz,2H),2.14-2.04(m,2H)。LCMS(ES)[M+1]+m/z:364.1。
实施例1.37
合成2-{[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(喹啉-7-基)乙酰胺(化合物7)
流程14描绘用于制备例示性化合物的合成途径。
流程14
在0℃下向50mL圆底烧瓶中放入[[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(160mg,0.59mmol,1.0当量)、DMF(3.0mL)、喹啉-7-胺(128mg,0.88mmol,1.5当量)、DIEA(153mg,1.18mmol,2.0当量)及HATU(337mg,0.88mmol,1.5当量)。添加后,在室温下搅拌混合物2h。将反应溶液用5mL CH3CN稀释且过滤。通过使用以下条件的制备型HPLC纯化滤液:柱,Welch Xtimate C18,21.2*250mm,5um,移动相:水(10mmol/L NH4HCO3)及MeOH:CH3CN=1:1(15min内自25%相B达至70%);检测器,UV 254nm。由此获得118.0mg(50%)呈灰色固体的2-((2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)-N-(喹啉-7-基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ10.64(s,1H),8.82(dd,J=4.2,1.8Hz,1H),8.64-8.61(m,1H),8.43(d,J=1.8Hz,1H),8.29-8.25(m,2H),7.92(d,J=8.7Hz,1H),7.81-7.69(m,2H),7.54-7.50(m,1H),7.43-7.36(m,2H),4.30(d,J=5.7Hz,2H),2.90-2.76(m,4H),2.15-2.05(m,2H)。LCMS:(ES,m/z):[M+1]+m/z:397.1。
实施例1.38
合成N-叔丁基-2-{[2-(嘧啶-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物8)
流程15描绘用于制备例示性化合物的合成途径。
流程15
向在惰性氮气氛围中吹扫及维持的10mL密封管中放入N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基)乙酰胺(0.30g,1.06mmol,1.00当量)、二噁烷(10mL)、4-(三丁基锡烷基)嘧啶(0.47g,1.27mmol,1.20当量)及Pd(dppf)Cl2.CH2Cl2(0.17g,0.20当量)。在130℃下搅拌所得溶液过夜。浓缩所得混合物。将残余物施加至含MeOH/EA(1:9)的硅胶柱上。通过使用以下条件的制备型HPLC纯化粗产物:柱,welch X-timate C18,21.2*250mm,5um;移动相;相A水(10mmol/L NH4HCO3),相B CH3CN/MeOH(1:1)(15min内自15%B达至60%);检测器,220nm。由此产生57.7mg(16.7%)呈白色固体的N-叔丁基-2-[[2-(嘧啶-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1H-NMR:(300MHz,DMSO-d6,ppm):δ9.28(s,1H),8.93(d,J=5.1Hz),8.32(d,J=5.1Hz,1H),7.67(s,1H),7.29(t,J=6.0Hz,1H),3.97(d,J=5.7Hz,2H),2.87(q,J=7.8Hz,2H),2.76(q,J=7.2Hz,2H),2.13-2.06(m,2H),1.24(s,9H)。LCMS:(ES,m/z):[M+H]+:327.2。
实施例1.39
合成N-叔丁基-2-{[2-(吡啶-2-基)-5H,6H,7H-环戊并[b]吡啶-4-基]氨基}乙酰胺(化合物9)
流程16描绘用于制备例示性化合物的合成途径。
流程16
步骤1
向用惰性氮气氛围吹扫及维持的40mL小瓶中放入2,4-二氯-5H,6H,7H-环戊并[b]吡啶(500.00mg,2.66mmol,1.00当量)、2-(三丁基锡烷基)吡啶(1272.53mg,3.46mmol,1.30当量)、二噁烷(10.00mL)及Pd(PPh3)4(307.25mg,0.26mmol,0.10当量)。在110℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3.H2O)及CAN(11min内自50%相B达至80%);检测器,254。由此产生350mg(57.06%)呈白色固体的2-[4-氯-5H,6H,7H-环戊并[b]吡啶-2-基]吡啶。LCMS(ES)[M+H]+m/z:231。
步骤2
向使用惰性氮气氛围吹扫及维持的40mL小瓶中放入2-[4-氯-5H,6H,7H-环戊并[b]吡啶-2-基]吡啶(160.00mg,0.69mmol,1.00当量)、2-氨基-N-叔丁基乙酰胺(99.32mg,0.76mmol,1.10当量)、Pd(OAc)2(15.57mg,0.069mmol,0.10当量)、Cs2CO3(451.94mg,1.38mmol,2.00当量)、BINAP(86.37mg,0.14mmol,0.20当量)、二噁烷(10.00mL)。在100℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物(300mg):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自20%相B达至50%);检测器,254nm。由此产生167.7mg(74.53%)呈灰白色固体的N-叔丁基-2-[[2-(吡啶-2-基)-5H,6H,7H-环戊并[b]吡啶-4-基]氨基]乙酰胺。1HNMR(300MHz,DMSO-d6)δ8.59(ddd,J=4.8,1.9,0.9Hz,1H),8.30(dt,J=8.0,1.1Hz,1H),7.84(td,J=7.7,1.8Hz,1H),7.66(s,1H),7.41-7.30(m,2H),6.00(t,J=5.7Hz,1H),3.77(d,J=5.7Hz,2H),2.88(t,J=7.6Hz,2H),2.75(t,J=7.3Hz,2H),2.12-2.02(m,2H),1.27(s,9H)。LCMS(ES,m/z):[M+H]+:325.1。
实施例1.40
合成N-叔丁基-2-{[2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉-4-基]氨基}乙酰胺(化合物10)
流程17描绘用于制备例示性化合物的合成途径。
流程17
步骤1
向40mL小瓶中放入2,4-二氯-5,6,7,8-四氢喹唑啉(1.00g,4.92mmol,1.00当量)、2-氨基-N-叔丁基乙酰胺(0.71g,5.47mmol,1.11当量)、DIEA(1.27g,9.85mmol,2.00当量)及CH3CN(10.00mL)。在80℃下搅拌所得溶液过夜。将反应混合物冷却至室温。通过使用以下条件的制备型HPLC纯化粗产物(2g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3.H2O)及CAN(11min内自20%相B达至60%);检测器,254。由此产生1.1g(75.26%)呈白色固体的N-叔丁基-2-[(2-氯-5,6,7,8-四氢喹唑啉-4-基)氨基]乙酰胺。LCMS(ES)[M+H]+m/z:297。
步骤2
向用惰性氮气氛围吹扫及维持的40mL小瓶中放入N-叔丁基-2-[(2-氯-5,6,7,8-四氢喹唑啉-4-基)氨基]乙酰胺(500.00mg,1.68mmol,1.00当量)、2-(三丁基锡烷基)吡啶(806.26mg,2.19mmol,1.30当量)、二噁烷(10.00mL)及Pd(dppf)Cl2(123.26mg,0.17mmol,0.10当量)。在110℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物(800mg):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自20%相B达至50%);检测器,254nm。由此产生139.2mg(24.34%)呈白色固体的N-叔丁基-2-[[2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉-4-基]氨基]乙酰胺。1H-NMR(300MHz,DMSO-d6)δ8.65(ddd,J=4.8,1.8,0.9Hz,1H),8.33(dt,J=8.0,1.1Hz,1H),7.87(td,J=7.7,1.8Hz,1H),7.71(s,1H),7.45-7.40(m,1H),6.88(t,J=5.6Hz,1H),3.95(d,J=5.6Hz,2H),2.73-2.63(m,2H),2.46-2.38(m,2H),1.81-1.78(m,4H),1.24(s,9H)。LCMS(ES,m/z):[M+H]+:340.1
实施例1.41
合成N-(4-甲氧基苯基)-1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]哌啶-3-胺(化合物11)
步骤1
将1-溴-4-甲氧基苯(0.25g;1.34mmol;1当量)及3-氨基-1-哌啶甲酸叔丁酯(0.32g;1.6mmol;1.2当量)溶解于1,4-二噁烷(5ml)及叔丁醇(2.5ml)中。用Ar气体吹扫溶液,且添加叔丁醇钠(0.26g;2.67mmol;2当量)、2-[2-(二环己基磷烷基)苯基]-N,N-二甲基苯胺(52.6mg;0.13mmol;0.1当量)及参(二苯亚甲基丙酮)二钯(0)(61.2mg;0.07mmol;0.05当量)。在100℃下于热浴中在密封的反应容器中搅拌6h。冷却及蒸发后,通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈固体的3-[(4-甲氧基苯基)氨基]哌啶-1-甲酸叔丁酯(178mg,43%)。LCMS(ES+):(M+H)+=307.0。1H NMR(400MHz,氯仿-d)δ6.82-6.76(m,2H),6.76-6.60(m,2H),4.09-3.93(m,1H),3.76-3.67(m,4H),3.33-3.22(m,1H),3.09-2.95(m,1H),2.95-2.75(m,1H),2.07-1.95(m,1H),1.76-1.68(m,1H),1.45(s,9H)。
步骤2
将3-[(4-甲氧基苯基)氨基]哌啶-1-甲酸叔丁酯(178mg;0.58mmol;1当量)溶解于DCM(5ml)中且于冰浴中冷却。缓慢添加三氟乙酸(2.55mL)且在20℃下搅拌反应物1小时。蒸发反应物,且使残余物与甲苯共蒸发,得到三氟乙酸3-[(4-甲氧基苯基)氨基]哌啶-1-鎓,其直接用于下一步骤中。
步骤3
向圆底烧瓶中添加2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(100.00mg;0.53mmol;1.00当量)、乙腈(3.5ml)、三氟乙酸3-[(4-甲氧基苯基)氨基]哌啶-1-鎓(186.38mg;0.58mmol;1.10当量)、休尼格氏碱(0.38mL;2.17mmol;4.10当量)。在约70℃下搅拌混合物。冷却及蒸发后,通过硅胶色谱(0至50%乙酸乙酯/己烷梯度)纯化残余物,得到1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}-N-(4-甲氧基苯基)哌啶-3-胺(144mg,76%)。LCMS(ES+):(M+H)+=402.4。
步骤4
向圆底烧瓶中添加含1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}-N-(4-甲氧基苯基)哌啶-3-胺(144.00mg;0.40mmol;1.00当量)的1,4-二噁烷(无水,约3ml)。用Ar吹扫溶液。向混合物添加2-(三丁基锡烷基)吡啶(0.26mL;0.80mmol;2.00当量)及四(三苯基膦)钯(46.37mg;0.04mmol;0.10当量)。在105℃下于加热块中搅拌15h后,浓缩混合物且通过制备型HPLC纯化残余物,得到呈黄色固体的N-(4-甲氧基苯基)-1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]哌啶-3-胺(52mg)。LCMS(ES+):(M+H)+=402.4。1H NMR(400MHz,氯仿-d)δ9.01-8.83(m,1H),8.38(d,J=8.6Hz,1H),8.00-7.86(m,1H),7.55-7.43(m,1H),7.08-6.87(m,2H),6.87-6.69(m,2H),4.79(s,1H),4.16-4.00(m,1H),3.74(s,3H),3.62-3.44(m,3H),3.17-2.87(m,4H),2.17-1.99(m,3H),1.99-1.75(m,2H),1.70-1.52(m,1H)。
实施例1.42
合成N-叔丁基-2-{[2-(5-甲氧基吡嗪-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物12)
流程18描绘用于制备例示性化合物的合成途径。
流程18
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(200mg,0.674mmol,1.00当量)、二噁烷(10.0ml)、2-甲氧基-5-(三甲基锡烷基)吡嗪(275mg,1.01mmol,1.50当量)及Pd(PPh3)4(155mg,0.135mmol,0.20当量)的混合物。在110℃下搅拌所得溶液16小时。浓缩所得混合物。将粗反应混合物过滤且进行反相制备型MPLC(Prep-C18,20-45mM,120g,TianjinBonna-Agela Technologies;经15min时段自5%MeCN/水达至35%MeCN/水的梯度洗脱,其中两种溶剂皆含有0.1%甲酸)。由此产生71.7mg(28%)呈灰白色固体的N-(叔丁基)-2-((2-(5-甲氧基吡嗪-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1HNMR(300MHz,DMSO-d6,ppm):δ9.12(d,J=1.4Hz,1H),8.36(d,J=1.3Hz,1H),7.68(s,1H),4.13(s,2H),3.98(s,3H),3.27(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.00-1.95(m,2H),1.25-1.22(m,9H)。LCMS(ES)[M+1]+m/z:371.2。
实施例1.43A
合成N-叔丁基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物174)
流程19A描绘用于制备例示性化合物的合成途径。
流程19A
步骤1
向250mL 3颈圆底烧瓶中放入2-羟基-2-甲基丙酸乙酯(10.0g,75.8mmol,1.00当量)、含3,4-二氢-2H-吡喃(9.54g,113.7mmol,1.50当量)的二氯甲烷(100mL)及吡啶4-甲基苯磺酸酯(0.95g,3.79mmol,0.05当量)。在室温下搅拌所得溶液3h。将反应混合物倒入水中且用Et2O萃取。有机层经Na2SO4干燥,过滤,且真空浓缩滤液。通过硅胶色谱(己烷/乙酸乙酯,100:0至5:1)纯化粗残余物,得到15.6g(95%)呈无色油状物的2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙酸乙酯。
步骤2
向500mL 3圆底烧瓶中放入含2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙酸乙酯(15.0g,69.4mmol,1.00当量)的THF(150.00mL)。在0℃下分批添加氢化锂铝(69.4mL,1mol/L,69.4mmol,1.00当量)。搅拌反应混合物5h,之后减缓添加Na2SO4.10H2O(22.3g,69.4mmol,1.00当量)。在0℃下搅拌30分钟后,过滤混合物且真空浓缩滤液,得到呈无色油状物的2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇(8.9g,74%),其不经进一步纯化即用于下一步骤中。
步骤3
向250mL 3颈烧瓶中放入2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇(3.9g,22.4mmol,2.0当量)及DMF(50mL),在0-5℃下分批添加NaH(60%于矿物油中)(896mg,22.4mmol,2.0当量)。在室温下搅拌混合物1h。此后,在0-5℃下添加N-(叔丁基)-2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(4g,11.2mmol,1.00当量)。在50℃下搅拌反应混合物5h。(在2个批次中重复反应)。将反应混合物冷却至室温,用150mL水稀释,且用3×100mL乙酸乙酯萃取。将合并的有机相用3×150mL水及盐水1×100mL洗涤,经无水硫酸钠干燥,且浓缩,得到10g粗产物(产率87%)。此粗产物不经纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:512。
步骤4
向250mL 3颈烧瓶中放入N-(叔丁基)-2-(甲基(2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(来自步骤3的粗产物,10g,19.5mmol,1.00当量)及MeOH(50mL)。在0-5℃下分批添加HCl(20mL,1N)。在室温下搅拌混合物3h。浓缩反应混合物,且通过使用以下条件的制备型HPLC纯化残余物:柱,C18-800g,移动相,CH3CN/H2O(0.05%FA),27min内自10%升高至70%,流动速率,180mL/min,检测器,254nm。用K2CO3固体将洗脱份的pH值调节至7-8且用二氯甲烷(3×300mL)萃取。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。冷冻干燥残余物,且由此产生5.3g(64%)呈白色固体的N-(叔丁基)-2-((2-(4-(2-羟基-2-甲基丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS:(ES,m/z):[M+H]+:428.3。1H NMR(300MHz,DMSO-d6):δ8.47(d,J=5.6Hz,1H),7.82(d,J=2.5Hz,1H),7.67(s,1H),7.04(dd,J=5.7,2.6Hz,1H),4.69(s,1H),4.14(s,2H),3.86(s,2H),3.26(s,3H),3.15(t,J=7.4Hz,2H),2.81(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.25-1.24(m,15H)。
实施例1.43B(用于制备化合物174的替代方法)
流程19B
向250mL三颈圆底烧瓶中添加N-(叔丁基)-2-((2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(7.2g,19.3mmol,1.00当量)及DMSO(80mL)。之后在室温下添加NaH(60%于矿物油中)(1.5g,38.6mmol,2.00当量)。搅拌混合物0.5h,且将2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇(6.7g,38.6mmol,2.00当量)添加至以上混合物中并在40℃下再搅拌3h。将反应混合物冷却至室温,用H2O(100mL)淬灭,且用乙酸乙酯(100mL×2)萃取。将合并的有机相用盐水(100mL×2)洗涤,经无水硫酸钠干燥,且过滤。减压浓缩滤液,且通过使用以下条件的制备型HPLC纯化残余物:C18-500g,CH3CN/H2O(NH4HCO3 0.1%),30min内自15%达至70%,流动速率,150mL/min,检测器,UV 254nm。由此产生7.0g(71%)呈棕色固体的N-(叔丁基)-2-(甲基(2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。LCMS(ES,m/z):[M+H]+:512。
向250mL三颈圆底烧瓶中添加N-(叔丁基)-2-(甲基(2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(7.0g,13.7mmol,1.00当量)及甲醇(70mL)、HCl(c)(5mL)。将混合物搅拌0.5h,用H2O(200mL)稀释,且用K2CO3固体将pH值调节至9。用二氯甲烷(300mL×2)萃取混合物,使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。将残余物5.8g(纯度:96.7%)于CH3CN(120mL)中进行湿磨,过滤,且获得5.5g(纯度98.8%)。在60℃下将粗产物溶解于CH3CN(110mL)中且随后在20min内冷却至20℃。通过过滤收集固体且在红外灯下干燥1h。由此产生3.1g(纯度99.94%,产率56.3%)呈白色固体的N-(叔丁基)-2-((2-(4-(2-羟基-2-甲基丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS:(ES,m/z):[M+H]+:428.1H-NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.4Hz,1H),7.83(d,J=2.7Hz,1H),7.67(s,1H),7.05(dd,J=5.7,2.7Hz,1H),4.69(s,1H),4.14(s,2H),3.86(s,2H),3.26(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.25(s,9H),1.24(s,6H)。
实施例1.44
合成2-[4-(氮杂环庚-1-基)-5H,6H,7H-环戊并[d]嘧啶-2-基]-N,N-二甲基吡啶-4-胺(化合物13)
用N,N-二甲基-2-(三丁基锡烷基)吡啶-4-胺替换(2-三丁基锡烷基)吡啶,与化合物92类似地合成化合物13。1H NMR(400MHz,DMSO-d6)δ8.19(d,J=7.2Hz,1H),7.75(d,J=3.1Hz,1H),7.05(dd,J=7.3,2.9Hz,1H),3.86(d,J=3.4Hz,1H),3.86-3.72(m,3H),3.26(s,6H),3.12(hept,J=7.3,6.7Hz,2H),3.00-2.80(m,J=8.0Hz,2H),2.04(h,J=8.2,7.8Hz,2H),1.73(dq,J=18.9,7.4,6.4Hz,4H),1.48(dq,J=7.4,4.6,3.7Hz,4H)。LCMS(ES+):(M+H)+=338.1。
实施例1.45
合成1-[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷(化合物14)
用4-甲基-2-(三丁基锡烷基)吡啶替换(2-三丁基锡烷基)吡啶,与化合物92类似地合成化合物14。1H NMR(400MHz,DMSO-d6)δ8.69(d,J=5.0Hz,1H),8.27(d,J=1.7Hz,1H),7.64-7.58(m,1H),3.97(s,4H),3.22-3.10(m,2H),3.03(t,J=7.9Hz,2H),2.51(s,3H),2.09(p,J=7.7Hz,2H),1.82(s,4H),1.54(s,4H)。LCMS(ES+):(M+H)+=309.2。
实施例1.46
合成N-(2-甲氧基苯基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物15)
流程20描绘用于制备例示性化合物的合成途径。
流程20
向2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酸(65.00mg;0.23mmol;1.00当量)于DMF(1.5mL)中的溶液中添加2-甲氧基苯胺(33.79mg;0.27mmol;1.20当量),之后添加休尼格氏碱(0.08mL;0.46mmol;2.00当量)及HATU(86.93mg;0.23mmol;1.00当量)。在室温下搅拌1h后,用水及乙腈稀释,且通过制备型HPLC对混合物进行纯化,得到N-(2-甲氧基苯基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(9mg)。1H NMR(400MHz,DMSO-d6)δ9.39(s,1H),8.66-8.59(m,1H),8.31-8.24(m,1H),7.92(d,J=8.0Hz,1H),7.78(td,J=7.7,1.8Hz,1H),7.40(ddd,J=7.5,4.7,1.2Hz,1H),7.07-6.95(m,2H),6.85(td,J=7.5,7.0,1.7Hz,1H),4.49(s,2H),3.68(s,3H),3.31(s,3H),3.18(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.00(dq,J=15.2,8.3,7.8Hz,2H)。LCMS(ES+):(M+H)+=390.3。
实施例1.47
合成N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[b]吡啶-4-基]氨基}乙酰胺(化合物16)
流程21描绘用于制备例示性化合物的合成途径。
流程21
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入2-[4-氯-5H,6H,7H-环戊并[b]吡啶-2-基]吡啶(100.00mg,0.43mmol,1.00当量)、N-叔丁基-2-(甲基氨基)乙酰胺(81.27mg,0.56mmol,1.30当量)、Pd(OAc)2(9.73mg,0.04mmol,0.10当量)、BINAP(53.98mg,0.08mmol,0.20当量)、Cs2CO3(282.46mg,0.86mmol,2.00当量)及二噁烷(6.00mL)。在100℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物(200mg):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及AcCN(11min内自30%相B达至60%);检测器,254nm。由此产生71.5mg(48.74%)呈灰白色固体的N-叔丁基-2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[b]吡啶-4-基]氨基]乙酰胺。1H-NMR(300MHz,DMSO-d6)δ8.62(dd,J=4.8,1.7Hz,2H),8.31(dt,J=8.0,1.2Hz,1H),7.86(td,J=7.7,1.9Hz,1H),7.57(s,1H),7.55(s,1H),7.37(ddd,J=7.5,4.7,1.2Hz,1H),3.94(s,2H),3.07(s,3H),3.03(t,J=7.2Hz,2H),2.86(t,J=7.7Hz,2H),2.05-1.95(m,2H),1.28(s,9H)。LCMS(ES,m/z):[M+H]+:339.2。
实施例1.48
合成N-叔丁基-2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物245)
流程22描绘用于制备例示性化合物的合成途径。
流程22
步骤1
向使用惰性氮气氛围吹扫及维持的500mL 3颈圆底烧瓶中放入氧杂环丁-3-醇(8.45g,114.04mmol,1.50当量)及THF(100.00mL)。之后在0℃下分数批添加NaH(60%于矿物油中)(6.84g,171.06mmol,1.50当量)。在0℃下搅拌混合物30min。在0℃下于搅拌下逐滴添加2-氯-4-氟吡啶(10.00g,76.02mmol,1.00当量)。添加后,在室温下搅拌所得溶液6h。再次将反应混合物冷却至0℃,通过添加30mL水小心地淬灭,用3×100mL乙酸乙酯萃取。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。通过含乙酸乙酯/石油醚(1:2)的硅胶柱纯化残余物。由此产生11g(78%)呈白色固体的2-氯-4-(氧杂环丁-3-基氧基)吡啶。LCMS(ES)[M+1]+m/z:186。
步骤2
向使用惰性氮气氛围吹扫及维持的100mL 3颈圆底烧瓶中放入2-氯-4-(氧杂环丁-3-基氧基)吡啶(2.00g,10.81mmol,1.00当量)、甲苯(60.00mL)、Sn2Me6(3.71g,11.31mmol,1.05当量)、Pd(PPh3)4(1.25g,1.08mmol,0.10当量)。于油浴中在100℃下搅拌混合物4h。将反应混合物冷却至室温且不经纯化即用于下一步骤中。重复此反应三次。LCMS(ES)[M+1]+m/z:316。
步骤3
向使用惰性氮气氛围吹扫及维持的步骤3的反应溶液中添加N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(2.23g,7.54mmol,0.70当量)及Pd(PPh3)4(1.24g,1.07mmol,0.10当量)。在油浴中在100℃下搅拌所得溶液12h。重复此并行反应三次。将反应混合物冷却且浓缩以移除溶剂。通过含乙酸乙酯/石油醚(10%至100%)的硅胶柱纯化残余物。由此产生7.2g粗化合物,其通过使用如下条件的制备型HPLC进一步纯化:柱,C18-800g,移动相,CH3CN/H2O(0.05%FA),27min内自10%升高至70%,流动速率,180mL/min,检测器,254nm。用K2CO3固体将洗脱份的pH值调节至7-8,用二氯甲烷(3×300mL)萃取。使合并的有机相经无水硫酸钠干燥且过滤。减压浓缩滤液。将于二氯甲烷/己烷(1:10,30mL)中进行湿磨,过滤且冷冻干燥固体,得到5.2g(56%)呈白色固体的N-叔丁基-2-[甲基([2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基])氨基]乙酰胺。LCMS:(ES,m/z):[M+H]+:412.1H-NMR:(300MHz,DMSO-d6,ppm):δ8.49(d,J=5.4Hz,1H),7.77(d,J=2.4Hz,1H),7.70(s,1H),6.87(dd,J=5.7,2.4Hz,1H),5.52-5.45(m,1H),4.99(t,J=6.6Hz,2H),4.58(dd,J=7.2,4.8Hz,2H),4.13(s,2H),3.29(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.05-1.94(m,2H),1.26(s,9H)。
实施例1.49
合成N-环己基-1-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}环丙烷-1-甲酰胺(化合物17)
流程23描绘用于制备例示性化合物的合成途径。
流程23
步骤1
向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(500.00mg;2.64mmol;1.00当量)于AcCN(5mL)中的溶液中添加DIPEA(1.15mL;6.61mmol;2.50当量)及1-氨基环丙烷-1-甲酸乙酯(409.93mg;3.17mmol;1.20当量)。在60℃下加热混合物24h,且在80℃下再加热4天(HPLC显示转化率为约50%)。停止反应且浓缩混合物,通过柱色谱(己烷/EtOAc=1:1)纯化所得粗残余物,得到1-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)环丙烷-1-甲酸乙酯(135mg)。LCMS(ES+):(M+H)+=282.0,284.1。
步骤2
在0℃下向1-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)环丙烷-1-甲酸乙酯(135.00mg;0.48mmol;1.00当量)于DMF(2mL)中的溶液中添加氢化钠(57.49mg;1.44mmol;3.00当量)。搅拌10min后,向混合物添加碘甲烷(0.04mL;0.72mmol;1.50当量),且在环境温度下进一步搅拌溶液直至完成。用饱和NaHCO3及EtOAc稀释混合物,分离有机层,且用EtOAc(2×)进一步萃取水层。将合并的有机层用盐水洗涤,干燥,且浓缩,得到1-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)环丙烷-1-甲酸乙酯(66mg),其不经进一步纯化即用于下一步骤中。LCMS(ES+):(M+H)+=296.1,298.4。
步骤3
向1-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)环丙烷-1-甲酸乙酯(66.00mg;0.22mmol;1.00当量)于THF(1mL)中的溶液中添加MeOH(0.5mL)及水(0.5mL),之后添加单水合氢氧化锂(18.73mg;0.45mmol;2.00当量)。将混合物在室温下搅拌2h,且加热至60℃并再搅拌2h。将混合物冷却且真空浓缩,用1N HCl将残余物酸化至pH=3,冷冻干燥水层,得到1-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)环丙烷-1-甲酸,其不经纯化即用于下一步骤中。LCMS(ES+):(M+H)+=268.1,270.2。
步骤4
向1-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)环丙烷-1-甲酸(100.00mg;0.37mmol;1.00当量)及环己胺(0.05mL;0.45mmol;1.20当量)于DMF(1mL)中的溶液中添加DIPEA(0.13mL;0.75mmol;2.00当量)及HATU(142.03mg;0.37mmol;1.00当量)。在室温下搅拌1h后,用水稀释混合物且通过过滤收集沉淀物,并真空干燥,得到1-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-环己基环丙烷-1-甲酰胺(73mg)。LCMS(ES+):(M+H)+=268.1,270.2。
步骤5
向1-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-环己基环丙烷-1-甲酰胺(70.00mg;0.20mmol;1.00当量)及2-(三丁基锡烷基)吡啶(110.80mg;0.30mmol;1.50当量)于甲苯(1mL)中的溶液中添加四(三苯基膦)钯(23.19mg;0.02mmol;0.10当量)。用N2使溶液脱气且在105℃下加热15h。将混合物冷却且浓缩,且通过制备型HPLC对残余物进行纯化,得到N-环己基-1-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}环丙烷-1-甲酰胺(23mg)。1H NMR(400MHz,DMSO-d6)δ8.69-8.62(m,1H),8.27(d,J=7.9Hz,1H),7.88(td,J=7.7,1.8Hz,2H),7.58(ddd,J=18.1,10.7,6.9Hz,1H),7.42(ddd,J=7.5,4.7,1.2Hz,1H),3.62(s,1H),3.13(s,3H),2.93-2.81(m,1H),2.76(s,2H),2.02(s,1H),1.84(s,1H),1.64(m,4H),1.56(t,J=14.5Hz,2H),1.33(dd,J=24.0,10.8Hz,2H),1.19(m,4H),1.02(m,2H)。LCMS(ES+):(M+H)+=392.2。
实施例1.50
合成N-叔丁基-2-甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物19)
流程24描绘用于制备例示性化合物的合成途径。
流程24
步骤1
向小瓶中添加2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(150.00mg;0.79mmol;1.00当量)、乙腈(3ml)、氯化1-乙氧基-2-甲基-1-氧代丙-2-铵(159.62mg;0.95mmol;1.20当量)及休尼格氏碱(0.58mL;3.33mmol;4.20当量)。在60℃下于加热块中搅拌15h后,蒸发混合物且对残余物进行柱色谱,用(0至50%EtOAc/己烷)洗脱,得到2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)-2-甲基丙酸乙酯(88mg)。LCMS(ES+):(M+H)+=283.9。
步骤2
向圆底烧瓶中添加含2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)-2-甲基丙酸乙酯(88.00mg;0.31mmol;1.00当量)的1,4-二噁烷(无水,约2ml)。用Ar吹扫混合物。向混合物中添加2-(三丁基锡烷基)吡啶(0.20mL;0.62mmol;2.00当量)及四(三苯基膦)钯(35.84mg;0.03mmol;0.10当量)。在108℃下于加热块中搅拌15h后,将混合物冷却且浓缩,且通过柱色谱(0-5%MeOH/DCM)纯化残余物,得到2-甲基-2-{[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙酸乙酯。LCMS(ES+):(M+H)+=327.0。
步骤3
将2-甲基-2-{[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙酸乙酯(67mg;0.21mmol;1当量)溶解于四氢呋喃(2ml)及甲醇(0.5ml)中。逐滴添加溶解于水(约0.8ml)中的氢氧化锂(无水,25mg;1.03mmol;5当量)且在25℃下搅拌。4.5h后,将反应物用6M HCl小心地酸化至pH<3且蒸发至干燥。使残余物2-甲基-2-{[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙酸盐酸盐与甲苯共蒸发且高真空干燥。将此物质溶解于N,N-二甲基甲酰胺(3ml)中且于冰浴中冷却。添加碘甲烷(39μL;0.62mmol;3当量)及碳酸钾(142mg;1.03mmol;5当量),且在60℃下搅拌混合物。7h后,添加其他部分的碘甲烷及碳酸钾若干次,以驱动反应得到产物。将反应物溶解于乙酸乙酯(50ml)及水(25ml)中,分离各相,且用乙酸乙酯(50ml)萃取水相。将经合并的有机物用水(10ml)及氯化钠溶液(10ml)洗涤。将合并的水相用1:3异丙醇:氯仿(6×20ml)萃取,与有机物合并,且经硫酸钠干燥。通过反相色谱(Waters XSelect CSH C18柱,0-80%乙腈/0.1%甲酸水溶液梯度)纯化浓缩残余物,得到呈黄色固体的2-甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙酸甲酯(10mg,15%)。LCMS(ES+):(M+H)+=327.0。
步骤4
将2-甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙酸甲酯(10mg;30.64μmol;1当量)溶解于四氢呋喃(0.5ml)及甲醇(0.2ml)中。逐滴添加溶解于水(约0.2ml)中的氢氧化锂(无水,3.67mg;0.15mmol;5当量)且在25℃下搅拌混合物2h。随后将反应物用6M HCl小心地酸化至pH<3且蒸发至干燥。使残余物与甲苯共蒸发且高真空干燥。将残余物氯化2-{4-[(1-羧基-1-甲基乙基)(甲基)氨基]-5H,6H,7H-环戊并[d]嘧啶-2-基}吡啶-1-鎓(10.7mg;0.03mmol;1当量)溶解于N,N-二甲基甲酰胺(1.5ml)中。添加N,N-二异丙基乙胺(19μL;0.11mmol;3.5当量)及3-氧化六氟磷酸1-[双(二甲基氨基)亚甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓(HATU,23mg;0.06mmol;2当量),之后添加叔丁胺(6μL;0.05mmol;1.5当量)。15h后,添加其他部分的叔丁胺、HATU及N,N-二异丙基乙胺,以驱动反应完成。将反应物分配于水(5ml)、乙酸乙酯(50ml)及碳酸氢钠溶液(10ml)中。分离各相且用乙酸乙酯(50ml)及1:3异丙醇:氯仿(50ml)萃取水相。使合并的有机相经硫酸钠干燥,蒸发,且通过反相色谱(Waters XSelect CSH C18柱,0-90%乙腈/0.1%甲酸水溶液梯度)纯化,得到呈棕色固体的N-叔丁基-2-甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙烯酰胺(6mg,50%)。LCMS(ES+):(M+H)+=368.1。1H NMR(400MHz,氯仿-d)δ8.77-8.67(m,1H),8.52-8.43(m,2H),8.11-8.00(m,1H),7.74-7.65(m,1H),6.79-6.71(m,1H),4.73(s,3H),3.00-2.91(m,4H),2.21-2.12(m,2H),1.62(s,6H),1.18(s,9H)。
实施例1.51
合成N-叔丁基-2-{苯基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物20)
流程25描绘用于制备例示性化合物的合成途径。
流程25
步骤1
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(200mg;1.06mmol;1当量)溶解于乙腈(9.5ml)中。添加苯胺(0.12mL;1.27mmol;1.2当量)及N,N-二异丙基乙胺(0.55mL;3.17mmol;3当量)。密封反应物且在微波反应器中在120℃下加热1h。另外添加苯胺(1.2当量)及N,N-二异丙胺(1.5当量)且在100℃下继续加热4h,随后在90℃下于加热块中加热10h。随后将反应物浓缩至体积约2ml,添加更多N,N-二异丙基乙胺(0.75ml),且在90℃下继续加热4天。将反应物蒸发且通过硅胶色谱(乙酸乙酯/己烷梯度)纯化,得到呈淡黄色薄膜的2-氯-N-苯基-5H,6H,7H-环戊并[d]嘧啶-4-胺(194mg,74%)。LCMS(ES+):(M+H)+=245.9。
步骤2
将2-氯-N-苯基-5H,6H,7H-环戊并[d]嘧啶-4-胺(60mg;0.24mmol;1当量)溶解于N,N-二甲基甲酰胺(1ml)中。添加碳酸钾(67mg;0.49mmol;2当量),且在50℃下于加热块中搅拌混合物2h。将反应混合物冷却至20℃,且添加含2-溴-N-叔丁基丙酰胺(76mg;0.37mmol;1.5当量)的N,N-二甲基甲酰胺(1ml),且在80℃下搅拌反应物24h。添加附加量的溴酰胺(38mg)及碳酸钾(33mg),且再加热反应物24h。将反应混合物溶解于乙酸乙酯(50ml)、水(10ml)及碳酸氢钠溶液(10ml)中。分离各相,且用乙酸乙酯(50ml)萃取水相。将合并的有机物用水(10ml)及氯化钠溶液(10ml)洗涤,经无水硫酸钠干燥,且蒸发。通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈白色固体的N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(苯基)氨基)丙烯酰胺(48mg,52%)。LCMS(ES+):(M+H)+=372.9。
步骤3
将N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(苯基)氨基)丙酰胺(48mg;0.13mmol;1当量)悬浮于1,4-二噁烷(2ml)中。用Ar气体吹扫混合物。添加2-(三丁基锡烷基)吡啶(0.08mL;0.26mmol;2当量)及四(三苯基膦)钯(15mg;0.01mmol;0.1当量),且在108℃下于加热块中搅拌混合物18h。添加附加量的锡试剂(0.08ml)及钯催化剂(15mg)且继续加热14h。将反应物蒸发,过滤,且通过反相色谱(Waters XSelect CSH C18柱,5-80%乙腈/0.1%甲酸水溶液梯度)纯化,得到呈白色固体的N-叔丁基-2-{苯基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙烯酰胺(19mg,35%)。LCMS(ES+):(M+H)+=415.8。1H NMR(400MHz,氯仿-d)δ8.82(d,J=4.8Hz,1H),8.49(d,J=8.0Hz,1H),7.92-7.83(m,1H),7.43-7.33(m,4H),7.33-7.26(m,2H),7.26-7.21(m,1H),5.44(s,1H),2.92(t,J=7.8Hz,2H),1.99-1.92(m,1H),1.80-1.63(m,3H),1.33(d,J=7.1Hz,3H),1.19(s,9H)。
实施例1.52
合成2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(喹啉-7-基)乙酰胺(化合物21)
流程26描绘用于制备例示性化合物的合成途径。
流程26
向100mL圆底烧瓶中放入N-甲基-N-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸(250mg,0.879mmol,1.00当量)、喹啉-7-胺(190.16mg,1.319mmol,1.5当量)、HATU(501.50mg,1.319mmol,1.50当量)、DIEA(227.29mg,1.759mmol,2当量)、DCM(10.00mL)。在室温下搅拌所得溶液4hr。用3×20mL二氯甲烷萃取所得溶液,且将有机层合并,且经无水硫酸钠干燥并真空浓缩。通过使用以下条件的制备型HPLC(2#SHIMADZU(HPLC-01))纯化粗产物:柱,Atlantis HILIC OBD柱,19*150mm*5um;移动相,水(0.05%NH3H2O)及ACN(14min内自25%相B达至42%)。由此产生137.7mg(38.2%)呈灰白色固体的2-(甲基(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)-N-(喹啉-7-基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ10.61(s,1H),8.86-8.80(m,1H),8.67-8.60(m,1H),8.39(s,1H),8.32-8.22(m,2H),7.92(d,J=8.8Hz,1H),7.83-7.66(m,2H),7.39(td,J=7.6,4.5Hz,2H),4.52(s,2H),3.42(s,3H),3.24(t,J=7.3Hz,2H),2.85(t,J=7.8Hz,2H),2.02(p,J=7.7Hz,2H)。LCMS(ES)[M+1]+m/z:411.2。
实施例1.53
合成N-(2-氟苯基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物22)
流程27描绘用于制备例示性化合物的合成途径。
流程27
向50mL圆底烧瓶中放入2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺(中间体I,100.00mg,0.353mmol,1.00当量)、二甲基甲酰胺(8mL)、2-氟苯胺(39.22mg,0.353mmol,1.00当量)、HATU(201.30mg,0.529mmol,1.50当量)及DIEA(136.84mg,1.059mmol,3.00当量)。在25℃下搅拌所得溶液2hr。将粗反应混合物过滤且进行反相制备型HPLC(Prep-C18,20-45M,120g,Tianjin Bonna-Agela Technologies;经10min时段自30%MeCN/水至40%MeCN/水的梯度洗脱,水含有0.1%FA),得到呈棕色固体的N-(2-氟苯基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(45.7mg,34.31%)。1H NMR(300MHz,DMSO-d6)δ10.05(s,1H),8.63(d,J=4.4Hz,1H),8.29(d,J=7.8Hz,1H),7.89-7.64(m,2H),7.47-7.34(m,1H),7.32-7.20(m,1H),7.14(dt,J=6.4,3.2Hz,2H),4.50(s,2H),3.36-3.32(m,3H),3.21(t,J=7.4Hz,2H),2.84(t,J=7.8Hz,2H),2.01(p,J=7.6Hz,2H)。LCMS(ES)[M+1]+m/z 378.2。
实施例1.54
合成N-叔丁基-2-{甲基[2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉-4-基]氨基}乙酰胺(化合物23)
流程28描绘用于制备例示性化合物的合成途径。
流程28
步骤1
向50mL圆底烧瓶中放入2,4-二氯-5,6,7,8-四氢喹唑啉(300mg,1.477mmol,1.00当量)、MeOH(10.00mL)、N-叔丁基-2-(甲基氨基)乙酰胺(319mg,2.21mmol,1.50当量)及DIEA(286mg,2.21mmol,1.50当量)的混合物。在室温下搅拌所得溶液16小时。浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1/3)的硅胶柱上。由此产生260mg(56.62%)呈白色固体的N-叔丁基-2-[(2-氯-5,6,7,8-四氢喹唑啉-4-基)(甲基)氨基]乙酰胺。LCMS(ES)[M+1]+m/z:311。
步骤2
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入N-叔丁基-2-[(2-氯-5,6,7,8-四氢喹唑啉-4-基)(甲基)氨基]乙酰胺(200mg,0.643mmol,1.00当量)、二噁烷(15.0mL)、2-(三丁基锡烷基)吡啶(473mg,1.28mmol,2.00当量)及Pd(PPh3)4(223mg,0.193mmol,0.30当量)的混合物。在110℃下搅拌所得溶液16小时。将粗反应混合物过滤且进行反相制备型MPLC(Prep-C18,20-45mM,120g,Tianjin Bonna-Agela Technologies;经12min时段自5%MeCN/水达至26%MeCN/水的梯度洗脱,其中两种溶剂皆含有0.1%甲酸)。由此产生127.1mg(55.88%)呈灰白色固体的N-叔丁基-2-[甲基[2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉-4-基]氨基]乙酰胺。1H NMR(300MHz,DMSO-d6,ppm):δ8.70(d,J=4.3Hz,1H),8.37(d,J=7.9Hz,1H),7.93(td,J=7.7,1.8Hz,1H),7.77(s,1H),7.52-7.47(m,1H),4.04(s,2H),3.21(s,3H),2.83-2.79(m,2H),2.73-2.70(m,2H),1.82-1.80(m,2H),1.69-1.67(m,2H),1.23(s,9H)。LCMS(ES)[M+1]+m/z:354.2。
实施例1.55
合成N-叔丁基-2-{甲基[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物24)
流程29描绘用于制备例示性化合物的合成途径。
流程29
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(中间体II,0.30g,1.01mmol,1.00当量)、二噁烷(15mL)、Pd(dppf)Cl2.CH2Cl2(0.22g,0.30mmol,0.30当量)及4-甲基-2-(三丁基锡烷基)-吡啶(0.58g,1.52mmol,1.50当量)。将所得溶液在110℃下搅拌过夜。浓缩所得混合物。通过使用以下条件的急骤制备型HPLC(IntelFlash-1)纯化粗产物:柱,C18硅胶;移动相,相A:水(0.05%FA),相B CH3CN(0-30%,6min);检测器,220及254nm。由此产生0.1g粗产物。通过使用以下条件的制备型HPLC进一步纯化粗产物(0.1g):柱,X-Bridge C18 OBD,5um,19*150mm;移动相,相A:水(0.05%NH4OH),相B CH3CN(8min内自25%B达至45%);检测器,220nm;流动速率20mL/min。由此产生88.9mg(24.88%)呈灰白色固体的(N-叔丁基)-2-(甲基(2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。1H-NMR:(300MHz,DMSO-d6,ppm):δ8.50(d,J=4.9Hz,1H),8.16(s,1H),7.71(s,1H),7.26(d,J=4.2Hz,1H),4.14(s,2H),3.27(s,3H),3.14(t,J=7.2Hz,2H),2.81(t,J=7.8Hz,2H),2.41(s,3H),2.0-1.99(m,2H),1.23(s,9H)。LCMS:(ES,m/z):[M+H]+:354.2。
实施例1.56
合成2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(1-甲基环己基)乙酰胺(化合物25)
流程30描绘用于制备例示性化合物的合成途径。
流程30
向8mL小瓶中放入[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(中间体I,150mg,0.53mmol,1.0当量)、DMF(3.0mL)、1-甲基环己胺(66mg,0.58mmol,1.1当量)及DIPEA(341mg,2.64mmol,5.0当量)。之后在0℃下添加HATU(301mg,0.79mmol,1.5当量)。在室温下搅拌混合物1h。过滤混合物,且通过使用以下条件的制备型HPLC纯化滤液:120g C18柱,CH3CN/H2O(0.05%NH4OH),5%至80%,15min,流动速率,70mL/min,检测器,254nm。获得101.6mg(51%)呈淡黄色固体的2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]-N-(1-甲基环己基)乙酰胺。1H-NMR(300MHz,DMSO-d6,ppm):δ8.66(dd,J=4.7,1.8Hz,1H),8.34(dt,J=8.0,1.1Hz,1H),7.86(td,J=7.7,1.8Hz,1H),7.43(ddd,J=7.5,4.7,1.2Hz,1H),7.37(s,1H),4.20(s,2H),3.28(s,3H),3.16(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.02-1.96(m,4H),1.33-1.24(m,8H),1.19(s,3H)。LCMS:(ES,m/z):[M+H]+:380.3。
实施例1.57
合成2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(氧杂环己-3-基)乙酰胺(化合物26)
流程31描绘用于制备例示性化合物的合成途径。
流程31
向8mL小瓶中放入[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(中间体I,150mg,0.53mmol,1.0当量)、DMF(3.0mL)、氧杂环己-3-胺盐酸盐(80mg,0.58mmol,1.1当量)及DIEA(341mg,2.64mmol,5.0当量)。之后在0℃下添加HATU(301mg,0.79mmol,1.5当量)。在室温下搅拌混合物1h,过滤,且通过使用如下条件的制备型HPLC纯化滤液:C18-120g柱,CH3CN/H2O(0.05%NH4OH),5%至80%,15min,流动速率,70mL/min,检测器,254nm。得到108.5mg(56%)呈灰白色固体的2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]-N-(氧杂环己-3-基)乙酰胺。1H-NMR:(300MHz,DMSO-d6,ppm):δ8.67(d,J=4.2Hz,1H),8.29(d,J=7.8Hz,1H),8.09(d,J=7.5Hz,1H),7.90-7.85(m,1H),7.46-7.42(m,1H),4.20(s,2H),3.71-3.63(m,3H),3.33-3.29(m,1H),3.26(s,3H)3.15-3.05(m,3H),2.82(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.79-1.71(m,1H),1.64-1.55(m,1H),1.49-1.43(m,2H)。LCMS:(ES,m/z):[M+H]+:368.2。
实施例1.58
合成N-苯甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物27)
流程32描绘用于制备例示性化合物的合成途径。
流程32
向8mL小瓶中放入[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(200mg,0.70mmol,1.0当量)、DMF(3.00mL)、苯甲胺(83mg,0.77mmol,1.1当量)及DIEA(455mg,3.52mmol,5.0当量)。之后在0℃下添加HATU(321mg,0.84mmol,1.2当量)。在室温下搅拌反应溶液1h,过滤,且通过使用如下条件的制备型HPLC纯化滤液:C18-120g柱,CH3CN/H2O(0.05%NH4OH),5%至80%,15min,流动速率,70mL/min,检测器,254nm。得到101.6mg(39%)呈灰白色固体的N-苯甲基-2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1H-NMR(300MHz,DMSO-d6,ppm):δ8.64(d,J=5.4Hz2H),8.26(d,J=7.8Hz,1H),7.83(td,J=7.7,1.9Hz,1H),7.43(dd,J=7.5,4.9Hz,1H),7.22-7.10(m,5H),4.31(s,2H),4.30(s,2H),3.32(s,3H),3.17(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.03-1.93(m,2H)。LCMS:(ES,m/z):[M+H]+:374.2
实施例1.59
合成N-叔丁基-2-{[2-(5-羟基吡嗪-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物28)
流程33描绘用于制备例示性化合物的合成途径。
流程33
向50mL圆底烧瓶中放入N-(叔丁基)-2-((2-(5-甲氧基吡嗪-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(120mg,0.324mmol,1.00当量)、DCM(20.0mL)及AlCl3(431mg,3.23mmol,10.00当量)的混合物。在室温下搅拌所得溶液24小时。随后通过添加100mL水/冰来淬灭反应物。用3×50mL二氯甲烷萃取所得溶液。将有机层分离,经无水硫酸镁干燥,且浓缩。通过使用以下条件的制备型HPLC纯化粗产物:柱,XBridge Prep C18OBD柱,19×150mm,5um;移动相,相A:H2O(0.05%NH3H2O);相B:CH3CN(8min内自10%CH3CN达至30%CH3CN)。由此产生57.2mg(49.54%)呈白色固体的N-(叔丁基)-2-((2-(5-羟基吡嗪-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6,ppm):δ12.63(br,1H),8.26(br,1H),8.05(d,J=1.3Hz 1H),7.61(s,1H),4.08(s,2H),3.3(s,3H),3.10(t,J=7.3Hz,2H),2.76(t,J=7.8Hz,2H),2.05-1.93(m,2H),1.24(s,9H)。LCMS(ES)[M+1]+m/z:357.2。
实施例1.60
合成N-环己基-1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环丁烷-3-甲酰胺(化合物29)
流程34描绘用于制备例示性化合物的合成途径。
流程34
步骤1
在室温下向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(300.00mg;1.59mmol;1.00当量)及1-氯氮杂环丁烷-3-甲酸甲酯HCl盐(300.71mg;1.98mmol;1.25当量)于AcCN(4mL)中的溶液中添加三乙胺(0.44mL;3.17mmol;2.00当量)。在室温下搅拌反应混合物30min且在75℃下搅拌3h。将所得混合物冷却且用水及EtOAc稀释。收集且浓缩有机层,且通过柱色谱(己烷/EtOAc=30:70)纯化所得残余物,得到1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氮杂环丁烷-3-甲酸甲酯(390mg)。LCMS(ES+):(M+H)+=268.1,270.1。
步骤2
向1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氮杂环丁烷-3-甲酸甲酯(390.00mg;1.46mmol;1.00当量)于THF(2mL)中的溶液中添加MeOH(1mL)及水(1mL),之后添加单水合氢氧化锂(122.26mg;2.91mmol;2.00当量)。将混合物搅拌2h且浓缩,且用1N HCl将残余物酸化至pH=3。通过过滤收集所得沉淀物,得到1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氮杂环丁烷-3-甲酸(339mg)。LCMS(ES+):(M+H)+=254.0,256.2。
步骤3
向1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氮杂环丁烷-3-甲酸(156.00mg;0.61mmol;1.00当量)及环己胺(0.11mL;0.92mmol;1.50当量)于DMF(2mL)中的溶液中添加DIPEA(0.27mL;1.54mmol;2.50当量)及HATU(257.20mg;0.68mmol;1.10当量)。搅拌反应物直至完成,且将混合物倒至饱和NaHCO3及水上方。通过过滤收集所得沉淀物,得到1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}-N-环己基氮杂环丁烷-3-甲酰胺(198mg)。LCMS(ES+):(M+H)+=335.0,337.1。
步骤4
向1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}-N-环己基氮杂环丁烷-3-甲酰胺(100.00mg;0.30mmol;1.00当量)于DMF(2mL)中的悬浮液中添加2-(三丁基锡烷基)吡啶(164.92mg;0.45mmol;1.50当量)及四(三苯基膦)钯(34.51mg;0.03mmol;0.10当量)。在115℃下加热混合物15h,将混合物冷却且用水及AcCN稀释,滤出不可溶物质,且通过制备型HPLC纯化滤液,得到N-环己基-1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环丁烷-3-甲酰胺(63mg)。1H NMR(400MHz,DMSO-d6)δ8.66(ddd,J=4.8,1.8,0.9Hz,1H),8.25(dt,J=7.9,1.2Hz,1H),7.89(td,J=7.7,1.8Hz,2H),7.45(ddd,J=7.6,4.7,1.2Hz,1H),4.33(t,J=8.6Hz,2H),4.24(t,J=7.4Hz,2H),3.58-3.50(m,1H),3.48-3.39(m,1H),2.93(t,J=7.4Hz,2H),2.81(t,J=7.8Hz,2H),2.01(p,J=7.7Hz,2H),1.77-1.62(m,4H),1.53(d,J=12.3Hz,1H),1.32-1.03(m,5H)。LCMS(ES+):(M+H)+=378.3。
实施例1.61
合成N-环己基-1-[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环丁烷-3-甲酰胺(化合物30)
用4-甲基-2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)吡啶,与化合物29类似地合成化合物30。1H NMR(400MHz,DMSO-d6)δ8.51-8.46(m,1H),8.06(dd,J=1.8,0.9Hz,1H),7.88(d,J=7.8Hz,1H),7.27-7.21(m,1H),4.29(t,J=8.5Hz,2H),4.21(t,J=7.3Hz,2H),3.60-3.48(m,1H),3.48-3.38(m,1H),2.92(t,J=7.4Hz,2H),2.78(t,J=7.8Hz,2H),2.37(s,3H),1.99(p,J=7.7Hz,2H),1.77-1.73(m,2H),1.66(dt,J=12.6,3.7Hz,2H),1.53(d,J=12.8Hz,1H),1.33-1.18(m,2H),1.22-1.03(m,3H)。LCMS(ES+):(M+H)+=392.4。
实施例1.62
合成N-(1-甲基-2-氧代吡咯烷-3-基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物31)
用3-氨基-1-甲基吡咯烷-2-酮替换4-甲氧基苯胺,与化合物75类似地合成化合物31。LCMS(ES+):(M+H)+=381.3。1H NMR(400MHz,乙腈-d3)δ8.60-8.55(m,1H),8.37(d,J=8.0Hz,1H),8.02(d,J=8.3Hz,1H),7.90-7.84(m,1H),7.40(ddd,J=7.6,4.8,1.2Hz,1H),4.43(q,J=9.0Hz,1H),4.31-4.10(m,2H),3.34(s,3H),3.23-3.14(m,4H),2.89-2.85(m,2H),2.74(s,3H),2.28(dddd,J=12.5,9.0,6.9,2.2Hz,1H),2.10-1.99(m,2H),1.79-1.67(m,1H)。
实施例1.63
合成N-(2,2-二氟-2H-1,3-苯并间二氧杂环戊烯-5-基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物32)
用2,2-二氟-1,3-苯并间二氧杂环戊烯-5-胺替换4-甲氧基苯胺,与化合物75类似地合成化合物32。LCMS(ES+):(M+H)+=440.3。1H NMR(400MHz,乙腈-d3)δ9.91(s,1H),8.68(d,J=4.7Hz,1H),8.39(d,J=8.0Hz,1H),7.92-7.84(m,1H),7.69(d,J=2.1Hz,1H),7.46(dd,J=7.6,4.9Hz,1H),7.24(dd,J=8.7,2.1Hz,1H),7.07(d,J=8.7Hz,1H),4.35(s,2H),3.43(s,3H),3.28-3.22(m,2H),2.96-2.90(m,2H),2.11-2.06(m,2H)。
实施例1.64
合成N-叔丁基-2-{[2-(嘧啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物33)
流程35描绘用于制备例示性化合物的合成途径。
流程35
步骤1
向500mL圆底烧瓶中放入嘧啶-2-甲脒盐酸盐(10.0g,63.0mmol,1.00当量)、MeOH(200mL)、2-氧代环戊烷-1-甲酸乙酯(14.7g,94.5mmol,1.50当量)及NaOMe(6.81g,126mmol,2.00当量)的混合物。在60℃下搅拌所得溶液16小时。浓缩所得混合物。随后通过添加200mL水淬灭反应物。用HCl(2mol/L)将溶液的pH值调节至3。用3×150mL二氯甲烷萃取所得溶液,将有机层分离及合并,经无水硫酸钠干燥,且浓缩。由此产生1.1g(8.14%)呈灰白色油状物的2-(嘧啶-2-基)-3,5,6,7-四氢-4H-环戊并[d]嘧啶-4-酮。LCMS(ES)[M+1]+m/z:215。
步骤2
向20mL小瓶中放入2-(嘧啶-2-基)-3,5,6,7-四氢-4H-环戊并[d]嘧啶-4-酮(1.00g,4.66mmol,1.00当量)及氧氯化磷(10mL)。在100℃下搅拌所得溶液4小时。浓缩所得混合物。随后通过添加50mL水淬灭反应物。用饱和碳酸钠溶液将溶液的pH值调节至9。用3×50mL二氯甲烷萃取所得溶液,将有机层分离且在烘箱中减压干燥。由此产生560mg(51.56%)呈黑色油状物的4-氯-2-(嘧啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶。LCMS(ES)[M+1]+m/z:233。
步骤3
向40mL小瓶中放入4-氯-2-(嘧啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶(500mg,2.14mmol,1.00当量)、MeOH(10.0mL)、2-氨基-N-叔丁基乙酰胺(419mg,3.22mmol,1.50当量)及DIEA(416mg,3.22mmol,1.50当量)。在80℃下搅拌所得溶液16小时。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物:柱,SunFire Prep C18 OBD柱,19×150mm,5um;移动相,相A:H2O(0.1%FA);相B:CH3CN(10min内自5%CH3CN达至35%CH3CN)。由此产生111mg(15.82%)N-(叔丁基)-2-((2-(嘧啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6,ppm):δ8.91(d,J=4.9Hz,2H),7.63(s,1H),7.56(t,J=4.9Hz,1H),7.08(t,J=5.8Hz,1H),3.97(d,J=5.8Hz,2H),2.84(t,J=7.7Hz,2H),2.76(t,J=7.4Hz,2H),2.10-2.05(m,2H),1.22(s,9H)。LCMS(ES)[M+1]+m/z:327.2。
实施例1.65
合成N-叔丁基-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物34)
流程36描绘用于制备例示性化合物的合成途径。
流程36
步骤1
向在惰性氩气氛围中吹扫及维持的100mL 3颈圆底烧瓶中放入2-氯-4-甲氧基吡啶(500mg,3.48mmol,1.00当量)、六甲基二锡烷(1.48g,4.527mmol,1.3当量)、二噁烷(20mL)及Pd(PPh3)4(804mg,0.69mmol,0.2当量)。于油浴中在110℃下搅拌所得溶液16h。滤出固体。浓缩滤液,得到950mg 4-甲氧基-2-(三甲基锡烷基)吡啶。粗产物不经进一步纯化即用于下一步骤中。LCMS(ES)[M+1]+m/z:274.02。
步骤2
向在惰性氩气氛围中吹扫及维持的100mL 3颈圆底烧瓶中放入4-甲氧基-2-(三甲基锡烷基)吡啶(947mg,3.48mmol,1.00当量)、N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(中间体II,310mg,1.04mmol,0.3当量)、Pd(dppf)Cl2(254mg,0.35mmol,0.1当量)及二噁烷(15mL)。在100℃下搅拌所得溶液16hr。真空浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:50至3:1)的硅胶柱上。通过急骤制备型HPLC纯化粗产物(160mg)。由此产生50mg(3.9%)呈白色固体的N-叔丁基-2-[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.49(d,J=5.4Hz,1H),7.86(d,J=2.4Hz,1H),7.69(s,1H),7.06(dd,J=5.7,2.4Hz,1H),4.14(s,2H),3.92(s,3H),3.27(s,3H),3.14(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),1.99(t,J=7.5Hz,2H),1.23(s,9H)。LCMS(ES)[M+1]+m/z:370.2。
实施例1.66
合成N-叔丁基-2-({2-[4-(甲氧基甲基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物35)
流程37描绘用于制备例示性化合物的合成途径。
流程37
步骤1
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入(2-氯吡啶-4-基)甲醇(5.00g,34.826mmol,1.00当量)、THF(20mL)。在0℃下搅拌所得溶液40min,且添加NaH(1.25g,52.088mmol,1.50当量)。在室温下再对所得溶液进行搅拌4hr。通过添加水淬灭反应物。用乙酸乙酯(3×30mL)萃取所得混合物,将有机层合并,经无水硫酸钠干燥且真空浓缩。通过含乙酸乙酯/石油醚(1:4)的硅胶柱色谱纯化残余物。由此产生3.1g(56.5%)呈淡黄色固体的2-氯-4-(甲氧基甲基)吡啶。LCMS(ES)[M+1]+m/z:158。
步骤2
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入2-氯-4-(甲氧基甲基)吡啶(1.00g,6.345mmol,1.00当量)、六甲基二锡烷(2.49g,7.600mmol,1.20当量)、Pd(dppf)Cl2(0.93g,0.001mmol,0.2当量)及二噁烷(20.00mL)。在100℃下搅拌所得溶液4hr。冷却且浓缩溶液,且所得4-(甲氧基甲基)-2-(三甲基锡烷基)吡啶直接用于下一步骤中。LCMS(ES)[M+1]+m/z:288。
步骤3
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入4-(甲氧基甲基)-2-(三甲基锡烷基)吡啶(中间体II,500.00mg,1.748mmol,1.00当量)、N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(415.16mg,1.399mmol,0.8当量)、Pd(dppf)Cl2(255.87mg,0.350mmol,0.20当量)及二噁烷(20.00mL)。在100℃下搅拌所得溶液16秒。将所得溶液冷却且用乙酸乙酯(3×20mL)萃取。将有机层合并,经无水硫酸钠干燥,且真空浓缩。通过使用以下条件的制备型HPLC(2#SHIMADZU(HPLC-01))纯化粗产物:柱,WelchXtimate C18,21.2*250mm,5um;移动相,水(0.05%TFA)及MeOH:ACN=1:1(17min内自10%相B达至60%)。由此产生51.2mg(7.6%)呈粉色固体的N-(叔丁基)-2-((2-(4-(甲氧基甲基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.83(dd,J=5.0,0.8Hz,1H),8.46-8.39(m,1H),7.97(s,1H),7.73(dd,J=5.0,1.7Hz,1H),4.64(s,2H),4.41(s,2H),3.49(s,3H),3.42(s,3H),3.32-3.18(m,2H),3.07(t,J=7.9Hz,2H),2.11(p,J=7.7Hz,2H),1.25(s,9H)。LCMS(ES)[M+1]+m/z:384.2。
实施例1.67
合成N-叔丁基-2-{乙基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物36)
流程38描绘用于制备例示性化合物的合成途径。
流程38
步骤1
向50mL圆底烧瓶中放入N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(500.00mg,1.768mmol,1.00当量)于DMF(10mL)中的溶液、碘乙烷(303.36mg,1.945mmol,1.1当量)及K2CO3(366.57mg,2.652mmol,1.5当量)。在室温下搅拌所得溶液3hr。将所得溶液用50mL H2O稀释且用2×50mL乙酸乙酯萃取。将有机层合并,经无水硫酸钠干燥,且真空浓缩。由此产生390mg(78.00%)呈淡黄色固体的N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(乙基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:311。
步骤2
向在惰性氮气氛围中吹扫及维持的25mL圆底烧瓶中放入N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(乙基)氨基)乙酰胺(230.00mg,0.813mmol,1.00当量)于Tol(8mL)中的溶液、2-(三丁基锡烷基)吡啶(359.34mg,0.976mmol,1.2当量)及Pd(PPh3)4(93.99mg,0.081mmol,0.1当量)。在油浴中在100℃下搅拌所得溶液12hr。将所得溶液用10mL H2O稀释且用2×15mL乙酸乙酯萃取。将有机层合并,经无水硫酸钠干燥,且浓缩。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上。通过使用以下条件的急骤制备型HPLC(IntelFlash-1)进一步纯化收集的粗产物:柱,C18硅胶;移动相,15内自CAN:H2O=1:20增加至ACN:H2O=1:4;检测器,254nm。获得产物且浓缩。由此产生120mg(41.74%)呈固体的N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(乙基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.67(dd,J=4.8,1.9Hz,1H),8.35(d,J=8.1Hz,1H),7.88(td,J=7.7,1.9Hz,1H),7.71(s,1H),7.44(ddd,J=7.5,4.7,1.2Hz,1H),4.10(s,2H),3.66(q,J=7.1Hz,2H),3.09(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.08-1.95(m,2H),1.23(s,9H),1.19(t,J=7.0Hz,3H)。LCMS(ES)[M+1]+m/z 354.2。
实施例1.68
合成N-叔丁基-2-[(2-羟乙基)[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺(化合物37)
流程39描绘用于制备例示性化合物的合成途径。
流程39
步骤1
向在惰性氮气氛围中吹扫及维持的25mL圆底烧瓶中放入N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。于油浴中在室温下搅拌所得溶液12hr。用25mL H2O稀释所得溶液。将所得溶液用2×25mL乙酸乙酯萃取,经无水硫酸钠干燥,且浓缩。将残余物施加至含乙酸乙酯/石油醚(1:3)的硅胶柱上。将收集的洗脱份合并且浓缩。由此产生420mg(57.8%)N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(2-((四氢-2H-吡喃-2-基)氧基)乙基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:411。
步骤2
向在惰性氮气氛围中吹扫及维持的25mL圆底烧瓶中放入N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(2-((四氢-2H-吡喃-2-基)氧基)乙基)氨基)乙酰胺(400mg,0.97mmol,1.00当量)于二氧杂环己烯(8mL)中的溶液、2-(三丁基锡烷基)吡啶(243mg,0.97mmol,1当量)及Pd(PPh3)4(112mg,0.097mmol,0.1当量)。在油浴中在100℃下搅拌所得溶液12hr。将所得溶液用20mL H2O稀释且用3×20mL乙酸乙酯萃取。将有机层合并且浓缩。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上。将收集的洗脱份合并且浓缩。由此产生230mg(52.09%)呈固体的N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(乙基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:454。
步骤3
向25mL圆底烧瓶中放入N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(乙基)氨基)乙酰胺(150.00mg,0.331mmol,1.00当量)于MeOH(7mL)中的溶液、pTSA(5.69mg,0.033mmol,0.1当量)。在室温下搅拌所得溶液12hr。浓缩所得混合物。通过使用以下条件者急骤制备型HPLC(IntelFlash-1)纯化粗产物:柱,硅胶;移动相,在9内自ACN:H2O(0.01%TFA)=1:15增加至ACN:H2O(0.01%TFA)=1:3;检测器,UV 254nm。由此产生80mg(65.48%)N-(叔丁基)-2-((2-羟乙基)(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:370.2。1H NMR(300MHz,DMSO-d6)δ8.67(d,J=4.9Hz,1H),8.36(d,J=7.9Hz,1H),7.93-7.80(m,2H),7.48-7.40(m,1H),5.15(t,J=5.5Hz,1H),4.16(s,2H),3.78-3.61(m,4H),3.10(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.06-1.96(m,2H),1.22(s,9H)。
实施例1.69
合成2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-[(吡啶-2-基)甲基]乙酰胺(化合物38)
流程40描绘用于制备例示性化合物的合成途径。
流程40
向8mL小瓶中放入[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(200mg,0.70mmol,1.0当量)、DMF(3.0mL)、2-吡啶甲胺(84mg,0.77mmol,1.1当量)及DIEA(455mg,3.52mmol,5.0当量)。之后在0℃下添加HATU(401mg,1.06mmol,1.5当量)。在室温下搅拌混合物1h,过滤,且通过使用如下条件的制备型HPLC纯化滤液:C18-120g柱,CH3CN/H2O(0.05%NH4OH),5%至80%,15min,流动速率,70mL/min,检测器,254nm。由此产生62.8mg(24%)呈淡棕色固体的2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]-N-(吡啶-2-基甲基)乙酰胺甲酸盐。1H-NMR(300MHz,DMSO-d6,ppm):δ8.72(t,J=6.0Hz,1H),8.64(dd,J=4.7,1.8Hz,1H),8.43(dd,J=4.8,1.9Hz,1H),8.28(dt,J=8.0,1.1Hz,1H),8.16(s,1H),7.85(td,J=7.7,1.8Hz,1H),7.44(ddd,J=7.5,4.7,1.2Hz,1H),7.35(td,J=7.7,1.8Hz,1H),7.21-7.14(m,2H),4.37(d,J=6.0Hz,2H),4.34(s,2H),3.34(s,3H),3.20(t,J=7.2Hz,2H),2.83(t,J=7.8Hz,2H),1.99(p,J=7.7Hz,2H)。LCMS:(ES,m/z):[M+H]+:375.2。
实施例1.70
合成N-叔丁基-2-({2-[6-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物39)
流程41描绘用于制备例示性化合物的合成途径。
流程41
步骤1
向100mL圆底烧瓶中放入6-氯吡啶-2-醇(5.00g,38.59mmol,1.00当量)、DMF(50.0mL)、2-(2-溴乙氧基)氧杂环己烷(9.68g,46.31mmol,1.20当量)及K2CO3(10.67g,77.19mmol,2.00当量)。在70℃下搅拌混合物2h。将反应混合物冷却并用200mL H2O稀释,且用3×50mL乙酸乙酯萃取。将有机层合并并经无水硫酸钠干燥,过滤,且减压浓缩滤液。通过含乙酸乙酯/石油醚(1/3)的硅胶柱纯化残余物,得到9.0g(90%)呈无色油状物的2-氯-6-[2-(氧杂环己-2-基氧基)乙氧基]吡啶。LCMS(ES)[M+1]+m/z:258。
步骤2
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入2-氯-6-[2-(氧杂环己-2-基氧基)乙氧基]吡啶(600mg,2.42mmol,1.00当量)、二噁烷(10.0mL)、六甲基二锡烷(872mg,2.66mmol,1.10当量)及Pd(dppf)Cl2(177mg,0.24mmol,0.10当量)。在100℃下搅拌混合物2h。将反应混合物冷却并用20mL H2O稀释,且用3×10mL乙酸乙酯萃取。将有机层合并并经无水硫酸钠干燥,过滤,且减压浓缩滤液。由此产生500mg呈棕色油状物的2-[2-(氧杂环己-2-基氧基)乙氧基]-6-(三甲基锡烷基)吡啶,且粗产物不经纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:388。
步骤3
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入2-[2-(氧杂环己-2-基氧基)乙氧基]-6-(三甲基锡烷基)吡啶(468mg,1.21mmol,1.20当量)、二噁烷(5.0mL)、N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(300mg,1.01mmol,1.00当量)及Pd(PPh3)4(116mg,0.10mmol,0.10当量)。在100℃下搅拌混合物16h。将反应混合物冷却并用20mL EA稀释,过滤,且减压浓缩滤液。通过含乙酸乙酯/石油醚(4/1)的硅胶柱纯化残余物。由此产生400mg(82%)呈棕色固体的N-叔丁基-2-[甲基(2-[6-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺。LCMS(ES)[M+1]+m/z:484。
步骤4
向100mL圆底烧瓶中放入N-叔丁基-2-[甲基(2-[6-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(400mg,0.82mmol,1.00当量)、MeOH(5.0mL)及TsOH(142mg,0.82mmol,1.00当量)。在室温下搅拌所得溶液1h。将所得混合物浓缩且用5mL H2O稀释。用NH3.H2O(30%)将溶液的pH值调节至8。用3×5mL乙酸乙酯萃取混合物,将有机层合并,经无水硫酸钠干燥,过滤,且浓缩滤液。通过使用以下条件的制备型HPLC纯化残余物:柱,Welch XB-C18,21.2*250mm,5um,移动相,水(0.05%NH4OH)及CH3CN(15min内自10%相B达至65%),检测器,UV 254nm。由此产生121.1mg(36.6%)呈白色固体的N-叔丁基-2-([2-[6-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ7.96(d,J=7.2Hz,1H),7.79(t,J=7.8Hz,1H),7.63(s,1H),6.89(d,J=8.1Hz,1H),5.18(br,1H),4.43-4.39(m,2H),4.16(s,2H),3.79-3.75(m,2H),3.27(s,3H),3.13(t,J=7.5Hz,2H),2.82(t,J=7.8Hz,2H),2.04-1.96(m,2H),1.23(s,9H)。LCMS(ES)[M+1]+m/z:400.2。
实施例1.71
合成N-叔丁基-2-({2-[5-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物40)
流程42描绘用于制备例示性化合物的合成途径。
流程42
步骤1
向250mL圆底烧瓶中放入6-溴吡啶-3-醇(2.00g,11.49mmol,1.00当量)、DMF(30.00mL)、2-(2-溴乙氧基)氧杂环己烷(2.88g,13.79mmol,1.20当量)及K2CO3(3.18g,22.99mmol,2.00当量)。在70℃下搅拌所得溶液2h。将反应混合物冷却至室温。随后通过添加50mL水淬灭反应物。用3×50mL乙酸乙酯萃取所得混合物,将有机层合并,经无水硫酸钠干燥,且浓缩。将残余物施加至含乙酸乙酯/石油醚(15%)的硅胶柱上。由此产生3.2g(92.13%)呈黄色油状物的2-溴-5-[2-(氧杂环己-2-基氧基)乙氧基]吡啶。LCMS(ES)[M+H]+m/z:302。
步骤2
向100mL圆底烧瓶中放入2-溴-5-[2-(氧杂环己-2-基氧基)乙氧基]吡啶(1.00g,3.31mmol,1.00当量)、六甲基二锡烷(1.30g,3.97mmol,1.20当量)、Pd(PPh3)4(0.38g,0.33mmol,0.1当量)及二噁烷(10.00mL)。在100℃下搅拌所得溶液3h。将反应混合物冷却至室温且添加N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(中间体II,0.49g,1.65mmol,0.50当量)及Pd(dppf)Cl2(0.24g,0.33mmol,0.10当量)。在100℃下搅拌所得溶液5h。将反应混合物冷却至室温。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自30%相B达至60%);检测器,254nm。由此产生150mg(9.37%)呈黄色固体的N-叔丁基-2-[甲基(2-[5-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺。LCMS(ES)[M+H]+m/z:484。
步骤3
向8mL小瓶中放入N-叔丁基-2-[甲基(2-[5-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(150.00mg,0.31mmol,1.00当量)、MeOH(5.00mL)及PTSA(10.68mg,0.06mmol,0.20当量)。在室温下搅拌所得溶液1h。通过使用以下条件的制备型HPLC纯化粗产物(150mg):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自20%相B达至50%);检测器,254nm。由此产生45.0mg(36.32%)呈白色固体的N-叔丁基-2-([2-[5-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺。1H-NMR(300MHz,DMSO-d6)δ8.38-8.27(m,2H),7.68(s,1H),7.43(dd,J=8.8,3.0Hz,1H),4.94(t,J=5.5Hz,1H),4.18-4.09(m,4H),3.78-3.73(m,2H),3.25(s,3H),3.12(t,J=7.3Hz,2H),2.79(t,J=7.8Hz,2H),2.10-1.89(m,2H),1.24(s,9H)。LCMS:(ES,m/z):[M+H]+:400.3。
实施例1.72
合成N-叔丁基-2-({2-[4-(羟甲基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物41)
流程43描绘用于制备例示性化合物的合成途径。
流程43
向在惰性氮气氛围中吹扫及维持的50mL圆底烧瓶中放入N-(叔丁基)-2-((2-(4-(甲氧基甲基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(100mg,0.261mmol,1.00当量)、BBr3(0.78mL,0.780mmol,2.99当量)及DCM(10.00mL)。在-78℃下搅拌所得溶液4hr。通过添加水淬灭反应物。用二氯甲烷(3×20mL)萃取所得溶液,将有机层合并,经无水硫酸钠干燥,且真空浓缩。通过使用以下条件的制备型HPLC(2#SHIMADZU(HPLC-01))纯化粗产物:柱,Welch XB-C18,21.2*250mm,5um;移动相,水(0.05%NH3H2O)及AcCN(16min内自5%相B达至50%)。由此产生30.2mg(31.4%)呈白色固体的N-(叔丁基)-2-((2-(4-(羟甲基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.60(d,J=4.9Hz,1H),8.26(s,1H),7.68(s,1H),7.39(d,J=5.0Hz,1H),5.48(br,1H),4.62(s,2H),4.16(s,2H),3.32(s,3H),3.14(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),1.99(p,J=7.5Hz,2H),1.24(s,9H)。LCMS(ES)[M+1]+m/z:370.2。
实施例1.73
合成N-叔丁基-2-{甲基[2-(4-甲基吡啶-2-基)-5,6,7,8-四氢喹唑啉-4-基]氨基}乙酰胺(化合物42)
流程44描绘用于制备例示性化合物的合成途径。
流程44
步骤1
向40mL小瓶中放入2,4-二氯-5,6,7,8-四氢喹唑啉(500.00mg,2.46mmol,1.00当量)、CH3CN(8.00mL)、DIEA(636.45mg,4.92mmol,2.00当量)及N-叔丁基-2-(甲基氨基)乙酰胺(390.60mg,2.71mmol,1.10当量)。在80℃下搅拌所得溶液3h。将反应混合物冷却至室温。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自30%相B达至60%);检测器,254。由此产生410mg(53.57%)呈白色固体的N-叔丁基-2-[(2-氯-5,6,7,8-四氢喹唑啉-4-基)(甲基)氨基]乙酰胺。LCMS(ES)[M+H]+m/z:311。
步骤2
向用惰性氮气氛围吹扫及维持的40mL小瓶中放入N-叔丁基-2-[(2-氯-5,6,7,8-四氢喹唑啉-4-基)(甲基)氨基]乙酰胺(350.00mg,1.12mmol,1.00当量、4-甲基-2-(三丁基锡烷基)吡啶(559.44mg,1.46mmol,1.30当量)及二噁烷(8.00mL)、Pd(dppf)Cl2(82.39mg,0.11mmol,0.10当量)。在110℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物(500mg):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自30%相B达至60%);检测器,254。由此产生86.4mg(20.88%)呈灰白色固体的N-叔丁基-2-[甲基[2-(4-甲基吡啶-2-基)-5,6,7,8-四氢喹唑啉-4-基]氨基]乙酰胺。1H-NMR(300MHz,DMSO-d6)δ8.51(d,J=4.9Hz,1H),8.15(d,J=1.6Hz,1H),7.77(s,1H),7.31-7.23(m,1H),3.99(s,2H),3.15(s,3H),2.78(t,J=6.4Hz,2H),2.69(t,J=6.0Hz,2H),2.40(s,3H),1.82(s,2H),1.68(d,J=6.9Hz,2H),1.22(s,9H)。LCMS(ES,m/z):[M+H]+:368.2。
实施例1.74
合成N-叔丁基-2-({2-[5-(2-羟乙基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物43)
流程45描绘用于制备例示性化合物的合成途径。
流程45
步骤1
向250mL 3颈圆底烧瓶中放入(6-氯吡啶-3-基)乙酸(5.0g,29.14mmol,1.0当量)、THF(50.0mL)。之后在0℃下添加B2H6(1M于THF中)(88.0mL,3.0当量)。添加后,在室温下搅拌混合物12h。随后通过添加MeOH(30mL)将反应物淬灭,用H2O(100mL)稀释,且用3×100mL二氯甲烷萃取。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。得到3.09g(67%)呈黄色油状物的2-(6-氯吡啶-3-基)乙醇。LCMS(ES)[M+1]+m/z:158。
步骤2
向100mL圆底烧瓶中放入2-(6-氯吡啶-3-基)乙醇(3.09g,19.61mmol,1.0当量)、DCM(30.0mL)、DHP(3.30g,39.23mmol,2.0当量)及TsOH(340mg,1.97mmol,0.10当量)。在室温下搅拌反应溶液2h。将混合物用饱和Na2CO3(20.0mL)稀释,且用3×50mL二氯甲烷萃取。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。通过含乙酸乙酯/石油醚(7%)的硅胶柱纯化残余物。由此产生3.0g(63%)呈黄色油状物的2-氯-5-(2-((四氢-2H-吡喃-2-基)氧基)乙基)吡啶。LCMS(ES)[M+1]+m/z:242。
步骤3
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入2-氯-5-[2-(氧杂环己-2-基氧基)乙基]吡啶(1.17g,4.84mmol,1.0当量)、二噁烷(30.0mL)、六甲基二锡烷(1.60g,4.88mmol,1.0当量)及Pd(PPh3)4(1.44g,1.25mmol,0.26当量)。在100℃下搅拌混合物2h。将反应物冷却至室温,过滤,且减压浓缩滤液。粗产物不经进一步纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:372。
步骤4
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入5-[2-(氧杂环己-2-基氧基)乙基]-2-(三甲基锡烷基)吡啶(1.50g,4.05mmol,1.0当量)、二噁烷(20.0mL)、N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(中间体II,700mg,2.36mmol,0.58当量)及Pd(PPh3)4(932.00mg,0.81mmol,0.20当量)。在100℃下搅拌混合物12h。浓缩混合物以移除溶剂,且通过含THF/石油醚(70%)的硅胶柱纯化残余物。由此产生184mg(9.7%)呈黄色油状物的N-(叔丁基)-2-(甲基(2-(5-(2-((四氢-2H-吡喃-2-基)氧基)乙基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:468。
步骤5
向20mL小瓶中放入N-叔丁基-2-[甲基(2-[5-[2-(氧杂环己-2-基氧基)乙基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(184mg,0.39mmol,1.0当量)、甲醇(5.0mL)及TsOH(68mg,0.40mmol,1.0当量)。在室温下搅拌混合物1h。通过使用以下条件的制备型HPLC纯化粗产物:柱,Atlantis HILIC OBD柱,19*150mm*5um;移动相,水(10mmol/LNH4HCO3)及MeOH:CH3CN=1:1(9min内自33%相B达至45%);检测器,UV 254nm。由此产生89.2mg(59%)呈灰白色固体的N-(叔丁基)-2-((2-(5-(2-羟乙基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H-NMR(300MHz,DMSO-d6,ppm):δ8.51(d,J=1.8Hz,1H),8.25(d,J=8.1Hz,1H),7.72(dd,J=8.1,2.1Hz,1H),7.68(s,1H),4.72(t,J=5.1Hz,1H),4.13(s,2H),3.70-3.63(m,2H),3.26(s,3H),3.14(t,J=7.2Hz,2H),2.84-2.78(m,4H),2.04-1.96(m,2H),1.25(s,9H)。LCMS:(ES,m/z):[M+H]+:384.2。
实施例1.75
合成N-叔丁基-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物44)
流程46a描绘用于制备例示性化合物的合成途径。
流程46a
步骤1
向50mL圆底烧瓶中放入2-氯吡啶-4-醇(2.00g,15.439mmol,1.00当量)、DMF(20ml)、K2CO3(4.27g,30.878mmol,2.00当量)及2-(2-溴乙氧基)氧杂环己烷(4.84g,23.159mmol,1.50当量)的混合物。在70℃下搅拌所得溶液16小时。用100mL H2O稀释所得溶液。用3×100mL乙酸乙酯萃取所得溶液。将有机层合并,用100ml盐水洗涤,经无水硫酸钠干燥,且浓缩。由此产生2.15g(54.04%)呈淡黄色油状物的2-氯-4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶。LCMS(ES)[M+1]+m/z:258。
步骤2
向40mL小瓶中放入2-氯-4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶(1.00g,3.88mmol,1.00当量)、二噁烷(10.0mL)、六甲基二锡烷(1.91g,5.82mmol,1.50当量)及Pd(PPh3)4(896mg,0.776mmol,0.20当量)的混合物。在100℃下搅拌所得溶液2小时。浓缩所得混合物。此所得产物直接用于下一步骤中。LCMS(ES)[M+1]+m/z:388。
步骤3
向40mL小瓶中放入4-[2-(氧杂环己-2-基氧基)乙氧基]-2-(三甲基锡烷基)吡啶(800mg,2.07mmol,1.00当量)、二噁烷(10.00mL)、N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(中间体II,430mg,1.45mmol,0.70当量)及Pd(PPh3)4(478mg,0.414mmol,0.20当量)的混合物。在100℃下搅拌所得溶液16小时。将粗反应混合物过滤且进行反相制备型MPLC(Prep-C18,20-45mM,120g,Tianjin Bonna-AgelaTechnologies;经15min时段自10%MeCN/水达至48%MeCN/水的梯度洗脱,其中两种溶剂皆含有0.1%NH4HCO3)。浓缩所得混合物。由此产生280mg(27.94%)呈灰白色固体的N-(叔丁基)-2-(甲基(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:484。
步骤4
向40mL小瓶中放入N-(叔丁基)-2-(甲基(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(250mg,0.517mmol,1.00当量)、MeOH(10.0mL)及TsOH(89mg,0.52mmol,1.0当量)的混合物。在室温下搅拌所得溶液2小时。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物:柱,XBridgePrep C18 OBD柱,19×150mm,5um;移动相,相A:H2O(0.05%NH3H2O);相B:CH3CN(13min内自20%CH3CN达至70%CH3CN)。由此产生72.6mg(35.15%)呈白色固体的N-(叔丁基)-2-((2-(4-(2-羟乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1HNMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.6Hz,1H),7.85(d,J=2.5Hz,1H),7.68(s,1H),7.04(dd,J=5.7,2.6Hz,1H),4.92(t,J=5.4Hz,1H),4.19-4.10(m,4H),3.76(q,J=5.1Hz,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.01-1.96(m,2H),1.24(s,9H)。LCMS(ES)[M+1]+m/z:400.2。
流程46b描绘用于制备例示性化合物的合成途径。
流程46b
步骤1
向50mL 3颈圆底烧瓶中放入N-(叔丁氧羰基)-N-甲基甘氨酸(20.0g,0.105mol,1.00当量)、DMF(200.00mL)、2-甲基丙-2-胺(8.43g,0.115mol,1.10当量)及DIEA(27.21g,0.211mmol,2.00当量)。之后在0℃下分数批添加HATU(44.08g,0.115mol,1.10当量)。添加后,在室温下搅拌所得溶液16h。将反应物用200mL水淬灭,用3×100mL乙酸乙酯萃取。将合并的有机相用2×200mL水及1×200mL盐水洗涤,经无水硫酸钠干燥且过滤。减压浓缩滤液,通过含乙酸乙酯/石油醚(1:1)的硅胶柱纯化残余物,得到20.6g(80%)呈灰白色固体的(2-(叔丁基氨基)-2-氧代乙基)(甲基)氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z:245。
步骤2
向500mL 3颈圆底烧瓶中放入(2-(叔丁基氨基)-2-氧代乙基)(甲基)氨基甲酸叔丁酯(25g,102.4mmol,1.00当量)及DCM(100.00mL)。之后在0℃下在搅拌下逐滴添加HCl(g)(4M于二噁烷中)(200.00mL)。将所得溶液在室温下搅拌16h,真空浓缩以移除溶剂且用乙酸乙酯(150mL)洗涤。由此产生16g(86%)N-(叔丁基)-2-(甲基氨基)乙酰胺盐酸盐。LCMS(ES)[M-HCl+1]+m/z:145。
步骤3
向500mL 3颈圆底烧瓶中放入N-(叔丁基)-2-(甲基氨基)乙酰胺盐酸盐(16g,88.9mmol,1.00当量)、NMP(200.00mL)、2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(16.8g,88.9mmol,1.00当量)及DIEA(40.6g,0.315mol,3.00当量)。在油浴中在50℃下搅拌所得溶液6h。将反应混合物冷却至室温,用200mL水稀释且用3×200mL乙酸乙酯萃取。将合并的有机相用3×300mL水及盐水1×200mL洗涤,经无水硫酸钠干燥且过滤。减压浓缩滤液,将残余物用乙酸乙酯湿磨且过滤。由此产生18.4g(70%)呈白色固体的N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:297。
步骤4
如下合成4-氟-2-(三丁基锡烷基)吡啶:在-78℃下向2-溴-4-氟吡啶(25g,142mmol,1.00当量)于甲苯(300mL)中的溶液中添加丁基锂(62.5mL,2.50mol/L,156mmol,1.10当量),搅拌1h后,向混合物中添加三丁基(氯)锡烷(50.7g,156mmol,1.10当量)且在-78℃下进一步搅拌30min并在室温下搅拌3h。将混合物用冰水淬灭,用己烷萃取,将有机层合并且用饱和NaHCO3、盐水洗涤,干燥且过滤。浓缩滤液,得到呈澄清黄色油状物的粗产物(51g),其不经纯化即使用。LCMS(ES)[M+1]+m/z:388。
向用惰性氮气氛围吹扫且维持的250mL三颈圆底烧瓶中放入N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(10g,33.8mmol,1.00当量)、甲苯(150.00mL)、4-氟-2-(三丁基锡烷基)吡啶(21.7g,60.84mmol,1.8当量)及Pd(PPh3)4(3.57g,3.38mmol,0.10当量)。于油浴中在110℃下搅拌混合物60h。将反应混合物冷却至室温,浓缩以移除溶剂;通过含二氯甲烷/甲醇(10:1)的硅胶柱纯化残余物。由此产生7g(58%)呈黄色固体的N-(叔丁基)-2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:358。
步骤5
向250mL 3颈烧瓶中放入乙烷-1,2-二醇(9.55g,154mmol,10.0当量)及DMF(100mL),在0-5℃下分批添加NaH(60%于矿物油中)(6.16g,154mmol,10.0当量)。在室温下搅拌混合物1h,且在0-5℃下添加N-(叔丁基)-2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(5.5g,15.4mmol,1.00当量)。在50℃下搅拌反应混合物5h。(在2个批次中重复反应)。将反应混合物冷却至室温,用200mL水稀释,用3×200mL乙酸乙酯萃取。将合并的有机相用3×300mL水及盐水1×200mL洗涤,经无水硫酸钠干燥。通过使用如下条件的制备型HPLC纯化残余物:柱,C18-800g,移动相,CH3CN/H2O(0.05%FA),27min内自10%增加至70%,流动速率,180mL/min,检测器,254nm。用K2CO3固体将洗脱份的pH值调节至7-8,用二氯甲烷(3×300mL)萃取。使合并的有机相经无水硫酸钠干燥且过滤。减压浓缩滤液且冷冻干燥残余物,由此产生5.03g(41%)呈白色固体的N-(叔丁基)-2-((2-(4-(2-羟乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS:(ES,m/z):[M+H]+:400。1H-NMR:(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.6Hz,1H),7.86(d,J=2.5Hz,1H),7.68(s,1H),7.04(dd,J=5.6,2.6Hz,1H),4.92(t,J=5.4Hz,1H),4.19-4.10(m,4H),3.77(q,J=5.1Hz,2H),3.26(s,3H),3.13(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.01-1.96(m,2H),1.24(s,9H)。
合成化合物44—途径2。
流程4-1
向250mL圆底烧瓶中放入N-叔丁基-2-[[2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺(7.40g,19.79mmol,1.00当量)、2-(氧杂环己-2-基氧基)乙醇(4.34g,29.69mmol,1.50当量)、DMF(150.00mL)及t-BuOK(6.66g,59.37mmol,3.00当量)。在25℃下搅拌所得溶液过夜。随后通过添加水/冰来淬灭反应物。用3×200mL乙酸乙酯萃取所得溶液,且将有机层合并,经无水硫酸钠干燥并浓缩。通过使用以下条件的制备型HPLC纯化粗产物(8g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3.H2O)及CAN(11min内自20%相B达至60%);检测器,254。由此产生6g(62.69%)呈黄色固体的N-叔丁基-2-[甲基(2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺。LCMS(ES)[M+1]+m/z:484。
向40mL小瓶中放入N-叔丁基-2-[甲基(2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(1.00g,2.07mmol,1.00当量)、MeOH(10.00mL)及HCl(6M)(1.00mL)。在室温下搅拌所得溶液1h。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridge Prep C18OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3·H2O)及ACN(11min内自15%相B达至60%);检测器,254nm。由此产生613.5mg(74.27%)呈白色固体的N-叔丁基-2-([2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺。LCMS(ES,m/z):[M+H]+:400。1H-NMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.6Hz,1H),7.85(d,J=2.5Hz,1H),7.68(s,1H),7.04(dd,J=5.7,2.6Hz,1H),4.92(t,J=5.4Hz,1H),4.21-4.07(m,4H),3.76(q,J=5.1Hz,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.01-1.96(m,2H),1.24(s,9H)。
实施例1.76
合成4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚-2-酮(化合物47)
用1,4-二氮杂环庚-2-酮替换氮杂环庚烷,与化合物92类似地合成化合物47。LCMS(ES+):(M+H)+=310.0。1H NMR(400MHz,DMSO-d6)δ8.82-8.76(m,1H),8.52(d,J=7.9Hz,1H),8.12-8.05(m,1H),7.70-7.61(m,2H),6.52(s,1H),4.48(s,2H),4.16-4.06(m,2H),3.27-3.22(m,4H),2.99(t,J=7.9Hz,2H),2.14-2.03(m,2H),1.92-1.83(m,2H)。
实施例1.77
合成1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚-5-酮(化合物50)
用1,4-二氮杂环庚-5-酮替换氮杂环庚烷,与化合物92类似地合成化合物50。LCMS(ES+):(M+H)+=309.9。1H NMR(400MHz,DMSO-d6)δ8.76-8.69(m,1H),8.34(d,J=7.9Hz,1H),8.01-7.92(m,1H),7.73-7.64(m,1H),7.57-7.48(m,1H),3.98-3.92(m,4H),3.29-3.26(m,2H),3.10-3.03(m,2H),2.93-2.87(m,2H),2.65-2.60(m,2H),2.09-2.00(m,2H)。
实施例1.78
合成(2R)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物51)
流程47描绘用于制备例示性化合物的合成途径。
流程47
步骤1
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(130.00mg;0.69mmol;1.00当量)溶解于乙腈(2.5ml)中,且向溶液中添加(2R)-2-(甲基氨基)丙酸甲酯盐酸盐(126.76mg;0.83mmol;1.20当量)及休尼格氏碱(0.48mL;2.75mmol;4.00当量)。在约55℃下搅拌15h后,蒸发混合物且对残余物进行柱色谱,得到呈薄膜的(2R)-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙酸甲酯(54mg,31%)。LCMS(ES+):(M+H)+=270.2。
步骤2
将(2R)-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙酸甲酯(54mg;0.20mmol;1当量)溶解于THF(2ml)及甲醇(0.5ml)中。逐滴添加溶解于约0.8ml水中的氢氧化锂(无水,19mg;0.8mmol;4当量)且在25℃下搅拌反应物1.5h。小心地添加6M HCl以将反应物酸化至pH<3。蒸发溶剂且高真空干燥残余物。将残余物(2R)-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙酸(51mg;0.2mmol;1当量)溶解于N,N-二甲基甲酰胺(2ml)中。添加N,N-二异丙基乙胺(0.12mL;0.7mmol;3.5当量)且于冰浴中搅拌反应物。添加叔丁胺(32μL;0.3mmol;1.5当量)及3-氧化六氟磷酸1-[双(二甲基氨基)亚甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓(HATU,152mg;0.4mmol;2当量)。4h后,添加乙酸乙酯(50ml)、水(10ml)及碳酸氢钠溶液(10ml)。分离各相,且用乙酸乙酯(50ml)萃取水相。将有机相用水(10ml)及氯化钠溶液(20ml)洗涤,且经硫酸钠干燥。蒸发后,通过硅胶色谱(乙酸乙酯/己烷梯度)纯化产物,得到(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙烯酰胺(12.5mg,20%)。MS(ES+):(M+H)+=310.9。
步骤3
将(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙酰胺(30.00mg;0.10mmol;1.00当量)溶解于1,4-二噁烷(1ml)中且用Ar气体吹扫溶液。添加2-(三丁基锡烷基)吡啶(0.06mL;0.19mmol;2.00当量)及四(三苯基膦)钯(11.15mg;0.01mmol;0.10当量)。密封反应容器且在110℃下于热浴中搅拌15h。蒸发后,通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈灰白色固体的(2R)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(11mg,32%)。LCMS(ES+):(M+H)+=354.4。1H NMR(400MHz,甲醇-d4)δ8.72(ddd,J=4.9,1.8,0.9Hz,1H),8.46-8.41(m,1H),8.02-7.95(m,1H),7.68(s,1H),7.57-7.50(m,1H),5.26(q,J=7.1Hz,1H),3.38-3.33(m,1H),3.28-3.18(m,1H),3.08-2.91(m,2H),2.24-2.06(m,2H),1.48(d,J=7.1Hz,3H),1.25(s,9H)。
实施例1.79
合成(2S)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物52)
用(2S)-2-(甲基氨基)丙酸酯替换(2R)-2-(甲基氨基)丙酸酯,与化合物51类似地合成化合物52。LCMS(ES+):(M+H)+=354.4。1H NMR(400MHz,甲醇-d4)δ8.72(ddd,J=4.8,1.8,0.9Hz,1H),8.46-8.40(m,1H),8.02-7.95(m,1H),7.68(s,1H),7.54(ddd,J=7.6,4.8,1.2Hz,1H),5.26(q,J=7.1Hz,1H),3.38-3.32(m,1H),3.28-3.18(m,1H),3.09-2.91(m,2H),2.23-2.04(m,2H),1.48(d,J=7.2Hz,3H),1.25(s,9H)。
实施例1.80
合成1-[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷(化合物53)
用4-甲氧基-2-(三丁基锡烷基)吡啶替换(2-三丁基锡烷基)吡啶,与化合物92类似地合成化合物53。1H NMR(400MHz,甲醇-d4)δ8.48(d,J=5.8Hz,1H),7.86(d,J=2.6Hz,1H),7.06(dd,J=5.8,2.6Hz,1H),3.94(s,3H),3.86(t,J=6.1Hz,4H),3.15(t,J=7.3Hz,2H),2.92(t,J=7.9Hz,2H),2.16-2.04(m,2H),1.83(q,J=5.5Hz,4H),1.59(p,J=2.7Hz,4H)。LCMS(ES+):(M+H)+=325.1。
实施例1.81
合成(3R)-6,6-二甲基-3-{[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}哌啶-2-酮(化合物55)
流程48描绘用于制备例示性化合物的合成途径。
流程48
步骤1
在100mL 3颈圆底烧瓶中,在氮气氛围下将Zn(2.98g,45.6mmol,3.0当量)悬浮于无水DMF(30mL)中,且立即添加碘(两种晶体)。观测到色彩自无色变成深棕色且再次变成无色。添加(2S)-2-[(叔丁氧羰基)氨基]-3-碘丙酸甲酯(5.0g,15.2mmol,1.0当量),紧接着添加碘(三种晶体),再次观测到前述色彩变化,且插入过程进行2h。将含有CuBr-Me2S(0.31g,1.53mmol,0.1当量)的烧瓶置于真空下且猛烈加热直至灰色CuBr-Me2S变成淡绿色/黄色。随后将烧瓶置于氮气流下且使其冷却至室温。再次重复此过程,且使烧瓶冷却至室温。将Zn试剂于DMF中的制备溶液转移至含有CuBr-Me2S(2.06g,22.78mmol,2.0当量)的烧瓶中,且在室温下搅拌反应物72h。随后经由用EtOAc洗脱的硅柱过滤反应混合物。用水(2×50mL)及盐水(50mL)洗涤有机相。将有机相用Na2SO4干燥,过滤,且减压移除溶剂。将残余物施加至含乙酸乙酯/石油醚(1:50至1:1)的硅胶柱上。由此产生3g(76.7%)呈油状物的(2R)-2-[(叔丁氧羰基)氨基]-5-甲基己-5-烯酸甲酯。LCMS(ES)[M+1]+m/z:258.2。
步骤2
在500mL 3颈圆底烧瓶中,将Fe2(OX)3.6H2O(3.76g,7.77mmol,2.0当量)搅拌于H2O(150mL)中直至完全溶解(通常2h)。将澄清黄色溶液冷却至0℃且用Ar脱气10min。添加NaN3(0.76g,11.66mmol,3.0当量)及乙醇(75mL)。20min后,在0℃下将(2R)-2-[(叔丁氧羰基)氨基]-5-甲基己-5-烯酸甲酯(1.00g,3.886mmol,1.00当量)于EtOH(75mL)中的溶液添加至反应混合物中,之后添加NaBH4(1.03g,27.202mmol,7当量)。搅拌所得混合物30min,之后通过添加30%NH4OH水溶液(4mL)来淬灭。用10%MeOH/CH2Cl2萃取混合物,使有机层经Na2SO4干燥且浓缩。通过急骤色谱(SiO2,20%EtOAc/PE)纯化残余物,得到呈无色油状物的(2R)-5-叠氮基-2-[(叔丁氧羰基)氨基]-5-甲基己酸甲酯(450mg,38.5%)。LCMS(ES)[M+1]+m/z:301.2。
步骤3
在室温下向(2R)-5-叠氮基-2-[(叔丁氧羰基)氨基]-5-甲基己酸甲酯(450mg,1.50mmol,1.0当量)于EtOAc(15mL)中的溶液中添加Pd/C(200mg)。添加后,用H2吹扫反应物三次。于H2氛围下在25℃下搅拌所得混合物16hr。过滤所得混合物,且浓缩滤液,得到220mg(60.6%)呈灰白色固体的N-[(3R)-6,6-二甲基-2-氧代哌啶-3-基]氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z:243.3。
步骤4
向100mL圆底烧瓶中放入N-[(3R)-6,6-二甲基-2-氧代哌啶-3-基]氨基甲酸叔丁酯(220mg,0.91mmol,1.0当量)、EtOAc(5mL)及HCl/EtOAc(2mL,2M,4.0mmol,4.4当量)。在25℃下搅拌所得溶液5h。真空浓缩所得混合物。由此产生150mg(100%)呈灰白色固体的(3R)-3-氨基-6,6-二甲基哌啶-2-酮。LCMS(ES)[M+1]+m/z:143.
步骤5
向50mL圆底烧瓶中放入(3R)-3-氨基-6,6-二甲基哌啶-2-酮(150mg,1.05mmol,1.0当量)、2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(199mg,1.05mmol,1.0当量)、NMP(5mL)及DIPEA(409mg,3.16mmol,3.0当量)。在60℃下于油浴中搅拌所得溶液16h。将反应混合物冷却至室温。随后通过添加20mL水淬灭反应物。将所得溶液用3×30mL乙酸乙酯萃取,经无水硫酸钠干燥且浓缩。将残余物施加至含乙酸乙酯/石油醚(1:50至1:1)的硅胶柱上。由此产生160mg(51.5%)呈白色固体的(3R)-3-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基)-6,6-二甲基哌啶-2-酮。LCMS(ES)[M+1]+m/z:295.2。
步骤6
在25℃下向(3R)-3-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基)-6,6-二甲基哌啶-2-酮(160mg,0.54mmol,1.0当量)及2-(三丁基锡烷基)吡啶(200mg,0.54mmol,1.0当量)于二噁烷(5mL)中的溶液中一次性添加Pd(PPh3)4(62mg,0.05mmol,0.1当量)。添加后,于Ar氛围下在100℃下搅拌所得溶液16hr。真空浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:50至10:1)的硅胶柱上。通过使用以下条件的急骤制备型HPLC(IntelFlash-1)纯化粗产物(150mg):柱,C18硅胶;移动相,15min内自MeCN=10/90增加至MeCN=90/10;检测器,220。由此产生57.5mg(31.4%)呈白色固体的(3R)-6,6-二甲基-3-[[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]哌啶-2-酮。1H NMR(300MHz,DMSO-d6,ppm)δ8.65(d,J=3.9Hz,1H),8.23(d,J=7.8Hz,1H),7.89(dd,J=1.5Hz,7.5Hz,1H),7.57(s,1H),7.44(dd,J=1.2Hz,6.0Hz,1H),7.06(d,J=8.1Hz,1H),4.67-4.52(m,1H),2.84(t,J=7.5Hz,2H),2.72(t,J=7.2Hz,2H),2.12-1.96(m,4H),1.78-1.76(m,2H),1.23(d,J=10.8Hz,6H)。LCMS(ES)[M+1]+m/z:338.2。
实施例1.82
合成(3S)-6,6-二甲基-3-{[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}哌啶-2-酮(化合物56)
通过用(2R)-2-[(叔丁氧羰基)氨基]-3-碘丙酸甲酯替换(2S)-2-[(叔丁氧羰基)氨基]-3-碘丙酸甲酯,与化合物55类似地合成化合物56。1H NMR(300MHz,DMSO-d6,ppm)δ8.65(d,J=3.6Hz,1H),8.23(d,J=7.8Hz,1H),7.89(dd,J=1.8Hz,7.8Hz,1H),7.57(s,1H),7.44(dd,J=0.9Hz,4.8Hz,1H),7.06(d,J=8.1Hz,1H),4.71-4.53(m,1H),2.84(t,J=8.1Hz,2H),2.72(t,J=7.2Hz,2H),2.15-1.95(m,4H),1.79-1.76(m,2H),1.25(d,J=10.8Hz,6H)。LCMS(ES)[M+1]+m/z:338.2。
实施例1.83
合成N-叔丁基-2-{[2-(4-环丙基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物57)
流程49描绘用于制备例示性化合物的合成途径。
流程49
步骤1
在室温下向2-氯-4-甲氧基吡啶(1.0g,6.32mmol,1.00当量)、环丙基硼酸(0.68g,6.9mmol,1.25当量)及Na2CO3(1.68g,15.8mmol,2.50当量)于二噁烷(20mL)/H2O(1mL)中的混合物中添加Pd(dppf)Cl2.CH2Cl2(50mg,0.064mmol,0.01当量)。在Ar氛围下于油浴中在80℃下搅拌所得混合物16h。浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:100至1:10)的硅胶柱上。由此产生500mg(66.29%)呈固体的4-环丙基吡啶。LCMS(ES)[M+1]+m/z:120.1。1H NMR(300MHz,CDCl3,ppm)δ8.45(d,J=5.1Hz,2H),6.98(dd,J=4.5,1.5Hz,2H),1.92-1.84(m,1H),1.28-1.10(m,2H),0.84-0.81(m,2H)。
步骤2
于N2氛围下在-78℃下向2-(二甲基氨基)乙-1-醇(523mg,5.87mmol,2.0当量)于己烷(20mL)中的混合物中添加n-BuLi(2.3mL,2.5M,5.87mmol,2.0当量)。在-78℃下搅拌反应物20min后,添加Bu3SnCl(1.9g,5.8mmol,2.0当量)及4-环丙基吡啶(350mg,2.94mmol,1.0当量)。在-78℃至室温之间搅拌所得混合物2h。随后通过添加水来淬灭反应物。用3×50mL乙酸乙酯萃取所得溶液,将有机层合并,经Na2SO4干燥,且真空浓缩,得到600mg呈黄色胶状物的粗4-环丙基-2-(三丁基锡烷基)吡啶。LCMS(ES)[M+1]+m/z:410.1。
步骤3
向在惰性氩气氛围中吹扫及维持的50mL 3颈圆底烧瓶中放入4-环丙基-2-(三丁基锡烷基)吡啶(200mg,0.49mmol,1.00当量)、N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(中间体II,72.7mg,0.25mmol,0.5当量)、Pd(PPh3)4(56.6mg,0.05mmol,0.1当量)及二噁烷(5mL)。在100℃下搅拌所得溶液16hr。浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:10至10:1)的硅胶柱上。通过使用以下条件的急骤制备型HPLC(IntelFlash-1)纯化粗产物(150mg):柱,C18;移动相,移动相:MeCN=5/1B:水流动速率:20mL/min柱:DAICEL CHIRALPAK IC,250*20mm,220nm梯度:50%B,20min;220nm;由此产生87.6mg(47.11%)呈白色固体的N-叔丁基-2-[[2-(4-环丙基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.1Hz,1H),8.16(s,1H),8.08(d,J=1.8Hz,1H),7.68(s,1H),7.06(dd,J=5.1,1.8Hz,Hz,1H),4.15(s,2H),3.50(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.28-1.97(m,3H),1.23(s,9H),1.13-1.07(m,2H),0.88-0.82(m,2H)。LCMS(ES)[M+1]+m/z:380.2。
实施例1.84
合成N-叔丁基-2-{[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物58)
流程50描绘用于制备例示性化合物的合成途径。
流程50
向在惰性氮气氛围中吹扫及维持的50mL圆底烧瓶中放入4-氟-2-(三甲基锡烷基)吡啶(1.00g,3.85mmol,1.00当量)、N-叔丁基-2-[5H,6H,7H-环戊并[d]嘧啶-4-基(甲基)氨基]乙酰胺(中间体II,500mg,1.91mmol,0.50当量)、Pd(dppf)Cl2(350mg,0.43mmol,0.10当量)及二噁烷(20.0mL)。在100℃下搅拌混合物12h。浓缩混合物以移除溶剂,通过含THF/PE(70%)的硅胶柱纯化所得残余物,且通过使用如下条件的制备型HPLC进一步纯化收集的产物:柱,Welch Xtimate C18,21.2*250mm,5um,移动相,水(10mmol/L NH4HCO3)及MeOH:CH3CN=1:1(15min内自25%相B达至65%),检测器,UV,254nm。由此产生42.9mg(3%)呈白色固体的N-(叔丁基)-2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H-NMR(300MHz,DMSO-d6,ppm):δ8.69(dd,J=9.0,5.4Hz,1H),8.16(dd,J=10.8,2.7Hz,1H),7.73(s,1H),7.42-7.37(m,1H),4.12(s,2H),3.30(s,3H),3.17(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.05-1.95(m,2H),1.24(s,9H)。
LCMS(ES,m/z):[M+H]+:358.1。
实施例1.85
合成-叔丁基-2-{甲基[2-(6-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物59)
流程51描绘用于制备例示性化合物的合成途径。
流程51
向N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(中间体II,200.00mg,0.674mmol,1.00当量)及2-甲基-6-(三丁基锡烷基)吡啶(386.30mg,1.011mmol,1.5当量)于二噁烷(4ml)中的溶液中添加Pd(dppf)Cl2(49.31mg,0.067mmol,0.10当量)。于氮气氛围下在100℃下搅拌4h后,减压浓缩所得混合物。残余物通过硅胶柱色谱纯化且用PE/THF(1:5)洗脱,得到呈白色固体的N-叔丁基-2-[甲基[2-(6-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺(125mg,52.48%)。1H NMR(300MHz,DMSO-d6)1H NMR(300MHz,DMSO-d6)δ8.15(d,J=7.8Hz,1H),7.75(t,J=7.7Hz,1H),7.66(s,1H),7.29(d,J=7.6Hz,1H),4.13(s,2H),3.27(s,3H),3.14(t,J=7.4Hz,2H),2.83(t,J=7.8Hz,2H),2.55(s,3H),2.14-1.83(m,2H),1.24(s,9H)。LCMS(ES)[M+1]+m/z:354.3。
实施例1.86
合成N-叔丁基-2-{[2-(4,5-二甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物60)
流程52描绘用于制备例示性化合物的合成途径。
流程52
步骤1
向在惰性氮气氛围中吹扫及维持的250mL 3颈圆底烧瓶中放入3,4-二甲基吡啶(1.00g,9.332mmol,1.00当量)及THF(20.00mL)。在0℃下搅拌混合物,随后逐滴添加丁基锂(1.76mL,27.448mmol,2当量)。在0℃下搅拌所得溶液1hr且逐滴添加二甲氨基乙醇(1.25g,14.023mmol,1.50当量)。将所得溶液在0℃下再搅拌1hr,冷却至-78℃且逐滴添加氯化三丁基锡(4.56g,13.998mmol,1.5当量)。在-78℃下再搅拌所得溶液1h。随后通过添加水来淬灭反应物。用3×30mL乙酸乙酯萃取所得混合物,且将有机层合并,且经无水硫酸钠干燥并真空浓缩。由此产生400mg(10.82%)呈固体的4,5-二甲基-2-(三丁基锡烷基)吡啶。LCMS(ES)[M+1]+m/z:398。
步骤2
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入4,5-二甲基-2-(三丁基锡烷基)吡啶(400.48mg,1.011mmol,1.20当量)、N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(中间体II,250.00mg,0.842mmol,1.00当量)、Pd(PPh3)4(97.33mg,0.084mmol,0.10当量)、LiCl(35.71mg,0.842mmol,1.00当量)及甲苯(10.00mL)。在100℃下搅拌所得溶液16hr。将反应混合物冷却且浓缩。将残余物施加至硅胶柱上且用二氯甲烷/甲醇(10:1)洗脱。通过使用以下条件的制备型HPLC(2#SHIMADZU(HPLC-01))进一步纯化收集的粗产物:柱,Welch Xtimate C18,21.2*250mm,5um;移动相,水(0.05%TFA)及MeOH:ACN=1:1(17min内自10%相B达至60%)。由此产生68.3mg(22.06%)呈白色固体的N-(叔丁基)-2-((2-(4,5-二甲基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.37(s,1H),8.14(s,1H),7.72(s,1H),4.14(s,2H),3.27(s,3H),3.14(t,J=7.3Hz,2H),2.80(t,J=7.8Hz,2H),2.34(s,3H),2.27(s,3H),2.03-1.92(m,2H),1.24(s,9H)。LCMS(ES)[M+1]+m/z:368.2
实施例1.87
合成N-(1-羟基-2-甲基丙-2-基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物61)
流程53描绘用于制备例示性化合物的合成途径。
流程53
向20mL小瓶中放入[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(中间体I,200mg,0.70mmol,1.0当量)、DMF(3.0mL)、2-氨基-2-甲基-1-丙醇(69mg,0.77mmol,1.1当量)及DIEA(455mg,3.52mmol,5.0当量)。之后在0℃下添加HATU(401mg,1.06mmol,1.5当量)。在室温下搅拌反应溶液1h。通过C18-120g柱,用CH3CN/H2O(1%NH4OH)(在12min内自5%至80%,流动速率,70mL/min,检测器,254nm)洗脱来直接纯化反应溶液。由此产生93.9mg(38%)呈白色固体的N-(1-羟基-2-甲基丙-2-基)-2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1H-NMR(300MHz,DMSO-d6,ppm):δ8.66(dd,J=4.7,1.8Hz,1H),8.33(dt,J=8.0,1.1Hz,1H),7.88(td,J=7.7,1.8Hz,1H),7.51(s,1H),7.44(ddd,J=7.5,4.8,1.2Hz,1H),4.82(t,J=6.0Hz,1H),4.16(s,2H),3.37(d,J=5.7Hz,2H),3.27(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.03-1.97(m,2H),1.17(s,6H)。LCMS(ES,m/z):[M+H]+:356.2。
实施例1.88
合成N-(1-羟基-2-甲基丙-2-基)-2-{甲基[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物62)
流程54描绘用于制备例示性化合物的合成途径。
流程54
步骤1
向250mL圆底烧瓶中放入2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(10.00g,52.899mmol,1.00当量)、NMP(100.00mL)、2-(甲基氨基)乙酸乙酯盐酸盐(8.13g,52.899mmol,1.00当量)及DIEA(13.67g,105.798mmol,2.00当量)。在60℃下搅拌所得溶液1hr。将混合物倒入200mL乙酸乙酯中。将有机层分离且用3×100ml水洗涤。使有机层经无水硫酸钠干燥且真空浓缩。将残余物施加至硅胶柱上且使用乙酸乙酯/石油醚(1:3)洗脱。将收集的洗脱份合并且浓缩。由此产生8.2g(57.47%)呈黄色固体的N-(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯。LCMS(ES)[M+1]+m/z 270。
步骤2
向250mL圆底烧瓶中放入N-(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯(8.00g,29.659mmol,1.00当量)、二噁烷(100.00mL)、4-甲基-2-(三丁基锡烷基)吡啶(13.60g,35.591mmol,1.20当量)及四(三苯基膦)钯(0)(3.43g,2.966mmol,0.10当量)。在110℃下搅拌所得溶液16hr。浓缩所得混合物。将残余物施加至硅胶柱上且使用乙酸乙酯/石油醚(1:3)洗脱。将收集的洗脱份合并且浓缩。由此产生7.5g(77.5%)呈黄色固体的N-甲基-N-(2-(4-甲基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸乙酯。LCMS(ES)[M+1]+m/z 327。
步骤3
向250mL圆底烧瓶中放入N-甲基-N-(2-(4-甲基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸乙酯(3.80g,11.642mmol,1当量)、四氢呋喃(30mL),water(30mL)及氢氧化锂(0.56g,23.284mmol,2.00当量)。在25℃下搅拌所得溶液2hr。浓缩所得混合物。用50mL水稀释所得溶液。用HCl(1mol/L)将溶液的pH值调节至4。通过过滤来收集沉淀的固体。由此产生3.4g(97.89%)呈灰白色油状物的N-甲基-N-(2-(4-甲基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸。LCMS(ES)[M+1]+m/z 299。
步骤4
向50mL圆底烧瓶中放入N-甲基-N-(2-(4-甲基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸(100.00mg,0.335mmol,1.00当量)、二甲基甲酰胺(4.00mL)、2-氨基-2-甲基-1-丙醇(29.88mg,0.335mmol,1.00当量)、HATU(191.17mg,0.503mmol,1.50当量)及DIEA(129.96mg,1.006mmol,3.00当量)。在25℃下搅拌所得溶液2hr。将粗反应混合物过滤且进行反相制备型HPLC(Prep-C18,20-45M,120g,Tianjin Bonna-Agela Technologies;经10min时段自25%MeCN/水至35%MeCN/水的梯度洗脱,水含有0.1%NH3H2O),得到呈黄色固体的N-(1-羟基-2-甲基丙-2-基)-2-{甲基[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(69.6mg,56.20%)。1H NMR(300MHz,DMSO-d6)δ8.61(d,J=5.0Hz,1H),8.28(s,1H),7.72(s,1H),7.46(d,J=4.9Hz,1H),4.83(s,1H),4.30(s,2H),3.32(s,5H),3.21(t,J=7.4Hz,2H),2.93(t,J=7.8Hz,2H),2.47(s,3H),2.11-1.97(m,2H),1.17(s,6H)。LCMS(ES)[M+1]+m/z 370.1。
实施例1.89
合成N-(4-羟基-2-甲基丁-2-基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物63)
流程55描绘用于制备例示性化合物的合成途径。
流程55
向20mL小瓶中放入[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(150mg,0.53mmol,1.0当量)、DMF(3.0mL)、3-氨基-3-甲基丁-1-醇(60mg,0.58mmol,1.10当量)及DIEA(341mg,2.64mmol,5.0当量)。之后在0℃下添加HATU(301mg,0.79mmol,1.5当量)。在室温下搅拌反应溶液1h。通过使用如下条件的制备型HPLC纯化反应溶液:C18-120g柱,CH3CN/H2O(0.5%NH4OH),15min内自5%达至80%,流动速率:70mL/min,检测器,254nm。由此产生86.5mg(44%)呈灰白色固体的N-(4-羟基-2-甲基丁-2-基)-2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1H-NMR(300MHz,DMSO-d6,ppm):δ8.67(ddd,J=4.8,1.8,0.9Hz,1H),8.32(dt,J=7.9,1.1Hz,1H),7.88(td,J=7.7,1.8Hz,1H),7.69(s,1H),7.44(ddd,J=7.5,4.8,1.3Hz,1H),4.40(t,J=4.8Hz,1H),4.14(s,2H),3.47-3.41(m,2H),3.26(s,3H),3.14(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.05-1.95(m,2H),1.76(t,J=6.9Hz,2H),1.23(s,6H)。LCMS(ES,m/z):[M+H]+:370.3。
实施例1.90
合成N-环戊基-2-{甲基[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物64)
用环戊胺替换2-氨基-2-甲基-1-丙醇,与化合物62类似地合成化合物64。1H NMR(300MHz,DMSO-d6)δ8.51(d,J=4.9Hz,1H),8.16-8.07(m,2H),7.31-7.23(m,1H),4.17(s,2H),4.06-3.95(m,1H),3.30-3.20(m,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.40(s,3H),2.03-1.93(m,2H),1.85-1.68(m,2H),1.70-1.30(m,6H)。LCMS(ES)[M+1]+m/z366.2。
实施例1.91
合成2-{甲基[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(3-甲基氧杂环戊-3-基)乙酰胺(化合物65)
用3-甲基氧杂环戊-3-胺替换2-氨基-2-甲基-1-丙醇,与化合物62类似地合成化合物65。1H NMR(300MHz,DMSO-d6)δ8.51(d,J=4.9Hz,1H),8.20(s,1H),8.16(d,J=1.8Hz,1H),7.27(dd,J=5.1,1.4Hz,1H),4.18(s,2H),3.80(d,J=8.7Hz,1H),3.77-3.67(m,2H),3.49(d,J=8.7Hz,1H),3.29(s,3H),3.16(t,J=7.4Hz,2H),2.82(t,J=7.8Hz,2H),2.40(s,3H),2.12-2.28(m,1H),1.81-2.02(m,2H),1.71-1.79(m,1H),1.31(s,3H)。LCMS(ES)[M+1]+m/z:382.3。
实施例1.92
合成N-(3-氟苯基)-2-{甲基[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物66)
用3-氟苯胺替换2-氨基-2-甲基-1-丙醇,与化合物62类似地合成化合物66。1HNMR(300MHz,DMSO-d6)δ10.49(s,1H),8.47(d,J=4.9Hz,1H),8.03(s,1H),7.65-7.55(m,1H),7.39-7.26(m,2H),7.25-7.17(m,1H),6.93-6.80(m,1H),4.40(s,2H),3.39(s,3H),3.22(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.18(s,3H),2.11-1.94(m,2H)。LCMS(ES)[M+1]+m/z 392.1。
实施例1.93
合成N-叔丁基-2-{甲基[2-(嘧啶-2-基)-5H,6H,7H-环戊并[b]吡啶-4-基]氨基}乙酰胺(化合物67)
流程56描绘用于制备例示性化合物的合成途径。
流程56
步骤1
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入2,4-二氯-5H,6H,7H-环戊并[b]吡啶(500.00mg,2.66mmol,1.00当量)、2-(三丁基锡烷基)嘧啶(1275.94mg,3.46mmol,1.30当量)、CsF(807.78mg,5.32mmol,2.00当量)、Pd(PPh3)4(307.25mg,0.26mmol,0.10当量)、CuI(50.64mg,0.26mmol,0.10当量)及DMF(10.00mL)。在110℃下搅拌所得溶液8h。将反应混合物冷却至室温。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridge PrepC18OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自30%相B达至60%);检测器,254nm。由此产生200mg(32.47%)呈棕色固体的2-[4-氯-5H,6H,7H-环戊并[b]吡啶-2-基]嘧啶。LCMS(ES)[M+H]+m/z:232。
步骤2
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入2-[4-氯-5H,6H,7H-环戊并[b]吡啶-2-基]嘧啶(150.00mg,0.65mmol,1.00当量)、N-叔丁基-2-(甲基氨基)乙酰胺(121.39mg,0.84mmol,1.30当量)、Pd(OAc)2(14.54mg,0.06mmol,0.10当量)、BINAP(80.63mg,0.13mmol,0.20当量)、Cs2CO3(421.90mg,1.29mmol,2.00当量)及二噁烷(8.00mL)。在100℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物(500mg):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%HCOOH)及CAN(11min内自20%相B达至50%);检测器,254nm。由此产生82.1mg(32.90%)呈黄色油状物的N-叔丁基-2-[甲基[2-(嘧啶-2-基)-5H,6H,7H-环戊并[b]吡啶-4-基]氨基]乙酰胺甲酸盐。1H-NMR(300MHz,DMSO-d6)δ8.91(d,J=4.8Hz,2H),8.17(s,1H),7.61(s,1H),7.57-7.45(m,2H),3.98(s,2H),3.09(s,3H),3.04(t,J=7.2Hz,2H),2.88(t,J=7.7Hz,2H),2.09-1.93(m,2H),1.27(s,9H)。LCMS(ES,m/z):[M+H]+:340.1。
实施例1.94
合成N-叔丁基-2-{甲基[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[b]吡啶-4-基]氨基}乙酰胺(化合物68)
流程57描绘用于制备例示性化合物的合成途径。
流程57
步骤1
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入2,4-二氯-5H,6H,7H-环戊并[b]吡啶(500.00mg,2.66mmol,1.00当量)、4-甲基-2-(三丁基锡烷基)吡啶(1321.01mg,3.46mmol,1.30当量)、Pd(PPh3)4(307.25mg,0.26mmol,0.10当量)及二噁烷(10.00mL)。在110℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自40%相B达至70%);检测器,254。由此产生300mg(46.11%)呈白色固体的2-[4-氯-5H,6H,7H-环戊并[b]吡啶-2-基]-4-甲基吡啶。LCMS(ES)[M+H]+m/z:245。
步骤2
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入2-[4-氯-5H,6H,7H-环戊并[b]吡啶-2-基]-4-甲基吡啶(200.00mg,0.82mmol,1.00当量)、N-叔丁基-2-(甲基氨基)乙酰胺(153.22mg,1.06mmol,1.30当量)、Pd(OAc)2(18.35mg,0.08mmol,0.10当量)、Cs2CO3(532.56mg,1.64mmol,2.00当量)、BINAP(101.78mg,0.16mmol,0.20当量)、二噁烷(8.00mL)。在100℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。通过使用以下条件的制备型HPLC纯化粗产物(0.5g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自40%相B达至70%);检测器,254nm。由此产生118.1mg(41.00%)呈白色固体的N-叔丁基-2-[甲基[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[b]吡啶-4-基]氨基]乙酰胺。1H-NMR(300MHz,DMSO-d6)δ8.46(d,J=4.9Hz,1H),8.16(d,J=1.8Hz,1H),7.56(s,1H),7.54(s,1H),7.19(dd,J=5.0,1.8Hz,1H),3.93(s,2H),3.06(s,3H),3.02(t,J=7.1Hz,2H),2.85(t,J=7.7Hz,2H),2.39(s,3H),2.08-1.95(m,2H),1.27(s,9H)。LCMS(ES,m/z):[M+H]+:353.2。
实施例1.95
合成N-[2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙基]-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物69)
流程58描绘用于制备例示性化合物的合成途径。
流程58
步骤1
向在惰性氮气氛围中吹扫及维持的250mL圆底烧瓶中放入3-((叔丁氧羰基)氨基)丙酸(7.56g,39.955mmol,1.00当量)、DCM(100.00mL)及CDI(6.48g,39.955mmol,1当量)。在室温下搅拌所得溶液2h。之后在室温下在搅拌下逐滴添加2-丙炔胺(2.20g,39.942mmol,1.00当量)。在室温下搅拌所得溶液过夜。浓缩所得混合物。将残余物施加至硅胶柱上且用PE/THF(50%THF)洗脱。由此产生3g(33.18%)呈灰白色固体的(3-氧代-3-(丙-2-炔-1-基氨基)丙基)氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z 227。
步骤2
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入(3-氧代-3-(丙-2-炔-1-基氨基)丙基)氨基甲酸叔丁酯(500.00mg,2.210mmol,1.00当量)、环丁胺(188.59mg,2.652mmol,1.20当量)、三氟甲烷磺酸锌(160.67mg,0.442mmol,0.20当量)及甲苯(30.00mL)。于油浴中在100℃下搅拌所得溶液过夜。用水浴将反应混合物冷却至室温。用K2CO3(10%)将溶液的pH值调节至8。用3×100mL乙酸乙酯萃取所得溶液,将有机层合并,经无水硫酸钠干燥,且浓缩。由此产生600mg(粗)呈黄色油状物的(2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙基)氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z 280。
步骤3
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入(2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙基)氨基甲酸叔丁酯(600.00mg,2.148mmol,1.00当量)、含HCl(气体)的EA(10.00mL)。在室温下搅拌所得溶液过夜。浓缩所得混合物。通过过滤分离固体且真空干燥。由此产生300mg(77.92%)呈黄色固体的2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙-1-胺。LCMS(ES)[M+1]+m/z 180。
步骤4
向100mL圆底烧瓶中放入N-甲基-N-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸(200.00mg,0.703mmol,1.00当量)、2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙-1-胺(151.32mg,0.844mmol,1.20当量)、HATU(294.21mg,0.774mmol,1.10当量)、DIEA(272.74mg,2.110mmol,3.00当量)及DCM(20.00mL)。在室温下搅拌所得溶液4hr。浓缩所得混合物。通过急骤制备型HPLC(Prep-C18,20-45M,120g,Tianjin Bonna-AgelaTechnologies;经10min时段自35%MeCN/水至60%MeCN/水的梯度洗脱,其中两种溶剂皆含有0.1%NH3H2O)纯化粗产物。由此产生100.6mg(32.10%)呈白色固体的N-(2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙基)-2-(甲基(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6,ppm)δ8.66(d,J=3.6Hz,1H),8.22-8.35(m,2H),7.86(td,J=7.7,1.9Hz,1H),7.49-7.38(m,1H),6.40(s,1H),4.41-4.56(m,1H),4.19(s,2H),3.25-3.39(m,2H),3.28(s,3H),3.15(t,J=7.4Hz,2H),2.82(t,J=7.9Hz,2H),2.70(t,J=7.3Hz,2H),2.45-2.23(m,4H),2.18(s,3H),1.87-2.05(m,2H),1.55-1.71(m,2H)。LCMS(ES)[M+1]+m/z 446.2。
实施例1.96
合成N-[5-(氮杂环庚-1-基)-1,3,4-噻二唑-2-基]-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物70)
流程59描绘用于制备例示性化合物的合成途径。
流程59
步骤1
向50mL圆底烧瓶中放入5-溴-1,3,4-噻二唑-2-胺(500mg,2.78mmol,1.0当量)、DMF(10.0mL)、K2CO3(1.15g,8.33mmol,3.0当量)及六亚甲基亚胺(276mg,2.78mmol,1.0当量)。于油浴中在80℃下搅拌混合物12h。冷却至室温后,将反应物用20mL水稀释且用3×20mL乙酸乙酯萃取。将合并的有机相用3×20ml盐水洗涤,经无水硫酸钠干燥,过滤,且减压浓缩滤液。通过含乙酸乙酯/石油醚(1:1)的硅胶柱纯化残余物。由此产生450mg(82%)呈粉色固体状5-(氮杂环庚-1-基)-1,3,4-噻二唑-2-胺。
步骤2
向20mL小瓶中放入5-(氮杂环庚-1-基)-1,3,4-噻二唑-2-胺(230mg,1.16mmol,1.1当量)、DMF(3.0mL)、[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(300mg,1.06mmol,1.0当量)及DIEA(682mg,5.28mmol,5.0当量)。之后在0℃下添加EDC.HCl(243mg,1.27mmol,1.2当量)及HOBt(171mg,1.27mmol,1.2当量)。在室温下搅拌混合物1h。通过使用如下条件的制备型HPLC纯化反应溶液:C18-120g柱,CH3CN/H2O(0.5%NH4OH),15min内自5%达至80%,流动速率:70mL/min,检测器,254nm。获得106.6mg(22%)呈灰白色固体的N-[5-(氮杂环庚-1-基)-1,3,4-噻二唑-2-基]-2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1H NMR(300MHz,DMSO-d6,ppm):δ12.19(br,1H),8.64(ddd,J=4.8,1.8,0.9Hz,1H),8.19(dt,J=7.9,1.1Hz,1H),7.77(td,J=7.7,1.8Hz,1H),7.41(ddd,J=7.5,4.7,1.2Hz,1H),4.50(s,2H),3.48(t,J=5.7Hz,4H),3.36(s,3H),3.20(t,J=7.2Hz,2H),2.84(t,J=7.8Hz,2H),2.06-1.96(m,2H),1.73-1.67(m,4H),1.50-1.46(m,4H)。LCMS(ES,m/z):[M+H]+:465.3。
实施例1.97
合成1-[2-(1,3-噻唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷(化合物94)
用4-(三丁基锡烷基)噻唑替换2-(三丁基锡烷基)吡啶,与化合物92类似地合成化合物94。1H NMR(400MHz,DMSO-d6)δ9.13(d,J=2.1Hz,1H),8.32(d,J=2.1Hz,1H),3.75(t,J=6.1Hz,4H),3.05(t,J=7.3Hz,2H),2.78(t,J=7.9Hz,2H),1.97(p,J=7.7Hz,2H),1.73(q,J=5.5Hz,4H),1.47(p,J=2.8Hz,4H)。LCMS(ES)[M+1]+m/z:301.2。
实施例1.98
合成3-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-1-苯基吡咯烷-2-酮(化合物95)
用3-氨基-1-苯基吡咯烷-2-酮替换2-吡啶基甲胺,与化合物73类似地合成化合物95。LCMS(ES+):(M+H)+=386.3。1H NMR(400MHz,DMSO-d6)δ8.65-8.45(m,1H),8.23-8.06(m,1H),7.79-7.56(m,3H),7.44-7.08(m,4H),5.48-5.17(m,1H),4.01-3.85(m,2H),3.24(s,5H),2.90-2.79(m,2H),2.44-2.27(m,2H),2.09-1.95(m,2H)。
实施例1.99
合成1-[2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷(化合物96)
用4-氯-2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)吡啶,与化合物92类似地合成化合物96。1H NMR(400MHz,甲醇-d4)δ8.59(d,J=5.3Hz,1H),8.30(d,J=2.0Hz,1H),7.50(dd,J=5.3,2.1Hz,1H),3.81(t,J=6.1Hz,4H),3.11(t,J=7.3Hz,2H),2.89(t,J=7.9Hz,2H),2.07(p,J=7.7Hz,2H),1.81(dq,J=9.2,4.0Hz,4H),1.51(m,4H)。LCMS(ES)[M+1]+m/z:329.3,331.4。
实施例1.100
合成1-[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚烷(化合物97)
用1-甲基-4-(三丁基锡烷基)-1H-咪唑替换2-(三丁基锡烷基)吡啶,与化合物92类似地合成化合物97。1H NMR(400MHz,甲醇-d4)δ7.86(d,J=1.3Hz,1H),7.73(d,J=1.3Hz,1H),3.88(t,J=6.1Hz,4H),3.80(s,3H),3.12(t,J=7.4Hz,2H),2.91(t,J=7.9Hz,2H),2.09(h,J=8.1Hz,2H),1.82(q,J=5.7Hz,4H),1.58(p,J=2.7Hz,4H)。LCMS(ES)[M+1]+m/z:298.2。
实施例1.101
合成2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-[1-(三氟甲基)环丙基]乙酰胺(化合物98)
流程60描绘用于制备例示性化合物的合成途径。
流程60
步骤1
向[(叔丁氧羰基)(甲基)氨基]乙酸(302.51mg;1.60mmol;1.00当量)于DMF(2.5mL)中的溶液中添加1-(三氟甲基)环丙-1-胺(200.00mg;1.60mmol;1.00当量),之后添加DIPEA(0.42mL;2.40mmol;1.50当量)及HATU(607.92mg;1.60mmol;1.00当量)。在室温下搅拌15h后,用水稀释,且用EtOAc萃取。将有机层合并,干燥,且浓缩,得到N-甲基-N-({[1-(三氟甲基)环丙基]氨甲酰基}甲基)氨基甲酸叔丁酯,其不经纯化即用于下一步骤中。LCMS(ES)[M+1]+m/z:297.5。
步骤2
向N-甲基-N-({[1-(三氟甲基)环丙基]氨甲酰基}甲基)氨基甲酸叔丁酯(0.47g;1.60mmol;1.00当量)于DCM(4mL)中的溶液中添加含4N HCl的二噁烷(4mL)。进一步搅拌混合物,浓缩,且冻干,得到2-[氯(甲基)氨基]-N-[1-(三氟甲基)环丙基]乙酰胺,其不经纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:197.3。
步骤3
向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(0.13g;0.70mmol;1.00当量)于AcCN(2mL)中的溶液中添加2-[氯(甲基)氨基]-N-[1-(三氟甲基)环丙基]乙酰胺(0.19g;0.80mmol;1.15当量)及三乙胺(0.29mL;2.10mmol;3.00当量)。在75℃下加热4h后,将混合物冷却且浓缩,用水稀释,且通过过滤收集所得沉淀物并干燥,得到2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-[1-(三氟甲基)环丙基]乙酰胺(200mg)。LCMS(ES)[M+1]+m/z:349.0,351.1。
步骤4
向2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-[1-(三氟甲基)环丙基]乙酰胺(50.00mg;0.20mmol;1.00当量)及2-(三丁基锡烷基)吡啶(190.01mg;0.52mmol;2.00当量)于甲苯(1mL)中的溶液中添加四(三苯基膦)钯(29.82mg;0.03mmol;0.10当量)。在115℃下加热混合物15h。将混合物冷却且浓缩,且通过制备型HPLC纯化粗残余物,得到2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-[1-(三氟甲基)环丙基]乙酰胺(49.8mg)。1H NMR(400MHz,DMSO-d6)δ9.05(s,1H),8.80(d,J=4.7Hz,1H),8.35(d,J=8.2Hz,1H),8.07(s,1H),7.70(s,1H),4.37(s,2H),3.44(s,3H),3.20(m,2H),3.00(t,J=7.9Hz,2H),2.11-2.03(m,2H),1.25-1.17(m,2H),0.96(s,2H)。LCMS(ES)[M+1]+m/z:392.0。
实施例1.102
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-[1-(三氟甲基)环丙基]乙酰胺(化合物99)
用4-甲氧基-2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)吡啶,与化合物98类似地合成化合物99。1H NMR(400MHz,DMSO-d6)δ9.04(s,1H),8.65(d,J=6.1Hz,1H),7.91(d,J=2.6Hz,1H),7.41(dd,J=6.2,2.6Hz,1H),4.35(s,2H),4.02(s,3H),3.40(s,3H),3.22(m,2H),2.96(t,J=7.9Hz,2H),2.11-1.99(m,2H),1.23-1.09(m,2H),0.96(s,2H)。LCMS(ES)[M+1]+m/z:421.7。
实施例1.103
合成N-叔丁基-2-{[2-(4-乙基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物100)
流程61描绘用于制备例示性化合物的合成途径。
流程61
步骤1
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入2-溴-4-乙基吡啶(500mg,2.68mmol,1.00当量)、二噁烷(5.0mL)、六甲基二锡烷(1.06g,3.22mmol,1.20当量)及Pd(dppf)Cl2(196mg,0.26mmol,0.10当量)。在100℃下搅拌混合物2h。将反应混合物冷却并用20mL H2O稀释且用3×10mL乙酸乙酯萃取。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。由此产生600mg呈棕色油状物的粗产物4-乙基-2-(三甲基锡烷基)吡啶,其不经进一步纯化即直接用于下一步骤中。LCMS(ES):[M+1]+m/z:272。
步骤2
向在惰性氮气氛围中吹扫及维持的50mL圆底烧瓶中放入N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(300mg,1.01mmol,1.00当量)、二噁烷(5.0mL)、4-乙基-2-(三甲基锡烷基)吡啶(409mg,1.51mmol,1.50当量)及Pd(dppf)Cl2(73mg,0.10mmol,0.10当量)。在100℃下搅拌混合物16h。将反应混合物冷却并用20mL H2O稀释且用3×10mL乙酸乙酯萃取。使合并的有机相经无水硫酸钠干燥,过滤,且浓缩滤液。通过使用以下条件的制备型HPLC纯化粗残余物:柱,Kinetex EVO C18柱,21.2*150,5um,移动相,水(0.1%FA)及CH3CN(15min内自10%相B达至50%),检测器,UV 254nm。获得29.6mg(7.9%)呈粉色固体的N-叔丁基-2-[[2-(4-乙基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.54(d,J=4.8Hz,1H),8.16(s,1H),7.69(s,1H),7.30(dd,J=5.1,1.7Hz,1H),4.16(s,2H),3.27(s,3H),3.15(t,J=7.5Hz,2H),2.82(t,J=7.8Hz,2H),2.72(q,J=7.5Hz,2H),2.08-1.91(m,2H),1.30-1.19(m,12H)。LCMS(ES)[M+1]+m/z:368.2。
实施例1.104
合成(2R)-N-叔丁基-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}内酰胺(化合物101)
流程62描绘用于制备例示性化合物的合成途径。
流程62
步骤1
将(2R)-2-[(叔丁氧羰基)(甲基)氨基]丙酸(0.5g;2.46mmol;1当量)溶解于二氯甲烷(20ml)中且于冰浴中冷却。随后添加叔丁胺(0.28mL;2.71mmol;1.1当量)、3-氧化六氟磷酸1-[双(二甲基氨基)亚甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓(HATU,1.03g;2.71mmol;1.1当量)及N,N-二异丙基乙胺(0.90mL;5.17mmol;2.1当量)。经20h将反应物搅拌至25℃且随后溶解于乙酸乙酯(100ml)、水(10ml)及碳酸氢钠溶液(50ml)中。分离各相,且用更多乙酸乙酯(100ml)萃取水相。将合并的有机物用氯化钠溶液(30ml)洗涤,经硫酸钠干燥,且蒸发。通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈白色固体的N-[(1R)-1-(叔丁基氨甲酰基)乙基]-N-甲基氨基甲酸叔丁酯(0.61g,96%)。LCMS(ES+):(M+Na)+=281.0。
步骤2
将N-{1-[(1-羟基-3-苯基丙-2-基)氨甲酰基]乙基}-N-甲基氨基甲酸叔丁酯(0.56g;1.66mmol;1当量)溶解于二氯甲烷(8ml)中且于冰浴中冷却。缓慢添加三氟乙酸(4ml)且经3h将反应物搅拌至25℃。蒸发反应物,且使残余物与甲苯共蒸发并高真空干燥,得到(2R)-N-叔丁基-2-(甲基氨基)丙酰胺;三氟乙酸,其直接用于下一步骤中。LCMS(ES+):(M+Na)+=159.0。
步骤3
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(400.00mg;2.12mmol;1.00当量)(Combi-Blocks)溶解于乙腈(7ml)中,且向其添加(2R)-N-叔丁基-2-(甲基氨基)丙酰胺;三氟乙酸(633.70mg;2.33mmol;1.10当量)及休尼格氏碱(1.84mL;10.58mmol;5.00当量)。在70℃下搅拌混合物15h,随后减压蒸发溶剂,且通过柱色谱(50%EtOAc/己烷)纯化残余物,得到(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙烯酰胺(480mg,73%)。LCMS(ES+):(M+H)+=310.9。
步骤4
将(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙酰胺(140.00mg;0.45mmol;1.00当量)溶解于1,4-二噁烷(3.5ml)中,且用Ar气体吹扫溶液。添加4-甲氧基-2-(三丁基锡烷基)吡啶(0.36g;0.90mmol;2.00当量)及四(三苯基膦)钯(52.05mg;0.05mmol;0.10当量)。将反应容器密封且在110℃下于热浴中搅拌15h。蒸发后,通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈白色固体的(2R)-N-叔丁基-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}内酰胺(67mg,39%)。LCMS(ES+):(M+H)+=384.4。1H NMR(400MHz,甲醇-d4)δ8.51(d,J=5.8Hz,1H),7.95(d,J=2.6Hz,1H),7.63(s,1H),7.09(dd,J=5.8,2.6Hz,1H),5.24(q,J=7.1Hz,1H),3.98(s,3H),3.30-3.15(m,5H),3.04-2.86(m,2H),2.21-2.01(m,2H),1.45(d,J=7.1Hz,3H),1.23(s,9H)。
实施例1.105
合成N-叔丁基-2-({2-[4-(二甲基氨基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物102)
流程63描绘用于制备例示性化合物的合成途径。
流程63
步骤1
向在惰性氮气氛围中吹扫及维持的100mL 3颈圆底烧瓶中放入乙醇胺(1.00g,16.371mmol,2.00当量)及THF(40.00mL)。之后,在10min内,在0℃下于搅拌下逐滴添加n-BuLi(13.00mL,138.006mmol,16.86当量)。在0℃下搅拌所得溶液0.5h。在5min内,在0℃下于搅拌下向其逐滴添加4-二甲基氨基吡啶(1.00g,8.185mmol,1.00当量)于THF(5mL)中的溶液。在0℃下搅拌所得溶液1h。在室温下搅拌所得溶液0.5h。在10min内,在-78℃下于搅拌下向混合物逐滴添加氯化三丁基锡(6.66g,20.460mmol,2.50当量)。随后在室温下搅拌所得溶液过夜。将所得溶液用50mL H2O稀释且用3×50mL二氯甲烷萃取。将有机层合并,经无水硫酸钠干燥,且浓缩。将残余物施加至硅胶柱上且使用乙酸乙酯/石油醚(20%-50%EA)洗脱。由此产生0.8g(23.77%)呈黄色油状物的N,N-二甲基-2-(三丁基锡烷基)吡啶-4-胺。LCMS(ES)[M+1]+m/z 413.2。
步骤2
向在惰性氩气氛围中吹扫及维持的40mL圆底烧瓶中放入N,N-二甲基-2-(三丁基锡烷基)吡啶-4-胺(418.00mg,1.016mmol,1.00当量)、N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(301.69mg,1.016mmol,1.00当量)、Pd(PPh3)4(117.46mg,0.102mmol,0.10当量)及二噁烷(10.00mL)。于油浴中在100℃下搅拌所得溶液24hr。浓缩所得混合物。将残余物施加至硅胶柱上且用二氯甲烷/甲醇(10%-30%MeOH)洗脱。通过急骤制备型HPLC(Prep-C18,20-45M,120g,Tianjin Bonna-Agela Technologies;经10min时段自20%MeCN/水至45%MeCN/水的梯度洗脱,其中两种溶剂皆含有0.1%FA)纯化收集的粗产物。由此产生44.9mg(11.55%)呈淡黄色固体的N-(叔丁基)-2-((2-(4-(二甲基氨基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺甲酸盐。1HNMR(300MHz,DMSO-d6,ppm)δ8.23(s,1H),8.21(d,J=6.0Hz,1H),7.68(s,1H),7.59(d,J=2.7Hz,1H),6.72(dd,J=6.2,2.8Hz,1H),4.17(s,2H),3.13(t,J=7.3Hz,2H),3.07(s,6H),2.82(t,J=7.7Hz,2H),1.89-2.08(m,2H),1.22(s,9H)。LCMS(ES)[M+1]+m/z 383.2。
实施例1.106
合成N-叔丁基-2-{甲基[2-(3-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物103)
流程64描绘用于制备例示性化合物的合成途径。
流程64
向在惰性氮气氛围中吹扫且维持的100mL圆底烧瓶中放入N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(800.00mg,2.695mmol,1.00当量)、3-甲基-2-(三丁基锡烷基)吡啶(1.23g,3.235mmol,1.20当量)、Pd(dppf)Cl2(197.22mg,0.270mmol,0.10当量)、CsF(409.44mg,2.695mmol,1.00当量)及二噁烷(20.00mL)。在120℃下搅拌所得溶液16hr。使反应混合物冷却。用3×50mL二氯甲烷萃取所得溶液。将有机层合并,经无水硫酸钠干燥,且真空浓缩。通过使用以下条件的制备型HPLC(制备型HPLC-002)纯化粗产物:柱,XBridge BEH130 Prep C18 OBD柱,19*150mm 5um 13nm;移动相,水(0.05%FA)及ACN(8min内自10%相B达至50%)。由此产生41.3mg(4.3%)呈粉色固体的N-叔丁基-2-[甲基[2-(3-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺甲酸盐。1HNMR(300MHz,DMSO-d6)δ8.41(d,J=4.7Hz,1H),8.19(s,1H),7.68(d,J=7.7Hz,1H),7.49(s,1H),7.31(dd,J=7.7,4.7Hz,1H),4.11(s,2H),3.18(s,3H),3.14(d,J=7.4Hz,2H),2.78(t,J=7.8Hz,2H),2.28(s,3H),2.05-1.95(m,2H),1.22(s,9H)。LCMS(ES)[M+1]+m/z:354.2。
实施例1.107
合成N-叔丁基-2-{甲基[2-(5-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物104)
流程65描绘用于制备例示性化合物的合成途径。
流程65
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(500mg,1.69mmol,1.0当量)、5-甲基-2-(三丁基锡烷基)吡啶(712mg,1.86mmol,1.1当量)、二噁烷(5.0mL)及Pd(PPh3)4(391mg,0.34mmol,0.2当量)。在100℃下搅拌混合物12h。随后浓缩以移除溶剂,且通过使用以下条件的制备型HPLC纯化粗产物:柱,Atlantis HILIC OBD柱,19*150mm*5um,移动相,水(0.1%FA)及CH3CN(8min内自5%相B达至35%),检测器,UV 254nm。由此产生48.3mg(7%)呈淡棕色固体的N-(叔丁基)-2-(甲基(2-(5-甲基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺甲酸盐。1HNMR(300MHz,DMSO-d6,ppm):δ8.50(d,J=2.1Hz,1H),8.26(d,J=8.1Hz,1H),8.18(s,1H),7.70-7.68(m,2H),4.13(s,2H),3.26(s,3H),3.14(t,J=7.2Hz,2H),2.81(t,J=7.8Hz,2H),2.36(s,3H),2.01-1.96(m,2H),1.24(s,9H)。LCMS(ES,m/z):[M+H]+:354.1。
实施例1.108
合成2-{甲基[2-(4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(1-甲基环戊基)乙酰胺(化合物105)
用1-甲基环戊胺替换2-氨基-2-甲基-1-丙醇,与化合物62类似地合成化合物105。1H NMR(300MHz,DMSO-d6,ppm)δ8.51(d,J=4.9Hz,1H),8.16(s,1H),7.76(s,1H),7.27(dd,J=5.2,1.7Hz,1H),4.16(s,2H),3.28(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.41(s,3H),2.07-1.89(m,4H),1.60-1.40(m,6H),1.28(s,3H)。LCMS(ES)[M+1]+m/z380.2。
实施例1.109
合成N-叔丁基-2-{甲基[2-(嘧啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物106)
流程66描绘用于制备例示性化合物的合成途径。
流程66
步骤1
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入2,4-二氯-5H,6H,7H-环戊并[b]吡啶(500.00mg,2.66mmol,1.00当量)、2-(三丁基锡烷基)嘧啶(1275.94mg,3.46mmol,1.30当量)、CsF(807.78mg,5.32mmol,2.00当量)、Pd(PPh3)4(307.25mg,0.26mmol,0.10当量)、CuI(50.64mg,0.26mmol,0.10当量)及DMF(10.00mL)。在110℃下搅拌所得溶液8h。将反应混合物冷却至室温。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridge PrepC18OBD柱,19cm,150mm,5um;移动相,水(0.1%NH4HCO3)及CAN(11min内自30%相B达至60%);检测器,254。由此产生200mg(32.47%)呈棕色固体的2-[4-氯-5H,6H,7H-环戊并[b]吡啶-2-基]嘧啶。LCMS(ES)[M+H]+m/z:232。
步骤2
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入2-[4-氯-5H,6H,7H-环戊并[b]吡啶-2-基]嘧啶(150.00mg,0.65mmol,1.00当量)、N-叔丁基-2-(甲基氨基)乙酰胺(121.39mg,0.84mmol,1.30当量)、Pd(OAc)2(14.54mg,0.06mmol,0.10当量)、BINAP(80.63mg,0.13mmol,0.20当量)、Cs2CO3(421.90mg,1.29mmol,2.00当量)及二噁烷(8.00mL)。在100℃下搅拌所得溶液过夜。将反应混合物冷却至室温且浓缩。通过使用以下条件的制备型HPLC纯化粗产物(500mg):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%HCOOH)及CAN(11min内自20%相B达至50%);检测器,254。由此产生82.1mg(32.90%)呈黄色油状物的N-叔丁基-2-[甲基[2-(嘧啶-2-基)-5H,6H,7H-环戊并[b]吡啶-4-基]氨基]乙酰胺甲酸盐。1HNMR(300MHz,DMSO-d6)δ8.91(d,J=4.8Hz,2H),8.17(s,1H),7.61(s,1H),7.57-7.45(m,2H),3.98(s,2H),3.09(s,3H),3.04(t,J=7.2Hz,2H),2.88(t,J=7.7Hz,2H),2.09-1.93(m,2H),1.27(s,9H)。LCMS(ES,m/z):[M+H]+:341.2。
实施例1.110
合成N-叔丁基-2-({2-[5-(2-羟乙基)-1,3-噻唑-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物107)
流程67描绘用于制备例示性化合物的合成途径。
流程67
步骤1
向250mL圆底烧瓶中放入4-(苯甲氧基)丁-1-醇(5.00g,27.74mmol,1.00当量)、DCM(100mL)及PCC(11.96g,55.47mmol,2.00当量)。将混合物在室温下搅拌16h,过滤,且减压浓缩滤液。残余物通过硅胶柱纯化且用乙酸乙酯/石油醚(1/10)洗脱。获得由此产生的2.5g(50%)呈无色固体的4-(苯甲氧基)丁醛。LCMS(ES)[M+1]+m/z:179。
步骤2
向100mL 3颈圆底烧瓶中放入4-(环己基甲氧基)丁-1-醇(2.50g,13.42mmol,1.00当量)、DMSO(30mL)。之后在0℃下于搅拌下逐滴添加溴三甲基硅烷(2.05g,13.42mmol,1.00当量)。在室温下搅拌所得溶液6h。将反应物用100mL H2O淬灭,用3×30mL乙酸乙酯萃取,将有机层合并并经无水硫酸钠干燥,过滤,且浓缩滤液。通过含乙酸乙酯/石油醚(1/10)的硅胶柱纯化残余物。由此产生1.5g(43.4%)呈淡棕色油状物的4-(苯甲氧基)-2-溴丁醛。LCMS(ES)[M+1]+m/z:257。
步骤3
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(600mg,2.02mmol,1.00当量)、DMA(6.0mL)、Zn(CN)2(474mg,4.04mmol,2.00当量)、Zn(264mg,4.04mmol,2.00当量)及Pd(dppf)Cl2(147mg,0.20mmol,0.10当量)。在100℃下搅拌混合物2h。使反应混合物冷却且过滤。将滤液用20mL H2O稀释,用3×20mL乙酸乙酯萃取,将有机层合并并经无水硫酸钠干燥,过滤,且浓缩滤液。通过含乙酸乙酯/石油醚(1/1)的硅胶柱纯化残余物。此产生550mg(95%)呈黄色固体的N-叔丁基-2-([2-氰基-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ7.64(s,1H),4.10(s,2H),3.18(s,3H),3.13(t,J=7.5Hz,2H),2.78(t,J=7.8Hz,2H),2.04-1.88(m,2H),1.27(s,9H)。LCMS(ES)[M+1]+m/z:288。
步骤4
向100mL圆底烧瓶中放入N-叔丁基-2-([2-氰基-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(530mg,1.84mmol,1.00当量)、DMF(6.0mL)、(NH4)2S(251mg,3.68mmol,2.00当量)及TEA(373mg,3.68mmol,2.00当量)。在室温下搅拌所得溶液0.5h。将反应溶液用20mL H2O稀释,用3×20mL乙酸乙酯萃取,将有机层合并并经无水硫酸钠干燥,过滤,且浓缩滤液。用30ml己烷洗涤粗产物。由此产生500mg(84.3%)呈黄色固体的N-叔丁基-2-([2-硫氨甲酰基-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ10.10(br,1H),9.45(br,1H),7.60(s,1H),4.01(s,2H),3.25(s,3H),3.12(t,J=7.5Hz,2H),2.79(t,J=7.8Hz,2H),2.04-1.88(m,2H),1.25(s,9H)。LCMS(ES)[M+1]+m/z:322。
步骤5
向100mL圆底烧瓶中放入N-叔丁基-2-([2-硫氨甲酰基-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(400mg,1.24mmol,1.00当量)、DMF(5.0mL)、DIEA(321mg,2.48mmol,2.00当量)及4-(苯甲氧基)-2-溴丁醛(383mg,1.49mmol,1.20当量)。在室温下搅拌所得溶液16h。将反应物用20mL H2O稀释,用3×20mL乙酸乙酯萃取,将有机层合并并经无水硫酸钠干燥,过滤,且浓缩滤液。通过含乙酸乙酯/石油醚(1/10)的硅胶柱纯化残余物。由此产生380mg(61%)呈棕色固体的2-[[2-([[4-(苯甲氧基)-1-氧代丁-2-基]硫基]甲酰亚氨基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-N-叔丁基乙酰胺。LCMS(ES)[M+1]+m/z:498。
步骤5
向100mL圆底烧瓶中放入2-[[2-([[4-(苯甲氧基)-1-氧代丁-2-基]硫基]甲酰亚氨基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-N-叔丁基乙酰胺(380mg,0.76mmol,1.00当量)及AcOH(4.0mL)。在100℃下搅拌混合物1h。将反应混合物冷却至室温,且用10mLH2O稀释。将溶液的pH值用NaHCO3(10%)调节至8,用3×10mL乙酸乙酯萃取,将有机层合并并经无水硫酸钠干燥,过滤,且浓缩滤液。通过含乙酸乙酯/石油醚(1/1)的硅胶柱纯化残余物。获得180mg(49%)呈棕色固体的2-[(2-[5-[2-(苯甲氧基)乙基]-1,3-噻唑-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-叔丁基乙酰胺。LCMS(ES)[M+1]+m/z:480。
步骤6
向在惰性氮气氛围中吹扫且维持的50mL 3颈圆底烧瓶中放入2-[(2-[5-[2-(苯甲氧基)乙基]-1,3-噻唑-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-叔丁基乙酰胺(180mg,0.37mmol,1.00当量)及DCM(3.0mL)。之后在-78℃下于搅拌下逐滴添加BBr3(1.8mL,1.80mmol,4.80当量)。在0℃下搅拌所得溶液2h。随后通过添加10mL水将反应物淬灭,且用3×5mL二氯甲烷萃取。将有机层合并,经无水硫酸钠干燥,过滤,且浓缩滤液。通过使用以下条件的制备型HPLC纯化粗产物:柱,Welch XB-C18,21.2*250mm,5um,移动相,水(0.05%NH4OH)及CH3CN(15min内自10%相B达至65%),检测器,UV 254nm。由此产生53.0mg(36.2%)呈白色固体的N-叔丁基-2-([2-[5-(2-羟乙基)-1,3-噻唑-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ7.68(s,1H),7.62(s,1H),4.91(t,J=5.1Hz,1H),4.14(s,2H),3.65(q,J=6.3Hz,2H),3.22(s,3H),3.10(t,J=7.5Hz,2H),2.98(t,J=6.3Hz,2H),2.79(t,J=7.8Hz,2H),2.06-1.90(m,2H),1.26(s,9H)。LCMS(ES)[M+1]+m/z:390.2。
实施例1.111
合成(2R)-N-环己基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物108)
步骤1
将(2R)-2-[(叔丁氧羰基)(甲基)氨基]丙酸(0.50g;2.46mmol;1.00当量)溶解于二氯甲烷(20ml)中且于冰浴中冷却。随后添加环己胺(0.31mL;2.71mmol;1.10当量)、3-氧化六氟磷酸1-[双(二甲基氨基)亚甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓(HATU,1.03g;2.71mmol;1.10当量))及休尼格氏碱(0.90mL;5.17mmol;2.10当量)。经20h将反应物搅拌至25℃且随后溶解于乙酸乙酯(100ml)、水(10ml)及碳酸氢钠溶液(50ml)中。分离各相,且用更多乙酸乙酯(100ml)萃取水相。将合并的有机物用氯化钠溶液(30ml)洗涤,经硫酸钠干燥,且蒸发。通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈白色固体的N-{1-[(1-羟基-3-苯基丙-2-基)氨甲酰基]乙基}-N-甲基氨基甲酸叔丁酯(0.7g,99%)。LCMS(ES+):(M+Na)+=307.0。
步骤2
将N-{1-[(1-羟基-3-苯基丙-2-基)氨甲酰基]乙基}-N-甲基氨基甲酸叔丁酯(0.56g;1.66mmol;1.00当量)溶解于二氯甲烷(8ml)中且于冰浴中冷却。缓慢添加三氟乙酸(4ml)且经3h将反应物搅拌至25℃。蒸发反应物,且使残余物与甲苯共蒸发并高真空干燥,得到(2R)-N-环己基-2-(甲基氨基)丙酰胺;三氟乙酸,其直接用于下一步骤中。
步骤3
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(420.00mg;2.22mmol;1.00当量)溶解于乙腈(7ml)中,且向其添加(2R)-N-环己基-2-(甲基氨基)丙酰胺;三氟乙酸(729.02mg;2.44mmol;1.10当量)及休尼格氏碱(1.93mL;11.11mmol;5.00当量)。在70℃下搅拌混合物15h,随后减压蒸发溶剂,且通过柱色谱(50%EtOAc/己烷)纯化残余物,得到(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙烯酰胺(480mg,73%)。LCMS(ES+):(M+H)+=336.9。
步骤4
将(2R)-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-环己基丙酰胺(150.00mg;0.45mmol;1.00当量)溶解于1,4-二噁烷(3.5ml)中,且用Ar气体吹扫溶液。添加2-(三丁基锡烷基)吡啶(0.29mL;0.89mmol;2.00当量)及四(三苯基膦)钯(51.46mg;0.04mmol;0.10当量)。密封反应容器且在110℃下于热浴中搅拌15h。蒸发后,通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈白色固体的(2R)-N-环己基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(132mg)。LCMS(ES+):(M+H)+=380.4.1H NMR(400MHz,DMSO-d6)δ8.82-8.56(m,1H),8.44-8.27(m,1H),8.27-8.07(m,1H),7.99-7.77(m,1H),7.57-7.36(m,1H),5.26-5.04(m,1H),3.65-3.50(m,1H),3.23-3.15(m,2H),3.09(s,3H),2.93-2.72(m,2H),2.11-1.89(m,2H),1.78-1.61(m,2H),1.61-1.47(m,3H),1.35-1.12(m,6H),1.06-0.89(m,2H)。
实施例1.112
合成(2R)-N-(3,3-二氟环丁基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物109)
通过用3,3-二氟环丁胺替换环己胺,与化合物108类似地合成化合物109。LCMS(ES+):(M+H)+=388.3。1H NMR(400MHz,DMSO-d6)δ8.82(d,J=7.1Hz,1H),8.72-8.66(m,1H),8.31(d,J=7.9Hz,1H),7.95-7.88(m,1H),7.51-7.43(m,1H),5.15(q,J=7.0Hz,1H),4.17-4.04(m,1H),3.24-3.14(m,2H),3.10(s,3H),2.95-2.58(m,5H),2.49-2.41(m,1H),2.09-1.90(m,2H),1.34(d,J=7.0Hz,3H)。
实施例1.113
合成N-叔丁基-2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物110)
流程68描绘用于制备例示性化合物的合成途径。
流程68
步骤2
于空气氛围下在室温下向5-溴-1H-吡唑并[3,4-c]吡啶(4.00g,20.200mmol,1.00当量)于DCM(32.00mL)、THF(32.00mL)及DMF(2.00mL)中的搅拌溶液中添加DHP(3.80g,45.175mmol,2.24当量)及对甲苯磺酸(0.35g,0.002mmol,0.10当量)。于空气氛围下在50℃下搅拌所得混合物12h。使混合物冷却至室温。减压浓缩所得混合物。将残余物溶解于10%NaHCO3(100mL)中。用EtOAc(3×100mL)萃取所得混合物。将合并的有机层用盐水(1×100mL)洗涤且经无水Na2SO4干燥。过滤后,减压浓缩滤液。由此产生呈黄色固体的5-溴-1-(氧杂环己-2-基)吡唑并[3,4-c]吡啶(3g,52.64%)。LCMS(ES)[M+1]+m/z:282。
步骤3
于氮气氛围下在100℃下搅拌2h后,向5-溴-1-(氧杂环己-2-基)吡唑并[3,4-c]吡啶(71.30mg,0.253mmol,1.5当量)及Sn2Me6(91.07mg,0.278mmol,1.65当量)于二噁烷(2.00mL)中的溶液中添加Pd(PPh3)4(19.5mg,0.017mmol,0.1当量)。将混合物冷却至室温。在室温下向以上混合物添加N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(中间体II,50.00mg,0.168mmol,1.00当量)、CsF(51.18mg,0.337mmol,2当量)及Pd(PPh3)4(19.5mg,0.017mmol,0.1当量)。于氮气氛围下在100℃下再搅拌所得混合物16h。减压浓缩所得混合物。残余物通过硅胶柱色谱纯化且用PE/THF(1:1)洗脱,得到呈黄色固体的N-叔丁基-2-[甲基([2-[1-(氧杂环己-2-基)吡唑并[3,4-c]吡啶-5-基]-5H,6H,7H-环戊并[d]嘧啶-4-基])氨基]乙酰胺(50mg,64.02%)。LCMS(ES)[M+1]+m/z:464。
步骤4
于空气氛围下在60℃下搅拌含N-叔丁基-2-[甲基([2-[1-(氧杂环己-2-基)吡唑并[3,4-c]吡啶-5-基]-5H,6H,7H-环戊并[d]嘧啶-4-基])氨基]乙酰胺(400.00mg,0.863mmol,1.00当量)的4N HCl(g)于MeOH(4.00mL,131.648mmol,152.57当量)中的溶液2h。将混合物冷却至室温。减压浓缩所得混合物。通过制备型HPLC纯化粗产物(500mg),得到呈白色固体的N-叔丁基-2-[甲基(2-[1H-吡唑并[3,4-c]吡啶-5-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺甲酸盐(76mg,23.21%)。1H NMR(300MHz,DMSO-d6)1H NMR(300MHz,DMSO-d6)δ13.71(br,3H),9.09(s,1H),8.81(d,J=1.2Hz,1H),8.28(s,1H),8.15(s,1H),7.77(s,1H),4.15(s,2H),3.30(s,3H),3.15(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.06-1.92(m,2H),1.22(s,9H)。LCMS(ES)[M+1]+m/z:380.2。
实施例1.114
合成2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-[1-(三氟甲基)环丙基]乙酰胺(化合物111)
通过用1-甲基-4-(三丁基锡烷基)-1H-咪唑替换2-(三丁基锡烷基)吡啶,与化合物98类似地合成化合物111。1H NMR(400MHz,DMSO-d6)δ9.15(s,1H),8.34(s,1H),8.22(s,1H),4.35(s,2H),3.80(s,3H),3.36(s,3H),3.14(s,2H),2.92(t,J=7.9Hz,2H),2.02(p,J=7.9Hz,2H),1.24-1.16(m,2H),0.98(s,2H)。LCMS(ES)[M+1]+m/z:395.2。
实施例1.115
合成(2R)-N-叔丁基-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物112)
用1-甲基-4-(三丁基锡烷基)-1H-咪唑替换而与化合物101类似地合成化合物112。1H NMR(400MHz,DMSO-d6)δ8.09(s,1H),8.02(s,1H),7.75(s,1H),5.17(q,J=7.0Hz,1H),3.75(s,3H),3.15(s,3H),3.24-3.01(m,3H),2.87-2.78(m,2H),2.06-1.90(m,1H),1.31(d,J=7.1Hz,3H),1.20(d,J=1.1Hz,9H)。LCMS(ES)[M+1]+m/z:357.4。
实施例1.116
合成N-叔丁基-2-({2-[4-(2-羟乙基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物113)
流程69描绘用于制备例示性化合物的合成途径。
流程69
步骤1
向在惰性氮气氛围中吹扫及维持的250mL 3颈圆底烧瓶中放入2-氯-4-甲基吡啶(10.0g,78.39mmol,1.0当量)及THF(100mL)。之后在-78℃下添加LDA(2M于THF中)(117.5mL,235.17mmol,3.0当量)。添加后,在-78℃下搅拌反应溶液2hr。向其添加碳酸二乙酯(13.9g,117.66mmol,1.50当量)。在室温下搅拌混合物3h。随后通过添加NH4Cl(水溶液)(200mL)将反应物淬灭且用3×100mL乙酸乙酯萃取。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。通过含乙酸乙酯/石油醚(4:1)的硅胶柱纯化残余物。由此产生10.0g(64%)呈黄色油状物的2-(2-氯吡啶-4-基)乙酸乙酯。LCMS(ES)[M+1]+m/z:200。
步骤2
向250mL 3颈圆底烧瓶中放入2-(2-氯吡啶-4-基)乙酸乙酯(10.0g,50.09mmol,1.0当量)及EtOH(100mL)。之后在0℃下分数批添加NaBH4(9.50g,251.10mmol,5.0当量)。添加后,在室温下搅拌混合物3h。随后通过添加水(300mL)将反应物淬灭且用3×100mL二氯甲烷萃取。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。由此产生7.5g(95%)呈黄色油状物的2-(2-氯吡啶-4-基)乙-1-醇,其不经进一步纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:158。
步骤3
向100mL圆底烧瓶中放入2-(2-氯吡啶-4-基)乙-1-醇(4.78g,30.33mmol,1.0当量)、DCM(40mL)、DHP(5.10g,60.63mmol,2.0当量)及TsOH(524mg,3.04mmol,0.1当量)。在室温下搅拌反应物2h。浓缩溶液以移除溶剂,且通过含乙酸乙酯/石油醚(1/3)的硅胶柱纯化残余物,得到2.0g(27%)呈无色油状物的2-氯-4-(2-((四氢-2H-吡喃-2-基)氧基)乙基)吡啶。LCMS(ES)[M+1]+m/z:242。
步骤4
向在惰性氮气氛围中吹扫及维持的50mL圆底烧瓶中放入2-氯-4-(2-((四氢-2H-吡喃-2-基)氧基)乙基)吡啶(800mg,3.31mmol,1.0当量)、二噁烷(10.0mL)、六甲基二锡烷(1.3g,3.97mmol,1.2当量)及Pd(PPh3)4(765mg,0.66mmol,0.2当量)。在100℃下搅拌混合物2h。冷却至室温后,反应溶液不经纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:372。
步骤5
向在惰性氮气氛围中吹扫及维持的40mL小瓶中放入4-(2-((四氢-2H-吡喃-2-基)氧基)乙基)-2-(三甲基锡烷基)吡啶(最后步骤的反应溶液)、二噁烷(10.0mL)、N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(中间体II,385mg,1.30mmol,0.6当量)及Pd(PPh3)4(500mg,0.43mmol,0.2当量)。在100℃下搅拌混合物12h。将混合物冷却且浓缩以移除溶剂,且通过含THF/PE(2/1)的硅胶柱纯化残余物,得到500mg(50%)呈黄色油状物的N-(叔丁基)-2-(甲基(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:468。
步骤6
向20mL小瓶中放入N-(叔丁基)-2-(甲基(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(184mg,0.39mmol,1.0当量)、甲醇(5.0mL)及对甲苯磺酸(68mg,0.39mmol,1.0当量)。在室温下搅拌反应溶液1h。通过使用以下条件的制备型HPLC纯化反应溶液:柱,Atlantis HILIC OBD柱,19*150mm*5um,移动相,含(0.5HCOOH)的水(10mmol/L)及MeOH:ACN=1:1(9min内自33%相B达至45%),检测器,UV254nm。由此产生89.2mg(59%)呈灰白色固体的N-(叔丁基)-2-((2-(4-(2-羟乙基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺甲酸盐。1H NMR(300MHz,DMSO-d6,ppm):δ8.53(d,J=4.8Hz,1H),8.24(br,1H),8.17(s,1H),7.70(s,1H),7.32(d,J=3.6Hz,1H),4.16(s,2H),3.70(t,J=6.6Hz,2H),3.27(s,3H),3.15(t,J=7.2Hz,2H),2.86-2.79(m,4H),2.04-1.94(m,2H),1.23(s,9H)。LCMS(ES,m/z):[M+H]+:384.2。
实施例1.117
合成(2R)-N-叔丁基-3-甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丁酰胺(化合物114)
流程70描绘用于制备例示性化合物的合成途径。
流程70
步骤1
将(2R)-2-[(叔丁氧羰基)氨基]-3-甲基丁酸(0.50g;2.30mmol;1.00当量)溶解于二氯甲烷(23ml)中且于冰浴中冷却。随后添加叔丁胺(0.27mL;2.53mmol;1.10当量)、3-氧化六氟磷酸1-[双(二甲基氨基)亚甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓(HATU,0.96g;2.53mmol;1.10当量)及休尼格氏碱(0.84mL;4.83mmol;2.10当量)。经20h将反应物搅拌至25℃且随后溶解于乙酸乙酯(100ml)、水(10ml)及碳酸氢钠溶液(50ml)中。分离各相,且用更多乙酸乙酯(100ml)萃取水相。将合并的有机物用氯化钠溶液(30ml)洗涤,经硫酸钠干燥,且蒸发。通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈白色固体的N-{1-[(1-羟基-3-苯基丙-2-基)氨甲酰基]乙基}-N-甲基氨基甲酸叔丁酯(0.6g,96%)。
将N-{1-[(1-羟基-3-苯基丙-2-基)氨甲酰基]乙基}-N-甲基氨基甲酸叔丁酯(0.56g;1.66mmol;1.00当量)溶解于二氯甲烷(7ml)中且于冰浴中冷却。缓慢添加三氟乙酸(3.7ml)且经3h将反应物搅拌至25℃。蒸发反应物,且使残余物与甲苯共蒸发并高真空干燥,得到(2R)-2-氨基-N-叔丁基-3-甲基丁酰胺;三氟乙酸,其直接用于下一步骤中。LCMS(ES+):(M+H)+=172.9。
步骤2
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(200.00mg;1.06mmol;1.00当量)溶解于乙腈(4ml)中,且向其添加(2R)-2-氨基-N-叔丁基-3-甲基丁酰胺;三氟乙酸(333.18mg;1.16mmol;1.10当量)及休尼格氏碱(0.92mL;5.29mmol;5.00当量)。在70℃下搅拌混合物15h,随后减压蒸发溶剂,且通过柱色谱(50%EtOAc/己烷)纯化残余物,得到(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)-3-甲基丁酰胺(266mg,77%)。LCMS(ES+):(M+H)+=324.9。1H NMR(400MHz,DMSO-d6)δ7.64(s,1H),6.85(d,J=8.3Hz,1H),4.32-4.24(m,1H),2.75-2.65(m,4H),2.09-1.96(m,3H),1.25(s,9H),0.92-0.86(m,6H)。
步骤3
将(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)-3-甲基丁酰胺(262mg;0.81mmol;1当量)溶解于N,N-二甲基甲酰胺(15ml)中且于冰浴中冷却。添加氢化钠(34mg;0.85mmol;1.05当量,60%)且搅拌混合物20min。随后添加碘甲烷(53μL;0.85mmol;1.05当量)且经1.5h将反应物搅拌至25℃。通过添加水(90ml)将反应物淬灭且随后用乙酸乙酯(2×100ml)萃取。将合并的有机相用水(30ml)及氯化钠溶液(30ml)洗涤,且随后经硫酸钠干燥。蒸发后,通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈薄膜的(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-3-甲基丁酰胺(255mg,93%)。MS(ES+):(M+H)+=339.3。
步骤4
将(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-3-甲基丁酰胺(147.00mg;0.43mmol;1.00当量)溶解于1,4-二噁烷(3.5ml)中,且用Ar气体吹扫溶液。添加2-(三丁基锡烷基)吡啶(0.28mL;0.87mmol;2.00当量)及四(三苯基膦)钯(50.13mg;0.04mmol;0.10当量)。密封反应容器且在110℃下于热浴中搅拌15h。蒸发后,通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈淡黄色固体的(2R)-N-叔丁基-3-甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丁酰胺(98mg,59%)。LCMS(ES+):(M+H)+=382.0。1H NMR(400MHz,DMSO-d6)δ8.72(ddd,J=4.8,1.8,0.9Hz,1H),8.41(dt,J=8.0,1.1Hz,1H),7.98-7.89(m,2H),7.52-7.46(m,1H),4.56(d,J=11.0Hz,1H),3.27-3.20(m,1H),3.14(s,3H),3.10-3.00(m,1H),2.99-2.88(m,1H),2.85-2.76(m,1H),2.36-2.25(m,1H),2.06-1.89(m,2H),1.18(s,9H),0.95(d,J=6.4Hz,3H),0.86(d,J=6.6Hz,3H)。
实施例1.118
合成(2S)-N-叔丁基-3-甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丁酰胺(化合物115)
通过用(2S)-2-[(叔丁氧羰基)氨基]-3-甲基丁酸替换(2R)-2-[(叔丁氧羰基)氨基]-3-甲基丁酸,与化合物114类似地合成化合物115。LCMS(ES+):(M+H)+=382.0。1H NMR(400MHz,DMSO-d6)δ8.73(ddd,J=4.8,1.8,0.9Hz,1H),8.45-8.40(m,1H),7.98-7.90(m,2H),7.51(ddd,J=7.5,4.8,1.2Hz,1H),4.57(d,J=11.0Hz,1H),3.28-3.21(m,1H),3.16(s,3H),3.10-3.00(m,1H),2.99-2.88(m,1H),2.86-2.76(m,1H),2.37-2.26(m,1H),2.15-1.91(m,2H),1.19(s,9H),0.95(d,J=6.5Hz,3H),0.86(d,J=6.6Hz,3H)。
实施例1.119
合成(2R)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-4-(甲基硫基)丁酰胺(化合物116)
通过用(2R)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸替换(2R)-2-[(叔丁氧羰基)氨基]-3-甲基丁酸,与化合物114类似地合成化合物116。LCMS(ES+):(M+H)+=414.0。1HNMR(400MHz,DMSO-d6)δ8.70(ddd,J=4.7,1.8,0.9Hz,1H),8.43-8.35(m,1H),7.97-7.88(m,2H),7.48(ddd,J=7.5,4.8,1.2Hz,1H),5.11(dd,J=8.9,6.2Hz,1H),3.26-3.17(m,1H),3.13-3.04(m,4H),2.97-2.87(m,1H),2.87-2.77(m,1H),2.48-2.36(m,2H),2.15-1.92(m,7H),1.20(s,9H)。
实施例1.120
合成(2S)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-4-(甲基硫基)丁酰胺(化合物117)
通过用(2S)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸替换(2R)-2-[(叔丁氧羰基)氨基]-3-甲基丁酸,与化合物114类似地合成化合物117。LCMS(ES+):(M+H)+=414.1。1HNMR(400MHz,DMSO-d6)δ8.72(ddd,J=4.8,1.8,0.9Hz,1H),8.45-8.36(m,1H),7.99-7.87(m,2H),7.51(ddd,J=7.5,4.7,1.2Hz,1H),5.13(dd,J=8.9,6.1Hz,1H),3.25-3.19(m,1H),3.15-3.05(m,4H),3.00-2.78(m,2H),2.48-2.37(m,2H),2.16-1.93(m,7H),1.20(s,9H)。
实施例1.121
合成(2R)-N-环己基-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物118)
流程71描绘用于制备例示性化合物的合成途径。
流程71
向(2R)-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-环己基丙酰胺(134.00mg;0.40mmol;1.00当量)及1-甲基-4-(三丁基锡烷基)-1H-咪唑(251.17mg;0.63mmol;2.00当量)于甲苯(2mL)中的溶液中添加四(三苯基膦)钯(45.97mg;0.04mmol;0.10当量)。将溶液在105℃下加热15h,冷却至室温,且浓缩以移除溶剂。通过制备型HPLC纯化残余物,得到(2R)-N-环己基-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙烯酰胺(135mg)。1H NMR(400MHz,DMSO-d6)δ8.15-8.05(m,2H),8.01(d,J=8.1Hz,1H),5.23(q,J=6.9Hz,1H),3.76(s,3H),3.52(s,1H),3.15(s,3H),3.24-3.03(m,2H),2.94-2.76(m,2H),1.99(ddt,J=20.4,13.0,5.5Hz,2H),1.72-1.62(m,2H),1.62-1.54(m,2H),1.51(d,J=12.3Hz,1H),1.33(d,J=7.0Hz,3H),1.30-1.12(m,3H),1.08(ddd,J=19.3,14.8,8.6Hz,2H)。LCMS(ES,m/z):[M+H]+:383.2。
实施例1.122
合成(2R)-N-环己基-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}内酰胺(化合物119)
流程72描绘用于制备例示性化合物的合成途径。
流程72
向(2R)-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-环己基丙酰胺(125.00mg;0.37mmol;1.00当量)及4-甲氧基-2-(三丁基锡烷基)吡啶(251.17mg;0.63mmol;2.00当量)于甲苯(2mL)中的溶液中添加四(三苯基膦)钯(42.88mg;0.04mmol;0.10当量)。将溶液在105℃下加热15h,冷却至室温,且浓缩以移除溶剂。通过制备型HPLC纯化残余物,得到(2R)-N-环己基-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}丙烯酰胺(62mg)。1H NMR(400MHz,DMSO-d6)δ8.54(d,J=5.8Hz,1H),8.11(d,J=8.0Hz,1H),7.91(d,J=2.6Hz,1H),7.16(dd,J=5.8,2.6Hz,1H),5.07(q,J=7.0Hz,1H),3.94(s,3H),3.53(d,J=6.6Hz,1H),3.25-3.17(m,1H),3.15(s,3H),3.15-3.05(m,1H),2.87(tdd,J=16.9,13.0,7.0Hz,2H),2.12-1.90(m,2H),1.71(s,1H),1.51(d,J=12.2Hz,1H),1.50(s,3H),1.34(d,J=7.1Hz,3H),1.20(t,J=9.7Hz,2H),1.16-1.06(m,1H),0.99(s,2H)。LCMS(ES,m/z):[M+H]+:410.1。
实施例1.123
合成(2S)-3-(叔丁氧基)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物120)
通过用(2S)-3-叔丁氧基-2-{[(9H-芴-9-基甲氧基)羰基]氨基}丙酸替换(2R)-2-[(叔丁氧羰基)氨基]-3-甲基丁酸,与化合物114类似地合成化合物120。MS(ES+):(M+H)+=426.1。1H NMR(400MHz,DMSO-d6)δ8.68(ddd,J=4.8,1.8,0.9Hz,1H),8.41-8.33(m,1H),7.94-7.86(m,1H),7.81(s,1H),7.46(ddd,J=7.5,4.7,1.2Hz,1H),5.00(dd,J=8.0,5.9Hz,1H),3.83-3.75(m,1H),3.73-3.65(m,1H),3.29-3.20(m,2H),3.18(s,3H),3.12-3.02(m,1H),2.93-2.74(m,2H),2.10-1.90(m,2H),1.19(s,9H),1.14(s,9H)。
实施例1.124
合成(2R)-3-(叔丁氧基)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物121)
通过用(2R)-3-叔丁氧基-2-{[(9H-芴-9-基甲氧基)羰基]氨基}丙酸替换(2R)-2-[(叔丁氧羰基)氨基]-3-甲基丁酸,与化合物114类似地合成化合物121。MS(ES+):(M+H)+=426.1。1H NMR(400MHz,DMSO-d6)δ8.69(ddd,J=4.7,1.8,0.9Hz,1H),8.41-8.33(m,1H),7.94-7.85(m,1H),7.81(s,1H),7.46(ddd,J=7.5,4.7,1.2Hz,1H),5.00(dd,J=7.9,5.9Hz,1H),3.82-3.76(m,1H),3.70(dd,J=9.5,8.0Hz,1H),3.26-3.20(m,1H),3.18(s,3H),3.12-3.02(m,1H),2.93-2.75(m,2H),2.10-1.90(m,2H),1.19(s,9H),1.14(s,9H)。
实施例1.125
合成N-叔丁基-2-[(2-{2H,3H-[1,4]间二氧杂环己烯并[2,3-c]吡啶-7-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物122)
流程73描绘用于制备例示性化合物的合成途径。
流程73
步骤1
向在惰性氮气氛围中吹扫及维持的250mL 3颈圆底烧瓶中放入2-溴-5-氟吡啶(9.80g,55.68mmol,1.00当量)及THF(100mL)。之后在-78℃下于搅拌下逐滴添加LDA(33.4mL,66.80mmol,1.20当量)。在-78℃下搅拌反应溶液0.5hr。在-78℃下于搅拌下向其逐滴添加碘(14.13g,55.68mmol,1.00当量)于THF(20mL)中的溶液且在-78℃下搅拌1.5hr。随后通过添加100mL NH4Cl(水溶液)将反应物淬灭且用3×50mL乙酸乙酯萃取。使合并的有机层经无水硫酸钠干燥,过滤,且减压浓缩滤液。通过含石油醚/THF(10/1)的硅胶柱纯化残余物,得到16.0g(95%)呈白色固体的2-溴-5-氟-4-碘吡啶。LCMS(ES)[M+1]+m/z:302。
步骤2
向250mL圆底烧瓶中放入2-溴-5-氟-4-碘吡啶(8.0g,26.50mmol,
1.00当量)、乙二醇(50.0mL)、NMP(50.0mL)及t-BuOK(5.95g,53.00mmol,2.0当量)。在65℃下搅拌反应物3h。将混合物冷却且用100mL H2O稀释,且用3×50mL乙酸乙酯萃取。使合并的有机层经无水硫酸钠干燥,过滤,且减压浓缩滤液。通过含石油醚/THF(3/1)的硅胶柱纯化残余物,得到4.9g(53.7%)呈灰白色固体的2-[(6-溴-4-碘吡啶-3-基)氧基]乙醇。LCMS(ES)[M+1]+m/z:344。
步骤3
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入2-[(6-溴-4-碘吡啶-3-基)氧基]乙醇(4.90g,14.24mmol,1.00当量)、异丙醇(50.00mL)、3,4,7,8-四甲基-1,10-啡啉(673mg,2.84mmol,0.20当量)、叔丁醇钾(3.20g,28.49mmol,2.00当量)及碘化铜(I)(542mg,2.84mmol,0.20当量)。在80℃下搅拌混合物2h。冷却至室温后,将反应溶液用50mLH2O稀释且用3×50mL二氯甲烷萃取。使合并的有机层经无水硫酸钠干燥,过滤,且减压浓缩滤液。通过含石油醚/THF(4/1)的硅胶柱纯化残余物,得到2.0G(65%)呈淡黄色固体的7-溴-2H,3H-[1,4]间二氧杂环己烯并[2,3-c]吡啶。LCMS(ES)[M+1]+m/z:216。
步骤4
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入7-溴-2H,3H-[1,4]间二氧杂环己烯并[2,3-c]吡啶(500mg,2.31mmol,1.00当量)、二噁烷(8.0mL)、六甲基二锡烷(909mg,2.77mmol,1.20当量)及Pd(PPh3)4(267mg,0.23mmol,0.10当量)。在100℃下搅拌混合物2h。将反应混合物冷却且用10mL H2O稀释,且用3×10mL乙酸乙酯萃取。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。获得600mg呈棕色油状物的粗产物7-(三甲基锡烷基)-2H,3H-[1,4]间二氧杂环己烯并[2,3-c]吡啶且不经纯化即用于下一步骤中。LCMS(ES)[M+1]+m/z:302。
步骤5
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入7-(三甲基锡烷基)-2H,3H-[1,4]间二氧杂环己烯并[2,3-c]吡啶(454mg,1.51mmol,1.50当量)、二噁烷(5.0mL)、N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(300mg,1.01mmol,1.00当量)及Pd(PPh3)4(116mg,0.10mmol,0.10当量)。在100℃下搅拌混合物16h。将反应混合物冷却且浓缩。通过含二氯甲烷/甲醇(10/1)的硅胶柱纯化残余物。通过使用以下条件的制备型HPLC进一步纯化收集的粗产物:柱,Atlantis HILIC OBD柱,19*150mm*5um,移动相,水(0.05%NH4OH)及CH3CN(15min内自20%相B达至45%,保持45%5min),检测器,UV 254nm。由此产生98.1mg(24.4%)呈白色固体的N-叔丁基-2-[(2-[2H,3H-[1,4]间二氧杂环己烯并[2,3-c]吡啶-7-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.17(s,1H),7.86(s,1H),7.69(s,1H),4.40-4.36(m,4H),4.10(s,2H),3.26(s,3H),3.12(t,J=7.5Hz,2H),2.79(t,J=7.8Hz,2H),2.02-1.95(m,2H),1.25(s,9H)。LCMS(ES)[M+1]+m/z:398.2。
实施例1.126
合成(2S)-N-叔丁基-3-羟基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物123)
流程74描绘用于制备例示性化合物的合成途径。
流程74
将(2S)-3-(叔丁氧基)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺及甲酸(62.5mg;0.13mmol;1当量)溶解于二氯甲烷(1ml)中且于冰浴中冷却。添加三氟乙酸(0.75mL;0.2mol/L;0.15mmol;1.13当量)(1ml)且在25℃下搅拌反应物3.5h。随后蒸发溶液,使残余物与甲苯共蒸发且通过反相色谱(Waters XSelect CSHC18柱,0-90%乙腈/0.1%甲酸水溶液梯度)纯化,得到呈灰白色固体的(2S)-N-叔丁基-3-羟基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(40mg,81%)。LCMS(ES+):(M+H)+=369.9。1H NMR(400MHz,DMSO-d6)δ8.79-8.74(m,1H),8.48(d,J=7.9Hz,1H),8.07-7.99(m,1H),7.87(s,1H),7.61(ddd,J=7.6,4.7,1.2Hz,1H),5.10(t,J=7.3Hz,1H),5.01(s,1H),3.91-3.81(m,2H),3.31-3.26(m,4H),3.17-3.10(m,1H),3.02-2.87(m,2H),2.15-1.96(m,2H),1.20(s,9H)。
实施例1.127
合成(2R)-N-叔丁基-3-羟基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物124)
流程75描绘用于制备例示性化合物的合成途径。
流程75
通过用(2R)-3-(叔丁氧基)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙烯酰胺替换(2S)-3-(叔丁氧基)-N-叔丁基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丙烯酰胺,与化合物123类似地合成化合物124。LCMS(ES+):(M+H)+=370.0。1H NMR(400MHz,DMSO-d6)δ8.88-8.81(m,1H),8.59(d,J=7.8Hz,1H),8.19-8.12(m,1H),7.89(s,1H),7.76(ddd,J=7.6,4.8,1.2Hz,1H),5.34-5.00(m,2H),3.92(d,J=7.1Hz,2H),3.45(s,3H),3.36-3.34(m,1H),3.23-3.16(m,1H),3.08-3.01(m,2H),2.20-2.02(m,2H),1.22(s,9H)。
实施例1.128
合成N-叔丁基-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物125)
流程76描绘用于制备例示性化合物的合成途径。
流程76
步骤1
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入4-溴-1-甲基咪唑(500mg,3.10mmol,1.00当量)、二噁烷(8.0mL)、六甲基二锡烷(1.22g,3.72mmol,1.20当量)及Pd(PPh3)4(358mg,0.31mmol,0.10当量)。在100℃下搅拌混合物4h。将反应混合物冷却且浓缩。由此产生600mg呈棕色油状物的粗产物1-甲基-4-(三甲基锡烷基)咪唑。LCMS(ES)[M+1]+m/z:247。
步骤2
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺(300mg,1.01mmol,1.00当量)、二噁烷(5.0mL)、1-甲基-4-(三甲基锡烷基)咪唑(371mg,1.51mmol,1.50当量)及Pd(PPh3)4(116mg,0.10mmol,0.10当量)。在100℃下搅拌混合物20h。将反应混合物冷却且浓缩以移除溶剂。通过含二氯甲烷/甲醇(10/1)的硅胶柱纯化残余物。通过具有以下条件的制备型HPLC进一步纯化产物:柱,Welch Xtimate C18,21.2*250mm,5um,移动相:水(10mmol/L NH4HCO3)及MeOH:CH3CN=1:1(15min内自25%相B达至65%);检测器,UV 254nm。由此产生47.0mg(13.5%)呈白色固体的N-叔丁基-2-[甲基[2-(1-甲基咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1H NMR(300MHz,DMSO-d6)δ7.73(d,J=1.5Hz,1H),7.67-7.52(m,2H),4.09(s,2H),3.69(s,3H),3.21(s,3H),3.06(t,J=7.5Hz,2H),2.73(t,J=7.8Hz,2H),2.02-1.86(m,2H),1.25(s,9H)。LCMS(ES)[M+1]+m/z:343.2。
实施例1.129
合成N-叔丁基-2-{乙基[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物126)
流程77描绘用于制备例示性化合物的合成途径。
流程77
步骤1
于空气氛围下在0℃下向叔丁胺(3.89g,53.186mmol,1.00当量)及K2CO3(7.34g,53.126mmol,1.00当量)于DCM(120.00mL)中的搅拌溶液中逐滴添加氯乙酰氯(6.00g,53.126mmol,1.00当量)。于空气氛围下在室温下搅拌所得混合物16h。在室温下用水淬灭反应物。用CH2Cl2(2×100mL)萃取所得混合物。将合并的有机层用盐水(1×100mL)洗涤,经无水Na2SO4干燥,且过滤。减压浓缩滤液,得到呈黄色固体的N-叔丁基-2-氯乙酰胺(4g,50.32%)。LCMS(ES)[M+1]+m/z:150。
步骤2
于空气氛围下在80℃下搅拌N-叔丁基-2-氯乙酰胺(4.00g,26.734mmol,1.00当量)及乙胺于EtOH(80mL)中的溶液16h。减压浓缩所得混合物。将所得混合物用水(50mL)稀释且用DCM:MeOH=10:1(3×100mL)萃取。将合并的有机层用盐水(1×100mL)洗涤,经无水Na2SO4干燥,且过滤。减压浓缩滤液,得到呈黄色固体的N-叔丁基-2-(乙基氨基)乙酰胺(3.3g,78.00%)。LCMS(ES)[M+1]+m/z:159。
步骤3
于空气氛围下在60℃下搅拌2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(3.00g,15.870mmol,1.00当量)、DIEA(6.15g,47.609mmol,3当量)及N-叔丁基-2-(乙基氨基)乙酰胺(3.01g,19.044mmol,1.20当量)于NMP(30.00mL,311.103mmol,19.60当量)中的溶液2h。将混合物冷却至室温。用EtOAc(3×100mL)萃取所得混合物。将合并的有机层用盐水(1×100mL)洗涤,经无水Na2SO4干燥,且过滤。减压浓缩滤液。通过硅胶柱色谱,用PE/EtOAc(1:1)洗脱来纯化残余物,得到呈白色固体的N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](乙基)氨基)乙酰胺(2.2g,44.60%)。LCMS(ES)[M+1]+m/z:311。
步骤4
向2-溴-4-甲氧基吡啶(453.68mg,2.413mmol,1.5当量)及2-叔丁基-1,1,1-三甲基二锡烷(906.82mg,2.654mmol,1.65当量)于二噁烷(2.00mL)中的溶液中添加Pd(PPh3)4(186mg,0.161mmol,0.1当量)。于氮气氛围下在100℃下搅拌2h后,将混合物冷却至室温。在室温下向以上混合物添加N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](乙基)氨基)乙酰胺(500.00mg,1.609mmol,1.00当量)、CsF(488.70mg,3.217mmol,2.00当量)及Pd(PPh3)4(186mg,0.161mmol,0.1当量)。于氮气氛围下在100℃下再搅拌所得混合物16h。将所得混合物冷却且减压浓缩。通过硅胶柱色谱,用PE/THF(1:1)洗脱来纯化残余物,得到呈黄色固体的N-叔丁基-2-[乙基[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺(89mg,13%)。1H NMR(300MHz,DMSO-d6)δ8.49(d,J=5.6Hz,1H),7.87(d,J=2.6Hz,1H),7.68(s,1H),7.16-6.82(m,1H),4.09(s,2H),3.90(s,3H),3.65(q,J=7.0Hz,2H),3.08(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.23-1.92(m,2H),1.23(s,9H),3.65(t,J=7.0Hz,3H)。LCMS(ES)[M+1]+m/z:384.1。
实施例1.130
合成N-(6-氟吡啶-3-基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物127)
流程78描绘用于制备例示性化合物的合成途径。
流程78
步骤1
向[(叔丁氧羰基)(甲基)氨基]乙酸(2.00g;10.57mmol;1.00当量)于DMF(15mL)中的溶液中添加6-氟-3-吡啶胺(1.18g;10.57mmol;1.00当量),之后添加休尼格氏碱(2.77mL;0.02mol;1.50当量)及HATU(4.02g;0.01mol;1.00当量)。在室温下搅拌15h后,用EtOAc萃取。将有机层合并,干燥,且浓缩,得到呈粗产物的(2-((6-氟吡啶-3-基)氨基)-2-氧代乙基)(甲基)氨基甲酸叔丁酯(5.6g)。用DCM(10mL)稀释粗产物,向其添加含4N HCl的二噁烷(10mL)。完成后,将混合物浓缩且用饱和NaHCO3稀释。用EtOAc萃取水层,将有机层合并,干燥,且浓缩,得到2-[氯(甲基)氨基]-N-(6-氟吡啶-3-基)乙酰胺(2.5g)。LCMS(ES)[M+1]+m/z:184。
步骤2
向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(1.00g;5.29mmol;1.00当量)于AcCN(15mL)中的溶液中添加三乙胺(1.48mL;10.58mmol;2.00当量)及2-[氯(甲基)氨基]-N-(6-氟吡啶-3-基)乙酰胺(1.74g;7.93mmol;1.50当量)。在80℃下加热15h后,将其浓缩并用饱和NaHCO3稀释,且用EtOAc萃取。将有机层合并,用盐水洗涤,干燥,且浓缩,得到粗产物,通过柱色谱(0至100%EtOAc)对其进行纯化,得到2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-氟吡啶-3-基)乙酰胺(1.78g)。LCMS(ES)[M+1]+m/z:336.0。
步骤3
向2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-氟吡啶-3-基)乙酰胺(95.00mg;0.28mmol;1.00当量)于甲苯(2mL)中的溶液中添加2-(三丁基锡烷基)吡啶(156.24mg;0.42mmol;1.50当量)及四(三苯基膦)钯(32.70mg;0.03mmol;0.10当量)。在105℃下加热过夜后,HPLC指示起始物质残留。浓缩混合物且添加DMF(1mL)、另外的四(三苯基膦)钯(32.70mg;0.03mmol;0.10当量)及2-(三丁基锡烷基)吡啶(156.24mg;0.42mmol;1.50当量)。在105℃下加热混合物5h。用水稀释且通过制备型HPLC进行纯化,得到N-叔丁基-2-{乙基[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(28.7mg)。1H NMR(400MHz,DMSO-d6)δ10.83(s,1H),8.81(d,J=4.9Hz,1H),8.47-8.40(m,2H),8.19-8.10(m,1H),8.05(t,J=7.5Hz,1H),7.71(dd,J=7.7,4.8Hz,1H),7.15(dd,J=8.8,3.2Hz,1H),4.69(s,2H),3.54(s,3H),3.04(t,J=7.9Hz,2H),2.49(m,2H),2.16-2.03(m,2H)。LCMS(ES)[M+1]+m/z:379.1。
实施例1.131
合成N-(6-氟吡啶-3-基)-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物128)
流程79描绘用于制备例示性化合物的合成途径。
流程79
向2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-氟吡啶-3-基)乙酰胺(95.00mg;0.28mmol;1.00当量)于DMF(1mL)中的溶液中添加4-甲氧基-2-(三丁基锡烷基)吡啶(168.99mg;0.42mmol;1.50当量)及四(三苯基膦)钯(32.70mg;0.03mmol;0.10当量)。在110℃下加热过夜后,将混合物冷却至室温且用水及AcCN稀释,且通过制备型HPLC进行纯化,得到N-(6-氟吡啶-3-基)-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(25.9mg)。1H NMR(400MHz,DMSO-d6)δ10.56(s,1H),8.45(d,J=5.7Hz,1H),8.39(d,J=3.3Hz,1H),8.12(td,J=8.4,7.9,2.7Hz,1H),7.77(d,J=2.6Hz,1H),7.13(dt,J=8.8,3.5Hz,1H),7.05(dd,J=5.7,2.6Hz,1H),4.44(s,2H),3.79(s,3H),3.21(t,J=7.4Hz,2H),3.11(t,J=7.3Hz,1H),2.85(t,J=7.9Hz,3H),2.72(t,J=7.9Hz,1H),2.04(d,J=11.3Hz,2H)。LCMS(ES)[M+1]+m/z:409.2。
实施例1.132
合成N-(6-氟吡啶-3-基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物129)
流程80描绘用于制备例示性化合物的合成途径。
流程80
向2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-氟吡啶-3-基)乙酰胺(95.00mg;0.28mmol;1.00当量)于DMF(1mL)中的溶液中添加1-甲基-4-(三丁基锡烷基)-1H-咪唑(157.52mg;0.42mmol;1.50当量)及四(三苯基膦)钯(32.70mg;0.03mmol;0.10当量)。在110℃下加热过夜后,将混合物冷却至室温且用水及AcCN稀释。通过制备型HPLC对混合物进行纯化,得到N-(6-氟吡啶-3-基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺。1H NMR(400MHz,DMSO-d6)δ10.86(s,1H),10.76(s,1H),8.47(s,1H),8.30(s,1H),8.18(s,2H),7.16(dd,J=8.8,3.2Hz,1H),4.62(d,J=4.0Hz,2H),3.75(s,4H),3.19(s,1H),2.91(t,J=7.9Hz,2H),2.78(s,1H),2.09-1.97(m,2H)。LCMS(ES)[M+1]+m/z:382.2。
实施例1.133
合成(3R)-3-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-1-苯基吡咯烷-2-酮(化合物130)
流程81描绘用于制备例示性化合物的合成途径。
流程81
步骤1
将(2R)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸(0.50g;2.01mmol;1.00当量)溶解于DCM(20ml)中。使混合物在冰水浴中冷却,且添加HATU(0.84g;2.21mmol;1.10当量)、休尼格氏碱(0.73mL;4.21mmol;2.10当量)及苯胺(0.20mL;2.21mmol;1.10当量)。在0℃至rt下搅拌15h后,将混合物用水稀释且用EtOAc萃取。将合并的有机相用盐水洗涤,干燥,且浓缩。通过柱色谱(己烷/EtOAc=3:1)纯化残余物,得到呈固体的N-[(1R)-3-(甲基硫基)-1-(苯基氨甲酰基)丙基]氨基甲酸叔丁酯(0.58g,89%)。LCMS(ES+):(M+Na)+=347.1。
步骤2
将N-[(1R)-3-(甲基硫基)-1-(苯基氨甲酰基)丙基]氨基甲酸叔丁酯(0.58g;1.78mmol;1当量)溶解于碘甲烷(2.66mL;43mmol;24当量)中且在25℃下搅拌溶液。19h后,将残余物真空干燥且直接用于下一步骤中。LCMS(ES+):(M+H)+=338.8。
步骤3
将碘化N-[(1R)-3-(二甲基锍基)-1-(苯基氨甲酰基)丙基]氨基甲酸叔丁酯(0.83g;1.78mmol;1当量)悬浮于四氢呋喃(35ml)中且于冰浴中冷却。缓慢地逐滴添加双(三甲基硅基)氨基化锂(1.78mL;1mol/L;1.78mmol;1当量)。在0℃下搅拌3h后,缓慢添加氯化铵溶液(10ml)。蒸发溶剂且将剩余物溶解于二氯甲烷(100ml)及碳酸氢钠溶液(50ml)中。分离各相,用二氯甲烷(2×50ml)萃取水相,且使合并的有机相经硫酸钠干燥。蒸发后,通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈白色固体的N-[(3R)-2-氧代-1-苯基吡咯烷-3-基]氨基甲酸叔丁酯(0.41g,82%)。MS(ES+):(M+Na)+=299.0。1H NMR(400MHz,氯仿-d)δ7.67-7.60(m,2H),7.42-7.34(m,2H),7.21-7.14(m,1H),5.28-5.17(m,1H),4.41-4.27(m,1H),3.85-3.76(m,2H),2.85-2.74(m,1H),2.06-1.93(m,1H),1.47(s,9H)。
步骤4
将N-[(3R)-2-氧代-1-苯基吡咯烷-3-基]氨基甲酸叔丁酯(0.41g;1.48mmol;1当量)溶解于二氯甲烷(5ml)中且于冰浴中冷却。缓慢添加三氟乙酸(2.5mL)且在25℃下搅拌反应物。1.5h后,蒸发反应物,使残余物与甲苯共蒸发且随后高真空干燥,得到(3R)-3-氨基-1-苯基吡咯烷-2-酮;三氟乙酸。
步骤5
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(0.25g;1.32mmol;1.00当量)溶解于乙腈(4.5ml,无水)中,且向溶液中添加(3R)-3-氨基-1-苯基吡咯烷-2-酮;三氟乙酸(0.42g;1.45mmol;1.10当量)及休尼格氏碱(1.15mL;6.61mmol;5.00当量)(无水)。在约70℃下搅拌20h后,冷却混合物且蒸发溶剂,通过柱色谱(己烷/EtOAc=1:1)纯化残余物,得到(3R)-3-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)-1-苯基吡咯烷-2-酮(170mg,39%)。LCMS(ES+):(M+H)+=342.9。
步骤6
将(3R)-3-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)-1-苯基吡咯烷-2-酮(170.00mg;0.52mmol;1.00当量)溶解于DMF(3ml)中且于冰浴中冷却。添加氢化钠(62.04mg;1.55mmol;3.00当量),且于冰浴中搅拌混合物30min,之后添加碘甲烷(96.56μL;1.55mmol;3.00当量)。在室温下搅拌1.5h后,将混合物用水稀释且用EtOAc萃取。将合并的有机相用盐水洗涤,干燥,且浓缩。通过柱色谱(己烷/EtOAc=1:1)纯化残余物,得到(3R)-3-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-苯基吡咯烷-2-酮(161mg,91%)。LCMS(ES+):(M+H)+=342.9。
步骤7
将(3R)-3-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-苯基吡咯烷-2-酮(100.00mg;0.29mmol;1.00当量)溶解于1,4-二噁烷(2.4ml)中且用Ar气体吹扫。添加2-(三丁基锡烷基)吡啶(0.19mL;0.58mmol;2.00当量)及四(三苯基膦)钯(33.71mg;0.03mmol;0.10当量),且在108℃下于热浴中搅拌混合物20h。蒸发溶剂,将残余物溶解于乙腈中,过滤,且通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化,得到呈白色固体的(3R)-3-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-1-苯基吡咯烷-2-酮(64mg,57%)。LCMS(ES+):(M+H)+=386.0。1H NMR(400MHz,DMSO-d6)δ8.57(dd,J=4.8,1.8Hz,1H),8.17(d,J=7.9Hz,1H),7.75-7.68(m,2H),7.67-7.58(m,1H),7.43-7.34(m,3H),7.20-7.12(m,1H),5.46-5.25(m,1H),4.00-3.82(m,2H),3.27-3.22(m,5H),2.86(dd,J=8.7,7.0Hz,2H),2.45-2.30(m,2H),2.07-1.97(m,2H)。
实施例1.134
合成(3S)-3-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-1-苯基吡咯烷-2-酮(化合物131)
通过用(2S)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸替换(2R)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸,与化合物130类似地合成化合物131。LCMS(ES+):(M+H)+=386.0。1H NMR(400MHz,DMSO-d6)δ8.57(dd,J=4.9,1.8Hz,1H),8.17(d,J=7.9Hz,1H),7.74-7.68(m,2H),7.66-7.57(m,1H),7.43-7.33(m,3H),7.19-7.12(m,1H),5.44-5.26(m,1H),3.92(dtd,J=18.6,9.5,7.4Hz,2H),3.26-3.21(m,5H),2.86(dd,J=8.7,7.0Hz,2H),2.47-2.29(m,2H),2.08-1.98(m,2H)。
实施例1.135
合成(3R)-3-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-1-苯基吡咯烷-2-酮(化合物132)
流程82描绘用于制备例示性化合物的合成途径。
流程82
将(3R)-3-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-苯基吡咯烷-2-酮(60mg;0.18mmol;1当量)溶解于1,4-二噁烷(2ml)中且用Ar气体吹扫。添加4-甲氧基-2-(三丁基锡烷基)吡啶(0.14g;0.35mmol;2当量)及随后的四(三苯基膦)钯(20mg;0.02mmol;0.1当量),且在108℃下于热浴中搅拌混合物20h。蒸发溶剂,将残余物溶解于乙腈中,过滤,且通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化,得到呈白色固体的(3R)-3-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-1-苯基吡咯烷-2-酮(25mg,35%)。LCMS(ES+):(M+H)+=415.9。1HNMR(400MHz,DMSO-d6)δ8.37(d,J=5.6Hz,1H),7.72(d,J=2.6Hz,1H),7.71-7.65(m,2H),7.41-7.33(m,2H),7.18-7.11(m,1H),6.97(dd,J=5.6,2.6Hz,1H),5.40(s,1H),3.92(dtd,J=16.7,9.4,7.3Hz,2H),3.78(s,3H),3.24-3.19(m,5H),2.84(td,J=7.5,1.6Hz,2H),2.48-2.29(m,2H),2.06-1.97(m,2H)。
实施例1.136
合成N-(2-羟乙基)-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物133)
流程83描绘用于制备例示性化合物的合成途径。
流程83
步骤1
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入2-溴-4-甲氧基吡啶(500.00mg,2.659mmol,1.00当量)、六甲基二锡烷(1045.49mg,3.191mmol,1.20当量)、Pd(dppf)Cl2(194.58mg,0.266mmol,0.1当量)及二噁烷(20.00mL)。在100℃下搅拌所得溶液4hr。将溶液冷却且随后直接用于下一步骤中。LCMS(ES)[M+1]+m/z:274。
步骤2
向在惰性氮气氛围中吹扫且维持的100mL圆底烧瓶中放入4-甲氧基-2-(三丁基锡烷基)吡啶(590.48mg,1.483mmol,1.00当量)、2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸乙酯(400.00mg,1.483mmol,1.00当量)、Pd(dppf)Cl2(108.51mg,0.148mmol,0.10当量)及二噁烷(20.00mL)。在100℃下搅拌所得溶液16hr。使反应混合物冷却。用3×30mL乙酸乙酯萃取所得溶液且将有机层合并,经无水硫酸钠干燥并真空浓缩。将残余物施加至硅胶柱上且用二氯甲烷/甲醇(10:1)洗脱。由此产生300mg(59.08%)呈棕色油状物的N-(2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯。LCMS(ES)[M+1]+m/z:343。
步骤3
向50mL圆底烧瓶中放入N-(2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯(300.00mg,0.876mmol,1.00当量)、乙醇胺(64.22mg,1.051mmol,1.20当量)、AlCl3(11.68mg,0.088mmol,0.10当量)及甲苯(20.00mL)。在90℃下搅拌所得溶液16hr。使反应混合物冷却。用3×30mL乙酸乙酯萃取所得溶液且将有机层合并,经无水硫酸钠干燥并真空浓缩。通过使用以下条件的制备型HPLC(2#SHIMADZU(HPLC-01))纯化粗产物:柱,Atlantis HILIC OBD柱,19*150mm*5um;移动相,水(0.05%NH3H2O)及ACN(8min内自5%相B达至18%)。由此产生47.2mg(15.07%)呈白色固体的N-(2-羟乙基)-2-((2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1HNMR(300MHz,DMSO-d6)δ8.48(d,J=5.7Hz,1H),8.14(t,J=5.7Hz,1H),7.81(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),4.65(s,1H),4.20(s,2H),3.90(s,3H),3.44-3.35(m,2H),3.28(s,3H),3.21-3.11(m,4H),2.83(t,J=7.8Hz,2H),2.01-1.96(m,2H)。LCMS(ES)[M+1]+m/z:358.2。
实施例1.137
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(氧杂环己-4-基)乙酰胺(化合物134)
流程84描绘用于制备例示性化合物的合成途径。
流程84
在20℃下向[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酸(200mg,0.63mmol,1.0当量)、DIEA(411mg,3.18mmol,5.0当量)及HATU(1.21g,3.181mmol,5.0当量)于THF(10mL)中的搅拌溶液中分批添加氧杂环己-4-胺(321mg,3.18mmol,5.0当量)。在60℃下搅拌所得混合物5h。减压浓缩反应物。通过使用以下条件的急骤制备型HPLC(IntelFlash-1)纯化残余物:柱,C18;移动相,移动相:MeCN=5/1B:水流动速率:20mL/min柱:DAICEL CHIRALPAK IC,250*20mm,220nm梯度:50%B,20min;220nm。由此产生47mg(18.5%)呈白色固体的2-[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-N-(氧杂环己-4-基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.49(d,J=5.7Hz,1H),8.13(d,J=7.5Hz,1H),7.81(d,J=2.4Hz,1H),7.05(dd,J=2.4Hz,5.7Hz,1H),4.18(s,2H),3.89(s,3H),3.81-3.77(m,3H),3.31-3.28(m,2H),3.18-3.16(m,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.67-1.63(m,2H),1.47-1.39(m,2H)。LCMS(ES)[M+1]+m/z:398.2。
实施例1.138
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(氧杂环戊-3-基)乙酰胺(化合物135)
流程85描绘用于制备例示性化合物的合成途径。
流程85
步骤1
向在惰性氮气氛围中吹扫及维持的250mL 3颈圆底烧瓶中放入2-溴-4-甲氧基吡啶(7.0g,37.22mmol,1.0当量)及甲苯(70.0mL)。之后在-78℃下于搅拌下逐滴添加n-BuLi(16.4mL,41.0mmol,1.10当量)及i-PrMgBr(22.3mL,22.30mmol,0.60当量)。添加后,在-78℃下搅拌所得溶液2hr。在-78℃下向混合物中添加氯化三丁基锡(14.54g,44.68mmol,1.20当量)。在室温下搅拌反应物1h。随后通过添加200mL NH4Cl(水溶液)将反应物淬灭,且用3×100mL甲苯萃取。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。获得呈棕色油状物的16.0g粗产物4-甲氧基-2-(三丁基锡烷基)吡啶且不经纯化即用于下一步骤中。LCMS(ES)[M+1]+m/z:400。
步骤2
向用惰性氮气氛围吹扫且维持的250mL圆底烧瓶中放入2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸乙酯(7.0g,25.95mmol,1.00当量)、甲苯(100.0mL)、4-甲氧基-2-(三丁基锡烷基)吡啶(15.5g,38.92mmol,1.50当量)及Pd(PPh3)4(3.0g,2.59mmol,0.10当量)。在100℃下搅拌混合物16h。将反应混合物冷却且浓缩以移除溶剂。通过含二氯甲烷/甲醇(10/1)的硅胶柱纯化残余物。由此产生3.5g(39%)呈棕色油状物的2-[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酸乙酯。LCMS(ES)[M+1]+m/z:343。
步骤3
向100mL圆底烧瓶中放入2-[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酸乙酯(3.5g,10.22mmol,1.00当量)、THF(30.0mL)、H2O(10.0mL)及LiOH.H2O(857mg,20.44mmol,2.00当量)。在室温下搅拌反应溶液16h。通过过滤收集固体且在红外灯下干燥。获得呈黄色固体的2.5g(77%)N-(2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸。LCMS(ES)[M+1]+m/z:315。
步骤4
向50mL圆底烧瓶中放入N-(2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸(200mg,0.63mmol,1.00当量)、THF(5.0mL)、氧杂环戊-3-胺(83mg,0.95mmol,1.50当量)、DIEA(246mg,1.90mmol,3.00当量)及HATU(362mg,0.95mmol,1.50当量)。在50℃下搅拌混合物4h。将反应混合物冷却且浓缩以移除溶剂。将残余物用5mL MeOH稀释且通过使用以下条件的制备型HPLC纯化:柱,Welch Xtimate C18,21.2*250mm,5um,移动相,水(10mmol/L NH4HCO3)及MeOH:CH3CN=1:1(15min内自25%相B达至65%),检测器,UV254nm。由此产生30mg(12%)呈白色固体的2-[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-N-(氧杂环戊-3-基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.7Hz,1H),8.35(d,J=6.9Hz,1H),7.80(d,J=2.7Hz,1H),7.03(dd,J=5.7,2.7Hz,1H),4.33-4.22(m,1H),4.18(d,J=2.4Hz,2H),3.89(s,3H),3.80-3.67(m,2H),3.70-3.57(m,1H),3.43(dd,J=8.7,3.9Hz,1H),3.27(s,3H),3.16(t,J=7.5Hz,2H),2.82(t,J=7.8Hz,2H),2.13-1.91(m,3H),1.77-1.67(m,1H)。LCMS(ES)[M+1]+m/z:384.1。
实施例1.139
合成N-(1-羟基-2-甲基丙-2-基)-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物136)
流程86描绘用于制备例示性化合物的合成途径。
流程86
向100mL圆底烧瓶中放入N-(2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸(150.00mg,0.477mmol,1.00当量)、2-氨基-2-甲基-1-丙醇(85.07mg,0.954mmol,2.00当量)、HATU(272.16mg,0.716mmol,1.50当量)、DIEA(185.02mg,1.432mmol,3.00当量)及DCM(20.00mL)。在室温下搅拌所得溶液6hr。用3×20mL二氯甲烷萃取所得溶液且将有机层合并,经无水硫酸钠干燥并浓缩。通过使用以下条件的制备型HPLC(2#SHIMADZU(HPLC-01))纯化粗产物:柱,Atlantis HILIC OBD柱,19*150mm*5um;移动相,水(0.05%NH3H2O)及ACN(8min内自5%相B达至18%)。由此产生66.9mg(36.37%)呈白色固体的N-(1-羟基-2-甲基丙-2-基)-2-((2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.68(d,J=6.1Hz,1H),8.04(d,J=2.7Hz,1H),7.69(s,1H),7.44(dd,J=6.1,2.6Hz,1H),4.88(br,1H),4.35(s,2H),4.06(s,3H),3.52-3.41(s,3H),3.39-3.25(m,2H),3.22-3.17(m,2H),3.01(t,J=7.9Hz,2H),2.15-1.99(m,2H),1.17(s,6H)。LCMS(ES)[M+1]+m/z:386.2。
实施例1.140
合成N-环己基-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物137)
流程87描绘用于制备例示性化合物的合成途径。
流程87
向50mL圆底烧瓶中放入[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酸(100.00mg,0.318mmol,1.00当量)、二甲基甲酰胺(4mL)、环己胺(31.55mg,0.318mmol,1.00当量)、HATU(181.44mg,0.477mmol,1.50当量)及DIEA(123.35mg,0.954mmol,3.00当量)。在25℃下搅拌所得溶液2hr。将粗反应混合物过滤且进行反相制备型HPLC(Prep-C18,20-45M,120g,Tianjin Bonna-Agela Technologies;经10min时段自25%MeCN/水至35%MeCN/水的梯度洗脱,水含有0.1%NH3H2O),得到呈白色固体的N-环己基-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(65mg,51.66%)。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.98(d,J=8.0Hz,1H),7.81(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.7Hz,1H),4.16(s,2H),3.89(s,3H),3.54(s,1H),3.26(s,3H),3.14(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),1.89-2.07(m,2H),1.81-1.45(m,5H),1.12-1.32(m,5H)。LCMS(ES)[M+1]+m/z396.2。
实施例1.141
合成N-(3-氟苯基)-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物138)
流程88描绘用于制备例示性化合物的合成途径。
流程88
向50mL圆底烧瓶中放入[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酸(100.00mg,0.318mmol,1.00当量)、二甲基甲酰胺(4mL)、3-氟苯胺(35.35mg,0.318mmol,1.00当量)、HATU(181.44mg,0.477mmol,1.50当量)及DIEA(123.35mg,0.954mmol,3.00当量)。在25℃下搅拌所得溶液2hr。将粗反应混合物过滤且进行反相制备型HPLC(Prep-C18,20-45M,120g,Tianjin Bonna-Agela Technologies;经10min时段自25%MeCN/水至35%MeCN/水的梯度洗脱,水含有0.1%NH3H2O),得到呈白色固体的N-(3-氟苯基)-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(62mg,47.83%)。1H NMR(300MHz,DMSO-d6)δ10.43(s,1H),8.44(d,J=5.6Hz,1H),7.77(d,J=2.6Hz,1H),7.57(d,J=11.5Hz,1H),7.40-7.28(m,2H),6.99(dd,J=5.6,2.6Hz,1H),6.86-6.92(m,1H),4.43(s,2H),3.76(s,3H),3.37(s,3H),3.21(t,J=7.4Hz,2H),2.84(t,J=7.8Hz,2H),1.94-2.09(m,2H)。LCMS(ES)[M+1]+m/z408.2。
实施例1.142
合成N-(1-甲氧基-2-甲基丙-2-基)-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物139)
流程89描绘用于制备例示性化合物的合成途径。
流程89
向100mL圆底烧瓶中放入N-(2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸(150.00mg,0.493mmol,1.00当量)、1-甲氧基-叔丁胺(76.27mg,0.739mmol,1.5当量)、HATU(281.10mg,0.739mmol,1.5当量)、DIEA(191.09mg,1.479mmol,3当量)及THF(20.00mL)。在室温下搅拌所得溶液4hr。用3×20mL乙酸乙酯萃取所得溶液且将有机层合并,经无水硫酸钠干燥并真空浓缩。通过使用以下条件的制备型HPLC(2#SHIMADZU(HPLC-01))纯化粗产物:柱,Welch Xtimate C18,21.2*250mm,5um;移动相,水(0.05%FA)及MeOH:ACN=1:1(17min内自10%相B达至60%)。由此产生55.8mg(29.07%)呈灰白色固体的N-(1-羟基-2-甲基丙-2-基)-2-((2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.85(d,J=2.5Hz,1H),7.57(s,1H),7.04(dd,J=5.6,2.6Hz,1H),4.17(s,2H),3.90(s,3H),3.34(s,2H),3.25(s,3H),3.18(s,3H),3.14(t,J=7.3Hz,2H),2.82(t,J=7.9Hz,2H),2.09-1.92(m,2H),1.19(s,6H)。LCMS(ES)[M+1]+m/z:400.2。
实施例1.143
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(氧杂环己-4-基)乙酰胺(化合物140)
流程90描绘用于制备例示性化合物的合成途径。
流程90
步骤1
向50mL圆底烧瓶中放入[甲基(2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酸(200mg,0.46mmol,1.00当量)、THF(5mL)、HATU(266mg,0.70mmol,1.50当量)、DIEA(180mg,1.40mmol,3.00当量)及氧杂环己-4-胺(70mg,0.70mmol,1.50当量)。在60℃下搅拌所得溶液3hr。随后通过添加50mL水淬灭反应物。用3×100mL乙酸乙酯萃取所得溶液且将有机层合并,用3×100ml盐水洗涤,经无水硫酸钠干燥并真空浓缩。由此产生90mg(37.69%)呈黄色油状物的2-[甲基(2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(氧杂环己-4-基)乙酰胺。LCMS(ES)[M+1]+m/z 512。
步骤2
向50mL圆底烧瓶中放入2-[甲基(2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(氧杂环己-4-基)乙酰胺(90mg,0.17mmol,1.00当量)、MeOH(3mL)及TsOH(15mg,0.08mmol,0.5当量)。在25℃下搅拌所得溶液2hr。通过使用以下条件的制备型HPLC(Waters I)纯化粗产物:柱,XBridge Prep C18 OBD柱,5um,19*150mm;移动相,水(0.1%FA)及CH3CN(15min内自30%CH3CN达至42%);检测器,UV254nm。由此产生38.6mg(51.33%)呈黄色固体的2-([2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(氧杂环己-4-基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.29-8.05(m,2H),7.81(d,J=2.6Hz,1H),7.05(dd,J=5.7,2.6Hz,1H),4.24-4.09(m,4H),3.84-3.72(m,5H),3.36-3.30(m,2H),3.28(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.00(q,J=7.6Hz,2H),1.67(d,J=11.3Hz,2H),1.49-1.37(m,2H)。LCMS(ES)[M+1]+m/z 428.2。
实施例1.144
合成N-[(1R,2R)-2-羟基环己基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物141)
流程91描绘用于制备例示性化合物的合成途径。
流程91
向100mL圆底烧瓶中放入N-(2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸(150.00mg,0.477mmol,1.00当量)、2-氨基环己-1-醇(82.44mg,0.716mmol,1.50当量)、HATU(272.16mg,0.716mmol,1.5当量)、DIEA(185.02mg,1.432mmol,3当量)及DCM(20.00mL)。在4℃下搅拌所得溶液4hr。用3×20mL二氯甲烷萃取所得溶液且将有机层合并,于烘箱中减压干燥并真空浓缩。通过使用以下条件的制备型HPLC(2#SHIMADZU(HPLC-01))纯化粗产物:柱,Atlantis HILIC OBD柱,19*150mm*5um;移动相,水(0.05%NH3H2O)及ACN(8min内自5%相B达至18%)。由此产生95.2mg(48.48%)呈白色固体的N-((1R,2R)-2-羟基环己基)-2-((2-(4-甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.91(d,J=8.1Hz,1H),7.82(d,J=2.6Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),4.54(d,J=4.8Hz,1H),4.25(d,J=16.4Hz,1H),4.15(d,J=16.3Hz,1H),3.89(s,3H),3.48-3.36(m,1H),3.31-3.22(m,4H),3.14(t,J=4.7Hz,2H),2.82(t,J=7.9Hz,2H),2.03-1.93(m,2H),1.86-1.49(m,4H),1.32-1.05(m,4H)。LCMS(ES)[M+1]+m/z:412.3。
实施例1.145
合成N-环己基-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物142)
流程92描绘用于制备例示性化合物的合成途径。
流程92
向20mL小瓶中放入[甲基[2-(1-甲基咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸盐酸盐(150mg,0.46mmol,1.00当量)、DMF(3.0mL)、环己胺(51mg,0.51mmol,1.10当量)及DIEA(240mg,1.85mmol,4.00当量)。之后在0℃下添加HATU(264mg,0.69mmol,1.50当量)。在室温下搅拌反应溶液2h。通过使用如下条件的急骤制备型HPLC纯化粗产物:柱,C18-120g,CH3CN/H2O(0.05%NH4OH),12min内自10%达至80%,流动速率:70ml/min,检测器,UV 254nm。获得83.8mg(49%)呈白色固体的N-环己基-2-[甲基[2-(1-甲基咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1HNMR(300MHz,DMSO-d6,ppm):δ7.95(d,J=8.1Hz,1H),7.71(d,J=1.5Hz,1H),7.60(d,J=1.5Hz,1H),4.12(s,2H),3.69(s,3H),3.57-3.53(m,1H),3.21(s,3H),3.06(t,J=7.5Hz,2H),2.73(t,J=7.8Hz,2H),1.99-1.89(m,2H),1.68(t,J=10.8Hz,4H),1.54(d,J=12.3Hz,1H),1.27-1.07(m,5H)。LCMS(ES,m/z):[M+H]+:369.2。
实施例1.146
合成N-(1-羟基-2-甲基丙-2-基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物143)
流程93描绘用于制备例示性化合物的合成途径。
流程93
向20mL小瓶中放入[甲基[2-(1-甲基咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸盐酸盐(150mg,0.46mmol,1.00当量)、DMF(3.00mL)、2-氨基-2-甲基-1-丙醇(45mg,0.51mmol,1.10当量)及DIEA(240mg,1.85mmol,4.00当量)。之后在0℃下添加HATU(264mg,0.69mmol,1.50当量)。在室温下搅拌所得溶液2h。通过使用如下条件的急骤制备型HPLC纯化粗产物:柱,C18-120g,CH3CN/H2O(0.05%NH4OH),12min内自10%达至80%,流动速率:70ml/min,检测器,UV 254nm。获得102.8mg(62%)呈白色固体的N-(1-羟基-2-甲基丙-2-基)-2-[甲基[2-(1-甲基咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺。1H-NMR(300MHz,DMSO-d6,ppm):δ7.74(d,J=1.5Hz,1H),7.59(d,J=1.5Hz,1H),7.46(s,1H),4.93(br,1H),4.10(s,2H),3.69(s,3H),3.37(d,J=3.9Hz,2H),3.21(s,3H),3.07(t,J=7.5Hz,2H),2.73(t,J=7.8Hz,2H),1.99-1.89(m,2H),1.18(s,6H)。LCMS(ES,m/z):[M+H]+:359.2。
实施例1.147
合成N-环己基-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物144)
流程94描绘用于制备例示性化合物的合成途径。
流程94
步骤1
向在惰性氮气氛围中吹扫及维持的100mL圆底烧瓶中放入4-[2-(氧杂环己-2-基氧基)乙氧基]-2-(三甲基锡烷基)吡啶(2.00g,5.18mmol,1.00当量)、二噁烷(40.0mL,454mmol)、N-(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯(1.40g,5.180mmol,1.00当量)及Pd(PPh3)4(598mg,0.518mmol,0.10当量)的混合物。在100℃下搅拌所得溶液16小时。冷却后,浓缩溶液。将残余物施加至硅胶柱上,用二氯甲烷/甲醇(10/1)洗脱。由此产生826mg(34.93%)呈棕色粗油状物的N-甲基-N-(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸乙酯。LCMS(ES)[M+1]+m/z:457。
步骤2
向20mL小瓶中放入N-甲基-N-(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸乙酯(800mg,1.75mmol,1.00当量)、MeOH(8.00mL)、H2O(2.00mL)及LiOH(83.9mg,3.50mmol,2.00当量)的混合物。在室温下搅拌所得溶液2小时。将粗反应混合物过滤且进行反相制备型MPLC(Prep-C18,20-45mM,120g,Tianjin Bonna-Agela Technologies;经12min时段自5%MeCN/水达至27%MeCN/水的梯度洗脱,其中两种溶剂皆含有0.1%NH3H2O)。由此产生568mg(75.65%)呈红色固体的N-甲基-N-(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸。LCMS(ES)[M+1]+m/z:429。
步骤3
向8mL小瓶中放入N-甲基-N-(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸(150mg,0.350mmol,1.00当量)、DMF(2.00mL)、环己胺(34.7mg,0.350mmol,1.00当量)、DIEA(135mg,1.05mmol,3.00当量)及HATU(159mg,0.420mmol,1.20当量)。在室温下搅拌所得溶液3小时。将粗反应混合物过滤且进行反相制备型MPLC(Prep-C18,20-45mM,120g,Tianjin Bonna-Agela Technologies;经12min时段自8%MeCN/水达至33%MeCN/水的梯度洗脱,其中两种溶剂皆含有0.1%NH3H2O)。由此产生126mg(70.62%)呈棕色油状物的N-环己基-2-(甲基(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:510。
步骤4
向8mL小瓶中放入N-环己基-2-(甲基(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(120mg,0.235mmol,1.00当量)、MeOH(3.00mL)及TsOH(20.2mg,0.118mmol,0.50当量)的混合物。在室温下搅拌所得溶液2小时。通过使用以下条件的制备型HPLC纯化粗产物:SunFire Prep C18 OBD柱,19×150mm,5um;移动相,相A:H2O(0.1%FA);相B:CH3CN(8min内自5%CH3CN达至20%CH3CN)。由此产生22.5mg(22.46%)呈灰白色固体的N-环己基-2-((2-(4-(2-羟乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。1H NMR(300MHz,DMSO-d6,ppm):δ8.55(d,J=5.9Hz,1H),8.14(s,0H),8.03(d,J=7.9Hz,1H),7.89(d,J=2.6Hz,1H),7.22(dd,J=5.9,2.6Hz,1H),4.96(br,1H),4.24-4.20(m,4H),3.77-3.68(m,2H),3.62-3.47(m,1H),3.33(s,3H),3.18(t,J=7.3Hz,2H),2.89(t,J=7.8Hz,2H),2.07-1.97(m,2H),1.72-1.52(m,5H),1.31-1.07(m,5H)。LCMS(ES)[M+1]+m/z:426.2。
实施例1.148
合成N-叔丁基-2-{[2-(4,5-二甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物145)
流程95描绘用于制备例示性化合物的合成途径。
流程95
步骤1
向25mL圆底烧瓶中放入6-溴吡啶-3-醇(800.00mg,4.598mmol,1.00当量)于DMF(10mL)中的溶液、碘甲烷(717.86mg,5.058mmol,1.10当量)及K2CO3(762.53mg,5.517mmol,1.2当量)。在室温下搅拌所得溶液12hr。将所得溶液用50mL H2O稀释,用2×50mL乙酸乙酯萃取,将有机层合并,经无水硫酸钠干燥,且浓缩。由此产生780mg(90.23%)呈淡黄色油状物的2-溴-5-甲氧基吡啶。LCMS(ES)[M+1]+m/z:188。
步骤2
向25mL圆底烧瓶中放入2-溴-5-甲氧基吡啶(700.00mg,3.723mmol,1.00当量)于DCM(15mL)中的溶液及mCPBA(770.94mg,4.468mmol,1.2当量)。在室温下搅拌所得溶液10hr。随后通过添加20mL水/冰来淬灭反应物。用2×20mL二氯甲烷萃取所得溶液。将合并的有机层用3×20mL Na2SO3水溶液洗涤,经无水硫酸钠干燥,且浓缩。将残余物施加至含乙酸乙酯/石油醚(1:2)的硅胶柱上。由此产生550mg(72.41%)呈淡黄色固体的2-溴-5-甲氧基吡啶1-氧化物。LCMS(ES)[M+1]+m/z:204。
步骤3
向50mL圆底烧瓶中放入H2SO4(12.00mL)、2-溴-5-甲氧基吡啶1-氧化物(500.00mg,2.451mmol,1.00当量)。之后在30min内在0℃下于搅拌下逐滴添加HNO3(8.00mL,0.127mmol,0.05当量)。在0℃下于冰/盐浴中搅拌所得溶液30min。于油浴中将温度维持于100℃下,同时再搅拌所得溶液12hr。用100mL冰水稀释所得溶液。用NaOH(5mol/L)将溶液的pH值调节至10。用3×30mL乙酸乙酯萃取所得混合物,且将合并的有机层干燥并浓缩。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上。由此产生220mg呈淡黄色固体的2-溴-5-甲氧基-4-硝基吡啶。LCMS(ES)[M+1]+m/z:233。
步骤4
向20mL圆底烧瓶中放入2-溴-5-甲氧基-4-硝基吡啶(200.00mg,0.858mmol,1.00当量)于MeOH(5mL)中的溶液及甲醇钠(69.55mg,1.287mmol,1.50当量)。在室温下搅拌所得溶液3hr。将所得溶液用20mL H2O稀释,用2×20mL二氯甲烷萃取。使合并的有机层经无水硫酸钠干燥且浓缩。由此产生110mg(58.78%)呈灰白色固体的2-溴-4,5-二甲氧基吡啶。LCMS(ES)[M+1]+m/z:218。
步骤5
向在惰性氮气氛围中吹扫及维持的25mL圆底烧瓶中放入2-溴-4,5-二甲氧基吡啶(300.00mg,1.376mmol,1.00当量)于甲苯(6mL)中的溶液、Sn2Me6(450.76mg,1.376mmol,1.00当量)及Pd(dppf)Cl2(1006.70mg,1.376mmol,1当量)。于油浴中在100℃下搅拌所得溶液3hr。将所得溶液用20mL H2O稀释,用2×20mL乙酸乙酯萃取。合并的有机层经无水硫酸钠干燥且真空浓缩。由此产生220mg(37.34%)呈棕色固体的4,5-二甲氧基-2-(三丁基锡烷基)吡啶。LCMS(ES)[M+1]+m/z:430。
步骤6
向在惰性氮气氛围中吹扫及维持的20mL圆底烧瓶中放入4,5-二甲氧基-2-(三丁基锡烷基)吡啶(220.00mg,0.514mmol,1.00当量)于Tol(6mL)中的溶液、2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸叔丁酯(152.99mg,0.514mmol,1当量)及Pd(dppf)Cl2(37.59mg,0.051mmol,0.10当量)。于油浴中在100℃下搅拌所得溶液12hr。浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上。将收集的洗脱份合并且浓缩。通过使用以下条件的急骤制备型HPLC(IntelFlash-1)来纯化粗产物:柱C18;移动相,15min内自ACN:H2O(0.01%TFA)=1:20增加至ACN:H2O(0.01%TFA)=1:5;检测器,UV254nm。由此产生80mg(38.98%)呈白色固体的N-(叔丁基)-2-((2-(4,5-二甲氧基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。H NMR(300MHz,DMSO-d6)δ8.24(s,1H),7.92(s,1H),7.64(s,1H),4.16(s,2H),3.93(s,3H),3.91(s,3H),3.25(s,3H),3.13(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.03-1.95(m,2H),1.22(s,9H)。LCMS(ES)[M+1]+m/z:400.2。
实施例1.149
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(3-甲基氧杂环戊-3-基)乙酰胺(化合物146)
流程96描绘用于制备例示性化合物的合成途径。
流程96
步骤1
向[(叔丁氧羰基)(甲基)氨基]乙酸(1.00g;5.29mmol;1.00当量)于DMF(15mL)中的溶液中添加3-甲基氧杂环戊-3-胺(0.53g;5.29mmol;1.00当量),之后添加休尼格氏碱(1.38mL;0.01mol;1.50当量)及HATU(2.01g;0.01mol;1.00当量)。在室温下搅拌15h后,用EtOAc萃取混合物,将有机层合并,干燥,且浓缩,得到所需粗产物。用DCM(10mL)稀释粗产物,向其添加含4N HCl的二噁烷(10mL)。完成后,将混合物浓缩且用饱和NaHCO3稀释。用EtOAc萃取水层,且随后将有机层合并并浓缩,得到2-[氯(甲基)氨基]-N-(3-甲基氧杂环戊-3-基)乙酰胺(2.80g)。LCMS(ES)[M+1]+m/z:173.4。
步骤2
向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(0.66g;3.50mmol;1.00当量)于AcCN(10mL)中的溶液中添加2-[氯(甲基)氨基]-N-(3-甲基氧杂环戊-3-基)乙酰胺(1.10g;5.25mmol;1.50当量)及三乙胺(1.96mL;14.00mmol;4.00当量)。在80℃下搅拌15h后,将混合物冷却至室温且浓缩以移除溶剂。通过柱色谱(DCM/MeOH=10:1)纯化残余物,得到2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-甲基氧杂环戊-3-基)乙酰胺。LCMS(ES)[M+1]+m/z:325.1,327.2。
步骤3
向4-甲氧基-2-(三丁基锡烷基)吡啶(183.88mg;0.46mmol;1.50当量)及2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-甲基氧杂环戊-3-基)乙酰胺(100.00mg;0.31mmol;1.00当量)于甲苯(1.0mL)中的溶液中添加四(三苯基膦)钯(35.58mg;0.03mmol;0.10当量)。使混合物脱气且在105℃下加热15h。HPLC指示缓慢转化。浓缩混合物且添加DMF(1mL)、更多4-甲氧基-2-(三丁基锡烷基)吡啶(183.88mg;0.46mmol;1.50当量)及四(三苯基膦)钯(35.58mg;0.03mmol;0.10当量)。将混合物在100℃下进一步加热15hr,冷却。用水及AcCN稀释且通过制备型HPLC进行纯化,得到N-叔丁基-2-{乙基[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(16mg)。1H NMR(400MHz,甲醇-d4)δ8.62(d,J=6.1Hz,1H),8.06(d,J=2.6Hz,1H),7.35(dd,J=6.1,2.7Hz,1H),4.49-4.33(m,2H),4.07(s,3H),3.96(dd,J=13.9,8.8Hz,1H),3.94-3.81(m,2H),3.61(t,J=8.3Hz,1H),3.51(s,3H),3.33(d,J=7.3Hz,2H),3.13-2.94(m,2H),2.30(dq,J=13.3,6.7Hz,1H),2.26-2.13(m,2H),2.07-1.86(m,1H),1.45(d,J=15.2Hz,3H)。LCMS(ES)[M+1]+m/z:398.0。
实施例1.150
合成2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(3-甲基氧杂环戊-3-基)乙酰胺(化合物147)
流程97描绘用于制备例示性化合物的合成途径。
流程97
向1-甲基-4-(三丁基锡烷基)-1H-咪唑(171.40mg;0.46mmol;1.50当量)及2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-甲基氧杂环戊-3-基)乙酰胺(100.00mg;0.31mmol;1.00当量)于DMF(1.0mL)中的溶液中添加四(三苯基膦)钯(35.58mg;0.03mmol;0.10当量)。使混合物脱气且在105℃下加热15h。将溶液冷却至室温且用水及AcCN稀释,且通过制备型HPLC纯化,得到2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(3-甲基氧杂环戊-3-基)乙酰胺(26.6mg)。1H NMR(400MHz,甲醇-d4)δ8.74(s,1H),8.37(s,1H),4.60(d,J=16.7Hz,1H),4.52(d,J=16.7Hz,1H),4.02(d,J=9.0Hz,1H),4.00(s,3H),3.96-3.82(m,2H),3.56(d,J=9.0Hz,1H),3.51(s,3H),3.30(d,J=12.2Hz,2H),3.10(t,J=7.9Hz,2H),2.33(ddd,J=12.9,7.6,5.3Hz,1H),2.23(p,J=7.8Hz,2H),1.95(dt,J=12.9,8.1Hz,1H),1.46(s,3H)。LCMS(ES)[M+1]+m/z:371.0。
实施例1.151
合成2-[甲基({2-[4-(2,2,2-三氟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物177)
流程98描绘用于制备例示性化合物的合成途径。
流程98
步骤1
向[(叔丁氧羰基)(甲基)氨基]乙酸(2.00g;10.57mmol;1.00当量)于DMF(15mL)中的溶液中添加1-甲基-1H-吡唑-4-基胺(1.54g;15.86mmol;1.50当量),之后添加休尼格氏碱(2.77mL;15.86mmol;1.50当量)及HATU(4.82g;12.68mmol;1.20当量)。搅拌4h后,用饱和NaHCO3稀释混合物,且用EtOAc萃取水层。将有机层合并,用盐水洗涤,干燥,且浓缩,得到粗产物,通过硅胶柱色谱(己烷/EtOAc=1:3)纯化,得到N-甲基-N-{[(1-甲基-1H-吡唑-4-基)氨甲酰基]甲基}氨基甲酸叔丁酯(2.75g,产率97%)。LCMS(ES+):(M+Na)+=291.1。
步骤2
向N-甲基-N-{[(1-甲基-1H-吡唑-4-基)氨甲酰基]甲基}氨基甲酸叔丁酯(2.75g;10.25mmol;1.00当量)于DCM(5mL)中的溶液中添加含4N HCl的二噁烷(5mL)。搅拌混合物2h。使用HPLC检验反应完成。浓缩悬浮液,得到2-[氯(甲基)氨基]-N-(1-甲基-1H-吡唑-4-基)乙酰胺(2.15g)。LCMS(ES+):(M+H)+=169.1。
步骤3
向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(1.32g;7.00mmol;1.00当量)于AcCN(15ml)中的溶液中添加三乙胺(2.94mL;21.01mmol;3.00当量)及2-[氯(甲基)氨基]-N-(1-甲基-1H-吡唑-4-基)乙酰胺(2.15g;10.51mmol;1.50当量)。将混合物在80℃下加热3h且用水稀释。真空移除AcCN且用EtOAc萃取水层。将有机层合并,用盐水洗涤,干燥且浓缩。将所得粗固体用EtOAc洗涤,过滤,且干燥,得到呈白色固体的2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(1-甲基-1H-吡唑-4-基)乙酰胺(1.61g)。LCMS(ES+):(M+H)+=321.1。
步骤4
合成施蒂勒锡试剂:在-78℃下向2-溴-4-(2,2,2-三氟乙氧基)吡啶(310.00mg;1.21mmol;1.00当量)于甲苯(10ml)中的溶液中添加丁基锂(0.54mL;2.70mol/L;1.45mmol;1.20当量)。在-78℃下搅拌30min后,向混合物中添加三丁基(氯)锡烷(0.36mL;1.33mmol;1.10当量)。在-78℃下搅拌30min后,使溶液升温至室温且进一步搅拌2h。将混合物用冰水及盐水淬灭且用己烷萃取。将有机层合并,干燥,且浓缩,得到2-(三丁基锡烷基)-4-(2,2,2-三氟乙氧基)吡啶(590mg)。
向2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(1-甲基-1H-吡唑-4-基)乙酰胺(175.00mg;0.55mmol;1.00当量)于DMF(2mL)中的溶液中添加上文合成的2-(三丁基锡烷基)-4-(2,2,2-三氟乙氧基)吡啶(508.64mg;1.09mmol;2.00当量)及四(三苯基膦)钯(63.04mg;0.05mmol;0.10当量)。用N2脱气后,在110℃下加热混合物15h。使混合物冷却且用AcCN/水稀释,过滤,且通过制备型HPLC对滤液进行纯化,得到2-[甲基({2-[4-(2,2,2-三氟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]-N-(1-甲基-1H-吡唑-4-基)乙酰胺(11.4mg)。LCMS(ES+):(M+H)+=462.1。1H NMR(400MHz,DMSO-d6)δ10.74(s,1H),8.68(d,J=5.8Hz,1H),7.94(s,1H),7.50(d,J=2.3Hz,1H),7.43(dd,J=5.8,2.6Hz,1H),6.33(d,J=2.2Hz,1H),5.01(dd,J=9.3,4.1Hz,2H),4.61(s,2H),3.69(s,3H),3.51(s,3H),3.31(m,2H),3.01(t,J=7.9Hz,2H),2.14-2.03(m,2H)。
实施例1.152
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物187)
流程99描绘用于制备例示性化合物的合成途径。
流程99
步骤1
向1L 3颈圆底烧瓶中放入N-(叔丁氧羰基)-N-甲基甘氨酸(40.0g,0.211mol,1.00当量)、DMF(300mL)、6-甲氧基吡啶-3-胺(28.8g,0.232mol,1.10当量)、DIEA(54.4g,0.422mmol,2.00当量)。之后在0℃下分数批添加HATU(88.16g,0.232mol,1.10当量)。添加后,在室温下搅拌所得溶液16h。将反应物用400mL水淬灭,用3×200mL乙酸乙酯萃取。将合并的有机相用2×400mL水及1×400mL盐水洗涤,经无水硫酸钠干燥且过滤。减压浓缩滤液,通过含乙酸乙酯/石油醚(1:1)的硅胶柱纯化残余物。由此产生40g(4%)呈灰白色固体的(2-((6-甲氧基吡啶-3-基)氨基)-2-氧代乙基)(甲基)氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z:296。
步骤2
向500mL 3颈圆底烧瓶中放入(2-((6-甲氧基吡啶-3-基)氨基)-2-氧代乙基)(甲基)氨基甲酸叔丁酯(40g,0.101mol,1.00当量)、DCM(200.00mL)。之后在0℃下于搅拌下逐滴添加HCl(g)(2M于乙酸乙酯中)(300.00mL)。将所得溶液在室温下搅拌16h,真空浓缩以移除溶剂且用乙酸乙酯(150mL)洗涤。由此产生25.5g(81%)N-(6-甲氧基吡啶-3-基)-2-(甲基氨基)乙酰胺盐酸盐。LCMS(ES)[M-HCl+1]+m/z:196。
步骤3
向1L 3颈圆底烧瓶中放入N-(6-甲氧基吡啶-3-基)-2-(甲基氨基)乙酰胺盐酸盐(38.6g,0.167mol,1.05当量)、NMP(300.00mL)、2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(30g,0.158mol,1.00当量)、DIEA(61.15g,0.474mol,3.00当量)。于油浴中在50℃下搅拌所得溶液18h。将反应混合物冷却至室温,用200mL水稀释,用3×200mL乙酸乙酯萃取。将合并的有机相用3×300ml水及盐水200mL洗涤,经无水硫酸钠干燥且过滤。减压浓缩滤液,通过含THF/石油醚(1:1)的硅胶柱纯化残余物。由此产生35g(63%)呈白色固体的2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺。LCMS(ES)[M+1]+m/z:348。
步骤4
向用惰性氮气氛围吹扫且维持的500mL三颈圆底烧瓶中放入2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(10g,28.8mmol,1.00当量)、甲苯(150mL)、4-氟-2-(三丁基锡烷基)吡啶(20g,51.84mmol,1.8当量)及Pd(PPh3)4(3.04g,2.88mmol,0.10当量)。于油浴中在110℃下搅拌混合物36h。在2个批次中重复反应。将反应混合物冷却至室温,浓缩以移除溶剂,通过含PE/THF(100:1至1:10)的硅胶柱纯化残余物。由此产生12.1g(51.5%)呈黄色油状物的2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺。LCMS(ES)[M+1]+m/z:409。
步骤5
向250mL 3颈烧瓶中放入乙烷-1,2-二醇(4.78g,77.0mmol,5.0当量)及DMSO(100mL),在5℃下分批添加NaH(60%于矿物油中)(3.08g,77.0mmol,5.0当量)。在室温下搅拌混合物1h。其后在5℃下添加2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(6.3g,15.4mmol,1.00当量)。在室温下搅拌反应混合物5h。(在2个批次中重复反应)。将反应混合物倒入200mL搅拌水中,用3×200mL乙酸乙酯萃取。将合并的有机相用3×300mL水及盐水1×200mL洗涤,经无水硫酸钠干燥。通过使用如下条件的制备型HPLC纯化残余物:柱,C18-800g,移动相,CH3CN/H2O(0.05%FA),27min内自10%增加至70%,流动速率,180mL/min,检测器,254nm。用K2CO3固体将洗脱份的pH值调节至7-8,用二氯甲烷(3×300mL)萃取。使合并的有机相经无水硫酸钠干燥且过滤。减压浓缩滤液。冷冻干燥残余物,得到5.7g(41%)呈白色固体的2-((2-(4-(2-羟乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺。LCMS:(ES,m/z):[M+H]+:451.2。1H-NMR:(300MHz,DMSO-d6,ppm):δ10.27(s,1H),8.44(d,J=5.6Hz,1H),8.35(d,J=2.6Hz,1H),7.89(dd,J=8.9,2.7Hz,1H),7.79(d,J=2.5Hz,1H),7.01(dd,J=5.7,2.6Hz,1H),6.78(d,J=8.9Hz,1H),4.91(t,J=5.4Hz,1H),4.41(s,2H),4.04(t,J=4.8Hz,2H),3.80(s,3H),3.69(q,J=5.1Hz,2H),3.37(s,3H),3.20(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.08-1.96(m,2H)。
实施例1.153
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物348)
流程100描绘用于制备例示性化合物的合成途径。
流程100
步骤1:添加氟吡啶:
流程100-1
向用惰性氮气氛围吹扫且维持的250mL三颈圆底烧瓶中放入N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(10g,33.8mmol,1.00当量)、甲苯(150.00mL)、4-氟-2-(三丁基锡烷基)吡啶(21.7g,60.84mmol,1.8当量)及Pd(PPh3)4(3.57g,3.38mmol,0.10当量)。于油浴中在110℃下搅拌60h后,将反应混合物冷却至室温,且浓缩以移除溶剂;通过含二氯甲烷/甲醇(10:1)的硅胶柱纯化残余物。由此产生7g(58%)呈黄色固体的N-(叔丁基)-2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:358。
步骤2:添加2-(二甲氨基)乙-1-醇:
流程100-2
向50mL 3颈烧瓶中放入2-(二甲基氨基)乙-1-醇(112mg,1.26mmol,3.0当量)及DMF(2mL)。在0-5℃下分批添加NaH(60%于矿物油中)(33.6mg,0.84mmol,2.0当量)。搅拌1h后,在0-5℃下向混合物中添加N-(叔丁基)-2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(150mg,0.42mmol,1.00当量)。随后在50℃下搅拌反应混合物5h。冷却至环境温度后,浓缩反应混合物,且通过使用以下条件的制备型HPLC纯化残余物:柱,C18-800g,移动相,CH3CN/H2O(0.05%FA),27min内自10%增加至70%,流动速率,80mL/min,检测器,254nm。用Na2CO3将洗脱份的pH值调节至7-8,且用二氯甲烷(3×300mL)萃取混合物。使合并的有机相经无水硫酸钠干燥,过滤,且减压浓缩滤液。由此产生100.9mg(56%)呈白色固体的N-(叔丁基)-2-((2-(4-(2-(二甲基氨基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES,m/z):[M+H]+:427。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.83(d,J=2.5Hz,1H),7.67(s,1H),7.05(dd,J=5.6,2.6Hz,1H),4.20(t,J=5.7Hz,2H),4.12(s,2H),3.31(s,3H),3.15(t,J=7.2Hz,2H),2.81(t,J=7.8Hz,2H),2.66(t,J=5.7Hz,2H),2.23(s,6H),2.05-1.94(m,2H),1.25(s,9H)。
替代方法:用于制备化合物348
流程100-3
向500mL圆底烧瓶中添加含4-氯吡啶甲腈(50g,360mmol,1.00当量)的MeOH及NaOMe(1.95g,36.1mmol,0.1当量)。在室温下于氮气氛围下搅拌混合物8小时,且添加NH4Cl(29.0g,541mmol,1.5当量)。在室温下于氮气氛围下进一步搅拌所得混合物16小时。过滤所得混合物,减压浓缩滤液。由此产生呈棕色固体的4-氯甲吡啶脒盐酸盐(63.0g,90.90%)。LCMS(ES)[M-HCl+1]+m/z 156。
流程100-4
在室温下向1L圆底烧瓶中添加含4-氯甲吡啶脒盐酸盐(60.0g,312mmol,1.00当量)的MeOH(600mL)、2-氧代环戊烷-1-甲酸甲酯(66.6g,468mmol,1.5当量)及含NaOMe(42.18g,781mmol,2.5当量)的MeOH。在70℃下于氮气氛围下搅拌混合物40小时。通过过滤收集沉淀的固体且用MeOH(1×1500mL)洗涤。由此产生呈棕色固体的2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-醇(62g,80.12%)。LCMS(ES)[M+1]+m/z 248。
流程100-5
向1L 3颈圆底烧瓶中添加含2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-醇(60g,242mmol,1.00当量)的DCM及TEA(123g,1211mmol,5.0当量)。在0℃下逐滴添加Tf2O(137g,484mmol,2.0当量)于DCM中的搅拌混合物。在0℃下再搅拌所得混合物2小时。通过在室温下添加NH4Cl(水溶液500mL)淬灭反应物。用DCM(3×600mL)萃取所得混合物,且将有机层合并且经无水Na2SO4干燥。过滤所得混合物,且减压浓缩滤液。通过硅胶柱色谱,用PE/EA(3:1)洗脱来纯化残余物,得到呈灰白色固体的三氟甲烷磺酸2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基酯(63g,68.48%)。LCMS(ES)[M+1]+m/z 380。
流程100-6
向500mL三颈圆底烧瓶中添加三氟甲烷磺酸2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基酯(24.0g,63.3mmol,1.00当量)、TEA(25.6g,253.2mmol,4.00当量)及二氯甲烷(300mL)。之后在室温下添加N-(叔丁基)-2-(甲基氨基)乙酰胺盐酸盐(14.8g,82.3mmol,1.30当量)。搅拌12h后,将反应物用H2O(200mL)淬灭,用二氯甲烷(100mL×1)萃取,且将有机层分离并经无水硫酸钠干燥。过滤混合物,且减压浓缩滤液。于乙酸乙酯/己烷(1:3)中湿磨残余物。通过过滤收集固体且在红外灯下干燥3h。由此产生21.3g(90%)呈灰白色固体的N-(叔丁基)-2-((2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES,m/z):[M+H]+:374。
流程100-7
向250mL三颈圆底烧瓶中添加2-(二甲基氨基)乙-1-醇(2.86g,32.17mmol,2.00当量)及DMF(80mL)。之后在室温下添加t-BuOK(3.6g,32.17mmol,2.00当量)。搅拌混合物0.5h,将N-(叔丁基)-2-((2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(6.0g,16.08mmol,1.00当量)添加至以上混合物中且在60℃下再搅拌5h。将反应混合物冷却至室温,用H2O(100mL)淬灭,且用乙酸乙酯(100mL×2)萃取。将合并的有机相用盐水(100mL×2)洗涤且经无水硫酸钠干燥。过滤混合物,且减压浓缩滤液。通过使用以下条件的制备型HPLC纯化残余物:C18-500g,CH3CN/H2O(NH4HCO3 0.1%),30min内自15%达至70%,流动速率,150mL/min,检测器,UV 254nm。由此产生5.5g(80.29%)呈棕色固体的N-(叔丁基)-2-((2-(4-(2-(二甲基氨基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。将固体于CH3CN(120mL)中湿磨,通过过滤收集且干燥,得到N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(5.5g,98.8%)。LCMS(ES,m/z):[M+H]+:427。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.84(d,J=2.5Hz,1H),7.68(s,1H),7.05(dd,J=5.7,2.6Hz,1H),4.20(t,J=5.7Hz,2H),4.12(s,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.67(t,J=5.6Hz,2H),2.23(s,6H),2.01-1.96(m,2H),1.24(s,9H)。
实施例1.154
合成N-(2,3-二氢-1H-茚-1-基)-N-甲基-2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-胺
通过用N-甲基-1-茚满胺替换氮杂环庚烷,与化合物92的合成类似地合成标题化合物。MS(ES+):(M+H)+=342.9。1H NMR(400MHz,氯仿-d)δ8.78(d,J=5.6Hz,1H),8.38(d,J=7.9Hz,1H),7.83-7.74(m,1H),7.36(dd,J=7.6,4.8Hz,1H),7.32-7.27(m,1H),7.25-7.14(m,2H),6.44(t,J=8.2Hz,1H),3.21(t,J=7.3Hz,2H),3.14-3.03(m,3H),3.03-2.91(m,4H),2.56-2.43(m,1H),2.18-2.05(m,3H)。
实施例1.155
合成2-{4-[(5aS,8aS)-八氢-2H-环戊并[b][1,4]噁氮杂卓-5-基]-5H,6H,7H-环戊并[d]嘧啶-2-基}吡啶(化合物18)
流程101
步骤1
向N-[(1S,2S)-2-羟基环戊基]氨基甲酸叔丁酯(1.24g;6.16mmol;1.00当量)于叔丁醇(20mL)及丙-2-烯酸叔丁酯(20mL)中的溶液中添加碳酸铯(2.0g;6.16mmol;1.00当量),将混合物在室温下搅拌15h,加热至50℃且搅拌8h。将溶液用EtOAc稀释,用盐水洗涤,且用EtOAc萃取。将有机层合并,干燥且浓缩,通过柱色谱纯化残余物,得到3-{[(1S,2S)-2-{[(叔丁氧基)羰基]氨基}环戊基]氧基}丙酸叔丁酯(1.22g,60.1%)。
步骤2
在室温下搅拌3-{[(1S,2S)-2-{[(叔丁氧基)羰基]氨基}环戊基]氧基}丙酸叔丁酯(1.22g;3.70mmol;1.00当量)于含4N HCl的二噁烷(20mL)中的溶液15h,浓缩混合物,得到呈浓稠油状物的3-{[(1S,2S)-2-(氯氨基)环戊基]氧基}丙酸(0.98g,126%),其不经纯化即用于下一步骤中。LCMS(ES)(M+H)+=174.4。
步骤3
向3-{[(1S,2S)-2-氨基环戊基]氧基}丙酸(1.00g;5.77mmol;1.00当量)于DCM(125mL)中的溶液中添加休尼格氏碱(5.03mL;28.87mmol;5.00当量)及2,4,6-三丙基-1,3,5,2,4,6-三氧杂三磷杂环己烷2,4,6-三氧化物(5.16mL;8.66mmol;1.50当量),在室温下搅拌15h后,HPLC检验所需质量实验值。浓缩混合物且通过柱色谱(DCM/MeOH=10:1)纯化残余物,得到(5aS,8aS)-八氢-2H-环戊并[b][1,4]噁氮杂卓-4-酮(460mg,51%)。LCMS(ES)(M+H)+=156.2。
步骤4
在室温下向(5aS,8aS)-八氢-2H-环戊并[b][1,4]噁氮杂卓-4-酮(200.00mg;1.29mmol;1.00当量)于THF(4.5mL)中的溶液中添加氢化锂铝(1.29mL;2.00mol/L;2.58mmol;2.00当量)。随后在55℃下加热混合物2h,再添加1当量的LiAH4。30min后,再添加1当量的LiAH4,再搅拌30min,于冰浴中冷却混合物,添加0.4mL水及0.1mL的4M NaOH,将悬浮液用EtOAc(30mL)稀释且经由硅藻土过滤,浓缩滤液,得到(5aS,8aS)-八氢-2H-环戊并[b][1,4]氧氮杂环庚烷(175mg,96%),其不经进一步纯化即用于下一步骤中。LCMS(ES)(M+H)+=142.2。
步骤5
在室温下向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(100.00mg;0.53mmol;1.00当量)及(5aS,8aS)-八氢-2H-环戊并[b][1,4]噁氮杂卓(93.37mg;0.66mmol;1.25当量)于AcCN(1mL)中的溶液中添加DIPEA(0.18mL;1.06mmol;2.00当量)。将反应混合物在环境温度下搅拌30min且在80℃向搅拌过夜。浓缩溶液,且通过柱色谱(己烷/EtOAc=2:1)纯化粗油状物,得到4-[(5aS,8aS)-八氢-2H-环戊并[b][1,4]噁氮杂卓-5-基]-2-氯-5H,6H,7H-环戊并[d]嘧啶(130mg,产率83.6%)。LCMS(ES)(M+H)+=293.5。
步骤6
向4-[(5aS,8aS)-八氢-2H-环戊并[b][1,4]噁氮杂卓-5-基]-2-氯-5H,6H,7H-环戊并[d]嘧啶(136.00mg;0.46mmol;1.00当量)于甲苯(2mL)中的溶液中添加2-(三丁基锡烷基)吡啶(255.63mg;0.69mmol;1.50当量),之后添加四(三苯基膦)钯(53.49mg;0.05mmol;0.10当量)。将溶液在105℃下加热15h,冷却且浓缩,得到粗产物,通过制备型HPLC纯化,得到2-{4-[(5aS,8aS)-八氢-2H-环戊并[b][1,4]噁氮杂卓-5-基]-5H,6H,7H-环戊并[d]嘧啶-2-基}吡啶(101mg,64.5%)。LCMS(ES)(M+H)+=337.3。1H NMR(400MHz,DMSO-d6)δ8.74(d,J=4.7Hz,1H),8.31(d,J=7.9Hz,1H),8.01(td,J=7.7,1.8Hz,1H),7.57(dd,J=7.5,4.8Hz,1H),4.40(dd,J=15.3,5.9Hz,1H),4.23(tt,J=17.0,10.0Hz,2H),3.91-3.83(m,1H),3.73(dd,J=15.4,10.9Hz,1H),3.52(td,J=12.1,2.5Hz,1H),3.12(dp,J=29.5,7.3,6.9Hz,2H),2.91(t,J=7.9Hz,2H),2.44-2.32(m,1H),2.03(dd,J=10.8,5.0Hz,2H),2.01-1.83(m,2H),1.78(q,J=9.5,8.4Hz,1H),1.71(t,J=4.3Hz,1H),1.70-1.63(m,1H),1.56(p,J=10.2Hz,1H),1.44-1.30(m,1H)。
实施例1.156
合成2-{4-[(5aS,8aS)-八氢-2H-环戊并[b][1,4]噁氮杂卓-5-基]-5H,6H,7H-环戊并[d]嘧啶-2-基}-4-甲基吡啶(化合物45)
用2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)吡啶,与化合物18类似地合成化合物45。LCMS(ES)[M+1]+m/z 351。1H NMR(400MHz,DMSO-d6)δ8.52(d,J=4.9Hz,1H),8.10(d,J=15.7Hz,1H),7.28(d,J=4.9Hz,1H),4.38(dd,J=15.1,5.9Hz,1H),4.18(dtd,J=23.0,10.0,7.0Hz,2H),3.91-3.82(m,1H),3.64(dd,J=15.3,10.8Hz,1H),3.49(td,J=12.0,2.5Hz,1H),3.16-3.00(m,2H),2.83(dd,J=8.7,7.1Hz,2H),2.41(s,1H),2.39(s,3H),2.00(p,J=7.6Hz,2H),1.94-1.84(m,2H),1.79-1.63(m,3H),1.55(p,J=10.3Hz,1H),1.40-1.25(m,1H)。
实施例1.157
合成1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚-2-酮(化合物46)
流程102
步骤1
向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(100.00mg;0.53mmol;1.00当量)及2-氮杂环庚烷酮(65.84mg;0.58mmol;1.10当量)于二噁烷(2mL)中的溶液中添加碳酸铯(258.53mg;0.79mmol;1.50当量)、Xantphos(30.61mg;0.05mmol;0.10当量)及参(二苯亚甲基丙酮)二钯(0)(24.22mg;0.03mmol;0.05当量)。在100℃加热3h后,将混合物用AcCN稀释,经由硅藻土过滤,浓缩滤液且通过制备型HPLC纯化,得到1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氮杂环庚-2-酮(16mg,产率11%)。LCMS(ES)(M+H)+=342.7。
步骤2
向2-(三丁基锡烷基)吡啶(44.33mg;0.12mmol;2.00当量)及1-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氮杂环庚-2-酮(16.00mg;0.06mmol;1.00当量)于甲苯(1mL)中的溶液中添加四(三苯基膦)钯(6.96mg;0.01mmol;0.10当量),脱气且在100℃加热过夜后,浓缩且通过制备型HPLC对残余物进行纯化,得到1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氮杂环庚-2-酮(5.4mg,29.1%)。LCMS(ES)(M+H)+=308.9。1H NMR(400MHz,DMSO-d6)δ8.77-8.71(m,1H),8.30(d,J=8.0Hz,1H),7.99(dd,J=8.5,6.8Hz,1H),7.54-7.47(m,1H),3.92(d,J=8.4Hz,2H),2.95(t,J=7.8Hz,2H),2.64(d,J=10.5Hz,2H),2.15-2.03(m,2H),1.80-1.68(m,8H)。
实施例1.158
合成2-{4-[(5aS,8aR)-八氢-2H-环戊并[b][1,4]噁氮杂卓-5-基]-5H,6H,7H-环戊并[d]嘧啶-2-基}吡啶(化合物48)
用N-[(1S,2R)-2-羟基环戊基]氨基甲酸叔丁酯替换N-[(1S,2S)-2-羟基环戊基]氨基甲酸叔丁酯,与化合物18类似地合成化合物48。LCMS(ES)[M+1]+m/z:337.1。1H NMR(400MHz,甲醇-d4)δ8.69(dt,J=4.8,1.3Hz,1H),8.33(dd,J=8.0,1.1Hz,1H),7.95(td,J=7.8,1.8Hz,1H),7.50(ddd,J=7.6,4.8,1.2Hz,1H),5.04-4.93(m,1H),4.16(dt,J=14.1,4.1Hz,1H),4.00(s,1H),4.02-3.92(m,1H),3.68(ddd,J=15.2,10.6,5.2Hz,1H),3.43(ddd,J=12.5,9.9,6.2Hz,1H),3.22-3.11(m,2H),3.14-3.04(m,1H),2.97(t,J=7.9Hz,2H),2.23-1.84(m,7H),1.81-1.58(m,2H)。
实施例1.159
合成2-{4-[(5aS,8aR)-八氢-2H-环戊并[b][1,4]噁氮杂卓-5-基]-5H,6H,7H-环戊并[d]嘧啶-2-基}-4-甲基吡啶(化合物49)
通过用N-[(1S,2R)-2-羟基环戊基]氨基甲酸叔丁酯替换N-[(1S,2S)-2-羟基环戊基]氨基甲酸叔丁酯且用2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)吡啶,与化合物18类似地合成化合物49。LCMS(ES)[M+1]+m/z:351.3。1H NMR(400MHz,甲醇-d4)δ8.54(d,J=5.0Hz,1H),8.15(s,1H),7.37(dd,J=5.2,1.6Hz,1H),5.00(dq,J=10.5,4.5Hz,1H),4.19(dt,J=14.6,4.2Hz,1H),3.99(ddd,J=15.8,6.6,3.4Hz,2H),3.69(ddd,J=15.2,10.5,5.3Hz,1H),3.44(ddd,J=12.5,9.9,6.3Hz,1H),3.23-3.12(m,1H),3.16-3.05(m,2H),2.98(t,J=7.9Hz,2H),2.47(s,3H),2.24-1.85(m,7H),1.82-1.58(m,2H)。
实施例1.160
合成2-{4-[(5aS,8aR)-八氢-2H-环戊并[b][1,4]噁氮杂卓-5-基]-5H,6H,7H-环戊并[d]嘧啶-2-基}-4-甲氧基吡啶(化合物54)
通过用N-[(1S,2R)-2-羟基环戊基]氨基甲酸叔丁酯替换N-[(1S,2S)-2-羟基环戊基]氨基甲酸叔丁酯且用4-甲氧基-2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)吡啶,与化合物18类似地合成化合物54。LCMS(ES)[M+1]+m/z:367.2。1H NMR(400MHz,甲醇-d4)δ8.50(d,J=5.8Hz,1H),7.87(d,J=2.6Hz,1H),7.10(dd,J=5.9,2.6Hz,1H),4.98(td,J=9.7,8.9,4.3Hz,1H),4.14(dt,J=14.6,4.2Hz,1H),4.05-3.93(m,2H),3.96(s,3H),3.68(ddd,J=15.2,10.5,5.2Hz,1H),3.44(ddd,J=12.5,10.0,6.2Hz,1H),3.22-3.12(m,1H),3.14-3.04(m,1H),2.95(t,J=7.9Hz,2H),2.23-1.84(m,5H),2.03(s,3H),1.81-1.69(m,1H),1.69-1.59(m,1H)。
实施例1.161
合成N-(1-羟基-2-甲基丙-2-基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物148)
通过用2-氨基-2-甲基-1-丙醇替换环己胺,与化合物144类似地合成化合物148。LCMS(ES)[M+1]+m/z 416。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.84(d,J=2.6Hz,1H),7.50(s,1H),7.04(dd,J=5.6,2.6Hz,1H),4.90(br,1H),4.28-4.07(m,4H),3.76(t,J=5.0Hz,2H),3.37(s,2H),3.25(s,3H),3.14(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.05-1.94(m,2H),1.18(s,6H)。
实施例1.162
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(氧杂环戊-3-基)乙酰胺(化合物149)
通过用氧杂环戊-3-胺盐酸盐替换环己胺,与化合物144类似地合成化合物149。LCMS(ES)[M+1]+m/z 414。1H NMR(300MHz,DMSO-d6,ppm):δ8.46(d,J=5.6Hz,1H),8.37(d,J=6.9Hz,1H),7.80(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),5.22-4.75(m,1H),4.34-4.12(m,5H),3.83-3.52(m,5H),3.49-3.39(m,1H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.15-1.89(m,3H),1.79-1.68(m,1H)。
实施例1.163
合成N-环戊基-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物150)
通过用环戊胺替换环己胺,与化合物142类似地合成化合物150。LCMS(ES,m/z):[M+H]+:355。1H-NMR(300MHz,DMSO-d6,ppm):δ8.05(d,J=7.5Hz,1H),7.71(s,1H),7.60(s,1H),4.11(s,2H),4.02(q,J=6.6,13.5Hz,1H),3.69(s,3H),3.22(s,3H),3.07(t,J=7.5Hz,2H),2.73(t,J=7.8Hz,2H),1.99-1.89(m,2H),1.80-1.72(m,2H),1.63-1.34(m,6H)。
实施例1.164
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物151)
通过用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物151。LCMS(ES,m/z):[M+H]+:421。1H-NMR(300MHz,DMSO-d6,ppm):δ10.26(s,1H),8.45(d,J=5.4Hz,1H),8.34(d,J=2.7Hz,1H),7.87(dd,J=9.0,2.7Hz,1H),7.79(d,J=2.7Hz,1H),7.01(dd,J=5.4,2.4Hz,1H),6.78(d,J=9.0Hz,1H),4.40(s,2H),3.80(s,3H),3.79(s,3H),3.37(s,3H),3.21(t,J=7.5Hz,2H),2.83(t,J=7.8Hz,2H),2.08-1.94(m,2H)。
实施例1.165
合成N-(5-甲氧基吡啶-2-基)-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物152)
通过用5-甲氧基吡啶-2-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物152。LCMS(ES,m/z):[M+H]+:421。1H-NMR(300MHz,DMSO-d6,ppm):δ10.55(s,1H),8.43(d,J=5.7Hz,1H),8.03(d,J=3.0Hz,1H),7.96(d,J=8.7Hz,1H),7.76(d,J=2.7Hz,1H),7.39(dd,J=9.0,3.0Hz,1H),6.96(dd,J=5.7,2.7Hz,1H),4.49(s,2H),3.79(s,3H),3.73(s,3H),3.35(s,3H),3.20(t,J=7.5Hz,2H),2.83(t,J=7.8Hz,2H),2.08-1.95(m,2H)。
实施例1.166
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(2-甲氧基嘧啶-5-基)乙酰胺(化合物153)
通过用5-甲氧基吡啶-2-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物153。LCMS(ES,m/z):[M+H]+:421。1H-NMR(300MHz,DMSO-d6,ppm):δ10.55(s,1H),8.43(d,J=5.7Hz,1H),8.03(d,J=3.0Hz,1H),7.96(d,J=8.7Hz,1H),7.76(d,J=2.7Hz,1H),7.39(dd,J=9.0,3.0Hz,1H),6.96(dd,J=5.7,2.7Hz,1H),4.49(s,2H),3.79(s,3H),3.73(s,3H),3.35(s,3H),3.20(t,J=7.5Hz,2H),2.83(t,J=7.8Hz,2H),2.08-1.95(m,2H)。
实施例1.167
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物154)
通过用1-甲基吡唑-4-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物154。LCMS(ES,m/z):[M+H]+:394。1H NMR(300MHz,DMSO-d6)δ10.24(s,1H),8.47(d,J=5.4Hz,1H),7.83(s,1H),7.78(d,J=2.4Hz,1H),7.38(s,1H),7.01(dd,J=5.7,2.4Hz,1H),4.35(s,2H),3.82(s,3H),3.76(s,3H),3.34(s,3H),3.19(t,J=7.5Hz,2H),2.83(t,J=7.8Hz,2H),2.08-1.95(m,2H)。
实施例1.168
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(1-甲基环戊基)乙酰胺(化合物155)
通过用1-甲基环戊-1-胺盐酸盐替换2氧杂环戊-3-胺,与化合物135类似地合成化合物155。LCMS(ES,m/z):[M+H]+:396。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.7Hz,1H),7.84(d,J=2.4Hz,1H),7.74(s,1H),7.04(dd,J=5.7,2.7Hz,1H),4.14(s,2H),3.89(s,3H),3.26(s,3H),3.14(t,J=7.5Hz,2H),2.82(t,J=7.8Hz,2H),2.06-1.87(m,4H),1.63-1.38(m,6H),1.27(s,3H)。
实施例1.169
合成N-叔丁基-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-甲基乙酰胺(化合物156)
通过用叔丁基(甲基)胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物156。LCMS(ES,m/z):[M+H]+:384。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.7Hz,1H),7.79(d,J=2.4Hz,1H),7.03(dd,J=5.7,2.7Hz,1H),4.43(s,2H),3.89(s,3H),3.25(s,3H),3.11(t,J=7.5Hz,2H),2.93(s,3H),2.80(t,J=7.8Hz,2H),2.08-1.95(m,2H),1.32(s,9H)。
实施例1.170
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N,N-二甲基乙酰胺(化合物157)
通过用二甲胺盐酸盐替换氧杂环戊-3-胺,与化合物135类似地合成化合物157。LCMS(ES,m/z):[M+H]+:342。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.7Hz,1H),7.74(d,J=2.4Hz,1H),7.02(dd,J=5.7,2.7Hz,1H),4.51(s,2H),3.89(s,3H),3.25(s,3H),3.12(t,J=7.5Hz,2H),3.05(s,3H),2.85(s,3H),2.81(t,J=7.8Hz,2H),2.03-1.93(m,2H)。
实施例1.171
合成N-叔丁基-2-{[2-(4-氰基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物158)
用2-(三甲基锡烷基)吡啶-4-甲腈替换4-甲基-2-(三丁基锡烷基)-吡啶,与化合物24类似地合成化合物158。LCMS(ES)[M+1]+m/z 365。1H NMR(300MHz,DMSO-d6)δ8.92(d,J=4.9Hz,1H),8.66(s,1H),7.92(dd,J=5.0,1.6Hz,1H),7.76(s,1H),4.14(s,2H),3.32(s,3H),3.19(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.01(t,J=7.6Hz,2H)。
实施例1.172
合成N-叔丁基-2-({2-[4-(环丙基甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物159)
用4-(环丙基甲氧基)-2-(三甲基锡烷基)吡啶替换4-甲基-2-(三丁基锡烷基)-吡啶,与化合物24类似地合成化合物159。LCMS(ES)[M+1]+m/z 410。1H NMR(300MHz,DMSO-d6)δ8.45(d,J=5.6Hz,1H),7.85(d,J=2.5Hz,1H),7.69(s,1H),7.01(dd,J=5.7,2.6Hz,1H),4.12(s,2H),3.97(d,J=7.1Hz,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.04-1.88(m,2H),1.25(s,9H),1.25-1.20(m,1H),0.66-0.54(m,2H),0.43-0.32(m,2H)。
实施例1.173
合成N-叔丁基-2-{甲基[2-(1-甲基-1H-吡唑-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物160)
通过用1-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧硼-2-基)吡唑替换4-甲基-2-(三丁基锡烷基)-吡啶,与化合物24类似地合成化合物160。LCMS(ES)[M+1]+m/z:343。1H NMR(300MHz,DMSO-d6)δ7.69(d,J=2.2Hz,1H),7.60(s,1H),6.81(d,J=2.2Hz,1H),4.09(s,2H),3.89(s,3H),3.21(s,3H),3.08(t,J=7.3Hz,2H),2.75(t,J=7.8Hz,2H),2.13-1.84(m,2H),1.24(s,9H)。
实施例1.174
合成2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(1-甲基环戊基)乙酰胺(化合物161)
通过用1-甲基环戊-1-胺替换环己胺,与化合物142类似地合成化合物161。LCMS(ES,m/z):[M+H]+:369。1H-NMR(300MHz,DMSO-d6,ppm):δ8.16(s,1H),7.74(d,J=1.5Hz,1H),7.71(br,1H),7.61(d,J=1.5Hz,1H),4.10(s,2H),3.69(s,3H),3.22(s,3H),3.07(t,J=7.5Hz,2H),2.74(t,J=7.8Hz,2H),1.99-1.89(m,4H),1.60-1.44(m,6H),1.29(s,3H)。
实施例1.175
合成N-叔丁基-2-{甲基[2-(1-甲基-1H-咪唑-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物162)
用1-甲基-2-(三丁基锡烷基)-1H-咪唑替换4-甲基-2-(三丁基锡烷基)-吡啶,与化合物24类似地合成化合物162。LCMS(ES)[M+1]+m/z:343。1H NMR(300MHz,DMSO-d6)δ7.68(d,J=1.2Hz,1H),7.62-7.54(m,2H),4.11(s,2H),3.97(s,3H),3.21(s,3H),3.09(t,J=7.2Hz,2H),2.75(t,J=7.8Hz,2H),1.95(m,2H),1.25(s,9H)。
实施例1.176
合成N-叔丁基-2-{甲基[2-(1,3-噁唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物163)
用2-(三异丙基硅基)-4-(三甲基锡烷基)噁唑替换4-甲基-2-(三丁基锡烷基)-吡啶,与化合物24类似地合成化合物163。LCMS(ES)[M+1]+m/z:330。1H NMR(300MHz,DMSO-d6)δ8.62(d,J=1.1Hz,1H),8.42(d,J=1.1Hz,1H),7.60(s,1H),4.10(s,2H),3.23(s,3H),3.10(t,J=7.3Hz,2H),2.77(t,J=7.9Hz,2H),2.05-1.92(m,,2H),1.24(s,9H)。
实施例1.177
合成N-叔丁基-2-{甲基[2-(1,3-噁唑-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物164)
通过用2-(三甲基锡烷基)-1,3-噁唑替换4-甲基-2-(三丁基锡烷基)-吡啶,与化合物24类似地合成化合物164。LCMS(ES)[M+1]+m/z:330。1H NMR(300MHz,DMSO-d6)δ8.23(d,J=0.7Hz,1H),7.60(s,1H),7.40(d,J=0.8Hz,1H),4.16(s,2H),3.20(s,3H),3.11(t,J=7.3Hz,2H),2.80(t,J=7.9Hz,2H),1.98-1.85(m,2H),1.25(s,9H)。
实施例1.178
合成N-叔丁基-2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物165)
用3-(三甲基锡烷基)异喹啉替换4-甲基-2-(三丁基锡烷基)-吡啶,与化合物24类似地合成化合物165。LCMS(ES)[M+1]+m/z:390。1H NMR(300MHz,DMSO-d6)δ9.40(s,1H),8.86(s,1H),8.21-8.16(m,2H),8.12(d,J=8.2Hz,1H),7.87-7.69(m,3H),4.20(s,2H),3.32(s,3H),3.18(t,J=7.3Hz,2H),2.86(t,J=7.8Hz,2H),2.10-1.93(m,2H),1.23(s,9H)。
实施例1.179
合成N-叔丁基-2-[(2-{咪唑并[1,2-a]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物166)
用2-(三甲基锡烷基)咪唑并[1,2-a]吡啶替换4-甲基-2-(三丁基锡烷基)-吡啶,与化合物24类似地合成化合物166。LCMS(ES)[M+1]+m/z 379。1H NMR(300MHz,DMSO-d6)δ8.52(d,J=7.1Hz,2H),7.68(s,1H),7.57(d,J=9.1Hz,1H),7.31-7.19(m,1H),6.92(td,J=6.7,1.2Hz,1H),4.16(s,2H),3.25(s,3H),3.11(t,J=7.3Hz,2H),2.79(t,J=7.9Hz,2H),1.99-1.85(m,2H),1.25(s,9H)。
实施例1.180
合成N-(3-氟苯基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物167)
通过用3-氟苯胺替换1-环己胺,与化合物144类似地合成化合物167。LCMS(ES)[M+1]+m/z 438。1H NMR(300MHz,DMSO-d6)δ10.46(br,1H),8.43(d,J=5.6Hz,1H),7.78(s,1H),7.57(d,J=11.2Hz,1H),7.41-7.25(m,2H),7.04-6.96(m,1H),6.85(dd,J=8.4,4.9Hz,1H),5.18-4.62(br,1H),4.55-4.31(m,2H),4.15-3.95(m,2H),3.71-3.62(m,2H),3.35(s,3H),3.21(t,J=7.2Hz,2H)2.83(t,J=7.9Hz,2H),2.22-1.98(m,2H)。
实施例1.181
合成N-[(1R,2S)-2-羟基环己基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物168)
通过用(1R,2S)-2-氨基环己-1-醇替换氧杂环戊-3-胺,与化合物135类似地合成化合物168。LCMS(ES)[M+1]+m/z:412。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.80(d,J=2.6Hz,1H),7.61(d,J=7.9Hz,1H),7.03(dd,J=5.6,2.6Hz,1H),4.59(d,J=3.9Hz,1H),4.31(d,J=16.6Hz,1H),4.18(d,J=16.6Hz,1H),3.89(s,3H),3.71-3.58(m,2H),3.25(s 3H),3.14(t,J=7.1Hz,2H),2.82(t,J=7.9Hz,2H),2.03-1.91(m,2H),1.67-1.15(m,8H)。
实施例1.182
合成N-[(1S,2R)-2-羟基环己基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物169)
通过用(1S,2R)-2-氨基环己-1-醇替换氧杂环戊-3-胺,与化合物135类似地合成化合物169。LCMS(ES)[M+1]+m/z:412。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.80(d,J=2.6Hz,1H),7.61(d,J=8.0Hz,1H),7.03(dd,J=5.6,2.6Hz,1H),4.59(d,J=3.9Hz,1H),4.31(d,J=16.7Hz,1H),4.18(d,J=16.7Hz,1H),3.89(s,3H),3.71-3.63(m,2H),3.25(s,3H),3.14(t,J=7.5Hz,2H),2.82(t,J=7.9Hz,2H),2.06-1.92(m,2H),1.69-1.32(m,6H),1.31-1.14(m,2H)。
实施例1.183a及实施例1.183b
合成N-[(1R,2S)-2-羟基环戊基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物170)及N-[(1S,2R)-2-羟基环戊基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物171)
向50mL圆底烧瓶中放入[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酸(120mg,0.38mmol,1.00当量)、DMF(5.00mL)、HATU(174mg,0.45mmol,1.20当量)、DIEA(148mg,1.145mmol,3.00当量)及(1S,2R)-2-氨基环戊-1-醇盐酸盐(63.04mg,0.45mmol,1.20当量)。在25℃下搅拌所得溶液3hr。通过使用以下条件的制备型HPLC纯化粗产物:柱,XBridge Prep C18 OBD柱,5um,19*150mm;移动相,水(0.05%NH3.H2O)及CH3CN(10min内自35%CH3CN达至50%);检测器,UV 254nm。将收集的洗脱份合并且真空浓缩。
通过使用以下条件的手性HPLC分离所得产物:柱:CHIRALPAK IC,20*250mm,5um;移动相:A:正己烷/DCM=5:1,B:乙醇+0.1%DEA;流动速率:90mL/min;梯度:30%B,20min。由此产生35.1mg(23.13%)呈白色固体的N-[(1R,2S)-2-羟基环戊基]-2-[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺及37.2mg(24.52%)呈白色固体的N-[(1S,2R)-2-羟基环戊基]-2-[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺。通过使用以下条件的分析型手性HPLC分析化合物:柱:CHIRALPAK IC,4.6*50mm,3um;移动相:A:正己烷/DCM=5:1,B:乙醇+0.1%DEA;流动速率:1mL/min;梯度:30%B,6min。
化合物170:CHIRAL_HPLC:保留时间3.09min。LCMS(ES,m/z):[M+H]+:398。1H-NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),7.81(d,J=2.6Hz,1H),7.65(d,J=7.8Hz,1H),7.03(dd,J=5.6,2.6Hz,1H),4.65(d,J=3.9Hz,1H),4.32(d,J=16.7Hz,1H),4.19(d,J=16.7Hz,1H),3.89(s,3H),3.98-3.79(m,2H),3.26(s,3H),3.15(t,J=7.5Hz,2H),2.82(t,J=7.8Hz,2H),2.05-1.94(m,2H),1.74-1.68(m,3H),1.58-1.39(m,3H)。化合物171:CHIRAL_HPLC:保留时间3.88min。LCMS(ES,m/z):[M+H]+:398。1H-NMR(300MHz,DMSO-d6,ppm):δ1H-NMR:(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),7.81(d,J=2.6Hz,1H),7.65(d,J=7.8Hz,1H),7.03(dd,J=5.6,2.6Hz,1H),4.65(d,J=3.9Hz,1H),4.32(d,J=16.7Hz,1H),4.19(d,J=16.7Hz,1H),3.89(s,3H),3.98-3.79(m,2H),3.26(s,3H),3.15(t,J=7.5Hz,2H),2.82(t,J=7.8Hz,2H),2.05-1.94(m,2H),1.74-1.68(m,3H),1.58-1.39(m,3H)。
实施例1.183c及实施例1.183d
合成N-[(1R,2R)-2-羟基环戊基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物172)及N-[(1S,2S)-2-羟基环戊基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物173)
流程103
在20℃下向[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酸(300mg,0.95mmol,1.0当量)、DIEA(616mg,4.77mmol,5.0当量)及HATU(1.819g,4.77mmol,5.0当量)于THF(30mL)中的搅拌溶液中分批添加(1R,2R)-2-氨基环戊-1-醇(482mg,4.77mmol,5.0当量)。在60℃下搅拌所得混合物5h。减压浓缩反应物。通过使用以下条件的急骤制备型HPLC(IntelFlash-1)纯化残余物:柱,C18;移动相A:CH3CN,移动相B:水;流动速率:20mL/min柱,得到200mg外消旋体产物,通过使用以下条件的手性HPLC分离:柱:Lux Amylose-1,50*250mm,10um;移动相A:正己烷,移动相B:乙醇;流动速率:90mL/min;梯度:50%B,36min;220nm。由此产生呈白色固体的N-[(1R,2R)-2-羟基环戊基]-2-[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺(85mg,22.41%)及N-[(1S,2S)-2-羟基环戊基]-2-[[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺(80mg,21.09%)。使用以下条件对化合物进行分析型手性HPLC:CHIRALPAK IC,4.6*50mm,3um;移动相:A:正己烷,移动相B:乙醇;流动速率:1mL/min;梯度:50%B,6min。
化合物172:CHIRAL_HPLC:保留时间4.594min。LCMS(ES,m/z):[M+H]+:398.2;1HNMR(300MHz,CDCl3,ppm):δ8.53(d,J=5.7Hz,1H),8.21(s,1H),7.95(d,J=2.4Hz,1H),6.88(dd,J=5.4,2.4Hz,1H),4.46(br,1H),4.22(s,2H),3.90(s,3H),3.89-3.82(m,1H),3.80-3.78(m,1H),3.40(s,3H),3.19(t,J=7.2Hz,2H),2.99(t,J=7.8Hz,2H),2.15-2.08(m,2H),2.05-1.96(m,2H),1.71-1.57(m,3H),1.48-1.38(m,1H)。
化合物173:CHIRAL_HPLC:保留时间5.942min。LCMS(ES,m/z):[M+H]+:398.2;1HNMR(300MHz,CDCl3,ppm):δ8.52(d,J=8.7Hz,1H),8.20(s,1H),7.95(d,J=2.4Hz,1H),6.88(dd,J=2.7,5.7Hz,1H),4.48(br,1H),4.22(br,2H),3.90(s,3H),3.89-3.82(m,1H),3.80-3.78(m,1H),3.40(s,3H),3.18(t,J=8.4Hz,2H),2.99(t,J=6.6Hz,2H),2.15-2.07(m,2H),2.05-1.94(m,2H),1.71-1.55(m,3H),1.48-1.38(m,1H)。
实施例1.184
合成N-叔丁基-2-{甲基[2-(哒嗪-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物175)
用3-(三丁基锡烷基)哒嗪替换4-甲基-2-(三甲基锡烷基)吡啶,与化合物24类似地合成化合物175。LCMS(ES)[M+1]+m/z:341,1H-NMR(300MHz,DMSO-d6)δ10.00(dd,J=2.3,1.3Hz,1H),9.36(dd,J=5.3,1.3Hz,1H),8.37(dd,J=5.3,2.3Hz,1H),7.77(s,1H),4.15(s,2H),3.32(s,3H),3.18(t,J=7.3Hz,2H),2.85(t,J=7.9Hz,2H),2.15-1.82(m,2H),1.25(s,9H)。
实施例1.185
合成N-叔丁基-2-[甲基(2-{1H-吡唑并[4,3-c]吡啶-6-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物176)
用6-(三甲基锡烷基)-1H-吡唑并[4,3-c]吡啶替换4-甲基-2-(三甲基锡烷基)吡啶,与化合物24类似地合成化合物176。LCMS(ES)[M+1]+m/z:380.2。1H NMR(300MHz,DMSO-d6,ppm):9.16(s,1H),8.45(s,1H),8.33(s,1H),7.69(s,1H),4.18(s,2H),3.26(s,3H),3.13(t,J=7.2Hz,2H),2.84(t,J=7.9Hz,2H),2.06-1.93(m,2H),1.25(s,9H)。
实施例1.186
合成2-[甲基({2-[4-(2,2,2-三氟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物178)
通过用5-氨基嘧啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物178。LCMS(ES)[M+1]+m/z:392。1H NMR(300MHz,DMSO-d6)δ10.69(s,1H),9.00(s,2H),8.87(s,1H),8.42(d,J=5.4Hz,1H),7.74(d,J=2.4Hz,1H),7.00(dd,J=5.4,2.4Hz,1H),4.45(s,2H),3.78(s,3H),3.39(s,3H),3.22(t,J=7.5Hz,2H),2.84(t,J=7.8Hz,2H),2.10-1.95(m,2H)。
实施例1.187
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(1-甲基环戊基)乙酰胺(化合物179)
通过用1-甲基环戊-1-胺盐酸盐替换环己胺,与化合物144类似地合成化合物179。LCMS(ES)[M+1]+m/z:426.3。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.4Hz,1H),7.84(d,J=2.4Hz,1H),7.74(s,1H),7.04(dd,J=5.4,2.4Hz,1H),4.93(br,1H),4.21-4.09(m,4H),3.76(t,J=4.8Hz,2H),3.26(s,3H),3.14(t,J=7.5Hz,2H),2.81(t,J=7.8Hz,2H),2.07-1.89(m,4H),1.60-1.40(m,6H),1.28(s,3H)。
实施例1.188
合成N-叔丁基-2-{[2-(3-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物180)
通过用3-甲氧基-2-(三甲基锡烷基)吡啶替换4-甲基-2-(三甲基锡烷基)吡啶,与化合物24类似地合成化合物180。LCMS(ES)[M+1]+m/z:370。1H NMR(300MHz,DMSO-d6)δ8.12(dd,J=4.6,1.3Hz,1H),7.55-7.36(m,3H),4.09(s,2H),3.74(s,3H),3.15-3.07(m,5H),2.74(t,J=7.8Hz,2H),2.06-1.87(m,2H),1.22(s,9H)。
实施例1.189
合成N-叔丁基-2-{[2-(3-羟基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物181)
向50mL圆底烧瓶中放入N-叔丁基-2-[[2-(3-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺(50mg,0.135mmol,1.00当量)、DCE(5mL)及AlCl3(54mg,0.406mmol,3.00当量)。在65℃下搅拌所得溶液7h。真空浓缩所得混合物。将残余物溶解于4mL MeOH中且通过使用以下条件的制备型HPLC(Waters I)纯化:柱,XBridge PrepC18 OBD柱,5um,19*150mm;移动相,水(0.05%FA)及CH3CN(15min内自5%CH3CN达至35%);检测器,UV 254nm。由此产生17.1mg(35.6%)呈白色固体的N-叔丁基-2-[[2-(3-羟基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺。LCMS(ES)[M+1]+m/z 356。1HNMR(300MHz,DMSO-d6)δ14.21(s,1H),8.31-8.13(m,1H),7.88-7.69(m,1H),7.38-7.31(m,2H),4.21(s,2H),3.25(s,3H),3.21-3.09(m,2H),2.99-2.81(m,2H),2.11-1.89(m,2H),1.25(s,9H)。
实施例1.190
合成N-叔丁基-2-{[2-(1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物182)
通过用1-(三苯甲基)咪唑-4-基硼酸替换4-甲基-2-(三甲基锡烷基)吡啶,与化合物24类似地合成化合物182。LCMS(ES)[M+1]+m/z:329;1H NMR(300MHz,DMSO-d6)δ12.44(br,1H),7.67(s,1H),7.61(s,1H),7.55(s,1H),4.12(s,2H),3.25(s,3H),3.09(t,J=7.4Hz,2H),2.76(t,J=7.8Hz,2H),2.15-1.77(m,2H),1.24(s,9H)。
实施例1.191
合成(2R)-N-叔丁基-2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]丙酰胺(化合物183)
通过用5-(三甲基锡烷基)-1H-吡唑并[3,4-c]吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶,与化合物101类似地合成化合物183。LCMS(ES)[M+1]+m/z:394.2;1H NMR(300MHz,DMSO-d6,ppm)δ13.75(s,1H),9.12(s,1H),8.85(d,J=1.3Hz,1H),8.30(d,J=0.9Hz,1H),7.92(s,1H),5.17(q,J=7.0Hz,1H),3.22(dt,J=15.6,7.9Hz,1H),3.16-3.08(m,4H),2.99-2.72(m,2H),2.11-1.88(m,2H),1.34(d,J=7.1Hz,3H),1.20(s,9H)。
实施例1.192
合成2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(1-甲基环戊基)乙酰胺(化合物184)
通过用1-甲基环戊-1-胺盐酸盐替换氧杂环戊-3-胺且用5-(三甲基锡烷基)-1H-吡唑并[3,4-c]吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶,与化合物135类似地合成化合物184。LCMS(ES)[M+1]+m/z:406.2;1HNMR(300MHz,DMSO-d6,ppm)δ13.40(s,1H),9.09(d,J=1.1Hz,1H),8.80(d,J=1.3Hz,1H),8.26(d,J=0.9Hz,1H),7.82(s,1H),4.17(s,2H),3.30(s,3H),3.15(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.09-1.97(m,4H),1.48(dt,J=16.7,7.2Hz,6H),1.28(s,3H)。
实施例1.193
合成2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(3-甲基氧杂环戊-3-基)乙酰胺(化合物185)
通过用3-甲基氧杂环戊-3-胺替换氧杂环戊-3-胺且用5-(三甲基锡烷基)-1H-吡唑并[3,4-c]吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶,与化合物135类似地合成化合物185。LCMS(ES)[M+1]+m/z:408.2;1H NMR(300MHz,DMSO-d6,ppm)δ13.71(br,1H),9.09(s,1H),8.78(d,J=1.3Hz,1H),8.26(d,J=7.9Hz,2H),4.19(s,2H),3.82(d,J=8.7Hz,1H),3.77-3.66(m,2H),3.49(d,J=8.7Hz,1H),3.31(s,3H),3.15(t,J=7.4Hz,2H),2.83(t,J=7.8Hz,2H),2.25(dt,J=12.9,6.5Hz,1H),2.01(h,J=8.1,7.5Hz,2H),1.80(dt,J=12.5,7.6Hz,1H),1.32(s,3H)。
实施例1.194
合成N-(2-甲氧基嘧啶-5-基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物186)
通过用2-甲氧基嘧啶-5-胺替换环己胺,与化合物142类似地合成化合物186。LCMS(ES)[M+1]+m/z:395;1H-NMR:(300MHz,DMSO-d6,ppm):δ10.49(s,1H),8.79(s,2H),7.69(d,J=1.2Hz,1H),7.61(d,J=1.2Hz,1H),4.37(s,2H),3.87(s,3H),3.66(s,3H),3.32(s,3H),3.12(t,J=7.2Hz,2H),2.74(t,J=7.8Hz,2H),2.00-1.90(m,2H)。
实施例1.195
合成1-(4-甲氧基苯基)-4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚-2-酮(化合物188)
流程104
向2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(200mg;1.06mmol;1当量)于乙腈(3.5ml)中的溶液中添加1,4-二氮杂环庚-2-酮盐酸盐(191mg;1.27mmol;1.2当量)及休尼格氏碱(0.74mL;4.23mmol;4当量)。在70℃下搅拌反应物24h。蒸发反应物,且通过硅胶色谱(甲醇/二氯甲烷梯度)纯化残余物,得到呈白色固体的4-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}-1,4-二氮杂环庚-2-酮(279mg,98%)。LCMS(ES+):[M+H]+=266.9。
步骤2
将4-{2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}-1,4-二氮杂环庚-2-酮(279mg;1.05mmol;1当量)悬浮于1,4-二噁烷(4ml)中且用氩气吹扫混合物。添加2-(三丁基锡烷基)吡啶(0.68mL;2.09mmol;2当量)及四(三苯基膦)钯(121mg;0.1mmol;0.1当量),且在108℃下于加热块中搅拌反应物18h。将反应混合物蒸发且通过反相色谱(C18,乙腈/0.1%HCOOH-水梯度)纯化,得到呈白色固体的4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚-2-酮(66mg)。LCMS(ES+):[M+H]+=310.0。
步骤3
将4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚-2-酮(59mg;0.19mmol;1当量)、1-碘-4-甲氧基苯(54mg;0.23mmol;1.2当量)、1-N,2-N-二甲基环己烷-1,2-二胺(13.5mg;0.1mmol;0.5当量)、磷酸三钾(121mg;0.57mmol;3当量)悬浮于1,4-二噁烷(3.5ml)中。用氩气吹扫混合物。添加碘化铜(I)(12.7mg;0.07mmol;0.35当量),将容器密封且在120℃下于加热块中搅拌48h。将反应物冷却,过滤,蒸发且通过反相色谱(Waters XSelect CSH C18柱,0-100%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈棕色固体的1-(4-甲氧基苯基)-4-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚-2-酮(33mg,42%)。LCMS(ES+):[M+H]+=416.1。1H NMR(400MHz,DMSO-d6,80℃)δ7.18-6.65(m,8H),4.43-4.11(m,2H),3.87-3.54(m,11H),2.15-1.96(m,4H)。
实施例1.196
合成N-(4-氟苯基)-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物189)
通过用4-氟苯胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物189。LCMS(ES)[M+1]+m/z:408。1H NMR(300MHz,DMSO-d6)δ10.34(s,1H),8.45(d,J=5.4Hz,1H),7.79(d,J=2.7Hz,1H),7.72-7.47(m,2H),7.16-7.10(m,2H),7.00(dd,J=5.7,2.7Hz,1H),4.42(s,2H),3.77(s,3H),3.37(s,3H),3.21(t,J=7.2Hz,2H),2.84(t,J=7.8Hz,2H),2.08-1.95(m,2H)。
实施例1.197
合成N-(5-甲氧基吡啶-2-基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物190)
通过用4-甲氧基吡啶-2-胺替换环己胺,与化合物142类似地合成化合物190。LCMS(ES)[M+1]+m/z:394;1H NMR:(300MHz,DMSO-d6,ppm):δ10.51(s,1H),8.06(d,J=2.7Hz,1H),7.95(d,J=9.0Hz,1H),7.66(d,J=1.2Hz,1H),7.55(d,J=1.2Hz,1H),7.41(dd,J=9.0,3.0Hz,1H),4.43(s,2H),3.80(s,3H),3.62(s,3H),3.30(s,3H),3.12(t,J=7.2Hz,2H),2.74(t,J=7.8Hz,2H),2.00-1.90(m,2H)。
实施例1.198
合成N-叔丁基-2-({2-[4-(2-羟乙氧基)-5-甲基吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物191)
用2-氯-5-甲基吡啶-4-醇替换2-氯吡啶-4-醇,与化合物44类似地合成化合物191。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.31(s,1H),7.85(s,1H),7.65(s,1H),4.93(t,J=5.5Hz,1H),4.20-4.17(m,4H),3.83-3.78(m,2H),3.25(s,3H),3.14(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.20(s,3H),2.11-1.93(m,2H),1.23(s,9H)。
实施例1.199
合成N-叔丁基-2-{[2-(4-甲氧基-5-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物192)
通过用4-甲氧基-5-甲基-2-(三甲基锡烷基)吡啶替换4-甲基-2-(三甲基锡烷基)吡啶,与化合物24类似地合成化合物192。LCMS(ES)[M+1]+m/z:384。1H NMR(300MHz,DMSO-d6)δ8.31(s,1H),7.88(s,1H),7.65(s,1H),4.17(s,2H),3.96(s,3H),3.26(s,3H),3.14(t,J=7.4Hz,2H),2.82(t,J=7.8Hz,2H),2.18(s,3H),2.04-1.94(m,2H),1.23(s,9H)。
实施例1.200及实施例1.201
合成N-叔丁基-2-{[2-(1-乙基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物193)及N-叔丁基-2-{[2-(1-乙基-1H-咪唑-5-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物194)
流程105
于空气氛围下在50℃下搅拌N-叔丁基-2-[[2-(3H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺(300.00mg,0.913mmol,1.00当量)、K2CO3(252.49mg,1.827mmol,2当量)及溴乙烷(149.30mg,1.370mmol,1.50当量)于DMF(5.00mL)中的溶液2h。通过制备型HPLC纯化粗产物,得到呈白色固体的N-叔丁基-2-[[2-(3-乙基咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺(化合物192,86mg,26.41%)及N-叔丁基-2-[[2-(1-乙基咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺(化合物193,102mg,31.32%)。
化合物193:LCMS(ES)[M+1]+m/z:357;1H NMR(300MHz,DMSO-d6)δ7.80(d,J=1.4Hz,1H),7.66(d,J=1.4Hz,1H),7.64(br,1H),4.09(s,2H),4.03(q,J=7.3Hz,2H),3.22(s,3H),3.08(t,J=7.2Hz,2H),2.73(t,J=7.8Hz,2H),2.05-1.86(m,2H),1.39(t,J=7.3Hz,3H),1.25(s,9H)。
化合物194:LCMS(ES)[M+1]+m/z:357;1H NMR(300MHz,DMSO-d6)δ7.75(d,J=1.3Hz,1H),7.61(d,J=1.2Hz,1H),7.58(br,1H),4.53(q,J=7.1Hz,2H),4.11(s,2H),3.19(s,3H),3.08(t,J=7.3Hz,2H),2.75(t,J=7.8Hz,2H),2.03-1.82(m,2H),1.31(t,J=7.1Hz,3H),1.24(s,9H)。
实施例1.202及实施例1.203
合成N-叔丁基-2-({2-[1-(2-羟乙基)-1H-咪唑-4-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物195)及N-叔丁基-2-({2-[1-(2-羟乙基)-1H-咪唑-5-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物196)
通过用2-(2-碘乙氧基)氧杂环己烷替换溴乙烷,与化合物193及化合物194类似地合成化合物195及化合物196。
化合物195:LCMS(ES)[M+1]+m/z:373;1H NMR(300MHz,DMSO-d6)δ7.77(d,J=1.4Hz,1H),7.62(br,1H),7.61(d,J=1.4Hz,1H),5.00(t,J=4.5Hz,1H),4.10(s,2H),4.03(t,J=5.4Hz,2H),3.69(q,J=5.1Hz,2H),3.20(s,3H),3.06(t,J=7.3Hz,2H),2.73(t,J=7.8Hz,2H),2.02-1.79(m,2H),1.25(s,9H)。
化合物196:LCMS(ES)[M+1]+m/z:373;1H NMR(300MHz,DMSO-d6)δ7.66(d,J=1.2Hz,1H),7.62(d,J=1.2Hz,1H),7.57(s,1H),4.89(t,J=5.3Hz,1H),4.56(t,J=5.5Hz,2H),4.09(s,2H),3.67(d,J=5.3Hz,2H),3.18(s,3H),3.08(t,J=7.3Hz,2H),2.75(t,J=7.8Hz,2H),2.00-1.90(m,2H),1.26(s,9H)。
实施例1.204
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(2-甲氧基嘧啶-5-基)乙酰胺(化合物197)
通过用2-甲氧基嘧啶-5-胺替换环己胺,与化合物144类似地合成化合物197。LCMS(ES)[M+1]+m/z:452。1H NMR(300MHz,DMSO-d6)δ10.51(s,1H),8.77(s,2H),8.44-8.42(d,J=5.6Hz,1H),7.77-7.76(d,J=2.5Hz,1H),7.03-7.01(dd,J=5.6,2.6Hz,1H),4.92(t,J=5.4Hz,1H),4.42(br,2H),4.05(t,J=4.9Hz,2H),3.88(s,3H),3.70(q,J=5.1Hz,2H),3.38(s,3H),3.21(t,J=7.2Hz,2H),2.83(t,J=7.9Hz,2H),2.10-2.00(m,2H)。
实施例1.205
合成N-(4-氟苯基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物198)
通过用4-氟苯胺替换环己胺,与化合物144类似地合成化合物198。LCMS(ES)[M+1]+m/z:438。1H NMR(300MHz,DMSO-d6)δ10.28(s,1H),8.43(d,J=5.6Hz,1H),7.78(d,J=2.5Hz,1H),7.60(dd,J=9.1,5.1Hz,2H),7.12(t,J=8.9Hz,2H),7.00(dd,J=5.6,2.6Hz,1H),4.90(s,1H),4.41(s,2H),4.02(t,J=4.8Hz,2H),3.67(t,J=4.8Hz,2H),3.36(s,3H),3.21(t,J=7.3Hz,2H),2.83(t,J=7.9Hz,2H),2.08-1.95(m,2H)。
实施例1.206
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺(化合物199)
通过用6-甲基吡啶-3-胺替换环己胺,与化合物144类似地合成化合物199。LCMS(ES)[M+1]+m/z:435。1H NMR(300MHz,DMSO-d6)δ10.37(s,1H),8.62(d,J=2.5Hz,1H),8.43(d,J=5.6Hz,1H),7.91(dd,J=8.4,2.6Hz,1H),7.77(d,J=2.5Hz,1H),7.18(d,J=8.4Hz,1H),7.01(dd,J=5.7,2.6Hz,1H),5.02(t,J=5.5Hz,1H),4.42(s,2H),4.03(t,J=4.8Hz,2H),3.69(q,J=5.1Hz,2H),3.38(s,3H),3.21(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.40(s,3H),2.08-2.01(m,2H)。
实施例1.207
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(6-甲基吡啶-3-基)乙酰胺(化合物200)
通过用6-甲基吡啶-3-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物200。LCMS(ES)[M+1]+m/z:405。1H NMR(300MHz,DMSO-d6)δ10.36(s,1H),8.60(d,J=2.7Hz,1H),8.44(d,J=5.7Hz,1H),7.89(dd,J=8.4,2.7Hz,1H),7.78(d,J=2.1Hz,1H),7.17(d,J=8.4Hz,1H),7.00(dd,J=5.7,2.7Hz,1H),4.43(s,2H),3.78(s,3H),3.37(s,3H),3.21(t,J=7.2Hz,2H),2.84(t,J=7.8Hz,2H),2.40(s,3H),2.11-1.96(m,2H)。
实施例1.208
合成N-(6-甲氧基吡啶-3-基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物201)
通过用5-氨基-2-甲氧基吡啶替换环己胺,与化合物142类似地合成化合物201。LCMS(ES)[M+1]+m/z:394;1H-NMR:(300MHz,DMSO-d6,ppm):δ10.27(s,1H),8.38(d,J=2.7Hz,1H),7.92(dd,J=8.7,2.7Hz,1H),7.69(d,J=1.2Hz,1H),7.60(d,J=1.2Hz,1H),6.79(d,J=8.7Hz,1H),4.35(s,2H),3.80(s,3H),3.64(s,3H),3.31(s,3H),3.13(t,J=7.2Hz,2H),2.74(t,J=7.8Hz,2H),2.00-1.90(m,2H)。
实施例1.209
合成N-(4-氟苯基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物202)
通过用4-氟苯胺替换环己胺,与化合物142类似地合成化合物202。LCMS(ES)[M+1]+m/z:381;1H-NMR:(300MHz,DMSO-d6,ppm):δ10.28(s,1H),7.70-7.60(m,4H),7.17-7.11(m,2H),4.35(s,2H),3.63(s,3H),3.31(s,3H),3.12(t,J=7.2Hz,2H),2.74(t,J=7.8Hz,2H),2.00-1.90(m,2H)。
实施例1.210
合成4-(4-甲氧基苯基)-1-[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]-1,4-二氮杂环庚-5-酮(化合物203)
通过用1,4-二氮杂环庚-5-酮盐酸盐替换1,4-二氮杂环庚-2-酮盐酸盐,与化合物188类似地合成化合物203。LCMS(ES+):[M+H]+=416.1。1H NMR(400MHz,甲醇-d4)δ7.16-6.73(m,8H),4.29-3.76(m,11H),3.06-2.85(m,6H)。
实施例1.211
合成(2R)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(1-甲基环丙基)丙酰胺(化合物204)
用1-甲基环丙-1-胺替换环己胺,与化合物108类似地合成化合物204。LCMS(ES+):[M+H]+=352.1。1H NMR(400MHz,DMSO-d6)δ8.78-8.71(m,1H),8.51(s,1H),8.43-8.35(m,1H),8.06-7.96(m,1H),7.59(ddd,J=7.6,4.7,1.2Hz,1H),5.02(q,J=7.0Hz,1H),3.25-3.14(m,5H),2.99-2.87(m,2H),2.14-1.93(m,2H),1.37(d,J=7.0Hz,3H),1.17(s,3H),0.61-0.41(m,4H)。
实施例1.212
合成(3S)-3-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-1-苯基吡咯烷-2-酮(化合物205)
通过用(2S)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸替换(2R)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸且用4-甲氧基-2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)吡啶,与化合物130类似地合成化合物205。LCMS(ES+):[M+H]+=416.3。1H NMR(400MHz,DMSO-d6)δ8.37(d,J=5.6Hz,1H),8.15(s,1H),7.72(d,1H),7.70-7.66(m,2H),7.40-7.34(m,2H),7.17-7.12(m,1H),6.97(dd,J=5.6,2.6Hz,1H),5.49-5.31(m,1H),3.99-3.86(m,2H),3.78(s,3H),3.24-3.19(m,5H),2.87-2.81(m,2H),2.46-2.30(m,2H),2.07-1.97(m,2H)。
实施例1.213
合成(3S)-1-(4-氟苯基)-3-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}吡咯烷-2-酮(化合物206)
通过用(2S)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸替换(2R)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸且用4-氟苯胺替换苯胺,与化合物130类似地合成化合物206。LCMS(ES+):[M+H]+=404.2。1H NMR(400MHz,DMSO-d6)δ8.54(d,J=4.7Hz,1H),8.15(d,J=2.5Hz,1H),7.73(dd,J=9.0,4.9Hz,2H),7.68-7.56(m,1H),7.39-7.33(m,1H),7.26-7.18(m,2H),5.29(s,1H),3.99-3.84(m,2H),3.25-3.21(m,5H),2.88-2.80(m,2H),2.46-2.27(m,2H),2.06-1.96(m,2H)。
实施例1.214
合成(3S)-3-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-1-(1-甲基环戊基)吡咯烷-2-酮(化合物207)
通过用(2S)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸替换(2R)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸且用氯化1-甲基环戊-1-铵替换苯胺,与化合物130类似地合成化合物207。LCMS(ES+):[M+H]+=392.2。1H NMR(400MHz,DMSO-d6)δ8.77-8.56(m,1H),8.25(d,J=7.8Hz,1H),7.95-7.79(m,1H),7.51-7.34(m,1H),5.36-5.12(m,1H),3.63-3.46(m,2H),3.22-3.14(m,2H),3.06(s,3H),2.82(t,J=8.0Hz,2H),2.33-2.22(m,1H),2.14-1.93(m,5H),1.78-1.54(m,6H),1.21(s,3H)。
实施例1.215
合成(3S)-3-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-1-(吡啶-4-基)吡咯烷-2-酮(化合物208)
通过用(2S)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸替换(2R)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸且用4-吡啶胺替换苯胺,与化合物130类似地合成化合物208。LCMS(ES+):[M+H]+=386.9。1H NMR(400MHz,甲醇-d4)δ8.53(d,J=4.9Hz,1H),8.48-8.44(m,2H),7.97(d,J=7.9Hz,1H),7.84-7.78(m,2H),7.49-7.42(m,1H),7.35-7.29(m,1H),4.14-3.91(m,3H),3.44(s,3H),2.99-2.93(m,2H),2.62-2.51(m,2H),2.17-2.11(m,2H)。
实施例1.216
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(5-甲氧基吡啶-2-基)乙酰胺(化合物209)
通过用5-甲氧基-2-氨基吡啶替换环己胺,与化合物144类似地合成化合物209。LCMS(ES)[M+1]+m/z:451。1H NMR(300MHz,DMSO-d6)δ10.54(s,1H),8.44-8.42(d,J=5.6Hz,1H),8.04-8.03(d,J=3.0Hz,1H),7.98-7.95(d,J=9.1Hz,1H),7.77-7.76(d,J=2.5Hz,1H),7.42-7.38(dd,J=9.1,3.0Hz,1H),6.99-6.96(dd,J=5.6,2.7Hz,1H),4.90-4.87(t,J=5.4Hz,1H),4.50(s,2H),4.02-3.96(q,J=7.4Hz,2H),3.80(s,3H),3.69-3.64(q,J=5.4Hz,2H),3.34(s,3H),3.22-3.17(t,J=7.3Hz,2H),2.85-2.80(t,J=7.8Hz,2H),2.05-1.98(m,2H)。
实施例1.217
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物210)
流程106
步骤1
向用惰性氮气氛围吹扫及维持的50mL 3颈圆底烧瓶中放入1-[(2-氯吡啶-4-基)氧基]-2-甲基丙-2-醇(1.00g,4.96mmol,1.00当量)、甲苯(30mL)、Sn2Me6(1.71g,5.22mmol,1.05当量)及Pd(PPh3)4(0.57g,0.49mmol,0.10当量)。在100℃下搅拌所得溶液2h。向此混合物中添加2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸乙酯(0.94g,3.48mmol,0.70当量)及Pd(PPh3)4(0.57g,0.49mmol,0.10当量)。在100℃下搅拌所得溶液过夜。冷却至环境温度后,真空浓缩所得混合物。将残余物施加至含二氯甲烷/甲醇(20:1)的硅胶柱上。由此产生300mg(15.11%)呈棕色油状物的2-([2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸乙酯。LCMS(ES)[M+1]+m/z401。
步骤2
向50mL圆底烧瓶中放入2-([2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸乙酯(300mg,0.75mmol,1.00当量)及MeOH(3mL)。之后在25℃下于搅拌下逐滴添加LiOH(36mg,1.50mmol,2.00当量)于H2O(1mL)中的溶液。将所得溶液在25℃下搅拌2hr且真空浓缩。用2×20mL二氯甲烷萃取所得溶液,且将水溶液分离并真空浓缩。由此产生150mg(52.92%)呈棕色固体的2-([2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸锂。LCMS(ES)[M-Li+H+1]+m/z 373。
步骤3
在0℃下向([2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸(200.00mg,0.537mmol,1.00当量)、5-氨基-2-甲氧基吡啶(80mg,0.64mmol,1.2当量)及DIEA(138.8mg,1.07mmol,2.0当量)于DMF(3mL)中的搅拌溶液中一次性添加HATU(265.4mg,0.69mmol,1.3当量)。在0 -25℃下搅拌5h后,通过制备型HPLC(柱,C18;移动相A:CH3CN,移动相B:水;流动速率:20mL/min)纯化所得混合物,得到呈灰白色固体的2-[2-[(2S)-2-(2-甲酰基-3-羟基苯氧基甲基)哌啶-1-羰基]苯基]乙酰胺(123.1mg,12.3%)。LCMS(ES)[M+1]+m/z:479。1H NMR(300MHz,DMSO-d6)δ10.27(s,1H),8.45(d,J=5.6Hz,1H),8.34(d,J=2.6Hz,1H),7.87(dd,J=8.9,2.7Hz,1H),7.79(d,J=2.6Hz,1H),7.03(dd,J=5.7,2.6Hz,1H),6.77(d,J=8.9Hz,1H),4.67(s,1H),4.41(s,2H),3.82-3.78(m,5H),3.37(s,3H),3.21(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.04-1.99(m,2H),1.17(s,6H)。
实施例1.218
合成N-叔丁基-2-[甲基(2-{4-[(氧杂环丁-3-基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物211)
用4-(氧杂环丁-3-基甲氧基)-2-(三丁基锡烷基)吡啶替换4-甲基-2-(三丁基锡烷基)-吡啶,与化合物24类似地合成化合物211。LCMS(ES+):[M+H]+=426.2。1H NMR(400MHz,DMSO-d6)δ8.60(d,J=5.8Hz,1H),7.95(d,J=2.6Hz,1H),7.82(s,1H),7.29(dd,J=5.9,2.6Hz,1H),4.77-4.69(m,2H),4.51-4.42(m,4H),4.22(s,2H),3.48-3.43(m,1H),3.37(s,3H),3.22-3.17(m,2H),2.96-2.87(m,2H),2.09-1.98(m,2H),1.24(s,9H)。
实施例1.219
合成(2R)-N-叔丁基-2-({2-[4-(二氟甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-4-(甲基硫基)丁酰胺(化合物212)
通过用(2R)-2-[(叔丁氧羰基)氨基]-4-(甲基硫基)丁酸替换(2R)-2-[(叔丁氧羰基)氨基]-3-甲基丁酸且用4-(二氟甲氧基)-2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)吡啶,与化合物114类似地合成化合物212。LCMS(ES+):[M+H]+=480.4。1H NMR(400MHz,DMSO-d6)δppm 1.16-1.20(m,9H)1.89-2.15(m,7H)2.34-2.46(m,2H)2.74-2.95(m,2H)3.00-3.14(m,4H)3.18-3.25(m,2H)4.97-5.09(m,1H)7.29(dd,J=5.48,2.35Hz,1H)7.57(t,J=72.78Hz,1H)7.81-7.87(m,1H)8.09(d,J=1.96Hz,1H)8.68(d,J=5.87Hz,1H)。
实施例1.220
合成2-({2-[4-(二氟甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物213)
通过用4-(二氟甲氧基)-2-(三丁基锡烷基)吡啶替换2-(三丁基锡烷基)-4-(2,2,2-三氟乙氧基)吡啶,与化合物177类似地合成化合物213。LCMS(ES+):[M+H]+=429.9。1HNMR(400MHz,DMSO-d6)δppm 2.04-2.16(m,2H)3.04(br t,J=7.83Hz,2H)3.26-3.28(m,2H)3.52(s,3H)3.70-3.74(m,3H)4.61-4.69(m,2H)6.32-6.38(m,1H)6.36(d,J=1.57Hz,1H)7.42-7.47(m,1H)7.43-7.83(m,2H)7.63(t,J=73.17Hz,1H)8.04-8.12(m,1H)8.77-8.85(m,1H)10.78-10.86(m,1H)。
实施例1.221
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(5-甲氧基吡啶-2-基)乙酰胺(化合物214)
用5-甲氧基吡啶-2-胺替换5-氨基-2-甲氧基吡啶,与化合物210类似地合成化合物214。LCMS(ES)[M+1]+m/z:479.3。1H NMR(300MHz,DMSO-d6)δ10.51(s,1H),8.44(d,J=5.6Hz,1H),8.28(s,1H),8.02(d,J=3.1Hz,1H),7.95(d,J=9.1Hz,1H),7.76(d,J=2.5Hz,1H),7.39(dd,J=9.1,3.1Hz,1H),7.00(dd,J=5.7,2.5Hz,1H),4.51(s,2H),3.81-3.76(m,5H),3.34(s,3H),3.19(t,J=7.3Hz,2H),2.83(t,J=7.9Hz,2H),2.08-1.95(m,2H),1.15(s,6H)。
实施例1.222
合成2-({2-[4-(环丙基甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物215)
用2-溴-4-(环丙基甲氧基)吡啶替换2-溴-4-(2,2,2-三氟乙氧基)吡啶,与化合物177类似地合成化合物215。LCMS(ES)[M+1]+m/z:443.1。1H NMR(400MHz,DMSO-d6)δ10.58(s,1H),8.47(d,J=5.8Hz,1H),7.78(d,J=2.6Hz,1H),7.50(d,J=2.2Hz,1H),7.10(dd,J=5.9,2.6Hz,1H),6.34(d,J=2.2Hz,1H),4.46(s,2H),3.92(d,J=7.1Hz,2H),3.71(s,3H),3.36(s,3H),3.20(d,J=14.8Hz,2H),2.87(t,J=7.9Hz,2H),2.09-1.94(m,2H),1.21(s,1H),0.63-0.52(m,2H),0.40-0.29(m,2H)。
实施例1.223
合成2-({2-[4-(二氟甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-氟吡啶-3-基)乙酰胺(化合物216)
用4-(二氟甲氧基)-2-(三丁基锡烷基)吡啶替换4-甲基-2-(三丁基锡烷基)-吡啶且用6-氟-3-吡啶胺替换叔丁胺,与化合物24类似地合成化合物216。LCMS(ES+):[M+H]+=445.1。1H NMR(400MHz,DMSO-d6)δppm 2.03-2.16(m,2H)3.02(br t,J=7.83Hz,2H)3.26-3.29(m,2H)3.53(s,2H)4.62-4.70(m,2H)7.11-7.18(m,1H)7.60(t,J=71.99Hz,1H)7.45-7.51(m,1H)8.05(br s,1H)8.10-8.18(m,1H)8.45(br s,1H)8.73-8.81(m,1H)10.80-10.89(m,1H)。
实施例1.224
合成2-({2-[4-(二氟甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(5-甲氧基吡啶-2-基)乙酰胺(化合物217)
用4-(二氟甲氧基)-2-(三丁基锡烷基)吡啶替换4-甲基-2-(三丁基锡烷基)-吡啶且用5-甲氧基吡啶-2-胺替换叔丁胺,与化合物24类似地合成化合物217。LCMS(ES+):[M+H]+=456.9。1H NMR(400MHz,DMSO-d6)δppm 2.04-2.13(m,2H)3.00(br t,J=7.83Hz,2H)3.28(br d,J=7.04Hz,2H)3.50(s,3H)3.77-3.80(m,3H)4.65-4.72(m,2H)7.39(dd,J=9.00,3.13Hz,1H)7.41-7.80(m,1H)7.46(dd,J=5.48,2.35Hz,1H)7.87-7.96(m,1H)8.03(d,J=2.74Hz,1H)8.04-8.08(m,1H)8.77(d,J=5.87Hz,1H)10.73-10.79(m,1H)。
实施例1.225
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物218)
通过用3-(三丁基锡烷基)异喹啉替换2-(三丁基锡烷基)-4-(2,2,2-三氟乙氧基)吡啶,与化合物177类似地合成化合物218。LCMS(ES+):[M+H]+=414.0。1H NMR(400MHz,DMSO-d6)δppm 2.08-2.19(m,2H)3.10(br t,J=7.83Hz,2H)3.30-3.36(m,2H)3.61(br s,3H)3.75-3.83(m,3H)4.61-4.72(m,2H)6.32-6.42(m,1H)7.45-7.54(m,1H)7.86-7.95(m,1H)7.95-8.08(m,2H)8.33(br d,J=8.22Hz,1H)8.79-8.98(m,1H)9.52-9.62(m,1H)10.98-11.15(m,1H)
实施例1.226
合成N-(6-甲氧基吡啶-3-基)-2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物219)
通过用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺且用5-(三甲基锡烷基)-1H-吡唑并[3,4-c]吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶,与化合物135类似地合成化合物219。LCMS(ES)[M+1]+m/z:431.2;1HNMR(300MHz,DMSO-d6,ppm)δ13.70(s,1H),10.37(s,1H),9.06(s,1H),8.70(d,J=1.2Hz,1H),8.41(t,J=2.4Hz,1H),8.09(s,1H),7.95(ddd,J=8.9,2.8,1.5Hz,1H),6.80(d,J=8.9Hz,1H),4.42(s,2H),3.80(s,3H),3.39(s,3H),3.20(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.11-1.93(m,2H)。
实施例1.227
合成N-(1-甲基-1H-吡唑-4-基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物220)
通过用1-甲基-4-(三丁基锡烷基)-1H-咪唑替换2-(三丁基锡烷基)-4-(2,2,2-三氟乙氧基)吡啶,与化合物177类似地合成化合物220。LCMS(ES)[M+1]+m/z:367.2;1H NMR(400MHz,dmso)δ10.73(s,1H),8.29(s,1H),8.16(s,1H),7.53(d,J=2.2Hz,1H),6.35(d,J=2.2Hz,1H),4.58(s,3H),4.55(s,2H),3.77(s,3H),3.73(s,3H),3.16(s,2H),2.92(t,J=7.9Hz,2H),2.09-1.96(m,2H)。
实施例1.228
合成N-(6-氟吡啶-3-基)-2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物221)
通过用3-(三丁基锡烷基)异喹啉替换4-甲氧基-2-(三甲基锡烷基)吡啶且用6-氟-3-吡啶胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物221。LCMS(ES+):[M+H]+=429.2。1H NMR(400MHz,DMSO-d6)δppm 1.99-2.08(m,2H)2.84-2.91(m,2H)3.20-3.26(m,2H)3.42(s,3H)4.46-4.51(m,2H)7.10-7.16(m,1H)7.67-7.73(m,1H)7.73-7.79(m,1H)7.81-7.86(m,1H)8.13-8.17(m,1H)8.17-8.24(m,1H)8.43-8.48(m,1H)8.71-8.75(m,1H)9.32-9.37(m,1H)10.67-10.74(m,1H)
实施例1.229
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(6-甲基吡啶-3-基)乙酰胺(化合物222)
通过用3-(三丁基锡烷基)异喹啉替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-甲基-2-吡啶胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物222。LCMS(ES+):[M+H]+=425.2。1H NMR(400MHz,DMSO-d6)δppm 2.09-2.19(m,2H)2.52-2.60(m,3H)3.11(br t,J=7.83Hz,2H)3.35-3.37(m,2H)3.64(s,3H)4.84-4.97(m,2H)7.66-7.75(m,1H)7.85-7.93(m,1H)7.93-8.00(m,1H)8.28-8.37(m,2H)8.45-8.65(m,1H)9.02-9.10(m,1H)9.18-9.28(m,1H)9.51-9.60(m,1H)12.14-12.47(m,1H)
实施例1.230
合成2-{[2-(4-乙氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物223)
通过用现场制备的4-乙氧基-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物223。LCMS(ES)[M+1]+m/z:435。1H NMR(300MHz,DMSO-d6)δ10.28(s,1H),8.46(d,J=5.7Hz,1H),8.35(d,J=2.6Hz,1H),7.89(dd,J=8.9,2.7Hz,1H),7.78(d,J=2.6Hz,1H),7.06(dd,J=5.6,2.6Hz,1H),6.78(d,J=8.8Hz,1H),4.42(s,2H),4.06(q,J=7.0Hz,2H),3.80(s,3H),3.40(s,3H),3.23(t,J=7.3Hz,2H),2.86(t,J=7.7Hz,2H),2.11-1.97(m,2H),1.28(t,J=6.9Hz,3H)。
实施例1.231
合成2-({2-[4-(环丙基甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物224)
通过用现场制备的4-环丙基甲氧基-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物224。LCMS(ES)[M+1]+m/z:461。1H NMR(300MHz,DMSO-d6)δ10.25(s,1H),8.42(d,J=5.6Hz,1H),8.33(d,J=2.7Hz,1H),7.86(dd,J=8.9,2.7Hz,1H),7.76(d,J=2.5Hz,1H),6.98(dd,J=5.6,2.6Hz,1H),6.77(d,J=8.9Hz,1H),4.39(s,2H),3.86(d,J=7.1Hz,2H),3.80(s,3H),3.37(s,3H),3.21(t,J=7.2Hz,2H),2.83(t,J=7.8Hz,2H),2.10-1.911(m,2H),1.38-1.09(m,1H),0.56(q,J=5.5Hz,2H),0.30(d,J=5.2Hz,2H)。
实施例1.232
合成2-({2-[4-(二氟甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物225)
通过用现场制备的4-(二氟甲氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物225。LCMS(ES)[M+1]+m/z:457。1H NMR(300MHz,DMSO-d6)δ10.23(br,1H),8.63(d,J=5.7Hz,1H),8.35(d,J=2.7Hz,1H),7.98(d,J=2.4Hz,1H),7.88(dd,J=9.0,2.7Hz,1H),7.49(t,J=72.6Hz 1H,CHF2),7.26(dd,J=5.7,2.4Hz,1H),6.75(d,J=9.0Hz,1H),4.43(s,2H),3.80(s,3H),3.37(s,3H),3.21(t,J=7.5Hz,2H),2.82(t,J=7.8Hz,2H),2.07-1.96(m,2H)。
实施例1.233
合成N-叔丁基-2-[(2-{2H-[1,3]间二氧杂环戊烯并[4,5-c]吡啶-6-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物226)
通过用6-(三甲基锡烷基)-[1,3]间二氧杂环戊烯并[4,5-c]吡啶替换4-甲基-2-(三丁基锡烷基)吡啶,与化合物24类似地合成化合物226。LCMS(ES)[M+1]+m/z:384。1H NMR(300MHz,DMSO-d6)δ8.20(s,1H),7.95(s,1H),7.71(s,1H),6.20(s,2H),4.10(s,2H),3.32(s,3H),3.14(t,J=7.4Hz,2H),2.79(t,J=7.9Hz,2H),2.05-1.89(m,2H),1.25(s,9H)。
实施例1.234
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物227)
通过用3-(三丁基锡烷基)异喹啉替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物227。LCMS(ES)[M+1]+m/z:457。1H NMR(300MHz,DMSO-d6)δ10.23(br,1H),8.63(d,J=5.7Hz,1H),8.35(d,J=2.7Hz,1H),7.98(d,J=2.4Hz,1H),7.88(dd,J=9.0,2.7Hz,1H),7.49(t,J=72.6Hz 1H,CHF2),7.26(dd,J=5.7,2.4Hz,1H),6.75(d,J=9.0Hz,1H),4.43(s,2H),3.80(s,3H),3.37(s,3H),3.21(t,J=7.5Hz,2H),2.82(t,J=7.8Hz,2H),2.07-1.96(m,2H)。
实施例1.235
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物228)
通过用3-(三丁基锡烷基)异喹啉替换4-甲氧基-2-(三甲基锡烷基)吡啶且用3-氨基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物228。LCMS(ES)[M+1]+m/z:411。1H NMR(300MHz,DMSO-d6)δ9.48(s,1H),9.28(d,J=2.4Hz,1H),9.14(s,1H),8.82(s,1H),8.52(s,1H),8.33-8.20(m,2H),8.00(t,J=7.1Hz,1H),7.93-7.79(m,2H),4.90(s,2H),3.57(s,3H),3.38-3.19(s,2H),3.18-2.99(m,2H),2.09-2.00(m,2H)。
实施例1.236
合成N-(6-甲氧基吡啶-3-基)-2-[甲基({2-[4-(三氟甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物229)
通过用4-(三氟甲氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物229。LCMS(ES)[M+1]+m/z:475。1H NMR(300MHz,DMSO-d6)δ10.22(s,1H),8.75(d,J=5.5Hz,1H),8.36(t,J=2.2Hz,1H),8.09(d,J=2.37Hz 1H),7.87(ddd,J=8.9,2.8,1.3Hz,1H),7.46(dd,J=5.3,2.1Hz,1H),6.77(d,J=8.8Hz,1H),4.41(s,2H),3.80(s,3H),3.38(s,3H),3.22(t,J=7.3Hz,2H),2.85(t,J=7.8Hz,2H),2.10-1.922(m,2H)。
实施例1.237
合成N-(6-甲氧基吡啶-3-基)-2-[甲基({2-[4-(三氟甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物230)
通过用4-(三氟甲氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物230。LCMS(ES)[M+1]+m/z:475。1H NMR(300MHz,DMSO-d6)δ10.22(s,1H),8.75(d,J=5.5Hz,1H),8.36(t,J=2.2Hz,1H),8.09(d,J=2.37Hz 1H),7.87(ddd,J=8.9,2.8,1.3Hz,1H),7.46(dd,J=5.3,2.1Hz,1H),6.77(d,J=8.8Hz,1H),4.41(s,2H),3.80(s,3H),3.38(s,3H),3.22(t,J=7.3Hz,2H),2.85(t,J=7.8Hz,2H),2.10-1.922(m,2H)。
实施例1.238
合成2-[甲基({2-[4-(三氟甲氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物231)
通过用4-(三氟甲氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用1-甲基吡唑-4-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物231。LCMS(ES)[M+1]+m/z:448。1H NMR(300MHz,DMSO-d6)δ10.16(s,1H),8.78(d,J=5.6Hz,1H),8.10(d,J=2.3Hz,1H),7.82(s,1H),7.47(dd,J=5.7,1.4Hz,1H),7.39(s,1H),4.36(s,2H),3.75(s,3H),3.28(s,3H),3.26-3.13(m,2H),2.85(t,J=7.8Hz,2H),2.10-1.93(m,2H)。
实施例1.239
合成2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(1-甲基-1H-吡唑-3-基)乙酰胺(化合物232)
通过用5-(三甲基锡烷基)-1H-吡唑并[3,4-c]吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用2-甲基嘧啶-5-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物232。LCMS(ES)[M+1]+m/z:404。1H NMR(300MHz,DMSO-d6)δ13.67(s,1H),10.68(s,1H),9.08(s,1H),8.68(d,J=1.4Hz,1H),8.12(s,1H),7.52(d,J=2.3Hz,1H),6.41(d,J=2.3Hz,1H),4.41(s,2H),3.76(s,3H),3.38(s,3H),3.18(t,J=7.4Hz,2H),2.83(t,J=7.8Hz,2H),2.03-1.98(m,2H)。
实施例1.240
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(5-甲氧基吡啶-2-基)乙酰胺(化合物233)
通过用3-(三丁基锡烷基)异喹啉替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-甲氧基吡啶-2-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物233。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6)δ10.71(s,1H),9.35(s,1H),8.72(s,1H),8.16(0.4HCOOH),8.14(d,J=7.8Hz,1H),8.10(d,J=3.0Hz,1H),7.99(d,J=9.0Hz,1H),7.85-7.63(m,3H),7.38(dd,J=9.1,3.1Hz,1H),4.51(s,2H),3.79(s,3H),3.41(s,3H),3.22(t,J=7.3Hz,2H),2.87(t,J=7.8Hz,2H),2.07-1.98(m,2H)。
实施例1.241
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-[6-(三氟甲氧基)吡啶-3-基]乙酰胺(化合物234)
通过用3-(三丁基锡烷基)异喹啉替换4-甲氧基-2-(三甲基锡烷基)吡啶且用6-(三氟甲氧基)吡啶-3-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物234。LCMS(ES)[M+1]+m/z:495。1H NMR(300MHz,DMSO-d6)δ11.51(br,1H),9.56(s,1H),9.10(s,1H),8.70(s,1H),8.32(d,J=8.1Hz,2H),8.10(s,1H),7.98-7.85(m,2H),7.27(d,J=8.8Hz,1H),4.83(s,2H),3.63(s,3H),3.37-3.22(m,2H),3.11(t,J=8.0Hz,2H),2.20-2.09(m,2H)。
实施例1.242
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(5-甲基吡啶-3-基)乙酰胺(化合物235)
通过用3-(三丁基锡烷基)异喹啉替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-甲基吡啶-3-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物235。LCMS(ES)[M+1]+m/z:425。1H NMR(300MHz,DMSO-d6)δ10.52(s,1H),9.36(s,1H),8.72(s,1H),8.61(d,J=2.4Hz,1H),8.20-8.11(m,2H),8.08(d,J=1.9Hz,1H),7.92(s,1H),7.85-7.64(m,3H),4.48(s,2H),3.43(s,3H),3.24(s,2H),2.88(t,J=7.8Hz,2H),2.21(s,3H),2.07-2.01(m,2H)。
实施例1.243
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(1-甲基-1H-咪唑-4-基)乙酰胺(化合物236)
通过用3-(三丁基锡烷基)异喹啉替换4-甲氧基-2-(三甲基锡烷基)吡啶且用1-甲基咪唑-4-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物236。LCMS(ES)[M+1]+m/z:414.3。1H NMR(300MHz,DMSO-d6)δ10.61(s,1H),9.37(d,J=3.1Hz,1H),8.71(d,J=2.9Hz,1H),8.15(dd,J=8.1,3.1Hz,1H),7.95-7.86(m,1H),7.82-7.64(m,2H),7.41(t,J=2.1Hz,1H),7.20-7.11(m,1H),4.44(s,2H),3.57(s,3H),3.38(s,3H),3.19(t,J=7.4Hz,2H),2.86(d,J=7.7Hz,2H),2.05-2.01(m,2H)。
实施例1.244
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(1-甲基-1H-吡唑-3-基)乙酰胺(化合物237)
通过用3-(三丁基锡烷基)异喹啉替换4-甲氧基-2-(三甲基锡烷基)吡啶且用1-甲基吡唑-3-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物237。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ10.75(s,1H),9.37(s,1H),8.69(s,1H),8.15(d,J=8.3Hz,1H),7.88(d,J=8.1Hz,1H),7.83-7.74(m,1H),7.74-7.66(m,1H),7.52(d,J=2.3Hz,1H),6.42(d,J=2.2Hz,1H),4.42(s,2H),3.77(s,3H),3.40(s,3H),3.21(t,J=7.2Hz,2H),2.86(t,J=7.8Hz,2H),2.08-2.00(m,2H)。
实施例1.245
合成2-({2-[4-(2-甲氧基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物238)
通过用4-(2-甲氧基乙氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物238。LCMS(ES)[M+1]+m/z:465。1H NMR(300MHz,DMSO-d6)δ10.29(s,1H),8.46(d,J=5.7Hz,1H),8.35(d,J=2.7Hz,1H),8.14(s,HCOOH),7.89(dd,J=9.0,2.7Hz,1H),7.79(d,J=2.7Hz,1H),7.05(dd,J=5.7,2.7Hz,1H),6.78(d,J=9.0Hz,1H),4.42(s,2H),4.16-4.09(m,2H),3.81(s,3H),3.62-3.60(m,2H),3.39(s,3H),3.29(s,3H),3.22(t,J=7.2Hz,2H),2.85(t,J=7.8Hz,2H),2.07-1.96(m,2H)。
实施例1.246
合成N-叔丁基-2-({2-[4-(2-甲氧基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物239)
通过用4-(2-甲氧基乙氧基)-2-(三甲基锡烷基)吡啶替换4-甲基-2-(三甲基锡烷基)吡啶,与化合物24类似地合成化合物239。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.7Hz,1H),8.14(s,HCOOH),7.86(d,J=2.4Hz,1H),7.69(s,1H),7.06(dd,J=5.7,2.7Hz,1H),4.27-4.24(m,2H),4.13(s,2H),3.72-3.69(m,2H),3.32(s,3H),3.27(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.05-1.94(m,2H),1.25(s,9H)。
实施例1.247
合成N-(5-氟吡啶-3-基)-2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物240)
通过用4-(2-甲氧基乙氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-氟吡啶-3-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物240。LCMS(ES)[M+1]+m/z:429.2。1H NMR(300MHz,DMSO-d6)δ10.87(s,1H),9.35(s,1H),8.71(s,1H),8.63(t,J=1.7Hz,1H),8.25(d,J=2.6Hz,1H),8.20-8.03(m,3H),7.81(d,J=8.3Hz,1H),7.82-7.64(m,2H),4.51(s,2H),3.43(s,3H),3.24(t,J=7.3Hz,2H),2.88(t,J=7.8Hz,2H),2.04(p,J=7.6Hz,2H)。
实施例1.248
合成N-叔丁基-2-({2-[4-(2-氟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物241)
通过用4-(2-氟乙氧基)-2-(三甲基锡烷基)吡啶替换4-甲基-2-(三甲基锡烷基)吡啶,与化合物24类似地合成化合物241。LCMS(ES)[M+1]+m/z:429.2。1H NMR(300MHz,DMSO-d6)δ8.50(d,J=5.6Hz,1H),7.89(d,J=2.6Hz,1H),7.69(s,1H),7.08(dd,J=5.6,2.6Hz,1H),4.91-4.82(m,1H),4.75-4.66(m,1H),4.48-4.44(m,1H),4.40-4.31(m,1H),4.12(s,2H),3.27(s,3H),3.15(t,J=7.4Hz,2H),2.81(t,J=7.9Hz,2H),2.02-1.97(m,2H),1.24(s,9H)。
实施例1.249
合成2-({2-[4-(2-氟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物242)
通过用4-(2-氟乙氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶且用5-氨基-2-甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物242。LCMS(ES)[M+1]+m/z:453。1H NMR(300MHz,DMSO-d6)δ10.27(s,1H),8.46(d,J=5.6Hz,1H),8.36(d,J=2.6Hz,1H),7.88(dd,J=8.9,2.7Hz,1H),7.80(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),6.77(d,J=8.9Hz,1H),4.84-4.75(m,1H),4.65-4.62(m,1H),4.40(s,2H),4.37-4.30(m,1H),4.28-4.19(m,1H),3.80(s,3H),3.38(s,3H),3.22(t,J=7.2Hz,2H),2.84(t,J=7.8Hz,2H),2.04-1.99(m,2H)。
实施例1.250
合成2-({2-[4-(2-氟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物243)
通过用4-(2-氟乙氧基)-2-(三甲基锡烷基)吡啶替换4-甲基-2-(三甲基锡烷基)吡啶且用1-甲基吡唑-4-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物243。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6)δ10.23(s,1H),8.48(d,J=5.6Hz,1H),7.84(s,1H),7.78(d,J=2.6Hz,1H),7.40(s,1H),7.05(dd,J=5.6,2.6Hz,1H),4.85-4.79(m,1H),4.69-4.62(m,1H),4.36-4.32(m,3H),4.28-4.21(m,1H),3.76(s,3H),3.35(s,3H),3.20(t,J=7.4Hz,2H),2.83(t,J=7.9Hz,2H),2.05-1.95(m,2H)。
实施例1.251
合成N-(6-甲氧基吡啶-3-基)-2-{甲基[2-(1,7-萘啶-6-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物244)
流程107
步骤1
向1L圆底烧瓶中放入3-甲基吡啶-2-甲腈(12.00g,101.58mmol,1.00当量)、NBS(36.10g,203.16mmol,2.00当量)、CCl4(500.00mL)及AIBN(1.67g,10.16mmol,0.10当量)。在80℃下搅拌所得溶液5h。将反应溶液冷却至室温,浓缩以移除溶剂。通过含乙酸乙酯/石油醚(1/2)的硅胶柱纯化残余物。由此产生9.0g(45%)呈黄色油状物的3-(溴甲基)吡啶-2-甲腈。LCMS(ES)[M+1]+m/z:197。
步骤2
向250mL圆底烧瓶中放入3-(溴甲基)吡啶-2-甲腈(9.00g,45.68mmol,1.00当量)、CH3CN(100.00mL)、TMSCN(13.59g,136.99mmol,3.00当量)及K2CO3(12.62g,91.31mmol,2.00当量)。在50℃下搅拌所得溶液12h。将反应物冷却至室温,过滤且浓缩滤液,通过含乙酸乙酯/石油醚(2/3)的硅胶柱纯化残余物。由此产生3.0g(46%)呈黄色固体的3-(氰基甲基)吡啶-2-甲腈。LCMS(ES)[M+1]+m/z:144。
步骤3
向100mL 3颈圆底烧瓶中放入HBr(40%于H2O中)(20.00mL)、HOAc(20.00mL)、3-(氰基甲基)吡啶-2-甲腈(3.00g,20.96mmol,1.00当量)。在室温下搅拌所得溶液1h。过滤溶液,且用H2O(20.00mL)稀释滤液,用NaHCO3固体将溶液的pH值调节至7,用3×50mL乙酸乙酯萃取。使合并的有机相经无水硫酸钠干燥,过滤,且真空浓缩滤液。由此产生2.2g(47%)呈黄色油状物的8-溴-1,7-萘啶-6-胺。LCMS(ES)[M+1]+m/z:224。
步骤4
向250mL圆底烧瓶中放入8-溴-1,7-萘啶-6-胺(2.20g,9.82mmol,1.00当量)、EtOH(100.00mL)、KOH(663mg,11.82mmol,1.20当量)、Pd/C(300mg)。将混合物于2-3atm的压力的氢气氛围下在室温下搅拌2h,经由硅藻土过滤,且真空浓缩滤液。由此产生1.3g(92%)呈黄色油状物的1,7-萘啶-6-胺。LCMS(ES)[M+1]+m/z:146。
步骤5
向250mL 3颈圆底烧瓶中放入1,7-萘啶-6-胺(1.30g,8.97mmol,1.00当量)、HCl(c)(40.00mL)。之后在0℃下添加NaNO2(1.36g,19.73mmol,2.20当量)且搅拌30min。向此混合物中添加CuCl(897mg,8.97mmol,1.00当量),在室温下再搅拌所得溶液2h。在0℃下用NaOH(4N)将溶液的pH值调节至7,用3×50mL乙酸乙酯萃取。使合并的有机相经无水硫酸钠干燥,过滤且减压浓缩滤液。通过含乙酸乙酯/石油醚(40%)的硅胶柱纯化残余物。由此产生530mg(36%)呈黄色油状物的6-氯-1,7-萘啶。LCMS(ES)[M+1]+m/z:165。
步骤6
向用惰性氮气氛围吹扫及维持的40mL小瓶中放入6-氯-1,7-萘啶(530mg,3.22mmol,1.00当量)、二噁烷(10.00mL)、Sn2Me6(1.16g,3.54mmol,1.10当量)及Pd(dppf)Cl2(234mg,0.32mmol,0.10当量)。在100℃下搅拌混合物3h。混合物不经纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:295。
步骤7
在用惰性氮气氛围吹扫及维持的40mL小瓶中放入6-(三甲基锡烷基)-1,7-萘啶(最后步骤的反应溶液)、二噁烷(5.00mL)、2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸乙酯(350mg,1.30mmol,0.70当量)及Pd(dppf)Cl2(139mg,0.19mmol,0.10当量)。在100℃下搅拌混合物12h。将所得混合物冷却至室温,浓缩以移除溶剂。通过含THF/PE(80%)的硅胶柱纯化残余物。由此产生507mg(75%)呈黄色油状物的N-(2-(1,7-萘啶-6-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯。LCMS(ES)[M+1]+m/z:364。
步骤8
向40mL小瓶中放入2-[甲基[2-(1,7-萘啶-6-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸乙酯(507mg,1.40mmol,1.00当量)、EtOH(5.00mL)、LiOH·H2O(117mg,2.79mmol,2.00当量)及H2O(10.00mL)。在室温下搅拌所得溶液1h。将反应溶液浓缩且通过使用以下条件的制备型HPLC纯化:柱,C18-120g,移动相,水及CH3CN,9min内自5%增加至10%,检测器,254nm。冷冻干燥洗脱份,由此产生161mg(34%)呈白色固体的2-[甲基[2-(1,7-萘啶-6-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸锂。LCMS(ES)[M-Li+1]+m/z:336。
步骤9
向8mL小瓶中放入2-[甲基[2-(1,7-萘啶-6-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸锂(161mg,0.47mmol,1.00当量)、DMF(4.00mL)、5-氨基-2-甲氧基吡啶(70mg,0.57mmol,1.20当量)、DIEA(122mg,0.95mmol,2.00当量)及HATU(215mg,0.57mmol,1.20当量)。在室温下搅拌所得溶液2h。通过使用以下条件的制备型HPLC纯化反应溶液:柱,Sunfire Prep C18 OBD柱,50*250mm 5um,移动相,水(0.1%FA)及CH3CN(15min内自5%相B达至30%),检测器,UV 254nm。由此产生89.6mg(43.02%)呈灰白色固体的N-(6-甲氧基吡啶-3-基)-2-{甲基[2-(1,7-萘啶-6-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺。LCMS:(ES,m/z)[M+H]+:442。1H NMR(300MHz,DMSO-d6)δ10.35(s,1H),9.44(s,1H),9.07(dd,J=4.2,1.5Hz,1H),8.82(s,1H),8.39(d,J=2.7Hz,1H),8.33(d,J=8.4Hz,1H),8.15(s,1H),7.93(dd,J=9.0,2.7Hz,1H),7.79(dd,J=8.4,4.2Hz,1H),6.77(d,J=9.0Hz,1H),4.48(s,2H),3.79(s,3H),3.42(s,3H),3.24(t,J=7.5Hz,2H),2.88(t,J=7.8Hz,2H),2.09-1.98(m,2H)。
实施例1.252
合成(2R)-3-甲基-N-(1-甲基-1H-吡唑-4-基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丁酰胺(化合物246)
流程108
步骤1
向40mL小瓶中放入2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(2.00g,10.58mmol,1.00当量)、(2R)-2-氨基-3-甲基丁酸甲酯(1.67g,12.73mmol,1.20当量)、NMP(20.00mL)及DIEA(4.10g,31.74mmol,3.00当量)。在80℃下搅拌所得溶液过夜。通过使用以下条件的制备型HPLC纯化粗产物(4g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%HCOOH)及CAN(11min内自50%相B达至90%);检测器,254nm。由此产生2.2g(73.28%)呈黄色固体的(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)缬氨酸甲酯。LCMS(ES)[M+1]+m/z:284。
步骤2
向100mL 3颈圆底烧瓶中放入(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)缬氨酸甲酯(2.20g,7.75mmol,1.00当量)、DMF(30.00mL)。之后在0℃下分批添加NaH(0.28g,11.67mmol,1.50当量)。在0℃下于搅拌下向其逐滴添加碘甲烷(1.32g,9.30mmol,1.20当量)。在室温下搅拌所得溶液2h。随后通过添加20mL水/冰将反应物淬灭,用3×30mL乙酸乙酯萃取。将有机层合并,经无水硫酸钠干燥且浓缩。将残余物施加至含THF/PE(6%)的硅胶柱上。由此产生1.9g(82.30%)呈黄色固体的N-(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基缬氨酸甲酯。LCMS(ES)[M+1]+m/z:298。
步骤3
向100mL圆底烧瓶中放入N-(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基缬氨酸甲酯(1.90g,6.38mmol,1.00当量)、2-(三丁基锡烷基)吡啶(3.05g,8.28mmol,1.30当量)、二噁烷(30.00mL)及Pd(dppf)Cl2(0.47g,0.64mmol,0.10当量)。在100℃下搅拌所得溶液过夜。浓缩所得混合物。将残余物施加至含THF/PE(70-100%)的硅胶柱上。由此产生1.5g(69.06%)呈黄色油状物的N-甲基-N-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)缬氨酸甲酯。LCMS(ES)[M+1]+m/z:341。
步骤4
向100mL圆底烧瓶中放入N-甲基-N-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)缬氨酸甲酯(1.50g,4.41mmol,1.00当量)、MeOH(10.00mL)、H2O(10.00mL)。之后在0℃下分批添加NaOH(0.35g,8.85mmol,2.00当量)。在室温下搅拌所得溶液过夜。用柠檬酸将溶液的pH值调节至5-6。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridgePrep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%HCOOH)及CAN(11min内自10%相B达至40%);检测器,254nm。由此产生800mg(55.63%)呈黄色固体的3-甲基-2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]丁酸。LCMS(ES)[M+1]+m/z:327。
步骤5
向40mL小瓶中放入3-甲基-2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]丁酸(330.00mg,1.01mmol,1.00当量)、5-氨基-2-甲氧基吡啶(125.51mg,1.01mmol,1.00当量)、DMF(5.00mL)及DIEA(261.34mg,2.02mmol,2.00当量)。之后在0℃下分批添加T3P(386.03mg,1.21mmol,1.20当量)。在室温下搅拌所得溶液3h。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3·H2O)及CAN(11min内自50%相B达至90%);检测器,254nm。由此产生310mg(70.89%)呈白色固体的N-(6-甲氧基吡啶-3-基)-3-甲基-2-[甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]丁酰胺。LCMS(ES)[M+1]+m/z:433。
通过使用以下条件的制备型手性HPLC纯化粗产物(310mg):柱,CHIRALPAK IC,20*250mm,5μm;移动相,正己烷/DCM=5/1及IPA(15%,25min);检测器,254nM。由此产生83.7mg(27.00%)呈白色固体的(2R)-3-甲基-N-(1-甲基-1H-吡唑-4-基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丁酰胺。手性HPLC保留时间:3.83min(条件:柱,YMC Cellulose-SB,100*4.6mm,3μm;移动相,正己烷/DCM=5/1及异丙醇(10%,6min))。LCMS(ES,m/z):[M+H]+:433。1H NMR(300MHz,DMSO-d6)δ10.75(s,1H),8.80-8.71(m,1H),8.42(d,J=7.9Hz,1H),8.31(d,J=2.6Hz,1H),8.04-7.87(m,2H),7.60-7.50(m,1H),6.76(d,J=8.9Hz,1H),4.75(d,J=11.1Hz,1H),3.78(s,3H),3.29-3.21(m,1H),3.18(s,3H),3.15-3.01(m,1H),3.01-2.74(m,2H),2.49-2.39(m,1H),2.14-1.95(m,2H),1.02(d,J=6.4Hz,3H),0.94(d,J=6.6Hz,3H)。
实施例1.253
合成(2S)-N-(6-甲氧基吡啶-3-基)-3-甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丁酰胺(化合物247)
通过使用以下条件的制备型手性HPLC纯化来自化合物246步骤1的粗产物(310mg):柱,CHIRALPAK IC,30*250mm,5μm;移动相,正己烷/DCM=5/1及IPA(15%,25min);检测器,254。由此产生105.5mg(34.03%)呈白色固体的(2S)-N-(6-甲氧基吡啶-3-基)-3-甲基-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丁酰胺。手性HPLC保留时间:5.19min(条件:柱,YMC Cellulose-SB,100*4.6mm,3μm;移动相,正己烷/DCM=5/1及异丙醇(10%,6min))。LCMS(ES,m/z):[M+H]+:433。1H NMR(300MHz,DMSO-d6)δ10.74(s,1H),8.75(dt,J=4.6,1.5Hz,1H),8.42(dt,J=8.0,1.2Hz,1H),8.31(d,J=2.6Hz,1H),8.04-7.87(m,2H),7.55(ddd,J=7.5,4.8,1.3Hz,1H),6.76(d,J=8.9Hz,1H),4.75(d,J=11.0Hz,1H),3.78(s,3H),3.30-3.20(m,1H),3.18(s,3H),3.15 -3.01(m,1H),3.01-2.74(m,2H),2.51-2.37(m,1H),2.17-1.91(m,2H),1.02(d,J=6.4Hz,3H),0.94(d,J=6.6Hz,3H)。
实施例1.254
合成(2R)-3-甲基-N-(1-甲基-1H-吡唑-4-基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丁酰胺(化合物248)
用1-甲基吡唑-4-胺替换5-氨基-2-甲氧基吡啶,与化合物246类似地合成化合物248。手性HPLC保留时间:3.68min(条件:柱,YMC Cellulose-SB,100*4.6mm,3μm;移动相,正己烷及乙醇(10%,8min))。LCMS(ES)[M+1]+m/z:406。1H NMR(300MHz,DMSO-d6)δ10.78(s,1H),8.85(ddd,J=4.8,1.7,0.7Hz,1H),8.41(dt,J=7.9,1.2Hz,1H),7.99(td,J=7.7,1.8Hz,1H),7.88(s,1H),7.57(ddd,J=7.5,4.8,1.3Hz,1H),7.34(s,1H),4.70(d,J=11.1Hz,1H),3.75(s,3H),3.23(dt,J=15.9,8.0Hz,1H),3.16(s,3H),3.14-3.00(m,1H),3.00-2.74(m,2H),2.49-2.35(m,1H),2.15-1.90(m,2H),0.97(d,J=6.4Hz,3H),0.93(d,J=6.6Hz,3H)。
实施例1.255
合成(2R)-3-甲基-N-(1-甲基-1H-吡唑-4-基)-2-{甲基[2-(吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}丁酰胺(化合物249)
用1-甲基吡唑-4-胺替换5-氨基-2-甲氧基吡啶,与化合物247类似地合成化合物249。手性HPLC保留时间:4.82min(条件:柱,YMC Cellulose-SB,100*4.6mm,3μm;移动相,正己烷及乙醇(10%,8min))。LCMS(ES)[M+1]+m/z:406。1H NMR(300MHz,DMSO-d6)δ10.78(s,1H),8.85(dt,J=5.1,1.2Hz,1H),8.41(dt,J=7.9,1.1Hz,1H),7.99(td,J=7.7,1.7Hz,1H),7.88(s,1H),7.57(ddd,J=7.5,4.7,1.3Hz,1H),7.35(s,1H),4.70(d,J=11.0Hz,1H),3.75(s,3H),3.23(dt,J=16.0,8.1Hz,1H),3.16(s,3H),3.14-3.00(m,1H),3.00-2.74(m,2H),2.49-2.35(m,1H),2.16-1.90(m,2H),0.97(d,J=6.4Hz,3H),0.93(d,J=6.6Hz,3H)。
实施例1.256
合成(2R)-2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(6-甲氧基吡啶-3-基)丙酰胺(化合物250)
用5-氨基-2-甲氧基吡啶替换环己胺且用3-(三甲基锡烷基)异喹啉替换2-(三丁基锡烷基)吡啶,与化合物108类似地合成化合物250。LCMS(ES)[M+1]+m/z:455。1H NMR(300MHz,DMSO-d6)δ10.61(s,1H),9.42(s,1H),8.85(s,1H),8.38(d,J=2.7Hz,1H),8.20(d,J=8.4Hz,1H),8.17(s,HCOOH),8.03(d,J=8.1Hz,1H),7.94(dd,J=8.7,2.7Hz,1H),7.84-7.72(m,2H),6.75(d,J=8.7Hz,1H),5.38(q,J=6.9Hz,1H),3.77(s,3H),3.29-3.13(m,2H),3.25(s,3H),2.95-2.86(m,2H),2.08-1.98(m,2H),1.50(d,J=6.9Hz,3H)。
实施例1.257
合成(2R)-N-(3-氟苯基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙酰胺(化合物251)
流程108
步骤1
向50mL 3颈圆底烧瓶中放入(2R)-2-[(叔丁氧羰基)(甲基)氨基]丙酸(2.00g,9.84mmol,1.00当量)、DMF(20.00mL)、3-氟苯胺(1.20g,10.82mmol,1.10当量)及DIEA(2.54g,19.68mmol,2.00当量)。之后在0℃下分数批添加HATU(4.12g,10.82mmol,1.10当量)。添加后,在室温下搅拌所得溶液1h。将反应物用20mL水淬灭,用3×20mL乙酸乙酯萃取。将合并的有机相用3×20ml盐水洗涤,经无水硫酸钠干燥且过滤。减压浓缩滤液,通过含乙酸乙酯/石油醚(1:1)的硅胶柱纯化残余物。由此产生2.2g(75%)呈白色固体的N-[(1R)-1-[(3-氟苯基)氨甲酰基]乙基]-N-甲基氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z:297。
步骤2
向50mL圆底烧瓶中放入N-[(1R)-1-[(3-氟苯基)氨甲酰基]乙基]-N-甲基氨基甲酸叔丁酯(2.20g,7.42mmol,1.00当量)及DCM(10.00mL)。之后在0℃下于搅拌下逐滴添加HCl(g)(2M于EA中)(19.00mL,37.10mmol,5.00当量)。在室温下搅拌所得溶液1h。真空浓缩混合物以移除溶剂。由此产生1.6g(93%)呈白色固体的(2R)-N-(3-氟苯基)-2-(甲基氨基)丙酰胺盐酸盐。LCMS(ES)[M-HCl+1]+m/z:197。
步骤3
向50mL圆底烧瓶中放入(2R)-N-(3-氟苯基)-2-(甲基氨基)丙酰胺盐酸盐(1.00g,4.29mmol,1.00当量)、NMP(20.00mL)、2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(1.06g,5.58mmol,1.30当量)及DIEA(2.78g,21.49mmol,5.00当量)。于油浴中在60℃下搅拌所得溶液48h。将反应混合物冷却至室温,用20mL水稀释且用3×20mL乙酸乙酯萃取。将合并的有机相用3×20ml盐水洗涤,经无水硫酸钠干燥且过滤。减压浓缩滤液,通过含乙酸乙酯/石油醚(1:1)的硅胶柱纯化残余物。由此产生1.0g(67%)呈白色固体的(2R)-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(3-氟苯基)丙酰胺。LCMS(ES)[M+1]+m/z:349。
步骤4
向用惰性氮气氛围吹扫及维持的100mL三颈圆底烧瓶中放入4-[2-(氧杂环己-2-基氧基)乙氧基]-2-(三甲基锡烷基)吡啶(由2-氯-4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶与六甲基二锡烷现场制备)(1.60g,4.14mmol,1.00当量)、甲苯(60.00mL)、(2R)-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(3-氟苯基)丙酰胺(1.01g,2.90mmol,0.70当量)、Pd(PPh3)4(479mg,0.41mmol,0.10当量)。于油浴中在105℃下搅拌混合物12h。将反应混合物冷却至室温,浓缩以移除溶剂;通过含二氯甲烷/甲醇(10:1)的硅胶柱纯化残余物。由此产生190mg(9%)呈黄色油状物的(2R)-N-(3-氟苯基)-2-[甲基([2-[(2E)-3-[2-(氧杂环己-2-基氧基)乙氧基]丁-2-烯亚酰胺基]-5H,6H,7H-环戊并[d]嘧啶-4-基])氨基]丙酰胺。LCMS(ES)[M+1]+m/z:536。
步骤5
向8mL小瓶中放入(2R)-N-(3-氟苯基)-2-[甲基(2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]丙酰胺(190mg,0.35mmol,1.00当量)、MeOH(4.00mL)及TsOH(73mg,0.42mmol,1.20当量)。在室温下搅拌所得溶液1h。通过使用以下条件的急骤制备型HPLC纯化反应溶液:柱,Welch XB-C18,21.2*250mm,5um,移动相,相A:水(0.05%NH4OH)及相B:CH3CN(15min内自10%相B达至65%),检测器,UV 254nm。冷冻干燥洗脱份,由此产生108.1mg(68%)呈白色固体的(2R)-N-(3-氟苯基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙酰胺。LCMS(ES,m/z):[M+H]+:452。1H-NMR(300MHz,DMSO-d6,ppm):δ10.58(br,1H),8.49(d,J=5.7Hz,1H),7.88(d,J=2.7Hz,1H),7.57-7.52(m,1H),7.36-7.22(m,2H),7.07(dd,J=5.7,2.7Hz,1H),6.86-6.80(m,1H),5.28(q,J=7.2Hz,1H),4.92(t,J=5.4Hz,1H),4.13(t,J=4.2Hz,2H),3.77-3.72(m,2H),3.30-3.06(m,5H),2.94-2.77(m,2H),2.06-1.95(m,2H),1.46(d,J=7.2Hz,3H)。
实施例1.258
合成N-(3-氟苯基)-2-[甲基(2-{4-[2-(吡咯烷-1-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物252)
流程109
步骤1
向用惰性氮气氛围吹扫及维持的100mL 3颈圆底烧瓶中放入1-(2-羟乙基)吡咯烷(4.82g,41.816mmol,1.1当量)于THF(50mL)中的溶液。之后在15min内在0℃下分批添加NaH(60%)(1.83g,45.750mmol,1.2当量)。在0℃下搅拌所得溶液1hr。在20min内在0℃下于搅拌下向其逐滴添加2-氯-4-氟吡啶(5.00g,38.014mmol,1.00当量)。在室温下搅拌所得溶液过夜。随后通过添加50mL水/冰来淬灭反应物。用3×50mL乙酸乙酯萃取所得溶液,且将有机层合并,用1×100mL盐水洗涤。过滤后,滤液经无水硫酸钠干燥且浓缩。通过含乙酸乙酯/石油醚(1/4)的硅胶柱纯化残余物。由此产生5.5g(63.95%)呈棕色油状物的2-氯-4-[2-(吡咯烷-1-基)乙氧基]吡啶。LCMS(ES)[M+1]+m/z:227。
步骤2
向用惰性氮气氛围吹扫及维持的40mL圆底烧瓶中放入2-氯-4-[2-(吡咯烷-1-基)乙氧基]吡啶(1.80g,7.940mmol,1.00当量)于1,4-二噁烷(20mL)中的溶液、六甲基二锡烷(2.86g,8.734mmol,1.1当量)及Pd(dppf)Cl2(400.00mg,0.547mmol,0.07当量)。于油浴中在100℃下搅拌所得溶液过夜。真空浓缩所得混合物。由此产生5.0g(粗)呈固体的4-[2-(吡咯烷-1-基)乙氧基]-2-(三甲基锡烷基)吡啶。其直接用于下一步骤中。LCMS(ES)[M+1]+m/z:357。
步骤3
向用惰性氮气氛围吹扫及维持的100mL圆底烧瓶中放入4-[2-(吡咯烷-1-基)乙氧基]-2-(三甲基锡烷基)吡啶(5.00g粗物质,14.082mmol,1.00当量)于甲苯(50mL)中的溶液、2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸乙酯(2.28g,8.449mmol,0.6当量)及Pd(PPh3)4(1.00g,0.865mmol,0.06当量)。于油浴中在100℃下搅拌所得溶液过夜。浓缩所得混合物。通过硅胶柱,用二氯甲烷/甲醇(10/1)洗脱来纯化残余物。由此产生400mg(粗)呈棕色油状物的2-[甲基(2-[4-[2-(吡咯烷-1-基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酸乙酯。LCMS(ES)[M+1]+m/z:426。
步骤4
向40mL圆底烧瓶中放入2-[甲基(2-[4-[2-(吡咯烷-1-基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酸乙酯(390.00mg,0.916mmol,1.00当量)、MeOH/H2O(3/1)(4mL)及LiOH.H2O(76.92mg,1.833mmol,2当量)。在室温下搅拌所得溶液过夜。浓缩所得混合物。由此产生350mg(粗)呈棕色固体的2-[甲基(2-[4-[2-(吡咯烷-1-基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酸锂。LCMS(ES)[M-Li+H+1]+m/z:398。
步骤5
向40mL圆底烧瓶中放入2-[甲基(2-[4-[2-(吡咯烷-1-基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酸锂(320.00mg,0.805mmol,1.00当量)于DCM(4mL)中的溶液、TEA(162.93mg,1.610mmol,2当量)、T3P(512.32mg,1.610mmol,2当量)及3-氟苯胺(107.35mg,0.966mmol,1.2当量)。在室温下搅拌所得溶液过夜。真空浓缩所得混合物。通过含THF/石油醚(10:1)的硅胶柱纯化残余物。将收集的洗脱份合并且真空浓缩。将残余物溶解于4mL MeOH中且通过使用以下条件的制备型HPLC(Waters I)进一步纯化:柱,XBridge Prep C18OBD柱,5um,19*150mm;移动相,水(0.1%TFA)及CH3CN(13min内自30%CH3CN达至40%);检测器,UV 254nm。由此产生35.0mg(8.99%)呈淡黄色固体的N-(3-氟苯基)-2-[甲基(2-{4-[2-(吡咯烷-1-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺。LCMS(ES)[M+1]+m/z:491。1H NMR(300MHz,氯仿-d)δ10.68(s,1H),8.64(s,1H),8.12(s,1H),7.56(d,J=11.4Hz,1H),7.43(d,J=8.3Hz,1H),7.24-7.14(m,1H),7.14(s,1H),6.77-6.72(m,1H),4.70(s,2H),4.56(s,2H),3.83(s,2H),3.64(s,3H),3.58(s,2H),3.42-3.26(m,2H),3.11-3.06(m,4H),2.23-2.16(m,6H)。
实施例1.259
合成N-(6-甲氧基吡啶-3-基)-2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物253)
流程110
步骤1
向使用惰性氮气氛围吹扫及维持的40mL小瓶中放入4-(氧杂环丁-3-基氧基)-2-(三甲基锡烷基)吡啶(1.00g,3.185mmol,1.00当量)、甲苯(20.0mL)、2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸乙酯(859mg,0.003mmol,1.00当量)、Pd(PPh3)4(368mg,0.319mmol,0.10当量)的混合物。在100℃下搅拌所得溶液16小时。浓缩所得混合物。将残余物施加至含二氯甲烷/甲醇(10/1)的硅胶柱上。由此产生540mg(44.10%)呈棕色油状物的N-甲基-N-(2-(4-(氧杂环丁-3-基氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸乙酯。LCMS(ES)[M+1]+m/z 385。
步骤2
向20mL小瓶中放入N-甲基-N-(2-(4-(氧杂环丁-3-基氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸乙酯(500mg,1.30mmol,1.00当量)、MeOH(10.00mL)、H2O(2.00mL)及NaOH(104.04mg,2.602mmol,2.00当量)的混合物。在室温下搅拌所得溶液2小时。将所得混合物浓缩且用20mL H2O稀释。用HCl(2mol/L)将溶液的pH值调节至6。通过过滤收集所得固体。由此产生420mg(90.61%)呈白色固体的N-甲基-N-(2-(4-(氧杂环丁-3-基氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸。LCMS(ES)[M+1]+m/z357。
步骤3
向8mL小瓶中放入N-甲基-N-(2-(4-(氧杂环丁-3-基氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸(150mg,0.421mmol,1.00当量)、DMA(5.00mL)、5-氨基-2-甲氧基吡啶(104mg,0.842mmol,2.00当量)、T3P(267mg,0.842mmol,2.00当量)及Et3N(127mg,1.26mmol,3.00当量)的混合物。在室温下搅拌所得溶液2小时。通过使用以下条件的制备型HPLC纯化粗产物:柱,XBridge Prep C18 OBD柱,19×150mm,5um;移动相,相A:H2O(0.05%NH3H2O);相B:CH3CN/MeOH=1/1(15min内自15%CH3CN/MeOH达至65%CH3CN/MeOH)。由此产生52.7mg(27.1%)呈灰白色固体的N-(6-甲氧基吡啶-3-基)-2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺。LCMS(ES)[M+1]+m/z:463。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),8.37(d,J=2.7Hz,1H),7.91(dd,J=8.9,2.8Hz,1H),7.64(d,J=2.6Hz,1H),6.85(dd,J=5.6,2.6Hz,1H),6.78(d,J=8.8Hz,1H),5.38-5.32(m,1H),4.91(t,J=6.7Hz,2H),4.53(dd,J=7.4,4.8Hz,2H),4.39(s,2H),3.80(s,3H),3.37(s,3H)3.21(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.07-1.96(m.2H)。
实施例1.260
合成2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物254)
用4-(氧杂环丁-3-基氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三丁基锡烷基)吡啶且用1-甲基-1H-吡唑-4-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物254。LCMS(ES)[M+1]+m/z:436。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.5Hz,1H),7.86(s,1H),7.58(d,J=2.6Hz,1H),7.42(s,1H),6.88(dd,J=5.9,2.6Hz,1H),5.48-5.35(m,1H),4.92(t,J=6.7Hz,2H),4.55(dd,J=7.4,4.8Hz,2H),4.35(s,2H),3.76(s,3H),3.41(s,3H),3.19(t,J=7.5Hz,2H),2.83(t,J=7.8Hz,2H),2.13-1.95(m,2H),1.86(s,1H)。
实施例1.261
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-1-(哌啶-1-基)乙-1-酮(化合物255)
用3-(三甲基锡烷基)异喹啉替换4-甲氧基-2-(三丁基锡烷基)吡啶且用哌啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物255。LCMS(ES)[M+1]+m/z:402。1H NMR(300MHz,DMSO-d6)δ9.39(s,1H),8.71(s,1H),8.23-8.15(m,1H),8.05(d,J=8.1Hz,1H),7.82(ddd,J=8.2,6.9,1.3Hz,1H),7.73(ddd,J=8.1,6.9,1.3Hz,1H),4.59(s,2H),3.54-3.39(m,4H),3.30(s,3H),3.16(t,J=7.2Hz,2H),2.92-2.80(m,2H),2.05-1.95(m,2H),1.72-1.59(m,4H),1.48-1.38(m,2H)。
实施例1.262
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-1-(4-甲基哌嗪-1-基)乙-1-酮(化合物256)
用3-(三甲基锡烷基)异喹啉替换4-甲氧基-2-(三丁基锡烷基)吡啶且用4-甲基哌嗪替换氧杂环戊-3-胺,与化合物135类似地合成化合物256。LCMS(ES)[M+1]+m/z:417。1HNMR(300MHz,DMSO-d6)δ9.40(s,1H),8.71(s,1H),8.19(d,J=8.0Hz,1H),8.09(d,J=8.1Hz,1H),7.82(ddd,J=8.2,6.9,1.3Hz,1H),7.73(ddd,J=8.1,6.9,1.2Hz,1H),4.60(s,2H),3.57(s,2H),3.45(s,2H),3.30(s,3H),3.16(t,J=7.3Hz,2H),2.86(t,J=8.1Hz,2H),2.42(s,2H),2.24(s,2H),2.18(s,3H),2.02(td,J=14.8,14.1,6.5Hz,2H)。
实施例1.263
合成N-(6-甲氧基吡啶-3-基)-2-{甲基[2-(1,6-萘啶-7-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物257)
流程111
步骤1
在20℃下向2-(3-溴吡啶-2-基)乙酸乙酯(14g,57.3mmol,1.0当量)、Zn(CN)2(10.1g,86.03mmol,1.5当量)及K2CO3(15.8g,114.7mmol,2.0当量)NMP(100mL)中的搅拌混合物中添加Pd(dppf)Cl2.CH2Cl2(4.7g,5.73mmol,0.10当量)。将所得混合物加热至70℃且在此温度下于N2氛围下搅拌16h。将所得混合物冷却至25℃且用水淬灭,用EtOAc(100mL×3)萃取,将有机层合并、浓缩,通过硅胶柱色谱纯化残余物,得到呈黄色胶状物的2-(3-氰基吡啶-2-基)乙酸乙酯(9.0g,产率81.8%)。LCMS(ES)[M+1]+m/z:191。
步骤2
在20℃下向2-(3-氰基吡啶-2-基)乙酸乙酯(6.0g,31.5mmol,1.0当量)于AcOH(12mL)及EtOH(60mL)中的搅拌混合物中添加Pd/C(600mg)。将所得混合物加热至40℃且在此温度下于H2氛围(10atm)下搅拌16h。将所得混合物冷却至25℃,过滤且浓缩。通过硅胶柱色谱纯化残余物,得到呈黄色固体的6,8-二氢-5H-1,6-萘啶-7-酮(4.0g,85.6%)。LCMS(ES)[M+1]+m/z:149。
步骤3
将6,8-二氢-5H-1,6-萘啶-7-酮(1.5g)于苯基膦酰二氯(10mL)中的搅拌溶液加热至130℃且在此温度下搅拌16h。将所得混合物冷却至25℃,倒入50mL水中且用固体NaHCO3将pH调节至8。用EtOAc萃取混合物,将有机层分离且浓缩。通过硅胶柱色谱纯化残余物,得到呈黄色固体的7-氯-1,6-萘啶(400mg,产率25.5%)。LCMS(ES)[M+1]+m/z:165。
步骤4
在室温下向7-氯-1,6-萘啶(200mg,1.21mmol,1.0当量)于甲苯(5mL)中的搅拌溶液中添加Sn2Me6(438mg,1.33mmol,1.1当量)及Pd(dppf)Cl2.CH2Cl2(89mg,0.12mmol,0.1当量)。于N2氛围下在100℃下搅拌反应物3h。反应混合物不经进一步纯化即用于下一步骤中(7-(三甲基锡烷基)-1,6-萘啶:理论重量358mg)。LCMS(ES)[M+1]+m/z:295。
步骤5
在室温下向7-(三甲基锡烷基)-1,6-萘啶(358mg,1.21mmol,1.0当量)于甲苯(10mL)中的混合物中添加2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(296mg,0.85mmol,0.70当量)及Pd(PPh3)4(140mg,0.12mmol,0.1当量)。用惰性氩气氛围吹扫反应物且维持2min。将所得溶液在100℃下搅拌16hr,冷却且真空浓缩。将残余物施加至含THF/石油醚(1:50至10:1)的硅胶柱上,得到150mg粗产物,通过制备型HPLC(柱,C18;流动速率:20mL/min柱:DAICEL CHIRALPAK IC,250*20mm,220nm)进一步纯化,得到呈灰白色固体的N-(6-甲氧基吡啶-3-基)-2-[甲基[2-(1,6-萘啶-7-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺(55mg,10.24%)。LCMS(ES)[M+1]+m/z:442。1HNMR(300MHz,DMSO-d6)δ10.31(s,1H),9.46(s,1H),9.16(d,J=4.2Hz,1H),8.82(s,1H),8.62(d,J=8.3Hz,1H),8.38(d,J=2.7Hz,1H),7.92(dd,J=8.6,2.7Hz,1H),7.72(dd,J=8.3,4.2Hz,1H),6.75(d,J=8.9Hz,1H),4.49(s,2H),3.78(s,3H),3.40(s,3H),3.23(t,J=7.4Hz,2H),2.88(t,J=7.8Hz,2H),2.09-2.02(m,2H)。
实施例1.264
合成N-(6-甲氧基吡啶-3-基)-2-{甲基[2-(2,6-萘啶-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物258)
流程12
步骤1
向500mL 3颈圆底烧瓶中放入2-(吡啶-3-基)乙酸乙酯(20.00g,121.07mmol,1.00当量)及CHCl3(300.00mL)。之后在0℃下分批添加mCPBA(31.34g,181.61mmol,1.50当量)。在室温下搅拌所得溶液5h。随后通过添加饱和Na2SO3来淬灭反应物。用饱和Na2CO3将溶液的pH值调节至8-9。用3×300mL二氯甲烷萃取所得溶液且将有机层合并,经无水硫酸钠干燥且浓缩。将残余物施加至含二氯甲烷/甲醇(100/5)的硅胶柱上。由此产生20g(91.17%)呈灰白色固体的3-(2-乙氧基-2-氧代乙基)吡啶-1-鎓-1-醇盐。LCMS(ES)[M+1]+m/z:182。
步骤2
向500mL圆底烧瓶中放入3-(2-乙氧基-2-氧代乙基)吡啶-1-鎓-1-醇盐(20.00g,110.38mmol,1.00当量)、碘乙烷(51.65g,331.16mmol,3.00当量)。在45℃下搅拌所得溶液6h。向所得溶液中添加CH3CN(350.00mL)、K2CO3(45.77g,331.14mmol,3.00当量)、TMSCN(32.85g,331.14mmol,3.00当量)。在50℃下搅拌所得溶液过夜。将反应混合物冷却至室温。滤出固体且浓缩滤液。将残余物施加至含THF/PE(10%)的硅胶柱上。由此产生10g(47.63%)呈黄色油状物的2-(4-氰基吡啶-3-基)乙酸乙酯。LCMS(ES)[M+1]+m/z:191。
步骤3
向250mL压力槽反应器中放入2-(4-氰基吡啶-3-基)乙酸乙酯(10.00g,52.57mmol,1.00当量)、EtOH(80.00mL)、AcOH(20.00mL)及Pd/C(0.56g,5.26mmol,0.10当量)。在35℃下搅拌所得溶液6h。滤出固体且浓缩滤液。通过使用以下条件的制备型HPLC纯化粗产物(10g):柱,XBridge Prep C18OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3·H2O)及CAN(11min内自10%相B达至30%);检测器,254nM。由此产生6g(77%)呈黄色固体的2,4-二氢-1H-2,6-萘啶-3-酮。LCMS(ES)[M+1]+m/z:149。
步骤4
向250mL圆底烧瓶中放入2,4-二氢-1H-2,6-萘啶-3-酮(6.00g,40.49mmol,1.00当量)及苯基膦酰二氯(60.00mL)。在125℃下搅拌所得溶液3h。将反应混合物冷却至室温。用饱和NaHCO3将溶液的pH值调节至8。用3×300mL二氯甲烷萃取所得溶液且将有机层合并,经无水硫酸钠干燥且浓缩。将残余物施加至含THF/PE(30%)的硅胶柱上。由此产生350mg(5.25%)呈黄色固体的3-氯-2,6-萘啶。LCMS(ES)[M+1]+m/z:165。
步骤5
向40mL小瓶中放入3-氯-2,6-萘啶(350.00mg,2.13mmol,1.00当量)、六甲基二锡烷(905.72mg,2.76mmol,1.30当量)、甲苯(10.00mL)及Pd(dppf)Cl2(155.60mg,0.21mmol,0.10当量)。在100℃下搅拌所得溶液3h。将反应混合物冷却至室温且添加2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酸乙酯(401.51mg,1.49mmol,0.70当量)。随后在100℃下搅拌所得溶液过夜。将反应混合物冷却至室温且浓缩。将残余物施加至含THF/PE(50%)的硅胶柱上。由此产生300mg(38.82%)呈黄色固体的2-[甲基[2-(2,6-萘啶-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸乙酯。LCMS(ES)[M+1]+m/z:364。
步骤6
向100mL圆底烧瓶中放入2-[甲基[2-(2,6-萘啶-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸乙酯(300.00mg,0.83mmol,1.00当量)、MeOH(5.00mL)及H2O(5.00mL)。之后在0℃下分批添加LiOH.H2O(69.28mg,1.65mmol,2.00当量)。在室温下搅拌所得溶液3h且用柠檬酸将溶液的pH值调节至7。通过使用以下条件的制备型HPLC纯化粗产物(0.5g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水及AcCN(11min内自10%相B达至30%);检测器,254nm。由此产生160mg(57.79%)呈黄色固体的[甲基[2-(2,6-萘啶-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸。LCMS(ES)[M+1]+m/z:336。
步骤7
向40mL小瓶中放入[甲基[2-(2,6-萘啶-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酸(160.00mg,0.47mmol,1.00当量)、DMF(5.00mL)、DIEA(123.32mg,0.95mmol,2当量)及5-氨基-2-甲氧基吡啶(59.23mg,0.47mmol,1.00当量)。之后在0℃下分批添加HATU(217.68mg,0.57mmol,1.20当量)。在室温下搅拌所得溶液2h。通过使用以下条件的制备型HPLC纯化粗产物(1g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3·H2O)及AcCN/MeOH=1:1(11min内自30%相B达至70%);检测器,254nm。由此产生127mg(33.97%)呈橙色固体的N-(6-甲氧基吡啶-3-基)-2-[甲基[2-(2,6-萘啶-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺;参(三氟乙酸)。LCMS(ES,m/z):[M+H]+:442。1H-NMR(300MHz,DMSO-d6,ppm):δ10.61(s,1H),9.70(s,1H),9.43(s,1H),9.14(s,1H),8.91(d,J=5.6Hz,1H),8.44(d,J=2.7Hz,1H),8.22(d,J=5.7Hz,1H),7.96(dd,J=8.9,2.8Hz,1H),6.79(d,J=8.9Hz,1H),4.75(s,2H),3.78(s,3H),3.63(s,3H),3.36-3.30(m,2H),3.11(t,J=7.8Hz,2H),2.19-2.02(m,2H)。
实施例1.265
合成2-{[2-(4-乙氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(2-甲氧基嘧啶-5-基)乙酰胺(化合物259)
通过用4-乙氧基-2-(三丁基锡烷基)吡啶替换4-甲氧基-2-(三丁基锡烷基)吡啶且用2-甲氧基嘧啶-5-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物259。LCMS(ES)[M+1]+m/z:436。1H NMR(300MHz,DMSO-d6)δ10.49(s,1H),8.76(s,2H),8.42(d,J=5.5Hz,1H),7.72(d,J=2.5Hz,1H),6.98(dd,J=5.7,2.5Hz,1H),4.39(s,2H),4.05(q,J=6.9Hz,2H),3.87(s,3H),3.38(s,3H),3.21(t,J=7.4Hz,2H),2.83(t,J=7.8Hz,2H),2.07-1.96(m,2H),1.29(t,J=7.0Hz,3H)。
实施例1.266
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(2-甲氧基嘧啶-5-基)乙酰胺(化合物260)
通过用2-甲氧基嘧啶-5-胺替换5-氨基-2-甲氧基吡啶,与化合物210类似地合成化合物260。LCMS(ES)[M+1]+m/z:480。1H NMR(300MHz,DMSO-d6)δ10.47(s,1H),8.74(s,2H),8.43(d,J=5.6Hz,1H),7.77(d,J=2.5Hz,1H),7.03(dd,J=5.7,2.6Hz,1H),4.66(s,1H),4.42(s,2H),3.87(s,3H),3.80(s,2H),3.38(s,3H),3.22(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.08-1.99(m,2H),1.16(s,6H)。
实施例1.267
合成N-叔丁基-2-{[2-(6-甲氧基异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物261)
通过用6-甲氧基-3-(三甲基锡烷基)异喹啉替换4-甲基-2-(三丁基锡烷基)吡啶,与化合物24类似地合成化合物261。LCMS(ES)[M+1]+m/z 420。1H NMR(300MHz,DMSO-d6)δ9.23(s,1H),8.80(s,1H),8.16(HCOOH),8.08(d,J=9.0Hz,1H),7.81(s,1H),7.50(s,1H),7.33(dd,J=8.9,2.5Hz,1H),4.19(s,2H),3.94(s,3H),3.33(s,3H),3.17(t,J=7.5Hz,2H),2.85(t,J=7.9Hz,2H),2.04-1.99(m,2H),1.23(s,9H)。
实施例1.268
合成N-叔丁基-2-{[2-(7-甲氧基异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物262)
通过用7-甲氧基-3-(三甲基锡烷基)异喹啉替换4-甲基-2-(三丁基锡烷基)吡啶,与化合物24类似地合成化合物262。LCMS(ES)[M+1]+m/z 420。1H NMR(300MHz,DMSO-d6)δ9.28(s,1H),8.79(s,1H),8.17(HCOOH),8.03(d,J=9.0Hz,1H),7.79(s,1H),7.59(d,J=2.5Hz,1H),7.48(dd,J=9.0,2.5Hz,1H),4.19(s,2H),3.95(s,3H),3.32(s,3H),3.17(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.06-1.99(m,2H),1.23(s,9H)。
实施例1.269
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-(哌啶-1-基)乙-1-酮(化合物263)
通过用哌啶替换环己胺,与化合物144类似地合成化合物263。LCMS(ES)[M+1]+m/z412。1H NMR(300MHz,DMSO-d6)δ8.45(d,J=5.7Hz,1H),7.75(d,J=2.7Hz,1H),7.03(dd,J=5.7,2.7Hz,1H),4.92(t,J=5.4Hz,1H),4.51(s,2H),4.13(t,J=4.8Hz,2H),3.75(q,J=5.1Hz,2H),3.47-3.37(m,4H),3.25(s,3H),3.13(t,J=7.5Hz,2H),2.81(t,J=7.8Hz,2H),2.04-1.93(m,2H),1.61(s,4H),1.44(s,2H)。
实施例1.270
合成N-(6-氟吡啶-3-基)-2-[甲基({2-[1-(氧杂环己-2-基)-1H-吡唑并[3,4-c]吡啶-5-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物264)
通过用1-(氧杂环己-2-基)-5-(三丁基锡烷基)-1H-吡唑并[3,4-c]吡啶替换4-甲氧基-2-(三丁基锡烷基)吡啶且用6-氟-3-吡啶胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物264。LCMS(ES)[M+1]+m/z:503.2。1H NMR(400MHz,DMSO-d6)δ9.39(s,1H),9.10-8.94(m,1H),8.52(d,J=2.3Hz,1H),8.37(s,1H),8.22(ddd,J=8.8,7.3,2.8Hz,1H),7.17(dd,J=8.8,3.2Hz,1H),6.18(dd,J=9.2,2.5Hz,1H),4.73(s,2H),3.92-3.76(m,2H),3.58(s,3H),3.25(m,2H),3.08(t,J=7.9Hz,2H),2.45-2.30(m,1H),2.16-2.01(m,4H),1.82-1.70(m,1H),1.66-1.57(m,2H)。
实施例1.271
合成N-(5-甲氧基吡啶-2-基)-2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物265)
通过用5-甲氧基吡啶-2-胺替换6-氟吡啶-3-胺,与化合物266类似地合成化合物265。LCMS(ES+):[M+H]+=431.1。1H NMR(400MHz,DMSO-d6)δ13.88(s,1H),10.77(s,1H),9.11(s,1H),8.78(d,J=1.3Hz,1H),8.16-8.09(m,2H),7.96(d,J=9.0Hz,1H),7.39(dd,J=9.1,3.1Hz,1H),4.58(s,2H),3.78(s,3H),3.30-3.18(m,9H),2.92(t,J=7.8Hz,2H),2.05(p,J=7.9Hz,2H)。
实施例1.272
合成N-(5-甲氧基吡啶-2-基)-2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物266)
流程112
将N-(6-氟吡啶-3-基)-2-[甲基({2-[1-(氧杂环己-2-基)-1H-吡唑并[3,4-c]吡啶-5-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(53mg;0.11mmol;1当量)溶解于甲醇(1ml)中且于冰水浴中冷却。缓慢添加氯化氢溶液(1mL;6mol/L异丙醇)且在25℃下搅拌反应物。3h后,再添加HCl(0.2ml),且再搅拌反应物1.5h。蒸发反应溶剂且通过反相色谱(Waters XSelect CSH C18柱,0-60%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈白色固体的N-(6-氟吡啶-3-基)-2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(22mg,49%)。LCMS(ES+):[M+H]+=419.0。1H NMR(400MHz,dmso)δ13.83(s,1H),10.73(s,1H),9.08(s,1H),8.78-8.73(m,1H),8.48(d,J=2.8Hz,1H),8.21(ddd,J=8.8,7.3,2.8Hz,1H),8.16(s,1H),7.16(dd,J=8.9,3.2Hz,1H),4.52(s,2H),3.45(s,3H),3.27-3.19(m,2H),2.95-2.86(m,2H),2.11-1.98(m,2H)。
实施例1.273
合成2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(6-甲基吡啶-3-基)乙酰胺(化合物267)
通过用6-甲基吡啶-3-胺替换6-氟吡啶-3-胺,与化合物266类似地合成化合物267。LCMS(ES+):[M+H]+=415.1。1H NMR(400MHz,dmso)δ11.81(s,1H),9.22(s,1H),9.09(s,1H),9.02(s,1H),8.50-8.31(m,2H),7.69-7.63(m,1H),4.83(s,2H),3.61(s,3H),3.09(t,J=7.9Hz,2H),2.55(s,3H),2.17-2.09(m,2H)。
实施例1.274
合成N-(6-甲氧基吡啶-3-基)-2-{甲基[2-(2,7-萘啶-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物268)
流程113
步骤1
在-78℃下于N2氛围下向4-甲基吡啶-3-甲腈(10g,84.646mmol,1.00当量)于THF(100mL)中的溶液中逐滴添加LiHDMS(1.0M于THF中,170mL,169.292mmol,2当量)。在-78℃下搅拌反应混合物1h。逐滴添加碳酸二甲酯(9.50g,105.464mmol,1.25当量)于50mL THF中的溶液且在-78℃下再搅拌混合物1h。在-78℃至0℃下于氮气氛围下搅拌所得混合物2h。用NH4Cl(200mL)淬灭反应物且用EtOAc(2×200mL)萃取所得混合物。将合并的有机层用水(1×100mL)洗涤,经无水Na2SO4干燥且过滤。减压浓缩滤液且通过硅胶柱色谱,用PE/EtOAc(10:1)洗脱来纯化残余物,得到呈黄色油状物的2-(3-氰基吡啶-4-基)乙酸甲酯(10.1g,67.73%)。LCMS(ES)[M+1]+m/z:177。
步骤2
在氮气氛围下于500mL 3颈圆底烧瓶中向2-(3-氰基吡啶-4-基)乙酸甲酯(10.00g,56.762mmol,1.00当量)于EtOH(200.00mL)及AcOH(20.00mL)中的溶液中添加Pd/C(1.21g,11.352mmol,0.20当量)。在40℃下向混合物中充入H2(1atm)过夜。过滤所得混合物;用MeOH(3×100mL)洗涤滤饼。减压浓缩滤液。通过硅胶柱色谱,用CH2Cl2/MeOH(10:1)洗脱来纯化残余物,得到呈黄色油状物的2,4-二氢-1H-2,7-萘啶-3-酮(4g,47.56%)。LCMS(ES)[M+1]+m/z:149;
步骤3
在室温下于空气氛围下搅拌2,4-二氢-1H-2,7-萘啶-3-酮(1.00g,6.749mmol,1.00当量)及DDQ(1.69g,7.424mmol,1.10当量)于甲苯(30.00mL)中的溶液1h。向以上混合物中添加POCl3(10.00mL,65.236mmol,15.90当量)。在90℃下再搅拌所得混合物16h。减压浓缩所得混合物。在室温下用水淬灭反应物。用饱和NaHCO3(水溶液)将混合物调节至pH 8。用EtOAc(2×200mL)萃取所得混合物。将合并的有机层用盐水(1×100mL)洗涤,经无水Na2SO4干燥且过滤。减压浓缩滤液且通过硅胶柱色谱,用PE/EtOAc(1:1)洗脱来纯化残余物,得到呈黄色固体的3-氯-2,7-萘啶(50mg,4.50%)。LCMS(ES)[M+1]+m/z:165。
步骤4
向3-氯-2,7-萘啶(220.00mg,1.337mmol,1.00当量)及六甲基二锡烷(481.72mg,1.471mmol,1.10当量)于甲苯(5.00mL,46.995mmol)中的溶液中添加Pd(dppf)Cl2 CH2Cl2(108.89mg,0.134mmol,0.10当量)。在100℃下于氮气氛围下搅拌2h后,使混合物冷却至室温。随后向混合物中添加2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(325.42mg,0.936mmol,0.70当量)及Pd(PPh3)4(108.89mg,0.134mmol,0.10当量)。在100℃下再搅拌所得混合物16h。冷却后,减压浓缩所得混合物且通过硅胶柱色谱,用PE/THF(1:10)洗脱来纯化残余物,得到呈白色固体的N-(6-甲氧基吡啶-3-基)-2-[甲基[2-(2,7-萘啶-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺(30mg,7.3%)。LCMS(ES)[M+1]+m/z:442;1H NMR(300MHz,DMSO-d6)δ10.35(s,1H),9.58(d,J=5.2Hz,2H),8.87-8.62(m,2H),8.39(d,J=2.7Hz,1H),7.93(dd,J=8.9,2.7Hz,1H),7.74(d,J=5.8Hz,1H),6.77(d,J=8.9Hz,1H),4.47(s,2H),3.79(s,3H),3.42(s,3H),3.31-3.11(m,2H),2.89(t,J=7.8Hz,2H),2.07-2.02(m,2H)。
实施例1.275
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(4-甲氧基苯基)乙酰胺(化合物269)
通过用4-甲氧基苯胺替换环己胺,与化合物144类似地合成化合物269。LCMS(ES)[M+1]+m/z 450。1H NMR(300MHz,DMSO-d6)δ10.07(s,1H),8.44(d,J=5.6Hz,1H),7.80(d,J=2.6Hz,1H),7.55-7.43(m,2H),7.00(dd,J=5.6,2.6Hz,1H),6.92-6.79(m,2H),4.90(t,J=5.4Hz,1H),4.39(s,2H),4.03(t,J=4.7Hz,2H),3.71(s,3H),3.77-3.62(m,2H),3.35(s,3H),3.20(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.01(p,J=7.8Hz,2H)。
实施例1.276
合成2-({2-[5-(羟甲基)异喹啉-3-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺(化合物270)
流程114
步骤1
向1000mL圆底烧瓶中放入1,3-二氯异喹啉(30.00g,151.477mmol,1.00当量)、NBS(28.31g,159.051mmol,1.05当量)、AcCN(600.00mL)及H2SO4(30.00mL)。在室温下搅拌所得溶液90h。通过过滤收集固体。由此产生18g(42.91%)呈黄色固体的5-溴-1,3-二氯异喹啉。LCMS(ES)[M+1]+m/z 276。
步骤2
向500mL圆底烧瓶中放入5-溴-1,3-二氯异喹啉(15.00g,54.163mmol,1.00当量)、AcOH(150.00mL)、HCl(30.00mL)及Sn(19.34g,162.490mmol,3当量)。在60℃下搅拌所得溶液0.5hr。用3×200mL乙酸乙酯萃取所得溶液,将有机层合并,用3×200ml盐水洗涤且过滤。浓缩滤液且将残余物施加至含乙酸乙酯/石油醚(1:5)的硅胶柱上。由此产生5.5g(41.87%)呈淡黄色固体的5-溴-3-氯异喹啉。LCMS(ES)[M+1]+m/z 242。
步骤3
向用惰性氮气氛围吹扫及维持的100mL3颈圆底烧瓶中放入5-溴-3-氯异喹啉(3.00g,12.371mmol,1.00当量)、THF(30.00mL)。之后在-78℃下在搅拌下逐滴添加含n-BuLi的己烷(5.9mL,14.862mmol,1.20当量)。在-78℃下搅拌所得溶液0.5hr。在-78℃下于搅拌下向其逐滴添加DMF(2.71g,37.113mmol,3.00当量)。使所得溶液升温至室温且再搅拌2hr。随后通过添加100mL NH4Cl淬灭反应物。用2×50mL乙酸乙酯萃取所得溶液。将有机层合并,用盐水洗涤且经无水硫酸钠干燥。过滤混合物,且浓缩滤液。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上。由此产生730mg(30.7%)呈淡黄色固体的3-氯异喹啉-5-甲醛。LCMS(ES)[M+1]+m/z 192。
步骤4
向40mL圆底烧瓶中放入3-氯异喹啉-5-甲醛(730.00mg,3.810mmol,1.00当量)、THF(10.00mL)及NaBH4(432.41mg,11.429mmol,3当量)。在室温下搅拌所得溶液2hr。随后通过添加10mL水将反应物淬灭且用3×20mL乙酸乙酯萃取。将合并的有机层用3×20mL盐水洗涤,经无水硫酸钠干燥且浓缩。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上。由此产生730mg(98.9%)呈淡黄色固体的(3-氯异喹啉-5-基)甲醇。LCMS(ES)[M+1]+m/z 194。
步骤5
向40mL圆底烧瓶中放入(3-氯异喹啉-5-基)甲醇(730.00mg,3.770mmol,1.00当量)、DCM(10mL)、TBSCl(852.35mg,5.655mmol,1.50当量)、咪唑(513.31mg,7.540mmol,2当量)。在室温下搅拌所得溶液12hr。浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:10)的硅胶柱上。由此产生800mg(68.9%)呈黄色油状物的5-[[(叔丁基二甲基硅基)氧基]甲基]-3-氯异喹啉。LCMS(ES)[M+1]+m/z 308。
步骤6
向40mL圆底烧瓶中放入2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺(215.53mg,0.650mmol,1.00当量)、六甲基二锡烷(212.82mg,0.650mmol,1当量)、二噁烷(6mL)及Pd(dppf)Cl2.CH2Cl2(52.92mg,0.065mmol,0.10当量)。在100℃下搅拌所得溶液3h并冷却,且添加5-[[(叔丁基二甲基硅基)氧基]甲基]-3-氯异喹啉(200.00mg,0.650mmol,1.00当量)及Pd(dppf)Cl2.CH2Cl2(52.92mg,0.065mmol,0.10当量)。随后在100℃下搅拌所得溶液过夜。浓缩所得混合物,将残余物施加至含二氯甲烷/甲醇(1:0至10:1)的硅胶柱上。由此产生120mg(8.12%)呈棕色固体的2-((2-(5-(((叔丁基二甲基硅基)氧基)甲基)异喹啉-3-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺。LCMS(ES)[M+1]+m/z 569。
步骤7
向40mL圆底烧瓶中放入2-[[2-(5-[[(叔丁基二甲基硅基)氧基]甲基]异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-N-(6-甲基吡啶-3-基)乙酰胺(120.00mg,0.211mmol,1.00当量)、THF(3.00mL)及Et3N.3HF(170.05mg,1.055mmol,5.00当量)。在室温下搅拌所得溶液12h。用NH3H2O将溶液的pH值调节至7-8。浓缩所得混合物且通过使用以下条件的制备型HPLC纯化粗产物:柱,SunFire Prep C18 OBD柱,19*150mm 5um10nm;移动相,水(0.1%FA)及ACN(在7min内自48.0%ACN达至53.0%,在1min内保持95.0%,在1min内降至48.0%,在1min内保持48.0%);检测器,UV 220nm。由此产生41.6mg(43.38%)呈白色固体的2-({2-[5-(羟甲基)异喹啉-3-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺。LCMS(ES)[M+1]+m/z 455。1H NMR(300MHz,DMSO-d6)δ10.40(s,1H),9.37(s,1H),8.88(s,1H),8.61(d,J=2.6Hz,1H),8.07(d,J=8.1Hz,1H),7.90(dd,J=8.4,2.6Hz,1H),7.82(d,J=7.1Hz,1H),7.74-7.63(m,1H),7.16(d,J=8.5Hz,1H),5.40(br,1H),4.98(d,J=4.2Hz,2H),4.51(s,2H),3.39(s,3H),3.23(t,J=7.1Hz,2H),2.90(t,J=7.9Hz,2H),2.38(s,3H),2.09-1.97(m,2H)。
实施例1.277
合成N-(3-氟苯基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物271)
通过用3-氟苯胺替换环己胺,与化合物142类似地合成化合物271。LCMS(ES)[M+1]+m/z:381;1H-NMR(300MHz,DMSO-d6,ppm):δ10.43(s,1H),7.69-7.55(m,3H),7.41-7.26(m,2H),6.93-6.80(m,1H),4.36(s,2H),3.61(s,3H),3.32(s,3H),3.13(t,J=7.2Hz,2H),2.75(t,J=7.8Hz,2H),2.01-1.91(m,2H)。
实施例1.278
合成N-(3-甲氧基苯基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物272)
通过用3-甲氧基苯胺替换环己胺,与化合物142类似地合成化合物272。LCMS(ES)[M+1]+m/z:393;1H-NMR(300MHz,DMSO-d6,ppm):δ10.19(s,1H),7.67(d,J=1.5Hz,1H),7.58(d,J=1.2Hz,1H),7.33(t,J=2.1Hz,1H),7.25-7.11(m,2H),6.63-6.59(m,1H),4.35(s,2H),3.69(s,3H),3.61(s,3H),3.31(s,3H),3.13(t,J=7.2Hz,2H),2.74(t,J=7.8Hz,2H),2.01-1.90(m,2H)。
实施例1.279
合成(2R)-2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(哒嗪-4-基)丙酰胺(化合物273)
通过用4-哒嗪胺替换环己胺且用3-(三丁基锡烷基)异喹啉替换2-(三丁基锡烷基)吡啶,与化合物108类似地合成化合物273。LCMS(ES+):[M+H]+=426。1H NMR(400MHz,DMSO-d6)δ11.87(s,1H),9.62-9.55(m,2H),9.15(s,1H),9.09(d,J=6.2Hz,1H),8.39-8.26(m,2H),8.22(dd,J=6.2,2.7Hz,1H),7.96(dddd,J=34.5,8.1,7.0,1.2Hz,2H),5.66(d,J=7.7Hz,1H),3.54(s,3H),3.47-3.29(m,2H),3.17-3.06(m,2H),2.26-2.08(m,2H),1.70(d,J=7.1Hz,3H)。
实施例1.280
合成(2R)-2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-[6-(三氟甲基)吡啶-3-基]丙酰胺(化合物274)
通过用6-三氟吡啶-3-胺替换环己胺,与化合物108类似地合成化合物274。LCMS(ES+):[M+H]+=426。1H NMR(400MHz,DMSO-d6)δ11.87(s,1H),9.62-9.55(m,2H),9.15(s,1H),9.09(d,J=6.2Hz,1H),8.39-8.26(m,2H),8.22(dd,J=6.2,2.7Hz,1H),7.96(dddd,J=34.5,8.1,7.0,1.2Hz,2H),5.66(d,J=7.7Hz,1H),3.54(s,3H),3.47-3.29(m,2H),3.17-3.06(m,2H),2.26-2.08(m,2H),1.70(d,J=7.1Hz,3H)。
实施例1.281
合成N-(1-羟基-2-甲基丙-2-基)-2-({2-[1-(3-羟丙基)-1H-咪唑-4-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物275)
流程115
步骤1
向100mL圆底烧瓶中放入N-(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯(2.00g,7.415mmol,1.00当量)、二噁烷(20.00mL,236.082mmol,31.84当量)、水(2mL)、1-(三苯基甲基)咪唑-4-基硼酸(3.94g,11.122mmol,1.50当量)、K3PO4(3.15g,14.830mmol,2.00当量)及Pd(dppf)Cl2(0.54g,0.741mmol,0.10当量)。在100℃下搅拌所得溶液16hr。浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(1:3)的硅胶柱上。由此产生0.88g(21.83%)呈黄色固体的N-甲基-N-(2-(1-三苯甲基-1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)苷氨酸乙酯。LCMS(ES)[M+1]+m/z:544。
步骤2
向100mL圆底烧瓶中放入N-甲基-N-(2-(1-三苯甲基-1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)苷氨酸乙酯(800.00mg,1.471mmol,1.00当量)、THF(5.00mL,61.715mmol,41.94当量)、H2O(5.00mL,277.542mmol,188.61当量)及NaOH(117.71mg,2.943mmol,2.00当量)。在25℃下搅拌所得溶液2hr。用20mL水稀释所得溶液。用HCl(1mol/L)将溶液的pH值调节至6。通过过滤收集固体。由此产生640mg(84.35%)呈灰白色固体的N-甲基-N-(2-(1-三苯甲基-1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸。LCMS(ES)[M+1]+m/z:516。
步骤3
向25mL圆底烧瓶中放入N-甲基-N-(2-(1-三苯甲基-1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)甘氨酸(640.00mg,1.241mmol,1.00当量)、DMF(10mL)、2-氨基-2-甲基-1-丙醇(110.64mg,1.241mmol,1.00当量)、HATU(707.93mg,1.862mmol,1.50当量)及DIEA(481.26mg,3.724mmol,3.00当量)。在25℃下搅拌所得溶液2hr。将粗反应混合物过滤且进行反相制备型HPLC(Prep-C18,20-45uM,120g,Tianjin Bonna-Agela Technologies;经10min时段自40%MeCN/水至50%MeCN/水的梯度洗脱,水含有0.1%NH3H2O)。由此产生(250mg,34.33%)呈淡黄色固体的N-(1-羟基-2-甲基丙-2-基)-2-(甲基(2-(1-三苯甲基-1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:587。
步骤4
向25mL圆底烧瓶中放入N-(1-羟基-2-甲基丙-2-基)-2-(甲基(2-(1-三苯甲基-1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(250.00mg,0.426mmol,1.00当量)、含HCl(气体)的1,4-二噁烷(10.00mL)。在25℃下搅拌所得溶液2hr。通过过滤收集固体。由此产生150mg(92.43%)呈黄色固体的2-((2-(1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(1-羟基-2-甲基丙-2-基)乙酰胺盐酸盐。LCMS(ES)[M+1]+m/z:381。
步骤5
向100mL圆底烧瓶中放入2-((2-(1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(1-羟基-2-甲基丙-2-基)乙酰胺盐酸盐(150.00mg,0.394mmol,1.00当量)、二甲基甲酰胺(10mL)、DIEA(152.70mg,1.181mmol,3.00当量)及叔丁基二甲基氯硅烷(71.23mg,0.473mmol,1.20当量)。在25℃下搅拌所得溶液16hr。将粗反应混合物过滤且进行反相制备型HPLC(Prep-C18,20-45M,120g,Tianjin Bonna-Agela Technologies;经10min时段自50%MeCN/水至60%MeCN/水的梯度洗脱,水含有0.1%NH3H2O),得到呈淡黄色固体的2-((2-(1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(1-((叔丁基二甲基硅基)氧基)-2-甲基丙-2-基)乙酰胺(120mg,66.43%)。LCMS(ES)[M+1]+m/z:459。
步骤6
向100mL圆底烧瓶中放入2-((2-(1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(1-((叔丁基二甲基硅基)氧基)-2-甲基丙-2-基)乙酰胺(120.00mg,0.262mmol,1.00当量)、二甲基甲酰胺(10mL)、3-溴丙醇(72.73mg,0.523mmol,2.00当量)、K2CO3(108.47mg,0.785mmol,3.00当量)。在70℃下搅拌所得溶液48hr。将残余物施加至含二氯甲烷/甲醇(10:1)的硅胶柱上。将收集的洗脱份合并且浓缩。由此产生80mg(59.17%)呈黄色固体的N-(1-((叔丁基二甲基硅基)氧基)-2-甲基丙-2-基)-2-((2-(1-(3-羟丙基)-1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:517。
步骤7
向100mL圆底烧瓶中放入N-(1-((叔丁基二甲基硅基)氧基)-2-甲基丙-2-基)-2-((2-(1-(3-羟丙基)-1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(80.00mg,0.155mmol,1.00当量)、四氢呋喃(5mL)、TBAF(4.05mg,0.015mmol,0.10当量)。在25℃下搅拌所得溶液2hr。将粗反应混合物过滤且进行反相制备型HPLC(Prep-C18,20-45uM,120g,Tianjin Bonna-Agela Technologies;经10min时段自25%MeCN/水至35%MeCN/水的梯度洗脱,水含有0.1%NH3H2O)。由此产生(18.6mg,29.85%)呈灰白色固体的N-(1-羟基-2-甲基丙-2-基)-2-((2-(1-(3-羟丙基)-1H-咪唑-4-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:403。1H NMR(300MHz,DMSO-d6)δ7.77(d,J=1.4Hz,1H),7.63(d,J=1.4Hz,1H),7.47(s,1H),4.95(t,J=5.9Hz,1H),4.65(t,J=5.1Hz,1H),4.10(s,2H),4.05(t,J=7.0Hz,2H),3.49-3.35(m,4H),3.21(s,3H),3.08(t,J=7.2Hz,2H),2.73(t,J=7.8Hz,2H),1.92(dt,J=13.2,7.3Hz,4H),1.18(s,6H)。
实施例1.282
合成2-[(2-{4-[(1-羟基-2-甲基丙-2-基)氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(2-甲氧基嘧啶-5-基)乙酰胺(化合物276)
通过用2-甲氧基嘧啶-5-胺替换环己胺且用4-[[2-甲基-1-(氧杂环己-2-基氧基)丙-2-基]氧基]-2-(三甲基锡烷基)吡啶替换4-[2-(氧杂环己-2-基氧基)乙氧基]-2-(三甲基锡烷基)吡啶,与化合物144类似地合成化合物276。LCMS(ES)[M+1]+m/z:480;1H-NMR(300MHz,DMSO-d6,ppm):δ10.49(s,1H),8.74(s,2H),8.43(d,J=5.4Hz,1H),7.77(d,J=2.4Hz,1H),7.03(dd,J=5.7,2.7Hz,1H),4.67(s,1H),4.42(s,2H),3.87(s,3H),3.80(s,2H),3.24(s,3H),3.22(t,J=7.2Hz,2H),2.84(t,J=7.8Hz,2H),2.07-1.99(m,2H),1.16(s,6H)。
实施例1.283
合成(2R)-N-(3-氟苯基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物277)
通过用3-氟苯胺替换1-环己胺且用1-甲基-4-(三丁基锡烷基)咪唑替换2-(三丁基锡烷基)吡啶,与化合物108类似地合成化合物277。LCMS(ES)[M+1]+m/z:395;1H-NMR(300MHz,DMSO-d6,ppm):δ10.60(s,1H),8.14(s,HCOOH),7.78(d,J=1.2Hz,1H),7.69(d,J=1.5Hz,1H),7.66(dt,J=12.0,2.4Hz,1H),7.45-7.40(m,1H),7.32-7.24(m,1H),6.83(td,J=8.4,2.7Hz,1H),5.26(q,J=7.2Hz,1H),3.68(s,3H),3.22-3.14(m,1H),3.13(s,3H),3.08-2.97(m,1H),2.86-2.66(m,2H),2.06-1.86(m,2H),1.43(d,J=7.2Hz,3H)。
实施例1.284
合成(2R)-N-(3-甲氧基苯基)-2-{甲基[2-(1-甲基-1H-咪唑-4-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物278)
通过用3-甲氧基苯胺替换1-环己胺且用1-甲基-4-(三丁基锡烷基)咪唑替换2-(三丁基锡烷基)吡啶,与化合物108类似地合成化合物278。LCMS(ES)[M+1]+m/z:407;1H-NMR(300MHz,DMSO-d6,ppm):δ10.58(s,1H),8.17(s,HCOOH),7.81(d,J=1.5Hz,1H),7.72(d,J=1.2Hz,1H),7.31(t,J=2.1Hz,1H),7.29-7.23(m,1H),7.14(t,J=8.1Hz,1H),6.60-6.55(m,1H),5.29(q,J=7.2Hz,1H),3.69(s,3H),3.63(s,3H),3.21-3.10(m,1H),3.13(s,3H),3.06-2.96(m,1H),2.86-2.66(m,2H),2.03-1.86(m,2H),1.42(d,J=7.2Hz,3H)。
实施例1.285
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-甲氧基苯基)乙酰胺(化合物279)
流程116
步骤1
向用惰性氮气氛围吹扫且维持的250mL三颈圆底烧瓶中放入N-(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯(2.0g,7.4mmol,1.00当量)、甲苯(40.00mL)、4-氟-2-(三丁基锡烷基)吡啶(4.3g,11.1mmol,1.5当量)、Pd(PPh3)4(780mg,0.74mmol,0.10当量)。于油浴中在110℃下搅拌混合物36h。将反应混合物冷却至室温,浓缩以移除溶剂;通过含二氯甲烷/甲醇(25:1)的硅胶柱纯化残余物。由此产生1.4g(产率57%)呈黄色固体的N-(2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯。LCMS(ES)[M+1]+m/z:331。
步骤2
向250mL圆底烧瓶中放入N-(2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯(1.4g,4.2mmol,1当量)、四氢呋喃(30mL)、水(15mL)、氢氧化钠(0.36g,8.4mmol,2.00当量)。在25℃下搅拌所得溶液2hr。浓缩所得混合物。用50mL水稀释所得溶液。用HCl(1mol/L)将溶液的pH值调节至4。通过过滤收集固体。由此产生0.68g(53%)呈灰白色固体的N-(2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸。LCMS(ES)[M+1]+m/z 303。
步骤3
向8mL小瓶中放入间甲氧基苯胺(102mg,0.83mmol,1.00当量)、DMF(5mL)、3-[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]丁酸(250mg,0.83mmol,1.00当量)及DIEA(322mg,2.49mmol,3.00当量)。之后在0℃下添加T3P(317mg,1.00mmol,1.20当量)。在25℃下搅拌所得溶液2hr。随后通过添加50mL水淬灭反应物。用3×100mL乙酸乙酯萃取所得溶液,且合并有机层。将所得混合物用3×100ml盐水洗涤且真空浓缩。将残余物施加至含二氯甲烷/甲醇(20:1)的硅胶柱上。由此产生180mg(53.25%)呈淡棕色油状物的2-[[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-N-(3-甲氧基苯基)乙酰胺。LCMS(ES)[M+1]+m/z 408。
步骤2
向50mL 3颈圆底烧瓶中放入乙二醇(114mg,1.84mmol,5.00当量)、THF(5mL)。之后在0℃下添加NaH(18mg,0.74mmol,2.00当量)。在0℃下搅拌所得溶液30min。在0℃下向其添加2-[[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-N-(3-甲氧基苯基)乙酰胺(150mg,0.37mmol,1.00当量)。在25℃下搅拌所得溶液1hr。随后通过添加30mL水淬灭反应物。用2×50mL乙酸乙酯萃取所得溶液,将有机层合并且真空浓缩。将残余物溶解于5mL MeOH中。通过使用以下条件的制备型HPLC(Prep-HPLC-001)纯化粗产物:柱,SunfirePrep C18 OBD柱,50*250mm,5μm 10nm;移动相,水(0.1%FA)及ACN(15min内自5%相B达至35%)。由此产生61.0mg(36.86%)呈白色固体的2-([2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(3-甲氧基苯基)乙酰胺。LCMS(ES)[M+1]+m/z450。1H NMR(300MHz,DMSO-d6)δ10.22(s,1H),8.46(d,J=5.7Hz,1H),8.14(s,0.4HCOOH),7.80(d,J=2.5Hz,1H),7.30(t,J=2.2Hz,1H),7.19(t,J=8.0Hz,1H),7.15-7.08(m,1H),7.04(dd,J=5.7,2.6Hz,1H),6.67-6.57(m,1H),4.90(t,J=5.4Hz,1H),4.44(s,2H),4.03(t,J=4.7Hz,2H),3.69(s,3H),3.69-3.64(m,2H),3.37(s,3H),3.21(t,J=7.3Hz,2H),2.85(t,J=7.8Hz,2H),2.05-1.93(m,2H)。
实施例1.286
合成N-(3-氟苯基)-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物280)
流程117
步骤1
向100mL圆底烧瓶中放入N-(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸乙酯(3.00g,11.1mmol,1.00当量)、MeOH(30.0mL)、H2O(6.00mL)、NaOH(889mg,0.022mmol,2.00当量)的混合物。在室温下搅拌所得溶液2小时。浓缩所得混合物。用50mLH2O稀释所得溶液。用HCl(2mol/L)将溶液的pH值调节至4。通过过滤收集固体且浓缩。由此产生1.3g(48.36%)呈白色固体的N-(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸。LCMS(ES)[M+1]+m/z 270。
步骤2
向50mL圆底烧瓶中放入N-(2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸(3.7g,15.29mmol,1.00当量)、DMF(30.00mL)、HATU(6.97g,18.34mmol,1.20当量)、DIEA(5.92g,45.86mmol,3.00当量)、3-氟苯胺(2.04g,18.34mmol,1.20当量)。在25℃下搅拌所得溶液2hr。用3×100mL乙酸乙酯萃取所得溶液,且合并有机层。将所得混合物用3×100盐水洗涤且真空浓缩。将残余物施加至含DCM/MeOH(10:1)的硅胶柱上。由此产生3.20g(62.50%)呈黄色固体的2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(3-氟苯基)乙酰胺。LCMS(ES)[M+1]+m/z 335。
步骤3
向用惰性氮气氛围吹扫及维持的40mL小瓶中放入1-[(2-氯吡啶-4-基)氧基]-2-甲基丙-2-醇(1.00g,4.96mmol,1.00当量)、Sn2Me6(1.71g,5.21mmol,1.05当量)、甲苯(30mL)、Pd(PPh3)4(0.57g,0.50mmol,0.10当量)。在100℃下搅拌所得溶液2hr。向其中添加2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(3-氟苯基)乙酰胺(1.16g,3.471mmol,0.7当量)、Pd(PPh3)4(0.57g,0.496mmol,0.10当量)。在100℃下搅拌所得溶液过夜。真空浓缩所得混合物。将残余物施加至含二氯甲烷/甲醇(20:1)的硅胶柱上。通过使用以下条件的制备型HPLC纯化粗产物:柱,Sunfire Prep C18 OBD柱,50*250mm,5μm 10nm;移动相A,水(0.1%FA)及移动相B,AcCN(15min内自5%移动相B至40%);由此产生48.2mg(2.09%)呈白色固体的N-(3-氟苯基)-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z466。1H NMR(300MHz,DMSO-d6)δ10.43(s,1H),8.44(d,J=5.6Hz,1H),7.78(d,J=2.5Hz,1H),7.60-7.49(m,1H),7.37-7.24(m,2H),7.02(dd,J=5.6,2.6Hz,1H),6.92-6.80(m,1H),4.65(s,1H),4.44(s,2H),3.80(s,2H),3.36(s,3H),3.21(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.07-1.99(m,2H),1.17(s,6H)。
实施例1.287
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(1-甲基-6-氧代-1,6-二氢吡啶-3-基)乙酰胺(化合物281)
用5-氨基-1-甲基吡啶-2-酮替换氧杂环戊-3-胺,与化合物135类似地合成化合物281。LCMS(ES)[M+1]+m/z:421;1H-NMR(300MHz,DMSO-d6,ppm):δ10.01(s,1H),8.46(d,J=5.6Hz,1H),8.07(d,J=2.8Hz,1H),7.78(d,J=2.6Hz,1H),7.40(dd,J=9.7,2.9Hz,1H),7.02(dd,J=5.6,2.6Hz,1H),6.38(d,J=9.6Hz,1H),4.35(s,2H),3.83(s,3H),3.37(s,3H),3.35(s,3H),3.20(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.04-1.99(m,2H)。
实施例1.288
合成2-[(2-{2H,3H-[1,4]间二氧杂环己烯并[2,3-c]吡啶-7-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(3-氟苯基)乙酰胺(化合物282)
通过用7-溴-2H,3H-[1,4]间二氧杂环己烯并[2,3-c]吡啶替换1-[(2-氯吡啶-4-基)氧基]-2-甲基丙-2-醇,与化合物280类似地合成化合物282。LCMS(ES)[M+1]+m/z:436;1H-NMR(300MHz,DMSO-d6,ppm):δ10.42(s,1H),8.16(0.3HCOOH),8.14(s,1H),7.77(s,1H),7.55(dd,J=12.0,2.1Hz,1H),7.38-7.25(m,2H),6.92-6.80(m,1H),4.45(s,2H),4.41(s,4H),3.35(s,3H),3.18(t,J=7.3Hz,2H),2.80(t,J=7.8Hz,2H),2.04-1.94(m,2H)。
实施例1.289
合成2-{[2-(异喹啉-3-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-[5-(三氟甲氧基)吡啶-3-基]乙酰胺(化合物283)
通过用3-(三甲基锡烷基)异喹啉替换4-甲氧基-2-(三丁基锡烷基)吡啶且用3-氨基-5-三氟甲氧基吡啶替换氧杂环戊-3-胺,与化合物135类似地合成化合物283。LCMS(ES)[M+1]+m/z:495。1H NMR(300MHz,氯仿-d)δ10.96(s,1H),9.33(s,1H),8.80(d,J=2.1Hz,1H),8.71(s,1H),8.33(d,J=2.5Hz,1H),8.23(s,1H),8.14(d,J=7.7Hz,1H),7.78-7.69(m,3H),4.51(s,2H),3.44(s,3H),3.24(m,2H),2.88(m,2H),2.05(m,2H)。
实施例1.290
合成2 2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(5-甲基吡嗪-2-基)乙酰胺(化合物284)
通过用5-甲基吡嗪-2-胺替换叔丁胺,与化合物44类似地合成化合物284。LCMS(ES)[M+1]+m/z:436.2。1H NMR(300MHz,氯仿-d)δ9.59(br,1H),9.40(s,1H),8.62-8.61(m,1H),8.08(s,1H),7.92(s,1H),6.89-6.88(s,1H),4.43-4.42(m,2H),4.21-4.20(m,2H),4.01-4.00(m,2H),3.28(s,3H),3.03-3.01(m,2H),2.76-2.75(m,2H),2.49(s,3H),2.13-4.11(m,2H)。
实施例1.291
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲氧基哒嗪-3-基)乙酰胺(化合物285)
通过用6-甲氧基哒嗪-3-胺替换叔丁胺,与化合物44类似地合成化合物285。LCMS(ES)[M+1]+m/z:452。1H NMR(300MHz,DMSO-d6,ppm)δ11.15(s,1H),8.41(d,J=5.7Hz,1H),8.21(d,J=9.6Hz,1H),8.15(HCOOH),7.74(d,J=2.7Hz,1H),7.22(d,J=9.6Hz,1H),6.98(dd,J=5.7,2.7Hz,1H),4.85(br,1H),4.55(s,2H),4.00-3.97(m,5H),3.66(t,J=4.8Hz,2H),3.36(s,3H),3.21(t,J=7.2Hz,2H),2.83(t,J=7.8Hz,2H),2.07-1.96(m,2H)。
实施例1.292
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲基哒嗪-3-基)乙酰胺(化合物286)
通过用6-甲基哒嗪-3-胺替换叔丁胺,与化合物44类似地合成化合物286。LCMS(ES)[M+1]+m/z:436。1H NMR(300MHz,DMSO-d6,ppmδ11.23(s,1H),8.40(d,J=5.6Hz,1H),8.15(d,9.4Hz),8.14(HCOOH),7.71(d,J=2.6Hz,1H),7.52(d,J=9.2Hz,1H),6.96(dd,J=5.6,2.5Hz,1H),4.86(s,1H),4.55(s,2H),3.97(t,J=4.8Hz,2H),3.63(s,2H),3.35(s,2H),3.21(t,J=7.5Hz,2H),2.83(t,J=7.9Hz,2H),2.55(s,3H),2.06-1.95(m,2H)。
实施例1.293
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(1-甲基-2-氧代-1,2-二氢吡啶-4-基)乙酰胺(化合物287)
通过用4-氨基-1-甲基吡啶-2-酮盐酸盐替换氧杂环戊-3-胺,与化合物135类似地合成化合物287。LCMS(ES)[M+1]+m/z:421;1H-NMR(300MHz,DMSO-d6,ppm):δ10.36(s,1H),8.44(d,J=5.6Hz,1H),7.74(d,J=2.5Hz,1H),7.58(d,J=7.4Hz,1H),7.00(dd,J=5.6,2.6Hz,1H),6.71(d,J=2.2Hz,1H),6.39(dd,J=7.4,2.3Hz,1H),4.42(s,2H),3.80(s,3H),3.36(s,3H),3.33(s,3H),3.20(t,J=7.3Hz,2H),2.84(t,J=7.7Hz,2H),2.04-1.99(m,2H)。
实施例1.294
合成2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-[6-(三氟甲基)吡啶-3-基]乙酰胺(化合物288)
通过用1-(氧杂环己-2-基)-5-(三丁基锡烷基)-1H-吡唑并[3,4-c]吡啶替换4-甲氧基-2-(三丁基锡烷基)吡啶且用6-三氟吡啶-3-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物288。LCMS(ES+):[M+H]+=469.1。1H NMR(400MHz,DMSO-d6)δ11.71(s,1H),9.20(s,1H),9.11(s,1H),9.05(s,1H),8.40(d,J=8.7Hz,1H),8.29(s,1H),7.86(d,J=8.6Hz,1H),4.83(s,2H),3.61(s,2H),3.35-3.32(m,2H),3.11-3.04(m,2H),2.18-2.05(m,2H)。
实施例1.295
合成N-(4-氟苯基)-2-[甲基(2-{1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物289)
通过用1-(氧杂环己-2-基)-5-(三丁基锡烷基)-1H-吡唑并[3,4-c]吡啶替换4-甲氧基-2-(三丁基锡烷基)吡啶且用4-氟苯胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物289。LCMS(ES+):[M+H]+=418.1。1H NMR(400MHz,DMSO-d6)δ10.65(s,1H),9.15(s,1H),8.88(s,1H),8.20(s,1H),7.73-7.67(m,2H),7.18-7.12(m,2H),4.60(s,2H),3.51(s,3H),3.26-3.24(m,2H),3.01-2.96(m,2H),2.12-2.03(m,2H)。
实施例1.296
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(5-甲氧基吡嗪-2-基)乙酰胺(化合物290)
通过用5-甲氧基吡嗪-2-胺替换叔丁胺,与化合物44类似地合成化合物290。LCMS(ES)[M+1]+m/z:452。1H NMR(300MHz,DMSO-d6,ppm)δ10.79(s,1H),8.81(s,1H),8.41(d,J=5.5Hz,1H),8.11(d,J=1.5Hz,1H),7.73(d,J=2.6Hz,1H),6.97(dd,J=5.6,2.6Hz,1H),4.85(br,1H),4.58(s,2H),4.00(t,J=4.7Hz,2H),3.85(s,3H),3.71-3.63(m,2H),3.41(s,3H),3.33-3.15(m,2H),2.83(t,J=7.9Hz,2H),2.08-1.88(m,2H)。
实施例1.297
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(2-甲基嘧啶-5-基)乙酰胺(化合物291)
通过用2-甲基嘧啶-5-胺替换叔丁胺,与化合物44类似地合成化合物291。LCMS(ES)[M+1]+m/z:436。1H NMR(300MHz,DMSO-d6,ppm)δ10.73(s,1H),8.89(s,2H),8.42(d,J=5.6Hz,1H),8.36(s,1H),7.76(d,J=2.5Hz,1H),7.01(dd,J=5.7,2.6Hz,1H),4.45(s,2H),4.04(t,J=4.8Hz,2H),3.70(q,J=5.0Hz,2H),3.36(s,3H),3.22(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.55(s,3H),2.15-1.96(m,2H)。
实施例1.298
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-甲基苯基)乙酰胺(化合物292)
通过用间甲苯胺替换叔丁胺,与化合物44类似地合成化合物292。LCMS(ES)[M+1]+m/z:434。1H NMR(300MHz,DMSO-d6,ppm)δ10.12(s,1H),8.44(d,J=5.6Hz,1H),7.79(d,J=2.5Hz,1H),7.46-7.33(m,2H),7.19-7.13(m,1H),7.00(dd,J=5.6,2.5Hz,1H),6.85(d,J=7.5Hz,1H),4.88(t,J=5.4Hz,1H),4.42(s,2H),4.02(t,J=4.7Hz,2H),3.66(q,J=5.0Hz,2H),3.36(s,3H),3.20(t,J=7.3Hz,2H),2.83(t,J=7.9Hz,2H),2.25(s,3H),2.07-1.96(m,2H)。
实施例1.299
合成2-({2-[4-(2-氨基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-氟苯基)乙酰胺(化合物293)
流程118
步骤1
向50mL 3颈圆底烧瓶中放入N-(2-羟乙基)氨基甲酸叔丁酯(1.47g,9.12mmol,1.20当量)及THF(10mL)。之后在0℃下添加NaH(0.22g,9.17mmol,1.20当量)。在0℃下搅拌所得溶液30min且添加2-氯-4-氟吡啶(1.00g,7.60mmol,1.00当量)。在25℃下搅拌2hr后,通过添加50mL水淬灭反应物。用3×100mL乙酸乙酯萃取所得混合物,将有机层合并,用3×100ml盐水洗涤,经无水硫酸钠干燥。滤出固体且真空浓缩滤液。由此产生1.5g(49.34%)呈黄色油状物的N-[2-[(2-氯吡啶-4-基)氧基]乙基]氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z273。
步骤2.向用惰性氮气氛围吹扫及维持的40mL小瓶中放入N-[2-[(2-氯吡啶-4-基)氧基]乙基]氨基甲酸叔丁酯(1.00g,3.67mmol,1.00当量)、甲苯(30mL)、Sn2Me6(1.26g,3.85mmol,1.05当量)及Pd(PPh3)4(0.42mg,0.36mmol,0.1当量)。在100℃下搅拌所得溶液4h。向其中添加C2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(3-氟苯基)乙酰胺(0.86g,2.57mmol,0.7当量)、Pd(PPh3)4(0.42g,0.36mmol,0.1当量)。在100℃下搅拌过夜后,真空浓缩混合物。将残余物施加至含二氯甲烷/甲醇(20:1)的硅胶柱上。由此产生300mg(15.25%)呈棕色油状物的N-[2-([2-[4-([[(3-氟苯基)氨甲酰基]甲基](甲基)氨基)-5H,6H,7H-环戊并[d]嘧啶-2-基]吡啶-4-基]氧基)乙基]氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z 537。
步骤3
向50mL圆底烧瓶中放入N-[2-([2-[4-([[(3-氟苯基)氨甲酰基]甲基](甲基)氨基)-5H,6H,7H-环戊并[d]嘧啶-2-基]吡啶-4-基]氧基)乙基]氨基甲酸叔丁酯(300mg,1.00当量)、DCM(2mL)及含HCl(气体)的1,4-二噁烷(2mL)。在25℃下搅拌所得溶液2hr。真空浓缩所得混合物。将残余物溶解于5mL MeOH中。通过使用以下条件的制备型HPLC纯化粗产物:柱,Sunfire Prep C18 OBD柱,50*250mm,5μm 10nm;移动相A,水(0.1%FA)及移动相B,AcCN(15min内自5%移动相B达至35%);检测器,UV 254nm。此产生60.5mg呈白色固体的2-({2-[4-(2-氨基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-氟苯基)乙酰胺。LCMS(ES)[M+1]+m/z 437。1H NMR(300MHz,DMSO-d6):δ10.56(s,1H),8.69(d,J=6.0Hz,1H),8.07(br,3H),7.96(d,J=2.6Hz,1H),7.65-7.54(m,1H),7.44-7.27(m,3H),6.97-6.84(m,1H),4.65(s,2H),4.37(s,2H),3.48(s,3H),3.26(s,4H),3.00(t,J=7.9Hz,2H),2.08-3.02(m,2H)。
实施例1.300
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(3-氟苯基)乙酰胺(化合物294)
用3-氟苯胺替换叔丁胺,与化合物348类似地合成化合物294。LCMS(ES)[M+1]+m/z:465。1H NMR(300MHz,DMSO-d6)δ10.44(s,1H),8.43(d,J=5.6Hz,1H),8.18(s,1H),7.75(d,J=2.5Hz,1H),7.60-7.50(m,1H),7.38-7.25(m,2H),7.00(dd,J=5.6,2.6Hz,1H),6.93-6.80(m,1H),4.43(s,2H),4.07(t,J=5.5Hz,2H),3.37(s,3H),3.21(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.59(t,J=5.5Hz,2H),2.21(s,6H),2.06-1.96(m,2H)。
实施例1.301
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(5-甲氧基嘧啶-2-基)乙酰胺(化合物295)
用5-甲氧基嘧啶-2-胺替换叔丁胺,与化合物44类似地合成化合物295。LCMS(ES)[M+1]+m/z:452。1H NMR(300MHz,DMSO-d6)δ10.67(s,1H),8.47-8.39(m,3H),7.77(d,J=2.6Hz,1H),6.98(dd,J=5.6,2.6Hz,1H),4.88(s,1H),4.62(s,2H),4.02(t,J=4.7Hz,2H),3.88(s,3H),3.67(t,J=4.7Hz,2H),3.33(s,3H),3.19(t,J=7.4Hz,2H),2.83(t,J=7.8Hz,2H),2.15-1.96(m,2H)。
实施例1.302
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(1-甲基-1H-吡唑-4-基)乙酰胺(化合物296)
用1-甲基吡唑-4-胺替换叔丁胺,与化合物44类似地合成化合物296。LCMS(ES)[M+1]+m/z:424。1H NMR(300MHz,DMSO-d6)δ10.23(s,1H),8.46(d,J=5.7Hz,1H),7.84(s,1H),7.77(d,J=2.5Hz,1H),7.40(s,1H),7.02(dd,J=5.7,2.3Hz,1H),4.92(t,J=5.4Hz,1H),4.35(s,2H),4.06(t,J=4.8Hz,2H),3.76(s,3H),3.72(d,J=5.0Hz,2H),3.32(s,3H),3.19(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.06-1.95(m,2H)。
实施例1.303
合成2-({2-[6-(羟甲基)异喹啉-3-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺(化合物297)
用6-(((叔丁基二甲基硅基)氧基)甲基)-3-(三甲基锡烷基)异喹啉替换5-[[(叔丁基二甲基硅基)氧基]甲基]-3-(三甲基锡烷基)异喹啉,与化合物270类似地合成化合物297。LCMS(ES)[M+1]+m/z:455。1H NMR(300MHz,DMSO-d6)δ10.51(s,1H),9.33(s,1H),8.69(d,J=2.3Hz,2H),8.13(d,J=8.6Hz,1H),7.96(dd,J=8.4,2.6Hz,1H),7.70-7.64(m,2H),7.18(d,J=8.4Hz,1H),5.49(t,J=5.5Hz,1H),4.68(d,J=5.3Hz,2H),4.49(s,2H),3.45(s,3H),3.29-3.22(m,2H),2.96-2.85(m,2H),2.39(s,3H),2.11-2.00(m,2H)。
实施例1.304
合成2-{[2-(5-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(6-甲基吡啶-3-基)乙酰胺(化合物298)
通过用5-氟-2-(三丁基锡烷基)吡啶替换2-三丁基锡烷基吡啶且用6-甲基吡啶-3-胺替换叔丁胺,与化合物24类似地合成化合物298。LCMS(ES+):[M+H]+=393.1。1H NMR(400MHz,DMSO-d6)δ10.77(s,1H),8.75(d,J=2.8Hz,1H),8.69(d,J=2.6Hz,1H),8.51(dd,J=8.9,4.6Hz,1H),7.98-7.87(m,2H),7.25(d,J=8.4Hz,1H),4.64(s,2H),3.49(s,3H),3.27-3.24(m,2H),3.00-2.95(m,2H),2.42(s,3H),2.12-2.03(m,2H)。
实施例1.305
合成N-叔丁基-2-{[2-(5-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物299)
通过用5-氟-2-(三丁基锡烷基)吡啶替换2-三丁基锡烷基吡啶,与化合物24类似地合成化合物299。LCMS(ES+):[M+H]+=358.1。1H NMR(400MHz,dmso)δ8.79(d,J=2.8Hz,1H),8.55(dd,J=8.8,4.6Hz,1H),8.02(td,J=8.7,2.9Hz,1H),7.88(s,1H),4.30(s,2H),3.40(s,3H),3.22-3.18(m,2H),3.01-2.93(m,2H),2.12-2.01(m,2H),1.24(s,9H)。
实施例1.306
合成N-叔丁基-2-{[2-(5-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物300)
通过用5-氯-2-(三丁基锡烷基)吡啶替换2-三丁基锡烷基吡啶,与化合物24类似地合成化合物300。LCMS(ES+):[M+H]+=374。1H NMR(400MHz,DMSO-d6)δ8.71(dd,J=2.5,0.7Hz,1H),8.38(dd,J=8.5,0.7Hz,1H),8.03(dd,J=8.5,2.5Hz,1H),7.68(s,1H),4.15(s,2H),3.27(s,3H),3.17-3.10(m,2H),2.86-2.79(m,2H),2.04-1.94(m,2H),1.23(s,9H)。
实施例1.307
合成N-叔丁基-2-[甲基(2-{[1,3]噻唑并[4,5-c]吡啶-6-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物301)
用6-溴-[1,3]噻唑并[4,5-c]吡啶替换2-氯-4-(氧杂环丁-3-基氧基)吡啶,与化合物245类似地合成化合物301。LCMS(ES)[M+1]+m/z:397。1H NMR(300MHz,DMSO-d6)δ9.58(s,1H),9.42(d,J=0.9Hz,1H),9.25(d,J=0.9Hz,1H),8.14(0.5HCOOH),7.79(s,1H),4.18(s,2H),3.34(s,3H),3.18(t,J=7.3Hz,2H),2.86(t,J=7.8Hz,2H),2.05-1.99(m,2H),1.22(s,9H)。
实施例1.308
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺(化合物302)
用6-甲基吡啶-3-胺替换5-氨基-2-甲氧基吡啶,与化合物210类似地合成化合物302。LCMS(ES)[M+1]+m/z:463。1H NMR(300MHz,DMSO-d6)δ10.36(s,1H),8.60(d,J=2.6Hz,1H),8.45(d,J=5.7Hz,1H),8.14(s,HCOOH),7.88(dd,J=8.4,2.6Hz,1H),7.79(d,J=2.5Hz,1H),7.17(d,J=8.4Hz,1H),7.05(dd,J=5.8,2.6Hz,1H),4.73(s,1H),4.43(s,2H),3.81(s,2H),3.38(s,3H),3.22(t,J=7.2Hz,2H),2.85(t,J=7.8Hz,2H),2.39(s,3H),2.04-1.96(m,2H),1.17(s,6H)。
实施例1.309
合成N-叔丁基-2-{[2-(5-氟-4-甲基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物303)
通过用5-氟-4-甲基-2-(三丁基锡烷基)吡啶替换2-三丁基锡烷基吡啶,与化合物24类似地合成化合物303。LCMS(ES+):[M+H]+=372.2。1H NMR(400MHz,DMSO-d6)δ8.50(d,J=1.1Hz,1H),8.30(dd,J=6.5,0.9Hz,1H),7.69(s,1H),4.14(s,2H),3.27(s,3H),3.17-3.11(m,2H),2.83-2.76(m,2H),2.37(dd,J=1.7,0.7Hz,3H),2.02-1.93(m,2H),1.22(s,9H)。
实施例1.310
合成N-(6-甲氧基吡啶-3-基)-2-[甲基(2-{[1,3]噻唑并[4,5-c]吡啶-6-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物304)
用6-溴-[1,3]噻唑并[4,5-c]吡啶替换3-氯-2,6-萘啶,与化合物258类似地合成化合物304。LCMS(ES)[M+1]+m/z:448。1H NMR(300MHz,DMSO-d6)δ10.34(s,1H),9.55(s,1H),9.38(d,J=0.9Hz,1H),9.11(d,J=0.9Hz,1H),8.39(d,J=2.6Hz,1H),7.92(dd,J=8.9,2.7Hz,1H),6.78(d,J=8.9Hz,1H),4.44(s,2H),3.79(s,3H),3.42(s,3H),3.23(t,J=7.2Hz,2H),2.87(t,J=7.8Hz,2H),2.12-1.95(m,2H)。
实施例1.311
合成(2R)-N-叔丁基-2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]丙酰胺(化合物305)
通过用4-(氧杂环丁-3-基氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三丁基锡烷基)吡啶,与化合物101类似地合成化合物305。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.49(d,J=5.6Hz,1H),8.15(s,HCOOH),7.90(d,J=2.5Hz,1H),7.81(s,1H),7.06(dd,J=5.7,2.6Hz,1H),5.09(q,J=7.0Hz,1H),4.16(t,J=4.9Hz,2H),3.77(t,J=4.9Hz,1H),3.21-3.01(m,2H),3.11(s,3H),2.95-2.72(m,2H),2.13-1.84(m,2H),1.32(d,J=7.0Hz,3H),1.20(s,9H)。
实施例1.312
合成2-{[2-(5-氟-4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(6-甲基吡啶-3-基)乙酰胺(化合物306)
通过用5-氟-4-甲氧基-2-(三丁基锡烷基)吡啶替换2-三丁基锡烷基吡啶且用6-甲基吡啶-3-胺替换叔丁胺,与化合物24类似地合成化合物306。LCMS(ES+):[M+H]+=423.1。1H NMR(400MHz,DMSO-d6)δ11.74(s,1H),8.97-8.91(m,1H),8.71(d,J=2.7Hz,1H),8.28(d,J=8.1Hz,1H),8.03(s,1H),7.62(d,J=8.6Hz,1H),4.82(s,2H),3.90(s,3H),3.60(s,3H),3.50-3.46(m,2H),3.09-3.05(m,2H),2.57(s,3H),2.17-2.08(m,2H)。
实施例1.313
合成N-(3-氟苯基)-2-[(2-{4-[(1-羟基环丙基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物307)
通过用{1-[(叔丁基二甲基硅基)氧基]环丙基}甲醇替换1-(2-羟乙基)吡咯烷,与化合物252类似地合成化合物307。LCMS(ES)[M+1]+m/z:464.2。1H NMR(300MHz,DMSO-d6)δ10.41(s,1H),8.43(d,J=5.6Hz,1H),7.84(d,J=2.5Hz,1H),7.55(ddd,J=11.4,3.4,1.9Hz,1H),7.45-7.21(m,2H),7.10(dd,J=5.6,2.5Hz,1H),6.86(ddt,J=8.8,5.5,2.9Hz,1H),4.98(s,1H),4.45(s,2H),3.65(s,2H),3.34(s,3H),3.20(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.05-1.96(m,2H),0.93(t,J=6.6Hz,2H),0.86(d,J=5.0Hz,2H)。
实施例1.314
合成N-(6-环丙基吡啶-3-基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物308)
通过用6-环丙基-3-氨基吡啶替换叔丁胺,与化合物44类似地合成化合物308。LCMS(ES)[M+1]+m/z:461。1H NMR(300MHz,DMSO-d6,ppm)δ10.34(s,1H),8.55(d,J=2.5Hz,1H),8.44(d,J=5.6Hz,1H),8.14(HCOOH),7.88(dd,J=8.5,2.6Hz,1H),7.78(d,J=2.5Hz,1H),7.20(d,J=8.5Hz,1H),7.02(dd,J=5.6,2.6Hz,1H),4.95(s,1H),4.42(s,2H),4.03(t,J=4.8Hz,2H),3.68(t,J=4.8Hz,2H),3.37(s,3H),3.21(t,J=7.3Hz,2H),2.84(t,J=7.9Hz,2H),2.06-1.97(m,3H),0.95-0.77(m,4H)。
实施例1.315
合成(2R)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲氧基吡啶-3-基)丙酰胺(化合物309)
用5-氨基-2-甲氧基吡啶替换3-氟苯胺,与化合物251类似地合成化合物309。LCMS(ES)[M+1]+m/z:465。1H NMR(300MHz,DMSO-d6,ppm)δ10.43(s,1H),8.48(d,J=5.6Hz,1H),8.33(d,J=2.6Hz,1H),7.93-7.83(m,2H),7.07(dd,J=5.6,2.6Hz,1H),6.76(d,J=8.9Hz,1H),5.26(q,J=6.9Hz,1H),4.94(t,J=5.4Hz,1H),4.13(t,J=4.8Hz,2H),3.79(s,3H),3.74(q,J=4.9Hz,2H),3.20(s,3H),3.24-3.06(m,2H),2.98-2.78(m,2H),2.12-1.92(m,2H),1.46(d,J=7.0Hz,3H)。
实施例1.316
合成(2R)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(1-甲基-1H-吡唑-4-基)丙酰胺(化合物310)
用1-甲基吡唑-4-胺替换3-氟苯胺,与化合物251类似地合成化合物310。LCMS(ES)[M+1]+m/z:438。1H NMR(300MHz,DMSO-d6,ppm)δ10.41(s,1H),8.54(d,J=5.7Hz,1H),7.88(d,J=2.6Hz,1H),7.84(s,1H),7.38(s,1H),7.12(dd,J=5.9,2.7Hz,1H),5.26(q,J=7.1Hz,1H),4.96(t,J=5.2Hz,1H),4.17(s,2H),3.87-3.68(m,5H),3.23-3.09(m,5H),3.03-2.77(m,2H),2.23-1.91(m,2H),1.44(d,J=7.0Hz,3H)。
实施例1.317
合成(2R)-N-叔丁基-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙酰胺(化合物311)
用2-甲基丙-2-胺替换3-氟苯胺,与化合物251类似地合成化合物311。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6,ppm)δ8.49(d,J=5.6Hz,1H),8.15(s,HCOOH),7.90(d,J=2.5Hz,1H),7.81(s,1H),7.06(dd,J=5.7,2.6Hz,1H),5.09(q,J=7.0Hz,1H),4.16(t,J=4.9Hz,2H),3.77(t,J=4.9Hz,1H),3.21-3.01(m,2H),3.11(s,3H),2.95-2.72(m,2H),2.13-1.84(m,2H),1.32(d,J=7.0Hz,3H),1.20(s,9H)。
实施例1.318
合成(2R)-N-(6-甲氧基吡啶-3-基)-2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]丙酰胺(化合物312)
用(2R)-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(6-甲氧基吡啶-3-基)丙酰胺替换N-叔丁基-2-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)乙酰胺,与化合物245类似地合成化合物312。LCMS(ES)[M+1]+m/z:477。1H NMR(300MHz,DMSO-d6,ppm)δ10.35(s,1H),8.50(d,J=5.6Hz,1H),8.33(d,J=2.6Hz,1H),8.15(s,HCOOH),7.89(dd,J=8.9,2.7Hz,1H),7.73(d,J=2.6Hz,1H),6.91(dd,J=5.6,2.6Hz,1H),6.75(d,J=8.9Hz,1H),5.50-5.42(m,1H),5.20(q,J=7.0Hz,1H),4.97(td,J=6.7,4.1Hz,2H),4.64-4.53(m,2H),3.79(s,3H),3.33-3.05(m,5H),2.96-2.73(m,2H),2.18-1.86(m,2H),1.47(d,J=7.0Hz,3H)。
实施例1.319
合成N-(4-氟苯基)-2-[甲基(2-{1-甲基-1H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物313)
通过用1-甲基-5-(三丁基锡烷基)-1H-吡唑并[3,4-c]吡啶替换2-三丁基锡烷基吡啶且用4-氟苯胺替换叔丁胺,与化合物24类似地合成化合物313。LCMS(ES+):[M+H]+=432.1。1H NMR(400MHz,DMSO-d6)δ10.70(s,1H),9.37(s,1H),8.95(s,1H),8.26(s,1H),7.71(dd,J=8.9,5.0Hz,2H),7.16(dd,J=8.9Hz,2H),4.69(s,2H),4.27(s,3H),3.58(s,3H),3.39-3.38(m,2H),3.11-3.04(m,2H),2.17-2.06(m,2H)。
实施例1.320
合成N-(4-氟苯基)-2-[甲基(2-{2-甲基-2H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物314)
通过用2-甲基-5-(三丁基锡烷基)-1H-吡唑并[3,4-c]吡啶替换2-三丁基锡烷基吡啶且用4-氟苯胺替换叔丁胺,与化合物24类似地合成化合物314。LCMS(ES+):[M+H]+=432.1。1H NMR(400MHz,DMSO-d6)δ10.77-10.64(m,1H),9.30(s,1H),8.93(d,J=1.3Hz,1H),8.69(s,1H),7.74-7.65(m,2H),7.15(dd,J=8.9Hz,2H),4.65(s,2H),4.33(s,3H),3.53(s,3H),3.04-2.99(m,2H),2.13-2.05(m,2H)。
实施例1.321
合成2-({2-[4-({[1-(3-氟苯基)-1H-1,2,4-三唑-5-基]甲基}(甲基)氨基)-5H,6H,7H-环戊并[d]嘧啶-2-基]吡啶-4-基}氧基)乙-1-醇(化合物315)
流程119
步骤1
在室温下向50mL圆底烧瓶中添加N-(氨甲酰基甲基)氨基甲酸叔丁酯(2.0g,11.48mmol,1.00当量)、THF(20mL)及DMF-DMA(2.74g,22.99mmol,2.00当量)。在60℃下搅拌所得混合物2h。将所得混合物冷却至室温且减压浓缩。由此产生2.5g呈黄色油状物的(2-(((二甲基氨基)亚甲基)氨基)-2-氧代乙基)氨基甲酸叔丁酯。粗产物不经进一步纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:230。
步骤2
在室温下向100mL圆底烧瓶中添加(2-(((二甲基氨基)亚甲基)氨基)-2-氧代乙基)氨基甲酸叔丁酯(2.5g,10.90mmol,1.00当量)、HOAc(30mL)及(3-氟苯基)肼盐酸盐(1.77g,10.90mmol,1.00当量)。在60℃下搅拌所得混合物1h。将所得混合物冷却至室温且减压浓缩。通过硅胶柱色谱,用PE/EA(5:1)洗脱来纯化残余物,得到呈棕色固体的((1-(3-氟苯基)-1H-1,2,4-三唑-5-基)甲基)氨基甲酸叔丁酯(1.5g,自步骤一起总计45%)。LCMS(ES)[M+1]+m/z:293。
步骤3
向100mL 3颈圆底烧瓶中添加((1-(3-氟苯基)-1H-1,2,4-三唑-5-基)甲基)氨基甲酸叔丁酯(1.5g,5.13mmol,1.00当量)及DMF(30mL)。在0℃下向以上混合物分批添加NaH(60%于矿物油中)(190mg,7.92mmol,1.50当量)。在相同温度下再搅拌所得混合物30min。在0℃下向以上混合物逐滴添加CH3I(1.75g,12.31mmol,2.4当量)。在室温下再搅拌所得混合物1h。通过添加水(30mL)将反应物淬灭,用EtOAc(50mL×2)萃取。将合并的有机相用盐水(30mL×3)洗涤,经无水硫酸钠干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用PE/EA(3:1)洗脱来纯化残余物,得到呈黄色油状物的((1-(3-氟苯基)-1H-1,2,4-三唑-5-基)甲基)(甲基)氨基甲酸叔丁酯(1.5g,95%)。LCMS(ES)[M+1]+m/z:307。
步骤4
在室温下向100mL圆底烧瓶中添加((1-(3-氟苯基)-1H-1,2,4-三唑-5-基)甲基)(甲基)氨基甲酸叔丁酯(1.5g,4.90mmol,1.00当量)、DCM(30mL)及HCl(g)(2M于Et2O中)(30mL)。在室温下搅拌所得混合物6h。真空浓缩所得混合物。由此产生1.5g呈黄色固体的粗物质1-(1-(3-氟苯基)-1H-1,2,4-三唑-5-基)-N-甲基甲胺盐酸盐,其不经进一步纯化即直接用于下一步骤中。LCMS(ES)[M-HCl+1]+m/z:207。
步骤5
在室温下向100mL圆底烧瓶中添加2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(777mg,4.11mmol,1.00当量)、NMP(30mL)、1-(1-(3-氟苯基)-1H-1,2,4-三唑-5-基)-N-甲基甲胺盐酸盐(1.56g,6.17mmol,1.5当量)及DIEA(1.6g,12.38mmol,3.00当量)。在60℃下搅拌所得混合物16h。将反应物冷却至室温且通过添加水(30mL)来淬灭,用EtOAc(50mL×2)萃取。将合并的有机相用盐水(30mL)洗涤,减压浓缩。通过硅胶柱色谱,用PE/EA(1:1)洗脱来纯化残余物,得到呈黄色油状物的2-氯-N-((1-(3-氟苯基)-1H-1,2,4-三唑-5-基)甲基)-N-甲基-6,7-二氢-5H-环戊并[d]嘧啶-4-胺(1.0g,68%)。LCMS(ES)[M+1]+m/z:359。
步骤6
在室温下向40mL小瓶中添加2-氯-N-((1-(3-氟苯基)-1H-1,2,4-三唑-5-基)甲基)-N-甲基-6,7-二氢-5H-环戊并[d]嘧啶-4-胺(650mg,1.81mmol,0.70当量)、甲苯(30mL)、4-[2-(氧杂环己-2-基氧基)乙氧基]-2-(三甲基锡烷基)吡啶(1g,2.59mmol,1.00当量)及Pd(PPh3)4(300mg,0.26mmol,0.10当量)。在100℃下于氮气氛围下搅拌所得混合物12h。将反应混合物冷却至室温,减压浓缩以移除溶剂,通过硅胶柱色谱,用CH2Cl2/MeOH(10:1)洗脱来纯化残余物,得到呈黄色油状物的N-((1-(3-氟苯基)-1H-1,2,4-三唑-5-基)甲基)-N-甲基-2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-胺(300mg,21%)。LCMS(ES)[M+1]+m/z:546。
步骤7
在室温下向20mL小瓶中添加N-((1-(3-氟苯基)-1H-1,2,4-三唑-5-基)甲基)-N-甲基-2-(4-(2-((四氢-2H-吡喃-2-基)氧基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-胺(300mg,0.55mmol,1.00当量)、MeOH(5mL)及TsOH(95mg,0.55mmol,1.00当量)。在室温下搅拌所得溶液1h。通过使用以下条件的制备型HPLC纯化反应溶液:Sunfire PrepC18 OBD柱,50*250mm,5μm,10nm,移动相,水(0.1%FA)及CH3CN(12min内自5%相B达至23%),检测器,UV 254nm。冷冻干燥目标的洗脱份,由此产生158.4mg(57%)呈棕色半固体的2-((2-(4-(((1-(3-氟苯基)-1H-1,2,4-三唑-5-基)甲基)(甲基)氨基)-6,7-二氢-5H-环戊并[d]嘧啶-2-基)吡啶-4-基)氧基)乙-1-醇甲酸盐。LCMS[M+H]+:462。1H NMR(300MHz,DMSO-d6)δ8.41(d,J=5.6Hz,1H),8.07(s,1H),7.66(dt,J=9.0,1.8Hz,1H),7.66-7.47(m,3H),7.39-7.26(m,1H),7.01(dd,J=5.6,2.6Hz,1H),5.15(s,2H),4.11(t,J=4.8Hz,2H),3.77(t,J=4.8Hz,2H),3.29(s,3H),3.06(t,J=7.3Hz,2H),2.79(t,J=7.8Hz,2H),2.00-1.90(p,J=7.6Hz,2H)。
实施例1.322
合成(2R)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲基吡啶-3-基)丙酰胺(化合物316)
通过用6-甲基吡啶-3-胺替换3-氟苯胺,与化合物251类似地合成化合物316。LCMS(ES)[M+1]+m/z:449。1H NMR(300MHz,DMSO-d6,ppm)δ10.58(s,1H),8.61(d,J=2.6Hz,1H),8.47(d,J=5.6Hz,1H),8.16(s,HCOOH),7.91(dd,J=8.4,2.6Hz,1H),7.86(d,J=2.5Hz,1H),7.15(d,J=8.4Hz,1H),7.06(dd,J=5.6,2.6Hz,1H),5.26(q,J=6.9Hz,1H),4.12(t,J=4.8Hz,2H),3.75(t,J=4.7Hz,2H),3.19(s,3H),3.26-3.00(m,2H),2.96-2.70(m,2H),2.37(s,3H),2.17-1.84(m,2H),1.46(d,J=7.0Hz,3H)。
实施例1.323
合成N-叔丁基-2-[甲基(2-{4-[(3S)-氧杂环戊-3-基氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物317)
通过用(3S)-氧杂环戊-3-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与化合物174类似地合成化合物317。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6,ppm)δ8.48(d,J=5.6Hz,1H),7.84(d,J=2.6Hz,1H),7.69(s,1H),7.04(dd,J=5.7,2.6Hz,1H),5.22(t,J=3.2Hz,1H),4.11(s,2H),3.95(dd,J=10.3,4.5Hz,1H),3.93 -3.73(m,3H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.39-2.21(m,1H),2.04-1.97(m,3H),1.25(s,9H)。
实施例1.324
合成N-叔丁基-2-[甲基(2-{4-[(3R)-氧杂环戊-3-基氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物318)
通过用(3R)-氧杂环戊-3-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与化合物174类似地合成化合物318。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6,ppm)δ8.48(d,J=5.6Hz,1H),7.84(d,J=2.6Hz,1H),7.69(s,1H),7.04(dd,J=5.7,2.6Hz,1H),5.22(t,J=3.2Hz,1H),4.11(s,2H),3.95(dd,J=10.3,4.5Hz,1H),3.93 -3.73(m,3H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.39-2.21(m,1H),2.04-1.97(m,3H),1.25(s,9H)。
实施例1.325
合成2-({2-[4-({[4-(3-氟苯基)-4H-1,2,4-三唑-3-基]甲基}(甲基)氨基)-5H,6H,7H-环戊并[d]嘧啶-2-基]吡啶-4-基}氧基)乙-1-醇(化合物319)
流程120
步骤1
向250mL圆底烧瓶中放入1-氟-3-异硫氰基苯(5g,32.643mmol,1.00当量)、2-甲氧基乙酰肼(3.98g,38.229mmol,1.17当量)及EtOH(60.00mL)。在80℃下搅拌所得溶液1hr。收集沉淀物且自H2O再晶体。将该固体及NaOH(130.57mL,261.144mmol,8.00当量)放入250mL圆底烧瓶中。使所得溶液在100℃下于搅拌下再反应1hr。将所得溶液转移至烧杯,用HCl(2mol/L)中和至6,应用于抽吸过滤,用水洗涤。由此产生6g(76.9%)呈白色固体的4-(3-氟苯基)-5-(甲氧基甲基)-2H-1,2,4-三唑-3-硫酮。LCMS(ES)[M+1]+m/z:240。
步骤2
将起始4-(3-氟苯基)-5-(甲氧基甲基)-2H-1,2,4-三唑-3-硫酮(5.5g,22.987mmol,1.00当量)于CH2Cl2(40mL)中的溶液冷却至0℃,且在冷却及搅拌下分批添加H2O2(1.18mL,50.649mmol,2.20当量)于AcOH(27mL)中的30%水溶液。随后移除冰浴,且在环境温度下继续搅拌3h。在冷却下用NaOH将反应混合物碱化至pH 10。分离有机层,且用CH2Cl2(2×100mL)洗涤水层。将合并的萃取物用Na2SO4干燥且蒸发。通过柱色谱(DCM/MeOH,100:0至70:30)纯化残余物。由此产生3.2g(67.18%)呈灰白色固体的4-(3-氟苯基)-3-(甲氧基甲基)-1,2,4-三唑。LCMS(ES)[M+1]+m/z:208。
步骤3
向250mL圆底烧瓶中放入4-(3-氟苯基)-3-(甲氧基甲基)-1,2,4-三唑(3.00g,14.478mmol,1.00当量)、AlCl3(19.31g,144.782mmol,10当量)、AcCN(100.00mL)。在80℃下搅拌所得溶液16hr。冷却反应混合物,且通过使用以下条件的急骤制备型HPLC(IntelFlash-1)纯化粗产物:柱,C18硅胶;移动相,15min内自H2O(FA)/ACN=10:1增加至H2O(FA)/ACN=5:1。由此产生1.2g(42.90%)呈黄色固体的[4-(3-氟苯基)-1,2,4-三唑-3-基]甲醇。LCMS(ES)[M+1]+m/z:194。
步骤4
向100mL圆底烧瓶中放入[4-(3-氟苯基)-1,2,4-三唑-3-基]甲醇(1.20g,6.212mmol,1.00当量)、SOCl2(1.11g,9.330mmol,1.50当量)、DCM(30.00mL)。在室温下搅拌所得溶液6hr。真空浓缩所得混合物。用3×30mL二氯甲烷萃取所得溶液,且将有机层合并且经无水硫酸钠干燥并浓缩。由此产生1.28g(97.37%)呈无色油状物的3-(氯甲基)-4-(3-氟苯基)-1,2,4-三唑。LCMS(ES)[M+1]+m/z:212。
步骤5
向100mL圆底烧瓶中放入3-(氯甲基)-4-(3-氟苯基)-1,2,4-三唑(1.20g,5.671mmol,1.00当量)、含甲胺的乙醇(30wt.%0.86g,8.372mmol,1.48当量)、EtOH(30.00mL)。在60℃下搅拌所得溶液4hr。用3×30mL二氯甲烷萃取所得溶液,且将有机层合并且经无水硫酸钠干燥并浓缩。由此产生1.0g(85.51%)呈白色固体的[[4-(3-氟苯基)-1,2,4-三唑-3-基]甲基](甲基)胺。LCMS(ES)[M+1]+m/z:207。
步骤6
向100mL圆底烧瓶中放入[[4-(3-氟苯基)-1,2,4-三唑-3-基]甲基](甲基)胺(1.00g,4.849mmol,1.00当量)、2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(1.10g,5.819mmol,1.20当量)、DIEA(1.25g,9.698mmol,2当量)、MeOH(20.00mL)。在室温下搅拌所得溶液8hr。用3×30mL二氯甲烷萃取所得溶液,且将有机层合并,经无水硫酸钠干燥并真空浓缩。将残余物施加至含乙酸乙酯/石油醚(3:1)的硅胶柱上。由此产生1g(57.47%)呈白色固体的2-氯-N-[[4-(3-氟苯基)-1,2,4-三唑-3-基]甲基]-N-甲基-5H,6H,7H-环戊并[d]嘧啶-4-胺。LCMS(ES)[M+1]+m/z:359。
步骤6
向用惰性氮气氛围吹扫及维持的100mL圆底烧瓶中放入2-氯-N-[[4-(3-氟苯基)-1,2,4-三唑-3-基]甲基]-N-甲基-5H,6H,7H-环戊并[d]嘧啶-4-胺(700.00mg,1.951mmol,1.00当量)、4-氟-2-(三丁基锡烷基)吡啶(903.99mg,2.341mmol,1.20当量)、Pd(dppf)Cl2(285.49mg,0.390mmol,0.2当量)、DMF(30.00mL)。在120℃下搅拌所得溶液16hr。使反应混合物冷却。将残余物施加至含二氯甲烷/甲醇(10:1)的硅胶柱上。由此产生230mg(28.11%)呈棕色油状物的N-[[4-(3-氟苯基)-1,2,4-三唑-3-基]甲基]-2-(4-氟吡啶-2-基)-N-甲基-5H,6H,7H-环戊并[d]嘧啶-4-胺。LCMS(ES)[M+1]+m/z:420。
步骤7
向100mL圆底烧瓶中放入N-[[4-(3-氟苯基)-1,2,4-三唑-3-基]甲基]-2-(4-氟吡啶-2-基)-N-甲基-5H,6H,7H-环戊并[d]嘧啶-4-胺(200.00mg,0.477mmol,1.00当量)、NaH(57.21mg,2.384mmol,5当量)、DMSO(10.00mL)。在0℃下搅拌所得溶液30min且添加乙二醇(147.98mg,2.384mmol,5.00当量),在室温下搅拌溶液2hr。用3×30mL二氯甲烷萃取所得溶液且将有机层合并,经无水硫酸钠干燥且浓缩。通过使用以下条件的制备型HPLC纯化残余物:柱:Sunfire Prep C18 OBD柱,50*250mm,5μm 10nm;移动相A:水(0.1%FA),移动相B:AcCN;流动速率:90mL/min;梯度:15min内自5%B至35%B,35%B;波长:220nm。由此产生63.9mg(29.04%)呈棕色固体的2-([2-[4-([[4-(3-氟苯基)-1,2,4-三唑-3-基]甲基](甲基)氨基)-5H,6H,7H-环戊并[d]嘧啶-2-基]吡啶-4-基]氧基)乙醇甲酸盐。LCMS(ES)[M+1]+m/z:462。1H NMR(300MHz,DMSO-d6)δ8.72(s,1H),8.43(d,J=5.6Hz,1H),7.67(d,J=2.6Hz,1H),7.63-7.53(m,1H),7.48-7.33(m,2H),7.25-7.19(m,1H),7.02(dd,J=5.7,2.6Hz,1H),5.13(s,2H),4.16(t,J=4.9Hz,2H),3.78(t,J=4.8Hz,2H),3.14(s,3H),2.99(t,J=7.3Hz,2H),2.77(t,J=7.8Hz,2H),1.98-1.88(m,2H)。
实施例1.326
合成(3S)-1-(3-氟苯基)-3-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)哌啶-2-酮(化合物320)
流程121
步骤1
向用惰性氮气氛围吹扫及维持的250mL圆底烧瓶中放入N-(2-氧代哌啶-3-基)氨基甲酸叔丁酯(10.00g,46.67mmol,1.00当量)、甲基[(甲基氨基)甲基]胺(0.69g,9.31mmol,0.20当量)、1-氟-3-碘苯(12.43g,56.01mmol,1.20当量)、二噁烷(100.00mL)、K3PO4(19.81g,93.34mmol,2.00当量)、CuI(0.89g,4.67mmol,0.10当量)。在110℃下搅拌所得溶液过夜。将反应混合物冷却至室温。滤出固体。浓缩所得混合物。将残余物施加至含THF/PE(15%)的硅胶柱上。由此产生8G(55.59%)呈黄色固体的N-[1-(3-氟苯基)-2-氧代哌啶-3-基]氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z:309。
步骤2
向250mL 3颈圆底烧瓶中放入N-[1-(3-氟苯基)-2-氧代哌啶-3-基]氨基甲酸叔丁酯(8.00g,25.94mmol,1.00当量)、DMF(100.00mL)。之后在0℃下分批添加NaH(0.93g,38.75mmol,1.49当量)。在0℃下于搅拌下向其逐滴添加MeI(4.42g,31.13mmol,1.20当量)。在室温下搅拌所得溶液3h。随后通过添加50mL水/冰来淬灭反应物。用3×100mL乙酸乙酯萃取所得溶液,且将有机层合并且经无水硫酸钠干燥并浓缩。将残余物施加至含THF/PE(20%)的硅胶柱上。由此产生6.5g(77.71%)呈无色油状物的N-[1-(3-氟苯基)-2-氧代哌啶-3-基]-N-甲基氨基甲酸叔丁酯。LCMS(ES)[M+1]+m/z:323。
步骤3
向250mL圆底烧瓶中放入N-[1-(3-氟苯基)-2-氧代哌啶-3-基]-N-甲基氨基甲酸叔丁酯(6.50g,20.16mmol,1.00当量)、DCM(20.00mL)。之后在0℃下于搅拌下逐滴添加含HCl(气体)的1,4-二噁烷(10.08mL,40.32mmol,2.00当量)。在室温下搅拌所得溶液3h。通过过滤收集固体。由此产生5g(95.85%)呈白色固体的1-(3-氟苯基)-3-(甲基氨基)哌啶-2-酮盐酸盐。LCMS(ES)[M-HCl+1]+m/z:223。
步骤4
向100mL圆底烧瓶中放入2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(2.00g,10.58mmol,1.00当量)、1-(3-氟苯基)-3-(甲基氨基)哌啶-2-酮盐酸盐(2.74g,10.58mmol,1.00当量)、NMP(20.00mL)、DIEA(4.10g,31.74mmol,3.00当量)。在60℃下搅拌所得溶液5h。将反应混合物冷却至室温。通过使用以下条件的制备型HPLC纯化粗产物(5g):柱,XBridge Prep C18OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3.H2O)及CAN(11min内自30%相B达至80%);检测器,254。由此产生2g(50.43%)呈黄色固体的3-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-1-(3-氟苯基)哌啶-2-酮。LCMS(ES)[M+1]+m/z:375。
步骤5
向用惰性氮气氛围吹扫及维持的40mL小瓶中放入3-([2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-1-(3-氟苯基)哌啶-2-酮(2.00g,5.34mmol,1.00当量)、DMF(20.00mL)、4-氟-2-(三丁基锡烷基)吡啶(2.68g,6.94mmol,1.30当量)、Pd(PPh3)4(0.62g,0.54mmol,0.10当量)。在120℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。将残余物施加至含THF/PE(60%)的硅胶柱上。由此产生1g(43.04%)呈黄色油状物的1-(3-氟苯基)-3-[[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]哌啶-2-酮。LCMS(ES)[M+1]+m/z:436。
步骤6
向100mL 3颈圆底烧瓶中放入2-(氧杂环己-2-基氧基)乙醇(0.30g,2.05mmol,1.00当量)、DMF(10.00mL)。之后在0℃下分批添加NaH(0.10g,4.17mmol,2.03当量)。在0℃下于搅拌下向其逐滴添加1-(3-氟苯基)-3-[[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]哌啶-2-酮(0.98g,2.26mmol,1.10当量)。在室温下搅拌所得溶液3h。随后通过添加10mL水/冰来淬灭反应物。用3×20mL乙酸乙酯萃取所得溶液,且将有机层合并且经无水硫酸钠干燥并浓缩。将残余物施加至含THF/PE(50%)的硅胶柱上。由此产生0.7g(60.73%)呈黄色油状物的1-(3-氟苯基)-3-[甲基(2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]哌啶-2-酮。LCMS(ES)[M+1]+m/z:562。
步骤7
向40mL小瓶放入1-(3-氟苯基)-3-[甲基(2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]哌啶-2-酮(700.00mg,1.25mmol,1.00当量)、MeOH(10.00mL)、PTSA(42.92mg,0.25mmol,0.20当量)。在室温下搅拌所得溶液3h。通过使用以下条件的制备型HPLC纯化粗产物(0.8g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3.H2O)及CAN(11min内自30%相B达至70%);检测器,254。由此产生400mg(67.21%)呈白色固体的1-(3-氟苯基)-3-([2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)哌啶-2-酮。LCMS(ES)[M+1]+m/z:478。
步骤8
向100mL圆底烧瓶中放入1-(3-氟苯基)-3-([2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)哌啶-2-酮(400.00mg,0.84mmol,1.00当量)、DCM(6.00mL)、咪唑(85.54mg,1.26mmol,1.50当量)。之后在0℃下分批添加叔丁基二甲基氯硅烷(151.50mg,1.01mmol,1.20当量)。在室温下搅拌所得溶液5h。浓缩所得混合物。通过使用以下条件的制备型手性HPLC纯化粗产物(500mg):柱,YMC Cellulose-SC,250*21.5mm,5μm;移动相,乙腈及乙醇(0.2%DEA)(70%,10min);检测器,254。由此产生220mg(44.38%)呈白色固体的(3S)-3-[[2-(4-[2-[(叔丁基二甲基硅基)氧基]乙氧基]吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-1-(3-氟苯基)哌啶-2-酮。LCMS(ES)[M+1]+m/z:592。
步骤9
向40mL小瓶中放入(3S)-3-[[2-(4-[2-[(叔丁基二甲基硅基)氧基]乙氧基]吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-1-(3-氟苯基)哌啶-2-酮(220.00mg,0.37mmol,1.00当量)、THF(6.00mL)、Et3N.3HF(299.64mg,1.86mmol,5.00当量)。在室温下搅拌所得溶液过夜。通过使用以下条件的制备型HPLC纯化粗产物(0.3g):柱,XBridge PrepC18 OBD柱,19cm,150mm,5um;移动相,水(0.1%FA)及CAN(11min内自5%相B达至40%);检测器,254。由此产生130mg(73.23%)呈白色固体的(3S)-1-(3-氟苯基)-3-([2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)哌啶-2-酮。手性分析型HPLC条件:柱,(R,R)-WHELK-O1 50*4.6mm,3.5um;移动相,正己烷及乙醇(0.2%DEA)(50%,6min);检测器,254,保留时间:3.233min。LCMS(ES,m/z):[M+H]+:478。1H-NMR(300MHz,DMSO-d6,ppm):δ8.45(d,J=5.6Hz,1H),7.76(d,J=2.6Hz,1H),7.34-7.23(m,1H),7.12-6.93(m,4H),4.92(d,J=6.3Hz,1H),4.61(s,1H),4.14(t,J=4.9Hz,3H),3.75(d,J=5.1Hz,2H),3.56(d,J=11.6Hz,1H),3.30(s,3H),3.21(q,J=6.8Hz,2H),2.83(t,J=7.9Hz,2H),2.55(s,1H),2.10-1.98(m,5H)。
实施例1.327
合成(3R)-1-(3-氟苯基)-3-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)哌啶-2-酮(化合物321)
流程122
步骤1
向100mL圆底烧瓶中放入1-(3-氟苯基)-3-([2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)哌啶-2-酮(400.00mg,0.84mmol,1.00当量)、DCM(6.00mL)、咪唑(85.54mg,1.26mmol,1.50当量)。之后在0℃下分批添加叔丁基二甲基氯硅烷(151.50mg,1.01mmol,1.20当量)。在室温下搅拌所得溶液5h。浓缩所得混合物。通过使用以下条件的制备型手性HPLC纯化粗产物(500mg):柱,YMC Cellulose-SC,250*21.5mm,5μm;移动相,乙腈及乙醇(0.2%DEA)(70%,10min);检测器,254。由此产生220mg(44.38%)呈白色固体的(3R)-3-[[2-(4-[2-[(叔丁基二甲基硅基)氧基]乙氧基]吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-1-(3-氟苯基)哌啶-2-酮。LCMS(ES)[M+1]+m/z:592。
步骤2
向40mL小瓶中放入(3S)-3-[[2-(4-[2-[(叔丁基二甲基硅基)氧基]乙氧基]吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-1-(3-氟苯基)哌啶-2-酮(220.00mg,0.37mmol,1.00当量)、THF(6.00mL)、Et3N·3HF(299.64mg,1.86mmol,5.00当量)。在室温下搅拌所得溶液过夜。通过使用以下条件的制备型HPLC纯化粗产物(0.3g):柱,XBridge PrepC18 OBD柱,19cm,150mm,5um;移动相,水(0.1%FA)及CAN(11min内自5%相B达至40%);检测器,254。由此产生109mg(61.40%)呈白色固体的(3R)-1-(3-氟苯基)-3-([2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)哌啶-2-酮。手性分析型HPLC条件:柱,(R,R)-WHELK-O1 50*4.6mm,3.5um;移动相,正己烷及乙醇(0.2%DEA)(50%,6min);检测器,254,保留时间:2.274min。LCMS(ES,m/z):[M+H]+:478。1H-NMR(300MHz,DMSO-d6,ppm):δ8.45(d,J=5.7Hz,1H),7.76(d,J=2.6Hz,1H),7.30(q,J=8.1,7.3Hz,1H),7.10-6.94(m,4H),4.94(s,1H),4.63(s,1H),4.15(t,J=4.9Hz,3H),3.75(d,J=4.7Hz,2H),3.56(d,J=11.4Hz,1H),3.31(s,3H),3.19(dt,J=11.9,7.8Hz,2H),2.83(t,J=7.9Hz,2H),2.55(s,1H),2.10-1.98(m,5H)。
实施例1.328
合成N-叔丁基-N-甲基-2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物322)
通过用叔丁基(甲基)胺替换5-氨基-2-甲氧基吡啶,与化合物253类似地合成化合物322。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6,ppm)δ8.41(d,J=5.7Hz,1H),7.59(d,J=2.6Hz,1H),6.79(dd,J=5.8,2.6Hz,1H),5.41-5.31(m,1H),4.97(t,J=6.7Hz,2H),4.55(dd,J=7.7,4.5Hz,2H),3.20(s,3H),3.07(t,J=7.5Hz,2H),2.90(s,3H),2.77(t,J=7.8Hz,2H),1.99-1.88(m,2H),1.25(s,9H)。
实施例1.329
合成2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]-1-(哌啶-1-基)乙-1-酮(化合物323)
通过用哌啶替换5-氨基-2-甲氧基吡啶,与化合物253类似地合成化合物323。LCMS(ES)[M+1]+m/z:424。1H NMR(300MHz,DMSO-d6,ppm)δ8.48(d,J=5.6Hz,1H),7.65(d,J=2.6Hz,1H),6.86(dd,J=5.6,2.6Hz,1H),5.49-5.43(m,1H),4.97(t,J=6.7Hz,2H),4.58(dd,J=7.5,4.9Hz,2H),4.51(s,2H),3.50-3.38(m,4H),3.25(s,3H),3.14(t,J=7.4Hz,2H),2.81(t,J=7.9Hz,2H),2.04-1.96(m,2H),1.69-1.57(m,4H),1.51-1.40(m,2H)。
实施例1.330
合成2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]-N-(6-甲基吡啶-3-基)乙酰胺(化合物324)
用6-甲基吡啶-3-胺替换5-氨基-2-甲氧基吡啶,与化合物253类似地合成化合物324。LCMS(ES)[M+1]+m/z:447。1H NMR(300MHz,DMSO-d6,ppm)δ10.35(s,1H),8.62(d,J=2.5Hz,1H),8.45(d,J=5.6Hz,1H),7.92(dd,J=8.4,2.6Hz,1H),7.63(d,J=2.5Hz,1H),7.18(d,J=8.4Hz,1H),6.84(dd,J=5.6,2.6Hz,1H),5.36-5.33(m,1H),4.95-4.85(m,2H),4.52(dd,J=7.6,4.8Hz,2H),4.42(s,2H),3.37(s,3H),3.21(t,J=7.4Hz,2H),2.83(t,J=7.8Hz,2H),2.40(s,3H),2.04-1.99(m,2H)。
实施例1.331
合成N-(4-氯苯基)-2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物325)
通过用4-氯苯胺替换5-氨基-2-甲氧基吡啶,与化合物253类似地合成化合物325。LCMS(ES)[M+1]+m/z:466。1H NMR(300MHz,DMSO-d6,ppm)δ10.36(s,1H),8.46(d,J=5.6Hz,1H),7.65(d,J=8.8Hz,2H),7.62(d,J=2.6Hz,1H),7.35(d,J=8.8Hz,2H),6.85(dd,J=5.6,2.6Hz,1H),5.41-5.28(m,1H),4.90(t,J=6.7Hz,2H),4.51(dd,J=7.5,4.7Hz,2H),4.42(s,2H),3.21(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.08-1.93(m,2H)。
实施例1.332
合成2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]-N-(4-甲基苯基)乙酰胺(化合物326)
通过用4-甲基苯胺替换5-氨基-2-甲氧基吡啶,与化合物253类似地合成化合物326。LCMS(ES)[M+1]+m/z:446。1H NMR(300MHz,DMSO-d6,ppm)δ10.11(s,1H),8.46(d,J=5.7Hz,1H),7.64(t,J=1.9Hz,1H),7.49(d,J=8.0Hz,2H),7.10(d,J=8.0Hz,2H),6.91-6.82(m,1H),5.38-5.29(m,1H),4.90(t,J=6.7Hz,2H),4.51(dd,J=7.4,4.7Hz,2H),4.41(s,2H),3.36(s,3H),3.21(t,J=7.4Hz,2H),2.83(t,J=7.9Hz,2H),2.24(s,3H),2.11-1.93(m,2H)。
实施例1.333
合成N-(4-甲氧基苯基)-2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物327)
通过用对甲氧基苯胺替换5-氨基-2-甲氧基吡啶,与化合物253类似地合成化合物327。LCMS(ES)[M+1]+m/z:462。1H NMR(300MHz,DMSO-d6,ppm)δ10.05(s,1H),8.46(d,J=5.6Hz,1H),7.64(d,J=2.5Hz,1H),7.57-7.46(m,2H),6.93-6.82(m,3H),5.38-5.31(m,1H),4.96-4.85(m,2H),4.52(dd,J=7.5,4.7Hz,2H),4.38(s,2H),3.71(s,3H),3.31(s,3H),3.20(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.11-1.93(m,2H)。
实施例1.334
合成N-叔丁基-2-[甲基(2-{[1,3]噻唑并[5,4-c]吡啶-6-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物328)
用6-氯-[1,3]噻唑并[5,4-c]吡啶替换2-氯-4-(氧杂环丁-3-基氧基)吡啶,与化合物245类似地合成化合物328。LCMS(ES)[M+1]+m/z:397。1H NMR(300MHz,DMSO-d6)δ9.71(s,1H),9.51(d,J=0.9Hz,1H),9.01(d,J=0.9Hz,1H),8.12(HCOOH),7.84(s,1H),4.18(s,2H),3.34(s,3H),3.18(t,J=7.3Hz,2H),2.87(d,J=7.8Hz,2H),2.05-1.97(m,2H),1.24(s,9H)。
实施例1.335
合成N-(6-甲氧基吡啶-3-基)-2-[甲基(2-{[1,3]噻唑并[5,4-c]吡啶-6-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物329)
用6-氯-[1,3]噻唑并[5,4-c]吡啶替换3-氯-2,6-萘啶,与化合物258类似地合成化合物329。LCMS(ES)[M+1]+m/z:448。1H NMR(300MHz,DMSO-d6)δ9.71(s,1H),9.49(d,J=0.9Hz,1H),8.93(d,J=0.9Hz,1H),8.37(d,J=2.7Hz,1H),7.91(dd,J=8.9,2.7Hz,1H),6.76(d,J=8.9Hz,1H),4.47(s,2H),3.79(s,3H),3.40(s,3H),3.22(t,J=7.8Hz,2H),2.87(t,J=7.8Hz,2H),2.07-2,01(m,2H)。
实施例1.336
合成2-[(2-{4-[(1-羟基环丙基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(6-甲基吡啶-3-基)乙酰胺(化合物330)
通过用{1-[(叔丁基二甲基硅基)氧基]环丙基}甲醇替换1-(2-羟乙基)吡咯烷且用6-甲基-3-氨基吡啶替换3-氟苯胺,与化合物252类似地合成化合物330。LCMS(ES)[M+1]+m/z:461.2。1H NMR(300MHz,DMSO-d6)δ10.34(s,1H),8.59(d,J=2.6Hz,1H),8.43(d,J=5.6Hz,1H),8.17(s,1H),7.99-7.75(m,2H),7.38-6.94(m,2H),4.43(s,2H),3.67(s,2H),3.35(s,3H),3.20(t,J=7.1Hz,2H),2.83(t,J=7.8Hz,2H),2.40(s,3H),2.05-1.95(m,2H),0.93(d,J=5.1Hz,2H),0.87(d,J=5.2Hz,2H)。
实施例1.337
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5,5-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺(化合物331)
流程123
步骤1
向用惰性氮气氛围吹扫及维持的500mL 3颈圆底烧瓶中放入NaH(6.82g,284.19mmol,1.10当量)、THF(300.00mL)。在0℃下向其逐滴添加乙酰乙酸甲酯(30.00g,258.36mmol,1.00当量)。在0℃下搅拌所得溶液15min。在15min内在0℃下于搅拌下向其逐滴添加n-BuLi(108.51mL,271.27mmol,1.05当量)。在0℃下,于搅拌下在30min内向混合物中逐滴添加1-碘-2-甲基丙烷(71.32g,387.54mmol,1.50当量)。在室温下搅拌所得溶液30min。用HCl(1mol/L)将溶液的pH值调节至6。用3×500mL乙醚萃取所得溶液,且合并有机层。用3×500mL NaCl萃取所得溶液,且将有机层合并且经无水硫酸钠干燥并浓缩。将残余物施加至含PE/THF(4%)的硅胶柱上。由此产生18g(40.45%)呈黄色液体的6-甲基-3-氧代庚酸甲酯。
步骤2
向用惰性氮气氛围吹扫且维持的500mL 3颈圆底烧瓶中放入6-甲基-3-氧代庚酸甲酯(18.00g,104.52mmol,1.00当量)、CH3CN(400.00mL)、4-乙酰胺基苯磺酰基叠氮化物(25.11g,104.52mmol,1.00当量)。之后在0℃下在搅拌下逐滴添加Et3N(31.73g,313.55mmol,3.00当量)。在室温下搅拌所得溶液过夜。浓缩所得混合物。用300mL乙醚/正己烷=1:1稀释所得溶液。滤出固体。浓缩所得混合物。将残余物施加至含THF/PE(10%)的硅胶柱上。由此产生17.8g(85.92%)呈黄色油状物的2-重氮-6-甲基-3-氧代庚酸甲酯。
步骤3
向用惰性氮气氛围吹扫及维持的500mL 3颈圆底烧瓶中放入Rh2(OAc)4(0.39g,0.87mmol,0.01当量)、DCM(250.00mL)。之后在0℃下于搅拌下逐滴添加2-重氮-6-甲基-3-氧代庚酸甲酯(17.30g,87.27mmol,1.00当量)于DCM(50mL)中的溶液。在室温下搅拌所得溶液4h。用3×200mL二氯甲烷萃取所得溶液,且将有机层合并且经无水硫酸钠干燥并浓缩。将残余物施加至含THF/PE(5.6%)的硅胶柱上。由此产生12.57g(84.62%)呈深绿色液体的2,2-二甲基-5-氧代环戊烷-1-甲酸甲酯。LCMS(ES)[M+1]+m/z:171。
步骤4
向500mL圆底烧瓶中放入2,2-二甲基-5-氧代环戊烷-1-甲酸甲酯(12.00g,70.50mmol,1.00当量)、脲(12.70g,211.47mmol,3.00当量)、EtOH(225.00mL)、含HCl(气体)的1,4-二噁烷(45.00mL)。在100℃下搅拌所得溶液3h。将反应混合物冷却至室温。浓缩所得混合物。用200mL 5%NaOH稀释所得溶液。在80℃下搅拌所得溶液1h。将反应混合物冷却至0℃。用HCl(1mol/L)将溶液的pH值调节至3。通过过滤收集固体。由此产生6.5g(51.16%)呈灰色固体的5,5-二甲基-1H,3H,6H,7H-环戊并[d]嘧啶-2,4-二酮。LCMS(ES)[M-1]+m/z:179。
步骤5
向250mL圆底烧瓶中放入5,5-二甲基-1H,3H,6H,7H-环戊并[d]嘧啶-2,4-二酮(6.50g,36.07mmol,1.00当量)、Et3N(3.65g,36.07mmol,1.00当量)。之后在室温下于搅拌下逐滴添加POCl3(80.00mL)。在80℃下搅拌所得溶液2h。将反应混合物冷却至室温。浓缩所得混合物。用200mL水/冰稀释所得溶液。用Na2CO3将溶液的pH值调节至7-8。用3×200mL二氯甲烷萃取所得溶液,且将有机层合并且经无水硫酸钠干燥并浓缩。将残余物施加至含THF/PE(10%)的硅胶柱上。由此产生7.15g(91.31%)呈淡黄色液体的2,4-二氯-5,5-二甲基-6H,7H-环戊并[d]嘧啶。LCMS(ES)[M+1]+m/z:217。
步骤6
向40mL小瓶中放入2,4-二氯-5,5-二甲基-6H,7H-环戊并[d]嘧啶(1.00g,4.61mmol,1.00当量)、2-(甲基氨基)-N-(6-甲基吡啶-3-基)乙酰胺(1.07g,5.97mmol,1.30当量)、NMP(20.00mL)、DIEA(2.98g,23.03mmol,5.00当量)。在60℃下搅拌所得溶液6h。将反应混合物冷却至室温。通过使用以下条件的制备型HPLC纯化粗产物(3g):柱,XBridge PrepC18 OBD柱,19cm,150mm,5um;移动相,水(0.1%FA)及CAN(11min内自20%相B达至60%);检测器,254。由此产生500mg(30.16%)呈灰白色固体的2-([2-氯-5,5-二甲基-6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺。LCMS(ES)[M+1]+m/z:360。
步骤7
向40mL小瓶中放入2-([2-氯-5,5-二甲基-6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺(500.00mg,1.39mmol,1.00当量)、甲苯(10.00mL)、4-氟-2-(三丁基锡烷基)吡啶(804.78mg,2.08mmol,1.50当量)、Pd(PPh3)4(160.56mg,0.14mmol,0.10当量)。在120℃下搅拌所得溶液过夜。将反应混合物冷却至室温。浓缩所得混合物。将残余物施加至含THF/PE(45%)的硅胶柱上。由此产生300mg(51.35%)呈白色固体的2-[[2-(4-氟吡啶-2-基)-5,5-二甲基-6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-N-(6-甲基吡啶-3-基)乙酰胺。LCMS(ES)[M+1]+m/z:421。
步骤8
向40mL小瓶中放入2-(氧杂环己-2-基氧基)乙醇(208.59mg,1.43mmol,2.00当量)、DMF(10.00mL)。之后在0℃下分批添加NaH(42.80mg,1.78mmol,2.50当量)。在室温下搅拌所得溶液0.5h。在0℃下向其分批添加2-[[2-(4-氟吡啶-2-基)-5,5-二甲基-6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]-N-(6-甲基吡啶-3-基)乙酰胺(300.00mg,0.71mmol,1.00当量)。在室温下搅拌所得溶液2h。随后通过添加20mL水/冰来淬灭反应物。用3×40mL乙酸乙酯萃取所得溶液,且将有机层合并且经无水硫酸钠干燥并浓缩。通过使用以下条件的制备型HPLC纯化粗产物(0.5g):柱,XBridge Prep C18 OBD柱,19cm,150mm,5um;移动相,水(0.1%NH3.H2O)及CAN(11min内自20%相B达至60%);检测器,254。由此产生230mg(58.97%)呈灰白色固体的2-[(5,5-二甲基-2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(6-甲基吡啶-3-基)乙酰胺。LCMS(ES)[M+1]+m/z:547。
步骤9
向20mL小瓶中放入2-[(5,5-二甲基-2-[4-[2-(氧杂环己-2-基氧基)乙氧基]吡啶-2-基]-6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(6-甲基吡啶-3-基)乙酰胺(230.00mg,0.42mmol,1.00当量)、MeOH(5.00mL)、PTSA(36.23mg,0.21mmol,0.50当量)。在室温下搅拌所得溶液1h。通过使用以下条件的制备型HPLC纯化粗产物(0.2g):柱,XBridgePrep C18 OBD柱,19cm,150mm,5um;移动相A,水(0.1%NH3·H2O)及移动相B,AcCN(11min内自20%相B达至60%);检测器,254nm。由此产生166.5mg(85.56%)呈白色固体的2-([2-[4-(2-羟乙氧基)吡啶-2-基]-5,5-二甲基-6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基)-N-(6-甲基吡啶-3-基)乙酰胺。LCMS(ES,m/z):[M+H]+:463。1H-NMR(300MHz,DMSO-d6,ppm):δ10.51(s,1H),8.59(d,J=2.6Hz,1H),8.42(d,J=5.7Hz,1H),7.89(dd,J=8.4,2.5Hz,1H),7.77(d,J=2.5Hz,1H),7.16(d,J=8.4Hz,1H),7.01(dd,J=5.6,2.5Hz,1H),5.00(t,J=5.1Hz,1H),4.30(s,2H),4.01(t,J=4.8Hz,2H),3.67(q,J=4.9Hz,2H),3.32(s,3H),2.88(t,J=7.3Hz,2H),2.39(s,3H),1.89(t,J=7.3Hz,2H),1.46(s,6H)。
实施例1.338及1.339
合成外消旋N-叔丁基-2-{甲基[2-(4-{[(2S,3S)-2-甲基氧杂环丁-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物332)及外消旋N-叔丁基-2-{甲基[2-(4-{[(2R,3S)-2-甲基氧杂环丁-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物333)
流程124
向50mL 3颈圆底烧瓶中放入2-甲基氧杂环丁-3-醇(222mg,2.52mmol,3.00当量)、DMSO(5mL)。之后在0℃下添加NaH(101mg,2.52mmol,3.00当量,60%)。在25℃下搅拌所得溶液30min。在0℃下于搅拌下向其逐滴添加N-叔丁基-2-[[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基]乙酰胺(300mg,0.84mmol,1.00当量)于DMSO(2mL)中的溶液。在25℃下搅拌所得溶液1hr。随后通过添加1mL水淬灭反应物。通过使用以下条件的制备型HPLC(2#SHIMADZU(HPLC-01))纯化粗产物:柱,Atlantis Prep T3 OBD柱,19*150mm5um;移动相,水(0.05%TFA)及ACN(15min内自16%相B达至30%);检测器,UV.254nm。由此产生108.8mg(33.78%)呈灰白色固体之外消旋N-叔丁基-2-[甲基[2-(4-[[(2R,3S)-2-甲基氧杂环丁-3-基]氧基]吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺(化合物332);参(三氟乙酸盐)及53.7mg(23.72%)呈灰白色固体之外消旋N-叔丁基-2-[甲基[2-(4-[[(2S,3S)-2-甲基氧杂环丁-3-基]氧基]吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基]乙酰胺(化合物333);三氟乙酸呈灰白色固体。
化合物332:LCMS(ES)[M+1]+m/z 426。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.79(d,J=2.5Hz,1H),7.69(s,1H),6.91(dd,J=5.6,2.6Hz,1H),5.44(q,J=5.7Hz,1H),5.21(p,J=6.3Hz,1H),4.93-4.83(m,1H),4.49(dd,J=7.4,4.8Hz,1H),4.23-4.04(m,2H),3.27(s,3H),3.15(t,J=7.4Hz,2H),2.81(t,J=7.8Hz,2H),1.98(q,J=7.8Hz,2H),1.30(d,J=6.5Hz,3H),1.26(s,9H)。
化合物333:LCMS(ES)[M+1]+m/z 426。1H NMR(300MHz,DMSO-d6)δ8.69(d,J=5.8Hz,1H),8.04-7.98(m,2H),7.22(dd,J=5.9,2.7Hz,1H),5.26(t,J=5.3Hz,1H),4.89(t,J=6.5Hz,2H),4.40(t,J=6.4Hz,1H),4.35(s,2H),3.47(s,3H),3.25(s,2H),3.04(t,J=7.9Hz,2H),2.10(t,J=7.6Hz,2H),1.50(d,J=6.3Hz,3H),1.27(s,9H)。
实施例1.340
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(4-甲氧基苯基)-N-甲基乙酰胺(化合物334)
通过用4-甲氧基-N-甲基苯胺替换叔丁胺,与化合物44类似地合成化合物334。LCMS(ES)[M+1]+m/z:464。1H NMR(300MHz,DMSO-d6)δ8.52(d,J=5.7Hz,1H),7.78(s,1H),7.48(d,J=8.4Hz,2H),7.05-7.03(m,3H),4.95(t J=5.5Hz,1H),4.19-4.15(m,4H),3.79(s,5H),3.29(s,3H),3.27-3.22(m,5H),3.14(s,2H),2.92-2.71(m,2H),2.13-1.85(m,2H)。
实施例1.341
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-(5-甲氧基-2,3-二氢-1H-吲哚-1-基)乙-1-酮(化合物335)
通过用5-甲氧基-2,3-二氢-1H-吲哚替换叔丁胺,与化合物44类似地合成化合物335。LCMS(ES)[M+1]+m/z:476。1H NMR(300MHz,DMSO-d6)δ8.42(d,J=5.6Hz,1H),7.90(d,J=8.7Hz,1H),7.70(d,J=2.5Hz,1H),6.98(dd,J=5.8,2.6Hz,1H),6.87(d,J=2.6Hz,1H),6.68(d,J=8.7Hz,1H),4.88(t,J=5.3Hz,1H),4.57(s,2H),4.25(t,J=8.3Hz,2H),3.97(d,J=4.9Hz,2H),3.71(s,3H),3.63(q,J=4.6Hz,2H),3.33(s,3H),3.18(t,J=7.7Hz,4H),2.82(t,J=7.9Hz,2H),2.02-1.96(m,2H)。
实施例1.342
合成N-叔丁基-2-[甲基(2-{2-甲基-2H-吡唑并[3,4-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物336)
通过用2-甲基-5-(三丁基锡烷基)-2H-吡唑并[3,4-c]吡啶替换2-三丁基锡烷基吡啶,与化合物24类似地合成化合物336。LCMS(ES+):[M+H]+=394.1。1H NMR(400MHz,DMSO-d6)δ9.37(s,1H),9.03(s,1H),8.84(s,1H),8.06(s,1H),4.45-4.32(m,6H),3.51(s,2H),3.09-3.03(m,2H),2.15-2.07(m,2H),1.25(s,9H)。
实施例1.343
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-[1-(三氟甲基)环丙基]乙酰胺(化合物337)
通过用1-(三氟甲基)环丙-1-胺盐酸盐替换3-氟苯胺,与化合物280类似地合成化合物337。LCMS(ES)[M+1]+m/z:480。1H NMR(300MHz,DMSO-d6)δ9.07(s,1H),8.46(d,J=5.6Hz,1H),8.18(s,HCOOH),7.76(d,J=2.5Hz,1H),7.05(dd,J=5.7,2.6Hz,1H),4.69(s,1H),4.18(s,2H),3.87(s,2H),3.28(s,3H),3.15(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.08-1.92(m,2H),1.24(s,6H),1.22-1.07(m,2H),1.04-0.94(m,2H)。
实施例1.344
合成2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]-N-[1-(三氟甲基)环丙基]乙酰胺(化合物338)
通过用1-(三氟甲基)环丙-1-胺盐酸盐替换5-氨基-2-甲氧基吡啶,与化合物253类似地合成化合物338。LCMS(ES)[M+1]+m/z:464。1H NMR(300MHz,DMSO-d6)δ8.98(s,1H),8.48(d,J=5.5Hz,1H),7.63(d,J=2.6Hz,1H),6.89(dd,J=5.6,2.6Hz,1H),5.54-5.41(m,1H),5.15-4.91(m,2H),4.64-4.54(m,2H),4.18(s,2H),3.33(s,3H),3.16(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.07-1.94(m,2H),1.25-1.14(m,2H),1.03-0.96(s,2H)。
实施例1.345
合成N-(4-氯苯基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物339)
通过用4-氯苯胺替换叔丁胺,与化合物44类似地合成化合物339。LCMS(ES)[M+1]+m/z:454。1H NMR(300MHz,DMSO-d6)δ10.37(s,1H),8.45(d,J=5.7Hz,1H),8.14(s,0.5HCOOH),7.78(d,J=2.4Hz,1H),7.64(d,J=8.9Hz,2H),7.36(d,J=8.9Hz,2H),7.02(s,1H),4.93(t,J=5.3Hz,1H),4.43(s,2H),4.05(t,J=4.7Hz,2H),3.69(d,J=5.0Hz,2H),3.37(s,3H),3.24(t,J=7.1Hz,2H),2.87(t,J=7.9Hz,2H),2.04-1.93(m,2H)。
实施例1.346
合成N-(4-氯苯基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物340)
通过用双环[1.1.1]戊-1-胺盐酸盐替换5-氨基-2-甲氧基吡啶,与化合物253类似地合成化合物340。LCMS(ES)[M+1]+m/z:422。1H NMR(300MHz,DMSO-d6,ppm)δ8.70(s,1H),8.50(dd,J=5.6,1.4Hz,1H),7.68(d,J=2.4Hz,1H),6.90(dt,J=5.6,2.8Hz,1H),5.58-5.43(m,1H),5.05-4.94(m,2H),4.59(dd,J=7.7,4.8Hz,2H),4.13(s,2H),3.30(s,3H),3.16(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.38(s,1H),2.08-1.97(m,2H),1.98(s,6H)。
实施例1.347
合成N-叔丁基-2-[(2-{呋喃并[3,2-c]吡啶-6-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物341)
用6-氯呋喃并[3,2-c]吡啶替换2-氯-4-(氧杂环丁-3-基氧基)吡啶,与化合物245类似地合成化合物341。LCMS(ES)[M+1]+m/z:380。1H NMR(300MHz,DMSO-d6)δ9.03(s,1H),8.60(s,1H),8.20(d,J=2.2Hz,2H),8.15(s,0.5HCOOH),7.79(s,1H),7.20-7.13(m,1H),4.15(s,2H),3.32(s,3H),3.17(t,J=7.4Hz,2H),2.84(t,J=7.8Hz,2H),2.05-1.96(m,2H),1.25(s,9H)。
实施例1.348
合成2-[甲基(2-{4-[(3R)-氧杂环戊-3-基氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-1-(哌啶-1-基)乙-1-酮(化合物342)
通过用哌啶替换叔丁胺,与化合物318类似地合成化合物342。LCMS(ES)[M+1]+m/z:438。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.15(s,0.5HCOOH),7.71(d,J=2.5Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),5.25-5.16(m,1H),4.49(s,2H),3.94(dd,J=10.3,4.5Hz,1H),3.90-3.73(m,3H),3.52-3.40(m,4H),3.25(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.38-2.20(m,1H),2.04-1.94(m,3H),1.71-1.61(m,4H),1.52-1.43(m,2H)。
实施例1.349
合成2-[甲基(2-{4-[(3S)-氧杂环戊-3-基氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-1-(哌啶-1-基)乙-1-酮(化合物343)
通过用哌啶替换叔丁胺,与化合物317类似地合成化合物343。LCMS(ES)[M+1]+m/z:438。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.15(s,0.5HCOOH),7.71(d,J=2.5Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),5.25-5.16(m,1H),4.49(s,2H),3.94(dd,J=10.3,4.5Hz,1H),3.90-3.73(m,3H),3.51-3.41(m,4H),3.25(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.38-2.20(m,1H),2.04-1.94(m,3H),1.71-1.61(m,4H),1.52-1.43(m,2H)。
实施例1.350
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物344)
通过用二甲氨基乙醇替换乙烷-1,2-二醇,与化合物187类似地合成化合物344。LCMS(ES)[M+1]+m/z:478。1H NMR(300MHz,DMSO-d6)δ10.27(s,1H),8.44(d,J=5.6Hz,1H),8.34(d,J=2.6Hz,1H),8.17(s,0.7HCOOH),7.89(dd,J=8.9,2.7Hz,1H),7.76(d,J=2.6Hz,1H),7.01(dd,J=5.6,2.6Hz,1H),6.78(d,J=8.9Hz,1H),4.39(s,2H),4.07(t,J=5.6Hz,2H),3.81(s,3H),3.38(s,3H),3.22(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.58(t,J=5.6Hz,2H),2.20(s,6H),2.06-1.99(m,2H)。
实施例1.351
合成N-(3-氟苯基)-2-[甲基(2-{4-[(1s,3s)-3-羟基环丁氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物345)
通过用4-((1s,3s)-3-(苯甲氧基)环丁氧基)-2-氯吡啶替换1-[(2-氯吡啶-4-基)氧基]-2-甲基丙-2-醇,与化合物280类似地合成化合物345。LCMS(ES)[M+1]+m/z:464。1HNMR(300MHz,DMSO-d6)δ8.55(d,J=6.0Hz,1H),7.89(d,J=2.5Hz,1H),7.55(d,J=11.5Hz,1H),7.43-7.28(m,2H),7.17(dd,J=6.1,2.7Hz,1H),6.92-6.81(m,1H),4.60(s,2H),4.53-4.37(m,1H),4.03-3.87(m,1H),3.59(s,3H),3.39(t,J=7.4Hz,2H),3.08(t,J=7.9Hz,2H),3.00-2.85(m,2H),2.30-2.16(m,2H),2.13-1.98(m,2H)。
实施例1.352
合成N-(6-甲氧基吡啶-3-基)-2-[甲基(2-{4-[(3R)-氧杂环戊-3-基氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物346)
通过用(3R)-氧杂环戊-3-醇替换乙烷-1,2-二醇,与化合物187类似地合成化合物346。LCMS(ES)[M+1]+m/z:477。1H NMR(300MHz,DMSO-d6)δ10.26(s,1H),8.45(d,J=5.6Hz,1H),8.35(d,J=2.6Hz,1H),7.89(dd,J=8.9,2.7Hz,1H),7.73(d,J=2.5Hz,1H),7.00(dd,J=5.7,2.6Hz,1H),6.78(d,J=8.9Hz,1H),5.13-5.06(m,1H),4.39(s,2H),3.80(s,3H),3.90-3.65(m,4H),3.37(s,3H),3.21(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.29-2.11(m,1H),2.09-1.85(m,3H)。
实施例1.353
合成N-(6-甲氧基吡啶-3-基)-2-[甲基(2-{4-[(3S)-氧杂环戊-3-基氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物347)
通过用(3S)-氧杂环戊-3-醇替换乙烷-1,2-二醇,与化合物187类似地合成化合物347。LCMS(ES)[M+1]+m/z:477。1H NMR(300MHz,DMSO-d6)δ10.26(s,1H),8.45(d,J=5.6Hz,1H),8.35(d,J=2.6Hz,1H),7.89(dd,J=8.9,2.7Hz,1H),7.73(d,J=2.5Hz,1H),7.00(dd,J=5.7,2.6Hz,1H),6.78(d,J=8.9Hz,1H),5.13-5.06(m,1H),4.39(s,2H),3.80(s,3H),3.90-3.65(m,4H),3.37(s,3H),3.21(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.29-2.11(m,1H),2.09-1.85(m,3H)。
实施例1.354
合成N-{双环[1.1.1]戊-1-基}-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物349)
通过用双环[1.1.1]戊-1-胺盐酸盐替换6-甲氧基吡啶-3-胺,与化合物187类似地合成化合物349。LCMS(ES)[M+1]+m/z:410。1H NMR(300MHz,DMSO-d6)δ8.73(s,1H),8.47(d,J=5.6Hz,1H),8.15(s,0.5HCOOH),7.81(d,J=2.6Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),4.93(s,1H),4.20-4.09(m,4H),3.77(s,2H),3.27(s,3H),3.16(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.37(s,1H),2.05-1.93(m,2H),1.92(s,6H)。
实施例1.355
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-甲基-1,2-噻唑-5-基)乙酰胺(化合物350)
通过用3-甲基异噻唑-5-胺盐酸盐替换6-甲氧基吡啶-3-胺,与化合物187类似地合成化合物350。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6)δ12.11(s,1H),8.45(d,J=5.7Hz,1H),8.14(s,HCOOH),7.68(d,J=2.7Hz,1H),7.01(dd,J=5.7,2.4Hz,1H),6.75(s,1H),4.92(br,1H),4.53(s,2H),4.03(t,J=4.8Hz,2H),3.73-3.70(m,2H),3.39(s,3H),3.22(t,J=7.5Hz,2H),2.84(t,J=7.8Hz,2H),2.30(s,3H),2.04-1.99(m,2H)。
实施例1.356
合成2-({2-[4-({[1-(3-氟苯基)-1H-1,2,4-三唑-3-基]甲基}(甲基)氨基)-5H,6H,7H-环戊并[d]嘧啶-2-基]吡啶-4-基}氧基)乙-1-醇(化合物351)
流程125
步骤1
将3-氟苯胺(10.00g,89.994mmol,1.00当量)于水(50.00mL)及浓盐酸(30.00mL)的混合物中的溶液冷却至0℃。在将温度维持于0℃与5℃之间的情况下,添加亚硝酸钠(7.45g,107.992mmol,1.20当量)于水(10.00mL)中的溶液。在0℃下继续搅拌5min。将此溶液逐滴添加至乙酸钠盐(55.37g,674.952mmol,7.50当量)及2-异氰基乙酸乙酯(11.20g,99.013mmol,1.10当量)于水(100.00mL)及甲醇(10.00mL)的混合物中的混合物中。将反应混合物在0℃下搅拌30min且升温至室温。继续搅拌过夜。用2×300mL乙酸乙酯萃取所得溶液。用2×300盐水洗涤所得混合物。使混合物经无水硫酸钠干燥且真空浓缩。将残余物施加至含乙酸乙酯/石油醚(EA)的硅胶柱上。由此产生5.5g(25.98%)呈淡黄色固体的1-(3-氟苯基)-1H-1,2,4-三唑-3-甲酸乙酯。LCMS(ES)[M+1]+m/z:236。
步骤2
向250mL 3颈圆底烧瓶中放入1-(3-氟苯基)-1H-1,2,4-三唑-3-甲酸乙酯(5.50g,23.383mmol,1.00当量)、THF(60.00mL)。之后在0℃下添加LiAlH4(1.33g,35.042mmol,1.50当量)。在0℃下搅拌所得溶液1h。随后通过添加1.5mL水、1.5mL 15%NaOH、4.5mL水淬灭反应物。使混合物经无水硫酸钠干燥。滤出固体。真空浓缩所得混合物。将残余物施加至含乙酸乙酯/石油醚(EA)的硅胶柱上。由此产生2.2g(48.70%)(1-(3-氟苯基)-1H-1,2,4-三唑-3-基)甲醇。
步骤3
向100mL 3颈圆底烧瓶中放入(1-(3-氟苯基)-1H-1,2,4-三唑-3-基)甲醇(2.00g,10.353mmol,1.00当量)、DCM(30.00mL)、PCl5(4.31g,20.697mmol,2.00当量)。在室温下搅拌所得溶液1h。随后通过添加30mLNH4Cl(水溶液)淬灭反应物。用2×40mL二氯甲烷萃取所得溶液。用2×40ml盐水洗涤所得混合物。使混合物经无水硫酸钠干燥且真空浓缩。将残余物施加至含乙酸乙酯/石油醚(1:1)的硅胶柱上。由此产生2g(91.29%)呈淡黄色固体的3-(氯甲基)-1-(3-氟苯基)-1H-1,2,4-三唑。LCMS(ES)[M+1]+m/z:212。
步骤4
向40mL圆底烧瓶中放入3-(氯甲基)-1-(3-氟苯基)-1H-1,2,4-三唑(2.00g,9.451mmol,1.00当量)、MeOH(20.00mL)、甲胺(2M于甲醇中,20.00mL)。于油浴中在50℃下搅拌所得溶液4h。真空浓缩所得混合物。将残余物施加至含二氯甲烷/甲醇(10:1)的硅胶柱上。由此产生1.5g(76.96%)呈灰白色固体的1-(1-(3-氟苯基)-1H-1,2,4-三唑-3-基)-N-甲基甲胺。LCMS(ES)[M+1]+m/z:207。
步骤5
向100mL 3颈圆底烧瓶中放入2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(1.38g,7.300mmol,1.00当量)、MeOH(30.00mL)、DIEA(2.35g,18.184mmol,2.50当量)。之后在0℃下添加1-(1-(3-氟苯基)-1H-1,2,4-三唑-3-基)-N-甲基甲胺(1.50g,7.274mmol,1.00当量)。在室温下搅拌所得溶液16h。真空浓缩所得混合物。将残余物施加至含二氯甲烷/甲醇(10:1)的硅胶柱上。由此产生1.8g(68.97%)呈淡黄色油状物的2-氯-N-((1-(3-氟苯基)-1H-1,2,4-三唑-3-基)甲基)-N-甲基-6,7-二氢-5H-环戊并[d]嘧啶-4-胺。LCMS(ES)[M+1]+m/z:359。
步骤6
向用惰性氮气氛围吹扫及维持的40mL密封管中放入2-氯-N-((1-(3-氟苯基)-1H-1,2,4-三唑-3-基)甲基)-N-甲基-6,7-二氢-5H-环戊并[d]嘧啶-4-胺(200.00mg,0.557mmol,1.00当量)、甲苯(6.00mL)、4-氟-2-(三丁基锡烷基)吡啶(322.85mg,0.836mmol,1.50当量)、Pd(PPh3)4(64.41mg,0.056mmol,0.10当量)。于油浴中在100℃下搅拌所得溶液16h。真空浓缩所得混合物。将残余物施加至含二氯甲烷/甲醇(10:1)的硅胶柱上。将此反应重复10次且获得650mg(69.44%)呈淡黄色油状物的N-((1-(3-氟苯基)-1H-1,2,4-三唑-3-基)甲基)-2-(4-氟吡啶-2-基)-N-甲基-6,7-二氢-5H-环戊并[d]嘧啶-4-胺。LCMS(ES)[M+1]+m/z:420。
步骤7
向50mL 3颈圆底烧瓶中放入乙二醇(887.87mg,14.305mmol,20.00当量)、DMF(3mL)。之后在0℃下添加NaH(85.82mg,3.576mmol,5.00当量)。在0℃下向其添加N-((1-(3-氟苯基)-1H-1,2,4-三唑-3-基)甲基)-2-(4-氟吡啶-2-基)-N-甲基-6,7-二氢-5H-环戊并[d]嘧啶-4-胺(300.00mg,0.715mmol,1.00当量)。在室温下搅拌所得溶液2h。用2×20mL二氯甲烷/甲醇(10:1)萃取所得溶液。用2×20ml盐水洗涤所得混合物。使混合物经无水硫酸钠干燥且真空浓缩。通过使用以下条件的制备型HPLC纯化粗产物:SunFire Prep C18 OBD柱,50*250mm 5um10nm;移动相,相A:H2O(0.05%NH3.H2O);相B:CH3CN(15min内自10%CH3CN达至50%CH3CN)。由此产生216.1mg(65.47%)呈白色固体的2-({2-[4-({[1-(3-氟苯基)-1H-1,2,4-三唑-3-基]甲基}(甲基)氨基)-5H,6H,7H-环戊并[d]嘧啶-2-基]吡啶-4-基}氧基)乙-1-醇。LCMS(ES)[M+1]+m/z:462。1H NMR(300MHz,DMSO-d6,ppm):δ9.27(s,1H),8.45(d,J=5.6Hz,1H),7.86(d,J=2.6Hz,1H),7.80-7.66(m,2H),7.63-7.55(m,1H),7.32-7.19(m,1H),7.02(dd,J=5.7,2.6Hz,1H),5.00(s,2H),4.93(t,J=5.5Hz,1H),4.13(t,J=4.9Hz,2H),3.77-3.72(m,J=5.0Hz,2H),3.38(s,3H),3.25(t,J=7.3Hz,2H),2.83(t,J=7.9Hz,2H),2.06-1.95(m,2H)。
实施例1.357
合成N-叔丁基-2-[甲基({2-[4-(1-甲基-1H-吡唑-4-基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物352)
用2-氯-4-(1-甲基-1H-吡唑-4-基)吡啶替换2-氯-4-(氧杂环丁-3-基氧基)吡啶,与化合物245类似地合成化合物352。LCMS(ES)[M+1]+m/z:420。1H NMR(300MHz,DMSO-d6)δ8.57(dd,J=5.1,0.8Hz,1H),8.47(s,1H),8.41(dd,J=1.8,0.8Hz,1H),8.14(d,J=0.8Hz,1H),7.65(s,1H),7.60(dd,J=5.1,1.8Hz,1H),4.19(s,2H),3.91(s,3H),3.30(s,3H),3.17(t,J=7.4Hz,2H),2.84(t,J=7.8Hz,2H),2.05-1.95(m,2H),1.18(s,9H)。
实施例1.358
合成N-(1-环丙基-1H-吡唑-4-基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物353)
通过用1-环丙基吡唑-4-胺替换6-甲氧基吡啶-3-胺,与化合物187类似地合成化合物353。LCMS(ES)[M+1]+m/z:450。1H NMR(300MHz,DMSO-d6)δ10.28(s,1H),8.46(d,J=5.6Hz,1H),7.87(s,1H),7.77(d,J=2.6Hz,1H),7.40(s,1H),7.02(dd,J=5.6,2.6Hz,1H),4.94(s,1H),4.35(s,2H),4.07-4.04(m,2H),3.71-3.66(m,2H),3.65-3.62(m,1H),3.30(s,3H),3.22-3.16(m,2H),2.85-2.80(m,2H),2.02-1.98(m,2H),0.98-0.95(m,4H)。
实施例1.359
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-(吡咯烷-1-基)乙-1-酮(化合物354)
通过用吡咯烷替换6-甲氧基吡啶-3-胺,与化合物187类似地合成化合物354。LCMS(ES)[M+1]+m/z:398。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),8.15(s,1H),7.72(d,J=2.5Hz,1H),7.03(dd,J=5.8,2.5Hz,1H),4.93(br,1H),4.39(s,2H),4.13(t,J=4.8Hz,2H),3.75(t,J=4.9Hz,2H),3.54(t,J=6.8Hz,2H),3.34-3.29(m,5H),3.21-3.14(t,J=7.4Hz,2H),2.92-2.81(m,2H),1.96-1.85(m,4H),1.79 1.68(m,2H)。
实施例1.360
合成1-(4,4-二氟哌啶-1-基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙-1-酮(化合物355)
通过用4,4-二氟哌啶替换6-甲氧基吡啶-3-胺,与化合物187类似地合成化合物355。LCMS(ES)[M+1]+m/z:448。1H NMR(300MHz,DMSO-d6)δ8.42(d,J=5.6Hz,1H),8.16(s,0.6HCOOH),7.77(d,J=2.6Hz,1H),7.03(dd,J=5.7,2.6Hz,1H),4.57(s,2H),4.12(t,J=5.0Hz,2H),3.75(t,J=4.9Hz,2H),3.69-3.52(m,4H),3.28(s,3H),3.16(t,J=7.3Hz,2H),2.82(t,J=7.9Hz,2H),2.23-2.14(m,2H),1.99-2.83(m,4H)。
实施例1.361
合成2-({2-[4-(2-乙酰胺基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-氟苯基)乙酰胺(化合物356)
通过用3-氟苯胺替换6-甲氧基吡啶-3-胺且用N-(2-羟乙基)乙酰胺替换乙烷-1,2-二醇,与化合物187类似地合成化合物356。LCMS(ES)[M+1]+m/z:479。1H NMR(300MHz,DMSO-d6)δ10.45(s,1H),8.45(d,J=5.6Hz,1H),8.07(t,J=5.3Hz,1H),7.78(d,J=2.5Hz,1H),7.64-7.53(m,1H),7.40-7.27(m,2H),7.02(dd,J=5.7,2.6Hz,1H),6.86(ddt,J=8.9,7.2,2.6Hz,1H),4.45(s,2H),4.05(t,J=5.5Hz,2H),3.39(d,J=5.5Hz,2H),3.36(s,3H),3.21(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.05-1.96(m,2H),1.83(s,3H)。
实施例1.362
合成1-(氮杂环庚-1-基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙-1-酮(化合物357)
通过用氮杂环庚烷替换6-甲氧基吡啶-3-胺,与化合物187类似地合成化合物357。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6)δ8.44(d,J=5.6Hz,1H),8.14(s,1H),7.72(d,J=2.6Hz,1H),7.02(dd,J=5.6,2.6Hz,1H),4.92(s,1H),4.54(s,2H),4.12(t,J=4.9Hz,2H),3.80-3.72(m,2H),3.50(t,J=6.0Hz,2H),3.41(t,J=5.9Hz,2H),3.26(s,3H),3.15(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.03-1.98(m,2H),1.84-1.72(m,2H),1.61-1.40(m,6H)。
实施例1.363
合成1-(氮杂环庚-1-基)-2-[甲基({2-[4-(氧杂环丁-3-基氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙-1-酮(化合物358)
用氮杂环庚烷替换6-甲氧基吡啶-3-胺且用氧杂环丁-3-醇替换乙-1,2-二醇,与化合物187类似地合成化合物358。LCMS(ES)[M+1]+m/z:438。1HNMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.61(d,J=2.6Hz,1H),6.87(dd,J=5.6,2.6Hz,1H),5.50-5.43(m,1H),5.02-4.91(m,2H),4.63-4.52(m,4H),3.50(t,J=6.0Hz,2H),3.42(t,J=5.9Hz,2H),3.26(s,3H),3.15(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.88-1.79(m,2H),1.62-1.43(m,6H)。
实施例1.364
合成1-(4-氟哌啶-1-基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙-1-酮(化合物359)
通过用4-氟哌啶替换6-甲氧基吡啶-3-胺,与化合物187类似地合成化合物359。LCMS(ES)[M+1]+m/z:430。1H NMR(300MHz,DMSO-d6)δ8.45(d,J=5.4Hz,1H),7.75(s,1H),7.02(dd,J=5.4,2.5Hz,1H),5.00-4.84(m,2H),4.63-4.45(m,2H),4.13-4.10(m,2H),3.76-3.74(d,J=6Hz,2H),3.70-3.40(m,4H),3.27(s,3H),3.17-3.12(m,2H),2.83-2.78(m,2H),2.20-1.50(m,6H)。
实施例1.365
合成N-叔丁基-2-[乙基({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物360)
与化合物126类似地合成化合物360。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.86(d,J=2.5Hz,1H),7.70(s,1H),7.04(dd,J=5.7,2.5Hz,1H),4.92(s,1H),4.19-4.06(m,4H),3.76(t,J=4.9Hz,2H),3.65(q,J=7.0Hz,2H),3.07(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.05-1.95(m,2H),1.23-1.16(m,12H)。
实施例1.366
合成N-叔丁基-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5,5-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物361)
通过用N-叔丁基-2-(甲基氨基)乙酰胺盐酸盐替换2-(甲基氨基)-N-(6-甲基吡啶-3-基)乙酰胺,与化合物331类似地合成化合物361。LCMS(ES)[M+1]+m/z:428。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.86(d,J=2.6Hz,1H),7.67(s,1H),7.05(dd,J=5.7,2.6Hz,1H),4.91(s,1H),4.15(t,J=5.0Hz,2H),4.03(s,2H),3.77(s,2H),3.18(s,3H),2.86(t,J=7.2Hz,2H),1.87(t,J=7.3Hz,2H),1.43(s,6H),1.21(s,9H)。
实施例1.367
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5,5-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-(哌啶-1-基)乙-1-酮(化合物362)
通过用2-(甲基氨基)-1-(哌啶-1-基)乙酮盐酸盐替换2-(甲基氨基)-N-(6-甲基吡啶-3-基)乙酰胺,与化合物331类似地合成化合物362。LCMS(ES)[M+1]+m/z:440。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),7.72(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.5Hz,1H),4.91(t,J=5.4Hz,1H),4.38(s,2H),4.13(t,J=4.9Hz,2H),3.76(q,J=5.1Hz,2H),3.44(d,J=17.6Hz,4H),3.21(s,3H),2.85(t,J=7.3Hz,2H),1.87(t,J=7.2Hz,2H),1.61(s,4H),1.44(s,8H)。
实施例1.368
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5,5-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(6-甲氧基吡啶-3-基)乙酰胺(化合物363)
通过用N-(6-甲氧基吡啶-3-基)-2-(甲基氨基)乙酰胺盐酸盐替换2-(甲基氨基)-N-(6-甲基吡啶-3-基)乙酰胺,与化合物331类似地合成化合物363。LCMS(ES)[M+1]+m/z:479。1H NMR(300MHz,DMSO-d6)δ10.44(s,1H),8.42(d,J=5.6Hz,1H),8.33(d,J=2.6Hz,1H),7.87(dd,J=9.0,2.6Hz,1H),7.79(d,J=2.5Hz,1H),7.02(dd,J=5.7,2.5Hz,1H),6.77(d,J=8.8Hz,1H),4.91(s,1H),4.29(s,2H),4.02(t,J=4.8Hz,2H),3.80(d,J=1.5Hz,3H),3.68(t,J=4.7Hz,2H),3.30(s,3H),2.88(t,J=7.2Hz,2H),1.89(t,J=7.2Hz,2H),1.46(s,6H)。
实施例1.369
合成1-{3-氮双环[3.1.1]庚-3-基}-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙-1-酮(化合物364)
通过用3-氮双环[3.1.1]庚烷盐酸盐替换6-甲氧基吡啶-3-胺,与化合物187类似地合成化合物364。LCMS(ES)[M+1]+m/z:424。1H NMR(300MHz,DMSO-d6)δ8.45(d,J=5.7Hz,1H),8.17(s,HCOOH),7.74(d,J=2.7Hz,1H),7.04(dd,J=6.0,3.0Hz,1H),4.50(s,2H),4.14(t,J=5.1Hz,2H),3.84(d,J=2.4Hz,2H),3.76(t,J=5.1Hz,2H),3.53(d,J=2.4Hz,2H),3.31(s,3H),3.17(t,J=7.2Hz,2H),2.83(t,J=8.1Hz,2H),2.48-2.43(m,2H),2.19-2.10(m,2H),2.03-1.93(m,2H),1.32(dt,J=6.8,4.1Hz,2H)。
实施例1.370
合成N-叔丁基-2-[(2-{呋喃并[2,3-c]吡啶-5-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物365)
用5-氯呋喃并[2,3-c]吡啶替换2-氯-4-(氧杂环丁-3-基氧基)吡啶,与化合物245类似地合成化合物365。LCMS(ES)[M+1]+m/z:380。1H NMR(300MHz,DMSO-d6)δ9.00(s,1H),8.73(s,1H),8.32-8.24(m,1H),8.14(s,0.5HCOOH),7.74(s,1H),7.10(d,J=2.4Hz,1H),4.16(s,2H),3.30(s,3H),3.15(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.05-1.95(m,2H),1.24(s,9H)。
实施例1.371
合成N-叔丁基-2-[(2-{4-[(2R)-2-羟基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物366)
通过用(2R)-2-(氧杂环己-2-基氧基)丙-1-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与化合物174类似地合成化合物366。分析型手性HPLC条件:柱,Lux-cellulose-2,100*4.6mm,3um;移动相A,乙醇;移动相B,CH3CN;流动速率:1mL/min;梯度:20%B,6min;254nm。保留时间:2.123min。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.47(dd,J=5.7,1.3Hz,1H),7.99-7.78(m,1H),7.69(s,1H),7.05-7.02(m,1H),4.94(d,J=3.9Hz,1H),4.13(s,2H),4.04-3.93(m,3H),3.26(s,3H),3.13(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.03-1.93(m,2H),1.25(s,9H),1.23(d,J=7.5Hz,3H)。
实施例1.372
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(2-甲基丁-2-基)乙酰胺(化合物367)
通过用2-甲基丁-2-胺替换叔丁胺,与化合物44类似地合成化合物367。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),7.84(d,J=2.5Hz,1H),7.49(s,1H),7.04(dd,J=5.6,2.6Hz,1H),4.91(t,J=5.4Hz,1H),4.20-4.10(m,4H),3.76(q,J=5.1Hz,2H),3.25(s,3H),3.14(t,J=7.2Hz,2H),2.81(t,J=7.8Hz,2H),2.15-1.91(m,2H),1.61(q,J=7.5Hz,2H),1.18(s,6H),0.71(t,J=7.4Hz,3H)。
实施例1.373
合成1-(2,2-二甲基吡咯烷-1-基)-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙-1-酮(化合物368)
通过用2,2-二甲基吡咯烷替换叔丁胺,与化合物44类似地合成化合物368。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.5Hz,1H),7.77(d,J=2.6Hz,1H),7.07-6.99(m,1H),4.91(s,1H),4.30(s,2H),4.13(t,J=4.9Hz,2H),3.78-3.74(m,2H),3.60(t,J=6.8Hz,2H),3.29(s,3H),3.12(t,J=7.1Hz,2H),2.80(t,J=7.8Hz,2H),2.04-1.75(m,4H),1.74-1.69(m,2H),1.31(s,6H)。
实施例1.374
合成N-叔丁基-2-({2-[4-(2-乙酰胺基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物369)
通过用N-(2-羟乙基)乙酰胺替换二甲氨基乙醇,与化合物348类似地合成化合物369。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),8.16(s,1HCOOH),8.11(t,J=5.5Hz,1H),7.85(d,J=2.5Hz,1H),7.68(s,1H),7.05(dd,J=5.6,2.6Hz,1H),4.17-4.13(m,4H),3.45(q,J=5.6Hz,2H),3.26(s,3H),3.13(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.03-1.96(p,J=7.6Hz,2H),1.84(s,3H),1.24(s,9H)。
实施例1.375
合成N-叔丁基-2-({2-[4-(2-乙酰胺基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物369)
通过用N-(2-羟乙基)乙酰胺替换二甲氨基乙醇,与化合物348类似地合成化合物369。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),8.16(s,1HCOOH),8.11(t,J=5.5Hz,1H),7.85(d,J=2.5Hz,1H),7.68(s,1H),7.05(dd,J=5.6,2.6Hz,1H),4.17-4.13(m,4H),3.45(q,J=5.6Hz,2H),3.26(s,3H),3.13(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.03-1.96(p,J=7.6Hz,2H),1.84(s,3H),1.24(s,9H)。
实施例1.376
合成N-叔丁基-2-[(2-{4-[(2S)-2-羟基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物370)
通过用(2S)-2-(氧杂环己-2-基氧基)丙-1-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与化合物174类似地合成化合物370。分析型手性HPLC条件:柱,Lux-cellulose-2,100*4.6mm,3um;移动相A,乙醇;移动相B,CH3CN;流动速率:1mL/min;梯度:20%B,6min;254nm。保留时间:3.022min。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.7Hz,1H),7.84(d,J=2.4Hz,1H),7.68(s,1H),7.04(dd,J=5.7,2.4Hz,1H),4.93(d,J=3.9Hz,1H),4.13(s,2H),4.04-3.93(m,3H),3.26(s,3H),3.14(t,J=7.5Hz,2H),2.81(t,J=7.8Hz,2H),2.04-1.93(m,2H),1.24(s,9H),8.47(d,J=5.7Hz,3H)。
实施例1.377
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-[(3S)-氧杂环戊-3-基]乙酰胺(化合物371)
通过用(S)-四氢呋喃-3-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物371。分析型手性HPLC条件:柱,CHIRALCEL OX-3,50*4.6mm,3um;移动相A,正己烷;移动相B,乙醇;流动速率:1mL/min;梯度:50%B,20min;270nm。保留时间:7.945min。LCMS(ES)[M+1]+m/z:384。1H NMR(300MHz,DMSO-d6)δ8.49(d,J=5.7Hz,1H),8.38(d,J=6.9Hz,1H),7.81(d,J=2.7Hz,1H),7.06(dd,J=5.4,2.4Hz,1H),4.31-4.25(m,1H),4.20(d,J=2.4Hz,2H),3.90(s,3H),3.78-3.60(m,3H),3.46(dd,J=9.0,4.2Hz,1H),3.28(s,3H),3.18(t,J=7.2Hz,2H),2.85(t,J=7.8Hz,2H),2.11-1.92(m,3H),1.77-1.67(m,1H)。
实施例1.378
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-[(3R)-氧杂环戊-3-基]乙酰胺(化合物372)
通过用(R)-四氢呋喃-3-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物372。分析型手性HPLC条件:柱,CHIRALCEL OX-3,50*4.6mm,3um;移动相A,正己烷;移动相B,乙醇;流动速率:1mL/min;梯度:50%B,20min;270nm。保留时间:10.028min。LCMS(ES)[M+1]+m/z:384。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.7Hz,1H),8.38(d,J=6.9Hz,1H),7.80(d,J=2.7Hz,1H),7.04(dd,J=5.4,2.7Hz,1H),4.31-4.25(m,1H),4.20(d,J=2.7Hz,2H),3.90(s,3H),3.78-3.60(m,3H),3.46(dd,J=9.0,4.2Hz,1H),3.28(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.10-1.94(m,3H),1.77-1.67(m,1H)。
实施例1.379
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-(氧杂环丁-3-基)乙酰胺(化合物373)
通过用氧杂环丁-3-胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物373。LCMS(ES)[M+1]+m/z:370。1H NMR(300MHz,DMSO-d6)δ8.96(d,J=6.9Hz,1H),8.48(d,J=5.4Hz,1H),7.79(d,J=2.7Hz,1H),7.03(dd,J=5.7,2.7Hz,1H),4.87-4.78(m,1H),4.67(t,J=6.9Hz,2H),4.43(t,J=6.3Hz,2H),4.20(s,2H),3.89(s,3H),3.29(s,3H),3.16(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.08-1.94(m,2H)。
实施例1.380
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(氧杂环丁-3-基)乙酰胺(化合物374)
通过用氧杂环丁-3-胺替换叔丁胺,与化合物44类似地合成化合物374。LCMS(ES)[M+1]+m/z:400。1H NMR(300MHz,DMSO-d6)δ8.94(d,J=6.8Hz,1H),8.48(d,J=5.7Hz,1H),7.79(d,J=2.5Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),4.93(t,J=5.5Hz,1H),4.90-4.74(m,1H),4.73-4.63(m,2H),4.44(t,J=6.3Hz,2H),4.20(s,2H),4.14(t,J=4.9Hz,2H),3.80-3.72(m,2H),3.29(s,3H),3.16(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.02-1.97(m,2H)。
实施例1.381
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-{5-甲氧基-1H,2H,3H-吡咯并[2,3-c]吡啶-1-基}乙-1-酮(化合物375)
通过用5-甲氧基-2,3-二氢-1H-吡咯并[2,3-c]吡啶替换叔丁胺,与化合物44类似地合成化合物375。LCMS(ES)[M+1]+m/z:477。1H NMR(300MHz,DMSO-d6)δ8.63(s,1H),8.43-8.41(m,1H),8.13(s,1HCOOH),7.69(s,1H),7.02-6.95(m,1H),6.77(m,1H),4.89-4.87(m,1H),4.59(s,2H),4.32-4.26(m,2H),4.01-3.99(m,2H),3.78(s,3H),3.65-3.63(m,2H),3.38(s,3H),3.26-3.20(m,4H),2.86-2.73(m,2H),2.07-1.95(m,2H)。
实施例1.382
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(1-甲基环丁基)乙酰胺(化合物376)
通过用1-甲基环丁-1-胺替换叔丁胺,与化合物44类似地合成化合物376。LCMS(ES)[M+1]+m/z:412。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),8.15(s,1H),7.85(d,J=2.6Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),4.92(t,J=5.4Hz,1H),4.19-4.10(m,4H),3.76(q,J=5.1Hz,2H),3.27(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.28-2.18(m,2H),2.04-1.95(m,2H),1.89-1.78(m,2H),1.78-1.65(m,2H),1.33(s,3H)。
实施例1.383
合成2-[(2-{4-[(2R)-2-羟基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(1-甲基环丁基)乙酰胺(化合物377)
通过用(2R)-2-(氧杂环己-2-基氧基)丙-1-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇且用1-甲基环丁-1-胺替换叔丁胺,与化合物174类似地合成化合物377。分析型手性HPLC条件:柱,Lux-cellulose-2,100*4.6mm,3um;移动相A,乙醇;移动相B,CH3CN;流动速率:1mL/min;梯度:10%B,8min;254nm。保留时间:2.712min。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),8.14(s,1H),7.84(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),4.93(d,J=4.1Hz,1H),4.13(s,2H),4.03-3.92(m,3H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.9Hz,2H),2.27-2.21(m,2H),2.05-1.94(m,2H),1.91-1.76(m,2H),1.76-1.65(m,2H),1.34(s,3H),1.18(d,J=5.8Hz,3H)。
实施例1.384
合成2-[(2-{4-[(2S)-2-羟基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(1-甲基环丁基)乙酰胺(化合物378)
通过用(2S)-2-(氧杂环己-2-基氧基)丙-1-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇且用1-甲基环丁-1-胺替换叔丁胺,与化合物174类似地合成化合物378。分析型手性HPLC条件:柱,Lux-cellulose-2,100*4.6mm,3um;移动相A,乙醇;移动相B,CH3CN;流动速率:1mL/min;梯度:10%B,8min;254nm。保留时间:4.827min。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),8.14(s,1H),7.84(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),4.93(d,J=4.1Hz,1H),4.13(s,2H),4.03-3.92(m,3H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.9Hz,2H),2.27-2.18(m,2H),2.05-1.94(m,2H),1.91-1.76(m,2H),1.76-1.65(m,2H),1.34(s,3H),1.18(d,J=5.8Hz,3H)。
实施例1.385
合成N-[(4-苯甲基-1,3-噁唑-2-基)甲基]-2-(4-甲氧基吡啶-2-基)-N-甲基-5H,6H,7H-环戊并[d]嘧啶-4-胺(化合物379)
流程126
步骤1
将(1,3-二氧代-1,3-二氢-2H-异吲哚-2-基)乙酸(2g;9.75mmol;1当量)溶解于N,N-二甲基甲酰胺(40mL)中且于冰浴中冷却。随后添加2-氨基-3-苯基-1-丙醇(1.55g;10.24mmol;1.05当量)、3-氧化六氟磷酸1-[双(二甲基氨基)亚甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓(HATU)(5.56g;14.62mmol;1.5当量)及休尼格氏碱(5.1mL;29.24mmol;3当量)。经3.5h将反应物搅拌至25℃。添加乙酸乙酯(100ml)、水及碳酸氢钠溶液(50ml),分离各相,且萃取水相一次(50ml)。将合并的有机相用水、饱和氯化钠溶液洗涤且经硫酸钠干燥。蒸发后,通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈白色固体的2-(1,3-二氧代-2,3-二氢-1H-异吲哚-2-基)-N-(1-羟基-3-苯基丙-2-基)乙酰胺(1.97g,60%)。LCMS(ES+):[M+H]+=339.1。
步骤2
将2-(1,3-二氧代-2,3-二氢-1H-异吲哚-2-基)-N-(1-羟基-3-苯基丙-2-基)乙酰胺(1.97g;5.82mmol;1当量)溶解于二氯甲烷(150ml)中且于冰浴中冷却。添加乙酸1,1-双(乙酰氧基-3-氧代-3H-15,2-苯并碘氧杂环戊-1-基酯(戴斯-马丁高碘烷)(2.83g;6.46mmol;1.11当量)且经2h将反应物搅拌至25℃。添加碳酸氢钠溶液及硫代硫酸钠溶液且搅拌混合物10m。分离各相,用二氯甲烷(2×50ml)萃取水相,将合并的有机相用饱和氯化钠溶液洗涤且经硫酸钠干燥。蒸发溶剂,得到呈固体的2-(1,3-二氧代-2,3-二氢-1H-异吲哚-2-基)-N-(1-氧代-3-苯基丙-2-基)乙酰胺,其按原样使用。LCMS(ES+):[M+H]+=337.1。
步骤3
将1,1,1,2,2,2-六氯乙烷(5.16g;21.8mmol;2.7当量)及三苯基膦(5.76g;22mmol;2.7当量)溶解于四氢呋喃(30ml)中且搅拌10m。添加悬浮于THF(8ml)中的2-(1,3-二氧代-2,3-二氢-1H-异吲哚-2-基)-N-(1-氧代-3-苯基丙-2-基)乙酰胺(3.62g;8.07mmol;1当量)且搅拌混合物10m。随后经15m逐滴添加含吡啶(4.18mL;51.7mmol;6.4当量)的THF(1ml)。在80℃下于加热块中搅拌反应物18h。蒸发后,通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈黄色晶体的2-[(4-苯甲基-1,3-噁唑-2-基)甲基]-2,3-二氢-1H-异吲哚-1,3-二酮(1.19g,46%)。LCMS(ES+):[M+H]+=319.0。
步骤4
将2-[(4-苯甲基-1,3-噁唑-2-基)甲基]-2,3-二氢-1H-异吲哚-1,3-二酮(1.19g;3.74mmol;1当量)悬浮于乙醇(37ml)中。添加肼(1.7mL;18.7mmol;5.00当量),且在90℃下于沙浴中加热反应物2h。使反应物冷却,用乙醇(20ml)稀释,过滤且用更多乙醇(20ml)冲洗。蒸发后,通过反相色谱(乙腈/水梯度)纯化残余物,得到呈油状物的(4-苯甲基-1,3-噁唑-2-基)甲胺(0.31g,44%)。LCMS(ES+):[M+H]+=189.1。
步骤5
将2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶(140mg;0.74mmol;1当量)添加至(4-苯甲基-1,3-噁唑-2-基)甲胺(153mg;0.81mmol;1.1当量)的乙腈溶液(5ml)中,添加休尼格氏碱(0.39mL;2.22mmol;3当量)且在60℃加热块中搅拌反应物66h。蒸发溶剂,且通过硅胶色谱(乙酸乙酯/二氯甲烷梯度)纯化残余物,得到呈固体的N-[(4-苯甲基-1,3-噁唑-2-基)甲基]-2-氯-5H,6H,7H-环戊并[d]嘧啶-4-胺(107mg,42%)。LCMS(ES+):[M+H]+=341.0。
步骤6
将N-[(4-苯甲基-1,3-噁唑-2-基)甲基]-2-氯-5H,6H,7H-环戊并[d]嘧啶-4-胺(107mg;0.31mmol;1当量)溶解于N,N-二甲基甲酰胺(3ml)中且于冰浴中冷却。添加碘甲烷(195μL;3.14mmol;10当量),之后添加氢化钠(38mg;0.94mmol;3当量)且经2.5h搅拌至25℃。添加水(1ml)、乙酸乙酯(50ml)及碳酸氢钠溶液(10ml),分离各相且用乙酸乙酯(1×10ml)萃取水相。将合并的有机相用水、饱和氯化钠溶液洗涤且经硫酸钠干燥。蒸发溶剂后,通过硅胶色谱(乙酸乙酯/己烷梯度)纯化残余物,得到呈薄膜的N-[(4-苯甲基-1,3-噁唑-2-基)甲基]-2-氯-N-甲基-5H,6H,7H-环戊并[d]嘧啶-4-胺(92mg,83%)。LCMS(ES+):[M+H]+=355.0。
步骤7
将N-[(4-苯甲基-1,3-噁唑-2-基)甲基]-2-氯-N-甲基-5H,6H,7H-环戊并[d]嘧啶-4-胺(63mg;0.17mmol;1当量)溶解于甲苯(2ml)中。添加含4-甲氧基-2-(三丁基锡烷基)吡啶(156mg;0.35mmol;2当量)的1ml甲苯,且用Ar气体吹扫溶液。添加[1,1'-双(二苯基膦基)二茂铁]二氯化钯(II)与二氯甲烷(14mg;17.5μmol;0.1当量)的错合物,且密封反应容器并在110℃下于加热块中搅拌17h。蒸发溶剂且通过反相色谱(Waters XSelect CSH C18柱,0-90%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈粉色固体的N-[(4-苯甲基-1,3-噁唑-2-基)甲基]-2-(4-甲氧基吡啶-2-基)-N-甲基-5H,6H,7H-环戊并[d]嘧啶-4-胺(22mg,40%)。LCMS(ES+):[M+H]+=428.2。1H NMR(400MHz,dmso)δ8.45(d,J=5.5Hz,1H),7.78(s,2H),7.73(s,1H),7.32-7.12(m,5H),7.01(d,J=5.5Hz,1H),4.94(s,2H),3.86(s,3H),3.77(s,2H),3.20-3.15(m,2H),2.86-2.75(m,2H),2.04-1.89(m,2H)。
实施例1.386
合成2-(4-甲氧基吡啶-2-基)-N-甲基-N-[(4-苯基-1,3-噁唑-2-基)甲基]-5H,6H,7H-环戊并[d]嘧啶-4-胺(化合物380)
通过用2-氨基-2-苯乙醇替换2-氨基-3-苯基-1-丙醇,与化合物379类似地合成化合物380,得到呈褐色固体的2-(4-甲氧基吡啶-2-基)-N-甲基-N-[(4-苯基-1,3-噁唑-2-基)甲基]-5H,6H,7H-环戊并[d]嘧啶-4-胺。LCMS(ES+):[M+H]+=414.2。1H NMR(400MHz,dmso)δ8.53(s,1H),8.45(d,J=5.6Hz,1H),7.82(d,J=2.6Hz,1H),7.77-7.71(m,2H),7.44-7.37(m,2H),7.33-7.27(m,1H),7.00(dd,J=5.6,2.6Hz,1H),5.04(s,2H),3.84(s,3H),3.42(s,3H),3.26-3.22(m,2H),2.87-2.80(m,2H),2.06-1.96(m,2H)。
实施例1.387
合成N-叔丁基-2-[(2-{4-[(1-羟基环戊基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物381)
通过用[1-(氧杂环己-2-基氧基)环戊基]甲醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与174类似地合成化合物381。LCMS(ES)[M+1]+m/z:454。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.83(d,J=2.5Hz,1H),7.67(s,1H),7.05(dd,J=5.7,2.6Hz,1H),4.61(s,1H),4.14(s,2H),4.01(s,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.04-1.96(m,2H),1.86-1.51(m,8H),1.25(s,9H)。
实施例1.388
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-(哌啶-1-基)乙-1-酮(化合物382)
通过用哌啶替换叔丁胺,与174类似地合成化合物382。LCMS(ES)[M+1]+m/z:440。1HNMR(300MHz,DMSO-d6)δ8.45(d,J=5.6Hz,1H),7.73(d,J=2.5Hz,1H),7.03(dd,J=5.7,2.6Hz,1H),4.72(s,1H),4.51(s,2H),3.85(s,2H),3.45(dt,J=11.2,5.1Hz,4H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.06-1.92(m,2H),1.61(s,4H),1.47-1.39(m,2H),1.23(s,6H)。
实施例1.389
合成N-{双环[1.1.1]戊-1-基}-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物383)
通过用双环[1.1.1]戊-1-胺替换叔丁胺,与174类似地合成化合物383。LCMS(ES)[M+1]+m/z:438。1H NMR(300MHz,DMSO-d6)δ8.74(s,1H),8.47(d,J=5.6Hz,1H),7.79(d,J=2.6Hz,1H),7.05(dd,J=5.7,2.6Hz,1H),4.70(s,1H),4.12(s,2H),3.87(s,2H),3.27(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.7Hz,2H),2.37(s,1H),2.03-1.91(m,7H),1.24(s,6H)。
实施例1.390
合成N-叔丁基-2-{[2-(4-{[(2R)-1-羟基丙-2-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物384)
通过用(2R)-1-((四氢-2H-吡喃-2-基)氧基)丙-2-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与174类似地合成化合物384。分析型手性HPLC条件:柱,CHIRALCEL OX-3,50*4.6mm,3um;移动相A,正己烷;移动相B,乙醇;流动速率:1mL/min;梯度:50%B,10min;270nm。保留时间:4.949min。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.45(d,J=5.4Hz,1H),7.83(d,J=2.4Hz,1H),7.68(s,1H),7.05(dd,J=5.7,2.4Hz,1H),4.93(t,J=5.6Hz,1H),4.70-4.60(m,1H),4.18-4.06(m,2H),3.63-3.48(m,2H),3.26(s,3H),3.14(t,J=7.2Hz,2H),2.81(t,J=7.8Hz,2H),2.04-1.93(m,2H),1.27(s,3H),1.25(s,9H)。
实施例1.391
合成N-叔丁基-2-{[2-(4-{[(2S)-1-羟基丙-2-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物385)
通过用(2S)-1-((四氢-2H-吡喃-2-基)氧基)丙-2-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与174类似地合成化合物385。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.45(d,J=5.7Hz,1H),7.83(d,J=2.6Hz,1H),7.69(s,1H),7.06(dd,J=5.7,2.6Hz,1H),4.93(t,J=5.6Hz,1H),4.69-4.60(m,1H),4.22-4.02(m,2H),3.56(tq,J=11.5,6.2,5.8Hz,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.04-1.96(m,2H),1.24(d,J=6.1Hz,3H),1.21(s,9H)。
实施例1.392
合成N-叔丁基-2-[(2-{4-[(2S)-2-羟基-3-甲基丁氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物386)
通过用(2S)-3-甲基-2-(氧杂环己-2-基氧基)丁-1-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与174类似地合成化合物386。分析型手性HPLC条件:柱,Lux-cellulose-2,100*4.6mm,3um;移动相A,AcCN;移动相B,甲醇;流动速率:1mL/min;梯度:50%B,15min;254nm。保留时间:9.997min。LCMS(ES)[M+1]+m/z:442。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.83(d,J=2.5Hz,1H),7.66(s,1H),7.06(dd,J=5.7,2.6Hz,1H),4.86(d,J=5.3Hz,1H),4.13(s,2H),4.09(dd,J=10.1,4.5Hz,1H),4.00(dd,J=10.1,6.2Hz,1H),3.60(q,J=5.1Hz,1H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.04-1.96(p,J=7.7Hz,2H),1.92-1.76(m,1H),1.24(s,9H),0.93(dd,J=6.8,5.3Hz,6H)。
实施例1.393
合成N-叔丁基-2-[(2-{4-[(2R)-2-羟基-3-甲基丁氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物387)
通过用(2R)-3-甲基-2-(氧杂环己-2-基氧基)丁-1-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与174类似地合成化合物387。分析型手性HPLC条件:柱,Lux-cellulose-2,100*4.6mm,3um;移动相A,AcCN;移动相B,甲醇;流动速率:1mL/min;梯度:50%B,15min;254nm。保留时间:2.582min。LCMS(ES)[M+1]+m/z:442。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.84(d,J=2.5Hz,1H),7.67(s,1H),7.08(dd,J=5.7,2.6Hz,1H),4.87(d,J=5.3Hz,1H),4.14(s,2H),4.09(J=10.1,4.5Hz,1H),4.01(dd,J=10.1,6.2Hz,1H),3.60(t,J=5.3Hz,1H),3.27(s,3H),3.14(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.02-1.97(m,2H),1.83(dt,J=13.4,6.7Hz,1H),1.24(s,9H),0.93(dd,J=6.8,5.2Hz,6H)。
实施例1.394
合成N-叔丁基-2-[(2-{4-[(1-羟基环丁基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物388)
通过用[1-(氧杂环己-2-基氧基)环丁基]甲醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与174类似地合成化合物388。LCMS(ES)[M+1]+m/z:440。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.85(d,J=2.5Hz,1H),7.67(s,1H),7.07(dd,J=5.7,2.6Hz,1H),5.29(s,1H),4.13(s,2H),4.06(s,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.17(d,J=10.2Hz,2H),2.00(h,J=8.7,7.8Hz,4H),1.62(dq,J=19.4,9.7Hz,2H),1.24(s,9H)。
实施例1.395
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(丙-2-基)乙酰胺(化合物389)
流程127
步骤1
在室温下向1L圆底烧瓶中添加含4-氯甲吡啶脒盐酸盐(60.0g,312mmol,1.00当量)的MeOH(600mL)、2-氧代环戊烷-1-甲酸甲酯(66.6g,468mmol,1.5当量)及含NaOMe(42.18g,781mmol,2.5当量)的MeOH。在70℃下于氮气氛围下搅拌混合物40小时。通过过滤收集沉淀的固体且用MeOH(1×1500mL)洗涤。由此产生呈棕色固体的2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-醇(62g,80.12%)。LCMS(ES)[M+1]+m/z 248。
步骤2
向1L 3颈圆底烧瓶中添加含2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-醇(60g,242mmol,1.00当量)的DCM及TEA(123g,1211mmol,5.0当量)。在0℃下逐滴添加Tf2O(137g,484mmol,2.0当量)于DCM中的搅拌混合物。在0℃下再搅拌所得混合物2小时。通过在室温下添加NH4Cl(水溶液500mL)淬灭反应物。用DCM(3×600mL)萃取所得混合物,且将有机层分离且经无水Na2SO4干燥。过滤所得混合物且减压浓缩滤液。通过硅胶柱色谱,用PE/EA(3:1)洗脱来纯化残余物,得到呈灰白色固体的三氟甲烷磺酸2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基酯(63g,68.48%)。LCMS(ES)[M+1]+m/z 380。
步骤3
向500mL三颈圆底烧瓶中添加三氟甲烷磺酸2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基酯(15.0g,39.6mmol,1.00当量)、TEA(16.0g,158.4mmol,4.00当量)及二氯甲烷(300mL)。之后在室温下添加N-异丙基-2-(甲基氨基)乙酰胺盐酸盐(8.5g,51.5mmol,1.30当量)。搅拌混合物12h。将反应物用H2O(200mL)淬灭,且用二氯甲烷(2×100mL)萃取。将有机层合并,且经无水硫酸钠干燥。过滤后,减压浓缩滤液。于乙酸乙酯/己烷(1:3)中湿磨残余物。通过过滤收集固体且在红外灯下干燥3h。由此产生13.0g(91%)呈灰白色固体的2-((2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-异丙基乙酰胺。LCMS(ES,m/z):[M+H]+:360。
步骤4
向500mL三颈圆底烧瓶中放入2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇(12.6g,72.4mmol,2.00当量)及DMSO(150mL)。在0℃下添加NaH(60%于矿物油中)(2.9g,72.4mmol,2.00当量)且搅拌1h。此后,分三份添加2-((2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-异丙基乙酰胺(13.0g,36.2mmol,1.00当量),且在40℃下再搅拌混合物3h。使反应混合物冷却至室温,用H2O(200mL)淬灭,且用乙酸乙酯(3×100mL)萃取。将有机层合并,用盐水(2×100mL)洗涤,且经无水硫酸钠干燥。过滤后,减压浓缩滤液。通过使用以下条件的制备型HPLC纯化残余物:C18-500g,CH3CN/H2O(NH4HCO30.1%),30min内自15%达至70%,流动速率,150mL/min,检测器,UV 254nm。由此产生15.0g(83%)呈棕色固体的N-异丙基-2-(甲基(2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。LCMS(ES,m/z):[M+H]+:498。
步骤5
向250mL三颈圆底烧瓶中添加N-异丙基-2-(甲基(2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(15.0g,30.2mmol,1.00当量)、甲醇(100mL)及HCl(c)(5mL)。将混合物搅拌0.5h且用H2O(200mL)稀释。用K2CO3固体将其pH调节至9,且随后用二氯甲烷(2×300mL)萃取。使合并的有机相经无水硫酸钠干燥。过滤后,减压浓缩滤液,于CH3CN(120mL)中湿磨残余物,且通过过滤收集固体,得到7.38g呈白色固体的2-((2-(4-(2-羟基-2-甲基丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-异丙基乙酰胺。LCMS(ES,m/z):[M+H]+:414。1H-NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.7Hz,1H),8.04(d,J=7.8Hz,1H),7.82(d,J=2.4Hz,1H),7.05(dd,J=5.7,2.7Hz,1H),4.70(s,1H),4.15(s,2H),3.93-3.82(m,3H),3.27(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.24(s,6H),1.05(d,J=6.6Hz,6H)。
实施例1.396
合成N-乙基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物390)
通过用乙胺替换丙烷-2-胺,与389类似地合成化合物390。LCMS(ES)[M+1]+m/z:400。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.18(t,J=5.1Hz,1H),7.81(d,J=2.5Hz,1H),7.04(dd,J=5.7,2.5Hz,1H),4.70(s,1H),4.15(s,2H),3.86(s,2H),3.27(s,3H),3.18-3.07(m,4H),2.82(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.23(s,6H),1.04(t,J=6.6Hz,3H)。
实施例1.397
合成1-(4,4-二氟哌啶-1-基)-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙-1-酮(化合物391)
通过用乙胺替换丙烷-2-胺,与389类似地合成化合物391。LCMS(ES)[M+1]+m/z:476。1H NMR(300MHz,DMSO-d6)δ8.42(d,J=5.6Hz,1H),8.15(s,HCOOH),7.76(d,J=2.5Hz,1H),7.03(dd,J=5.6,2.5Hz,1H),4.71(s,1H),4.58(s,2H),3.85(s,2H),3.61-3.54(m,4H),3.29(s,3H),3.17(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.31-2.09(m,2H),1.99-1.79(m,4H),1.22(s,6H)。
实施例1.398
合成2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-甲基戊-3-基)乙酰胺(化合物392)
用2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(3-甲基戊-3-基)乙酰胺替换中间体II,与化合物44类似地合成化合物392。LCMS(ES)[M+1]+m/z:428。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),8.16(s,HCOOH),7.83(d,J=2.5Hz,1H),7.33(s,1H),7.03(dd,J=5.6,2.6Hz,1H),4.20(s,2H),4.14(t,J=4.9Hz,2H),3.76(t,J=4.9Hz,2H),3.25(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.03-1.96(m,2H),1.71(dq,J=14.7,7.4Hz,2H),1.56-1.38(m,2H),1.09(s,3H),0.70(t,J=7.4Hz,6H)。
实施例1.399及实施例1.400
合成N-叔丁基-2-[(2-{4-[(2R)-2-羟基丁氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物393)及N-叔丁基-2-[(2-{4-[(2R)-2-羟基丁氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物394)
流程128
步骤1
向20mL小瓶中放入2-((四氢-2H-吡喃-2-基)氧基)丁-1-醇(390mg,2.24mmol,2.00当量)及DMSO(4.00mL)。添加NaH(60%于矿物油中)(90mg,2.24mmol,2.00当量)且在室温下搅拌混合物0.5h,且添加N-(叔丁基)-2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(400mg,1.12mmol,1.00当量)。将所得溶液在室温下搅拌1h,且随后用冷却水淬灭,用3×30mL乙酸乙酯萃取。将合并的有机相用盐水(20mL×2洗涤,经无水硫酸钠干燥,过滤且浓缩滤液。由此产生841mg呈黄色油状物的粗物质N-(叔丁基)-2-(甲基(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺且不经进一步纯化即用于下一步骤中。LCMS(ES)[M+1]+m/z:512。
步骤2
向50mL圆底烧瓶中放入N-(叔丁基)-2-(甲基(2-(4-(2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(841mg,1.65mmol,1.00当量)、MeOH(5.0mL)、TsOH(284mg,1.65mmol,1.00当量)。在室温下搅拌混合物1h。通过使用以下条件的制备型HPLC纯化反应混合物:Welch Xtimate C18,21.2*250mm,5um,移动相,水(10mmol/L NH4HCO3)及CH3CN(15min内自25%相B达至65%),检测器,UV254nm。获得520mg呈白色固体的N-(叔丁基)-2-((2-(4-(2-羟基丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES)[M+1]+m/z:428。
步骤3
手性HPLC分离:通过使用以下条件的制备型手性HPLC分离300mg N-(叔丁基)-2-((2-(4-(2-羟基丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺:柱,Lux 5um Cellulose-4,2.12*25cm,5μm,移动相,MeOH及EtOH(50%相B,23min),检测器,UV 254nm。冷冻干燥7min时的洗脱份,由此产生110mg(R)-N-(叔丁基)-2-((2-(4-(2-羟基丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(化合物393),且冷冻干燥16min时的洗脱份,由此产生120mg呈白色固体的(S)-N-(叔丁基)-2-((2-(4-(2-羟基丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(化合物394)。
化合物393:分析型手性HPLC条件:柱,Lux-cellulose-4,100*4.6mm,3um;移动相A,乙醇;移动相B,甲醇;流动速率:1mL/min;梯度:50%B,6min;254nm。保留时间:2.239min。LCMS(ES)[M+1]+m/z:428。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.7Hz,1H),7.84(d,J=2.4Hz,1H),7.67(s,1H),7.07(dd,J=5.7,2.4Hz,1H),4.90(d,J=5.1Hz,1H),4.13(s,2H),4.00(d,J=5.4Hz,2H),3.77-3.71(m,1H),3.26(s,3H),3.14(t,J=7.2Hz,2H),2.84(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.66-1.40(m,2H),1.25(s,9H),0.96(t,J=7.5Hz,3H)。
化合物394:分析型手性HPLC条件:柱,Lux-cellulose-4,100*4.6mm,3um;移动相A,乙醇;移动相B,甲醇;流动速率:1mL/min;梯度:50%B,6min;254nm。保留时间:4.139min。LCMS(ES)[M+1]+m/z:428。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.7Hz,1H),7.84(d,J=2.4Hz,1H),7.67(s,1H),7.07(dd,J=5.7,2.4Hz,1H),4.90(d,J=5.1Hz,1H),4.13(s,2H),4.00(d,J=5.4Hz,2H),3.77-3.71(m,1H),3.26(s,3H),3.14(t,J=7.2Hz,2H),2.84(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.66-1.40(m,2H),1.25(s,9H),0.96(t,J=7.5Hz,3H)。
实施例1.401
合成N-叔丁基-2-({2-[4-(2-乙基-2-羟基丁氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物395)
通过用2-乙基-2-(氧杂环己-2-基氧基)丁-1-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与化合物174类似地合成化合物395。LCMS(ES)[M+1]+m/z:456。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.81(d,J=2.5Hz,1H),7.67(s,1H),7.06(dd,J=5.7,2.6Hz,1H),4.41(s,1H),4.13(s,2H),3.87(s,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.07-1.88(m,2H),1.61-1.50(m,4H),1.25(s,9H),0.85(t,J=7.4Hz,6H)。
实施例1.402
合成N-叔丁基-2-[(2-{4-[(1-羟基环己基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物396)
通过用1-(羟甲基)环己-1-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与化合物174类似地合成化合物396。LCMS(ES)[M+1]+m/z:468。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.82(d,J=2.5Hz,1H),7.68(s,1H),7.06(dd,J=5.8,2.5Hz,1H),4.43(s,1H),4.14(s,2H),3.87(s,2H),3.27(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.05-1.97(m,2H),1.86-1.33(m,9H),1.25(s,9H),1.25-1.15(m,1H)。
实施例1.403
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-[(1R,2S)-2-羟基环戊基]乙酰胺(化合物397)
通过用(1S,2R)-2-氨基环戊-1-醇替换5-氨基-2-甲氧基吡啶,与210类似地合成化合物397。分析型手性HPLC条件:柱,(S,S)-WHELK-O1,100*4.6mm,3um;移动相A,正己烷;移动相B,乙醇;流动速率:1mL/min;梯度:50%B,10min;254nm。保留时间:3.293min。LCMS(ES)[M+1]+m/z:456。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),7.79(d,J=2.5Hz,1H),7.69(d,J=7.8Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),4.72(s,2H),4.31(d,J=16.6Hz,1H),4.20(d,J=16.7Hz,1H),3.94-3.87(m,4H),3.26(s,3H),3.14(t,J=7.6Hz,2H),2.82(t,J=7.9Hz,2H),2.01-1.96(m,2H),1.81-1.63(m,3H),1.58-1.39(m,3H),1.23(s,6H)。
实施例1.404
合成N-环丙基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物398)
通过用环丙胺替换丙烷-2-胺,与389类似地合成化合物398。LCMS(ES)[M+1]+m/z:412。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.25(d,J=4.1Hz,1H),7.79(d,J=2.5Hz,1H),7.04(dd,J=5.7,2.5Hz,1H),4.70(s,1H),4.14(s,2H),3.87(s,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.63(dq,J=7.4,3.8Hz,1H),2.04-1.95(m,2H),1.24(s,6H),0.69-0.46(m,2H),0.45-0.39(m,2H)。
实施例1.405
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-(吗啉-4-基)乙-1-酮(化合物399)
通过用吗啉替换丙烷-2-胺,与389类似地合成化合物399。LCMS(ES)[M+1]+m/z:442。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),7.75(d,J=2.5Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),4.70(s,1H),4.52(s,2H),3.86(d,J=4.8Hz,2H),3.72-3.41(m,8H),3.28(s,3H),3.16(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.11-1.91(m,2H),1.24(s,6H)。
实施例1.406
合成N-叔丁基-2-[(2-{4-[2-(二乙基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物400)
通过用二乙氨基乙醇替换二甲氨基乙醇,与化合物348类似地合成化合物400。LCMS(ES)[M+1]+m/z:455。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.83(d,J=2.5Hz,1H),7.67(s,1H),7.05(dd,J=5.6,2.6Hz,1H),4.16(t,J=6.1Hz,2H),4.13(s,2H),3.26(s,3H),3.15(t,J=7.3Hz,2H),2.87-2.76(m,4H),2.63-2.52(m,4H),2.02-1.99(m,2H),1.25(s,9H),0.98(t,J=7.1Hz,6H)。
实施例1.407
合成N-叔丁基-2-[甲基(2-{4-[2-(吡咯烷-1-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物401)
通过用羟乙基吡咯烷替换二甲氨基乙醇,与化合物348类似地合成化合物401。LCMS(ES)[M+1]+m/z:454。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.84(d,J=2.5Hz,1H),7.69(s,1H),7.05(dd,J=5.6,2.6Hz,1H),4.21(t,J=5.8Hz,2H),4.13(s,2H),3.27(s,3H),3.14(t,J=7.3Hz,2H),2.85-2.78(m,4H),2.62-2.43(m,4H),2.04-1.94(m,2H),1.77-1.61(m,4H),1.25(s,9H)。
实施例1.408
合成N-叔丁基-2-{[2-(4-{[(2S)-1-(二甲基氨基)丙-2-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物402)
通过用(S)-1-(二甲基氨基)丙-2-醇替换二甲氨基乙醇,与化合物348类似地合成化合物402。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6)δ8.45(d,J=5.6Hz,1H),7.82(d,J=2.5Hz,1H),7.68(s,1H),7.07(dd,J=5.7,2.6Hz,1H),4.83-4.77(m,1H),4.11(s,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.59-2.52(m,1H),2.39(dd,J=12.8,5.5Hz,1H),2.21(s,6H),2.04-1.97(m,2H),1.28(d,J=6.1Hz,3H),1.25(s,9H)。
实施例1.409
合成2-{[2-(4-{[(叔丁基氨甲酰基)甲基](甲基)氨基}-5H,6H,7H-环戊并[d]嘧啶-2-基)吡啶-4-基]氧基}-N,N-二甲基乙酰胺(化合物403)
通过用2-羟基-N,N-二甲基乙酰胺替换二甲氨基乙醇,与化合物348类似地合成化合物403。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6)δ8.45(d,J=5.6Hz,1H),7.83(d,J=2.6Hz,1H),7.66(s,1H),6.98(dd,J=5.7,2.6Hz,1H),5.00(s,2H),4.13(s,2H),3.25(s,3H),3.12(t,J=7.3Hz,2H),3.01(s,3H),2.85(s,3H),2.81(t,J=7.8Hz,2H),2.01-1.96(m,2H),1.24(s,9H)。
实施例1.410
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)-2-甲基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物404)
通过用2-(二甲基氨基)-2-甲基丙-1-醇替换二甲氨基乙醇,与化合物348类似地合成化合物404。LCMS(ES)[M+1]+m/z:455。1H NMR(300MHz,DMSO-d6)δ8.49(d,J=5.6Hz,1H),8.20(s,2H),7.83(d,J=2.5Hz,1H),7.67(s,1H),7.09(dd,J=5.6,2.5Hz,1H),4.14(s,2H),4.05(s,2H),3.26(s,3H),3.15(t,J=7.2Hz,2H),2.81(t,J=7.8Hz,2H),2.36(s,6H),2.04-1.97(m,2H),1.25(s,9H),1.19(s,6H)。
实施例1.411
合成N-叔丁基-2-[(2-{4-[(4-羟基氧杂环己-4-基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物405)
通过用4-(羟甲基)四氢-2H-吡喃-4-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与化合物174类似地合成化合物405。LCMS(ES)[M+1]+m/z:470。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.84(d,J=2.6Hz,1H),7.67(s,1H),7.06(dd,J=5.6,2.6Hz,1H),4.77(s,1H),4.14(s,2H),3.92(s,2H),3.76-3.63(m,4H),3.26(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.02-1.93(m,2H),1.86-1.70(m,2H),1.57-1.43(m,2H),1.25(s,9H)。
实施例1.412
合成N-叔丁基-2-{[2-(4-{[(2R)-1-(二甲基氨基)丙-2-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物406)
通过用(R)-1-(二甲基氨基)丙-2-醇替换二甲氨基乙醇,与化合物348类似地合成化合物406。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.7Hz,1H),7.82(d,J=2.4Hz,1H),7.67(s,1H),7.09(dd,J=5.7,2.7Hz,1H),4.84-4.78(m,1H),4.12(s,2H),3.27(s,3H),3.15(t,J=7.2Hz,2H),2.84(t,J=7.8Hz,2H),2.61-2.55(m,1H),2.46-2.40(m,1H),2.23(s,6H),2.04-1.94(m,2H),1.30(d,J=6.0Hz,3H),1.26(s,9H)。
实施例1.413
合成N-叔丁基-2-{[2-(4-{[1-(二甲基氨基)-2-甲基丙-2-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物407)
通过用1-(二甲基氨基)-2-甲基丙-2-醇替换二甲氨基乙醇,与化合物348类似地合成化合物407。LCMS(ES)[M+1]+m/z:455。1H NMR(300MHz,DMSO-d6)δ8.44(d,J=5.5Hz,1H),7.82(d,J=2.6Hz,1H),7.63(s,1H),7.09(dt,J=5.0,2.1Hz,1H),4.15(s,2H),3.24(s,3H),3.13(t,J=7.4Hz,2H),2.81(t,J=7.8Hz,2H),2.58(s,2H),2.28(s,6H),2.02-1.96(m,2H),1.44(s,6H),1.26(d,J=1.6Hz,9H)。
实施例1.414
合成(2R)-N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]丙酰胺(化合物408)
流程129
步骤1
向40mL小瓶中添加(2R)-N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)丙酰胺(330mg,1.06mmol,1.00当量)及甲苯(20mL)、4-氟-2-(三丁基锡烷基)吡啶(615mg,1.59mmol,1.50当量)、Pd(PPh3)4(123mg,0.10mmol,0.10当量)。在120℃下于氮气氛围下搅拌所得混合物12h。真空浓缩所得混合物。通过硅胶柱色谱,用CH2Cl2/MeOH(10:1)洗脱来纯化残余物,得到呈棕色固体的(2R)-N-叔丁基-2-{[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}内酰胺(240mg,61%)。LCMS(ES)[M+1]+m/z:372。
步骤2
向20mL小瓶添加二甲氨基乙醇(115mg,1.29mmol,2.00当量)及DMSO(3mL),向以上混合物分批添加NaH(60%于矿物油中)(52mg,1.29mmol,2.00当量)。在室温下搅拌所得混合物0.5h。向以上混合物分批添加(2R)-N-叔丁基-2-{[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}内酰胺(240mg,0.64mmol,1.00当量)。在室温下再搅拌所得混合物1h。将反应物用水(1mL)淬灭且通过使用以下条件的制备型HPLC纯化:SunfirePrep C18 OBD柱,50*250mm,5μm,10nm,移动相,水(0.1%NH4OH)及CH3CN(15min内自5%CH3CN达至25%),检测器,254nm UV),得到呈白色固体的(2R)-N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]丙酰胺(112.8mg,40%)。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6)δ8.49(d,J=5.6Hz,1H),7.89(d,J=2.5Hz,1H),7.80(s,1H),7.06(dd,J=5.7,2.6Hz,1H),5.06(q,J=7.0Hz,1H),4.21(t,J=5.7Hz,2H),3.22(dt,J=15.6,7.8Hz,1H),3.12(s,3H),3.13-2.99(m,1H),2.97-2.72(m,2H),2.66(t,J=5.7Hz,2H),2.23(s,6H),2.06 -1.97(m,2H),1.32(d,J=7.0Hz,3H),1.20(s,9H)。
实施例1.415
合成N-叔丁基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)乙酰胺(化合物409)
通过用2-氨基乙酸叔丁酯替换N-(叔丁基)-2-(甲基氨基)乙酰胺,与化合物174类似地合成化合物409。LCMS(ES)[M+1]+m/z:414。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),7.84(d,J=2.5Hz,1H),7.69(s,1H),7.14(t,J=5.9Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),4.70(s,1H),3.94(d,J=5.8Hz,2H),3.86(s,2H),2.84(t,J=7.7Hz,2H),2.74(t,J=7.4Hz,2H),2.09-2.05(m,2H),1.25(s,9H),1.24(s,6H)。
实施例1.416
合成N-(1-环丙基-1H-吡唑-4-基)-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物410)
通过用1-环丙基-1H-吡唑-4-胺替换叔丁胺,与化合物348类似地合成化合物410。LCMS(ES)[M+1]+m/z:477。1H NMR(300MHz,DMSO-d6)δ10.24(s,1H),8.46(d,J=5.6Hz,1H),7.88(s,1H),7.76(d,J=2.6Hz,1H),7.39(s,1H),7.02(dd,J=5.7,2.5Hz,1H),4.34(s,2H),4.11(t,J=5.5Hz,2H),3.64(tt,J=7.2,4.0Hz,1H),3.32(s,3H),3.19(t,J=7.3Hz,2H),2.83(t,J=7.8Hz,2H),2.60(t,J=5.5Hz,2H),2.21(s,6H),2.05-1.95(m,2H),1.02-0.83(m,4H)。
实施例1.417
合成N-叔丁基-2-{甲基[2-(4-{[(2R)-1-甲基吡咯烷-2-基]甲氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物411)
通过用(R)-(1-甲基吡咯烷-2-基)替换二甲氨基乙醇,与化合物348类似地合成化合物411。LCMS(ES)[M+1]+m/z:453。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.82(d,J=2.4Hz,1H),7.65(s,1H),7.05(dd,J=5.6,2.4Hz,1H),4.15-4.11(m,3H),4.01-3.96(m,1H),3.26(s,3H),3.16(t,J=7.2Hz,2H),2.99-2.96(m,1H),2.83(t,J=7.6Hz,2H),2.67-2.65(m,1H),2.40(s,3H),2.26-2.24(m,1H),2.02-1.95(m,3H),1.75-1.63(m,3H),1.24(s,9H)。
实施例1.418
合成N-叔丁基-2-{甲基[2-(4-{[(2S)-1-甲基吡咯烷-2-基]甲氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物412)
通过用(S)-(1-甲基吡咯烷-2-基)替换二甲氨基乙醇,与化合物348类似地合成化合物412。LCMS(ES)[M+1]+m/z:453。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.4Hz,1H),7.82(d,J=2.4Hz,1H),7.67(s,1H),7.05(dd,J=5.7,2.4Hz,1H),4.16-4.11(m,3H),4.01-3.97(m,1H),3.26(s,3H),3.16(t,J=7.2Hz,2H),2.99-2.96(m,1H),2.83(t,J=7.5Hz,2H),2.67-2.65(m,1H),2.40(s,3H),2.26-2.24(m,1H),2.02-1.95(m,3H),1.75-1.63(m,3H),1.24(s,9H)。
实施例1.419
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5,5-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物413)
通过用N-叔丁基-2-(甲基氨基)乙酰胺盐酸盐替换2-(甲基氨基)-N-(6-甲基吡啶-3-基)乙酰胺且用二甲氨基乙醇替换乙烷-1,2-二醇,与化合物331类似地合成化合物413。LCMS(ES)[M+1]+m/z:455。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.85(d,J=2.6Hz,1H),7.66(s,1H),7.07(dd,J=5.6,2.6Hz,1H),4.20(t,J=5.7Hz,2H),4.03(s,2H),3.19(s,3H),2.86(t,J=7.3Hz,2H),2.66(t,J=5.7Hz,2H),2.23(s,6H),1.87(t,J=7.3Hz,2H),1.43(s,6H),1.22(s,9H)。
实施例1.420
合成N-叔丁基-2-{[2-(4-{[(4R)-2,2-二甲基-1,3-二氧杂环戊-4-基]甲氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物414)
通过用4-{[(4S)-2,2-二甲基-1,3-二氧杂环戊-4-基]甲氧基}-2-(三丁基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶,与化合物34类似地合成化合物414。LCMS(ES)[M+1]+m/z:470.2。1H NMR(400MHz,DMSO-d6)δ8.50-8.47(m,1H),7.87-7.85(m,1H),7.69(s,1H),7.08(dd,J=5.6,2.6Hz,1H),4.48-4.40(m,1H),4.23-4.17(m,1H),4.15-4.06(m,4H),3.79(dd,J=8.4,6.4Hz,1H),3.27(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.03-1.95(m,2H),1.37-1.35(m,3H),1.32-1.30(m,3H),1.24(s,9H)。
实施例1.421
合成N-叔丁基-2-[(2-{4-[(2R)-2,3-二羟基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物415)
流程130
向N-叔丁基-2-{[2-(4-{[(4S)-2,2-二甲基-1,3-二氧杂环戊-4-基]甲氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(44mg;0.09mmol;1当量)于甲醇(1ml)中的溶液中添加HCl(1ml含5-6M HCl的异丙醇)。在25℃下搅拌1h后,浓缩混合物且通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈固体的N-叔丁基-2-[(2-{4-[(2R)-2,3-二羟基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(32mg,80%)。LCMS(ES+):[M+H]+=470.2。1HNMR(400MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.86-7.82(m,1H),7.69(s,1H),7.04(dd,J=5.7,2.6Hz,1H),5.01(d,J=5.1Hz,1H),4.73(s,1H),4.17-4.11(m,3H),4.01(dd,J=10.0,6.0Hz,1H),3.86-3.79(m,1H),3.49-3.44(m,2H),3.26(s,3H),3.16-3.10(m,2H),2.84-2.78(m,2H),2.02-1.94(m,2H),1.24(s,9H)。
实施例1.422
合成N-叔丁基-2-[甲基(2-{4-[(1-甲基氮杂环丁-3-基)氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物416)
通过用1-甲基氮杂环丁烷-3-醇替换二甲氨基乙醇,与化合物348类似地合成化合物416。LCMS(ES)[M+1]+m/z:425。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),7.78(d,J=2.5Hz,1H),7.71(s,1H),6.91(dd,J=5.6,2.6Hz,1H),4.95(q,J=5.6Hz,1H),4.12(s,2H),3.83-3.72(m,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),3.00(dd,J=8.0,5.5Hz,2H),2.80(t,J=7.8Hz,2H),2.30(s,3H),2.03-1.96(m,2H),1.26(s,9H)。
实施例1.423
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-1-(吡咯烷-1-基)乙-1-酮(化合物417)
通过用吡咯烷替换叔丁胺,与化合物348类似地合成化合物417。LCMS(ES)[M+1]+m/z:425。1H NMR(300MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),8.17(s,HCOOH),7.69(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),4.39(s,2H),4.19(t,J=5.7Hz,2H),3.54(t,J=6.8Hz,2H),3.32(t,J=6.8Hz,2H),3.29(s,3H),3.15(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.68(t,J=5.6Hz,2H),2.25(s,6H),2.06-1.88(m,4H),1.89-1.82(m,2H)。
实施例1.424
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-[1-(三氟甲基)环丙基]乙酰胺(化合物418)
通过用1-(三氟甲基)环丙-1-胺替换叔丁胺,与化合物348类似地合成化合物418。LCMS(ES)[M+1]+m/z:479。1H NMR(300MHz,DMSO-d6)δ9.04(s,1H),8.46(d,J=5.6Hz,1H),7.74(d,J=2.5Hz,1H),7.05(dd,J=5.6,2.6Hz,1H),4.25-4.13(m,4H),3.28(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.9Hz,2H),2.66(t,J=5.7Hz,2H),2.23(s,6H),2.04-1.97(m,2H),1.24-1.13(m,2H),1.00-0.91(m,2H)。
实施例1.425
合成N-叔丁基-2-[甲基(2-{4-[2-(甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物419)
通过用N-(2-羟乙基)-N-甲基氨基甲酸叔丁酯替换二甲氨基乙醇,与化合物348类似地合成化合物419。LCMS(ES)[M+1]+m/z:413。1H NMR(300MHz,DMSO-d6)δ9.36(br,2H),8.76(d,J=6.0Hz,1H),8.17(s,1H),8.11(br,1H),7.50(dd,J=6.1,2.6Hz,1H),4.62(t,J=5.0Hz,2H),4.42(s,2H),3.45 -3.36(m,5H),3.23(t,J=7.9Hz,2H),3.01(t,J=7.9Hz,2H),2.68-2.61(m,3H),2.14-2.03(m,2H),1.25(s,9H)。
实施例1.426
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-1-(吡咯烷-1-基)乙-1-酮(化合物420)
通过用吡咯烷替换丙烷-2-胺,与化合物389类似地合成化合物420。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6)δ8.45(d,J=5.6Hz,1H),7.71(s,1H),7.06-6.99(m,1H),4.70(s,1H),4.40(s,2H),3.85(s,2H),3.56(t,J=6.8Hz,2H),3.33-3.31(m,2H),3.30(s,3H),3.15(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),1.97(dp,J=14.0,7.4Hz,4H),1.79(p,J=6.8Hz,2H),1.22(s,6H)。
实施例1.427
合成N-环戊基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物421)
通过用1-环戊胺替换丙烷-2-胺,与化合物389类似地合成化合物421。LCMS(ES)[M+1]+m/z:440。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.28(s,1H),8.09(d,J=7.5Hz,1H),7.80(d,J=2.5Hz,1H),7.05(dd,J=5.7,2.6Hz,1H),4.17(s,2H),4.06-3.95(m,1H),3.87(s,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.02-1.95(m,2H),1.77(dq,J=13.1,6.8,6.2Hz,2H),1.57(tq,J=5.7,2.8Hz,2H),1.51-1.31(m,4H),1.24(s,6H)。
实施例1.428
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-[(3R)-氧杂环戊-3-基]乙酰胺(化合物422)
通过用(R)-四氢呋喃-3-胺替换丙烷-2-胺,与化合物389类似地合成化合物422。LCMS(ES)[M+1]+m/z:442。1H NMR(300MHz,DMSO-d6)δ8.49(d,J=5.7Hz,1H),8.40(d,J=6.9Hz,1H),7.81(d,J=2.4Hz,1H),7.09(dd,J=5.7,2.7Hz,1H),4.70(s,1H),4.32-4.24(m,1H),4.21(d,J=1.8Hz,2H),3.88(s,2H),3.78-3.70(m,2H),3.67-3.60(m,1H),3.46(dd,J=8.7,3.9Hz,1H),3.28(s,3H),3.18(t,J=7.2Hz,2H),2.86(t,J=7.8Hz,2H),2.11-1.95(m,3H),1.78-1.68(m,1H),1.24(s,6H)。
实施例1.429
合成2-[(2-{4-[2-(二甲基氨基)-2-甲基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-[1-(三氟甲基)环丙基]乙酰胺(化合物423)
通过用1-(三氟甲基)环丙-1-胺替换叔丁胺且用2-(二甲基氨基)-2-甲基丙-1-醇替换二甲氨基乙醇,与化合物348类似地合成化合物423。LCMS(ES)[M+1]+m/z:507。1H NMR(300MHz,DMSO-d6)δ9.04(s,1H),8.46(d,J=5.6Hz,1H),7.75(d,J=2.5Hz,1H),7.07(dd,J=5.7,2.5Hz,1H),4.17(s,2H),3.98(s,2H),3.29(s,3H),3.15(t,J=7.4Hz,2H),2.82(t,J=7.8Hz,2H),2.25(s,6H),2.06-1.93(m,2H),1.28-1.11(m,2H),1.12(s,6H),1.01-0.92(m,2H)。
实施例1.430
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-[(3R)-氧杂环戊-3-基]乙酰胺(化合物424)
流程131
步骤1
向20mL小瓶中添加二甲氨基乙醇(354mg,3.97mmol,2.00当量)、DMSO(5mL)。向以上混合物中添加NaH(60%于矿物油中)(159mg,3.97mmol,2.00当量)。在室温下搅拌所得混合物30min,之后添加2-{[2-(4-氟吡啶-2-基)-5,6,7,8-四氢喹唑啉-4-基](甲基)氨基}乙酸乙酯(683mg,1.98mmol,1.00当量)。在室温下再搅拌所得混合物1h。在室温下用水(2mL)淬灭反应物。用HCOOH将混合物酸化至pH 7。通过使用以下条件的反相急骤色谱纯化残余物:C18-120g柱,H2O(0.05%FA)/MeCN,10%至100%梯度,10min,检测器,UV 254nm。由此产生呈白色固体的N-(2-(4-(2-(二甲基氨基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸甲酸盐(410mg,53%)。LCMS(ES,m/z):[M-HCOOH+H]+:372。
步骤2
向20mL小瓶中添加N-(2-(4-(2-(二甲基氨基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-N-甲基甘氨酸甲酸盐(410mg,1.10mmol,1.00当量)、DMF(5mL)、(3R)-氧杂环戊-3-胺(125mg,1.43mmol,1.30当量)、DIEA(428mg,3.31mmol,3.00当量)。在0℃下添加HATU(546mg,1.44mmol,1.30当量)。在室温下搅拌所得混合物2h。通过使用以下条件的手性制备型HPLC纯化粗产物:XBridge Shield RP18 OBD柱,19*150mm,5μm;移动相,水(0.05%NH3.H2O)及CH3CN(8min内自16%达至33%)。由此产生呈灰白色固体的(R)-2-((2-(4-(2-(二甲基氨基)乙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-(四氢呋喃-3-基)乙酰胺(102.6mg,21%)。LCMS(ES,m/z):[M+H]+:441。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.36(d,J=6.9Hz,1H),7.78(d,J=2.5Hz,1H),7.05(dd,J=5.7,2.6Hz,1H),4.32-4.14(m,5H),3.80-3.59(m,3H),3.45(dd,J=8.9,4.1Hz,1H),3.28(s,3H),3.16(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.66(t,J=5.7Hz,2H),2.23(s,6H),2.15-1.91(m,3H),1.81-1.65(m,1H)。
实施例1.431
合成N-叔丁基-2-[(2-{4-[(1-羟基-2-甲基丙-2-基)氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物425)
通过用4-{[2-甲基-1-(氧杂环己-2-基氧基)丙-2-基]氧基}-2-(三丁基锡烷基)吡啶替换4-[2-(氧杂环己-2-基氧基)乙氧基]-2-(三甲基锡烷基)吡啶,与化合物44类似地合成化合物425。LCMS(ES+):[M+H]+=428.1。1H NMR(400MHz,DMSO-d6)δ8.49-8.42(m,1H),7.87-7.80(m,1H),7.69-7.62(m,1H),7.14-7.03(m,1H),5.04(t,J=5.9Hz,1H),4.16-4.11(m,2H),3.86(s,1H),3.50(d,J=5.8Hz,1H),3.27-3.23(m,3H),3.18-3.09(m,2H),2.85-2.77(m,2H),2.04-1.93(m,2H),1.39(s,3H),1.24(s,9H),1.23(s,3H)。
实施例1.432
合成N-叔丁基-2-[甲基({2-[4-(3,3,3-三氟-2-羟基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物426)
通过用3,3,3-三氟-2-(氧杂环己-2-基氧基)丙-1-醇替换2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇,与化合物174类似地合成化合物426。LCMS(ES+):[M+H]+=453.1。1H NMR(400MHz,DMSO-d6)δ8.51(d,J=5.6Hz,1H),7.85(d,J=2.5Hz,1H),7.65(s,1H),7.12(dd,J=5.7,2.6Hz,1H),6.72(d,J=6.6Hz,1H),4.48-4.39(m,1H),4.36(dd,J=10.7,4.1Hz,1H),4.25(dd,J=10.7,6.1Hz,1H),4.14(s,2H),3.25(s,3H),3.16-3.09(m,2H),2.86-2.78(m,2H),2.04-1.93(m,2H),1.23(s,9H)。
实施例1.433
合成N-叔丁基-2-({2-[4-(2-羟乙氧基)-6-甲基吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物427)
流程132
步骤1
在-78℃下向用惰性氮气氛围吹扫及维持的100mL 3颈圆底烧瓶中放入2-溴-4-氯-6-甲基吡啶(1.00g,4.88mmol,1.00当量)、Tol(30mL)、n-BuLi(2.4mL,1.2当量)的混合物,30min后,在-78℃下逐滴添加SnBu3Cl(1.75g,5.37mmol,1.1当量)。在-78℃至rt下搅拌所得溶液16小时。用1×30ml NH4Cl及1×30ml NaHCO3水溶液以及1×30ml NaCl水溶液洗涤所得混合物。使混合物经无水硫酸钠干燥且浓缩。由此产生1.6g(78.82%)呈黄色油状物的4-氯-2-甲基-6-(三丁基锡烷基)吡啶。LCMS(ES)[M+1]+m/z 418。
步骤2
向用惰性氮气氛围吹扫及维持的40mL小瓶中放入2-溴-4-氯-6-甲基吡啶(1.0g,23.98mmol,1.00当量)、甲苯(20.0mL)、N-(叔丁基)-2-((2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(710mg,23.98mmol,1.0当量)、Pd(PPh3)4(277mg,2.40mmol,0.10当量)的混合物。在120℃下搅拌所得溶液16小时。浓缩所得混合物。将残余物施加至含MeOH/DCM(13/87)的硅胶柱上。由此产生800mg(86.96%)呈黄色固体的4-氯-2-甲基-6-(三丁基锡烷基)吡啶。LCMS(ES)[M+1]+m/z 388。
步骤3
向8mL小瓶中放入NaH(60%)(165mg,2.06mmol,4.00当量)、DMF(4.0mL)、乙烷-1,2-二醇(320mg,2.58mmol,5.0当量)、N-(叔丁基)-2-((2-(4-氯-6-甲基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(200mg,0.516mmol,1.00当量)的混合物。在80℃下搅拌所得溶液16小时。随后通过添加0.5mL水淬灭反应物。通过使用以下条件的制备型HPLC纯化粗产物:SunFire Prep C18 OBD柱,30*50mm,5μm 10nm;移动相A:水(0.1%FA),移动相B:AcCN;流动速率:90mL/min;梯度:12min内自5%B达至35%B,35%B;波长:220nm nm;RT1(min):12;轮数:0。由此产生70mg(32.86%)呈白色固体的N-(叔丁基)-2-((2-(4-(2-羟乙氧基)-6-甲基吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES)[M-46+1]+m/z 414。1H NMR(400MHz,DMSO-d6,ppm):δ8.21(s,1H),7.67(d,J=2.4Hz,1H),7.65(s,1H),6.90(d,J=2.3Hz,1H),4.15-4.08(m,4H),3.74(t,J=4.9Hz,2H),3.25(s,3H),3.13(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.48(s,3H),2.04-1.92(m,1H),1.23(s,9H)。
实施例1.434
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)乙酰胺(化合物428)
通过用二甲氨基乙醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物389类似地合成化合物428。LCMS(ES)[M+1]+m/z:413。1H NMR(300MHz,DMSO-d6)δ8.47(dd,J=5.6,1.2Hz,1H),8.00(d,J=7.8Hz,1H),7.80(d,J=2.5Hz,1H),7.10-7.00(m,1H),4.20(t,J=5.6Hz,2H),4.15(s,2H),3.94-3.80(m,1H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.66(t,J=5.6Hz,2H),2.23(s,6H),2.04-1.97(m,2H),1.05(dd,J=6.6,1.2Hz,6H)。
实施例1.435
合成2-[甲基(2-{4-[2-(吡咯烷-1-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(丙-2-基)乙酰胺(化合物429)
通过用羟乙基吡咯烷替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物389类似地合成化合物429。LCMS(ES)[M+1]+m/z:439。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.99(d,J=7.8Hz,1H),7.80(d,J=2.5Hz,1H),7.05(dd,J=5.6,2.6Hz,1H),4.22(t,J=5.7Hz,2H),4.15(s,2H),3.87(dq,J=13.5,6.7Hz,1H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.87-2.76(m,4H),2.59-2.53(m,4H),2.04-1.97(m,2H),1.75-1.61(m,4H),1.04(d,J=6.6Hz,6H)。
实施例1.436
合成2-[甲基(2-{4-[2-(吗啉-4-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(丙-2-基)乙酰胺(化合物430)
通过用4-吗啉乙醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物389类似地合成化合物430。LCMS(ES)[M+1]+m/z:455。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.99(d,J=7.8Hz,1H),7.81(d,J=2.5Hz,1H),7.05(dd,J=5.6,2.6Hz,1H),4.24(t,J=5.6Hz,2H),4.15(s,2H),3.96-3.78(m,1H),3.64-3.53(m,4H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.73(t,J=5.6Hz,2H),2.50-2.47(m,4H),2.04-1.97(m,2H),1.04(d,J=6.6Hz,6H)。
实施例1.437
合成2-[(2-{4-[(1-羟基环丙基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)乙酰胺(化合物431)
通过用(1-((四氢-2H-吡喃-2-基)氧基)环丙基)甲醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物389类似地合成化合物431。LCMS(ES)[M+1]+m/z:412。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.00(d,J=8.0Hz,1H),7.83(d,J=2.4Hz,1H),7.05(dd,J=5.6,2.8Hz,1H),5.63(s,1H),4.16(s,2H),4.12(s,2H),3.91-3.83(m,1H),3.30(s,3H),3.17(t,J=7.2Hz,2H),2.84(t,J=7.6Hz,2H),2.03-1.96(m,2H),1.05(d,J=6.4Hz,6H),0.74-0.65(m,4H)。
实施例1.438
合成2-[甲基(2-{4-[2-(4-甲基哌嗪-1-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(丙-2-基)乙酰胺(化合物432)
通过用2-(4-甲基哌嗪-1-基)乙醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物389类似地合成化合物432。LCMS(ES)[M+1]+m/z:468。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.99(d,J=7.7Hz,1H),7.80(d,J=2.5Hz,1H),7.05(dd,J=5.7,2.5Hz,1H),4.22(t,J=5.7Hz,2H),4.15(s,2H),3.95-3.81(m,1H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.72(t,J=5.7Hz,2H),2.59-2.50(m,4H),2.40-2.28(m,4H),2.15(s,3H),2.04-1.94(p,J=7.6Hz,2H),1.05(d,J=6.6Hz,6H)。
实施例1.439及实施例1.440
合成(2R)-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)丙酰胺(化合物433)及(2S)-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)丙酰胺(化合物434)
流程133
步骤1
在室温下向100mL圆底烧瓶中添加三氟甲烷磺酸2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基酯(2.5g,6.58mmol,1.00当量)、N-异丙基-2-(甲基氨基)丙酰胺(1.42g,9.88mmol,1.5当量)、NMP(20mL)及DIEA(2.55g,19.75mmol,3当量)。在40℃下搅拌所得混合物4h。在室温下用水淬灭反应物,且用EtOAc(3×200mL)萃取所得混合物。将合并的有机层用盐水(3×200mL)洗涤,且经无水Na2SO4干燥。过滤后,减压浓缩滤液。使粗产物自EtOAc(100mL)再晶体,得到呈淡黄色固体的2-{[2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-异丙基丙酰胺(1g,40.63%)。LCMS(ES)[M+1]+m/z 374。
步骤2
在0℃下向40mL小瓶中添加二甲氨基乙醇(238mg,2.67mmol,2当量)及DMSO(5mL)。在0℃下向以上混合物分批添加NaH(107mg,2.67mmol,2当量)。在室温下再搅拌所得混合物30min。随后在0℃下向混合物中逐滴添加含2-{[2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-异丙基丙酰胺(500mg,1.34mmol,1.00当量)的DMSO。在室温下搅拌所得溶液1hr。通过使用以下条件的手性制备型HPLC(Prep-HPLC-003)纯化粗产物:柱,SunFire Prep C18 OBD柱,19*150mm,5μm 10nm;移动相,水(0.05%TFA)及ACN(8min内自35%ACN达至88%)。再次通过使用以下条件的手性制备型HPLC(XA-Prep Chiral HPLC-01)纯化粗产物:柱,CHIRAL ART Cellulose-SB,3*25cm,5um;移动相,己烷(0.5%2M NH3-MeOH)及EtOH(0.5%2M NH3-MeOH)(12min内保持30% EtOH(0.5%2M NH3-MeOH))。由此产生呈白色固体的(2R)-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-异丙基丙酰胺(111.6mg,39.13%)及(2S)-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-异丙基丙酰胺(114.9mg,36.36%)。
化合物433:分析型手性HPLC条件:柱,YMC-cellulose-SB,100*4.6mm,3um;移动相A,正己烷;移动相B,乙醇;流动速率:1mL/min;梯度:10%B,10min;254nm。保留时间:3.067min。LCMS(ES)[M+1]+m/z 427。1H NMR(400MHz,DMSO-d6)δ8.49(d,J=5.6Hz,1H),8.21(d,J=8.0Hz,1H),7.87(d,J=2.5Hz,1H),7.10-7.04(m,1H),5.07(q,J=7.0Hz,1H),4.24(t,J=5.6Hz,2H),3.95-3.82(m,1H),3.28-3.15(m,1H),3.11-3.03(m,4H),2.95-2.75(m,2H),2.72(t,J=5.7Hz,2H),2.27(s,6H),2.11-1.88(m,2H),1.34(d,J=7.0Hz,3H),1.08(d,J=6.6Hz,3H),0.91(d,J=6.6Hz,3H)。
化合物434:分析型手性HPLC条件:柱,YMC-cellulose-SB,100*4.6mm,3um;移动相A,正己烷;移动相B,乙醇;流动速率:1mL/min;梯度:10%B,10min;254nm。保留时间:4.820min。LCMS(ES)[M+1]+m/z427。1H NMR(400MHz,DMSO-d6)δ8.49(d,J=5.6Hz,1H),8.21(d,J=8.0Hz,1H),8.17(s,HCOOH),7.87(d,J=2.5Hz,1H),7.10-7.04(m,1H),5.07(q,J=7.0Hz,1H),4.24(t,J=5.6Hz,2H),3.95-3.82(m,1H),3.28-3.15(m,1H),3.11(s,4H),2.95-2.75(m,2H),2.72(t,J=5.7Hz,2H),2.27(s,6H),2.11-1.88(m,2H),1.34(d,J=7.0Hz,3H),1.08(d,J=6.6Hz,3H),0.91(d,J=6.6Hz,3H)。
实施例1.440
合成(2R)-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)丙酰胺(化合物433)
步骤1
在室温下于N2氛围下向二甲氨基乙醇(2.10g,24.22mmol,3.00当量)于DMSO(30mL)中的搅拌混合物中分批添加NaH(0.97g,24.22mmol,3.00当量)。在室温下搅拌反应物30min,之后添加2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-醇(2.0g,8.07mmol,1.00当量)。在40℃下搅拌所得混合物1h且用15℃的H2O(5mL)淬灭。通过制备型HPLC(柱,C18;移动相,移动相:MeCN=5/1B:水流动速率:50mL/min柱:DAICEL CHIRALPAK IC,250*20mm,220nm梯度:50%B,20min;220nm)纯化反应混合物,得到呈灰白色固体的2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-醇(2.1g,86.58%)。LCMS(ES)[M+1]+m/z:301。
步骤2
在0℃下于N2氛围下向2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-醇(2.00g,6.66mmol,1.00当量)及TEA(2.70g,26.63mmol,4.00当量)于DCM(30mL)中的搅拌溶液中逐滴添加(CF3SO2)2O(3.76g,13.31mmol,2.00当量)。在0 -25℃下搅拌反应物5h后,通过添加0℃的水(20mL)淬灭反应物。用DCM(50mL×3)萃取所得溶液,将合并的有机层用盐水洗涤,经无水硫酸钠干燥,且真空浓缩。由此产生呈棕色油状物的三氟甲烷磺酸2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基酯(2.6g,90.30%),其直接用于下一步骤中。
步骤3
在25℃下向三氟甲烷磺酸2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基酯(2.50g,5.78mmol,1.00当量)及TEA(2.93g,28.90mmol,5.00当量)于DCM(50mL)中的搅拌溶液中一次性添加(2R)-N-异丙基-2-(甲基氨基)丙酰胺盐酸盐(1.57g,8.67mmol,1.50当量),在25-40℃下搅拌所得反应物16h。将反应物用0℃的水(30mL)淬灭,用DCM(50mL×5)萃取。将合并的有机层用盐水(50mL)洗涤,经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过使用以下条件的制备型HPLC(柱,C18;移动相,移动相:MeCN=5/1B:水流动速率:40mL/min柱:DAICEL CHIRALPAK IC,250*20mm,220nm梯度:50%B,25min;220nm)纯化粗产物(2.1g),得到750mg(纯度99.75%)呈白色固体的所要产物。将750mg(纯度99.75%)的所要产物用庚烷/EtOAc(50:1,50mL)湿磨1h且过滤。浓缩滤液,得到呈白色固体的(2R)-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-异丙基丙酰胺(375mg,产率15.21%,纯度99.903%)。分析型手性HPLC条件:柱,YMC-cellulose-SB,100*4.6mm,3um;移动相A,正己烷;移动相B,乙醇;流动速率:1mL/min;梯度:10%B,10min;254nm。保留时间:3.341minLCMS(ES)[M+1]+m/z:427。1HNMR(400MHz,DMSO-d6)δ8.49(d,J=5.6Hz,1H),8.21(d,J=8.0Hz,1H),7.86(d,J=2.5Hz,1H),7.07(dd,J=5.6,2.6Hz,1H),5.07(d,J=7.1Hz,1H),4.22(t,J=5.7Hz,2H),3.89(dt,J=7.7,6.4Hz,1H),3.26-3.17(m,1H),3.11(s,3H),3.10-3.04(m,1H),2.94-2.75(m,2H),2.67(t,J=5.7Hz,2H),2.23(s,6H),2.10-1.87(m,2H),1.34(d,J=7.0Hz,3H),1.08(d,J=6.6Hz,3H),0.91(d,J=6.5Hz,3H)。
实施例1.441
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5,5-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)乙酰胺(化合物435)
通过用N-异丙基-2-(甲基氨基)乙酰胺盐酸盐替换2-(甲基氨基)-N-(6-甲基吡啶-3-基)乙酰胺且用二甲氨基乙醇替换乙烷-1,2-二醇,与化合物331类似地合成化合物435。LCMS(ES)[M+1]+m/z:441。1H NMR(400MHz,DMSO-d6)δ8.49(d,J=5.6Hz,1H),8.12(d,J=7.8Hz,1H),7.81(d,J=2.5Hz,1H),7.07(dd,J=5.6,2.6Hz,1H),4.20(t,J=5.7Hz,2H),4.05(s,2H),3.85(dq,J=13.5,6.7Hz,1H),3.20(s,3H),2.87(t,J=7.3Hz,2H),2.66(t,J=5.7Hz,2H),2.23(s,6H),1.87(t,J=7.3Hz,2H),1.43(s,6H),1.03(d,J=6.6Hz,6H)。
实施例1.442
合成2-[甲基(2-{4-[2-(3-氧代吗啉-4-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(丙-2-基)乙酰胺(化合物436)
通过用4-(2-(苯甲氧基)乙基)吗啉-3-酮替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物389类似地合成化合物436。LCMS(ES)[M+1]+m/z:469。1H NMR(400MHz,DMSO-d6)δ8.50(d,J=5.6Hz,1H),8.00(d,J=8.0Hz,1H),7.81(d,J=2.8Hz,1H),7.08(dd,J=4.8,2.8Hz,1H),4.32(t,J=5.6Hz,2H),4.15(s,2H),4.05(s,2H),3.92-3.85(m,1H),3.84(t,J=4.8Hz,2H),3.76(t,J=5.6Hz,2H),3.53(t,J=5.2Hz,2H),3.27(s,3H),3.17(t,J=7.2Hz,2H),2.84(t,J=7.6Hz,2H),2.03-1.96(m,2H),1.05(d,J=6.8Hz,6H)。
实施例1.443
合成N-叔丁基-2-{甲基[2-(4-{[(3R)-1-甲基吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物437)
在0℃下向40mL小瓶中添加(3R)-1-甲基吡咯烷-3-醇(108mg,1.07mmol,2当量)及DMSO(5mL)。在0℃下向以上混合物分批添加NaH(43mg,1.07mmol,2当量)。在室温下再搅拌所得混合物30min,且在0℃下逐滴添加含N-叔丁基-2-{[2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(200mg,0.54mmol,1.00当量)的DMSO。在室温下搅拌所得溶液1hr且通过使用以下条件的手性制备型HPLC(Prep-HPLC-003)纯化粗产物:柱,SunFire Prep C18 OBD柱,19*150mm,5μm 10nm;移动相,水(0.1%FA)及ACN(8min内自15%ACN达至55%);由此产生呈淡棕色半固体的N-叔丁基-2-{甲基[2-(4-{[(3R)-1-甲基吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(甲酸盐)(93.6mg,32.98%)。LCMS(ES)[M+1]+m/z:439。1H NMR(400MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),7.81(d,J=2.5Hz,1H),7.69(s,1H),6.99(dd,J=5.6,2.6Hz,1H),5.10-5.02(m,1H),4.12(s,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.93-2.85(m,1H),2.81(t,J=7.8Hz,2H),2.75-2.65(m,2H),2.49-2.33(m,2H),2.31(s,3H),2.05-1.93(m,2H),1.88-1.77(m,1H),1.25(s,9H)。
实施例1.444
合成N-叔丁基-2-{甲基[2-(4-{[(3S)-1-甲基吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物438)
通过用(3S)-1-甲基吡咯烷-3-醇替换二甲氨基乙醇,与化合物348类似地合成化合物438。LCMS(ES)[M+1]+m/z:439。1H NMR(400MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),7.81(d,J=2.5Hz,1H),7.69(s,1H),6.99(dd,J=5.6,2.6Hz,1H),5.10-5.02(m,1H),4.12(s,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.93-2.85(m,1H),2.81(t,J=7.8Hz,2H),2.75-2.65(m,2H),2.49-2.33(m,2H),2.31(s,3H),2.05-1.93(m,2H),1.88-1.77(m,1H),1.25(s,9H)。
实施例1.445
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5,5-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(丙-2-基)乙酰胺(化合物439)
通过用N-异丙基-2-(甲基氨基)乙酰胺盐酸盐替换2-(甲基氨基)-N-(6-甲基吡啶-3-基)乙酰胺且用2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇替换乙烷-1,2-二醇,与化合物331类似地合成化合物439。LCMS(ES)[M+1]+m/z:442。1H NMR(400MHz,DMSO-d6)δ8.49(d,J=5.6Hz,1H),8.18(d,J=7.8Hz,1H),7.83(d,J=2.5Hz,1H),7.07(dd,J=5.7,2.6Hz,1H),4.70(s,1H),4.06(s,2H),3.87(s,2H),3.92-3.79(m,1H),3.20(s,3H),2.87(t,J=7.2Hz,2H),1.88(t,J=7.3Hz,2H),1.43(s,6H),1.24(s,6H),1.02(d,J=6.6Hz,6H)。
实施例1.446
合成N-叔丁基-2-({2-[4-(2-羟基-2-甲基丙氧基)-6-甲基吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物440)
通过用2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙-1-醇替换乙烷-1,2-二醇,与化合物427类似地合成化合物440。LCMS(ES)[M+1]+m/z:442。1H NMR(300MHz,DMSO-d6,ppm):7.72-7.59(m,2H),6.98-6.88(m,1H),4.67(br,1H),4.13(s,2H),3.83(s,2H),3.26(s,3H),3.19-3.02(m,2H),2.91-2.74(m,2H),2.50(s,3H),2.13-1.86(m,2H),1.45-1.11(m,15H)。
实施例1.447
合成N-乙基-2-[(2-{4-[(1-羟基环丙基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物441)
通过用(1-((四氢-2H-吡喃-2-基)氧基)环丙基)甲醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇且用乙胺替换丙烷-2-胺,与化合物389类似地合成化合物441。LCMS(ES)[M+1]+m/z:398。1H NMR(400MHz,DMSO-d6)δ8.46(d,J=5.6Hz,1H),8.15(t,J=5.8Hz,1H),7.81(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),5.64(s,1H),4.17(s,2H),4.12(s,2H),3.31(s,3H),3.20-3.09(m,4H),2.82(t,J=7.9Hz,2H),2.03-1.95(m,2H),1.00(t,J=7.2Hz,3H),0.71(d,J=3.5Hz,2H),0.70-0.63(m,2H)。
实施例1.448
合成N-乙基-2-({2-[4-(2-乙基-2-羟基丁氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物442)
通过用2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁-1-醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇且用乙胺替换丙烷-2-胺,与化合物389类似地合成化合物442。LCMS(ES)[M+1]+m/z:428。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.18(t,J=5.7Hz,1H),7.80(d,J=2.5Hz,1H),7.05(dd,J=5.7,2.6Hz,1H),4.43(s,1H),4.17(s,2H),3.88(s,2H),3.28(s,3H),3.20-3.07(m,4H),2.82(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.62-1.46(m,4H),1.00(t,J=7.2Hz,3H),0.85(t,J=7.5Hz,6H)。
实施例1.449
合成2-({2-[4-(2-乙基-2-羟基丁氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-甲基乙酰胺(化合物443)
通过用2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁-1-醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇且用甲胺替换丙烷-2-胺,与化合物389类似地合成化合物443。LCMS(ES)[M+1]+m/z:414。1H NMR(400MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.14(s,1HCOOH),8.12(d,J=4.9Hz,1H),7.78(d,J=2.5Hz,1H),7.08-7.01(m,1H),4.42(s,1H),4.18(s,2H),3.89(s,2H),3.28(s,3H),3.16(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.63(d,J=4.5Hz,3H),2.04-1.94(m,2H),1.62-1.48(m,4H),0.86(t,J=7.5Hz,6H)。
实施例1.450
合成2-[(2-{4-[(4-羟基氧杂环己-4-基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)乙酰胺(化合物444)
通过用(4-(乙氧基甲氧基)四氢-2H-吡喃-4-基)甲醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物389类似地合成化合物444。LCMS(ES)[M+1]+m/z:456。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),8.15(s,1HCOOH),8.02(d,J=7.8Hz,1H),7.83(d,J=2.5Hz,1H),7.06(dd,J=5.7,2.6Hz,1H),4.79(s,1H),4.16(s,2H),3.93(s,2H),3.92-3.79(m,1H),3.67(dd,J=7.0,2.4Hz,4H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.85-1.67(m,2H),1.50(d,J=13.3Hz,2H),1.04(d,J=6.6Hz,6H)
实施例1.451
合成N-叔丁基-2-[(2-{4-[(2R)-2-羟基-2-甲基丁氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物445)
通过用(2S)-2-苯基丙酸(2R)-2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丁酯替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物174类似地合成化合物445。LCMS(ES)[M+1]+m/z:442。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.4Hz,1H),7.82(d,J=2.7Hz,1H),7.67(s,1H),7.07(dd,J=5.4,2.4Hz,1H),4.55(s,1H),4.14(s,2H),3.90(q,J=12.0,9.3Hz,2H),3.27(s,3H),3.14(d,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.01-1.96(m,2H),1.57(q,J=7.5Hz,2H),1.25(s,9H),1.19(s,3H),0.88(t,J=7.5Hz,3H)。
实施例1.452
合成N-叔丁基-2-[(2-{4-[(2R)-2-羟基-2-甲基丁氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物446)
通过用(2S)-2-苯基丙酸(2R)-2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丁酯替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物174类似地合成化合物446。LCMS(ES)[M+1]+m/z:442。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.4Hz,1H),7.82(d,J=2.7Hz,1H),7.67(s,1H),7.07(dd,J=5.4,2.4Hz,1H),4.55(s,1H),4.14(s,2H),3.90(q,J=12.0,9.3Hz,2H),3.27(s,3H),3.17(s,1H),3.14(d,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),1.99(p,J=7.7Hz,2H),1.57(q,J=7.5Hz,2H),1.25(s,9H),1.19(s,3H),0.88(t,J=7.5Hz,3H)。
实施例1.453
合成N-乙基-2-[(2-{4-[(4-羟基氧杂环己-4-基)甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物447)
通过用(4-(乙氧基甲氧基)四氢-2H-吡喃-4-基)甲醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇且用乙胺替换丙烷-2-胺,与化合物389类似地合成化合物447。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),8.18(t,J=5.6Hz,1H),7.82(d,J=2.5Hz,1H),7.07(dd,J=5.7,2.6Hz,1H),4.80(s,1H),4.18(s,2H),3.94(s,2H),3.76-3.63(m,4H),3.29(s,3H),3.21-3.05(m,4H),2.83(t,J=7.8Hz,2H),2.05-1.95(m,2H),1.76(dt,J=13.4,8.3Hz,2H),1.51(d,J=13.3Hz,2H),1.01(t,J=7.2Hz,3H)。
实施例1.454
合成2-[(2-{4-[(2R)-2-羟基-3-甲氧基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)乙酰胺(化合物448)
通过用(2S)-3-甲氧基-2-(氧杂环己-2-基氧基)丙-1-醇替换2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇,与化合物389类似地合成化合物448。LCMS(ES)[M+1]+m/z:430。1HNMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),8.01(d,J=7.8Hz,1H),7.82(d,J=2.5Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),5.19(d,J=5.0Hz,1H),4.16(s,2H),4.13-3.92(m,3H),3.86(dt,J=13.5,6.8Hz,1H),3.48-3.38(m,2H),3.30(s,3H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.04-1.96(m,2H),1.05(d,J=6.5Hz,6H)。
实施例1.455
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-6,6-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(丙-2-基)乙酰胺(化合物449)
通过用4,4-二甲基-2-氧代环戊烷-1-甲酸酯替换2-氧代环戊烷-1-甲酸甲酯,与化合物389类似地合成化合物449。LCMS(ES)[M+1]+m/z:442。1HNMR(400MHz,DMSO-d6)δ8.47(d,J=5.5Hz,1H),8.00(d,J=7.8Hz,1H),7.81(d,J=2.6Hz,1H),7.04(dd,J=5.7,2.7Hz,1H),4.70(s,1H),4.13(s,2H),3.92-3.82(m,3H),3.24(s,3H),2.95(s,2H),2.66(s,2H),1.24(s,6H),1.15(s,6H),1.05(d,J=6.6Hz,6H)。
实施例1.456
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-7,7-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(丙-2-基)乙酰胺(化合物450)
通过用3,3-二甲基-2-氧代环戊烷-1-甲酸酯替换2-氧代环戊烷-1-甲酸甲酯,与化合物389类似地合成化合物450。LCMS(ES)[M+1]+m/z:442。1HNMR(300MHz,DMSO-d6)δ8.50(d,J=5.6Hz,1H),8.02(d,J=7.8Hz,1H),7.81(d,J=2.5Hz,1H),7.06(dd,J=5.7,2.6Hz,1H),4.73(s,1H),4.16(s,2H),3.95-3.80(m,3H),3.28(s,3H),3.10(t,J=7.0Hz,2H),1.87(t,J=7.0Hz,2H),1.23(d,J=5.9Hz,12H),1.05(d,J=6.6Hz,7H)。
实施例1.457
合成N-叔丁基-2-[(2-{4-[(2S)-2,3-二羟基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物451)
通过用N-叔丁基-2-{[2-(4-{[(4R)-2,2-二甲基-1,3-二氧杂环戊-4-基]甲氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺替换N-叔丁基-2-{[2-(4-{[(4S)-2,2-二甲基-1,3-二氧杂环戊-4-基]甲氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺,与化合物415类似地合成化合物451。LCMS(ES)[M+1]+m/z:430.2。1H NMR(400MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.85(d,J=2.5Hz,1H),7.68(s,1H),7.05(dd,J=5.7,2.6Hz,1H),5.00(d,J=5.1Hz,1H),4.76-4.67(m,1H),4.18-4.10(m,3H),4.02(dd,J=10.0,6.0Hz,1H),3.86-3.79(m,1H),3.50-3.44(m,2H),3.26(s,3H),3.16-3.10(m,2H),2.84-2.78(m,2H),2.03-1.94(m,2H),1.24(s,9H)。
实施例1.458
合成N-叔丁基-2-[(2-{4-[(2S)-3-氟-2-羟基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物452)
流程134
步骤1
将(2S)-2-环氧乙烷基甲醇(28mg;0.38mmol;1.1当量)溶解于N,N-二甲基甲酰胺(1.5ml)中且于冰浴中冷却。添加氢化钠(60%,30mg;0.76mmol;2.2当量)。缓慢添加溶解于DMF(2ml)中的N-叔丁基-2-{[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(123mg;0.34mmol;1当量)(gcxy02152)且在25℃下搅拌反应物18h。小心地添加水(20ml)且用乙酸乙酯(3×25ml)萃取混合物。将合并的有机相饱和氯化钠溶液洗涤且经硫酸钠干燥。蒸发后,通过反相色谱(Waters XSelect CSH C18柱,0-70%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈灰白色固体的N-叔丁基-2-[甲基(2-{4-[(2R)-环氧乙烷-2-基甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(35mg,25%)。LCMS(ES+):[M+H]+=412.1。
步骤2
将N-叔丁基-2-[甲基(2-{4-[(2R)-环氧乙烷-2-基甲氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(40mg;0.1mmol;1当量)悬浮于甲苯(5ml)中。缓慢添加氟化四丁铵(0.49mL;1mol/L THF;0.49mmol;5当量)。使反应物于沙浴中升温至80℃,保持3h。蒸发溶剂且通过反相色谱(Waters XSelect CSH C18柱,0-60%乙腈/0.1%甲酸水溶液梯度)纯化残余物,得到呈白色固体的N-叔丁基-2-[(2-{4-[(2S)-3-氟-2-羟基丙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(18mg,43%)。LCMS(ES+):[M+H]+=432.1。1H NMR(400MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.85(d,J=2.5Hz,1H),7.68(s,1H),7.06(dd,J=5.6,2.6Hz,1H),5.52(s,1H),4.62-4.53(m,1H),4.50-4.41(m,1H),4.15-4.04(m,5H),3.26(s,3H),3.16-3.11(m,3H),2.84-2.77(m,2H),2.03-1.94(m,2H),1.24(s,9H)。
实施例1.459
合成(2R)-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(丙-2-基)丙酰胺(化合物453)
通过用(2R)-N-异丙基-2-(甲基氨基)丙烯酰胺替换N-异丙基-2-(甲基氨基)乙酰胺盐酸盐,与化合物389类似地合成化合物453。LCMS(ES)[M+1]+m/z:428。1H NMR(400MHz,DMSO-d6)δ8.50(d,J=5.6Hz,1H),8.27(d,J=8.0Hz,1H),7.88(d,J=2.6Hz,1H),7.07(dd,J=5.7,2.6Hz,1H),5.11(q,J=7.0Hz,1H),4.70(s,1H),3.89(s,2H),4-3.85(m,1H),3.28-3.16(m,1H),3.11-3.04(m,4H),2.96-2.77(m,2H),2.10-1.92(m,2H),1.34(d,J=7.0Hz,3H),1.24(s,6H),1.09(d,J=6.6Hz,3H),0.90(d,J=6.5Hz,3H)。
实施例1.460
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-6,6-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物454)
通过用4,4-二甲基-2-氧代环丙烷-1-甲酸酯替换2-氧代环丙烷-1-甲酸甲酯,与化合物348类似地合成化合物454。LCMS(ES)[M+1]+m/z:455。1H NMR(400MHz,DMSO-d6)δ8.47(d,J=5.7Hz,1H),7.83(d,J=2.6Hz,1H),7.65(s,1H),7.05(dd,J=5.7,2.7Hz,1H),4.20(t,J=5.7Hz,2H),4.10(s,2H),3.24(s,3H),2.95(s,2H),2.70-2.63(m,4H),2.23(s,6H),1.25(s,9H),1.15(s,6H)。
实施例1.461
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-6,6-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)乙酰胺(化合物455)
通过用4,4-二甲基-2-氧代环丙烷-1-甲酸酯替换2-氧代环丙烷-1-甲酸甲酯且用丙-2-胺替换叔丁胺,与化合物348类似地合成化合物455。LCMS(ES)[M+1]+m/z:441。1H NMR(400MHz,DMSO-d6)δ8.47(d,J=5.5Hz,1H),8.21(s,2HCOOH),7.97(d,J=7.9Hz,1H),7.80(d,J=2.6Hz,1H),7.05(dd,J=5.7,2.6Hz,1H),4.20(t,J=5.7Hz,2H),4.12(s,2H),3.92-3.83(m,1H),3.24(s,3H),2.95(s,2H),2.72-2.64(m,4H),2.24(s,6H),1.15(s,6H),1.05(d,J=6.6Hz,6H)。
实施例1.462
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-7,7-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(丙-2-基)乙酰胺(化合物456)
通过用3,3-二甲基-2-氧代环丙烷-1-甲酸酯替换2-氧代环丙烷-1-甲酸甲酯且用丙-2-胺替换叔丁胺,与化合物348类似地合成化合物456。LCMS(ES)[M+1]+m/z:441。1H NMR(300MHz,DMSO-d6,ppm):δ8.50(d,J=5.6Hz,1H),8.00(d,J=7.8Hz,1H),7.81(d,J=2.5Hz,1H),7.07(dd,J=5.7,2.6Hz,1H),4.19(t,J=5.7Hz,2H),4.14(s,2H),3.87(dq,J=13.3,6.6Hz,1H),3.28(s,3H),3.10(t,J=7.0Hz,2H),2.66(t,J=5.7Hz,2H),2.23(s,6H),1.87(t,J=7.0Hz,2H),1.22(s,6H),1.05(d,J=6.6Hz,6H)。
实施例1.463
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-7,7-二甲基-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物457)
通过用3,3-二甲基-2-氧代环丙烷-1-甲酸酯替换2-氧代环丙烷-1-甲酸甲酯,与化合物348类似地合成化合物457。LCMS(ES)[M+1]+m/z:441。1HNMR(300MHz,DMSO-d6,ppm):δ8.51(d,J=5.6Hz,1H),7.84(d,J=2.5Hz,1H),7.69(s,1H),7.08(dd,J=5.7,2.6Hz,1H),4.22(t,J=5.7Hz,2H),4.13(s,2H),3.28(s,3H),3.12(t,J=7.0Hz,2H),2.68(t,J=5.7Hz,2H),2.23(s,6H),1.89(t,J=7.0Hz,2H),1.25(s,9H),1.22(s,6H)。
实施例1.464
合成N-[(2R)-1-羟基丙-2-基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物458)
通过用(R)-2-氨基-1-丙醇替换氧杂环戊-3-胺,与化合物135类似地合成化合物458。LCMS(ES)[M+1]+m/z:372。1H NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),7.88(d,J=8.2Hz,1H),7.82(d,J=2.6Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),4.65(t,J=5.6Hz,1H),4.22(d,J=16.4Hz,1H),4.15(d,J=16.4Hz,1H),3.90(s,3H),3.80(p,J=6.8Hz,1H),3.39-3.32(m,1H),3.27(s,3H),3.21(q,J=5.4,4.6Hz,1H),3.16(q,J=7.4,5.5Hz,2H),2.82(t,J=7.9Hz,2H),2.02-1.95(m,2H),1.01(d,J=6.7Hz,3H)。
实施例1.465
合成N-[(2S)-1-羟基丙-2-基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物459)
通过用(S)-2-氨基-1-丙醇替换氧杂环戊-3-胺,与化合物135类似地合成化合物459。LCMS(ES)[M+1]+m/z:372。1H NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),7.88(d,J=8.1Hz,1H),7.82(d,J=2.6Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),4.65(t,J=5.6Hz,1H),4.22(d,J=16.4Hz,1H),4.14(d,J=16.4Hz,1H),3.89(s,3H),3.78(q,J=6.7Hz,1H),3.33(d,J=6.0Hz,1H),3.26(s,3H),3.25-3.11(m,3H),2.82(t,J=7.8Hz,2H),2.04-1.93(m,2H),1.00(d,J=6.7Hz,3H)。
实施例1.466
合成N-叔丁基-2-[甲基(2-{4-[2-(吗啉-4-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物460)
通过用4-吗啉乙醇替换二甲氨基乙醇,与化合物348类似地合成化合物460。LCMS(ES)[M+1]+m/z:469。1H NMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.6Hz,1H),7.84(d,J=2.5Hz,1H),7.68(s,1H),7.06(dd,J=5.7,2.6Hz,1H),4.24(t,J=5.6Hz,2H),4.13(s,2H),3.59(d,J=9.3Hz,4H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.88-2.67(m,4H),2.48(d,J=4.5Hz,4H),2.01-1.96(m,2H),1.25(s,9H)。
实施例1.467
合成N-叔丁基-2-{甲基[2-(4-{2-[(1S,4S)-2-氧杂-5-氮双环[2.2.1]庚-5-基]乙氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物461)
通过用(1S,4S)-2-氧杂-5-氮双环[2.2.1]庚烷盐酸盐替换双(甲基-d3)胺盐酸盐,与化合物508类似地合成化合物461。LCMS(ES)[M+1]+m/z:481。1H NMR(400MHz,DMSO-d6,ppm):δ8.47(d,J=5.5Hz,1H),8.16(s,2HCOOH),7.83(d,J=2.6Hz,1H),7.66(s,1H),7.05(dd,J=5.7,2.6Hz,1H),4.34(s,1H),4.17(t,J=5.7Hz,2H),4.13(s,2H),3.86(d,J=7.6Hz,1H),3.61-3.50(m,2H),3.26(s,3H),3.15(t,J=7.3Hz,2H),2.97(dq,J=11.6,6.6,6.2Hz,2H),2.92-2.88(m,1H),2.81(t,J=7.9Hz,2H),2.53(d,J=6.8Hz,1H),2.00-1.96(m,2H),1.74(d,J=9.4Hz,1H),1.60(d,J=9.6Hz,1H),1.25(s,9H)。
实施例1.468
合成N-叔丁基-2-{甲基[2-(4-{2-[(1R,4R)-2-氧杂-5-氮双环[2.2.1]庚-5-基]乙氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物462)
通过用2-[(1R,4R)-2-氧杂-5-氮双环[2.2.1]庚-5-基]乙醇替换二甲氨基乙醇,与化合物348类似地合成化合物462。LCMS(ES)[M+1]+m/z:481。1H NMR(400MHz,DMSO-d6,ppm):δ8.47(d,J=5.6Hz,1H),8.16(s,2HCOOH),7.83(d,J=2.5Hz,1H),7.67(s,1H),7.05(dd,J=5.7,2.5Hz,1H),4.35(s,1H),4.22-4.10(m,4H),3.86(d,J=7.6Hz,1H),3.59(s,1H),3.53(dd,J=7.6,1.8Hz,1H),3.26(s,3H),3.14(t,J=7.3Hz,2H),3.07-2.86(m,3H),2.81(t,J=7.8Hz,2H),2.55-2.50(m,1H),2.02-1.96(m,2H),1.75(dd,J=9.5,2.1Hz,1H),1.60(d,J=9.4Hz,1H),1.24(s,9H)。
实施例1.469
合成N-叔丁基-2-{[2-(4-{2-[(3R)-3-甲氧基吡咯烷-1-基]乙氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物463)
通过用(3R)-3-甲氧基吡咯烷盐酸盐替换双(甲基-d3)胺盐酸盐,与化合物508类似地合成化合物463。LCMS(ES)[M+1]+m/z:483。1H NMR(400MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),8.16(s,2HCOOH),7.84(d,J=2.6Hz,1H),7.67(s,1H),7.06(dd,J=5.7,2.6Hz,1H),4.23(t,J=5.6Hz,2H),4.13(s,2H),3.95-3.85(m,1H),3.27(s,3H),3.18(s,3H),3.14(7J=7.3Hz,2H),2.90(t,J=5.6Hz,2H),2.89-2.73(m,3H),2.77-2.52(m,3H),2.01-1.93(m,3H),1.73-1.53(m,1H),1.25(s,9H)。
实施例1.470
合成N-叔丁基-2-{[2-(4-{2-[(3S)-3-甲氧基吡咯烷-1-基]乙氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物464)
通过用(3S)-3-甲氧基吡咯烷盐酸盐替换双(甲基-d3)胺盐酸盐,与化合物508类似地合成化合物464。LCMS(ES)[M+1]+m/z:483。1H NMR(400MHz,DMSO-d6,ppm):δ8.49(d,J=5.6Hz,1H),8.15(s,1.5HCOOH),7.84(d,J=2.5Hz,1H),7.67(s,1H),7.07(dd,J=5.7,2.6Hz,1H),4.25(t,J=5.6Hz,2H),4.14(s,2H),3.94-3.89(m,1H),3.26(s,3H),3.18(s,3H),3.14(t,J=7.3Hz,2H),2.96(t,J=5.6Hz,2H),2.89(dd,J=10.5,6.1Hz,1H),2.83-2.77(m,3H),2.73(dd,J=10.5,3.0Hz,1H),2.69-2.62(m,1H),2.06-1.95(m,3H),1.75-1.68(m,1H),1.24(s,9H)。
实施例1.471
合成N-叔丁基-2-[(2-{4-[2-(1H-咪唑-1-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物465)
通过用1-(2-羟乙基)咪唑替换二甲氨基乙醇,与化合物348类似地合成化合物465。LCMS(ES)[M+1]+m/z:450。1H NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),7.82(d,J=2.6Hz,1H),7.75-7.63(m,2H),7.27(t,J=1.3Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),6.91(d,J=1.1Hz,1H),4.42(s,4H),4.14(s,2H),3.26(s,3H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.01-1.96(m,2H),1.23(s,10H)。
实施例1.472
合成N-叔丁基-2-[甲基(2-{4-[2-(1H-1,2,3,4-四唑-1-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物466)
通过用2-(1H-1,2,3,4-四唑-1-基)乙-1-醇替换二甲氨基乙醇,与化合物348类似地合成化合物466。LCMS(ES)[M+1]+m/z:452.2。1H NMR(400MHz,DMSO-d6,ppm):δ9.52(s,1H),8.54(d,J=5.7Hz,1H),7.84(d,J=2.6Hz,1H),7.71(s,1H),7.15(dd,J=5.8,2.6Hz,1H),4.96-4.91(m,2H),4.68-4.63(m,2H),4.17(s,2H),3.29(s,3H),3.17-3.12(m,2H),2.88-2.81(m,2H),2.04-1.96(m,2H),1.19(s,9H)。
实施例1.473
合成N-叔丁基-2-{[2-(4-乙氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物467)
通过用4-乙氧基-2-(三丁基锡烷基)吡啶替换4-甲氧基-2-(三甲基锡烷基)吡啶,与化合物34类似地合成化合物467。LCMS(ES+):[M+H]+=384.2。1H NMR(400MHz,DMSO-d6)δ8.48(d,J=5.7Hz,1H),7.86(d,J=2.5Hz,1H),7.72(s,1H),7.06(dd,J=5.7,2.6Hz,1H),4.19(q,J=7.0Hz,2H),4.13(s,2H),3.28(s,3H),3.19-3.11(m,2H),2.86-2.79(m,2H),2.04-1.94(m,2H),1.37(t,J=7.0Hz,3H),1.24(s,9H)。
实施例1.474
合成N-叔丁基-2-[甲基(2-{4-[2-(哒嗪-3-基氧基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物468)
通过用2-(哒嗪-3-基氧基)乙-1-醇替换二甲氨基乙醇,与化合物348类似地合成化合物468。LCMS(ES)[M+1]+m/z:478.2。1H NMR(400MHz,DMSO-d6,ppm):δ8.92(dd,J=4.5,1.3Hz,1H),8.50(d,J=5.6Hz,1H),7.91(d,J=2.6Hz,1H),7.68(s,1H),7.65(dd,J=8.9,4.5Hz,1H),7.26(dd,J=8.9,1.3Hz,1H),7.12(dd,J=5.7,2.6Hz,1H),4.83-4.78(m,2H),4.57-4.53(m,2H),4.10(s,2H),3.27(s,3H),3.17-3.12(m,2H),2.84-2.78(m,2H),2.03-1.94(m,2H),1.18(s,9H)。
实施例1.475
合成2-({2-[4-(2-乙基-2-羟基丁氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-[(1R,2S)-2-羟基环戊基]乙酰胺(化合物469)
流程135
步骤1
向20mL小瓶中放入NaH(60%于矿物油中)(68mg,1.71mmol,1.50当量)、DMSO(4.0mL),冷却至0℃后,添加2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁-1-醇(300mg,1.71mmol,1.50当量)且在室温下搅拌并搅拌0.5h。之后添加2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-醇(282mg,1.14mmol,1.00当量)。在40℃下搅拌所得溶液12h,将反应混合物冷却至室温且用H2O(1.0mL)淬灭,通过使用以下条件的制备型HPLC纯化所得溶液:Sunfire Prep C18 OBD柱,50*250mm,5μm,10nm,移动相A,水(0.05%NH3·H2O)及CH3CN(12min内自25%相B达至60%),检测器,220nm。获得305mg呈黄色油状物的2-(4-(2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-醇。LCMS(ES)[M+1]+m/z:414。
步骤2
向50mL三颈圆底烧瓶中放入2-(4-(2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-醇(305mg,0.74mmol,1.00当量)、DCM(10.00mL)及TEA(0.51mL,3.69mmol,5.00当量)。之后在0℃下添加三氟甲烷磺酸酐(0.14mL,0.96mmol,1.30当量)。在室温下搅拌所得溶液2h。将反应物用H2O(10mL)淬灭且用DCM(20mL×3)萃取。将有机层合并,经无水硫酸钠干燥且过滤。减压浓缩滤液,残余物不经进一步纯化即用于下一步骤中。由此产生763mg呈紫色油状物的粗物质三氟甲烷磺酸2-(4-(2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基酯。LCMS:(ES)[M+1]+m/z:546。
步骤3
向100mL圆底烧瓶中放入三氟甲烷磺酸2-(4-(2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基酯(763mg,1.40mmol,1.00当量)及DCM(10.0mL)。之后添加TEA(0.59mL,4.20mmol,3.00当量)及N-((1R,2S)-2-((叔丁基二苯基硅基)氧基)环戊基)-2-(甲基氨基)乙酰胺盐酸盐(874mg,1.96mmol,1.40当量)。在40℃下搅拌所得溶液12h。将反应物用H2O(20mL)淬灭,用DCM(20mL×2)萃取。将有机层合并,经无水硫酸钠干燥且过滤。减压浓缩滤液,残余物不经进一步纯化即用于下一步骤中。由此产生1.1g呈棕色油状物的粗物质N-((1R,2S)-2-((叔丁基二苯基硅基)氧基)环戊基)-2-((2-(4-(2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS:(ES)[M+1]+m/z:806。
步骤4
向100mL圆底烧瓶中放入N-((1R,2S)-2-((叔丁基二苯基硅基)氧基)环戊基)-2-((2-(4-(2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(1.10g,1.37mmol,1.00当量)、THF(10.00mL)及TBAF(0.37mL,1.37mmol,1.00当量)。在室温下搅拌反应溶液12h。减压浓缩所得溶液,通过使用以下条件的制备型HPLC纯化残余物:Welch-XB C18 50*250,10um,移动相A,水(0.05%NH3·H2O)及CH3CN(15min内自30%相B达至80%),检测器,220nm。获得268mg呈橙色固体的2-((2-(4-(2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-((1R,2S)-2-羟基环戊基)乙酰胺。LCMS(ES)[M+1]+m/z:568。
步骤5
向8mL小瓶中放入2-((2-(4-(2-乙基-2-((四氢-2H-吡喃-2-基)氧基)丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-((1R,2S)-2-羟基环戊基)乙酰胺(268mg,0.47mmol,1.00当量)、MeOH(3.0mL)及TsOH(81mg,0.47mmol,1.00当量)。在室温下搅拌混合物1h。通过使用以下条件的制备型HPLC纯化反应混合物:Welch-XB C1850*250,10um,移动相,水(0.5%NH3·H2O)及CH3CN/MeOH 1:1(15min内自25%相B达至75%),检测器,220nm。获得130mg呈白色固体的2-((2-(4-(2-乙基-2-羟基丁氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)-N-((1R,2S)-2-羟基环戊基)乙酰胺。LCMS(ES,m/z):[M+H]+:484。1H-NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),7.80(d,J=2.5Hz,1H),7.68(d,J=7.8Hz,1H),7.07(dd,J=5.6,2.6Hz,1H),4.69(d,J=3.8Hz,1H),4.44(s,1H),4.31(d,J=16.6Hz,1H),4.20(d,J=16.6Hz,1H),3.96-3.81(m,4H),3.26(s,3H),3.19-3.12(m,2H),2.85(t,J=7.8Hz,2H),2.04-1.94(m,2H),1.80-1.63(m,3H),1.59-1.35(m,7H),0.88(t,J=7.4Hz,6H)。
实施例1.476
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(2,2,2-三氟乙基)氨基]乙酰胺(化合物470)
流程136
步骤1
在0℃下向2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-醇(10g,40.375mmol,1.00当量)及TEA(8.17g,80.750mmol,2当量)于DCM(200mL)中的搅拌混合物中逐滴添加三氟甲烷磺酸(三氟甲烷)磺酰酯(22.78g,80.750mmol,2当量)。在室温下于氮气氛围下搅拌所得混合物4h。用CH2Cl2(3×300mL)萃取所得混合物。使合并的有机层经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用PE/EA(1:2)洗脱来纯化残余物,得到呈灰白色固体的三氟甲烷磺酸2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基酯(10g,65.22%)。LCMS(ES)[M+1]+m/z:380。
步骤2
在室温下向三氟甲烷磺酸2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基酯(3g,7.900mmol,1.00当量)及2,2,2-三氟乙胺(7.83g,79.000mmol,10当量)于DMF中的搅拌混合物中分批添加K2CO3(3.28g,23.700mmol,3当量)。用CH2Cl2(3×50mL)萃取所得混合物。使合并的有机层经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过使用以下条件的反相急骤色谱纯化残余物:柱,硅胶;移动相,MeCN/水(0.1%NH3),10%至60%梯度,20min,得到呈白色固体的2-(4-氯吡啶-2-基)-N-(2,2,2-三氟乙基)-5H,6H,7H-环戊并[d]嘧啶-4-胺(500mg,19.25%)。LCMS(ES)[M+1]+m/z:329。
步骤3
在0℃下于氮气氛围下向2-(4-氯吡啶-2-基)-N-(2,2,2-三氟乙基)-5H,6H,7H-环戊并[d]嘧啶-4-胺(400mg,1.217mmol,1.00当量)于DMF中的搅拌溶液中分批添加NaH(58.40mg,2.434mmol,2当量)。在0℃下于氮气氛围下搅拌所得混合物30min。在0℃下向以上混合物分批添加2-溴-N-叔丁基乙酰胺(354.23mg,1.826mmol,1.5当量)。在室温下再搅拌所得混合物4h。用CH2Cl2(3×30mL)萃取所得混合物。使合并的有机层经无水Na2SO4干燥且过滤。减压浓缩滤液。通过硅胶柱色谱,用CH2Cl2/MeOH(10:1)洗脱来纯化残余物,得到呈灰白色固体的N-叔丁基-2-{[2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](2,2,2-三氟乙基)氨基}乙酰胺(300mg,55.79%)。LCMS(ES)[M+1]+m/z:442。
步骤4
在100℃下向N-叔丁基-2-{[2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](2,2,2-三氟乙基)氨基}乙酰胺(130mg,0.294mmol,1.00当量)及二甲氨基乙醇(10mL)的搅拌溶液中分批添加CuCl2(3.96mg,0.029mmol,0.1当量)及K2CO3(81.32mg,0.588mmol,2当量)。用CH2Cl2(3×30mL)萃取所得混合物。使合并的有机层经无水Na2SO4干燥且过滤。减压浓缩滤液。通过使用以下条件的制备型HPLC(Sunfire Prep C18 XBridge柱,19*150mm;移动相A,水(0.05%NH3)及移动相B,AcCN(7min内自25%相B达至72%))纯化粗产物,得到呈白色固体的N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(2,2,2-三氟乙基)氨基]乙酰胺(49.3mg,33.88%)。LCMS(ES)[M+1]+m/z:495。1H NMR(400MHz,DMSO-d6)δ8.49(d,J=5.5Hz,1H),7.83(s,1H),7.68(s,1H),7.07(s,1H),4.59(q,J=9.2Hz,2H),4.27-4.17(m,4H),3.07(t,J=7.3Hz,2H),2.86(t,J=8.0Hz,2H),2.67(t,J=5.7Hz,2H),2.23(s,6H),2.05-1.97(m,2H),1.24(s,9H)。
实施例1.477
合成1-[(3R)-3-羟基吡咯烷-1-基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙-1-酮(化合物471)
通过用(3R)-吡咯烷-3-醇替换氧杂环戊-3-胺,与化合物135类似地合成化合物471。LCMS(ES)[M+1]+m/z:384。1H NMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.6Hz,1H),7.74(dd,J=4.2,2.6Hz,1H),7.02(dd,J=5.6,2.6Hz,1H),5.07(d,J=3.4Hz,1H),4.94(d,J=3.4Hz,1H),4.60-4.19(m,3H),3.88(s,3H),3.77-3.54(m,2H),3.50-3.36(m,1H),3.31-3.23(m,4H),3.14(t,J=7.4Hz,2H),2.81(t,J=7.9Hz,2H),2.05-1.78(m,4H)。
实施例1.478
合成1-[(3S)-3-羟基吡咯烷-1-基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙-1-酮(化合物472)
通过用(3S)-吡咯烷-3-醇替换氧杂环戊-3-胺,与化合物135类似地合成化合物472。LCMS(ES)[M+1]+m/z:384。1H NMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.6Hz,1H),7.74(dd,J=4.2,2.6Hz,1H),7.02(dd,J=5.6,2.6Hz,1H),5.07(d,J=3.5Hz,0.5H),4.94(d,J=3.5Hz,0.5H)4.60-4.21(m,3H),3.88(s,3H),3.75-3.51(m,2H),3.49-3.35(m,1H),3.32-3.21(m,4H),3.14(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.12-1.67(m,4H)。
实施例1.479
合成N-叔丁基-2-{[2-(4-{2-[(3R)-3-氟吡咯烷-1-基]乙氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物473)
通过用(3R)-3-氟吡咯烷盐酸盐替换双(甲基-d3)胺盐酸盐,与化合物508类似地合成化合物473。LCMS(ES)[M+1]+m/z:471。1H NMR(400MHz,DMSO-d6)δ8.48(d,J=5.5Hz,1H),7.84(d,J=2.5Hz,1H),7.67(s,1H),7.06(dd,J=5.7,2.6Hz,1H),5.20(dt,J=55.6,5.8Hz,1H),4.23(t,J=5.6Hz,2H),4.13(s,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.99-2.77(m,6H),2.79-2.63(m,1H),2.43(q,J=8.0Hz,1H),2.23-2.05(m,1H),2.04-1.78(m,3H),1.25(s,9H)。
实施例1.480
合成N-叔丁基-2-{[2-(4-{2-[(3S)-3-氟吡咯烷-1-基]乙氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物474)
通过用(3S)-3-氟吡咯烷盐酸盐替换双(甲基-d3)胺盐酸盐,与化合物508类似地合成化合物474。LCMS(ES)[M+1]+m/z:471。1H NMR(400MHz,DMSO-d6)δ8.48(d,J=5.4Hz,1H),8.16(s,1.3HCOOH)7.84(d,J=2.7Hz,1H),7.67(s,1H),7.06(dd,J=5.9,2.7Hz,1H),5.20(dt,J=55.8,5.8Hz,1H),4.23(t,J=5.7Hz,2H),4.13(s,2H),3.27(s,3H),3.15(t,J=7.4Hz,2H),3.00-2.77(m,6H),2.79-2.63(m,1H),2.43(q,J=7.9Hz,1H),2.23-2.04(m,1H),2.04-1.79(m,3H),1.25(s,9H)。
实施例1.481
合成N-叔丁基-2-[(2-{4-[3-(二甲基氨基)丙基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物475)
流程137
步骤1
在室温下向40mL小瓶中添加N-叔丁基-2-{[2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(415mg,1.11mmol,1.00当量)、二甲基(丙-2-炔-1-基)胺(185mg,2.23mmol,2.00当量)、DMF(10mL)、CuI(21mg,0.11mmol,0.10当量)、Et3N(337mg,3.33mmol,3.00当量)及Pd(PPh3)Cl2(79mg,0.11mmol,0.10当量)。在100℃下于氮气氛围下搅拌所得混合物3h。使反应物冷却至室温,通过使用以下条件的反相急骤色谱纯化残余物:C18-120g柱,移动相,相B,MeCN,相A,水,10%至50%梯度,10min,检测器,UV254nm。由此产生呈白色固体的N-(叔丁基)-2-((2-(4-(3-(二甲基氨基)丙-1-炔-1-基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(140mg,30%)。LCMS(ES,m/z):[M+H]+:421。
步骤2
在氢气氛围下于50mL压力槽反应器中向N-叔丁基-2-[(2-{4-[3-(二甲基氨基)丙-1-炔-1-基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(140mg,0.33mmol,1.00当量)于20mL MeOH中的溶液中添加Pd/C(10%,50mg)、Pd(OH)2/C(50mg)。将混合物于氢气氛围下在室温下搅拌1h,经由硅藻土垫过滤,且浓缩滤液。通过使用以下条件的制备型HPLC纯化粗产物:Sunfire Prep C18 OBD柱,50*250mm,5μm 10nm,移动相,水(0.1%FA)及CH3CN(保持5%相B 3min,在12min内达至23%),检测器,UV 254nm。由此产生呈棕色固体的N-(叔丁基)-2-((2-(4-(3-(二甲基氨基)丙基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(74.8mg,43%)。LCMS(ES,m/z):[M+H]+:425。1H-NMR(300MHz,DMSO-d6)δ8.55(d,J=4.9Hz,1H),8.23(s,2HCOOH),8.15(d,J=1.5Hz,1H),7.69(s,1H),7.31(dd,J=4.9,1.7Hz,1H),4.16(s,2H),3.27(s,3H),3.15(t,J=7.2Hz,2H),2.82(t,J=7.8Hz,2H),2.76-2.65(m,2H),2.48-2.37(m,2H),2.28(s,6H),2.07-1.91(m,2H),1.82(p,J=7.6Hz,2H),1.24(s,9H)。
实施例1.482
合成N-[2-(二甲基氨基)乙基]-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物476)
通过用(2-胺乙基)二甲基胺替换氧杂环戊-3-胺,与化合物135类似地合成化合物476。LCMS(ES)[M+1]+m/z:385。1H NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),8.06(t,J=5.8Hz,1H),7.81(d,J=2.6Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),4.18(s,2H),3.90(s,3H),3.27(s,3H),3.17(dq,J=8.2,5.6,4.1Hz,4H),2.82(t,J=7.8Hz,2H),2.23(t,J=6.8Hz,2H),2.07(s,6H),2.02-1.94(m,2H)。
实施例1.483
合成2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-1-(吗啉-4-基)乙-1-酮(化合物477)
通过用吗啉替换氧杂环戊-3-胺,与化合物135类似地合成化合物477。LCMS(ES)[M+1]+m/z:384。1H NMR(300MHz,DMSO-d6,ppm):δ8.49(d,J=5.6Hz,1H),7.78(d,J=2.6Hz,1H),7.06(dd,J=5.7,2.6Hz,1H),4.55(s,2H),3.90(s,3H),3.67-3.65(m,2H),3.58-3.53(m,4H),3.45-3.43(m,2H),3.28(s,3H),3.15(t,J=7.4Hz,2H),2.83(t,J=7.8Hz,2H),2.00(p,J=7.8Hz,2H)。
实施例1.484
合成2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]-N-(2,2,2-三氟乙基)乙酰胺(化合物478)
通过用三氟乙胺替换叔丁胺,与化合物348类似地合成化合物478。LCMS(ES+):[M+H]+=453.1。1H NMR(400MHz,dmso)δ8.93(t,J=6.4Hz,1H),8.46(d,J=5.6Hz,1H),7.77(d,J=2.5Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),4.28(s,2H),4.22(t,J=5.6Hz,2H),3.92(qd,J=9.8,6.3Hz,2H),3.29(s,3H),3.19-3.12(m,2H),2.86-2.79(m,2H),2.75(t,J=5.6Hz,2H),2.29(s,6H),2.04-1.94(m,2H)。
实施例1.485
合成2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-(2,2,2-三氟乙基)乙酰胺(化合物479)
通过用三氟乙胺替换叔丁胺,与化合物389类似地合成化合物479。LCMS(ES+):[M+H]+=454.1°1H NMR(400MHz,dmso)δ8.97(t,J=6.4Hz,1H),8.45(d,J=5.7Hz,1H),7.77(d,J=2.5Hz,1H),7.04(dd,J=5.6,2.6Hz,1H),4.77-4.62(m,1H),4.28(s,2H),3.92(qd,J=9.7,6.3Hz,2H),3.86(s,2H),3.29(s,3H),3.17-3.10(m,2H),2.86-2.77(m,2H),2.03-1.94(m,2H),1.22(s,6H)。
实施例1.486
合成N-叔丁基-2-[甲基(2-{4-[3-(甲基氨基)丙基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物480)
流程138
步骤1
向100mL圆底烧瓶中放入(3-羟丙基)(甲基)氨基甲酸叔丁酯(2.00g,10.60mmol,1.00当量)、DCM(20.00mL)及PPh3(3.67g,13.80mmol,1.30当量)。之后在0℃下添加CBr4(5.20g,13.80mmol,1.30当量)。在0℃下搅拌所得溶液1.5h。将反应混合物用H2O(50.00mL)淬灭,用DCM(100mL×2)萃取。将合并的有机相用Na2CO3(水溶液)、盐水洗涤且经无水硫酸钠干燥。过滤后,减压浓缩滤液。通过含石油醚/乙酸乙酯(93%/7%)的硅胶柱纯化残余物。由此产生2.6g呈淡黄色油状物的(3-溴丙基)(甲基)氨基甲酸叔丁酯。
步骤2
向用惰性氢气氛围吹扫及维持的40mL小瓶中放入DMAC(10mL)、甲吡啶脒盐酸盐(14mg,0.09mmol,0.05当量)、NiI2(28mg,0.09mmol,0.05当量)、碘化钠(71mg,0.47mmol,0.25当量)、(3-溴丙基)(甲基)氨基甲酸叔丁基酯(577mg,2.30mmol,1.20当量)、N-(叔丁基)-2-((2-(4-氯吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(700mg,1.88mmol,1.00当量)、金属锌粉(246mg,3.76mmol,2.00当量)及三氟乙酸(22mg,0.19mmol,0.10当量)。将反应混合物加热至60℃且搅拌12h。通过使用以下条件的制备型HPLC纯化反应混合物:Welch-XB C18 50*250,10um,移动相A,水(0.1%TFA)及CH3CN(12min内自13%相B达至47%),检测器,220nm。由此产生252mg呈淡黄色油状物的(3-(2-(4-((2-(叔丁基氨基)-2-氧代乙基)(甲基)氨基)-6,7-二氢-5H-环戊并[d]嘧啶-2-基)吡啶-4-基)丙基)(甲基)氨基甲酸叔丁酯。LCMS:(ES)[M+1]+m/z:511。
步骤3
向20mL小瓶中放入(3-(2-(4-((2-(叔丁基氨基)-2-氧代乙基)(甲基)氨基)-6,7-二氢-5H-环戊并[d]嘧啶-2-基)吡啶-4-基)丙基)(甲基)氨基甲酸叔丁酯(252mg,0.79mmol,1.00当量)、HCl(g)/MeOH(4M)(0.78mL)、DCM(3mL)。在室温下搅拌混合物12h。通过使用以下条件的制备型HPLC纯化反应混合物:Sunfire Prep C18 OBD柱,50*250mm,5μm,10nm,移动相,水(0.1%FA)及CH3CN(12min内自5%相B达至25%),检测器,220nm。获得169mg呈灰白色固体的N-(叔丁基)-2-(甲基(2-(4-(3-(甲基氨基)丙基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺。LCMS(ES,m/z):[M+H]+:411。1H NMR(300MHz,DMSO-d6,ppm):δ8.58(d,J=4.9Hz,1H),8.30(s,1.4HCOOH),8.17(s,1H),7.76(s,1H),7.33(dd,J=4.9,1.7Hz,1H),4.17(s,2H),3.26(s,3H),3.17(t,J=7.3Hz,2H),2.84-2.73(m,6H),2.49(s,3H),2.04-1.88(m,4H),1.24(s,9H)。
实施例1.487
合成N-叔丁基-2-({2-[4-(3-羟基-3-甲基丁基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物481)
通过用2-甲基-3-丁炔-2-醇替换二甲基(丙-2-炔-1-基)胺,与化合物475类似地合成化合物481。LCMS(ES)[M+1]+m/z:426。1H NMR(300MHz,DMSO-d6,ppm):δ8.53(d,J=4.9Hz,1H),8.16(s,0.7HCOOH),8.14(d,J=1.7Hz,1H),7.69(s,1H),7.28(dd,J=5.0,1.7Hz,1H),4.16(s,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.76-2.67(m,2H),2.07-1.91(m,2H),1.75-1.64(m,2H),1.24(s,9H),1.17(s,6H)。
实施例1.488
合成N-叔丁基-2-{[2-(4-羟基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物482)
流程139
向20mL小瓶中添加N-叔丁基-2-{[2-(4-甲氧基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(200mg,0.54mmol,1.00当量)及THF(5mL)。在氮气氛围下向以上混合物逐滴添加三仲丁基硼氢化锂(1.62mL,1.62mmol,3.00当量)。在60℃下再搅拌所得混合物3h。使混合物冷却至室温。将反应物用水(5mL)淬灭,真空浓缩以移除溶剂,通过使用以下条件的制备型HPLC纯化残余物:Sunfire Prep C18 OBD柱,50*250mm,5μm,10nm,移动相,水(0.05%NH3H2O)及CH3CN(15min内自10%达至70%),得到呈灰白色固体的N-叔丁基-2-{[2-(4-羟基吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(49.5mg,26%)。LCMS(ES,m/z):[M+H]+:356。1H-NMR(300MHz,DMSO-d6,ppm):δ7.71(s,1H),7.64(d,J=7.4Hz,1H),7.10(s,1H),6.14(d,J=7.4Hz,1H),4.13(s,2H),3.30(s,3H),3.16(t,J=7.3Hz,2H),2.84(t,J=7.8Hz,2H),2.02-1.97(m,2H),1.24(s,9H)。
实施例1.489
合成2-({2-[4-(2-氨基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)-N-叔丁基乙酰胺(化合物483)
通过用乙醇胺替换二甲氨基乙醇,与化合物348类似地合成化合物483。LCMS(ES)[M+1]+m/z:399。1H NMR(300MHz,DMSO-d6,ppm):δ8.75(d,J=6.0Hz,1H),8.20(br,3H),8.04(d,J=2.6Hz,1H),7.88(s,1H),7.47(dd,J=6.1,2.6Hz,1H),4.49(t,J=5.1Hz,2H),4.38(s,2H),3.42(s,3H),3.33(q,J=5.5Hz,2H),3.20(s,2H),3.02(t,J=7.9Hz,2H),2.18-2.00(m,2H),1.26(s,9H)。
实施例1.490
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物484)
通过用2-氨基-N-叔丁基乙酰胺盐酸盐替换N-(叔丁基)-2-(甲基氨基)乙酰胺盐酸盐,与化合物348类似地合成化合物484。LCMS(ES)[M+1]+m/z:413。1H NMR(300MHz,DMSO-d6,ppm):δ8.46(d,J=5.6Hz,1H),7.86(d,J=2.6Hz,1H),7.69(s,1H),7.14(t,J=5.8Hz,1H),7.04(dd,J=5.7,2.6Hz,1H),4.19(t,J=5.6Hz,2H),3.93(d,J=5.7Hz,2H),2.83(t,J=7.7Hz,2H),2.78-2.70(m,2H),2.66(t,J=5.6Hz,2H),2.23(s,6H),2.14-1.98(m,2H),1.25(s,9H)。
实施例1.491
合成N-叔丁基-2-[(2-{4-[2-(甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物485)
通过用2-氨基-N-叔丁基乙酰胺盐酸盐替换N-(叔丁基)-2-(甲基氨基)乙酰胺盐酸盐且用甲基乙醇胺替换二甲氨基乙醇,与化合物348类似地合成化合物485。LCMS(ES)[M+1]+m/z:399。1H NMR(300MHz,DMSO-d6,ppm):δ9.23(br,2H),8.69(d,J=5.9Hz,1H),8.41(br,1H),8.08(d,J=2.6Hz,1H),7.95(s,1H),7.38(dd,J=6.2,2.5Hz,1H),4.56(t,J=5.0Hz,2H),4.16(d,J=5.8Hz,2H),2.99(t,J=7.5Hz,2H),2.81(t,J=7.4Hz,2H),2.65(s,3H),2.19-2.09(m,2H),1.25(s,9H)。
实施例1.492
合成2-{[2-(4-{[(2R)-1-(二甲基氨基)丙-2-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}-N-[1-(三氟甲基)环丙基]乙酰胺(化合物486)
通过用(2R)-1-(二甲基氨基)丙-2-醇替换二甲氨基乙醇且用1-(三氟甲基)环丙-1-胺替换叔丁胺,与化合物348类似地合成化合物486。LCMS(ES)[M+1]+m/z:493。1H NMR(300MHz,DMSO-d6,ppm):δ9.02(s,1H),8.45(dd,J=5.7,1.7Hz,1H),8.17(s,1.7HCOOH),7.73(t,J=2.2Hz,1H),7.13-7.03(m,1H),4.86-4.80(m,J=7.9Hz,1H),4.16(s,2H),3.28(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.70-2.59(m,1H),2.52-2.49(m,1H),2.27(s,6H),2.04-1.94(m,2H),1.29(dd,J=6.1,1.6Hz,3H),1.22-1.15(m,2H),1.03-0.95(m,2H)。
实施例1.493
合成2-{甲基[2-(4-{[(3R)-1-甲基吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-[1-(三氟甲基)环丙基]乙酰胺(化合物487)
通过用(3R)-1-甲基吡咯烷-3-醇替换二甲氨基乙醇且用1-(三氟甲基)环丙-1-胺替换叔丁胺,与化合物348类似地合成化合物487。LCMS(ES)[M+1]+m/z:491。1H NMR(300MHz,DMSO-d6,ppm):δ9.02(s,1H),8.45(d,J=5.6Hz,1H),8.17(s,1HCOOH),7.68(d,J=2.5Hz,1H),6.99(dd,J=5.6,2.5Hz,1H),5.09-5.00(m,1H),4.18(s,2H),3.28(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=8.0Hz,3H),2.76-2.63(m,2H),2.42-2.31(m,2H),2.29(s,3H),2.06-1.93(m,2H),1.86-1.75(m,1H),1.24-1.13(m,2H),1.03-0.94(m,2H)。
实施例1.494
合成N-叔丁基-2-{[2-(4-{[(3R,5R)-1,5-二甲基吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物488)
通过用(3R,5R)-1,5-二甲基吡咯烷-3-醇替换二甲氨基乙醇,与化合物348类似地合成化合物488。LCMS(ES)[M+1]+m/z:453。1H NMR(300MHz,DMSO-d6,ppm):δ8.45(d,J=5.6Hz,1H),7.81(d,J=2.5Hz,1H),7.70(s,1H),6.99(dd,J=5.7,2.5Hz,1H),5.02-4.96(m,1H),4.11(s,2H),3.62(dd,J=10.2,6.6Hz,1H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.81(t,J=7.9Hz,2H),2.41(dt,J=11.4,6.0Hz,1H),2.28-2.24(m,1H),2.24(s,3H),2.05-1.91(m,3H),1.91-1.78(m,1H),1.26(s,9H),1.06(d,J=5.9Hz,3H)。
实施例1.495
合成N-叔丁基-2-{甲基[2-(4-{[(3R)-1-甲基哌啶-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物489)
通过用(3R)-1-甲基哌啶-3-醇替换二甲氨基乙醇,与化合物348类似地合成化合物489。LCMS(ES)[M+1]+m/z:453。1H NMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.7Hz,1H),8.18(s,1.7HCOOH),7.84(d,J=2.5Hz,1H),7.71(s,1H),7.09(dd,J=5.7,2.6Hz,1H),4.66(dt,J=8.0,4.1Hz,1H),4.11(s,2H),3.27(s,3H),3.14(t,J=7.3Hz,2H),2.93(dd,J=10.6,3.4Hz,1H),2.81(t,J=7.8Hz,2H),2.66-2.51(m,1H),2.28(s,3H),2.36-2.16(m,2H),2.05-1.92(m,3H),1.84-1.71(m,1H),1.69-1.55(m,1H),1.52-1.38(m,1H),1.25(s,9H)。
实施例1.496
合成N-叔丁基-2-{甲基[2-(4-{[(3S)-1-甲基哌啶-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(化合物490)
通过用(3S)-1-甲基哌啶-3-醇替换二甲氨基乙醇,与化合物348类似地合成化合物490。LCMS(ES)[M+1]+m/z:453。1H NMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.7Hz,1H),8.18(s,1.7HCOOH),7.84(d,J=2.5Hz,1H),7.71(s,1H),7.09(dd,J=5.7,2.6Hz,1H),4.66(dt,J=8.0,4.1Hz,1H),4.11(s,2H),3.27(s,3H),3.14(t,J=7.3Hz,2H),2.93(dd,J=10.6,3.4Hz,1H),2.81(t,J=7.8Hz,2H),2.66-2.51(m,1H),2.28(s,3H),2.36-2.16(m,2H),2.05-1.92(m,3H),1.84-1.71(m,1H),1.69-1.55(m,1H),1.52-1.38(m,1H),1.25(s,9H)。
实施例1.497
合成N-叔丁基-2-{[2-(4-{[(3R)-1-(2,2-二氟乙基)吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物491)
通过用(3R)-1-(2,2-二氟乙基)吡咯烷-3-醇替换二甲氨基乙醇,与化合物348类似地合成化合物491。LCMS(ES)[M+1]+m/z:489。1H NMR(300MHz,DMSO-d6,ppm):δ8.46(d,J=5.6Hz,1H),7.81(d,J=2.5Hz,1H),7.69(s,1H),7.00(dd,J=5.7,2.6Hz,1H),6.12(tt,J=55.8,4.2Hz,1H),5.06(dt,J=7.1,3.3Hz,1H),4.12(s,2H),3.27(s,3H),3.14(t,J=7.3Hz,2H),3.02(dd,J=10.7,6.0Hz,1H),2.95-2.74(m,6H),2.65-2.55(m,1H),2.34(dt,J=13.6,6.9Hz,1H),2.02 -1.95(m,2H),1.88-1.70(m,1H),1.25(s,9H)。
实施例1.498
合成N-叔丁基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5-氧代-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物492)
在低于10℃下于空气氛围下向N-叔丁基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(400mg,0.94mmol,1.00当量)于HOAc(1.5mL)及H2SO4(0.3mL)中的搅拌溶液中逐滴添加含CrO3(196mg,1.96mmol,2.0当量)的HOAc(2.0mL)及H2O(0.4mL)。在室温下搅拌所得混合物16h。用含(3N)NaOH的H2O将混合物碱化至pH约13,用CH2Cl2/MeOH=10:1(3×30mL)萃取。将合并的有机层用盐水(1×30mL)洗涤,经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过使用以下条件的制备型HPLC纯化残余物:C18 OBD柱,50*250mm,5μm,10nm,移动相,CH3CN/H2O(FA:0.1%),自5%至35%,12min,流动速率,80mL/min,检测器,UV 254nm。由此产生呈白色固体的N-叔丁基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5-氧代-6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(65mg,16%)。LCMS(ES,m/z):[M+H]+:442。1H-NMR(300MHz,DMSO-d6,ppm):δ8.55(d,J=5.6Hz,1H),7.92(d,J=2.5Hz,1H),7.74(s,1H),7.15(dd,J=5.6,2.6Hz,1H),4.72(s,1H),4.42(s,2H),3.89(s,2H),3.34(s,3H),3.12-2.97(m,2H),2.69-2.58(m,2H),1.25(s,6H),1.23(s,9H)。
实施例1.499
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5-羟基-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物493)
流程140
步骤1
在0℃下向N-叔丁基-2-{[2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(1.0g,2.67mmol,1.00当量)于t-BuOH(10.0mL)及H2O(2.0mL)中的搅拌混合物中分批添加MgSO4(0.97g,8.02mmol,3.00当量)及KMnO4(850mg,5.35mmol,2.00当量)在室温下搅拌所得溶液16h,过滤且浓缩,通过使用以下条件的制备型HPLC纯化残余物:Sunfire Prep C18 OBD柱,50*250mm,5μm,10nm,移动相,水(0.1%FA)及CH3CN(12min内自15%达至50%),检测器,UV 220nm,得到呈黄色固体的N-叔丁基-2-{[2-(4-氯吡啶-2-基)-5-氧代-6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(350mg,33.7%)。LCMS(ES)[M+1]+m/z:388。
步骤2
在0℃下于N2氛围下向N-叔丁基-2-{[2-(4-氯吡啶-2-基)-5-氧代-6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(300mg,0.77mmol,1.00当量)于MeOH(10mL)中的搅拌溶液中分批添加NaBH4(58mg,1.54mmol,2.00当量)。在相同温度下搅拌所得溶液1h。随后通过添加水/冰(10mL)将反应物淬灭,用EtOAc(30mL×5)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,减压浓缩滤液。由此产生呈黄色固体的N-叔丁基-2-{[2-(4-氯吡啶-2-基)-5-羟基-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(286mg,95%),其不经进一步纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:390。
步骤3
在室温下向N-叔丁基-2-{[2-(4-氯吡啶-2-基)-5-羟基-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(300mg,0.76mmol,1.00当量)于DMF(8mL)中的搅拌溶液中分批添加咪唑(157mg,2.31mmol,3.00当量)及TBSCl(232mg,1.53mmol,2.00当量)。在60℃下搅拌反应物16h。将反应物用室温下的水(10mL)淬灭,用EtOAc(3×30mL)萃取。将合并的有机层用盐水(20mL×1)洗涤,经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用THF/PE(1:100至1:1)洗脱来纯化残余物,得到呈灰白色固体的N-叔丁基-2-({5-[(叔丁基二甲基硅基)氧基]-2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(370mg,95%)。LCMS(ES)[M+1]+m/z:504。
步骤4
在15℃下向二甲氨基乙醇(124mg,1.39mmol,2.00当量)于DMSO(5.0mL)中的溶液中添加氢化钠(60%于矿物油中,55mg,1.39mmol,2.00当量)。在15至25℃下搅拌反应物1h,一次性添加N-叔丁基-2-({5-[(叔丁基二甲基硅基)氧基]-2-(4-氯吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(350mg,0.69mmol,1.00当量)。随后在40℃下再搅拌所得混合物2h。使反应物冷却至室温且通过使用如下条件的制备型HPLC纯化:KinetexEVO C18柱,21.2*150,5um,移动相A,水(0.1%FA)及移动相B,CH3CN(15min内自10%相B达至50%),检测器,UV 254nm,得到呈灰白色固体的N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5-羟基-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(72mg,23.43%)。LCMS(ES)[M+1]+m/z:443。1H NMR(400MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.84(d,J=2.5Hz,1H),7.68(s,1H),7.07(dd,J=5.7,2.5Hz,1H),5.32(d,J=7.1Hz,1H),5.27-5.20(m,1H),4.34-4.09(m,4H),3.36(s,3H),3.04(dt,J=16.9,8.4Hz,1H),2.66(t,J=5.6Hz,3H),2.23(s,6H),2.25-2.15(m,1H),1.93(dd,J=13.6,8.2Hz,1H),1.25(s,9H)。
实施例1.500
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-7-羟基-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物494)
流程141
步骤1
在室温下250mL圆底烧瓶中添加2,4-二氯-5H,6H,7H-环戊并[d]嘧啶(6.0g,31.74mmol,1.00当量)、HOAc(60mL)及Pb(OAc)4(28.2g,63.60mmol,2.00当量)。将混合物加热至120℃且搅拌16h。在室温下添加另一批Pb(OAc)4(28.2g,63.60mmol,2.00当量)且在120℃下搅拌16h。将反应物冷却至室温且减压浓缩以移除溶剂。通过使用以下条件的反相急骤色谱纯化残余物:柱,C18-120g,移动相,MeCN/水,10%至50%梯度,10min;检测器,UV254nm。冷冻干燥目标的洗脱份,由此产生呈棕色固体的乙酸2,4-二羟基-6,7-二氢-5H-环戊并[d]嘧啶-7-基酯(1.4g,21%)。LCMS(ES)[M+1]+m/z:211。
步骤2
在室温下向250mL圆底烧瓶中添加乙酸2,4-二羟基-6,7-二氢-5H-环戊并[d]嘧啶-7-基酯(1.4g,6.66mmol,1.00当量)、DCE(20mL)、TEA(1.35g,13.34mmol,2.00当量)及POCl3(20.4g,133.04mmol,20.00当量)。在90℃下搅拌所得混合物2h。减压浓缩所得混合物。将残余物用DCM(100mL)稀释,用水(50mL)淬灭,用CH2Cl2(50mL×1)萃取,经无水硫酸钠干燥。过滤后,减压浓缩滤液,通过硅胶柱色谱,用PE/EA(3:1)洗脱来纯化残余物,得到呈黄色油状物的乙酸2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶-7-基酯(1.3g,79%)。LCMS(ES)[M+1]+m/z:247。
步骤3
在室温下向40mL小瓶中添加乙酸2,4-二氯-6,7-二氢-5H-环戊并[d]嘧啶-7-基酯(1.3g,5.26mmol,1.00当量)、NMP(15mL)、DIEA(2.04g,15.78mmol,3.00当量)及N-叔丁基-2-(甲基氨基)乙酰胺盐酸盐(1.43g,7.92mmol,1.50当量)。在60℃下搅拌所得混合物2h。将反应物冷却至室温,用水(20mL)淬灭,用EtOAc(30mL×3)萃取水层。将合并的有机相用盐水(20mL×3)洗涤,经无水硫酸钠干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用PE/EA(1:1)洗脱来纯化残余物,得到呈黄色固体的乙酸4-((2-(叔丁基氨基)-2-氧代乙基)(甲基)氨基)-2-氯-6,7-二氢-5H-环戊并[d]嘧啶-7-基酯(1.5g,80%)。LCMS(ES)[M+1]+m/z:355。
步骤4
在室温下向50mL圆底烧瓶中添加乙酸4-((2-(叔丁基氨基)-2-氧代乙基)(甲基)氨基)-2-氯-6,7-二氢-5H-环戊并[d]嘧啶-7-基酯(1.5g,4.23mmol,1.00当量)、THF(18mL)、LiOH(0.20g,8.45mmol,2.00当量)及H2O(9mL)。在室温下搅拌所得混合物1h。将反应物用水(30mL)稀释,用EtOAc(30mL×2)萃取。合并的有机相经无水钠干燥,过滤,且减压浓缩滤液。粗产物不经进一步纯化即直接用于下一步骤中。LCMS(ES)[M+1]+m/z:313。
步骤5
在室温下向50mL圆底烧瓶中添加N-(叔丁基)-2-((2-氯-7-羟基-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(1.2g,3.84mmol,1.00当量)、DCM(15mL)、咪唑(0.52g,7.67mmol,2.00当量)及TBSCl(0.69g,4.60mmol,1.20当量)。在室温下搅拌所得混合物12h。用水(30mL)淬灭反应物,用EtOAc(50mL×2)萃取水层。通过硅胶柱色谱,用PE/EA(10:1)洗脱来纯化残余物,得到呈白色固体的N-(叔丁基)-2-((7-((叔丁基二甲基硅基)氧基)-2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(1.3g,79%)。LCMS(ES)[M+1]+m/z:427。
步骤6
在室温下向40mL小瓶中添加N-(叔丁基)-2-((7-((叔丁基二甲基硅基)氧基)-2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(1.3g,3.05mmol,1.00当量)、甲苯(20mL)、4-氟-2-(三丁基锡烷基)吡啶(1.88g,4.87mmol,1.60当量)及Pd(PPh3)4(350mg,0.30mmol,0.10当量)。在120℃下于氮气氛围下搅拌所得混合物12h。将反应物冷却至室温,减压浓缩。通过硅胶柱色谱,用乙酸乙酯洗脱来纯化残余物,得到呈黄色固体的N-(叔丁基)-2-((7-((叔丁基二甲基硅基)氧基)-2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(900mg,61%)。LCMS(ES)[M+1]+m/z:488。
步骤7
向20mL小瓶中添加二甲氨基乙醇(158mg,1.77mmol,2.00当量)、DMSO(7mL)、NaH(60%于矿物油中)(71mg,1.78mmol,2.00当量)。在室温下搅拌所得混合物30min。在室温下向以上混合物添加N-叔丁基-2-({7-[(叔丁基二甲基硅基)氧基]-2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(432mg,0.89mmol,1.00当量)。在室温下再搅拌所得混合物4h。将反应物用水(0.5mL)淬灭且通过使用以下条件的制备型HPLC纯化:XBridge Shield RP18OBD柱,19*150mm,5μm;移动相,水(0.05%NH3.H2O)及CH3CN(8min内自16%达至33%)。由此产生呈灰白色固体的N-(叔丁基)-2-((2-(4-(2-(二甲基氨基)乙氧基)吡啶-2-基)-7-羟基-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(57mg,14.54%)。LCMS(ES,m/z):[M+H]+:443。1H-NMR(300MHz,DMSO-d6)δ8.48(d,J=5.6Hz,1H),7.87(d,J=2.6Hz,1H),7.70(s,1H),7.07(dd,J=5.7,2.6Hz,1H),5.44(s,1H),4.82(t,J=6.5Hz,1H),4.20(t,J=5.7Hz,2H),4.14(s,2H),3.29(s,3H),3.18(ddd,J=13.8,8.4,4.4Hz,1H),2.99(dt,J=15.1,7.1Hz,1H),2.67(t,J=5.6Hz,2H),2.28(dt,J=7.5,4.9Hz,1H),2.23(s,6H),1.77(dt,J=13.6,6.8Hz,1H),1.25(s,9H)。
实施例1.501
合成N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[b]吡啶-4-基)(甲基)氨基]乙酰胺(化合物495)
流程142
步骤1
向50mL圆底烧瓶中添加2,4-二氯-5H,6H,7H-环戊并[b]吡啶(500.00mg,2.66mmol,1.00当量)、4-氟-2-(三丁基锡烷基)吡啶(1129.37mg,2.93mmol,1.10当量)、DMF(25.00mL)、CsF(807.78mg,5.32mmol,2.00当量)、CuI(50.64mg,0.27mmol,0.10当量)及Pd(PPh3)4(307.25mg,0.27mmol,0.10当量)。在110℃下于氮气氛围下搅拌所得混合物过夜。使混合物冷却至室温。用水/冰淬灭反应物。用EA(3×30mL)萃取所得混合物。将合并的有机层用盐水(3×100mL)洗涤,经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用THF/PE(5%)洗脱来纯化残余物,得到呈白色固体的2-{4-氯-5H,6H,7H-环戊并[b]吡啶-2-基}-4-氟吡啶(185.00mg,27.98%)。LCMS(ES)[M+1]+m/z:249。
步骤2
向40mL小瓶中添加二甲氨基乙醇(1290.35mg,14.48mmol,20.00当量)及DMF(20.00mL)。在0℃下向以上溶液分批添加NaH(60%)(86.85mg,2.172mmol,3.00当量)。在室温下再搅拌所得混合物30min。在室温下向以上混合物中分批添加2-{4-氯-5H,6H,7H-环戊并[b]吡啶-2-基}-4-氟吡啶(180.00mg,0.72mmol,1.00当量)。在50℃下再搅拌所得混合物1h。使混合物冷却至室温且用饱和NH4Cl(水溶液)淬灭。用DCM:MeOH(10:1)(3×30mL)萃取水层。使合并的有机层经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用DCM/MeOH(10%)洗脱来纯化残余物,得到呈黄色固体的{2-[(2-{4-氯-5H,6H,7H-环戊并[b]吡啶-2-基}吡啶-4-基)氧基]乙基}二甲胺(145.00mg,63.03%)。LCMS(ES)[M+1]+m/z:318。
步骤3
向40mL小瓶中添加{2-[(2-{4-氯-5H,6H,7H-环戊并[b]吡啶-2-基}吡啶-4-基)氧基]乙基}二甲胺(140.00mg,0.44mmol,1.00当量)、N-叔丁基-2-(甲基氨基)乙酰胺盐酸盐(79.59mg,0.44mmol,1.00当量)、BINAP(54.86mg,0.09mmol,0.20当量)、Cs2CO3(287.05mg,0.88mmol,2.00当量)、1,4-二噁烷(14.00mL)及Pd(OAc)2(9.89mg,0.04mmol,0.10当量)。在100℃下于氮气氛围下搅拌所得混合物1h。使混合物冷却至室温且用水/冰淬灭。用DCM:MeOH(10:1)(3×30mL)萃取水层。使合并的有机层经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过使用以下条件的制备型HPLC纯化粗产物:柱,Sunfire Prep C18 OBD柱,50*250mm5um 10nm;移动相,水(0.1%FA)及ACN(13min内自5%相B达至20%);检测器,254。由此产生呈黄色胶状物的N-叔丁基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[b]吡啶-4-基)(甲基)氨基]乙酰胺;双(甲酸)(132.50mg,58.11%)。LCMS(ES,m/z):[M+H]+:426。1H-NMR(300MHz,DMSO-d6,ppm):δ8.43(d,J=5.6Hz,1H),8.18(s,2HCOOH),7.86(d,J=2.5Hz,1H),7.57(s,1H),7.54(s,1H),6.97(dd,J=5.9,2.6Hz,1H),4.24(t,J=5.5Hz,2H),3.94(s,2H),3.06(s,3H),3.01(t,J=7.3Hz,2H),2.85(t,J=7.6Hz,2H),2.79(t,J=5.8Hz,2H),2.32(s,6H),2.02-1.97(m,2H),1.27(s,9H)。
实施例1.502
合成N-叔丁基-2-{[2-(4-{[(3R)-1-乙基吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物496)
通过用(3R)-1-乙基吡咯烷-3-醇替换二甲氨基乙醇,与化合物348类似地合成化合物496。LCMS(ES)[M+1]+m/z:453。1H NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.7Hz,1H),8.28(br,HCOOH),7.82(d,J=2.4Hz,1H),7.72(s,1H),7.02(dd,J=5.7,2.7Hz,1H),5.14-5.08(m,1H),4.12(s,2H),3.27(s,3H),3.14(t,J=2.4Hz,2H),3.06(dd,J=11.1,5.7Hz,1H),2.92-2.78(m,4H),2.67-2.60(m,3H),2.42-2.30(m,1H),2.04-1.82(m,3H),1.25(s,9H),1.08(t,J=7.2Hz,3H)。
实施例1.503
合成N-叔丁基-2-{[2-(4-{[(3R)-1-(2-氟乙基)吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物497)
通过用(3R)-1-(2-氟乙基)吡咯烷-3-醇替换二甲氨基乙醇,与化合物348类似地合成化合物497。LCMS(ES)[M+1]+m/z:471。1H NMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.6Hz,1H),8.17(1.60HCOOH),7.83(d,J=2.5Hz,1H),7.72(s,1H),7.01(dd,J=5.7,2.6Hz,1H),5.11-5.01(m,1H),4.61(t,J=4.9Hz,1H),4.46(t,J=4.9Hz,1H),4.12(s,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.97(dd,J=10.7,6.0Hz,1H),2.88-2.73(m,5H),2.71(t,J=4.9Hz,1H),2.60-2.46(m,1H),2.43-2.25(m,1H),2.01-1.96(m,2H),1.89-1.74(m,1H),1.25(s,9H)。
实施例1.504
合成N-叔丁基-2-[甲基({2-[4-(甲基硫基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基})氨基]乙酰胺(化合物498)
通过用MeSNa替换二甲氨基乙醇,与化合物348类似地合成化合物498。LCMS(ES)[M+1]+m/z:386。1H NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.2Hz,1H),8.15(d,J=1.8Hz,1H),7.68(s,1H),7.30(dd,J=5.3,2.0Hz,1H),4.14(s,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.58(s,3H),2.08-1.86(m,2H),1.25(s,9H)。
实施例1.505
合成N-叔丁基-2-{[2-(4-{[2-(二甲基氨基)乙基]硫基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物499)
通过用2-(二甲基氨基)乙硫醇替换二甲氨基乙醇,与化合物348类似地合成化合物499。LCMS(ES)[M+1]+m/z:443。1H NMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.2Hz,1H),8.16(s,0.5HCOOH),8.15(d,J=2.5Hz1H),7.67(s,1H),7.33(dd,J=5.3,2.0Hz,1H),4.14(s,2H),3.26(s,3H),3.25-3.20(m,2H),3.13(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.58(t,J=7.0Hz,2H),2.23(s,6H),2.01-1.96(m,2H),1.25(s,9H)。
实施例1.506
合成N-环丙基-2-[(2-{4-[2-(二甲基氨基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)(甲基)氨基]乙酰胺(化合物500)
通过用1-环丙胺替换叔丁胺,与化合物348类似地合成化合物500。LCMS(ES)[M+1]+m/z:411。1H NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),8.24(d,J=4.1Hz,1H),7.80(d,J=2.5Hz,1H),7.05(dd,J=5.7,2.6Hz,1H),4.26(t,J=5.5Hz,2H),4.13(s,2H),3.27(s,3H),3.14(t,J=7.3Hz,2H),2.89-2.76(m,4H),2.63(tq,J=8.3,4.8Hz,1H),2.36(s,6H),2.04-1.94(m,2H),0.67-0.50(m,2H),0.47-0.36(m,2H)。
实施例1.507
合成N-叔丁基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-7-氧代-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物501)
流程143
步骤1
在室温下向40mL小瓶中添加2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇(643mg,3.69mmol,2.00当量)、DMSO(16mL)及NaH(60%于矿物油中)(148mg,3.70mmol,2.00当量)。在室温下搅拌所得混合物30min。在室温下向以上混合物添加N-(叔丁基)-2-((7-((叔丁基二甲基硅基)氧基)-2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(900mg,1.84mmol,1.00当量)。在室温下再搅拌所得混合物2h。将反应物用水(2mL)淬灭且通过使用以下条件的反相急骤色谱纯化:C18-120g,柱,移动相,MeCN/水,10%至80%梯度,10min,检测器,UV 254nm,流动速率,70mL/min。由此产生呈黄色固体的N-(叔丁基)-2-((7-羟基-2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(500mg,51%)。LCMS(ES)[M+1]+m/z:528。
步骤2
在室温下向50mL圆底烧瓶中添加N-(叔丁基)-2-((7-羟基-2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺(500mg,0.95mmol,1.00当量)、DCM(30mL)及MnO2(824mg,9.48mmol,10.00当量)。在室温下搅拌所得混合物36h。过滤所得混合物,用MeOH洗涤滤饼。减压浓缩滤液。由此产生呈棕色固体的N-(叔丁基)-2-(甲基(2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-7-氧代-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(300mg,60%)。LCMS(ES)[M+1]+m/z:526。
步骤3
在室温下向50mL圆底烧瓶中添加含N-(叔丁基)-2-(甲基(2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-7-氧代-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(300mg,0.57mmol,1.00当量)、二噁烷(10mL)及HCl(气体)(2M)的1,4-二噁烷(0.1mL)。在室温下搅拌所得混合物1h且浓缩以移除溶剂。将残余物溶解于CH3CN(5mL)中且通过使用以下条件的制备型HPLC纯化:SunFire Prep C18 OBD柱,19*150mm,5um,移动相,水(0.1%TFA)及CH3CN(7min内自36%达至68%)。由此产生呈黄色固体的N-(叔丁基)-2-((2-(4-(2-羟基-2-甲基丙氧基)吡啶-2-基)-7-氧代-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基)氨基)乙酰胺。LCMS(ES)[M-TFA+1]+m/z:442。1H NMR(300MHz,DMSO-d6)δ8.76(d,J=6.9Hz,1H),8.21(d,J=2.7Hz,1H),7.90(s,1H),7.73(dd,J=7.0,2.8Hz,1H),4.37(s,2H),4.22(s,2H),3.60-3.33(m,5H),2.77-2.68(m,2H),1.27(s,6H),1.24(s,9H)。
实施例1.508
合成N-叔丁基-2-{[2-(4-{[(3R,5S)-1,5-二甲基吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物502)
通过用(3R,5S)-1,5-二甲基吡咯烷-3-醇替换二甲氨基乙醇,与化合物348类似地合成化合物502。LCMS(ES)[M+1]+m/z:453。1H NMR(300MHz,DMSO-d6,ppm):δ8.45(d,J=5.6Hz,1H),8.17(s,1HCOOH),7.80(d,J=2.5Hz,1H),7.71(s,1H),6.96(dd,J=5.6,2.6Hz,1H),4.99-4.89(m,1H),4.12(d,J=2.4Hz,2H),3.27(s,3H),3.20-3.08(m,3H),2.81(t,J=7.9Hz,2H),2.60(dt,J=15.0,7.8Hz,1H),2.53-2.50(m,1H),2.22(s,3H),2.27-2.13(m,1H),2.06-1.94(m,2H),1.54-1.39(m,1H),1.25(s,9H),1.09(d,J=6.0Hz,3H)。
实施例1.509
合成(2R)-N-叔丁基-2-{甲基[2-(4-{[(3R)-1-甲基吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}内酰胺(化合物503)
通过用(R)-4-((1-甲基吡咯烷-3-基)氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三丁基锡烷基)吡啶,与化合物101类似地合成化合物503。LCMS(ES)[M+1]+m/z:453。1H NMR(300MHz,DMSO-d6,ppm):δ8.48(d,J=5.7Hz,1H),8.19(s,2H),7.85(d,J=2.5Hz,1H),7.79(s,1H),7.01(dd,J=5.6,2.6Hz,1H),5.10(t,J=4.6Hz,1H),5.04(q,J=7.2Hz,1H),3.29-2.99(m,2H),3.13(s,3H),2.95(dd,J=10.9,5.8Hz,1H),2.87-2.71(m,4H),2.58-2.50(m,1H),2.44-2.37(m,1H),2.36(s,3H),2.14-1.76(m,3H),1.33(d,J=7.0Hz,3H),1.21(s,9H)。
实施例1.510
合成(2R)-2-{甲基[2-(4-{[(3R)-1-甲基吡咯烷-3-基]氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}-N-(丙-2-基)丙酰胺(化合物504)
通过用(R)-4-((1-甲基吡咯烷-3-基)氧基)-2-(三甲基锡烷基)吡啶替换4-甲氧基-2-(三丁基锡烷基)吡啶且用异丙胺替换叔丁胺,与化合物101类似地合成化合物504。LCMS(ES)[M+1]+m/z:439。1H NMR(300MHz,DMSO-d6,ppm):δ8.49(d,J=5.6Hz,1H),8.18(s,HCOOH),8.17(d,J=9.1Hz,1H),7.81(d,J=2.5Hz,1H),7.01(dd,J=5.6,2.6Hz,1H),5.17-5.08(m,1H),5.06(q,J=6.9Hz,1H),3.98-3.80(m,1H),3.31-3.02(m,2H),3.11(s,3H),2.99-2.71(m,5H),2.56-2.51(m,1H),2.46-2.36(m,1H),2.36(s,3H),2.10-1.78(m,3H),1.34(d,J=7.0Hz,3H),1.08(d,J=6.6Hz,3H),0.92(d,J=6.6Hz,3H)。
实施例1.511
合成2-[甲基(2-{4-[2-(硫吗啉-4-基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]-N-(丙-2-基)乙酰胺(化合物505)
通过用2-硫吗啉乙酸酯替换二甲氨基乙醇且用异丙胺替换叔丁胺,与化合物389类似地合成化合物505。LCMS(ES)[M+1]+m/z:471。1H NMR(300MHz,DMSO-d6,ppm):δ8.47(d,J=5.6Hz,1H),7.99(d,J=7.8Hz,1H),7.80(d,J=2.6Hz,1H),7.05(dd,J=5.6,2.6Hz,1H),4.22(t,J=5.7Hz,2H),4.15(s,2H),3.87(dq,J=13.4,6.7Hz,1H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.82(t,J=7.8Hz,2H),2.78(dd,J=6.1,4.0Hz,6H),2.64-2.57(m,4H),2.05-1.93(m,2H),1.04(d,J=6.6Hz,6H)。
实施例1.512
合成N-叔丁基-2-[甲基(2-{4-[2-(甲基硫基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(化合物506)
流程144
在室温下向50mL圆底烧瓶中添加甲烷磺酸2-{[2-(4-{[(叔丁基氨甲酰基)甲基](甲基)氨基}-5H,6H,7H-环戊并[d]嘧啶-2-基)吡啶-4-基]氧基}乙酯(500mg,1.05mmol,1.00当量)、DMF(5.0mL)及(甲基硫基)钠(220mg,3.14mmol,3.00当量)。在60℃下搅拌所得混合物2h。使反应物冷却至室温且用水(1.0mL)淬灭,通过使用以下条件的反相急骤色谱纯化:C18硅胶,移动相,水(0.05%NH3·H2O),10%至80%梯度,10min,检测器,UV 254nm。由此产生呈黄色半固体的N-叔丁基-2-[甲基(2-{4-[2-(甲基硫基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(400mg,89%)。LCMS(ES)[M+1]+m/z:430。1H NMR(400MHz,DMSO-d6,ppm):δ8.48(d,J=5.6Hz,1H),7.84(d,J=2.4Hz,1H),7.67(s,1H),7.05(dd,J=5.6,2.8Hz,1H),4.30(t,J=6.4Hz,2H),4.12(s,2H),3.32(s,3H),3.14(t,J=6.8Hz,2H),2.88(t,J=6.8Hz,2H),2.50(t,J=1.6Hz,2H),2.17(s,3H),2.0(m,2H),1.24(s,9H)。
实施例1.513
合成N-叔丁基-2-({2-[4-(2-甲烷磺酰基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(化合物507)
流程145
在0℃下向40mL小瓶中添加N-叔丁基-2-[甲基(2-{4-[2-(甲基硫基)乙氧基]吡啶-2-基}-5H,6H,7H-环戊并[d]嘧啶-4-基)氨基]乙酰胺(200mg,0.47mmol,1.00当量)、THF(4.0mL)、H2O(0.5mL)及过氧硫酸钾(1.14g,1.86mmol,4.00当量)。在室温下搅拌所得混合物2h。将残余物溶解于MeOH(10mL)中。过滤所得混合物,用MeOH(2×5mL)洗涤滤饼。减压浓缩滤液。将残余物溶解于MeOH(5mL)中且通过使用以下条件的制备型HPLC纯化:SunfirePrep C18 OBD柱,50*250mm,5μm,10nm,移动相,水(0.1%FA)及CH3CN(12min内自5%达至35%),得到呈白色固体的N-叔丁基-2-({2-[4-(2-甲烷磺酰基乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺甲酸盐(124.8mg,53%)。LCMS(ES)[M+1]+m/z462。1H NMR(400MHz,DMSO-d6)δ8.52(d,J=5.6Hz,1H),8.15(s,1H),7.85(d,J=2.5Hz,1H),7.64(s,1H),7.12(dd,J=5.6,2.6Hz,1H),4.53(t,J=5.7Hz,2H),4.15(s,2H),3.68(t,J=5.7Hz,2H),3.25(s,3H),3.14(t,J=7.28Hz,2H),3.11(s,3H),2.82(t,J=7.8Hz,2H),2.00-1.96(m,2H),1.24(s,9H)。
实施例1.513
合成N-叔丁基-2-({2-[4-(2-羟基-2-甲基丙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}((2H3)甲基)氨基)乙酰胺(化合物509)
流程146
步骤1
在室温下搅拌N-叔丁基-2-({2-氯-5H,6H,7H-环戊并[d]嘧啶-4-基}氨基)乙酰胺(2g,7.073mmol,1.00当量)、(Boc)2O(3.09g,14.146mmol,2当量)、TEA(1.43g,14.146mmol,2当量)及DMAP(0.17g,1.415mmol,0.2当量)于DCM(30mL)中的混合物24h。用CH2Cl2(3×100mL)萃取所得混合物。使合并的有机层经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用PE/THF(2:1)洗脱来纯化残余物,得到呈白色固体的(2-(叔丁基氨基)-2-氧代乙基)(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基甲酸叔丁酯(1.6g,59.08%)。LCMS(ES)[M+1]+m/z:383。
步骤2
在100℃下于氮气氛围下搅拌(2-(叔丁基氨基)-2-氧代乙基)(2-氯-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基甲酸叔丁酯(1g,2.612mmol,1.00当量)、4-氟-2-(三丁基锡烷基)吡啶(1.51g,3.918mmol,1.5当量)及Pd(PPh3)4(0.60g,0.522mmol,0.2当量)于甲苯(20mL)中的混合物16h。真空浓缩所得混合物。通过硅胶柱色谱,用PE/THF(1:1)洗脱来纯化残余物,得到呈灰白色固体的N-[(叔丁基氨甲酰基)甲基]-N-[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基甲酸叔丁酯1.0g(86.33%)。LCMS(ES)[M+1]+m/z:444。
步骤3
在室温下向N-[(叔丁基氨甲酰基)甲基]-N-[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基甲酸叔丁酯(500mg,1.127mmol,1.00当量)于EA(20mL,204.301mmol,181.22当量)中的搅拌溶液中分批添加含HCl的乙醚(2M)(1.69mL,3.381mmol,3当量)。减压浓缩所得混合物,得到呈白色固体的N-叔丁基-2-{[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺盐酸盐(360mg,92.99%)。LCMS(ES)[M-HCl+1]+m/z:344。
步骤4
在0℃下于氮气氛围下向N-叔丁基-2-{[2-(4-氟吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基]氨基}乙酰胺(360mg,1.048mmol,1.00当量)于DMF中的搅拌溶液中分批添加NaH(50.31mg,2.096mmol,2当量)。在0℃下于氮气氛围下搅拌所得混合物20min。在0℃下向以上混合物逐滴添加CD3I(227.94mg,1.572mmol,1.50当量)。在室温下再搅拌所得混合物6h。用CH2Cl2(3×50mL)萃取所得混合物。使合并的有机层经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用PE/EA(1:4)洗脱来纯化残余物,得到呈白色固体的N-(叔丁基)-2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基-d3)氨基)乙酰胺(300mg,79.39%)。LCMS(ES)[M+1]+m/z:361。
步骤5
在0℃下于氮气氛围下向2-甲基-2-(氧杂环己-2-基氧基)丙-1-醇(435.05mg,2.496mmol,3当量)于DMF(30mL)中的搅拌溶液中分批添加NaH(39.95mg,1.664mmol,2当量)。在0℃下于氮气氛围下搅拌所得混合物20min。在0℃下向以上混合物分批添加N-(叔丁基)-2-((2-(4-氟吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基-d3)氨基)乙酰胺(300mg,0.832mmol,1.00当量)。在室温下再搅拌所得混合物4h。用CH2Cl2(3×30mL)萃取所得混合物。使合并的有机层经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用PE/EA(1:4)洗脱来纯化残余物,得到呈白色固体的N-(叔丁基)-2-((甲基-d3)(2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(300mg,70.03%)。LCMS(ES)[M+1]+m/z:515。
步骤6
在室温下搅拌N-(叔丁基)-2-((甲基-d3)(2-(4-(2-甲基-2-((四氢-2H-吡喃-2-基)氧基)丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)氨基)乙酰胺(300mg,0.583mmol,1.00当量)于EtOAc(5mL)及含HCl(g)的乙醚(2M)(0.58mL,1.166mmol,2当量)中的混合物3h。通过使用以下条件的制备型HPLC(Prep-HPLC-001)纯化粗产物:柱,SunfirePrep C18 OBD柱,50*250mm,5μm 10nm;移动相,水(0.1%FA)及ACN(15min内自5%相B达至25%),得到呈黄绿色固体的N-(叔丁基)-2-((2-(4-(2-羟基-2-甲基丙氧基)吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)(甲基-d3)氨基)乙酰胺(175.9mg,70.09%)。LCMS(ES)[M+1]+m/z:431。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.83(d,J=2.5Hz,1H),7.68(s,1H),7.05(dd,J=5.9,2.6Hz,1H),4.13(s,2H),3.86(s,2H),3.14(t,J=7.2Hz,2H),2.81(t,J=7.7Hz,2H),2.04-1.93(m,2H),1.25(s,9H),1.24(s,6H)。
实施例1.513
合成N-叔丁基-2-{[2-(4-{2-[二(2H3)甲基氨基]乙氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(化合物508)
流程147
步骤1
在0℃下向N-叔丁基-2-({2-[4-(2-羟乙氧基)吡啶-2-基]-5H,6H,7H-环戊并[d]嘧啶-4-基}(甲基)氨基)乙酰胺(1.4g,3.50mmol,1.00当量)于DCM(20mL)中的搅拌溶液中逐滴添加TEA(709mg,7.00mmol,2.0当量)及甲磺酰氯(482mg,4.20mmol,1.2当量)。将所得混合物在室温下搅拌2h且用30mL H2O稀释。用CH2Cl2(3×20mL)萃取混合物。将合并的有机层用盐水(50mL)洗涤,经无水Na2SO4干燥。过滤后,减压浓缩滤液。通过硅胶柱色谱,用CH2Cl2/MeOH(10:1)洗脱来纯化残余物,得到呈白色固体的甲烷磺酸2-{[2-(4-{[(叔丁基氨甲酰基)甲基](甲基)氨基}-5H,6H,7H-环戊并[d]嘧啶-2-基)吡啶-4-基]氧基}乙酯(1.3g,77.6%)。LCMS(ES)[M+1]+m/z:478。
步骤2
向甲烷磺酸2-{[2-(4-{[(叔丁基氨甲酰基)甲基](甲基)氨基}-5H,6H,7H-环戊并[d]嘧啶-2-基)吡啶-4-基]氧基}乙酯(300mg,0.62mmol,1.00当量)及双(甲基-d3)胺盐酸盐(64mg,1.25mmol,2.00当量)于CH3CN(5mL)中的搅拌混合物添加Cs2CO3(818mg,2.51mmol,4.00当量)。在60℃下搅拌所得混合物3h。将混合物冷却至室温且过滤。通过使用以下条件的制备型HPLC纯化滤液:XBridge Prep C18 OBD柱,19*150mm,5um,移动相,水(10mmol/LNH4HCO3)及CH3CN(7min内自30%相B达至40%),检测器,UV 254nm。冷冻干燥所需洗脱份,得到呈白色固体的N-叔丁基-2-{[2-(4-{2-[二(2H3)甲基氨基]乙氧基}吡啶-2-基)-5H,6H,7H-环戊并[d]嘧啶-4-基](甲基)氨基}乙酰胺(114.7mg,42.2%)。LCMS(ES)[M+1]+m/z:433。1H NMR(300MHz,DMSO-d6)δ8.47(d,J=5.6Hz,1H),7.84(d,J=2.6Hz,1H),7.68(s,1H),7.05(dd,J=5.7,2.6Hz,1H),4.19(t,J=5.7Hz,2H),4.13(s,2H),3.27(s,3H),3.15(t,J=7.3Hz,2H),2.81(t,J=7.8Hz,2H),2.66(t,J=5.7Hz,2H),2.01-1.96(m,2H),1.25(s,9H)。
2.生物学实施例
实施例2.1
生物体外运铁素内化分析
用于此分析的方案大体上如以全文引用的方式并入本文中的WO2018/128828中所描述。使用表达经标记于荧光素酶报导子的人类运铁素的经稳定转染CHO细胞株量测运铁素蛋白的功能性内化。在柠檬酸铁铵(FAC)存在下涂铺细胞,保持24h。用多西环素诱导运铁素蛋白表达24h。次日,添加化合物。将测试化合物溶解于DMSO中。将细胞与测试化合物一起培育6h,且随后使用Nano-Glo荧光素酶分析系统及Glomax(Promega,Madison,WI)量测荧光素酶活性。
测定测试化合物的平均pEC50。数据提供于下表2中。
表2
已努力确保关于所使用的数量(例如量、温度等)的准确性,但应当考虑存在一些实验性误差及偏差。
本领域技术人员将认识到与本文所描述的方法及材料类似或等效的许多方法及材料,其可用于实践本文所描述的主题。本发明决不仅限于所描述的方法及材料。
除非另外定义,否则本文所用的技术及科学术语具有与本主题所属领域普通技术人员通常所理解相同的含义,且与以下一致:Singleton等人(1994)Dictionary ofMicrobiology and Molecular Biology,第2版,J.Wiley&Sons,New York,NY;及Janeway,C.、Travers,P.、Walport,M.,Shlomchik(2001)Immunobiology,第5版,GarlandPublishing,New York。
在整个本说明书及权利要求书中,字语“包含(comprise、comprises及comprising)”为以非排他性意义使用,上下文另有要求的情况除外。应理解,本文中所描述的实施方案包括“由实施方案组成”和/或“基本上由实施方案组成”。
当提供值的范围时,应理解除非上下文另外明确指示,否则涵盖范围的上限与下限之间的各中间值(至下限的单位的十分之一)及所述范围内的任何其他指定值或中间值。亦涵盖可独立地包括于较小范围中的这些小范围的上限及下限,在所述范围内受到任何特定排他性限制。在所述范围包括限值中之一或两者的情况下,亦包括排除那些所包括的限值的任一者或两者的范围。
得益于在前述描述及相关图式中所呈现的教示内容,本主题所属领域的技术人员将想到本文中所阐述的许多修改及其他实施方案。因此,应理解,主题不限于所公开的特定实施方案且修改及其他实施方案意欲包括于随附权利要求书的范畴内。虽然本文中使用特定术语,但其仅以通用及描述性意义且不出于限制的目的使用。
Claims (103)
1.一种式(I')化合物:
或其药学上可接受的盐;其中
Z为N或CH;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C10烷氧基、羟基-C1-C10烷基、氰基、-NRGRH、卤代-C1-C3烷氧基、-O-(C1-C6烷基)-Rbb、-O-Rbb、-(C1-C6烷基)-NRGIRHI、-S-C1-C3烷基、-S-C1-C3烷基-NRG1RH1、卤代-C1-C3烷基、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
羟基-C1-C10烷氧基或-O-(C1-C6烷基)-Rbb中的该烷基部分任选经氰基、羟基、羟基-C1-C3烷基、卤素或C1-C3烷氧基取代;
Rbb为4元至7元单环或桥联杂环基、C3-C7环烷基、5元或6元单环杂芳基、-SO2-C1-C3烷基、-S-C1-C3烷基、-C(O)NRG1RH1或-NRGRH;
Rcc为C1-C3烷基;且
Rdd为C1-C3烷基或6元杂芳基;
其中R6、Rbb或Rdd的该环烷基、杂环基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:羟基、卤素、卤代-C1-C3烷基、氧代、C1-C3烷氧基及C1-C3烷基;
RG1及RH1各独立地为氢或C1-C3烷基;
且
RG及RH各独立地为氢、-C(O)RGa或任选氘代的C1-C3烷基;其中
RGa为C1-C3烷基或氢;
或
两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元至6元单环杂芳基;其中
与环B稠合的该杂环基、苯基、环烷基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基;
n为0、1、2或3;
Y1、Y2、Y3及Y4各独立地选自由以下组成的组:CH、N、NH、O、S、SH、S-R6、N-R6及C-R6,条件是Y1、Y2、Y3及Y4中的1或2者可为N、N-R6、NH、O、SH或S-R6;
f为0或1;
p为1或2;
Rx在各情况下为卤素、C1-C6烷基、C1-C3烷氧基、羟基、氧代或氰基;
m为0、1或2;
R3选自由以下组成的组:氢、任选氘代的C1-C3烷基、羟基-C1-C3烷基、卤代-C1-C3烷基、环丙基及苯基;
R4选自由以下组成的组:
i.(5元至10元单环或稠合双环杂芳基)-C1-C3烷基或(6元或7元单环杂环基)-C1-C3烷基;其中
该杂芳基或杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C6-C10单环或稠合双环芳基、C3-C7环烷基、5元或6元杂芳基、-(C1-C3烷基)-T及5元至7元单环杂环基;
T选自由以下组成的组:C6-C10单环或稠合双环芳基、C3-C7环烷基、5元或6元杂芳基及5元至7元单环杂环基;且
其中R4的T或该芳基、环烷基、杂芳基或杂环基取代基任选经一个或两个各自个别地选自由C1-C3烷基、卤素及羟基组成的组的取代基取代;且
当p为1时,该(5元至10元单环或稠合双环杂芳基)-C1-C3烷基中的C1-C3烷基为直链的;
及
其中
R4a及R4g各独立地选自由以下组成的组:氢;C1-C10烷基;羟基-C1-C6烷基;卤代-C1-C3烷基;C1-C3烷氧基-C1-C6烷基;-C1-C6烷基-NRJ1RJ2;C3-C7环烷基;4元至10元单环、稠合双环、桥联双环或螺杂环基;C6-C10单环或稠合双环芳基;5元至10元单环或稠合双环杂芳基;(C6-C10单环或稠合双环芳基)-C1-C3烷基;及(5元至10元单环或稠合双环杂芳基)-C1-C3烷基;
RJ1及RJ2独立地为氢或C1-C3烷基;
其中R4a或R4g的该环烷基、杂环基、芳基、杂芳基、芳基-烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素;C1-C6烷基;卤代-C1-C3烷基;羟基;C1-C3烷氧基;卤代-C1-C3烷氧基;氧代;C3-C7环烷基;及5元至10元单环、稠合双环或螺杂环基;
R4b为氢或C1-C6烷基;或
R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基;或
R4b及R4c与其各自所连接的原子一起形成任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代的5元至7元单环杂环基:羟基、卤素及C1-C3烷基;或
R4c及R4d各独立地选自由以下组成的组:氢、C1-C3烷氧基、羟基、C1-C3烷基-硫基-C1-C3烷基、羟基-C1-C6烷基、C1-C6烷氧基-C1-C3烷基、C3-C7环烷基及C1-C3烷基;或
R4c及R4d与其各自所连接的原子一起形成C3-C7环烷基;
或当p为1时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个或两个杂原子的7元稠合双环杂环基、7元桥联双环杂环基或7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷氧基、氧代及-(CH2)sC(=O)NRkRl;其中
s为0、1、2或3;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、羟基、C1-C3烷基、C3-C7环烷基及C6-C10单环或稠合双环芳基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及-NRqRw;其中
Rq为氢或C1-C3烷基;且
Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;
或
iii.8元、9元、10元或11元稠合双环杂环基,或12元双环桥联及稠合杂环基,其中该8元、9元或11元杂环基含有一个杂原子且该10元或12元杂环基含有一个或两个杂原子;且其中该10元、11元或12元杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、C1-C3烷氧基及羟基;
或当p为2时,
R3及R4与其各自所连接的氮原子一起可形成:
i.含有一个杂原子的6元单环杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、羟基-(C1-C6烷基)、羟基、氧代及C1-C3烷氧基;或
ii.含有一个或两个杂原子的4元或7元单环杂环基,或含有一个、两个或三个杂原子的7元、8元、9元、10元或11元桥联双环、稠合双环或螺杂环基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、氧代、氰基、C1-C3烷基、羟基、-NRGRH及-(CH2)sC(=O)NRkRl;
条件是当该式(I)结构为
且
其中该式(I)化合物不为:
N-((1,4-二氧杂环己-2-基)甲基)-2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-胺;
4-(哌啶-1-基)-2-(吡啶-2-基)-5,6,7,8-四氢喹唑啉;
4-(氮杂环庚-1-基)-2-(6-丙基吡啶-2-基)-5,6,7,8-四氢喹唑啉;
1-丙基-4-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,4-二氮杂环庚-2-酮;或
2-(2-(吡啶-2-基)-6,7-二氢-5H-环戊并[d]嘧啶-4-基)-1,2-氧氮杂环庚烷;或其盐。
2.根据权利要求1的化合物或其药学上可接受的盐,其中p为1。
3.根据权利要求1或2的化合物或其药学上可接受的盐,其中Z为N。
4.根据权利要求1至3中任一项的化合物或其药学上可接受的盐,其中Y1、Y2、Y3及Y4各为CH或C-R6。
5.根据权利要求4的化合物或其药学上可接受的盐,其中Y1为CH,Y2为C-R6,Y3为CH,且Y4为CH。
6.根据权利要求1至3中任一项的化合物或其药学上可接受的盐,其中Y3为N且Y1、Y2及Y4各为CH或C-R6。
7.根据权利要求1至3中任一项的化合物或其药学上可接受的盐,其中Y2为N且Y1、Y3、Y4各为CH或C-R6。
8.根据权利要求1至3中任一项的化合物或其药学上可接受的盐,其中Y1为N且Y2、Y3及Y4各为CH或C-R6。
9.根据权利要求1至8中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C10烷氧基、羟基-C1-C10烷基、-O-(C1-C6烷基)-Rbb、卤代-C1-C3烷氧基、-O-Rcc-O-Rdd、卤代-C1-C3烷基、-(C1-C6烷基)-NRGIRHI、-S-CH3、-S(CH2)2N(CH3)2及-NRGRH;其中
Rbb为-NRGRH、-C(O)N(CH3)2、-S(O)2CH3或-SCH3;
RG及RH各独立地为氢、任选氘代的C1-C3烷基或-C(O)RGa;其中RGa为C1-C3烷基;
RGI及RHI各独立地为氢或C1-C3烷基;
Rcc及Rdd各独立地为C1-C3烷基;且
其中羟基-C1-C10烷氧基中的该烷基部分任选经羟基、卤素或C1-C3烷氧基取代。
10.根据权利要求9的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:甲氧基、乙氧基、甲基、氟、氯、乙基、-N(CH3)2、羟基、-OCH2CH2OH、-CH2OH、-CH2OCH3、-OCH2CH2NH2、-OCH2CH2N(CH3)2、-OCH2C(CH3)2OH、-OCH2CF3、-OCHF2、-OCF3、-OCH2CH2OCH3、-OCH2CH2F、-OC(CH3)2CH2OH、-OCH2CH(CH3)OH、-OCH2CH2NHC(O)CH3、-OC(CH3)2CH2N(CH3)2、-OCH(CH3)CH2OH、-OCH2CH(CH(CH3)2)OH、-OCH2CH(CH2CH3)OH、-OCH2C(CH2CH3)2OH、-OCH2CH2N(CH2CH3)2、-OCH(CH3)CH2N(CH3)2、-OCH2C(O)N(CH3)2、-OCH2C(CH3)2N(CH3)2、-OCH2CH(CH2OH)OH、-OCH2CH2NH(CH3)、-OCH2CH(CF3)OH、-OCH2C(CH3)(CH2CH3)OH、-OCH2CH(CH2OCH3)OH、-OCH2CH(CH2F)OH、-(CH2)3N(CH3)2、-(CH2)3N(CH3)H、-O(CH2)2S(O)2CH3、-O(CH2)2SCH3、-(CH2)2C(CH3)2OH、-OCH2CH2N(CD3)2及-CH2CH2OH。
11.根据权利要求10的化合物或其药学上可接受的盐,其中R6在各情况下为甲氧基、-OCH2CH2N(CH3)2、-OCH2CH2OH或-OCH2C(CH3)2OH。
12.根据权利要求11的化合物或其药学上可接受的盐,其中R6在各情况下为-OCH2CH2N(CH3)2或-OCH2C(CH3)2OH。
13.根据权利要求1至8中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:-O-(C1-C6烷基)-Rbb、-O-Rbb、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
Rcc为C1-C3烷基且Rdd为6元杂芳基;
Rbb为4元至7元单环或桥联杂环基、5元或6元单环杂芳基或C3-C7环烷基;且
其中R6、Rbb或Rdd的该环烷基、杂芳基或杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:羟基、卤素、C1-C3烷氧基、氧代、卤代-C1-C3烷基及C1-C3烷基。
14.根据权利要求13的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:环丙基、-O-Rbb、-O-(CH2)-Rbb、-O-(CH2)2-Rbb、-O-(CH2)2-O-哒嗪基及任选存在的经C1-C3烷基取代的咪唑基;其中
Rbb选自由以下组成的组:环丙基、环丁基、环戊基、环己基、四氢呋喃基、四氢吡喃醇、氧杂环丁烷基、二氧杂环戊烷基、氮杂环丁烷基、吗啉基、哌嗪基、2-氧杂-5-氮双环[2.2.1]庚烷、咪唑基、四唑基、哒嗪基、哌啶基、硫吗啉基及吡咯烷基,其各任选经羟基、氧代、氟、-CF3、-CH2CF3、-CH2CHF2、-CH2CH2F、甲氧基、乙基或甲基取代。
17.根据权利要求1至8中任一项的化合物或其药学上可接受的盐,其中两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元或6元单环杂芳基,其各任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3-烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基。
18.根据权利要求1至8中任一项的化合物或其药学上可接受的盐,其中两个R6基团与其各自所连接的原子一起形成与环B稠合的吡唑基、二氧杂环己烷基、吡啶基、嘧啶基、噻唑基、呋喃基、二氧杂环戊烷基或苯基环,其中该环任选经一个选自由以下组成的组的取代基取代:羟基、甲氧基、四氢吡喃基、-CH2OH及甲基。
21.根据权利要求1至20中任一项的化合物或其药学上可接受的盐,其中f为1。
25.根据权利要求22至24中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:C1-C3烷基及羟基-C1-C3烷基。
26.根据权利要求25的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:甲基、乙基、正丙基、-CH2CH2OH及-CH2CH2CH2OH。
27.根据权利要求1至26中任一项的化合物或其药学上可接受的盐,其中n为1。
28.根据权利要求1至26中任一项的化合物或其药学上可接受的盐,其中n为0。
29.根据权利要求1至16中任一项的化合物或其药学上可接受的盐,其中n为2。
30.根据权利要求29的化合物或其药学上可接受的盐,其中一个R6选自由甲基及甲氧基组成的组,且另一R6选自由甲基、甲氧基、卤素及-OCH2CH2OH组成的组。
31.根据权利要求1至30中任一项的化合物或其药学上可接受的盐,其中R3选自由以下组成的组:氢、甲基、-CD3、乙基、苯基、-CH2CF3及-CH2CH2OH。
32.根据权利要求31的化合物或其药学上可接受的盐,其中R3为甲基。
33.根据权利要求1至32中任一项的化合物或其药学上可接受的盐,其中R4为(5元至10元单环或稠合双环杂芳基)-甲基,其中该杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:苯基、C3-C7环烷基、-(C1-C3烷基)-苯基及5元至7元单环杂环基,且其中单独的或-(C1-C3烷基)-苯基中的该苯基、环烷基或杂环基任选经一个或两个各自个别地选自由C1-C3烷基、卤素及羟基组成的组的取代基取代。
34.根据权利要求33的化合物或其药学上可接受的盐,其中R4为(6元杂芳基)-甲基,其中该6元杂芳基中在连接点的邻位的环原子中的至少一者为氮。
35.根据权利要求33或34的化合物或其药学上可接受的盐,其中R4选自由以下组成的组:吡啶基-甲基、嘧啶基-甲基、苯并噁唑-甲基、噁唑基-甲基及三唑基-甲基,其各任选经苯基或苯甲基取代,且其中该苯基任选经一个选自由氟、甲基及氯组成的组的取代基取代。
38.根据权利要求37的化合物或其药学上可接受的盐,其中R4c选自由以下组成的组:氢、甲基、异丙基、-CH2OH、-CH2OC(CH3)3及-CH2CH2SCH3;且R4d选自由氢及甲基组成的组;或R4c及R4d与其各自所连接的原子一起形成环丙基环。
39.根据权利要求38的化合物或其药学上可接受的盐,其中R4c及R4d各为氢。
40.根据权利要求37至39中任一项的化合物或其药学上可接受的盐,其中R4b为氢。
41.根据权利要求37至40中任一项的化合物或其药学上可接受的盐,其中R4a为C1-C6烷基。
42.根据权利要求41的化合物或其药学上可接受的盐,其中R4a为甲基、乙基、异丙基、叔丁基或3-甲基戊-3-基。
43.根据权利要求42的化合物或其药学上可接受的盐,其中R4a为叔丁基或异丙基。
44.根据权利要求37至40中任一项的化合物或其药学上可接受的盐,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的苯基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环或稠合双环杂环基。
45.根据权利要求44的化合物或其药学上可接受的盐,其中R4a为任选经一个选自由以下组成的组的取代基取代的苯基:氟、氯、甲基及甲氧基。
47.根据权利要求37至40中任一项的化合物或其药学上可接受的盐,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环或稠合双环杂芳基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、稠合双环或螺杂环基。
48.根据权利要求47的化合物或其药学上可接受的盐,其中R4a为吡啶基、嘧啶基、吡唑基、异噻唑基、哒嗪基或喹啉基,其任选经一个选自由以下组成的组的取代基取代:氟、氯、甲氧基、氮杂环庚烷基、环丙基、-CF3、-OCF3或甲基。
50.根据权利要求37至40中任一项的化合物或其药学上可接受的盐,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的C3-C7环烷基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环或稠合双环杂环基。
51.根据权利要求50的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:环丙基、环丁基、环戊基、环己基及双环[1.1.1]戊-1-基,其任选经一个或两个各独立地选自由甲基、-CF3、氟或羟基组成的组的取代基取代。
53.根据权利要求37至40中任一项的化合物或其药学上可接受的盐,其中R4a为任选经一个或两个各独立地选自由以下组成的组的取代基取代的4元至10元单环或稠合双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、氧代、C3-C7环烷基及5元至10元单环或稠合双环杂环基。
54.根据权利要求53的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:四氢呋喃基、吡咯烷基、苯并[d][1,3]间二氧杂环戊烯基、氧杂环丁烷基及四氢吡喃基,其任选经一个或两个各独立地选自由甲基、甲氧基及氧代组成的组的取代基取代。
56.根据权利要求37至40中任一项的化合物或其药学上可接受的盐,其中R4a为(C6-C10单环或稠合双环芳基)-C1-C3烷基或(5元至10元单环或稠合双环杂芳基)-C1-C3烷基,其任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、C3-C7环烷基及5元至10元单环、稠合双环杂环基。
57.根据权利要求56的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:苯甲基、2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙基及吡啶基-甲基。
59.根据权利要求37至40中任一项的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:羟基-C1-C6烷基、卤代-C1-C3烷基、C1-C3烷氧基-C1-C6烷基及-C1-C6烷基-NRJ1RJ2,其中RJ1及RJ2各独立地为氢或C1-C3烷基。
60.根据权利要求59的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:-C(CH3)2CH2OH、-CH2CH2OH、-C(CH3)2CH2OCH3、-CH(CH3)CH2OH、-CH2CH2N(CH3)2及-CH2CF3。
61.根据权利要求60的化合物或其药学上可接受的盐,其中R4a为-C(CH3)2CH2OH。
62.根据权利要求37至39中任一项的化合物或其药学上可接受的盐,其中R4a及R4b与其各自所连接的原子一起形成5元至10元单环、稠合双环或桥联双环杂环基,所述基团任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基。
63.根据权利要求62的化合物或其药学上可接受的盐,其中R4a及R4b与其各自所连接的原子一起形成哌啶基、吗啉基、吡咯烷基、氮杂环庚烷基、吲哚啉基、氮双环[3.1.1]庚烷基、2,3-二氢-1H-吡咯并[2,3-c]吡啶或哌嗪基,所述基团任选经一个或两个各独立地选自由羟基、甲基、氟及甲氧基组成的组的取代基取代。
65.根据权利要求37或41至61中任一项的化合物或其药学上可接受的盐,其中R4b及R4c与其各自所连接的原子一起形成任选经一个或两个各独立地选自C1-C3烷基的取代基取代的5元至7元单环杂环基。
66.根据权利要求65的化合物或其药学上可接受的盐,其中R4b及R4c与其各自所连接的原子一起形成任选经甲基取代一次或两次的哌啶-2-酮或吡咯烷-2-酮。
68.根据权利要求67的化合物或其药学上可接受的盐,其中R4g选自由苯基及甲基组成的组。
69.根据权利要求1至30中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个或两个杂原子的7元单环或桥联双环杂环基;
其中当该7元杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基。
70.根据权利要求69的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成:含有一个杂原子的单环7元杂环基,其中该杂环基任选经甲基或氧代取代一次;或含有两个杂原子的7元单环或桥联双环杂环基,其中所述杂原子为N或O,且该杂环基任选经一个或两个各独立地选自由苯基、甲基及氧代组成的组的取代基取代,且其中该苯基任选经甲氧基取代。
72.根据权利要求1至30中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的10元或11元稠合双环杂环基,或12元双环稠合及桥联杂环基,所述基团各任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、C1-C3烷氧基、羟基及卤素。
74.根据权利要求1至30中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的4元或6元单环杂环基;其中
该4元单环杂环基任选经-(CH2)sC(=O)NRkRl取代;其中
s为0、1或2;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、甲基、苯基、环戊基及环己基;
且
该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及-NRqRw;其中
Rq为氢或C1-C3烷基;
Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基;且
其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基。
76.根据权利要求1至75中任一项的化合物或其药学上可接受的盐,其中Rx在各情况下为甲基。
77.根据权利要求1至76中任一项的化合物或其药学上可接受的盐,其中m为0。
78.根据权利要求1至76中任一项的化合物或其药学上可接受的盐,其中m为2。
79.根据权利要求1的化合物或其药学上可接受的盐,其中
Z为N;
p为1;
f为1;
Y1、Y2、Y3及Y4各独立地选自由CH、N及C-R6组成的组,条件是Y1、Y2、Y3及Y4中的1或2者可为N;
R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C10烷氧基、羟基-C1-C10烷基、氰基、-NRGRH、卤代-C1-C3烷氧基、-O-(C1-C6烷基)-Rbb、-O-Rbb、-(C1-C6烷基)-NRGIRHI、卤代-C1-C3烷基、-O-Rcc-O-Rdd、5元至7元单环杂芳基及C3-C6环烷基;其中
羟基-C1-C10烷氧基或-O-(C1-C6烷基)-Rbb中的该烷基部分任选经羟基、羟基-C1-C3烷基、卤素或C1-C3烷氧基取代;
Rbb为4元至7元单环杂环基、C3-C7环烷基或-NRGRH;
Rcc及Rdd各独立地为C1-C3烷基;
其中R6或Rbb的该环烷基、杂环基或杂芳基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代;
且
RG1及RH1各独立地为氢或C1-C3烷基;
RG及RH各独立地为氢、-C(O)RGa或任选氘代的C1-C3烷基;其中
RGa为C1-C3烷基或氢;
或
两个R6基团与其各自所连接的原子一起形成与环B稠合的5元或6元单环杂环基、与环B稠合的C4-C7环烷基、与环B稠合的苯基或与环B稠合的5元至6元单环杂芳基;其中
与环B稠合的该杂环基、苯基、环烷基或杂芳基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、羟基-C1-C3烷基、C1-C3烷基、C3-C7环烷基及5元或6元单环杂环基;
n为0、1或2;
R3选自由以下组成的组:氢、苯基、-CH2CH2OH及任选氘代的甲基或乙基;
R4c选自由以下组成的组:氢、甲基、异丙基、-CH2OH、-CH2OC(CH3)3及-CH2CH2SCH3;
R4d选自由氢及甲基组成的组;
或
R4c及R4d与其各自所连接的原子一起形成环丙基环;
R4b为氢或甲基;
R4a选自由以下组成的组:氢;C1-C10烷基;羟基-C1-C6烷基;C1-C3烷氧基-C1-C6烷基;-C1-C6烷基-NRJ1RJ2;C3-C7环烷基;5元至10元单环、稠合双环或桥联双环杂环基;C6-C10单环或稠合双环芳基;4元至10元单环或稠合双环杂芳基;(C6-C10单环或稠合双环芳基)-C1-C3烷基;及(5元至10元单环或稠合双环杂芳基)-C1-C3烷基;其中R4a的该环烷基、杂环基、芳基、杂芳基、芳基烷基或杂芳基-烷基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基、C1-C3烷氧基、卤代-C1-C3烷氧基、氧代、C3-C7环烷基及5元至10元单环或稠合双环杂环基;
RJ1及RJ2独立地为氢或C1-C3烷基;
或
R4a及R4b与其各自所连接的原子一起形成任选经一个或两个各独立地选自由以下组成的组的取代基取代的5元至10元单环、稠合双环或桥联双环杂环基:卤素、C1-C6烷基、卤代-C1-C3烷基、羟基及C1-C3烷氧基;
Rx在各情况下为C1-C3烷基;且
m为0、1或2。
80.根据权利要求79的化合物或其药学上可接受的盐,其中m为0。
81.根据权利要求79的化合物或其药学上可接受的盐,其中m为2且Rx在各情况下为甲基。
82.根据权利要求79至81中任一项的化合物或其药学上可接受的盐,其中Y1、Y2、Y3及Y4各为CH或C-R6;
Y3为N且Y1、Y2及Y4各为CH或C-R6;
Y2为N且Y1、Y3、Y4各为CH或C-R6;
或
Y1为N且Y2、Y3及Y4各为CH或C-R6。
83.根据权利要求82的化合物或其药学上可接受的盐,其中Y1为CH,Y2为C-R6,Y3为CH,且Y4为CH。
84.根据权利要求79至83中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:卤素、羟基、C1-C3烷氧基、C1-C3烷基、C1-C3烷氧基-C1-C3烷基、羟基-C1-C6烷氧基、羟基-C1-C10烷基、-O-Rbb、-O-(C1-C6烷基)-Rbb、卤代-C1-C3烷氧基、-O-Rcc-O-Rdd、卤代-C1-C3烷基、C3-C6环烷基及-NRGRH;其中
Rbb为-NRGRH、4元至6元单环杂环基或C3-C7环烷基;
RG及RH各独立地为氢或C1-C3烷基;
Rcc及Rdd各独立地为C1-C3烷基;且其中
R6或Rbb的该环烷基或杂环基任选经一个或两个各独立地选自由羟基、C1-C3烷氧基及C1-C3烷基组成的组的取代基取代。
85.根据权利要求84的化合物或其药学上可接受的盐,其中Rbb选自由以下组成的组:环丙基、环丁基、四氢呋喃基、氧杂环丁烷基、吗啉基及吡咯烷基,其各任选经羟基或甲基取代;或Rbb为-N(CH3)2。
86.根据权利要求79至85中任一项的化合物或其药学上可接受的盐,其中R6在各情况下选自由以下组成的组:甲氧基、乙氧基、甲基、氟、氯、乙基、-N(CH3)2、羟基、-OCH2CH(CH3)OH、-OCH2CH2N(CH2CH3)2、-OCH2C(CH3)(CH2CH3)OH、-OCH2CH(CH2OCH3)OH、-OCH2CH2OH、-CH2OH、-CH2OCH3、-OCH2CH2NH2、-OCH2CH2N(CH3)2、-OCH2C(CH3)2OH、-OCH2CF3、-OCHF2、-OCF3、-OCH2CH2OCH3、-OCH2CH2F、-OC(CH3)2CH2OH、-CH2CH2OH、 及其中指示与环B的连接点。
89.根据权利要求79至83中任一项的化合物或其药学上可接受的盐,其中两个R6基团与其各自所连接的原子一起形成与环B稠合的吡唑基、二氧杂环己烷基、吡啶基、嘧啶基、噻唑基、呋喃基、二氧杂环戊烷基或苯基环,其中该环任选经一个选自由以下组成的组的取代基取代:羟基、甲氧基、四氢吡喃基、-CH2OH及甲基。
90.根据权利要求79至89中任一项的化合物或其药学上可接受的盐,其中R3为甲基。
91.根据权利要求79至90中任一项的化合物或其药学上可接受的盐,其中n为1。
92.根据权利要求79至91中任一项的化合物或其药学上可接受的盐,其中R4b为氢。
93.根据权利要求79至92中任一项的化合物或其药学上可接受的盐,其中R4a选自由以下组成的组:
i.叔丁基或异丙基;
ii.苯基,其任选经一个选自由氟、氯、甲基及甲氧基组成的组的取代基取代;
iii.吡啶基、嘧啶基、吡唑基、异噻唑基、哒嗪基或喹啉基,其任选经一个选自由以下组成的组的取代基取代:氟、氯、甲氧基、氮杂环庚烷基、环丙基、-CF3、-OCF3及甲基;
iv.环丙基、环丁基、环戊基、环己基及双环[1.1.1]戊-1-基,其任选经一个或两个各独立地选自由甲基、-CF3、氟及羟基组成的组的取代基取代;
v.四氢呋喃基、吡咯烷基、苯并[d][1,3]间二氧杂环戊烯基及四氢吡喃基,其任选经一个或两个各独立地选自由甲基、甲氧基及氧代组成的组的取代基取代;
vi.苯甲基、2-(1-环丁基-5-甲基-1H-咪唑-2-基)乙基及吡啶基-甲基;及
vii.-C(CH3)2CH2OH、-CH2CH2OH及-C(CH3)2CH2OCH3。
94.根据权利要求79至91中任一项的化合物,其中R4a及R4b与其各自所连接的原子一起形成哌啶基、吗啉基、吡咯烷基、氮杂环庚烷基、吲哚啉基、氮双环[3.1.1]庚烷基或哌嗪基,所述基团任选经一个或两个各独立地选自由甲基、氟及甲氧基组成的组的取代基取代。
95.根据权利要求1的化合物或其药学上可接受的盐,其中
Z为N;
f为1;
R6在各情况下选自由以下组成的组:C1-C3烷基、-NRGRH、卤素及C1-C3烷氧基;
p为1;
n为0或1;
RG及RH各独立地为氢或C1-C3烷基;
Y1、Y2、Y3及Y4各独立地选自由CH、N及C-R6组成的组,条件是Y1、Y2、Y3及Y4中的1或2者可为N;
Rx在各情况下为卤素、C1-C6烷基、C1-C3烷氧基、羟基或氰基;
m为0;且
R3及R4与其各自所连接的氮原子一起形成:
i.含有一个或两个杂原子的7元稠合双环杂环基、7元桥联双环杂环基或7元单环杂环基;
其中当该7元单环杂环基含有一个杂原子时,该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:氧代、卤素、羟基、C1-C3烷氧基、氰基及C1-C3烷基;且
当该7元单环杂环基含有两个杂原子时,所述杂原子各独立地为N或O,且该杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、氰基、氧代、卤素、卤代-C1-C3烷基及C6-C10单环或稠合双环芳基;且
其中该芳基任选经一个或两个各自个别地选自由以下组成的组的取代基取代:C1-C3烷氧基、羟基、卤素及C1-C3烷基;
ii.含有一个杂原子的4元或6元单环杂环基;
其中该4元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷氧基、氧代及-(CH2)sC(=O)NRkRl;其中
s为0、1、2或3;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、羟基、C1-C3烷基、C3-C7环烷基及C6-C10单环或稠合双环芳基;
其中该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及NRqRw;其中
Rq为氢或C1-C3烷基;且
Rw为C6-C10单环或双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基;
或
iii.8元、9元、10元或11元稠合双环杂环基,或12元双环桥联稠合杂环基,其中该8元、9元或11元杂环基含有一个杂原子且该10元或12元杂环基含有一个或两个杂原子;且其中该10元、11元或12元杂环基任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、C1-C3烷氧基及羟基。
96.根据权利要求95的化合物或其药学上可接受的盐,其中Y1、Y2、Y3及Y4各为CH或C-R6。
97.根据权利要求95或96的化合物或其药学上可接受的盐,其中R6若存在则选自由以下组成的组:-N(CH3)2、甲基、甲氧基、氟及氯。
98.根据权利要求95至97中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成:含有一个杂原子的7元单环杂环基,其中该杂环基任选经甲基或氧代取代一次;或含有两个杂原子的7元单环或桥联双环杂环基,其中所述杂原子为N或O,且该杂环基任选经一个或两个各独立地选自由苯基、甲基及氧代组成的组的取代基取代,且其中该苯基任选经甲氧基取代。
99.根据权利要求95至97中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的10元或11元稠合双环杂环基,或12元双环稠合桥联杂环基,所述基团各任选经一个、两个或三个各独立地选自由以下组成的组的取代基取代:C1-C3烷基、C1-C3烷氧基、羟基及卤素。
100.根据权利要求95至97中任一项的化合物或其药学上可接受的盐,其中R3及R4与其各自所连接的氮原子一起形成含有一个杂原子的4元或6元单环杂环基;其中
该4元单环杂环基任选经-(CH2)sC(=O)NRkRl取代;其中
s为0、1或2;
Rk为氢或C1-C3烷基;且
Rl选自由以下组成的组:氢、甲基、苯基、环戊基及环己基;
且
该6元单环杂环基任选经一个或两个各独立地选自由以下组成的组的取代基取代:C1-C3烷氧基、氧代、卤素、氰基及NRqRw;其中
Rq为氢或C1-C3烷基;
Rw为C6-C10单环或稠合双环芳基或C3-C7环烷基,其中该芳基或环烷基任选经一个或两个各独立地选自由以下组成的组的取代基取代:卤素、C1-C3烷基、羟基及C1-C3烷氧基。
101.根据权利要求1的化合物或其药学上可接受的盐,该化合物选自表1。
102.一种药物组合物,其包含根据权利要求1至101中任一项的化合物或其药学上可接受的盐,及药学上可接受的赋形剂。
103.一种抑制受试者中由运铁素介导的铁转运的方法,其包含向该受试者施用有效量的根据权利要求1至101中任一项的化合物或根据权利要求102的药物组合物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063016891P | 2020-04-28 | 2020-04-28 | |
| US63/016,891 | 2020-04-28 | ||
| US202063127774P | 2020-12-18 | 2020-12-18 | |
| US63/127,774 | 2020-12-18 | ||
| PCT/US2021/029574 WO2021222363A1 (en) | 2020-04-28 | 2021-04-28 | Cycloalkyl pyrimidines as ferroportin inhibitors |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN115836063A true CN115836063A (zh) | 2023-03-21 |
| CN115836063B CN115836063B (zh) | 2025-07-29 |
Family
ID=75954294
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202180047289.0A Active CN115836063B (zh) | 2020-04-28 | 2021-04-28 | 作为运铁素(ferroportin)抑制剂的环烷基嘧啶 |
Country Status (19)
| Country | Link |
|---|---|
| US (3) | US11746100B2 (zh) |
| EP (1) | EP4143178A1 (zh) |
| JP (1) | JP7742850B2 (zh) |
| KR (1) | KR20230007441A (zh) |
| CN (1) | CN115836063B (zh) |
| AU (1) | AU2021263818A1 (zh) |
| BR (1) | BR112022021806A2 (zh) |
| CA (1) | CA3180661A1 (zh) |
| CL (1) | CL2022003013A1 (zh) |
| CO (1) | CO2022015395A2 (zh) |
| CR (1) | CR20220556A (zh) |
| DO (1) | DOP2022000236A (zh) |
| EC (1) | ECSP22084239A (zh) |
| IL (1) | IL297624B2 (zh) |
| MX (1) | MX2022013518A (zh) |
| PE (1) | PE20230845A1 (zh) |
| TW (1) | TWI908795B (zh) |
| WO (1) | WO2021222363A1 (zh) |
| ZA (1) | ZA202211401B (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2021263818A1 (en) * | 2020-04-28 | 2022-11-03 | Global Blood Therapeutics, Inc. | Cycloalkyl pyrimidines as ferroportin inhibitors |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0407899A2 (de) * | 1989-07-11 | 1991-01-16 | Hoechst Schering AgrEvo GmbH | Aminopyrimidin-Derivate, Verfahren zu ihrer Herstellung, sie enthaltende Mittel und ihre Verwendung als Fungizide |
| WO2005014558A1 (en) * | 2003-08-05 | 2005-02-17 | Vertex Pharmaceuticals Incorporated | Condensed pyramidine compounds as inhibitors of voltage-gated ion channels |
| WO2011026835A1 (de) * | 2009-09-02 | 2011-03-10 | Vifor (International) Ag | Neue pyrimidin- und triazin-hepcidin-antagonisten |
| WO2018237084A1 (en) * | 2017-06-21 | 2018-12-27 | SHY Therapeutics LLC | COMPOUNDS INTERACTING WITH RAS SUPERFAMIL FOR USE IN THE TREATMENT OF CANCERS, INFLAMMATORY DISEASES, RASOPATHIES AND FIBROTIC DISEASES |
| WO2019222238A2 (en) * | 2018-05-15 | 2019-11-21 | Arbutus Biopharma, Inc. | Substituted 2,2'-bipyrimidinyl compounds, analogues thereof, and methods using same |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3845770A (en) | 1972-06-05 | 1974-11-05 | Alza Corp | Osmatic dispensing device for releasing beneficial agent |
| US4326525A (en) | 1980-10-14 | 1982-04-27 | Alza Corporation | Osmotic device that improves delivery properties of agent in situ |
| US5364620A (en) | 1983-12-22 | 1994-11-15 | Elan Corporation, Plc | Controlled absorption diltiazem formulation for once daily administration |
| US5023252A (en) | 1985-12-04 | 1991-06-11 | Conrex Pharmaceutical Corporation | Transdermal and trans-membrane delivery of drugs |
| US4992445A (en) | 1987-06-12 | 1991-02-12 | American Cyanamid Co. | Transdermal delivery of pharmaceuticals |
| US5001139A (en) | 1987-06-12 | 1991-03-19 | American Cyanamid Company | Enchancers for the transdermal flux of nivadipine |
| US4902514A (en) | 1988-07-21 | 1990-02-20 | Alza Corporation | Dosage form for administering nilvadipine for treating cardiovascular symptoms |
| WO2013086143A1 (en) | 2011-12-09 | 2013-06-13 | The Regents Of The University Of California | Modified mini-hepcidin peptides and methods of using thereof |
| CN102245626A (zh) | 2008-12-05 | 2011-11-16 | 加利福尼亚大学董事会 | 微型铁调素肽及其使用方法 |
| DK2968443T3 (da) | 2013-03-15 | 2021-12-06 | Protagonist Therapeutics Inc | Hepcidinanaloger og anvendelser deraf |
| WO2015042515A1 (en) | 2013-09-20 | 2015-03-26 | University Of Virginia Patent Foundation | Compositions and methods for protecting the kidney from ischemia reperfusion injury |
| US9315545B2 (en) | 2014-04-07 | 2016-04-19 | Merganser Biotech, Inc. | Hepcidin mimetic peptides and uses thereof |
| KR20170043509A (ko) | 2014-06-27 | 2017-04-21 | 프로타고니스트 테라퓨틱스, 인코포레이티드 | 헵시딘 및 미니-헵시딘 유사체 및 그의 용도 |
| WO2016109363A1 (en) | 2014-12-29 | 2016-07-07 | The Regents Of The University Of California | S-Alkylated Hepcidin Peptides and Methods of Making and Using Thereof |
| CA3002416C (en) * | 2015-10-23 | 2023-10-24 | Vifor (International) Ag | Benzimidazolyl derivatives for use as ferroportin inhibitors |
| JOP20180036A1 (ar) * | 2017-04-18 | 2019-01-30 | Vifor Int Ag | أملاح لمثبطات فروبورتين جديدة |
| JOP20190257A1 (ar) * | 2017-04-28 | 2019-10-28 | Novartis Ag | مركبات أريل غير متجانسة ثنائية الحلقة مندمجة 6-6 واستخدامها كمثبطات lats |
| ES2934492T3 (es) * | 2018-12-13 | 2023-02-22 | Global Blood Therapeutics Inc | Inhibidores de ferroportina y métodos de uso |
| AU2021263818A1 (en) * | 2020-04-28 | 2022-11-03 | Global Blood Therapeutics, Inc. | Cycloalkyl pyrimidines as ferroportin inhibitors |
-
2021
- 2021-04-28 AU AU2021263818A patent/AU2021263818A1/en active Pending
- 2021-04-28 IL IL297624A patent/IL297624B2/en unknown
- 2021-04-28 TW TW110115440A patent/TWI908795B/zh active
- 2021-04-28 WO PCT/US2021/029574 patent/WO2021222363A1/en not_active Ceased
- 2021-04-28 CA CA3180661A patent/CA3180661A1/en active Pending
- 2021-04-28 JP JP2022566040A patent/JP7742850B2/ja active Active
- 2021-04-28 BR BR112022021806A patent/BR112022021806A2/pt unknown
- 2021-04-28 CN CN202180047289.0A patent/CN115836063B/zh active Active
- 2021-04-28 EP EP21726289.8A patent/EP4143178A1/en active Pending
- 2021-04-28 MX MX2022013518A patent/MX2022013518A/es unknown
- 2021-04-28 US US17/242,731 patent/US11746100B2/en active Active
- 2021-04-28 PE PE2022002516A patent/PE20230845A1/es unknown
- 2021-04-28 KR KR1020227041423A patent/KR20230007441A/ko active Pending
- 2021-04-28 CR CR20220556A patent/CR20220556A/es unknown
-
2022
- 2022-10-18 ZA ZA2022/11401A patent/ZA202211401B/en unknown
- 2022-10-28 EC ECSENADI202284239A patent/ECSP22084239A/es unknown
- 2022-10-28 CO CONC2022/0015395A patent/CO2022015395A2/es unknown
- 2022-10-28 CL CL2022003013A patent/CL2022003013A1/es unknown
- 2022-10-28 DO DO2022000236A patent/DOP2022000236A/es unknown
-
2023
- 2023-06-15 US US18/335,480 patent/US12202817B2/en active Active
-
2024
- 2024-11-21 US US18/954,838 patent/US20250109122A1/en active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0407899A2 (de) * | 1989-07-11 | 1991-01-16 | Hoechst Schering AgrEvo GmbH | Aminopyrimidin-Derivate, Verfahren zu ihrer Herstellung, sie enthaltende Mittel und ihre Verwendung als Fungizide |
| WO2005014558A1 (en) * | 2003-08-05 | 2005-02-17 | Vertex Pharmaceuticals Incorporated | Condensed pyramidine compounds as inhibitors of voltage-gated ion channels |
| WO2011026835A1 (de) * | 2009-09-02 | 2011-03-10 | Vifor (International) Ag | Neue pyrimidin- und triazin-hepcidin-antagonisten |
| WO2018237084A1 (en) * | 2017-06-21 | 2018-12-27 | SHY Therapeutics LLC | COMPOUNDS INTERACTING WITH RAS SUPERFAMIL FOR USE IN THE TREATMENT OF CANCERS, INFLAMMATORY DISEASES, RASOPATHIES AND FIBROTIC DISEASES |
| WO2019222238A2 (en) * | 2018-05-15 | 2019-11-21 | Arbutus Biopharma, Inc. | Substituted 2,2'-bipyrimidinyl compounds, analogues thereof, and methods using same |
Non-Patent Citations (2)
| Title |
|---|
| STN: "STN检索记录一", REGISTRY, 10 January 2020 (2020-01-10) * |
| STN: "STN检索记录二", REGISTRY, 28 August 2020 (2020-08-28) * |
Also Published As
| Publication number | Publication date |
|---|---|
| US20240140932A1 (en) | 2024-05-02 |
| EP4143178A1 (en) | 2023-03-08 |
| JP2023524033A (ja) | 2023-06-08 |
| IL297624A (en) | 2022-12-01 |
| US20250109122A1 (en) | 2025-04-03 |
| WO2021222363A1 (en) | 2021-11-04 |
| TWI908795B (zh) | 2025-12-21 |
| CN115836063B (zh) | 2025-07-29 |
| CR20220556A (es) | 2022-12-15 |
| IL297624B2 (en) | 2026-04-01 |
| US12202817B2 (en) | 2025-01-21 |
| CL2022003013A1 (es) | 2023-06-30 |
| TW202206421A (zh) | 2022-02-16 |
| CO2022015395A2 (es) | 2022-11-08 |
| IL297624B1 (en) | 2025-12-01 |
| BR112022021806A2 (pt) | 2022-12-13 |
| US20220396562A1 (en) | 2022-12-15 |
| ZA202211401B (en) | 2025-04-30 |
| JP7742850B2 (ja) | 2025-09-22 |
| MX2022013518A (es) | 2023-02-01 |
| AU2021263818A1 (en) | 2022-11-03 |
| KR20230007441A (ko) | 2023-01-12 |
| DOP2022000236A (es) | 2023-01-31 |
| CA3180661A1 (en) | 2021-11-04 |
| ECSP22084239A (es) | 2023-01-31 |
| US11746100B2 (en) | 2023-09-05 |
| PE20230845A1 (es) | 2023-05-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN109195965B (zh) | Wdr5蛋白质-蛋白质结合的抑制剂 | |
| CN114437105B (zh) | 受体相互作用蛋白激酶1的抑制剂 | |
| CN104470925B (zh) | 作为激酶抑制剂的咪唑并三嗪甲腈 | |
| CN105683188B (zh) | 作为fgfr4抑制剂的稠环二环吡啶基衍生物 | |
| TW201920115A (zh) | 化合物、組合物及方法 | |
| CN107949562B (zh) | 毒蕈碱性m2受体的正性变构调节剂 | |
| CN112055709A (zh) | 吡嗪化合物和其用途 | |
| EP4423068B1 (en) | Rxfp1 agonists | |
| KR20220125278A (ko) | 비페닐 유도체 억제제, 이의 제조 방법 및 용도 | |
| EP4142732A1 (en) | Methods of use for pyrimidines as ferroportin inhibitors | |
| US20250109122A1 (en) | Cycloalkyl pyrimidines as ferroportin inhibitors | |
| CN112279837B (zh) | 吡嗪化合物和其用途 | |
| CN111747954B (zh) | 吡嗪化合物和其用途 | |
| CN110225912A (zh) | Gsk-3抑制剂 | |
| EA048667B1 (ru) | Циклоалкилпиримидины как ингибиторы ферропортина | |
| CN117597333A (zh) | 作为髓样细胞上表达的触发受体2激动剂的杂环化合物和使用方法 | |
| HK40045062A (zh) | 吡嗪化合物和其用途 | |
| HK40037929A (zh) | 吡嗪化合物和其用途 | |
| HK40037929B (zh) | 吡嗪化合物和其用途 | |
| HK40100136A (zh) | 作为lpa受体拮抗剂的三唑-吡啶基取代的氮杂环己基乙酸化合物 | |
| HK40045062B (zh) | 吡嗪化合物和其用途 | |
| HK40038625A (zh) | 吡嗪化合物和其用途 | |
| HK40068840B (zh) | 稠合吡啶酮类化合物及其制备方法和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |