TWI845890B - 苯二氮平衍生物之選擇性磺化 - Google Patents
苯二氮平衍生物之選擇性磺化 Download PDFInfo
- Publication number
- TWI845890B TWI845890B TW111103323A TW111103323A TWI845890B TW I845890 B TWI845890 B TW I845890B TW 111103323 A TW111103323 A TW 111103323A TW 111103323 A TW111103323 A TW 111103323A TW I845890 B TWI845890 B TW I845890B
- Authority
- TW
- Taiwan
- Prior art keywords
- ala
- cytotoxic agent
- imine
- cdata
- val
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D243/00—Heterocyclic compounds containing seven-membered rings having two nitrogen atoms as the only ring hetero atoms
- C07D243/06—Heterocyclic compounds containing seven-membered rings having two nitrogen atoms as the only ring hetero atoms having the nitrogen atoms in positions 1 and 4
- C07D243/10—Heterocyclic compounds containing seven-membered rings having two nitrogen atoms as the only ring hetero atoms having the nitrogen atoms in positions 1 and 4 condensed with carbocyclic rings or ring systems
- C07D243/14—1,4-Benzodiazepines; Hydrogenated 1,4-benzodiazepines
- C07D243/16—1,4-Benzodiazepines; Hydrogenated 1,4-benzodiazepines substituted in position 5 by aryl radicals
- C07D243/18—1,4-Benzodiazepines; Hydrogenated 1,4-benzodiazepines substituted in position 5 by aryl radicals substituted in position 2 by nitrogen, oxygen or sulfur atoms
- C07D243/24—Oxygen atoms
- C07D243/26—Preparation from compounds already containing the benzodiazepine skeleton
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/68035—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a pyrrolobenzodiazepine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2896—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against molecules with a "CD"-designation, not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/526—CH3 domain
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Cell Biology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
本發明係關於製備細胞結合劑-細胞毒性劑結合物之新穎方法,其中該細胞毒性劑係帶有順丁烯二醯亞胺基團之含亞胺細胞毒性劑。在一些實施例中,該細胞結合劑(CBA)透過經工程改造Cys諸如重鏈CH3域中之經工程改造Cys、在對應於抗體CBA上之EU/OU编号442位(或C442)的位置處共價連接至該細胞毒性劑。本發明亦提供藉由本發明之該等方法製備之結合物、實用於使用本發明之該等結合物於哺乳動物中抑制異常細胞生長或治療增生性病症之組成物及方法。
Description
相關申請案
本申請案根據35 U.S.C. § 119(e)主張2016年11月23日申請之美國臨時申請案第62/425,761號之申請日之權益,該案之全部內容,包括所有圖式、結構式、說明書、申請專利範圍及序列號,均以引用方式併入本文。
抗體-細胞毒性劑結合物(或「抗體-藥物結合物(ADC)」)及細胞結合劑-藥物結合物正作為跨一定範圍的癌症具有功效的一類強大的抗腫瘤劑。細胞結合劑-藥物結合物(諸如ADC)通常包含三種不同要素:細胞結合劑(
例如,抗體);連接基;及細胞毒性部分。細胞毒性藥物部分可共價連接至抗體上之離胺酸,得到結合物,該等結合物係帶有不同數目的在抗體分子之不同位置處連接的藥物之ADC之非均勻混合物。替代地,細胞毒性藥物部分可透過硫醇反應性基團諸如順丁烯二醯亞胺基團共價連接至抗體上之半胱胺酸硫醇基團以形成位點特異性ADC。抗體與細胞毒性劑之間的結合反應時常於水或水溶液中進行,其中使細胞毒性劑增溶需要少量有機溶劑。
苯二氮平化合物,包括三環苯二氮平(諸如吡咯并苯二氮平(PBD))及四環苯二氮平(諸如吲哚啉并苯二氮平),已用作與抗體鍵聯以生成ADC之細胞毒性劑,其已顯示有前景的抗腫瘤活性。此等苯二氮平化合物含有亞胺鍵,其可結合至DNA之小溝並干擾DNA功能,導致細胞死亡。苯二氮平化合物通常在水中具有非常低的溶解度。為了在與抗體之結合反應中使苯二氮平化合物增溶,需要相對大量的有機溶劑,其可使抗體不穩定。
因此,需要開發用於製備細胞結合劑及含亞胺苯二氮平藥物之結合物的新方法。
為了改良水溶性,可將含亞胺苯二氮平化合物在與抗體進行結合反應以形成抗體-苯二氮平結合物之前用亞胺反應性試劑(諸如亞硫酸氫鹽或偏亞硫酸氫鹽)處理。亞胺基團之磺化可增加苯二氮平化合物之水溶性,導致與CBA (諸如抗體)之結合反應之條件改良。然而,親核劑與α,β-不飽和羰基之間的親核加成為合成有機化學中熟知的。亞硫酸氫鹽向順丁烯二醯亞胺之活性烯烴之親核加成係此反應之一個此類實例。因此,當含亞胺苯二氮平化合物帶有順丁烯二醯亞胺時,與抗體共價鍵聯之反應性基團順丁烯二醯亞胺部分及亞胺部分均與該亞硫酸氫鹽或該偏亞硫酸氫鹽反應以形成磺化順丁烯二醯亞胺及/或磺化亞胺。意外地發現,使帶有順丁烯二醯亞胺基團之含亞胺吲哚啉并苯二氮平化合物在低pH下與亞硫酸氫鹽或偏亞硫酸氫鹽反應可選擇性地且有效地影響亞胺基團之磺化而無順丁烯二醯亞胺基團之顯著磺化,從而增加吲哚啉并苯二氮平化合物與抗體之間的結合反應之反應產率。此外,磺化吲哚啉并苯二氮平化合物具有增加的於水中之溶解度,且因此,與抗體之結合反應中需要顯著較少量的有機溶劑(
例如,DMA)。結合反應中大量有機溶劑之存在可使抗體不穩定。
本發明提供一種用於製備細胞結合劑-細胞毒性劑結合物之新穎方法,該細胞結合劑-細胞毒性劑結合物包含帶有順丁烯二醯亞胺基團之含亞胺細胞毒性劑,該順丁烯二醯亞胺基團共價連接至細胞結合劑(CBA)。在一些實施例中,本發明提供一種製備細胞結合劑-細胞毒性劑結合物之方法,其包含以下步驟:
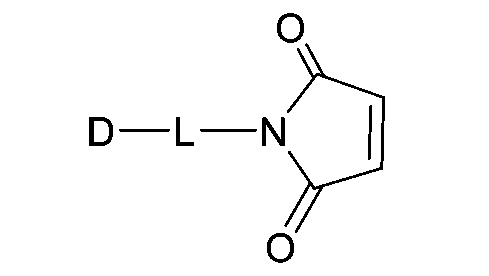
(a)使由下式表示之含亞胺細胞毒性劑或其醫藥學上可接受之鹽中亞胺部分:
與二氧化硫、亞硫酸氫鹽、或偏亞硫酸氫鹽於pH 1.9至5.0之水溶液中反應以形成包含由下式表示之經修飾亞胺部分之經修飾細胞毒性劑:
或其醫藥學上可接受之鹽;以及
(b)使該經修飾細胞毒性劑與細胞結合劑反應以形成該細胞結合劑-細胞毒性劑結合物,
其中D係含亞胺細胞毒性化合物;且L係連接基。
在一些實施例中,D係含亞胺三環或四環苯二氮平化合物。
在一些實施例中,D係含亞胺三環苯二氮平化合物。
在一些實施例中,D係含亞胺四環苯二氮平化合物。
如本文所用,含亞胺三環苯二氮平化合物係指具有稠合至苯二氮平核心之二氮平部分之單環的化合物。單環可含有一或多個額外雜原子諸如氧、硫、或氮,及取代基諸如單環或多環。示範性三環苯二氮平化合物包括但不限於吡咯并苯二氮平(PBD),諸如WO2010/043880、WO2011/130616、WO2009/016516、WO 2013/177481、及WO 2012/112708中所述者。
如本文所用,含亞胺四環苯二氮平化合物係指具有稠合至苯二氮平核心之二氮平部分之雙環的化合物。該雙環係視情況含有一或多個額外雜原子諸如氧、硫、或氮之稠合雙環。示範性四環苯二氮平化合物包括但不限於吲哚啉并苯二氮平(IGN),諸如WO/2010/091150及WO 2012/128868中所述者。
在一些實施例中,D係吲哚啉并苯二氮平。
在一些實施例中,D係吡咯并苯二氮平(PBD)。
本發明亦提供藉由本文所述之方法製備之細胞結合劑-細胞毒性劑結合物及經修飾細胞毒性劑。
應理解,除非明確否決或不適當,否則本文所述之任何實施例,包括僅在本發明之一個態樣下而非其他態樣所述之實施例,且包括僅出現於實例中之實施例,可與任何一或多個其他實施例組合。
現將詳細參照本發明某些實施例,該等實施例之實例以所附結構及式予以說明。儘管本發明將結合列舉之實施例進行描述,但應瞭解,其不欲將本發明局限於該等實施例。相反,本發明意欲涵蓋可包括在由申請專利範圍所界定之本發明範疇內的所有替代物、修改、及等效物。熟習此項技術者將認識到與本文所述者類似或等效之許多方法及材料,其可用於實踐本發明。
應瞭解,除非明確否決或不適當,否則本文所述之任一實施例,包括在本發明不同態樣及本說明書不同部分(包括僅在實例中所述之實施例)下所述者,可與本發明一或多個其他實施例組合。實施例組合不限於經由多個獨立申請專利範圍主張之該等具體組合。
定義
如本文所用之「
烷基」或「
直鏈或
支鏈烷基」係指飽和直鏈或支鏈單價烴基。在較佳實施例中,直鏈或支鏈烷基具有三十個或更少碳原子(
例如,直鏈烷基為C
1-C
30且支鏈烷基為C
3-C
30),且更佳二十個或更少碳原子。甚至更佳的是,直鏈或支鏈烷基具有十個或更少碳原子(
亦即,直鏈烷基為C
1-C
10且支鏈烷基為C
3-C
10)。在其他實施例中,直鏈或支鏈烷基具有六個或更少碳原子(
亦即,直鏈烷基為C
1-C
6或支鏈烷基為C
3-C
6)。烷基之實例包括但不限於甲基、乙基、1-丙基、2-丙基、1-丁基、2-甲基-1-丙基、-CH
2CH(CH
3)
2)、2-丁基、2-甲基-2-丙基、1-戊基、2-戊基 3-戊基、2-甲基-2-丁基、3-甲基-2-丁基、3-甲基-1-丁基、2-甲基-1-丁基、1-己基)、2-己基、3-己基、2-甲基-2-戊基、3-甲基-2-戊基、4-甲基-2-戊基、3-甲基-3-戊基、2-甲基-3-戊基、2,3-二甲基-2-丁基、3,3-二甲基-2-丁基、1-庚基、1-辛基、及其類似基團。此外,本說明書、實例、及申請專利範圍通篇所使用之術語「烷基」意欲包括「未取代烷基」及「經取代烷基」,其後者係指具有置換烴骨幹之一或多個碳上之氫的取代基的烷基部分。如本文所用,(C
x-C
xx)烷基或C
x-xx烷基意指具有x-xx個碳原子之直鏈或支鏈烷基。
「
烯基」或「
直鏈或
支鏈烯基」係指具有二至二十個碳原子及至少一個不飽和位點(
亦即,碳-碳雙鍵)之直鏈或支鏈單價烴基,其中烯基包括具有「順式」及「反式」定向或者「E」及「Z」定向之基團。實例包括但不限於乙烯基(ethylenyl或vinyl,-CH=CH
2)、烯丙基(-CH
2CH=CH
2)、及其類似基團。較佳的是,烯基具有二至十個碳原子。更佳的是,烷基具有二至四個碳原子。
「
炔基」或「
直鏈或
支鏈炔基」係指具有二至二十個碳原子及至少一個不飽和位點(
亦即,碳-碳參鍵)之直鏈或支鏈單價烴基。實例包括但不限於乙炔基、丙炔基、1-丁炔基、2-丁炔基、1-戊炔基、2-戊炔基、3-戊炔基、己炔基、及其類似基團。較佳的是,炔基具有二至十個碳原子。更佳的是,炔基具有二至四個碳原子。
術語「
環狀烷基」及「
環烷基」可互換使用。如本文所用,該術語係指飽和碳環之基團。在較佳實施例中,環烷基在其環結構中具有3至10個碳原子,且更佳在環結構中具有5至7個碳原子。在一些實施例中,兩個環可具有共同的二或更多個原子,
例如,該等環為「稠環」。合適環烷基包括但不限於環庚基、環己基、環戊基、環丁基、及環丙基。在一些實施例中,環烷基為單環基團。在一些實施例中,環烷基為雙環基團。在一些實施例中,環烷基為三環基團。
術語「
環烷基烷基」係指上文所述之經環烷基取代之烷基。
術語「
環狀烯基」係指在環結構中具有至少一個雙鍵之碳環基團。
術語「
環狀炔基」係指在環結構中具有至少一個參鍵之碳環基團。
如本文所用之術語「
芳基」包括經取代或未取代之單環芳族基團,其中各環原子係碳。較佳的是,該環係5至7員環,更佳6員環。芳基包括但不限於苯基、苯酚、苯胺、及其類似基團。術語「芳基」亦包括具有其中二或更多個原子為兩個鄰接環(
例如,該等環係「稠環」)所共有之二或更多個環的「多環基」、「多環(polycycle)」、及「多環(polycyclic)」系統,其中該等環之至少一者係芳族,
例如,其他環可係環烷基、環烯基、環炔基、或芳族環。在一些較佳實施例中,多環具有2-3個環。在某些較佳實施例中,多環系統具有其中兩個環係芳族的兩個環。該多環之各環可係經取代或未取代。在某些實施例中,該多環之各環在環中含有3至10個碳原子,較佳5至7個。例如,芳基包括但不限於苯基(苯)、甲苯基、蒽基、茀基、茚基、薁基、及萘基、以及苯并稠合碳環部分諸如5,6,7,8-四氫萘基及其類似基團。在一些實施例中,芳基係單環芳族基團。在一些實施例中,芳基係二環芳族基團。在一些實施例中,芳基係三環芳族基團。
如本文所用之術語「
雜環 (heterocycle)」、「
雜環基」、及「
雜環 (heterocyclic ring)」係指3至18員環、較佳3至10員環、更佳3至7員環之經取代或未取代非芳族環結構,其環結構包括至少一個雜原子、較佳一至四個雜原子、更佳一個或兩個雜原子。在某些實施例中,該環結構可具有兩個環。在一些實施例中,兩個環可具有共同的二或更多個原子,
例如,該等環為「稠環」。雜環基包括例如哌啶、哌嗪、吡咯啶、嗎啉、內酯、內醯胺、及其類似基團。雜環描述於Paquette, Leo A.; 「Principles of Modern Heterocycle Chemistry」(W. A. Benjamin, New York, 1968),尤其第1、3、4、6、7、及9章;「The Chemistry of Heterocyclic Compounds, A series of Monographs」(John Wiley & Sons, New York, 1950出版),尤其第13、14、16、19、及28卷;及J. Am. Chem. Soc. (1960) 82:5566。雜環之實例包括但不限於四氫呋喃、二氫呋喃、四氫噻吩(tetrahydrothiene)、四氫哌喃、二氫哌喃、四氫硫哌喃、硫嗎啉、噻噁烷、高哌嗪、吖呾、氧呾、硫呾、高哌啶、哌啶、哌嗪、吡咯啶、嗎啉、噁庚環、噻庚環、噁氮平、二氮平、噻氮平(thiazepine)、2-吡咯啉、3-吡咯啉、吲哚啉、2H-哌喃、4H-哌喃、二噁烷、1,3-二氧戊環、吡唑啉、二噻口山、二硫戊環、二氫哌喃、二氫噻吩、二氫呋喃、吡唑啶基咪唑啶、咪唑啶、3-氮雜雙環[3.1.0]己烷、3-氮雜雙環[4.1.0]庚烷、及氮雜雙環[2.2.2]己烷。螺環部分亦包括在此定義之範疇內。環原子經側氧基(=O)部分取代之雜環基團之實例為嘧啶酮及1,1-二側氧基-硫嗎啉基。
如本文所用之術語「
雜芳基」係指環結構包括至少一個雜原子(
例如,O、N、或S)、較佳一至四個或一至三個雜原子、更佳一或兩個雜原子之經取代或未取代芳族單環結構,較佳5至7員環、更佳5至6員環。當二或更多個雜原子存在於雜芳環中時,其可相同或不同。術語「雜芳基」亦包括具有其中二或更多個環原子為兩個鄰接環(
例如,該等環係「稠環」)所共有之二或更多個環之「多環基」、「多環」、及「多環」系統,其中該等環之至少一者係雜芳族,
例如,其他環可係環烷基、環烯基、環炔基、芳基、雜芳族、及/或雜環。在一些較佳實施例中,多環雜芳基具有2-3個環。在某些實施例中,較佳多環雜芳基具有其中兩個環係芳族的兩個環。在某些實施例中,該多環之各環在環中含有3至10個原子,較佳在環中具有5至7個原子。例如,雜芳基包括但不限於吡咯、呋喃、噻吩、咪唑、噁唑、噻唑、吡唑、吡啶、吡嗪、噠嗪、喹啉、嘧啶、吲哚嗪、吲哚、吲唑、苯并咪唑、苯并噻唑、苯并呋喃、苯并噻吩、口辛啉、酞嗪、喹唑啉、咔唑、啡噁嗪、喹啉、嘌呤、及其類似物。在一些實施例中,雜芳基係單環芳族基團。在一些實施例中,雜芳基係二環芳族基團。在一些實施例中,雜芳基係三環芳族基團。
可能時,雜環或雜芳基可為碳(碳連接)或氮(氮連接)連接的。例如且不限於,碳鍵接之雜環或雜芳基係在吡啶之2、3、4、5或6位;噠嗪之3、4、5或6位;嘧啶之2、4、5或6位;吡嗪之2、3、5或6位;呋喃、四氫呋喃、硫呋喃、噻吩、吡咯或四氫吡咯之2、3、4或5位;噁唑、咪唑或噻唑之2、4或5位;異噁唑、吡唑或異噻唑之3、4或5位;氮雜環丙烷之2或3位;氮雜環丁烷之2、3或4位;喹啉之2、3、4、5、6、7或8位;或異喹啉之1、3、4、5、6、7或8位鍵接。
例如且不限於,氮鍵結之雜環或雜芳基係在氮丙啶、吖呾、吡咯、吡咯啶、2-吡咯啉、3-吡咯啉、咪唑、咪唑啶、2-咪唑啉、3-咪唑啉、吡唑、吡唑啉、2-吡唑啉、3-吡唑啉、哌啶、哌嗪、吲哚、吲哚啉、1H-吲唑之1位;異吲哚或異吲哚啉之2位;嗎啉之4位;及咔唑或或O-咔啉之9位鍵結。
雜芳基或雜環基中存在之雜原子包括氧化形式諸如NO、SO、及SO
2。
術語「
鹵基」或「
鹵素」係指氟(F)、氯(Cl)、溴(Br)、或碘(I)。
如本文所用,術語「
鹵烷基」係指經一或多個如本文定義之鹵基取代之如本文定義之烷基。鹵基烷基可係單鹵基烷基、二鹵基烷基、或多鹵基烷基。單鹵基烷基可具有一個氟、氯、溴、或碘取代基。二鹵烷基或多鹵烷基可經二或更多個相同鹵原子或不同鹵基之組合取代。鹵烷基之實例包括但不限於氟甲基、二氟甲基、三氟甲基、氯甲基、二氯甲基、三氯甲基、五氟乙基、七氟丙基、二氟氯甲基、二氯氟甲基、二氟乙基、二氟丙基、二氯乙基、及二氯丙基。
本文所用之「
烷氧基」係指烷基-O-,其中烷基係在上文中加以定義。烷氧基之實例包括但不限於甲氧基、乙氧基、丙氧基、2-丙氧基、丁氧基、第三丁氧基、戊氧基、己氧基、及其類似基團。
上文所述之烷基、鹵烷基、烷氧基、烯基、炔基、環狀烷基、環狀烯基、環狀炔基、碳環基、芳基、雜環基、及雜芳基可視情況經一或多個(
例如,2、3、4、5、6、或更多個)取代基取代。
除非明確陳述為「未取代」,否則對本文化學部分之參考理解為亦包括經取代變異體。例如,對「烷基」或部分之參考隱含包括經取代及未取代變異體。化學部分上取代基之實例包括但不限於鹵素、羥基、羰基(諸如羧基、烷氧基羰基、甲醯基、或醯基)、硫羰基(諸如硫酯、硫乙酸酯、或硫甲酸酯)、烷氧基、烷基硫基、醯氧基、磷醯基、磷酸酯、膦酸酯、胺基、醯胺基、脒、亞胺、氰基、硝基、疊氮基、巰基、烷基噻、硫酸酯、磺酸酯、胺磺醯基、磺醯胺基、磺醯基、雜環基、芳烷基、或芳基或雜芳基部分。
「視情況(optional或optionally)」意指隨後描述之情況可能發生或可能不發生,使得本申請案包括情況發生之情形及情況不發生之情形。例如,短語「視情況經取代」意指非氫取代基可能或可不存在於給定原子上,且因此,本申請書包括其中存在非氫取代基之結構及其中不存在非氫取代基之結構。
術語「經取代」係指部分具有置換一或多個碳、氮、氧、或硫原子上氫之取代基。應瞭解「取代」或「經…取代」包括隱含限制條件,即此取代符合取代之原子及取代基之允許價態,且取代產生穩定化合物,例如不自發經受諸如藉由重排、環化、消除等所達成之轉化之穩定化合物。如本文所用,術語「經取代」意欲包括有機化合物之所有可允許取代基。在一廣泛態樣中,可允許之取代基包括有機化合物之非環及環狀、支鏈及非支鏈、碳環及雜環、芳族及非芳族取代基。對於適當有機化合物,可允許取代基可為一或多種取代基且可為相同或不同。出於本發明之目的,諸如氮之雜原子可具有氫取代基及/或本文所述之有機化合物之滿足雜原子價態的任何可允許取代基。取代基可包括本文所述之任何取代基,例如,鹵素、羥基、羰基(諸如羧基、烷氧基羰基、甲醯基、或醯基)、硫羰基(諸如硫酯、硫乙酸酯、或硫甲酸酯)、烷氧基、烷基硫基、醯氧基、磷醯基、磷酸酯、膦酸酯、胺基、醯胺基、脒、亞胺、氰基、硝基、疊氮基、巰基、烷基硫基、硫酸酯、磺酸酯、胺磺醯基、磺醯胺基、磺醯基、雜環基、芳烷基、或其芳族或雜芳族部分。為了說明,單氟烷基為經氟取代基取代之烷基,且二氟烷基為經兩個氟取代基取代之烷基。應認識到,若在取代基上存在一個以上取代,則各非氫取代基可相同或不同(除非另外說明)。
若一取代基之碳描述為視情況經取代基清單中之一或多者取代,則該碳上之一或多個氫(在存在的氫原子數情況下)可單獨及/或一起經獨立選擇之視情況選用之取代基置換。若一取代基之氮描述為視情況經取代基清單中之一或多者取代,則該氮上之一或多個氫(在存在的氫原子數情況下)可各自經獨立選擇之視情況選用之取代基置換。一個示範性取代基可描述為-NR'R'',其中R'及R''連同其所連接之氮原子一起可形成雜環。由R'及R''連同其所連接之氮原子一起形成之雜環可為部分或完全飽和的。在一些實施例中,雜環由3至7個原子組成。在其他實施例中,雜環選自由以下所組成之群:吡咯基、咪唑基、吡唑基、三唑基、四唑基、異噁唑基、吡啶基、及噻唑基。
本說明書可互換使用術語「
取代基」及「
基團 (radical/group)」。
若一組取代基統一描述為視情況經取代基清單中之一或多者取代,則該組可包括:(1)不可取代之取代基、(2)未經視情況之取代基取代的可取代之取代基、及/或(3)經一或多個視情況選用之取代基取代之可取代之取代基。
若一取代基描述為視情況經至多特定數量之非氫取代基取代,則該取代基可為(1)未取代的;或(2)經至多該特定數量之非氫取代基或取代基上至多最大數量之可取代位置取代,以數量較少者為準。因此,例如,若一取代基描述為視情況經至多3個非氫取代基取代之雜芳基,則具有少於3個可取代位置之任何雜芳基將視情況經至多僅該雜芳基所具有之可取代位置之數量的非氫取代基取代。在非限制性實例中,此類取代基可選自具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基,芳基,雜芳基,雜環基,鹵素,鈲[-NH(C=NH)NH
2],-OR
100,NR
101R
102,-NO
2,-NR
101COR
102,-SR
100,由-SOR
101表示之亞碸,由-SO
2R
101表示之碸,磺酸酯-SO
3M,硫酸酯-OSO
3M,由-SO
2NR
101R
102表示之磺醯胺,氰基,疊氮基,-COR
101,-OCOR
101,-OCONR
101R
102,及聚乙二醇單元(-OCH
2CH
2)
nR
101,其中M係H或陽離子(諸如Na
+或K
+);R
101、R
102、及R
103各獨立選自H,具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元(-OCH
2CH
2)
n-R
104(其中n係整數1至24),具有6至10個碳原子之芳基,具有3至10個碳原子之雜環,及具有5至10個碳原子之雜芳基;且R
104係H或具有1至4個碳原子之直鏈或支鏈烷基,其中由R
100、R
101、R
102、R
103、及R
104表示之基團中之烷基、烯基、炔基、芳基、雜芳基、及雜環己視情況經一或多個(
例如,2、3、4、5、6、或更多個)獨立選自鹵素、-OH、-CN、-NO
2、及具有1至4個碳原子之直鏈或支鏈烷基之取代基取代。較佳的是,上文所述之視情況經取代烷基、烯基、炔基、環狀烷基、環狀烯基、環狀炔基、碳環基、芳基、雜環基、及雜芳基之取代基包括鹵素、-CN、-NR
102R
103、-CF
3、-OR
101、芳基、雜芳基、雜環基、-SR
101、-SOR
101、-SO
2R
101、及-SO
3M。
基團中之碳原子數在本文中藉由字首「C
x-xx」或「C
x-C
xx」指定,其中x及xx為整數。例如,「C
1-4烷基」或「C1-C4烷基」為具有1至4個碳原子之烷基。
術語「
化合物」或「
細胞毒性化合物」、「
細胞毒性二聚體」及「
細胞毒性二聚體化合物」可互換使用。其意欲包括結構或式或其任何衍生物已經揭示於本發明中或結構或式或其任何衍生物以引用方式併入的化合物。該術語亦包括本發明中揭示之所有式之化合物之立體異構物、幾何異構物、互變異構物、溶劑合物、代謝物、鹽(
例如,醫藥學上可接受之鹽)以及前藥及前藥鹽。該術語亦包括前述任一者之任何溶劑合物、水合物、及多形體。在本申請案中所述本發明某些態樣中「立體異構物」、「幾何異構物」、「互變異構物」、「溶劑合物」、「代謝物」、「鹽」、「前藥」、「前藥鹽」、「結合物」、「結合物鹽」、「溶劑合物」、「水合物」、或「多形體」之具體陳述不應解釋為意欲在術語「化合物」之使用未用該等其他形式陳述之本發明其他態樣中省略該等形式。
如本文使用之術語「
結合物」係指連接至細胞結合劑之本文所述化合物或其衍生物。
如本文所用,術語「
可連接至細胞結合劑」係指本文所述之化合物或其衍生物包含至少一個合適於將該等化合物或其衍生物鍵結至細胞結合劑之連接基團或其前驅物。
術語給定基團之「
前驅物」係指可藉由任何脫保護、化學改質、或偶合反應產生該基團之任何基團。
術語「
對掌性」係指分子具有與鏡像搭配物不可重疊之性質,而術語「非對掌性」係指分子可重疊於其鏡像搭配物上。
術語「
立體異構物」係指具有相同化學構成及連接性但原子之空間定向不同,無法藉由圍繞單鍵之旋轉而相互轉化的化合物。
「
非鏡像異構物」係指具有二或更多個對掌性中心且分子不互為鏡像之立體異構物。非鏡像異構物具有不同物理性質,
例如熔點、沸點、光譜性質、及反應性。非鏡像異構物之混合物可在諸如結晶、電泳、及層析之高解析度分析程序下分離。
「
鏡像異構物」係指化合物之兩個互為不可重疊鏡像之立體異構物。
本文使用之立體化學定義及慣例通常遵循S. P. Parker編, McGraw-Hill Dictionary of Chemical Terms(1984) McGraw-Hill Book Company, New York;及Eliel, E.及Wilen, S., 「Stereochemistry of Organic Compound,」 John Wiley & Sons, Inc., New York, 1994。本發明化合物可含有不對稱或對掌性中心,且因此以不同立體異構形式存在。意欲本發明化合物之所有立體異構形式,包括但不限於非鏡像異構物、鏡像異構物、及阻轉異構物,以及其混合物(諸如外消旋混合物),均形成本發明之一部分。許多有機化合物以光學活性形式存在,
亦即,其能夠使平面偏振光之平面旋轉。在描述光學活性化合物時,字首D及L、或R及S用於表示分子圍繞其對掌性中心之絕對組態。字首d及l或(+)及(-)用於表示化合物旋轉平面偏振光之符號,其中(-)或l意指該化合物為左旋的。字首為(+)或d之化合物為右旋的。對於給定化學結構,此等立體異構物相同,除了其互為鏡像。特定立體異構物亦可稱為鏡像異構物,且此類異構物之混合物常稱為鏡像異構混合物。鏡像異構物之50:50混合物稱為外消旋混合物或外消旋物,其可在化學反應或製程中不存在立體選擇或立體特異性時存在。術語「外消旋混合物」及「外消旋物」係指兩種鏡像異構物質之缺乏光學活性之等莫耳混合物。
術語「
互變異構物」或「
互變異構形式」係指具有不同能量之結構異構物,其可經由低能障壁相互轉化。例如,質子互變異構物(亦稱為質子轉移互變異構物)包括經由質子遷移發生之相互轉化,諸如酮基-烯醇及亞胺-烯胺異構化。價態互變異構物包括藉由一些鍵結電子之重排發生之相互轉化。
如本文使用,「
苯二氮平」化合物係具有苯二氮平核心結構之化合物。苯二氮平核心可係經取代或未取代、及/或與一或多個環結構稠合。其亦包括具有兩個藉由連接基連接之苯二氮平核心之化合物。作為苯二氮平核心之部分之亞胺官能基(-C=N-)可經還原。
如本文所用,「
吡咯并苯二氮平」(PBD)化合物係具有吡咯并苯二氮平核心結構之化合物。吡咯并苯二氮平可經取代或未取代。其亦包括具有兩個藉由連接基連接之吡咯并苯二氮平之化合物。作為吲哚啉并苯二氮平核心之部分之亞胺官能基(-C=N-)可經還原。
在某些實施例中,吡咯并苯二氮平化合物包含由
表示之核心結構,其可視情況經取代。
在某些實施例中,吡咯并苯二氮平化合物包含由
表示之核心結構,其可視情況經取代。
如本文所用,「
吲哚啉并苯
二氮平」(IGN)化合物係具有吲哚啉并苯二氮平核心結構之化合物。吲哚啉并苯二氮平可經取代或未取代。其亦包括具有兩個藉由連接基連接之吲哚啉并苯二氮平之化合物。作為吲哚啉并苯二氮平核心之部分之亞胺官能基(-C=N-)可經還原。
在某些實施例中,吲哚啉并苯二氮平化合物包含由
表示之核心結構,其可視情況經取代。
在一些實施例中,吲哚啉并苯二氮平化合物包含由
表示之核心結構,其可進一步經取代。
如本文使用之短語「
醫藥學上可接受之鹽」係指本發明化合物之醫藥學上可接受之有機或無機鹽。示範性鹽包括但不限於硫酸鹽、檸檬酸鹽、乙酸鹽、草酸鹽、氯化物、溴化物、碘化物、硝酸鹽、硫酸氫鹽、磷酸鹽、酸式磷酸鹽、異菸鹼酸鹽、乳酸鹽、柳酸鹽、酸式檸檬酸鹽、酒石酸鹽、油酸鹽、丹寧酸鹽、泛酸鹽、酒石酸氫鹽、抗壞血酸鹽、琥珀酸鹽、順丁烯二酸鹽、龍膽酸鹽(gentisinate)、反丁烯二酸鹽、葡糖酸鹽、葡糖醛酸鹽、蔗糖酸鹽、甲酸鹽、苯甲酸鹽、麩胺酸鹽、甲烷磺酸鹽「甲磺酸鹽」、乙烷磺酸鹽、苯磺酸鹽、對甲苯磺酸鹽、帕莫酸鹽(pamoate) (
亦即,1,1'-亞甲基-雙-(2-羥基-3-萘酸鹽))、鹼金屬(
例如,鈉及鉀)鹽、鹼土金屬(
例如,鎂)鹽、及銨鹽。醫藥學上可接受之鹽可涉及包括另一分子,諸如乙酸根離子、琥珀酸根離子、或其他相對離子。該相對離子可為使親體化合物上之電荷穩定的任何有機或無機部分。此外,醫藥學上可接受之鹽之結構中可具有一個以上帶電原子。多個帶電原子為醫藥學上可接受之鹽之一部分的情況可具有多個相對離子。因此,醫藥學上可接受之鹽可具有一或多個帶電原子及/或一或多個相對離子。
若本發明化合物為鹼,則所需醫藥學上可接受之鹽可藉由此項技術中可用之任何合適方法製備,例如用諸如鹽酸、氫溴酸、硫酸、硝酸、甲烷磺酸、磷酸、及其類似酸之無機酸或用諸如乙酸、順丁烯二酸、琥珀酸、扁桃酸、反丁烯二酸、丙二酸、丙酮酸、草酸、乙醇酸、水楊酸、哌喃糖苷酸(pyranosidyl acid) (諸如葡糖醛酸或半乳糖醛酸)、α羥基酸(諸如檸檬酸或酒石酸)、胺基酸(諸如天冬胺酸或麩胺酸)、芳族酸(諸如苯甲酸或肉桂酸)、磺酸(諸如對甲苯磺酸或乙烷磺酸)、或其類似酸之有機酸處理遊離鹼。
若本發明之化合物為酸,則所需醫藥學上可接受之鹽可藉由任何合適之方法製備,例如用諸如胺(一級、二級、或三級胺)、鹼金屬氫氧化物或鹼土金屬氫氧化物、或其類似鹼之無機或有機鹼處理遊離酸。合適之鹽之說明性實例包括但不限於衍生自胺基酸(諸如甘胺酸及精胺酸)、氨、一級胺、二級胺、及三級胺、及環狀胺(諸如哌啶、嗎啉、及哌嗪)之有機鹽,以及衍生自鈉、鈣、鉀、鎂、錳、鐵、銅、鋅、鋁、及鋰之無機鹽。
如本文所用,術語「
溶劑合物」意指進一步包括藉由非共價分子間力結合之化學計量或非化學計量之量的溶劑(諸如水、異丙醇、丙酮、乙醇、甲醇、DMSO、乙酸乙酯、乙酸以及乙醇胺二氯甲烷、2-丙醇、或其類似溶劑)的化合物。化合物之溶劑合物或水合物易於藉由將至少一莫耳當量羥基溶劑(諸如甲醇、乙醇、1-丙醇、2-丙醇、或水)添加至化合物以得到亞胺部分之溶劑化或水合作用來製備。
短語「
醫藥學上可接受之」表示物質或組成物必須與構成調配物之其他成分及/或用其治療之哺乳動物在化學上及/或毒理學上相容。
術語「
保護基」或「
保護部分」係指常用於在化合物、其衍生物、或其結合物上之其他官能基反應時阻斷或保護特定官能基的取代基。例如,「
胺保護基」或「
胺基保護部分」為連接至胺基以阻斷或保護化合物中之胺基官能基的取代基。此類基團為此項技術中熟知的(參見例如P. Wuts及T. Greene, 2007, Protective Groups in Organic Synthesis, 第7章, J. Wiley & Sons, NJ)且例證為胺基甲酸酯,諸如胺基甲酸甲酯及胺基甲酸乙酯、FMOC、經取代胺基甲酸乙酯、藉由1,6-β-消除反應(亦稱「
自消耗 (self immolative)」)裂解之胺基甲酸酯;脲;醯胺;肽;烷基及芳基衍生物。合適之胺基保護基包括乙醯基、三氟乙醯基、第三丁氧羰基(BOC)、苯甲氧基羰基(CBZ)及9-茀基亞甲基氧基羰基(Fmoc)。有關保護基及其應用之一般描述,
參見P. G.M. Wuts & T. W. Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, New York, 2007。
術語「
離去基團」係指一組在取代或置換期間離去之帶電或不帶電部分。此類離去基團為此項技術中熟知的,且包括但不限於鹵素、酯、烷氧基、羥基、甲苯磺酸酯、三氟甲磺酸酯、甲磺酸酯、腈、疊氮基、胺基甲酸酯、二硫化物、硫酯、硫醚、及重氮化合物。
術語「
雙官能交聯劑」、「
雙官能連接基」、或「
交聯劑」係指具有兩個反應性基團之改質劑;該兩個反應性基團之一者能夠與細胞結合劑反應,而另一者與細胞毒性化合物反應,以將兩個部分連接在一起。此類雙官能交聯劑為此項技術中熟知的(參見例如Isalm及Dent 於
Bioconjugation第5章, 第218-363頁, Groves Dictionaries Inc. New York, 1999中)。例如,能夠經由硫醚鍵鍵聯之雙官能交聯劑包括用以引入順丁烯二醯亞胺基之
N-琥珀醯亞胺基-4-(N-順丁烯二醯亞胺基甲基)-環己烷-1-甲酸酯(SMCC)或用以引入碘代乙醯基之
N-琥珀醯亞胺基-4-(碘代乙醯基)-胺基苯甲酸酯(SIAB)。將順丁烯二醯亞胺基或鹵代乙醯基引入細胞結合劑上之其他雙官能交聯劑為此項技術中熟知的(參見美國專利申請案2008/0050310、20050169933,可從Pierce Biotechnology Inc. P.O. Box 117, Rockland, IL 61105, USA獲得)且包括但不限於雙-順丁烯二醯亞胺基聚乙二醇(BMPEO)、BM(PEO)
2、BM(PEO)
3、N-(β-順丁烯二醯亞胺基丙氧基)琥珀醯亞胺酯(BMPS)、γ-順丁烯二醯亞胺基丁酸N-琥珀醯亞胺酯(GMBS)、ε-順丁烯二醯亞胺基己酸N-羥基琥珀醯亞胺酯(EMCS)、5-順丁烯二醯亞胺基戊酸NHS、HBVS、N-琥珀醯亞胺基-4-(N-順丁烯二醯亞胺基甲基)-環己烷-1-羧基-(6-醯胺基己酸酯)(其為SMCC(LC-SMCC)之「長鏈」類似物)、間順丁烯二醯亞胺基苯甲醯基-N-羥基琥珀醯亞胺酯(MBS)、4-(4-N-順丁烯二醯亞胺基苯基)-丁醯肼或鹽酸鹽(MPBH)、N-琥珀醯亞胺基3-(溴乙醯胺基)丙酸酯(SBAP)、N-琥珀醯亞胺基碘代乙酸酯(SIA)、κ-順丁烯二醯亞胺基十一烷酸N-琥珀醯亞胺酯(KMUA)、N-琥珀醯亞胺基4-(對順丁烯二醯亞胺基苯基)-丁酸酯(SMPB)、琥珀醯亞胺基-6-(β-順丁烯二醯亞胺基丙醯胺)己酸酯(SMPH)、琥珀醯亞胺基-(4-乙烯基磺醯基)苯甲酸酯(SVSB)、二硫代雙-順丁烯二醯亞胺基乙烷(DTME)、1,4-雙-順丁烯二醯亞胺基丁烷(BMB)、1,4雙順丁烯二醯亞胺基-2,3-二羥基丁烷(BMDB)、雙-順丁烯二醯亞胺基己烷(BMH)、雙-順丁烯二醯亞胺基乙烷(BMOE)、磺基琥珀醯亞胺基4-(N-順丁烯二醯亞胺基-甲基)環己烷-1-甲酸酯(磺基-SMCC)、磺基琥珀醯亞胺基(4-碘-乙醯基)胺基苯甲酸酯(磺基-SIAB)、間順丁烯二醯亞胺基苯甲醯基-N-羥基磺基琥珀醯亞胺酯(磺基-MBS)、N-(γ-順丁烯二醯亞胺基丁醯氧基)磺基琥珀醯亞胺酯(磺基-GMBS)、N-(ε-順丁烯二醯亞胺基己醯氧基)磺基琥珀醯亞胺酯(磺基-EMCS)、N-(κ-順丁烯二醯亞胺基十一烷醯基)磺基琥珀醯亞胺酯(磺基-KMUS)、及磺基琥珀醯亞胺基4-(對順丁烯二醯亞胺基苯基)丁酸酯(磺基-SMPB)。
異雙官能交聯劑為具有兩個不同反應性基團之雙官能交聯劑。亦可使用含有胺反應性
N-羥基琥珀醯亞胺基(NHS基團)及羰基反應性肼基之異雙官能交聯劑將本文所述細胞毒性化合物與細胞結合劑(
例如,抗體)連接。該等市售異雙官能交聯劑之實例包括琥珀醯亞胺基6-肼基菸醯胺丙酮腙(SANH)、琥珀醯亞胺基4-肼基對苯二甲酸酯鹽酸鹽(SHTH)、及琥珀醯亞胺基肼菸酸酯鹽酸鹽(SHNH)。帶有酸不穩定鍵聯之連結物亦可使用帶有肼之本發明苯并二氮呯衍生物製備。可使用之雙官能交聯劑之實例包括琥珀醯亞胺基-對甲醯基苯甲酸酯(SFB)及琥珀醯亞胺基-對甲醯基苯氧基乙酸酯(SFPA)。
能夠經由二硫鍵將細胞結合劑與細胞毒性化合物鍵聯之雙官能交聯劑為此項技術中已知的且包括用以引入二硫吡啶基之
N-琥珀醯亞胺基-3-(2-吡啶基二硫基)丙酸酯(SPDP)、
N-琥珀醯亞胺基-4-(2-吡啶基二硫基)戊酸酯(SPP)、
N-琥珀醯亞胺基-4-(2-吡啶基二硫基)丁酸酯(SPDB)、
N-琥珀醯亞胺基-4-(2-吡啶基二硫基)2-磺基丁酸酯(磺基-SPDB)。可用以引入二硫基團之其他雙官能交聯劑為此項技術中已知的且揭示於:美國專利6,913,748、6,716,821、及US專利公開案20090274713及20100129314,所有該等專利皆以引用方式併入本文中。替代地,亦可使用交聯劑諸如2-亞胺基硫雜環戊烷、高半胱胺酸硫內酯、或S-乙醯基琥珀酸酐引入硫醇基。
如本文所定義,「
連接基」、「
連接部分」、或「
連接基團」係指將兩個基團(諸如細胞結合劑及細胞毒性化合物)連接在一起之部分。通常,連接基在連接其所連接之兩個基團之條件下實質上呈惰性。雙官能交聯劑可包含兩個反應性基團,在連接基部分各端各一個,以致一個反應性基團可首先與細胞毒性化合物反應以提供帶有連接基部分及第二反應性基團之化合物,該化合物然後可與細胞結合劑反應。替代地,雙官能交聯劑之一端可首先與細胞結合劑反應以提供帶有連接基部分及第二反應性基團之細胞結合劑,該細胞結合劑然後可與細胞毒性化合物反應。連接部分可含有允許細胞毒性部分在特定位點釋放之化學鍵。合適之化學鍵為此項技術中熟知的且包括二硫鍵、硫醚鍵、酸不穩定鍵、光不穩定鍵、肽酶不穩定、鍵及酯酶不穩定鍵(參見例如美國專利5,208,020;5,475,092;6,441,163;6,716,821;6,913,748;7,276,497;7,276,499;7,368,565;7,388,026及7,414,073)。較佳為二硫鍵、硫醚鍵、及肽酶不穩定鍵。可用於本發明中之其他連接基包括不可裂解之連接基,諸如美國公開案第20050169933號中詳細描述者;或帶電連接基或親水性連接基,且描述於US 2009/0274713、US 2010/01293140、及WO 2009/134976,各案以引用之方式清楚地併入本文中,各案以引用之方式清楚地併入本文中。
術語「
胺基酸」係指天然存在之胺基酸或非天然存在之胺基酸。在一些實施例中,胺基酸由NH
2-C(R
aa'R
aa)-C(=O)OH表示,其中R
aa及R
aa'各獨立係H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,芳基,雜芳基,或雜環基,或R
aa及N末端氮原子可一起形成雜環(
例如,如在脯胺酸中)。術語「
胺基酸殘基」係指當一個氫原子自胺基酸之胺及/或羧基端移除時得到之對應殘基,諸如-NH-C(R
aa'R
aa)-C(=O)O-。
術語「
肽」係指肽(醯胺)鍵連接之胺基酸單體之短鏈。在一些實施例中,肽含有2至20個胺基酸殘基。在其他實施例中,肽含有2至10個胺基酸殘基。在又其他實施例中,肽含有2至5個胺基酸殘基。如本文所用,當肽係細胞毒性劑或本文所述之由具體胺基酸序列表示之連接基之一部分時,該肽可在兩個方向上連接至該細胞毒性劑或該連接基之其餘部分。例如,二肽X
1-X
2包括X
1-X
2及X
2-X
1。類似地,三肽X
1-X
2-X
3包括X
1-X
2-X
3及X
3-X
2-X
1,且四肽X
1-X
2-X
3-X
4包括X
1-X
2-X
3-X
4及X
4-X
2-X
3-X
1。X
1、X
2、X
3、及X
4表示胺基酸殘基。
術語「
陽離子」係指帶正電之離子。陽離子可為單價(
例如,Na
+、K
+ 等)、二價(
例如,Ca
2+、Mg
2+ 等)、或多價(
例如,Al
3+ 等)。較佳的是,陽離子為單價。
術語「
半胱胺酸工程改造抗體」包括具有至少一個通常不存在於抗體輕鏈或重鏈之給定殘基之半胱胺酸(Cys)的抗體。此類Cys (其亦可稱為「經工程改造Cys」)可例如藉由標準重組技術(
例如,藉由用Cys之編碼序列置換標靶殘基處非Cys殘基之編碼序列)引入。在某些實施例中,本發明之Cys工程改造抗體在重鏈中具有經工程改造Cys。在某些實施例中,經工程改造Cys在重鏈之CH3域中或附近。在某些實施例中,經工程改造Cys在重鏈之殘基442處(EU/OU編號)。
如本文所用,本文所述之所有抗體胺基酸殘基係根據EU索引, Kabat
等人,
Sequences of Proteins of Immunological Interest, 第5版, NIH出版號91-3242, 1991 (EU/OU編號,全部內容以引用方式併入)。共同的同型稱為G1、G2、G4等。
C442殘基可透過C442殘基之游離硫醇基團,諸如透過與細胞毒性藥物之硫醇反應性試劑(
例如,順丁烯二醯亞胺基),與細胞毒性藥物/試劑結合。
如本文所用,「
水溶液」係指其中溶劑係水或水及一或多種有機溶劑之混合物的溶液。
如本文所用,術語「
治療 (treating 或 treatment)」包括以改良或穩定受試者之病狀之方式逆轉、減輕、或遏止病狀之症狀、臨床徵象、及根本病理學。如本文所用,且如此項技術中所理解,「治療」係一種用於獲得有益或所需結果包括臨床結果之方法。有益或所需臨床結果可包括但不限於可偵測或不可偵測地減輕、改善、或減緩與病狀(例如,癌症)相關之一或多個症狀或病狀,降低疾病程度,使疾病狀態穩定(亦即,不惡化),延遲或延緩疾病進展,改善或緩解疾病狀態,以及緩和(部分或完全)。「治療」亦可意指與在不接受治療情況下預期之存活相比使存活延長。本文描述示範性有益臨床結果。
本發明之方法
本發明提供用於製備細胞結合劑-細胞毒性劑結合物之新穎方法,該細胞結合劑-細胞毒性劑結合物包含帶有順丁烯二醯亞胺基團之含亞胺細胞毒性劑,該順丁烯二醯亞胺基團共價連接至細胞結合劑(CBA)。
在一些實施例中,本發明之用於製備細胞結合劑-細胞毒性劑結合物之方法包含以下步驟:
(a)使由下式表示之含亞胺細胞毒性劑或其醫藥學上可接受之鹽中亞胺部分:
(A)
與二氧化硫、亞硫酸氫鹽、或偏亞硫酸氫鹽於pH 1.9至5.0之水溶液中反應以形成包含由下式表示之經修飾亞胺部分之經修飾細胞毒性劑:
或其醫藥學上可接受之鹽;以及
(b)使該經修飾細胞毒性劑與細胞結合劑反應以形成該細胞結合劑-細胞毒性劑結合物。在一些實施例中,該亞硫酸氫鹽係亞硫酸氫鈉或亞硫酸氫鉀。更具體而言,該亞硫酸氫鹽係亞硫酸氫鈉。在又其他實施例中,該偏亞硫酸氫鹽係偏亞硫酸氫鈉或偏亞硫酸氫鉀。更具體而言,該偏亞硫酸氫鹽係偏亞硫酸氫鈉。
本發明亦提供一種製備經修飾細胞毒性劑之方法,其包含將由下式表示之含亞胺細胞毒性劑之亞胺部分:
(A)
與二氧化硫、亞硫酸氫鹽、或偏亞硫酸氫鹽於pH 1.9至5.0之水溶液中反應以形成包含由下式表示之經修飾亞胺部分之經修飾細胞毒性劑:
或其醫藥學上可接受之鹽。在一些實施例中,該反應可在下文第一、第二、第三、第四、第五、第六或第七態樣中所述之反應條件下進行。
在第一態樣中,對於上文所述之本發明方法,步驟(a)之反應係在pH 1.9至5.0下進行。更具體而言,pH係2.5至4.9、1.9至4.8、2.0至4.8、2.5至4.5、2.9至4.5、2.9至4.0、2.9至3.7、3.1至3.5、或3.2至3.4。在另一具體實施例中,步驟(a)之反應係在pH 1.9、2.0、2.1、2.2、2.3、2.4、2.5、2.6、2.7、2.8、2.9、3.0、3.1、3.2、3.3、3.4、3.5、3.6、3.7、3.8、3.9、4.0、4.1、4.2、4.3、4.5、4.6、4.7、4.8、4.9、或5.0下進行。在又另一具體實施例中,步驟(a)之反應係在pH 3.3下進行。
如本文所用,具體pH值意指具體值± 0.05。
在一些實施例中,步驟(a)之反應係在緩衝溶液之存在下進行。此項技術中已知之任何合適之緩衝溶液可用於本發明方法中。合適之緩衝溶液包括例如但不限於檸檬酸鹽緩衝液、乙酸鹽緩衝液、琥珀酸鹽緩衝液、磷酸鹽緩衝液、含甘胺酸緩衝液(
例如,甘胺酸-HCl緩衝液)、苯二甲酸鹽緩衝液(
例如,包含苯二甲酸氫鈉或苯二甲酸氫鉀之緩衝溶液)、及其組合。在一些實施例中,緩衝溶液係琥珀酸鹽緩衝液。在一些實施例中,緩衝溶液係磷酸鹽緩衝液。在一些實施例中,緩衝液係檸檬酸鹽-磷酸鹽緩衝液。在一些實施例中,緩衝液係包含檸檬酸及Na
2HPO
4之檸檬酸鹽-磷酸鹽緩衝液。在其他實施例中,緩衝液係包含檸檬酸及K
2HPO
4之檸檬酸鹽-磷酸鹽緩衝液。在一些實施例中,上文所述之緩衝溶液之濃度可在10至250 mM、10至200 mM、10至150 mM、10至100 mM、25至100 mM、25至75 mM、10至50 mM、或20至50 mM之範圍內。
在第二態樣中,反應步驟(a)係在不存在緩衝溶液(
例如,第一態樣中所述之緩衝液)之情況下進行。在一些實施例中,本發明方法包含以下步驟:(a)使由式(A)表示之含亞胺細胞毒性劑或其醫藥學上可接受之鹽中之亞胺部分與二氧化硫、亞硫酸氫鹽、或偏亞硫酸氫鹽於水溶液中反應以形成包含由下式表示之經修飾亞胺部分之經修飾細胞毒性劑:
或其醫藥學上可接受之鹽,其中該水溶液不含有緩衝液;以及
(b)使該經修飾細胞毒性劑與細胞結合劑反應以形成該細胞結合劑-細胞毒性劑結合物。在一些實施例中,步驟(a)之反應係於有機溶劑及水之混合物中進行。更具體而言,步驟(a)之反應係於二甲基乙醯胺(DMA)及水之混合物中進行。在一些實施例中,DMA及水之混合物包含按體積計小於60%的DMA。甚至更具體而言,DMA及水之體積比係1:1。
在第三態樣中,對於上文所述或第一或第二態樣中之方法,對於步驟(a)之反應中每1當量含亞胺細胞毒性劑使用0.5至5.0當量該亞硫酸氫鹽或0.25或2.5當量該偏亞硫酸氫鹽。在一些實施例中,對於每1當量含亞胺細胞毒性劑使用0.5至4.5、0.5至4.0、0.5至3.5、0.5至4.0、0.5至3.5、0.5至3.0、0.5至2.5、0.8至2.0、0.9至1.8、1.0至1.7、1.1至1.6、或1.2至1.5當量該亞硫酸氫鹽,或0.25至2.25、0.25至2.0、0.25至1.75、0.25至2.0、0.25至1.75、0.25至1.5、0.25至1.25、0.4至1.0、0.45至0.9、0.5至0.85、0.55至0.8、或0.6至0.75當量該偏亞硫酸氫鹽。在其他實施例中,對於每1當量含亞胺細胞毒性劑使用0.5、0.6、0.7、0.8、0.9、1.0、1.1、1.2、1.3 1.4、1.5、1.6、1.7、1.8、1.9、2.0、2.1、2.2、2.3、2.4、2.5、2.6、2.7、2.8、2.9、3.0、3.1、3.2、3.3、3.4、3.5、4.0、4.5、或5.0當量該亞硫酸氫鹽,或0.25、0.3、0.35、0.4、0.45、0.5、0.55、0.6、0.65 0.7、0.75、0.8、0.85、0.9、0.95、1.0、1.05、1.1、1.15、1.2、1.25、1.3、1.35、1.4、1.45、1.5、1.55、1.6、1.65、1.7、1.75、2.0、2.25、或2.5當量該偏亞硫酸氫鹽。在又其他實施例中,對於每1當量含亞胺細胞毒性劑使用1.4當量該亞硫酸氫鹽或0.7當量該偏亞硫酸氫鹽。在其他實施例中,對於每1當量含亞胺細胞毒性劑使用1.2當量該亞硫酸氫鹽或0.6當量該偏亞硫酸氫鹽。
如本文所用,具體當量意指具體值± 0.05。
在第四態樣中,對於本發明方法,步驟(a)之反應係在pH 2.9至3.7下進行,且使1.0至1.8當量該亞硫酸氫鹽或0.5至0.9當量該偏亞硫酸氫鹽與1當量含亞胺細胞毒性劑反應。在一些實施例中,步驟(a)之反應係在pH 3.1至3.5下進行,且使1.1至1.6當量該亞硫酸氫鹽或0.55至0.8當量該偏亞硫酸氫鹽與1當量含亞胺細胞毒性劑反應。在其他實施例中,步驟(a)之反應係在pH 3.2至3.4下進行,且使1.3至1.5當量該亞硫酸氫鹽或0.65至0.75當量該偏亞硫酸氫鹽與1當量含亞胺細胞毒性劑反應。在其他實施例中,步驟(a)之反應係在pH 3.3下進行,且使1.4當量該亞硫酸氫鹽或0.7當量該偏亞硫酸氫鹽與1當量含亞胺細胞毒性劑反應。在又其他實施例中,在其他實施例中,步驟(a)之反應係在pH 3.3下進行,且使1.4當量亞硫酸氫鈉與1當量含亞胺細胞毒性劑反應。
在第五態樣中,對於本文所述或第一、第二、第三、或第四態樣中之方法,步驟(a)之反應係在有機溶劑及水之混合物中進行。可使用任何合適之有機溶劑。示範性有機溶劑包括但不限於醇(
例如,甲醇、乙醇、丙醇等)、二甲基甲醯胺(DMF)、二甲基亞碸(DMSO)、乙腈、丙酮、二氯甲烷等。在一些實施例中,有機溶劑可與水混溶。在其他實施例中,有機溶劑不可與水混溶,
亦即,步驟(a)之反應係在雙相溶液中進行。在一些實施例中,有機溶劑係二甲基乙醯胺(DMA)。按水及有機溶劑之總體積計,有機溶劑(
例如,DMA)可以1%-99%、1-95%、10-80%、20-70%、30-70%、1-60%、5-60%、10-60%、20-60%、30-60%、40-60%、45-55%、10-50%、或20-40%之量存在。步驟(a)之該反應係於DMA及水之混合物中進行,其中DMA與水之體積比係1:1。
在第六態樣中,對於本文所述或第一、第二、第三、第四、或第五態樣中之本發明方法,步驟(a)之反應可在任何合適之溫度下進行。在一些實施例中,該反應係在0℃至50℃、10℃至50℃、10℃至40℃、或10℃至30℃之溫度下進行。在其他實施例中,該反應係在15℃至30℃、20℃至30℃、15℃至25℃、16℃至24℃、17℃至23℃、18℃至22℃、或19℃至21℃之溫度下進行。在又其他實施例中,該反應可在15℃、16℃、17℃、18℃、19℃、20℃、21℃、22℃、23℃、24℃、或25℃下進行。在一些實施例中,該反應可在0℃至15℃、0℃至10℃、1℃至10℃、5℃至15℃、或5℃至10℃下進行。
在第七態樣中,對於本文所述或第一、第二、第三、第四、第五、或第六態樣中之本發明方法,步驟(a)之反應進行1分鐘至48小時、5分鐘至36小時、10分鐘至24小時、30分鐘至24小時、30分鐘至20小時、1小時至20小時、1小時至15小時、1小時至10小時、2小時至10小時、3小時至9小時、3小時至8小時、4小時至6小時、或1小時至4小時。在一些實施例中,使該反應進行4至6小時。在其他實施例中,使該反應進行10分鐘、15分鐘、20分鐘、30分鐘、1小時、2小時、3小時、4小時、5小時、6小時、7小時、8小時、9小時、10小時、11小時、12小時、13小時、14小時、15小時等。在其他實施例中,使該反應進行4小時。在又其他實施例中,使該反應進行2小時。
在第八態樣中,對於本文所述或第一、第二、第三、第四、第五、第六、或第七態樣中之本發明方法,步驟(b)之反應可在pH 4至9下進行。在一些實施例中,步驟(b)之反應係在pH 4.5至8.5、5至8.5、5至8、5至7.5、5至7、5至6.5、或5.5至6.5下進行。在其他實施例中,步驟(b)之反應係在pH 5.0、5.1、5.2、5.3、5.4、5.5、5.6、5.7、5.8、5.9、6.0、6.1、6.2、6.3、6.4、6.5、6.6、6.7、6.8、6.9、7.0、7.1、7.2、7.3、7.4、7.5、7.6、7.7、7.8、7.9、或8.0下進行。
在一些實施例中,對於本文所述或第一、第二、第三、第四、第五、第六、第七、或第八態樣中之本發明方法,步驟(b)之反應係在包含水及有機溶劑之混合物之水溶液中進行。可使用上文所述之任何合適之有機溶劑。更具體而言,有機溶劑係DMA。在一些實施例中,水溶液包含按體積計小於50%、小於40%、小於30%、小於25%、小於20%、小於15%、小於10%、小於5%、小於3%、小於2%、或小於1%有機溶劑(
例如DMA)。
在一些實施例中,對於本文所述或第一、第二、第三、第四、第五、第六、第七、或第八態樣中之本發明方法,經修飾細胞毒性劑在步驟(b)中與細胞毒性劑反應之前未純化。替代地,經修飾細胞毒性劑在步驟(b)中與細胞結合劑反應之前係經純化。本文所述之任何合適之方法可用於純化經修飾細胞毒性劑。在某些實施例中,本發明提供藉由本發明方法製備之經分離之經修飾細胞毒性劑。經分離之經修飾細胞毒性劑可在與細胞結合劑反應之前儲存一段時間。較佳的是,經分離之經修飾細胞毒性劑在以下條件下儲存,該等條件將防止經修飾細胞毒性劑分解,例如,呈經純化固體或呈冷凍溶液,或保持在低溫(例如,低於10℃或低於5℃)。
在一些實施例中,對於本文所述或上文所述之任一實施例中之本發明方法,步驟(b)之細胞結合劑-細胞毒性劑結合物經歷純化步驟。就此而言,細胞結合劑-細胞毒性劑結合物可使用切向流過濾(TFF)、非吸附層析、吸附層析、吸附過濾、選擇性沉澱、或任何其他合適之純化過程、以及其組合自混合物之其他組分純化。
在本發明之一些實施例中,細胞結合劑-細胞毒性劑結合物係使用單個純化步驟(
例如,TFF)純化。較佳的是,結合物係使用單個純化步驟(
例如,TFF)純化並交換至適當調配物中。在本發明之其他實施例中,細胞結合劑-細胞毒性劑結合物係使用兩個順序純化步驟純化。例如,結合物可首先藉由選擇性沉澱、吸附過濾、吸附層析、或非吸附層析純化,接著用TFF純化。一般熟習此項技術者將理解,細胞結合劑-細胞毒性劑結合物之純化實現包含化學偶合至細胞毒性劑之細胞結合劑的穩定結合物之隔離。
任何合適之TFF系統可用於純化,包括Pellicon型系統(Millipore, Billerica, Mass.)、Sartocon Cassette系統(Sartorius AG, Edgewood, N.Y.)、及Centrasette型系統(Pall Corp., East Hills, N.Y.)。
任何合適之吸附層析樹脂可用於純化。較佳吸附層析樹脂包括氫氧磷灰石層析、疏水性電荷誘導層析(HCIC)、疏水性相互作用層析(HIC)、離子交換層析、混合模式離子交換層析、固定金屬親和層析(IMAC)、染料配體層析、親和層析、逆相層析、及其組合。合適之氫氧磷灰石樹脂之實例包括陶瓷氫氧磷灰石(CHT I型及II型,Bio-Rad Laboratories, Hercules, Calif.)、HA Ultrogel氫氧磷灰石(Pall Corp., East Hills, N.Y.)、及陶瓷氟磷灰石(CFT I型及II型,Bio-Rad Laboratories, Hercules, Calif.)。合適之HCIC樹脂之實例係MEP Hypercel樹脂(Pall Corp., East Hills, N.Y.)。合適之HIC樹脂之實例包括丁基-瓊脂糖、己基-瓊脂糖、苯基-瓊脂糖、及辛基-瓊脂糖樹脂(所有均來自GE Healthcare, Piscataway, N.J.)、以及Macro-prep甲基及Macro-Prep第三丁基樹脂(Biorad Laboratories, Hercules, Calif.)。合適之離子交換樹脂之實例包括SP-瓊脂糖、CM-瓊脂糖、及Q-瓊脂糖樹脂(所有均來自GE Healthcare, Piscataway, N.J.)、及Unosphere S樹脂(Bio-Rad Laboratories, Hercules, Calif.)。合適之混合模式離子交換劑之實例包括Bakerbond ABx樹脂(JT Baker, Phillipsburg N.J.)。合適之IMAC樹脂之實例包括Chelating瓊脂糖樹脂(GE Healthcare, Piscataway, N.J.)及Profinity IMAC樹脂(Bio-Rad Laboratories, Hercules, Calif.)。合適之染料配體樹脂之實例包括藍色瓊脂糖樹脂(GE Healthcare, Piscataway, N.J.)及Affi-gel藍色樹脂(Bio-Rad Laboratories, Hercules, Calif.)。合適之親核樹脂之實例包括蛋白質A瓊脂糖樹脂(
例如,MabSelect, GE Healthcare, Piscataway, N.J.),其中細胞結合劑係抗體;及凝集素親和樹脂,
例如Lentil凝集素瓊脂糖樹脂(GE Healthcare, Piscataway, N.J.),其中細胞結合劑帶有適當凝集素結合位點。替代地,可使用特異於細胞結合劑之抗體。此一抗體可固定至例如瓊脂糖4快速流動樹脂(GE Healthcare, Piscataway, N.J.)。合適之逆相樹脂之實例包括C4、C8、及C18樹脂(Grace Vydac, Hesperia, Calif.)。
任何合適之非吸附層析樹脂可用於純化。合適之非吸附層析樹脂之實例包括但不限於SEPHADEX
TMG-25、G-50、G-100、SEPHACRYL
TM樹脂(
例如,S-200及S-300)、SUPERDEX
TM樹脂(
例如,SUPERDEX
TM75及SUPERDEX
TM200)、BIO-GEL
®樹脂(
例如,P-6、P-10、P-30、P-60、及P-100)、及一般熟習此項技術者已知之其他樹脂。
在一些實施例中,經純化細胞結合劑-細胞毒性劑結合物係調配成合適之調配緩衝液。在一些實施例中,調配緩衝液包含亞硫酸氫鹽,諸如亞硫酸氫鈉或亞硫酸氫鉀。更具體而言,調配緩衝液包含亞硫酸氫鈉。在一些實施例中,調配緩衝液包含5至200 µM、10至200 µM、10至150 µM、20至100 µM、30至90 µM、40至80 µM、50至70 µM、40至60 µM、45至55 µM或55至65 µM該亞硫酸氫鹽(
例如,亞硫酸氫鈉)。在其他實施例中,調配緩衝液包含20、30、40、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、70、80、90、或100 µM該亞硫酸氫鹽(
例如,亞硫酸氫鈉)。
在其他實施例中,調配緩衝液進一步包含海藻糖。可使用任何合適量海藻糖。在一些實施例中,調配緩衝液進一步包含按重量計2至15%、5至10%、6至10%、或7至9%、或6至8%海藻糖。
在另一實施例中,調配緩衝液具有pH 4至6、4至5、或4至4.5。在其他實施例中,調配緩衝液之pH係4.0、4.1、4.2、4.3、4.4、4.5、4.6、4.7、4.8、4.9、或5.0。
在又其他實施例中,調配緩衝液包含在pH 4.2下之10 mM琥珀酸鈉、50 µM亞硫酸氫鈉、8%海藻糖二水合物、及0.01%聚山梨醇酯20。
在一些實施例中,對於本文所述之本發明方法,步驟(a)之反應不導致順丁烯二醯亞胺基團之實質磺化。在一些實施例中,少於50%、40%、30%、20%、10%、9%、8%、7%、6%、5%、4%、3%、2%、或1%順丁烯二醯亞胺基團係磺化的。順丁烯二醯亞胺磺化之百分比等於順丁烯二醯亞胺-磺化細胞毒性劑(僅在順丁烯二醯亞胺上具有磺化之細胞毒性劑)及二磺化細胞毒性劑(在順丁烯二醯亞胺及亞胺部分上具有磺化之細胞毒性劑)之總量除以含亞胺細胞毒性劑在其與該亞硫酸氫鹽或該偏亞硫酸氫鹽反應之前只起始量。
在第九態樣中,本發明提供一種製備由下式表示之細胞結合劑-細胞毒性劑結合物之方法:
;
或其醫藥學上可接受之鹽,其包含以下步驟:
(a)使由下式表示之含亞胺細胞毒性劑或其醫藥學上可接受之鹽中亞胺部分:
與二氧化硫、亞硫酸氫鹽、或偏亞硫酸氫鹽於pH 3.1至3.5之水溶液中反應以形成由下式表示之經修飾細胞毒性劑:
或其醫藥學上可接受之鹽;以及
(b)使該經修飾細胞毒性劑或其醫藥學上可接受之鹽與細胞結合劑Ab反應以形成該細胞結合劑-細胞毒性劑結合物,其中:
Ab係抗CD123抗體,其包含具有胺基酸序列SEQ ID NO:25之免疫球蛋白重鏈及具有胺基酸序列SEQ ID NO:26之免疫球蛋白輕鏈;且
w係1或2。
在一些實施例中,第九態樣之方法係在第一、第二、第三、第四、第五、第六、第七或第八態樣及其中所述之任何實施例中所述之反應條件下進行。
在第十態樣中,第九態樣之方法中步驟(a)之反應係在pH 3.2至3.4下進行。更具體而言,pH係3.3。
在一些實施例中,步驟(a)之反應係在緩衝溶液之存在下進行。示範性緩衝溶液包括但不限於檸檬酸鹽緩衝液、乙酸鹽緩衝液、琥珀酸鹽緩衝液或磷酸鹽緩衝液。更具體而言,緩衝液係琥珀酸鹽緩衝液。
在第十一態樣中,對於第九態樣之方法中步驟(a)之反應,使1.1至1.6當量該亞硫酸氫鹽或0.55至0.8當量該偏亞硫酸氫鹽與1當量含亞胺細胞毒性劑反應。其餘反應條件係如上文在第十態樣或其中所述之任何實施例中所述。在一些實施例中,使1.3至1.5當量該亞硫酸氫鹽或0.65至0.75當量該偏亞硫酸氫鹽與1當量該含亞胺細胞毒性劑反應。更具體而言,使1.4當量該亞硫酸氫鹽或0.7當量該偏亞硫酸氫鹽與1當量該含亞胺細胞毒性劑反應。
在第十二態樣中,第九態樣之方法中步驟(a)之反應係在pH 3.2至3.4下進行,且使1.3至1.5當量該亞硫酸氫鈉與1當量該含亞胺細胞毒性劑反應。在一些實施例中,該反應係在pH 3.3下進行,且使1.4當量亞硫酸氫鈉與1當量含亞胺細胞毒性劑反應。
在一些實施例中,第九、第十、第十一或第十二態樣之方法中步驟(a)之反應係在合適的溶劑或溶劑混合物中進行。在一些實施例中,步驟(a)之反應係在包含水及有機溶劑之水溶液中進行。可使用上文所述之任何合適之有機溶劑。更具體而言,有機溶劑係DMA。在一些實施例中,水溶液包含按體積計小於50%、小於40%、小於30%、小於25%、小於20%、小於15%、小於10%、小於5%、小於3%、小於2%、或小於1%有機溶劑(
例如DMA)。
在一些實施例中,步驟(a)之反應係在合適的溫度下(例如,在室溫或在15至25℃下)進行足夠的一段之間,諸如1小時、2小時、3小時、4小時、5小時、6小時、7小時、8小時、9小時、10小時、12小時、15小時、20小時、24小時、48小時等。
在一些實施例中,自步驟(a)之反應獲得之經修飾細胞毒性劑在步驟(b)中與細胞結合劑反應之前未經純化。
在一些實施例中,自步驟(a)之反應獲得之經修飾細胞毒性劑在步驟(b)中與細胞結合劑反應之前經純化。可使用本文所述之任何合適的純化方法。
在第十三態樣中,第九態樣之方法中步驟(b)之反應係在pH 5.5至6.5下進行,且其餘反應條件係如第九、第十、第十一或第十二態樣中所述。在一些實施例中,pH係5.5、5.6、5.7、5.8、5.9、6.0、6.1、6.2、6.3、6.4或6.5。在一些實施例中,pH係6.0。
在一些實施例中,藉由第九、第十、第十一、第十二或第十三態樣之方法製備之結合物係藉由本文所述之合適方法純化。在一個實施例中,該結合物係藉由切向流過濾來純化以產生經純化結合物。
在一些實施例中,經純化結合物係於包含40至80 µM亞硫酸氫鈉、具有pH 4至5的調配緩衝液中調配。在一些實施例中,調配緩衝液包含50 µM亞硫酸氫鈉,具有pH 4.2。在一些實施例中,調配緩衝液包含在pH 4.2下之10 mM琥珀酸鈉、50 µM亞硫酸氫鈉、8%海藻糖二水合物、及0.01%聚山梨醇酯20。
在一些實施例中,對於本文(例如,第一、第二、第三、第四、第五、第六、第七或第八態樣及其中所述之任何實施例)所述之本發明之方法,細胞結合劑非係抗CD123抗體。
在一些實施例中,對於本文(例如,第一、第二、第三、第四、第五、第六、第七或第八態樣及其中所述之任何實施例)所述之本發明之方法,細胞結合劑非係包含具有胺基酸序列SEQ ID NO:25之免疫球蛋白重鏈及具有胺基酸序列SEQ ID NO:26之免疫球蛋白輕鏈之抗CD123抗體。
在一些實施例中,藉由本文(例如,第一、第二、第三、第四、第五、第六、第七或第八態樣及其中所述之任何實施例)所述之本發明之方法製備之細胞結合劑-細胞毒性劑結合物非係由以下結構表示之結合物:
;
或其醫藥學上可接受之鹽,其中Ab係抗CD123抗體,其包含具有胺基酸序列SEQ ID NO:25之免疫球蛋白重鏈及具有胺基酸序列SEQ ID NO:26之免疫球蛋白輕鏈;且
w係1或2。
本發明之含亞胺細胞毒性劑及結合物
在一些實施例中,對於本文所述之本發明方法,含亞胺細胞毒性劑係由下式表示:
(A)
或其醫藥學上可接受之鹽,以及
細胞結合劑-細胞毒性劑結合物係由下式表示:
(B)
其中D
M係包含由下式表示之經修飾亞胺部分之經修飾細胞毒性劑:
或其醫藥學上可接受之鹽;L係連接基;
表示經由硫醇基團連接至細胞毒性劑之細胞結合劑;且w係整數1至10。
在一些實施例中,CBA係抗體且該抗體經由一或多個半胱胺酸硫醇基團連接至細胞毒性劑。在一些實施例中,游離硫醇基團係在抗體之重鏈CH3區之經工程改造Cys殘基上,在該重鏈之EU/OU編號442位(或簡稱C442)處。更具體而言,在442位處之半胱胺酸殘基重組引入至抗體中。
在其他實施例中,w係1或2。更具體而言,w係2。
下文描述本文所述之本發明之方法(
例如,上文所述之第一、第二、第三、第四、第五、第六、第七或第八態樣及其中所述之實施例之方法)之某些實施例及具體實施例。
在第一具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,D係由以下結構式表示:
(IGN1');
(IGN1);
(IGN2');
(IGN2);
(IGN3');
(IGN3);
(IGN4');或
(IGN4);
或其醫藥學上可接受之鹽,其中:
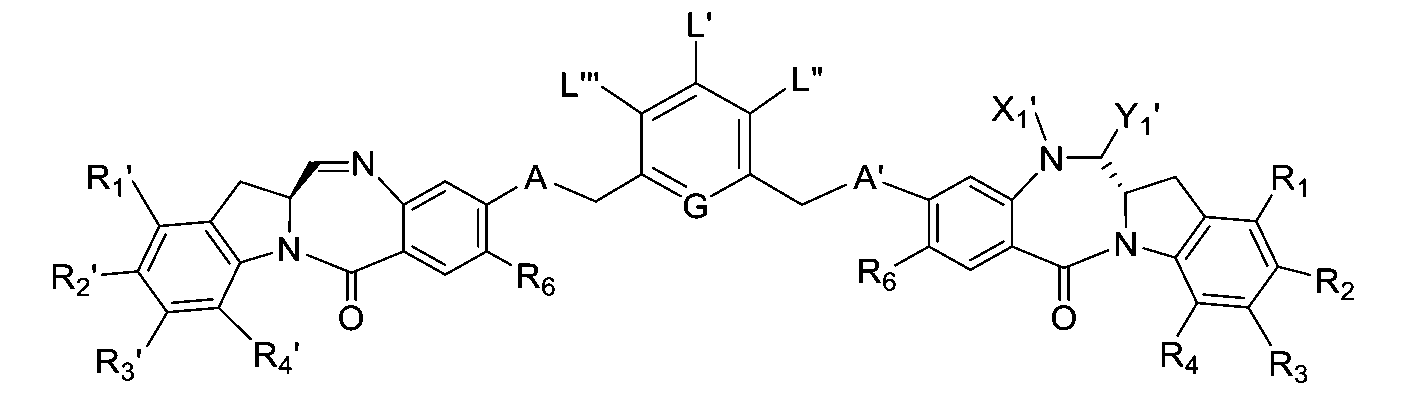
L'、L''、及L'''之一係由下式表示:
-Z
1-P
1-Z
2-R
x1-C(=O)- (A'),或
-N(R
e)-R
x1-C(=O)- (D');
且另兩者各獨立選自-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,鹵素,鈲[-NH(C=NH)NH
2],-OR,-NR'R'',-NO
2,-NR'COR'',-SR,-SOR',-SO
2R',-SO
3H,-OSO
3H,-SO
2NR'R'',氰基,疊氮基,-COR',-OCOR',及-OCONR'R'';
Z
1及Z
2之一係-C(=O)-,且另一者係-NR
5-;
P
1係胺基酸殘基或含有2至20之間個胺基酸殘基之肽;
R
x1係具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基;
R
e係-H,具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基,或-(CH
2-CH
2-O)
n-R
k,其中R
k係-H,具有1至6個碳原子之直鏈、支鏈、環狀烷基,其視情況帶有二級胺基(
例如,-NHR
101)或三級胺基(-NR
101R
102)基團,或5或6員含氮雜環,諸如哌啶或嗎啉,其中R
101及R
102各獨立地係具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基;
R在每次出現時獨立選自由以下所組成之群:-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,具有6至18個碳原子之視情況經取代芳基,含有一或多個獨立選自氮、氧、及硫之雜原子之視情況經取代5至18員雜芳環,或含有1至6個獨立選自O、S、N、及P之雜原子之視情況經取代3至18員雜環;
R'及R''各獨立選自-H,-OH,-OR,-NHR,-NR
2,-COR,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,及具有1至6個獨立選自O、S、N、及P之雜原子之視情況經取代3至18員雜環;
R
c係-H或具有1至4個碳原子之視情況經取代直鏈或支鏈烷基;
n係整數1至24;
X
1'係選自-H,胺保護基,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,具有6至18個碳原子之視情況經取代芳基,含有一或多個獨立選自氮、氧、及硫之雜原子之視情況經取代5至18員雜芳環,及含有1至6個獨立選自O、S、N、及P之雜原子之視情況經取代3至18員雜環;
Y
1'係選自-H,側氧基(亦即,Y
1'連同其所連接之碳原子一起形成-C(=O)-基團),具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,視情況經取代6至18員芳基,含有一或多個獨立選自氮、氧、及硫之雜原子之視情況經取代5至18員雜芳環,具有1至6個雜原子之視情況經取代3至18員雜環;
R
1、R
2、R
3、R
4、R
1'、R
2'、R
3'、及R
4'各獨立選自由以下所組成之群:-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,鹵素,鈲[-NH(C=NH)NH
2],-OR,-NR'R'',-NO
2,-NCO,-NR'COR'',-SR,-SOR',-SO
2R',-SO
3 -H,-OSO
3H,-SO
2NR'R'',氰基,疊氮基,-COR',-OCOR',及-OCONR'R'';
R
6係-H、-R、-OR、-SR、-NR'R''、-NO
2、或鹵素;
G係-CH-或-N-;
A及A'相同或不同,且獨立選自-O-、側氧基(-C(=O)-)、-CRR'O-、-CRR'-、-S-、-CRR'S-、-NR
5、及-CRR'N(R
5)-;且
R
5在每次出現時獨立地係-H或具有1至10個碳原子之視情況經取代直鏈或支鏈烷基。
在更具體實施例中,D係由式(IGN1')或(IGN1)表示。
在另一更具體實施例中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),L'、L''、及L'''之一係由式(A')或(D')表示,且另外兩者係:-H,具有1至6個碳原子之直鏈或支鏈烷基,鹵素,-OH,(C
1-C
6)烷氧基,或-NO
2。
在另一更具體實施例中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),L'係由式(A')表示;且L''及L'''均係-H。
在另一更具體實施例中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),L'係由式(D')表示;且L''及L'''均係-H。
在另一更具體實施例中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),R
x1係具有1至6個碳原子之直鏈、支鏈、或環狀烷基,其視情況經鹵素、-OH、-SO
3H、(C
1-C
3)烷基、(C
1-C
3)烷氧基、鹵基(C
1-C
3)烷基、或帶電取代基或可離子化基團Q取代。
在第二具體態樣中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),L'係由下式表示:
-NR
5-P
1-C(=O)-(CR
aR
b)
s-C(=O)- (B1');
-NR
5-P
1-C(=O)-Cy-(CR
aR
b)
s1'-C(=O)- (B2');
-C(=O)-P
1-NR
5-(CR
aR
b)
s-C(=O)- (C1');或
-C(=O)-P
1-NR
5-Cy-(CR
aR
b)
s1'-C(=O)- (C2')
其中:
R
a及R
b在每次出現時各獨立地係-H、(C
1-C
3)烷基、或帶電取代基或可離子化基團Q;
s係整數1至6;
s1'係0或整數1至6;且
Cy係具有5或6個環碳原子之環狀烷基,其視情況經鹵素、-OH、(C
1-C
3)烷基、(C
1-C
3)烷氧基、或鹵基(C
1-C
3)烷基取代;
且其餘變數係如上文在第一具體態樣或其中所述之任何具體或更具體實施例中所述。
在更具體實施例中,R
a及R
b均係H;式(B2')及(C2')中之Cy係環己烷;且R
5係H或Me。甚至更具體而言,s1'係0或1。
在第三具體態樣中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),P
1係含有2至10個胺基酸殘基之肽;且其餘變數係如第一或第二具體態樣或其中所述之任何具體或更具體實施例中所述。
在具體實施例中,P
1係含有2至5個胺基酸殘基之肽。
在另一具體實施例中,P
1係Gly-Gly-Gly、Ala-Val、Val-Cit、Val-Lys、Phe-Lys、Lys-Lys、Ala-Lys、Phe-Cit、Leu-Cit、Ile-Cit、Trp、Cit、Phe-Ala、Phe-N
9-甲苯磺醯基-Arg、Phe-N
9-硝基-Arg、Phe-Phe-Lys、D-Phe-Phe-Lys、Gly-Phe-Lys、Leu-Ala-Leu、Ile-Ala-Leu、Val-Ala-Val、Ala-Leu-Ala-Leu (SEQ ID NO: 1)、β-Ala-Leu-Ala-Leu (SEQ ID NO: 2)、Gly-Phe-Leu-Gly (SEQ ID NO: 3)、Val-Arg、Arg-Arg、Val-D-Cit、Val-D-Lys、Val-D-Arg、D-Val-Cit、D-Val-Lys、D-Val-Arg、D-Val-D-Cit、D-Val-D-Lys、D-Val-D-Arg、D-Arg-D-Arg、Ala-Ala、Ala-D-Ala、D-Ala-Ala、D-Ala-D-Ala、Ala-Met、Gln-Val、Asn-Ala、Gln-Phe、及Gln-Ala。甚至更具體而言,P係Gly-Gly-Gly、Ala-Val、Ala-Ala、Ala-D-Ala、D-Ala-Ala、或D-Ala-D-Ala。
在第四具體態樣中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),X
1'係選自由以下所組成之群:-H,-OH,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,及苯基;Y
1'係選自由以下所組成之群:-H,側氧基,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基;且其餘變數係如上文在第一、第二、或第三具體態樣或其中所述之任何具體或更具體實施例中所述。更具體而言,X
1'係-H、-OH、(C
1-C
3)烷基、鹵基(C
1-C
3)烷基、或苯基;且Y
1'係-H、側氧基、(C
1-C
3)烷基、或鹵基(C
1-C
3)烷基。在另一更具體實施例中,X
1'係-H、-OH、或-Me;且Y
1'係-H或側氧基。甚至更具體而言,X
1'係-H;且Y
1'係-H。
在第五具體態樣中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),A及A'相同或不同,且係-O-、-S-、-NR
5-、或側氧基-(C=O)-;且其餘變數係如上文在第一、第二、第三、或第四具體態樣或其中所述之任何具體或更具體實施例中所述。更具體而言,A及A'相同或不同,且係-O-或-S-。甚至更具體而言,A及A'係-O-。
在第六具體態樣中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),R
6係-OR,其中R係具有1至6個碳原子之烷基;且其餘變數係如上文在第一、第二、第三、第四、或第五具體態樣或其中所述之任何具體或更具體實施例中所述。更具體而言,R
6係-OMe。
在第七具體態樣中,對於式(IGN1)-(IGN4),R
1、R
2、R
3、R
4、R
1'、R
2'、R
3'、及R
4'各獨立係-H、鹵素、-NO
2、-OH、(C
1-C
3)烷基、鹵基(C
1-C
3)烷基、或(C
1-C
3)烷氧基;且其餘變數係如上文在第一、第二、第三、第四、第五、或第六具體態樣或其中所述之任何具體或更具體實施例中所述。更具體而言,R
1、R
2、R
3、R
4、R
1'、R
2'、R
3'、及R
4'全部係-H。
在第八具體態樣中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4),R、R'、R''、及R
5各獨立係-H或(C
1-C
3)烷基;且其餘變數係如上文在第一、第二、第三、第四、第五、第六、或第七具體態樣或其中所述之任何具體或更具體實施例中所述。
在第九具體態樣中,對於式(IGN1')-(IGN4')及(IGN1)-(IGN4):
R
1、R
2、R
3、R
4、R
1'、R
2'、R
3'、及R
4'全部係-H;
R
6係-OMe;
X
1'及Y
1'均係-H;且
A及A'係-O-;
且其餘變數係如上文在第一、第二、或第三具體態樣或其中所述之任何具體或更具體實施例中所述。更具體而言,R、R'、R''、及R
5各獨立係-H或(C
1-C
3)烷基。甚至更具體而言,R、R'、R''、及R
5全部係-H。
在第十具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,D係由以下結構式表示:
;
;
;
;
;
;
;
;
;
;
;或
,
或其醫藥學上可接受之鹽;且其餘變數係針對上文所述之式(A)或(B)加以描述。
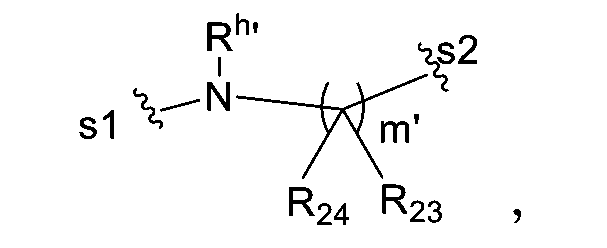
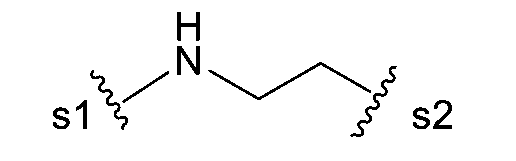
在第十一具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,-L-係由以下結構式表示:
(L1),`
其中:
s1係共價連接至D之位點;s2係共價連接至順丁烯二醯亞胺基團之位點;
R
23及R
24在每次出現時獨立係H或視情況經取代烷基;
m'係0與10之間的整數;且
R
h'係H或視情況經取代烷基;
且其餘變數係如上文針對式(A)或式(B),或在第一至第十具體態樣,或其中所述之任何具體或更具體實施例中所述。
在具體實施例中,m'係整數1至6。甚至更具體而言,m'係整數1至3。
在另一具體實施例中,R
23及R
24在每次出現時獨立係H或(C
1-C
3)烷基。甚至更具體而言,R
23及R
24均係H。
在另一具體實施例中,R
h'係H或(C
1-C
3)烷基。更具體而言,R
h'係H。
在另一具體實施例中,R
23及R
24均係H;m'係整數1至6。甚至更具體而言,m'係整數1至3。
在第十二具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,-L-係由以下結構式表示:
;
其中s1係共價連接至D之位點;s2係共價連接至順丁烯二醯亞胺基團之位點;且其餘變數係如上文針對式(A)或式(B),或在第一至第十態樣或其中所述之任何具體或更具體實施例中所述。
在第十三具體態樣中,含亞胺細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽,且該經修飾細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽。更具體而言,經修飾細胞毒性劑係由下式表示:
,
或其鈉鹽或鉀鹽。甚至更具體而言,經修飾細胞毒性劑係由下式表示:
。
在一些實施例中,含亞胺細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽,且該經修飾細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽。更具體而言,經修飾細胞毒性劑係由下式表示:
,
或其鈉鹽或鉀鹽。甚至更具體而言,經修飾細胞毒性劑係由下式表示:
。
在第十四具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,D係由以下結構式表示:
(IGN5');
(IGN5);
(IGN6');
(IGN6);
(IGN7');
(IGN7);
(IGN8');或
(IGN8),
或其醫藥學上可接受之鹽,其中:
X'係選自由以下所組成之群:-H,-OH,具有1至10個碳原子之經取代或未取代直鏈、支鏈、或環狀烷基、烯基、或炔基,苯基,及胺保護基;
Y'選自由以下組成之群:-H、側氧基、取代或未取代之具有1至10個碳原子之直鏈、支鏈或環狀烷基、烯基或炔基;
A及A'係選自-O-及-S-;
W'不存在,或選自-O-、-N(R
e)-、-N(R
e)-C(=O)-、-N(C(=O)R
e)-、-S-、或-CH
2-S-、-CH
2NR
e-;
R
x不存在,或選自具有1至10個碳原子之直鏈、支鏈、或環狀烷基;
R
e係-H,具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基,或-(CH
2-CH
2-O)
n-R
k,其中R
k係-H,具有1至6個碳原子之直鏈、支鏈、環狀烷基,其視情況帶有二級胺基(
例如,-NHR
101)或三級胺基(-NR
101R
102)基團,或5或6員含氮雜環,其中R
101及R
102各獨立地係具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基;
n係整數1至24;
G係選自-CH-或-N-;
R
6係-H、-R、-OR、-SR、-NR'R''、-NO
2、或鹵素;且
R係-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,或PEG基團-(CH
2CH
2O)
n-R
c,其中n係整數1至24,且R
c係具有1至4個碳原子之直鏈或支鏈烷基;
R'及R''各獨立選自-H,-OH,-OR,-NRR
g',-COR,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,具有6至18個碳原子之視情況經取代芳基,具有1至6個選自O、S、N、及P之雜原子之視情況經取代3至18員雜環,PEG基團-(CH
2CH
2O)
n-R
c,且R
g'係-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,或PEG基團-(CH
2CH
2O)
n-R
c。
在更具體實施例中,D係由上文式(IGN5')或(IGN5)表示,或其醫藥學上可接受之鹽。
在另一具體實施例中,對於式(IGN5')-(IGN8')及(IGN5)-(IGN8):
X'及Y'均係-H;
A及A'均係-O-;
R
6係-OMe;
W'係-N(R
e)-或-N(R
e)-C(=O)-;
R
e係-H,具有1至4個碳原子之直鏈或支鏈烷基,或-(CH
2-CH
2-O)
n-R
k,其中R
k係-H,具有1至4個碳原子之直鏈或支鏈烷基;
n係整數2至6;且
R
x係具有1至6個碳原子之直鏈或支鏈烷基。
在第十五具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,D係由以下結構式表示:
;
;
;
;
;
;
;
;
或其醫藥學上可接受之鹽,其中其餘變數係如上文針對式(A)或(B)所述。
在第十六具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,-L-係由以下結構式表示:
(L2),
其中:
s1係共價連接至D之位點,且s2係共價連接至順丁烯二醯亞胺基團之位點;
E係-(CR
10R
11)
q-、環烷基、或環烷基烷基;
Z係不存在、-SO
2NR
9-、-NR
9SO
2-、-C(=O)-NR
9-、-NR
9-C(=O)-、-C(=O)-O-、-O-C(=O)-、-C(=O)-NR
9-(CH
2CH
2O)
p-、-NR
9-C(=O)-(CH
2CH
2O)
p-、-(OCH
2CH
2)
p-C(=O)NR
9-、或-(OCH
2CH
2)
p-NR
9-C(=O)-;
p係整數1至24;
Q係H、帶電取代基、或可離子化基團;
R
9、R
10、R
11、R
12、及R
13在每次出現時獨立係H或視情況經取代烷基;且,
q及r在每次出現時獨立係0與10之間的整數;且其餘變數係如上文針對式(A)或式(B),或在第十四或第十五具體態樣,或其中所述之任何具體或更具體實施例中所述。
在更具體實施例中,q及r獨立係整數1至6,更具體而言,1至3。
在另一更具體實施例中,R
9、R
10、R
11、R
12、及R
13在每次出現時獨立係H或C
1-3烷基。更具體而言,R
9、R
10、R
11、R
12、及R
13全部自係H。
在另一更具體實施例中,p係整數2至14。更具體而言,p係整數2至8、2至6、或2至4。
在更具體實施例中,E係-(CR
10R
11)
q-;且式(L2)中之其餘變數係如上文在第十六具體態樣中所述。
在另一更具體實施例中,E係
;且式(L2)中之其餘變數係如上文在第十六具體態樣中所述。
在又另一具體實施例中,Z係-C(=O)-NR
9-或-NR
9-C(=O)-;且式(L2)中之其餘變數係如上文在第十六具體態樣或上文所述之任何具體或更具體實施例中所述。甚至更具體而言,R
9係H或Me。替代地,R
9係H。
在又另一更具體實施例中,Q係i) H;ii) -SO
3H、-Z'-SO
3H、-OPO
3H
2、-Z'-OPO
3H
2、-PO
3H
2、-Z'-PO
3H
2、-CO
2H、-Z'-CO
2H、-NR
14R
15、或-Z'-NR
14R
15,或其醫藥學上可接受之鹽;或,iii) -N
+R
14R
15R
16X
-或-Z'-N
+R
14R
15R
16X
-;Z'係視情況經取代伸烷基、視情況經取代伸環烷基、或視情況經取代伸苯基;R
14至R
16各獨立係視情況經取代烷基;且X
-係醫藥學上可接受之陰離子;且式(L2)中之其餘變數係如上文在第十六具體實施例或上文所述之任何更具體實施例中所述。在一些實施例中,Z'係視情況經取代伸烷基。在又其他實施例中,Z'係C
1-3伸烷基(
例如,-CH
2);且R
14至R
16各獨立係C
1-4烷基。
在又另一更具體實施例中,Q係H、或-SO
3H、或醫藥學上可接受之陽離子(
例如,鈉鹽或鉀鹽);且式(L2)中之其餘變數係如上文在第十六具體態樣或上文所述之任何具體或更具體實施例中所述。
在另一更具體實施例中,對於式(L2):
R
12及R
13在每次出現時各獨立係H或(C
1-C
3)烷基;
Q係H、或-SO
3H、或其醫藥學上可接受之鹽;
Z係-C(=O)-NR
9-或-NR
9-C(=O)-;
R
9係H或(C
1-C
3)烷基;
E係-(CR
10R
11)
q-;
R
10及R
11在每次出現時獨立係H或(C
1-C
3)烷基;且
q及r各係整數1至5。
在第十七具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,-L-係由以下結構式中任一者表示:
(L2a);或
(L2b),
或其醫藥學上可接受之鹽(
例如,鈉鹽或鉀鹽),其中s1係共價連接至D之位點,且s2係共價連接至順丁烯二醯亞胺基團之位點;
q及r各獨立係整數1至6;且其餘變數係如上文針對式(A)或式(B),或在第十四或第十五具體態樣,或其中所述之任何具體或更具體實施例中所述。更具體而言,q及r各獨立係整數1至3。
在第十八具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,-L-係由以下結構式中任一者表示:
及
,
或其醫藥學上可接受之鹽(
例如,鈉鹽或鉀鹽),其中s1係共價連接至D之位點,且s2係共價連接至順丁烯二醯亞胺基團之位點;
且其餘變數係如上文針對式(A)或式(B),或在第十四或第十五具體態樣,或其中所述之任何具體或更具體實施例中所述。
在第十九具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,-L-係由以下結構式表示:
(L3),
其中:
s1係共價連接至D之位點;s2係共價連接至順丁烯二醯亞胺基團之位點;
R
19、R
20、R
21、及R
22在每次出現時獨立係H或視情況經取代烷基;
m及n各獨立係0與10之間的整數;
R
h係H或視情況經取代烷基;
P
L係視情況經取代伸烷基、-(CH
2-CH
2-O)
j-(其中氧原子連接至-(C=O)-基團,該基團連接至P)、胺基酸殘基、或含有2至20個胺基酸殘基之肽;且
j係整數1至24;且其餘變數係如上文針對式(A)或式(B),或第十四或第十五具體態樣,或其中所述之任何具體或更具體實施例中所述。
在第二十具體態樣中,對於式(L3),R
19、R
20、R
21、及R
22各係H或(C
1-C
3)烷基;m及n各獨立係1與6之間的整數;且其餘變數係上文在第十九具體實施例或其中所述之任何具體或更具體實施例中所述。更具體而言,R
19、R
20、R
21、及R
22全部自係H。甚至更具體而言,R
19、R
20、R
21、及R
22全部係H;且m及n各獨立係1與3之間的整數。
在第二十一具體態樣中,對於式(L3),P
L係胺基酸殘基或含有2至10個胺基酸殘基之肽;且其餘變數係如上文在第十九或二十具體態樣或其中所述之任何具體或更具體實施例中所述。更具體而言,P
L係含有2至5個胺基酸殘基之肽。
在一些實施例中,各胺基酸殘基係獨立選自以下之胺基酸之殘基:天然存在之胺基酸、合成胺基酸、胺基酸類似物、及以類似於天然存在之胺基酸之方式起作用的胺基酸模擬物。
在其他實施例中,各胺基酸殘基係獨立選自由以下組成之群之胺基酸之殘基:組胺酸、丙胺酸、異白胺酸、精胺酸、白胺酸、天冬醯胺、離胺酸、天冬胺酸、甲硫胺酸、半胱胺酸、苯基丙胺酸、麩胺酸、蘇胺酸、麩醯胺酸、色胺酸、甘胺酸、纈胺酸、脯胺酸、絲胺酸、酪胺酸、N-甲基-組胺酸、N-甲基-丙胺酸、N-甲基-異白胺酸、N-甲基-精胺酸、N-甲基-白胺酸、N-甲基-天冬醯胺、N-甲基-離胺酸、N-甲基-天冬胺酸、N-甲基-甲硫胺酸、N-甲基-半胱胺酸、N-甲基-苯基丙胺酸、N-甲基-麩胺酸、N-甲基-蘇胺酸、N-甲基-麩醯胺酸、N-甲基-色胺酸、N-甲基-甘胺酸、N-甲基-纈胺酸、N-甲基-脯胺酸、N-甲基-絲胺酸、N-甲基-酪胺酸、羥基脯胺酸、γ-羧基麩胺酸鹽、硒半胱胺酸、O-磷酸絲胺酸、高絲胺酸、正白胺酸、甲硫胺酸亞碸、甲硫胺酸甲基鋶、瓜胺酸、鳥胺酸、半胱胺酸磺酸、半胱胺酸亞磺酸、3-胺基丙胺酸、3-二甲基胺基丙胺酸、2-胺基-4-(二甲基胺基)丁酸、2,4-二胺基丁酸、2-胺基-6-(二甲基胺基)己酸、2-胺基-5-(二甲基胺基)戊酸、及β-丙胺酸,其各獨立呈L或D異構物。更具體而言,各胺基酸殘基係經獨立選擇之甘胺酸或丙胺酸之殘基。
在其他實施例中,P
L係可藉由蛋白酶裂解之肽。更具體而言,P
L係可藉由腫瘤組織中表現之蛋白酶裂解之肽。替代地,P
L係可藉由溶酶體蛋白酶裂解之肽。
在又其他實施例中,P
L係選自由以下所組成之群:Ala-Val、Val-Cit、Val-Lys、Phe-Lys、Lys-Lys、Ala-Lys、Phe-Cit、Leu-Cit、Ile-Cit、Trp-Cit、Phe-Ala、Phe-N
9-甲苯磺醯基-Arg、Phe-N
9-硝基-Arg、Phe-Phe-Lys、D-Phe-Phe-Lys、Gly-Phe-Lys、Leu-Ala-Leu、Ile-Ala-Leu、Val-Ala-Val、Ala-Leu-Ala-Leu (SEQ ID NO: 1)、β-Ala-Leu-Ala-Leu (SEQ ID NO: 2)、Gly-Phe-Leu-Gly (SEQ ID NO: 3)、Val-Arg、Arg-Arg、Val-D-Cit、Val-D-Lys、Val-D-Arg、D-Val-Cit、D-Val-Lys、D-Val-Arg、D-Val-D-Cit、D-Val-D-Lys、D-Val-D-Arg、D-Arg-D-Arg、Ala-Ala、Ala-D-Ala、D-Ala-Ala、D-Ala-D-Ala.、Ala-Met、Met-Ala、Gln-Val、Asn-Ala、Gln-Phe、Gln-Ala、Gly-Gly-Gly、Ala-Ala-Ala、D-Ala-Ala-Ala、Ala-D-Ala-Ala、Ala-Ala-D-Ala、Ala-Val-Cit、Ala-Val-Ala、及β-Ala-Gly-Gly-Gly (SEQ ID NO: 27)。更具體而言,P
L係Gly-Gly-Gly、Ala-Ala-Ala、D-Ala-Ala-Ala、Ala-D-Ala-Ala、Ala-Val-Ala、或β-Ala-Gly-Gly-Gly (SEQ ID NO: 27)。
在第二十二具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,-L-係由以下結構式表示:
,
或其醫藥學上可接受之鹽,其中s1係共價連接至D之位點;s2係共價連接至順丁烯二醯亞胺基團之位點;且其餘變數係如上文針對式(A)或式(B),或在第十四或第十五具體態樣中所述。
在第二十三具體態樣中,含亞胺細胞毒性劑係由下式表示:
;或
,
或其醫藥學上可接受之鹽,且該經修飾細胞毒性劑係由下式表示:
;或
,
或其醫藥學上可接受之鹽。
在更具體實施例中,經修飾細胞毒性劑係由下式表示:
;或
,
或其鈉鹽或鉀鹽。甚至更具體而言,經修飾細胞毒性劑係由下式表示:
;或
。
在一些實施例中,含亞胺細胞毒性劑係由下式表示:
;或
,
或其醫藥學上可接受之鹽,且該經修飾細胞毒性劑係由下式表示:
;或
,
或其醫藥學上可接受之鹽。
在第二十四具體態樣中,可藉由本發明方法製備之結合物係由以下結構式表示:
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;或
,
或其醫藥學上可接受之鹽(
例如,鈉鹽或鉀鹽)。
在一個態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,D係含亞胺PBD化合物。
在第二十五具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,D係由下式表示:
(PBD1');
(PBD1);
(PBD2');
(PBD2);
(PBD3');
(PBD3);
(PBD4');或
(PBD4),
或其醫藥學上可接受之鹽,其中:
W係選自C=O、C=S、CH
2、BH、SO及SO
2;
X
1'係選自-H,胺保護基,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,具有6至18個碳原子之視情況經取代芳基,含有一或多個獨立選自氮、氧、及硫之雜原子之視情況經取代5至18員雜芳環,及含有1至6個獨立選自O、S、N、及P之雜原子之視情況經取代3至18員雜環;
Y
1'係選自-H,側氧基,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,視情況經取代6至18員芳基,含有一或多個獨立選自氮、氧、及硫之雜原子之視情況經取代5至18員雜芳環,具有1至6個雜原子之視情況經取代3至18員雜環;
R
6係-H、-R、-OR、-SR、-NR'R''、-NO
2、或鹵素;
A及A'相同或不同,且獨立選自-O-、側氧基(-C(=O)-)、-CRR'O-、-CRR'-、-S-、-CRR'S-、-NR
5及-CRR'N(R
5)-,
R在每次出現時獨立選自由以下所組成之群:-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,具有6至18個碳原子之視情況經取代芳基,含有一或多個獨立選自氮、氧、及硫之雜原子之視情況經取代5至18員雜芳環,或含有1至6個獨立選自O、S、N、及P之雜原子之視情況經取代3至18員雜環;
R'及R''各獨立選自-H,-OH,-OR,-NHR,-NR
2,-COR,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,及具有1至6個獨立選自O、S、N、及P之雜原子之視情況經取代3至18員雜環;
R
c係-H,或經取代或未取代之具有1至4個碳原子之直鏈或支鏈烷基,或該鍵接至反應性基團之連接基團;
n係整數1至24;
R
5在每次出現時獨立地係-H或具有1至10個碳原子之視情況經取代直鏈或支鏈烷基;
D
0及D
0'相同或不同,且獨立地不存在,或選自由以下所組成之群:視情況經取代之具有1至10個碳原子之直鏈、支鏈或環狀烷基、烯基或炔基,胺基酸,帶有2至6個胺基酸之肽,及聚乙二醇單元(-OCH
2CH
2)
n-;
L係不存在,連接基,聚乙二醇單元(-OCH
2CH
2)
n-,視情況經取代具有1至10個碳原子之直鏈、支鏈或環狀烷基或烯基,視情況經取代苯基,視情況經取代具有1至6個獨立選自O、S、N及P之3至18員雜環或5至18員雜芳環;
R
a、R
a'、R
b及R
b'係相同或不同,且獨立選自由以下所組成之群:-H,鹵化物或視情況經取代具有1至10個碳原子之支鏈、直鏈或環狀烷基;或R
a及R
a'及/或R
b及R
b'在一起分別形成含有雙鍵之基團=B及=B';
=B及=B'係相同或不同,且獨立選自視情況經取代支鏈或直鏈烯基或羰基;
Q係Q
1-Ar-Q
2;
Q'係Q
1'-Ar'-Q
2';
Q
1及Q
1'各獨立係不存在,直鏈、支鏈或環狀1至6個碳原子之烷基或-CH=CH單元;
Ar及Ar'各獨立係不存在或表示芳基;
Q
2及Q
2'各獨立選自H,連接基,經取代或未取代具有1至10個碳原子之直鏈、支鏈或環狀烷基、烯基或炔基,聚乙二醇單元-R
c'-(OCH
2CH
2)
n-R
c,或選自以下之取代基:鹵素、鈲[-NH(C=NH)NH
2]、-R、-OR、-NR'R''、-NO
2、-NCO、-NR'COR''、NR'(C=O)OR''-SR、由-SOR'表示之亞碸、由SO
2R'表示之碸、磺酸鹽-SO
3M、硫酸鹽-OSO
3M、由SO
2NR'R''表示之磺醯胺、氰基、疊氮基、-COR'、-OCOR'或-OCONR'R'';且
R
c'係不存在或選自具有1至5個碳原子之直鏈或支鏈烷基、烯基或炔基。
在第二十六具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,D係選自以下之一:
(PBD5')
(PBD5)、
(PBD6')、
(PBD6)、
(PBD7')、
(PBD7)、
(PBD8')、
(PBD8)、
(PBD9')、
(PBD9)、
(PBD10')及
(PBD10),
或其醫藥學上可接受之鹽,其中:
式(PBD5')、(PBD6')、(PBD7')、(PBD8')、(PBD5)、(PBD6)、(PBD7)或(PBD8)中L'、L''及L'''之一係由下式表示:
-Z
1-P
1-Z
2-R
x1-C(=O)- (A'),或
-N(R
e)-R
x1-C(=O)- (D');
且另兩者各獨立選自-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,鹵素,鈲[-NH(C=NH)NH
2],-OR,-NR'R'',-NO
2,-NR'COR'',-SR,-SOR',-SO
2R',-SO
3H,-OSO
3H,-SO
2NR'R'',氰基,疊氮基,-COR',-OCOR',及-OCONR'R'';
式(PBD9')、(PBD10')、(PBD9)或(PBD10)中Q
2及Q
2'之一係由下式表示:
-Z
1-P
1-Z
2-R
x1-C(=O)- (A')、
--N(R
e)-R
x1-C(=O)- (D');或
-Z
1-P
1-Z
2-
(E'),
且另一者係選自-H、-R、-OR、-NR'R''、-NO
2、-NR'(C=O)OR''、-SR或-NO
2;
Z
1及Z
2之一係-C(=O)-,且另一者係-NR
5-;
P
1係胺基酸殘基或含有2至20之間個胺基酸殘基之肽;
R
x1係具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基;
R
e係-H,具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基,或-(CH
2-CH
2-O)
n-R
k,其中R
k係-H,具有1至6個碳原子之直鏈、支鏈、環狀烷基,其視情況帶有二級胺基(
例如,-NHR
101)或三級胺基(-NR
101R
102)基團,或5或6員含氮雜環,其中R
101及R
102各獨立地係具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基;
R
c係-H或具有1至4個碳原子之視情況經取代直鏈或支鏈烷基;
R
5在每次出現時獨立地係-H或具有1至10個碳原子之視情況經取代直鏈或支鏈烷基。
R
a''及R
b''係相同或不同,且選自-H及-Me;且
n'係選自0、1、2及3;且其餘變數係如第二十五具體態樣中所述。
在第二十七具體態樣中,式(PBD5')、(PBD6')、(PBD7')、(PBD8')、(PBD5)、(PBD6)、(PBD7)或(PBD8)中L'、L''及L'''之一係由式(A')或(D')表示,且另兩者係-H、具有1至6個碳原子之直鏈或支鏈烷基、鹵素、-OH、(C
1-C
6)烷氧基或-NO
2;或式(PBD9')、(PBD10')、(PBD9)或(PBD10)中Q
2及Q
2'之一係由式(A')、(D')或(E')表示;且另一者係-H、具有1至6個碳原子之直鏈或支鏈烷基、鹵素、-OH、(C
1-C
6)烷氧基或-NO
2;且其餘變數係如第二十六具體態樣中所述。
在第二十八具體態樣中,L''及L'''均係-H;且式(PBD5')、(PBD6')、(PBD7')、(PBD8')、(PBD5)、(PBD6)、(PBD7)或(PBD8)中L'係由下式表示:
-NR
5-P
1-C(=O)-(CR
aR
b)
s-C(=O)- (B1');
-NR
5-P
1-C(=O)-Cy-(CR
aR
b)
s1'-C(=O)- (B2');
-C(=O)-P
1-NR
5-(CR
aR
b)
s-C(=O)- (C1');或
-C(=O)-P
1-NR
5-Cy-(CR
aR
b)
s1'-C(=O)- (C2');
式(PBD9')、(PBD10')、(PBD9)或(PBD10)中Q
2及Q
2'之一係由下式表示:
-NR
5-P
1-C(=O)-(CR
aR
b)
s-C(=O)- (B1');
-NR
5-P
1-C(=O)-Cy-(CR
aR
b)
s1'-C(=O)- (B2');
-C(=O)-P
1-NR
5-(CR
aR
b)
s-C(=O)- (C1'),
-C(=O)-P
1-NR
5-Cy-(CR
aR
b)
s1'-C(=O)- (C2');
-NR
5-P
1-C(=O)- (E1');或
-C(=O)-P
1-NR
5- (E2');
其中:
R
a及R
b在每次出現時各獨立地係-H、(C
1-C
3)烷基、或帶電取代基或可離子化基團Q;
s係整數1至6;
s1'係0或整數1至6;且
Cy係具有5或6個環碳原子之環狀烷基,其視情況經鹵素、-OH、(C
1-C
3)烷基、(C
1-C
3)烷氧基、或鹵基(C
1-C
3)烷基取代;且其餘變數係如第二十七具體態樣中所述。在一些實施例中,R
a及R
b均係H;式(B2')及(C2')中Cy係環己烷;R
5係H或Me;且s1'係0或1。
在第二十九具體態樣中,P
1係含有2至10個胺基酸殘基之肽;且其餘變數係如第二十八具體態樣中所述。在一些實施例中,P
1係含有2至5個胺基酸殘基之肽。在一些實施例中,P
1係Gly-Gly-Gly、Ala-Val、Val-Cit、Val-Lys、Phe-Lys、Lys-Lys、Ala-Lys、Phe-Cit、Leu-Cit、Ile-Cit、Trp、Cit、Phe-Ala、Phe-N
9-甲苯磺醯基-Arg、Phe-N
9-硝基-Arg、Phe-Phe-Lys、D-Phe-Phe-Lys、Gly-Phe-Lys、Leu-Ala-Leu、Ile-Ala-Leu、Val-Ala-Val、Ala-Leu-Ala-Leu (SEQ ID NO: 1)、β-Ala-Leu-Ala-Leu (SEQ ID NO: 2)、Gly-Phe-Leu-Gly (SEQ ID NO: 3)、Val-Arg、Arg-Arg、Val-D-Cit、Val-D-Lys、Val-D-Arg、D-Val-Cit、D-Val-Lys、D-Val-Arg、D-Val-D-Cit、D-Val-D-Lys、D-Val-D-Arg、D-Arg-D-Arg、Ala-Ala、Ala-D-Ala、D-Ala-Ala、D-Ala-D-Ala、Ala-Met、Gln-Val、Asn-Ala、Gln-Phe、及Gln-Ala。在一些實施例中,P
1係Gly-Gly-Gly、Ala-Val、Ala-Ala、Ala-D-Ala、D-Ala-Ala、或D-Ala-D-Ala。
在第三十具體態樣中,對於第二十五、第二十六、第二十七、第二十八或第二十九具體態樣中任一項及其中所述之實施例中所述之方法,R
6係-OMe;X
1'及Y
1'均係-H;且A及A'係-O-。
在第三十一具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,D係由以下結構式表示:
;
;
;
;
;或
,
或其醫藥學上可接受之鹽。
在第三十二具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,-L-係由以下結構式表示:
,
或其醫藥學上可接受之鹽,其中:
s1係共價連接至D之位點;s2係共價連接至順丁烯二醯亞胺基團之位點;
R
23及R
24在每次出現時獨立係H或視情況經取代烷基;
m'係0與10之間的整數;且
R
h'係H或視情況經取代烷基;且其餘變數係如上文第二十五、第二十六、第二十七、第二十八、第二十九、第三十、第三十一或第三十二具體態樣中所述。
在一些實施例中,R
23及R
24均係H;且m'係1與6之間的整數。
在一些實施例中,R
h'係H。
在一些實施例中,L係由以下結構式表示:
。
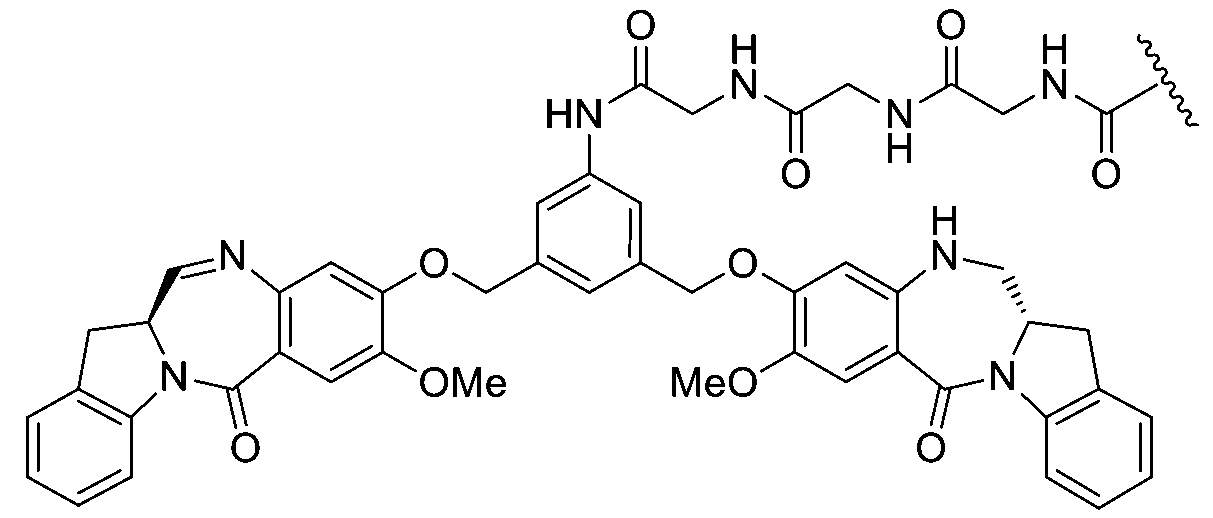
在第三十四具體態樣中,含亞胺細胞毒性劑係由下式表示:
;
;
;
;
;或
或其醫藥學上可接受之鹽。
在一些實施例中,含亞胺細胞毒性劑係由下式表示:
,或其醫藥學上可接受之鹽;該經修飾含亞胺細胞毒性劑係由下式表示:
或其醫藥學上可接受之鹽;且該結合物係由下式表示:
或其醫藥學上可接受之鹽。
在第三十五具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,D係由下式表示:
(PBD11')、
(PBD11)、
(PBD12')、
(PBD12)、
(PBD13')、
(PBD13)、
(PBD14')、
(PBD14)、
(PBD15')、
(PBD15)、
(PBD16')及
(PBD16),
或其醫藥學上可接受之鹽,其中:
X
1'係選自由以下所組成之群:-H,-OH,具有1至10個碳原子之經取代或未取代直鏈、支鏈、或環狀烷基、烯基、或炔基,苯基,及胺保護基;
Y
1'選自由以下組成之群:-H、側氧基、取代或未取代之具有1至10個碳原子之直鏈、支鏈或環狀烷基、烯基或炔基;
式(PBD15)或(PBD16)中Q
2及Q
2'之一係-W'-R
x-S-;且另一者係選自-H,具有1之10個碳原子之視情況經取代直鏈、支鏈或環狀烷基、烯基或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
c,鹵素,鈲[-NH(C=NH)NH
2],-OR,-NR'R'',-NO
2,-NR'COR'',-SR,-SOR',-SO
2R',-SO
3H,-OSO
3H,-SO
2NR'R'',氰基,疊氮基,-COR',-OCOR'及-OCONR'R'';
W'不存在,或選自-O-、-N(R
e)-、-N(R
e)-C(=O)-、-N(C(=O)R
e)-、-S-、或-CH
2-S-、-CH
2NR
e-;
R
x不存在,或選自具有1至10個碳原子之直鏈、支鏈、或環狀烷基;
R
e係-H,具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基,或-(CH
2-CH
2-O)
n-R
k,其中R
k係-H,具有1至6個碳原子之直鏈、支鏈、環狀烷基,其視情況帶有二級胺基(
例如,-NHR
101)或三級胺基(-NR
101R
102)基團,或5或6員含氮雜環,其中R
101及R
102各獨立地係具有1至10個碳原子之直鏈、支鏈、或環狀烷基、烯基、或炔基;
n係整數1至24;
R
6係-H、-R、-OR、-SR、-NR'R''、-NO
2、或鹵素;且
R係-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,或PEG基團-(CH
2CH
2O)
n-R
c,其中n係整數1至24,且R
c係具有1至4個碳原子之直鏈或支鏈烷基;
R'及R''各獨立選自-H,-OH,-OR,-NRR
g',-COR,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,具有6至18個碳原子之視情況經取代芳基,具有1至6個選自O、S、N、及P之雜原子之視情況經取代3至18員雜環,PEG基團-(CH
2CH
2O)
n-R
c,且R
g'係-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,或PEG基團-(CH
2CH
2O)
n-R
c。
在第三十六具體態樣中,對於式(PBD11')、(PBD12')、(PBD13')、(PBD14')、(PBD15')、(PBD16')、(PBD11)、(PBD12)、(PBD13)、(PBD14)、(PBD15)或(PBD16),X
1'及Y
1'均係-H;
R
6係-OMe;
W'係-N(R
e)-或-N(R
e)-C(=O)-;
R
e係-H,具有1至4個碳原子之直鏈或支鏈烷基,或-(CH
2-CH
2-O)
n-R
k,其中R
k係-H,具有1至4個碳原子之直鏈或支鏈烷基;
n係整數2至6;且
R
x係具有1至6個碳原子之直鏈或支鏈烷基;且其餘變數係如第三十五具體態樣中所述。
在第三十七具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,L係由以下結構式表示:
,
或其醫藥學上可接受之鹽,其中:
s1係共價連接至D之位點,且s2係共價連接至順丁烯二醯亞胺基團之位點;
E係-(CR
10R
11)
q-、環烷基、或環烷基烷基;
Z係不存在、-SO
2NR
9-、-NR
9SO
2-、-C(=O)-NR
9-、-NR
9-C(=O)-、-C(=O)-O-、-O-C(=O)-、-C(=O)-NR
9-(CH
2CH
2O)
p-、-NR
9-C(=O)-(CH
2CH
2O)
p-、-(OCH
2CH
2)
p-C(=O)NR
9-、或-(OCH
2CH
2)
p-NR
9-C(=O)-;
p係整數1至24;
Q係H、帶電取代基、或可離子化基團;
R
9、R
10、R
11、R
12、及R
13在每次出現時獨立係H或視情況經取代烷基;且,
q及r在每次出現時獨立係0與10之間的整數;且其餘變數係如第三十五或第三十六具體態樣中所述。
在一些實施例中,E係-(CR
10R
11)
q-。在一些實施例中,Z係-C(=O)-NR
9-或-NR
9-C(=O)-。在一些實施例中,R
9係-H。在一些實施例中,R
9、R
10、R
11、R
12及R
13全部係H;且q及r各獨立係1與6之間的整數。
在一些實施例中,對於第三十七具體態樣中所述之-L-:
R
12及R
13在每次出現時各獨立係H或(C
1-C
3)烷基;
Q係H、或-SO
3H、或其醫藥學上可接受之鹽
Z係-C(=O)-NR
9-或-NR
9-C(=O)-;
R
9係H或(C
1-C
3)烷基;
E係-(CR
10R
11)
q-。
R
10及R
11在每次出現時獨立係H或(C
1-C
3)烷基;且
q及r各係整數1至5。
在第三十八具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,L係由以下結構式中任一者表示:
及
,
或其醫藥學上可接受之鹽,且其餘變數係如第三十五或第三十六具體態樣中所述。
在第三十九具體態樣中,對於式(A)之含亞胺細胞毒性劑或式(B)之結合物,L係由以下結構式表示:
,
或其醫藥學上可接受之鹽,其中:
s1係共價連接至D之位點;s2係共價連接至順丁烯二醯亞胺基團之位點;
R
19、R
20、R
21、及R
22在每次出現時獨立係H或視情況經取代烷基;
m及n各獨立係0與10之間的整數;
R
h係H或視情況經取代烷基;
P
L係視情況經取代伸烷基、-(CH
2-CH
2-O)
j-(其中氧原子連接至-(C=O)-基團,該基團連接至P)、胺基酸殘基、或含有2至20個胺基酸殘基之肽;且
j係整數1至24;且其餘變數係如第三十五或第三十六具體態樣中所述。
在一些實施例中,R
19、R
20、R
21及R
22各自係H;且m及n各獨立係1與6之間的整數。
在一些實施例中,P
L係含有2至10個胺基酸殘基之肽。更具體而言,P
L係含有2至5個胺基酸殘基之肽。甚至更具體而言,P
L係選自由以下所組成之群:Ala-Val、Val-Ala、Val-Cit、Cit-Val、Val-Lys、Phe-Lys、Lys-Lys、Ala-Lys、Phe-Cit、Leu-Cit、Ile-Cit、Trp-Cit、Phe-Ala、Phe-N
9-甲苯磺醯基-Arg、Phe-N
9-硝基-Arg、Phe-Phe-Lys、D-Phe-Phe-Lys、Gly-Phe-Lys、Leu-Ala-Leu、Ile-Ala-Leu、Val-Ala-Val、Ala-Leu-Ala-Leu (SEQ ID NO: 1)、β-Ala-Leu-Ala-Leu (SEQ ID NO: 2)、Gly-Phe-Leu-Gly (SEQ ID NO: 3)、Val-Arg、Arg-Arg、Val-D-Cit、Val-D-Lys、Val-D-Arg、D-Val-Cit、D-Val-Lys、D-Val-Arg、D-Val-D-Cit、D-Val-D-Lys、D-Val-D-Arg、D-Arg-D-Arg、Ala-Ala、Ala-D-Ala、D-Ala-Ala、D-Ala-D-Ala.、Ala-Met、Met-Ala、Gln-Val、Asn-Ala、Gln-Phe、Gln-Ala、Gly-Gly-Gly、Ala-Ala-Ala、D-Ala-Ala-Ala、Ala-D-Ala-Ala、Ala-Ala-D-Ala、Ala-Val-Cit、Ala-Val-Ala及β-Ala-Gly-Gly-Gly。
在一些實施例中,L係由以下結構式表示:
,
或其醫藥學上可接受之鹽。
在第四十具體實施例中,對於本文所述之方法,含亞胺細胞毒性劑係由下式表示:
(PBD17');
(PBD17);
(PBD18'),或
(PBD18),
或其醫藥學上可接受之鹽,其中:
點線指示視情況存在雙鍵;
R
3''係C
3-12伸烷基,
各X'在每次出現時獨立地係-O-、-S-或-N(H)-,
各R
2獨立地選自-H、-OH、-CN、-R
1'、-OR
1'、-O-SO
2-R
1'、-CO
2R
1'、-COR
1'或鹵基,或兩個R
2在一起係=O、=CH
2、=CH-R
a或=C(R
a)
2;
各R
2'獨立地選自-H、OH、-CN、-R
1'、-OR
1'、-O-SO
2-R
1'、-CO
2R
1'、-COR
1'或鹵基;
R
4b係選自以下之離去基團:-OR
6'、-OCOR
4'、-OCOOR
4'、-OCONR
4'R
5'、-NR
4'R
5'、-NR
4'COR
5'、-NR
4'NR
4'R
5'、視情況經取代5員或6員含氮雜環(
例如,哌啶、四氫吡咯、吡唑、嗎啉)、由-NR
4'(C=NH)NR
4'R
5'表示之鈲、胺基酸或由-NR
6'COP'表示之肽,其中P'係胺基酸或含有2至20之間個胺基酸單元之肽、-SR
6'、-SOR
4'、-SO
2M、-SO
3M、-OSO
3M、鹵素、氰基及疊氮基;
R
L係帶有可與細胞結合劑(CBA)形成共價鍵的順丁烯二醯亞胺部分的連接基;
R
6及R
9獨立選自-H、-R
1'、-OH、-OR
1'、-SH、-SR
1'、-NH
2、-NHR
1'、-NR
1'R
3'、-NO
2、Me
3Sn及鹵基;且,
R
1'及R
3'各獨立選自視情況經取代C
1-12烷基、C
3-20雜環基或C
5-20芳基,且視情況關於基團-NR
1'R
3'、R
1'及R
3'與其所連接的氮原子一起形成視情況經取代4、5、6或7員雜環;或R
6至R
9之任一對相鄰基團在一起形成基團-O-(CH
2)
p-O-,其中p係1或2;
R
4'及R
5'各獨立選自-H,-OH,-OR
6',-NHR
6',-NR
6' 2,-COR
6',具有1至10個碳原子之視情況經取代直鏈、支鏈或環烷基、烯基或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
b或具有1至6個獨立選自O、S、N或P之雜原子的視情況經取代3-18員雜環;
R
6'在每次出現時獨立選自由以下所組成之群:-H,具有1至10個碳原子之視情況經取代直鏈、支鏈、或環狀烷基、烯基、或炔基,聚乙二醇單元-(CH
2CH
2O)
n-R
b,具有6至18個碳原子之視情況經取代芳基,含有一或多個獨立選自氮、氧或硫之雜原子之視情況經取代5至18員雜芳環,及含有1至6個獨立選自O、S、N或P之雜原子之視情況經取代3至18員雜環;
R
a獨立選自-R
1'、-CO
2R
1'、-COR
1'、-CHO、-CO
2H或鹵基;
R
b係-H或具有1至4個碳原子之經取代或未取代直鏈或支鏈烷基;
M係H或醫藥學上可接受之陽離子;且
n係整數1至24。
在第四十一具體態樣中,對於本文所述之方法,含亞胺細胞毒性劑係由下式表示:
(PBD19');
(PBD19);
(PBD20')或
(PBD20),
或其醫藥學上可接受之鹽,其中R
3''係C
3-5伸烷基;且其餘變數係如上文第四十具體態樣中所述。
在第四十二具體態樣中,對於式(PBD17')、(PBD18')、(PBD19')、(PBD20')、(PBD17)、(PBD18)、(PBD19)或(PBD20),R
L係
,其中L
1係可裂解連接基,A係帶有能夠將L
1連接至該細胞結合劑之順丁烯二醯亞胺的連接基團,L
2係共價鍵或與-OC(=O)-一起形成自消耗連接基;且其餘變數係如上文第四十或第四十一具體態樣中所述。
在第四十三具體態樣中,對於第四十二具體態樣中所述之R
L,L
1係含有2至10個胺基酸殘基之肽;且其餘變數係如上文第四十二具體態樣中所述。更具體而言,L
1係含有2至5個胺基酸殘基之肽。甚至更具體而言,L
1係選自由以下所組成之群:Phe-Lys、Val-Ala、Val-Lys、Ala-Lys、Val-Cit、Phe-Cit、Leu-Cit、Ile-Cit、Phe-Arg、Trp-Cit、Lys-Lys、Phe-Ala、Phe-N9-甲苯磺醯基-Arg、Phe-N9-硝基-Arg、Val-Arg、Arg-Val、Arg-Arg、Val-D-Cit、Val-D-Lys、Val-D-Arg、D-Val-Cit、D-Val-Lys、D-Val-Arg、D-Val-D-Cit、D-Val-D-Lys、D-Val-D-Arg、D-Arg-D-Arg、Gly-Gly-Gly、Phe-Phe-Lys、D-Phe-Phe-Lys、Gly-Phe-Lys、Leu-Ala-Leu、Ile-Ala-Leu、Val-Ala-Val、Ala-Leu-Ala-Leu (SEQ ID NO:1)、β-Ala-Leu-Ala-Leu (SEQ ID NO:2)及Gly-Phe-Leu-Gly (SEQ ID NO:3)。
在第四十四具體態樣中,對於第四十二具體態樣中所述之R
L,-C(=O)O-及L
2一起形成以下基團:
其中星號指示至N10位之連接點,波形線指示至該連接基L
1之連接點,Y'係NH-、-O-、-C(=O)NH-或-C(=O)O-,且n係0至3;且其餘變數係如第四十二或第四十三具體態樣中所述。
在第四十五具體態樣中,對於第四十二具體態樣中所述之R
L,-C(=O)O-及L
2一起形成以下基團:
,
且其餘變數係如第四十二或第四十三具體態樣中所述。
在第四十六具體態樣中,對於第四十二具體態樣中所述之R
L,L
1及L
2與-OC(=O)-一起組成選自以下之基團:
或
,
其中星號指示至N10位之連接點,且波形線指示至該連接基L
1之其餘位之連接點或至A之連接點。
在第四十七具體態樣中,對於第四十二具體態樣中所述之R
L,A係由以下之一表示:
(i)
,其中星號指示至L
1之連接點,且p係1至6;或
(ii)
,其中星號指示至L
1之連接點,r係0或1,且s係0至30;
且其餘變數係如第四十二、第四十三、第四十四、第四十五或第四十六具體態樣中所述。
在一些實施例中,p係4至6;r係1;且s係1至10。
在第四十八具體態樣中,對於本發明中所述之方法,含亞胺細胞毒性劑係由下式表示:
;
或其醫藥學上可接受之鹽;該經修飾含亞胺細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽,且該結合物係由下式表示:
其中s係2至8;w係1或2;且CBA係本文所述之細胞結合劑。在一些實施例中,s係7。
在一些實施例中,對於本發明中所述之方法,含亞胺細胞毒性劑係由下式表示:
;
或其醫藥學上可接受之鹽;該經修飾含亞胺細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽,且該結合物係由下式表示:
其中s係2至8;w係1或2;且CBA係本文所述之細胞結合劑。在一些實施例中,s係7。
在第四十九具體態樣中,對於本發明中所述之方法,含亞胺細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽;該經修飾含亞胺細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽,且該結合物係由下式表示:
或其醫藥學上可接受之鹽,其中s係2至8;w係1或2;且CBA係本文所述之細胞結合劑。在一些實施例中,s係7。
在一些實施例中,對於本發明中所述之方法,含亞胺細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽;該經修飾含亞胺細胞毒性劑係由下式表示:
,
或其醫藥學上可接受之鹽,且該結合物係由下式表示:
或其醫藥學上可接受之鹽,其中s係2至8;w係1或2;且CBA係本文所述之細胞結合劑。在一些實施例中,s係7。
在一些實施例中,上文任何實施例中所述之帶電取代基或可離子化基團Q係i) -SO
3H、-Z'-SO
3H、-OPO
3H
2、-Z'-OPO
3H
2、-PO
3H
2、-Z'-PO
3H
2、-CO
2H、-Z'-CO
2H、-NR
11R
12、或-Z'-NR
11R
12、或其醫藥學上可接受之鹽;或ii) -N
+R
14R
15R
16X
-或-Z'-N
+R
14R
15R
16X
-;Z'係視情況經取代伸烷基、視情況經取代伸環烷基、或視情況經取代伸苯基;R
14至R
16各獨立地係視情況經取代烷基;且X
-係醫藥學上可接受之陰離子。更具體而言,Q係-SO
3H或其醫藥學上可接受之鹽。甚至更具體而言,Q係-SO
3Na。
細胞結合劑
在一些實施例中,可用於本發明方法之細胞結合劑係具有經工程改造半胱胺酸殘基(
例如,在重鏈之EU/OU編號442位)之抗體。經工程改造Cys殘基可定位於抗體之一或兩條重鏈上、抗體之一或兩條輕鏈上、或其抗原結合部分、或其組合。在一些實施例中,Cys殘基定位於抗體重鏈之EU/OU編號442位。在一些實施例中,抗體係如本文所述之半胱胺酸工程改造抗體。
在一些實施例中,本發明抗體係單株抗體、嵌合抗體、人源化抗體、表面重塑抗體、或人類抗體。
在其他實施例中,細胞結合劑係抗體、單鏈抗體、特異性結合至靶細胞之抗體片段、單株抗體、單鏈單株抗體、特異性結合至靶細胞之單株抗體片段(或「抗原結合部分」)、嵌合抗體、特異性結合至靶細胞之嵌合抗體片段(或「抗原結合部分」)、域抗體(
例如,sdAb)、或特異性結合至靶細胞之域抗體。
在又其他實施例中,細胞結合劑係人源化抗體、人源化單鏈抗體、或人源化抗體片段(或「抗原結合部分」)。在具體實施例中,人源化抗體係huMy9-6或另一相關抗體,其描述於美國專利第7,342,110號及第7,557,189號中。在另一具體實施例中,人源化抗體係美國專利第8,557,966號中所述之抗葉酸受體抗體。在又其他實施例中,人源化抗體係2016年6月28日提交之標題為「ANTI-CD123 ANTIBODIES AND CONJUGATES AND DERIVATIVES THEREOF」之美國申請案第15/195,401號中所述之抗CD123抗體。所有該等申請案之教導皆以全文引用之方式併入本文中。
在一些實施例中,細胞結合劑係表面重塑抗體、表面重塑單鏈抗體、表面重塑抗體片段(或「抗原結合部分」)、或雙特異性抗體。
本發明之又另一態樣提供一種重組抗體,其包含重鏈、輕鏈、或其抗原結合部分之成熟加工序列,其衍生自本文所述之標的重組抗體重鏈(HC)、輕鏈(LC)、或其抗原結合部分之任一者。
例如,重組抗體可係或可包含scFv-Fc、Fcab、mAb2、小模組免疫醫藥(SMIP)、Genmab/unibody或duobody、微型抗體、IgGΔCH2、DVD-Ig、probody、內抗體(intrabody)、或多特異性抗體。
DUOBODY ® 係雙特異性經修飾IgG1抗體異源二聚物IgG1鉸鏈區,其通常包括(i)合適鉸鏈區,其含有CPPC序列且不容許
體內Fab臂交換;及(ii) 類IgG4 CH3域,其經修飾以含有F405L及K409R殘基,此舉使其容許
體內Fab臂交換。(參見例如,WO2008119353及WO2011131746)。
在一些實施例中,重組抗體可包含重鏈、輕鏈、或其抗原結合部分之成熟加工序列之一、二、三、或四者,其各自衍生自本文所述之標的重組抗體重鏈(HC)、輕鏈(LC)、或其抗原結合部分之任一者。
在其他實施例中,重組抗體可係包含第一重鏈多肽及第二重鏈多肽之異源二聚抗體,其中第一重鏈多肽之Fc區及第二重鏈多肽之Fc區在一界面處相接,且第二重鏈多肽之Fc區之界面包含隆凸,其可定位於第一重鏈多肽之Fc區之界面中之空腔中。在某些實施例中,提高雙特異性抗體中重鏈之特異性配對的孔中結技術可基於例如Genentech / Roche之CrossMab技術,
例如,藉由調換CH1及κ恆定區以進一步減少或消除輕鏈失配而進一步改良。
替代地,在開發全雙特異性抗體中,類似結果亦可使用LC異源二聚物來達成,諸如充分補充多種其他生物方法的Zymeworks AZYMETRIC™異源二聚IgG1輕鏈平台技術,包括共同輕鏈、域抗體、及單鏈格式。
在一些實施例中,第二重鏈多肽之Fc區與模板/原始多肽不同以編碼隆凸,或第一重鏈多肽之Fc區與模板/原始多肽不同以編碼空腔,或兩者。
在其他實施例中,隆凸及空腔各包含天然存在之胺基酸殘基。
在其他實施例中,包含隆凸之第二重鏈多肽之Fc區係藉由用側鏈體積大於原始殘基的輸入殘基置換模板/原始多肽之界面之原始殘基來產生。
在又其他實施例中,包含隆凸之第二重鏈多肽之Fc區係藉由包含以下步驟之方法來產生,在該步驟中,將編碼該多肽之界面之原始殘基的核酸用編碼側鏈體積大於原始殘基之輸入殘基之核酸置換。
在一些實施例中,抗體包括雙特異性、多特異性、及單特異性抗體變異體,其包括抗原結合區及重鏈恆定域,其中重鏈恆定域經修飾以在EU/OU編號之442位處包括Cys。
在其他實施例中,抗體可結合至靶細胞上之配體,諸如細胞表面配體,包括細胞表面受體。
具體示範性抗原或配套可包括腎素;生長激素(
例如,人類生長激素及牛生長激素);生長激素釋放因子;副甲狀腺激素;促甲狀腺激素;脂蛋白;α-1-抗胰蛋白酶;胰島素A鏈;胰島素B鏈;胰島素原;促濾泡激素;降鈣素;黃體激素;升糖素;凝血因子(
例如,因子vmc、因子IX、組織因子、及溫韋伯氏因子(von Willebrands factor));抗凝血因子(
例如,蛋白質C);心房利鈉因子;肺界面活性物質;纖維蛋白溶酶原活化劑(
例如,尿激酶、人尿、或組織型纖維蛋白溶酶原活化劑);鈴蟾素;凝血酶;造血生長因子;腫瘤壞死因子-α及腫瘤壞死因子-β;腦啡勝肽酶;RANTES (
亦即,調控活化正常T細胞表現及分泌因子);人類巨噬細胞炎性蛋白-1-α;血清白蛋白(人類血清白蛋白);苗勒管抑制物(Muellerian-inhibiting substance);鬆弛素A鏈;鬆弛素B鏈;鬆弛素原;小鼠促性腺素相關肽;微生物蛋白(β-內醯胺酶);DNase;IgE;細胞毒性T淋巴細胞相關抗原(
例如,CTLA-4);抑制素;活化素;血管內皮生長因子;激素或生長因子受體;蛋白質A或D;類風濕因子;神經營養因子(
例如,骨源性神經營養因子、神經營養素-3、神經營養素-4、神經營養素-5、或神經營養素-6)、神經生長因子(
例如,NGF-β);血小板源性生長因子;纖維母細胞生長因子(
例如,aFGF及bFGF);纖維母細胞生長因子受體2;表皮生長因子;轉化生長因子(
例如,TGF-α、TGF-β1、TGF-β2、TGF-β3、TGF-β4、及TGF-β5);類胰島素生長因子-I及類胰島素生長因子-II;des(1-3)-IGF-I (腦IGF-I);類胰島素生長因子結合蛋白;黑素轉鐵蛋白(melanotransferrin);EpCAM;GD3;FLT3;PSMA;PSCA;MUC1;MUC16;STEAP;CEA;TENB2;EphA受體;EphB受體;葉酸受體;FOLR1;間皮素;槲皮素;α
vβ
6;整合素;VEGF;VEGFR;EGFR;轉鐵蛋白受體;IRTA1;IRTA2;IRTA3;IRTA4;IRTA5;CD蛋白(
例如,CD2、CD3、CD4、CD5、CD6、CD8、CD11、CD14、CD19、CD20、CD21、CD22、CD25、CD26、CD28、CD30、CD33、CD36、CD37、CD38、CD40、CD44、CD52、CD55、CD56、CD59、CD70、CD79、CD80。CD81、CD103、CD105、CD123、CD134、CD137、CD138、及CD152;一或多種腫瘤相關抗原或細胞表面受體(參見美國公開案第2008/0171040號或美國公開案第2008/0305044號,其以全文應用方式併入);紅血球生成素;骨生成誘導因子;免疫毒素;骨形態生成蛋白;干擾素(
例如,干擾素-α、干擾素-β、及干擾素-γ);集落刺激因子(
例如,M-CSF、GM-CSF、及G-CSF);白介素(
例如,IL-1至IL-10);超氧化物歧化酶;T細胞受體;表面膜蛋白;衰變加速因子;病毒抗原(
例如,HIV包膜之一部分);運輸蛋白;歸巢受體;地址素(addressin);調控蛋白;整合素(
例如,CD11a、CD11b、CD11c、CD18、ICAM、VLA-4、及VCAM);腫瘤相關抗原(
例如,HER2、HER3、及HER4受體);內皮蛋白(endoglin);c-Met;c-kit;1GF1R;PSGR;NGEP;PSMA;PSCA;TMEFF2;LGR5;B7H4;及上文所列多肽中任一者之片段。
在一些實施例中,細胞結合劑係抗葉酸受體抗體。更具體而言,抗葉酸受體抗體係特異性結合人類葉酸受體1之人源化抗體,其中該抗體包含:(a)重鏈CDR1,其包含GYFMN (SEQ ID NO: 4);重鏈CDR2,其包含RIHPYDGDTFYNQXaa
1FXaa
2Xaa
3(SEQ ID NO: 5);及重鏈CDR3,其包含YDGSRAMDY (SEQ ID NO: 6);以及(b)輕鏈CDR1,其包含KASQSVSFAGTSLMH (SEQ ID NO: 7);輕鏈CDR2,其包含RASNLEA (SEQ ID NO: 8);及輕鏈CDR3,其包含QQSREYPYT (SEQ ID NO: 9);其中Xaa
1係選自K、Q、H、及R;Xaa
2係選自Q、H、N、及R;且Xaa
3係選自G、E、T、S、A、及V。較佳的是,重鏈CDR2序列包含RIHPYDGDTFYNQKFQG(SEQ ID NO: 10)。
在其他實施例中,抗葉酸受體抗體係特異性結合人類葉酸受體1之人源化抗體或其抗原結合片段,其包含具有以下胺基酸序列之重鏈:QVQLVQSGAEVVKPGASVKISCKASGYTFTGYFMNWVKQSPGQSLEWIGRIHPYDGDTFYNQKFQGKATLTVDKSSNTAHMELLSLTSEDFAVYYCTRYDGSRAMDYWGQGTTVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLCLSPG (SEQ ID NO: 11)。
在其他實施例中,抗葉酸受體抗體係特異性結合人類葉酸受體1之人源化抗體或其抗原結合片段,其包含具有以下胺基酸序列之輕鏈:DIVLTQSPLSLAVSLGQPAIISCKASQSVSFAGTSLMHWYHQKPGQQPRLLIYRASNLEAGVPDRFSGSGSKTDFTLNISPVEAEDAATYYCQQSREYPYTFGGGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(SEQ ID NO: 12);或DIVLTQSPLSLAVSLGQPAIISCKASQSVSFAGTSLMHWYHQKPGQQPRLLIYRASNLEAGVPDRFSGSGSKTDFTLTISPVEAEDAATYYCQQSREYPYTFGGGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(SEQ ID NO: 13)。
在其他實施例中,抗葉酸受體抗體為特異性結合至人類葉酸受體1之人源化抗體或其抗原結合片段,其包含具有胺基酸序列SEQ ID NO: 11之重鏈及具有胺基酸序列SEQ ID NO: 12或SEQ ID NO: 13之輕鏈。較佳的是,該抗體包含具有胺基酸序列SEQ ID NO: 11之重鏈及具有胺基酸序列SEQ ID NO: 13之輕鏈(huMov19)。
在其他實施例中,抗葉酸受體抗體為人源化抗體或其抗原結合片段,其包含經工程改造Cys殘基(例如,C442)及與以下序列具有至少約90%、95%、99%、或100%一致性之重鏈可變域:QVQLVQSGAEVVKPGASVKISCKASGYTFTGYFMNWVKQSPGQSLEWIGRIHPYDGDTFYNQKFQGKATLTVDKSSNTAHMELLSLTSEDFAVYYCTRYDGSRAMDYWGQGTTVTVSS (SEQ ID NO: 14),及與以下序列具有至少約90%、95%、99%、或100%一致性之輕鏈可變域:DIVLTQSPLSLAVSLGQPAIISCKASQSVSFAGTSLMHWYHQKPGQQPRLLIYRASNLEAGVPDRFSGSGSKTDFTLNISPVEAEDAATYYCQQSREYPYTFGGGTKLEIKR (SEQ ID NO: 15);或DIVLTQSPLSLAVSLGQPAIISCKASQSVSFAGTSLMHWYHQKPGQQPRLLIYRASNLEAGVPDRFSGSGSKTDFTLTISPVEAEDAATYYCQQSREYPYTFGGGTKLEIKR (SEQ ID NO: 16)。
在具體實施例中,人源化抗體係huMy9-6或另一相關抗體,其描述於美國專利第7,342,110號及第7,557,189號中。在另一具體實施例中,人源化抗體係美國專利第8,577,966號中所述之抗葉酸受體抗體(例如,huMov19)。在某些實施例中,人源化抗體係美國專利第8,765,917號中所述之抗CD37抗體(例如,抗CD37-3)。在某些實施例中,人源化抗體係美國專利第8,790,649號中所述之抗EGFR抗體。在其他實施例中,抗體係抗EGFR抗體。在一些實施例中,抗EGFR抗體係非拮抗劑抗體,其包括例如WO2012058592中所述之抗體,該案以引用方式併入本文。在其他實施例中,抗EGFR抗體係非功能性抗體,例如,人源化ML66。更具體而言,抗EGFR抗體係huML66。
在一些實施例中,該抗體係抗CD123抗體,諸如2016年6月28日提交標題為「ANTI-CD123 ANTIBODIES AND CONJUGATES AND DERIVATIVES THEREOF」之美國申請案第15/195,401號(其全部內容包括所有序列及圖式均併入本文)中所述之人源化huCD123抗體。在具體實施例中,抗CD123抗體或其抗原結合片段包含:a)至少一個重鏈可變區或其片段,其分別包含三個順序互補決定區(CDR) CDR1、CDR2、及CDR3,其中,CDR1具有序列SSIMH (SEQ ID NO:17),CDR2具有序列YIKPYNDGTKYNEKFKG (SEQ ID NO:18),且,CDR3具有序列EGGNDYYDTMDY (SEQ ID NO:19);以及b)至少一個輕鏈可變區或其片段,其分別包含三個順序互補決定區(CDR) CDR1、CDR2、及CDR3,其中,CDR1具有序列RASQDINSYLS (SEQ ID NO:20),CDR2具有序列RVNRLVD (SEQ ID NO:21),且,CDR3具有序列LQYDAFPYT (SEQ ID NO:22)。
在另一具體實施例中,抗CD123抗體或其抗原結合片段包含經工程改造Cys殘基(
例如,C442);與以下序列具有至少約90%、95%、99%、或100%一致性之免疫球蛋白重鏈可變域:QXQLVQSGAEVKKPGASVKVSCKASGYIFTSSIMHWVRQAPGQGLEWIGYIKPYNDGTKYNEKFKGRATLTSDRSTSTAYMELSSLRSEDTAVYYCAREGGNDYYDTMDYWGQGTLVTVSS (SEQ ID NO:23);及與以下序列具有至少約90%、95%、99%、或100%一致性之免疫球蛋白輕鏈可變區:DIQMTQSPSSLSASVGDRVTITCRASQDINSYLSWFQQKPGKAPKTLIYRVNRLVDGVPSRFSGSGSGNDYTLTISSLQPEDFATYYCLQYDAFPYTFGQGTKVEIKR (SEQ ID NO:24)。在某些實施例中,Xaa (SEQ ID NO: 23之N末端之第二殘基)係Phe。在其他實施例中,Xaa係Val。
在某些實施例中,抗CD123抗體或其抗原結合片段可包含:具有以下胺基酸序列之免疫球蛋白重鏈區:QVQLVQSGAEVKKPGASVKVSCKASGYIFTSSIMHWVRQAPGQGLEWIGYIKPYNDGTKYNEKFKGRATLTSDRSTSTAYMELSSLRSEDTAVYYCAREGGNDYYDTMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLCLSPG (SEQ ID NO:25);
及具有以下胺基酸序列之免疫球蛋白輕鏈區:DIQMTQSPSSLSASVGDRVTITCRASQDINSYLSWFQQKPGKAPKTLIYRVNRLVDGVPSRFSGSGSGNDYTLTISSLQPEDFATYYCLQYDAFPYTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID NO:26)。
組成物及使用方法
本發明亦包括藉由本發明之任何方法製備之細胞結合劑-細胞毒性劑結合物、包含藉由本發明之任何方法製備之細胞結合劑-細胞毒性劑結合物及載劑(醫藥學上可接受之載劑)之組成物(
例如,醫藥組成物)。本發明結合物及組成物可用於在哺乳動物(
例如,人類)中抑制異常細胞生長或治療增生性病症。本發明包括一種在哺乳動物(
例如,人類)中抑制異常細胞生長或治療增生性病症之方法,其包含單獨或與第二治療劑組合向該哺乳動物投予治療有效量藉由上文所述之本發明方法製備之結合物或其組成物。
在一些實施例中,增生性病症為癌症。癌症可包括血癌或實體腫瘤。更具體而言,癌症係白血病(例如,急性骨髓性白血病(AML)、急性淋巴母細胞白血病(ALL)諸如急性B淋巴母細胞白血病(B-ALL)、慢性骨髓性白血病(CML)、慢性淋巴球性白血病(CLL))或淋巴瘤、黑色素瘤、肺癌(
例如,非小細胞肺癌)、卵巢癌、子宮內膜癌、腹膜癌、胰腺癌、乳癌、前列腺癌、及子宮頸癌。
本發明亦提供治療方法,其包括對有需要之受試者投予有效量之上述任一連結物。
類似地,本發明提供一種用於在經選擇細胞群體中誘導細胞死亡之方法,其包含將靶細胞或含有靶細胞之組織與有效量包含上文所述之任一結合物之細胞毒性劑接觸。靶細胞為細胞結合劑可結合之細胞。
需要時,其他活性劑,諸如其他抗腫瘤劑,可與該結合物一起投予。
合適之醫藥學上可接受之載劑、稀釋劑、及賦形劑為熟知的且可由一般熟習此項技術者依據臨床狀況許可確定。合適之載劑、稀釋劑、及/或賦形劑之實例包括:(1)杜貝卡氏磷酸鹽緩衝鹽水(Dulbecco's phosphate buffered saline),pH為約7.4,含有或不含約1 mg/mL至25 mg/mL人類血清白蛋白;(2) 0.9%鹽水(0.9% w/v NaCl);及(3) 5% (w/v)右旋糖;且亦可含有抗氧化劑諸如色胺、及穩定劑諸如Tween 20。
實例
實例1. 含亞胺細胞毒性劑之製備
以下溶劑、試劑、保護基、部分、及其他指定可藉由其括號中之縮寫來提及:
A.
合成 N1-(2-(2,5- 二側氧基 -2,5- 二氫 -1H- 吡咯 -1- 基 ) 乙基 )-N6-((S)-1-(((S)-1-((3-((((S)-8- 甲氧基 -6- 側氧基 -11,12,12a,13- 四氫 -6H- 苯并 [ 5,6][1,4] 二氮平并 [ 1,2-a] 吲哚 -9- 基 ) 氧基 ) 甲基 )-5-((((S)-8- 甲氧基 -6- 側氧基 -12a,13- 二氫 -6H- 苯并 [ 5,6][1,4] 二氮平并 [ 1,2-a] 吲哚 -9- 基 ) 氧基 ) 甲基 ) 苯基 ) 胺基 )-1- 側氧基丙 -2- 基 ) 胺基 )-1- 側氧基丙 -2- 基 ) 己二醯胺,化合物 D1
| Me | 甲基 | Et | 乙基 | Pr | 丙基 |
| i -Pr | 異丙基 | Bu | 丁基 | t -Bu | 第三丁基 |
| Ph | 苯基 | Ac | 乙醯基 | AcOH/HOAc | 乙酸 |
| Ala | 丙胺酸 | aq | 水性 | ACN/CH 3CN | 乙腈 |
| DI 水 | 去離子水 | DCM/CH 2Cl 2 | 二氯甲烷 | Boc/BOC | 第三丁氧基羰基 |
| g | 公克 | DMA | N,N-二甲基乙醯胺 | DIEA 或 DIPEA | N,N-二異丙基乙胺 |
| h | 小時 | DMF | N,N-二甲基甲醯胺 | EDC | 1-乙基-3-(3-二甲基胺基丙基)碳二亞胺 |
| min | 分鐘 | EtOAc | 乙酸乙酯 | ESI 或 ES | 電灑離子化 |
| mg | 毫克 | LC | 液相層析 | HPLC | 高效液相層析 |
| mL | 毫升 | mmol | 毫莫耳 | LCMS | 液相層析質譜 |
| µg | 微克 | µmol | 微莫耳 | MS | 質譜 |
| µL | 微升 | MeOH | 甲醇 | NHS | N-羥基琥珀醯胺 |
| sat 或 sat'd | 飽和 | RT 或 rt | 室溫(周圍,約25℃) | NMR | 核磁共振光譜法 |
| THF | 四氫呋喃 | TEA | 三乙胺(Et 3N) | RPHPLC 或 RP-HPLC | 逆相高效液相層析 |
在室溫下將NHS酯
1a(8.2 mg, 7.6 µmol) (根據US-2016/0082114中所述之程序製備,該案以引用方式併入本文)及1-(2-胺基乙基)-1H-吡咯-2,5-二酮鹽酸鹽(2.2 mg, 0.011 mmol)溶解於無水二氯甲烷(305µL)中。添加DIPEA (2.66µL, 0.015mmol),且將反應攪拌3.5小時。將反應混合物濃縮,且藉由RPHPLC (C18管柱, CH
3CN/H
2O, 梯度, 35%至55%)純化。將所需產物流份冷凍且凍乾以得到呈固體白色粉末之順丁烯二醯亞胺,化合物
D1(5.3 mg, 58%產率)。LCMS = 5.11 min (8 min方法)。MS (m/z): 1100.6 (M + 1)
+。
B. 合成 N-(2-(2,5- 二側氧基 -2,5- 二氫 -1H- 吡咯 -1- 基 ) 乙基 )-11-(3-((((S)-8- 甲氧基 -6- 側氧基 -11,12,12a,13- 四氫 -6H- 苯并 [5,6][1,4] 二氮平并 [1,2-a] 吲哚 -9- 基 ) 氧基 ) 甲基 )-5-((((S)-8- 甲氧基 -6- 側氧基 -12a,13- 二氫 -6H- 苯并 [5,6][1,4] 二氮平并 [1,2-a] 吲哚 -9- 基 ) 氧基 ) 甲基 ) 苯基 )-13,13- 二甲基 -2,5,8- 三噁 -14,15- 二噻 -11- 氮雜十九烷 -19- 醯胺,化合物 D2
向於無水二氯甲烷(0.5 mL)中之游離硫醇
2a(40 mg, 0.042 mmol)及NHS 4-(2-吡啶基二硫)丁烷(35 mg, 80%純, 0.085 mmol)中添加無水二異丙基乙胺(0.015 mL, 0.085 mmol)並在室溫下攪拌16小時。將反應混合物用飽和氯化銨淬滅並用二氯甲烷稀釋。將獲得之混合物於分液漏斗中分離。將有機層用鹽水洗滌,經無水硫酸鈉乾燥,過濾,且在減壓下汽提。將殘餘物藉由半製備型逆相HPLC (C18管柱, CH
3CN/H
2O)純化。將含有純產物之流份組合,冷凍,且凍乾以得到所需NHS酯,
2b(29.7 mg, 60%產率)。LCMS = 9.1 min (15 min方法)。MS (m/z): 1157.3 (M + 1)
+。
向於無水二氯甲烷(0.3 mL)中之NHS酯,
2b(12.3 mg, 0.011 mmol)及N-(2-胺基乙基)順丁烯二醯亞胺鹽酸鹽(2.0 mg, 0.011 mmol)中添加DIPEA (0.0022 mL, 0.013 mmol)。將混合物在室溫下攪拌3小時,然後將其在減壓下汽提。將殘餘物藉由半製備型逆相HPLC (C18管柱, CH
3CN/H
2O)純化。將含有純產物之流份組合,冷凍,且凍乾以得到所需順丁烯二醯亞胺,化合物
D2(10 mg, 80%產率)。LCMS = 8.3 min (15 min方法)。MS (m/z): 1181.8 (M + 1)
+。
C.
合成 1-((2-(2,5- 二側氧基 -2,5- 二氫 -1H- 吡咯 -1- 基 ) 乙基 ) 胺基 )-4-((5-((3-((((S)-8- 甲氧基 -6- 側氧基 -11,12,12a,13- 四氫 -6H- 苯并 [ 5,6][1,4] 二氮平并 [ 1,2-a] 吲哚 -9- 基 ) 氧基 ) 甲基 )-5-((((S)-8- 甲氧基 -6- 側氧基 -12a,13- 二氫 -6H- 苯并 [ 5,6][1,4] 二氮平并 [ 1,2-a] 吲哚 -9- 基 ) 氧基 ) 甲基 ) 苯基 ) 胺基 )-2- 甲基 -5- 側氧基戊 -2- 基 ) 二磺醯基 )-1- 側氧基丁 -2- 磺酸,化合物 D3
在氮氣、室溫下向游離硫醇,
3a(88 mg, 0.105 mmol)及1-((2,5-二側氧基吡咯啶-1-基)氧基)-1-側氧基-4-(吡啶-2-基二磺醯基)丁-2-磺酸(64.0 mg, 0.158 mmol)於無水二氯甲烷(2.10 mL)中之懸浮液中添加DIPEA (55.0 µL, 0.315 mmol)。將混合物攪拌16小時,然後添加1-(2-胺基乙基)-1H-吡咯-2,5-二酮鹽酸鹽(55.6 mg, 0.315 mmol)、無水二氯甲烷(1.0 mL)、及DIPEA (0.055 mL, 0.315 mmol)。在室溫下再將混合物攪拌5小時,之後將反應真空濃縮。將所得殘餘物藉由RP-HPLC (C18, CH
3CN/H
2O)純化。將含有所需產物之流份冷凍並凍乾以得到呈白色固體之順丁烯二醯亞胺,化合物
D3(20 mg, 16%產率)。LCMS = 4.92 min (8 min方法)。MS (m/z): 1158.6 (M + 1)
+。
D.
合成 N-(2-(2,5- 二側氧基 -2,5- 二氫 -1H- 吡咯 -1- 基 ) 乙基 )-11-(3-((((S)-8- 甲氧基 -6- 側氧基 -11,12,12a,13- 四氫 -6H- 苯并 [ 5,6][1,4] 二氮平并 [ 1,2-a] 吲哚 -9- 基 ) 氧基 ) 甲基 )-5-((((S)-8- 甲氧基 -6- 側氧基 -12a,13- 二氫 -6H- 苯并 [ 5,6][1,4] 二氮平并 [ 1,2-a] 吲哚 -9- 基 ) 氧基 ) 甲基 ) 苯基 )-2,5,8- 三噁 -11- 氮雜十五烷 -15- 醯胺,化合物 D4
在氮氣下向於無水二氯甲烷(200 µL)中之NHS酯,
4a(5 mg, 4.82 µmol)及1-(2-胺基乙基)-1H-吡咯-2,5-二酮鹽酸鹽(1.7 mg, 9.64 µmol)中添加DIPEA (1.512 µL, 8.68 µmol)。在室溫下將混合物攪拌4小時,然後真空濃縮。將所得殘餘物藉由RP-HPLC (C18, CH
3CN/H
2O)純化。將含有所需產物之流份冷凍並凍乾以得到順丁烯二醯亞胺,化合物
D4(3.5 mg, 68%產率)。LCMS = 4.61 min (15 min方法)。MS (m/z): 1062.8 (M + 1)
+。
實例 2. 帶有順丁烯二醯亞胺基團之含亞胺細胞毒性劑之選擇性磺化
向50 mM琥珀酸鈉pH 3.3 (116.5 mL)及DMA (98.5 mL)之混合物中添加溶解於21.4 mL DMA中之
D1(263.6 mg)。隨後,將3.4 mL含有1 v/v% DMA於水中之100 mM亞硫酸氫鈉溶液(1.4當量)引入至反應中。使均質混合物在25℃下反應2 h,此時藉由UPLC-MS分析反應之完整性。該反應混合物合適用於在不進一步純化之情況下結合。如圖1中所示,反應混合物之UPLC-MS分析顯示92.5%亞胺-磺基D1、1.9%未反應D1、0.8%順丁烯二醯亞胺-磺基D1、及4.8%二磺基D1。亞胺-磺基D1 (C
60H
62N
9O
15S
-)之ESI-MS負離子模式[M-H]
-計算值: 1180.41;實驗值: 1180.03。
實例 3. 亞硫酸氫鈉對選擇性磺化之影響
如
表 1中指出,以下列順序向所需體積的50 mM琥珀酸鈉pH 3.3緩衝液中添加以下試劑:DMA (38.8 uL)、所需體積的含有1 v/v% DMA之20或40 mM水性亞硫酸氫鈉儲備液、及8.9 mM
D1的DMA溶液(11.2 uL)。使按體積計含有50% DMA之所得反應混合物在25℃下反應20 h。藉由UPLC-MS分析反應產物。觀察之二磺基D1、順丁烯二醯亞胺-磺基D1、亞胺-磺基D1、及未磺化D1產物之相對豐度示出於
表 1中。
表 1
實例 4.pH 對磺化之影響
| 琥珀酸鈉緩衝液(uL) | 亞硫酸氫鈉儲備液 | D1反應產物(%) | |||||||
| 反應 | 總當量 | 儲備液濃度(mM) | 添加之體積(uL) | 二磺基 | 順丁烯二醯亞胺-磺基 | 亞胺-磺基 | 未磺化 | 剩餘之總反應性順丁烯二醯亞胺 | |
| 1 | 46 | 0.8 | 20 | 4 | 0.6 | 1.4 | 35.9 | 62.1 | 98.0 |
| 2 | 45 | 1.0 | 20 | 5 | 1.1 | 1.4 | 53.4 | 44.2 | 97.6 |
| 3 | 44 | 1.2 | 20 | 6 | 2.0 | 1.2 | 69.6 | 27.2 | 96.8 |
| 4 | 43 | 1.4 | 20 | 7 | 2.6 | 1.1 | 79.1 | 17.2 | 96.3 |
| 5 | 42 | 1.6 | 20 | 8 | 5.0 | 1.1 | 85.7 | 8.2 | 93.9 |
| 6 | 41 | 1.8 | 20 | 9 | 8.3 | 1.2 | 84.6 | 5.9 | 90.5 |
| 7 | 45 | 2.0 | 40 | 5 | 8.7 | 0.8 | 88.2 | 2.3 | 90.5 |
| 8 | 44 | 2.4 | 40 | 6 | 13.0 | 0.9 | 83.9 | 2.2 | 86.1 |
| 9 | 43 | 2.8 | 40 | 7 | 16.4 | 1.1 | 79.8 | 2.7 | 82.5 |
| 10 | 42 | 3.2 | 40 | 8 | 19.8 | 1.5 | 75.8 | 2.9 | 78.7 |
| 11 | 41 | 3.6 | 40 | 9 | 22.9 | 1.8 | 71.9 | 3.4 | 75.3 |
如
表 2中詳述,以下列順序向44.0 uL具有所指示之pH之50 mM琥珀酸鈉緩衝液中添加以下試劑:20 mM含有1% v/v DMA之水性亞硫酸氫鈉儲備液(6.0 uL)、DMA (38.8 uL)、及8.9 mM D1的DMA溶液(11.2 uL)。使按體積計含有50% DMA之所得反應混合物在25℃下反應4 h。藉由UPLC-MS分析反應產物。觀察之二磺基、順丁烯二醯亞胺-磺基、亞胺-磺基、及未磺化D1產物之相對豐度示出於
表 2中。
表 2.
實例 5. 具有或不具有緩衝液之選擇性磺化
| 琥珀酸鈉緩衝液pH | 亞硫酸氫鈉(總當量) | DGN549-C反應產物(%) | |||||
| 反應 | 二磺基 | 順丁烯二醯亞胺-磺基 | 亞胺-磺基 | 未磺化 | 剩餘之總反應性順丁烯二醯亞胺 | ||
| 1 | 2.9 | 1.2 | 0.7 | 1.0 | 68.5 | 29.8 | 98.3 |
| 2 | 3.1 | 1.2 | 0.8 | 1.3 | 65.0 | 33.0 | 97.9 |
| 3 | 3.3 | 1.2 | 1.1 | 1.7 | 66.9 | 30.3 | 97.1 |
| 4 | 3.4 | 1.2 | 1.3 | 1.4 | 66.5 | 30.7 | 97.3 |
| 5 | 3.7 | 1.2 | 2.3 | 2.7 | 65.6 | 29.4 | 94.9 |
如
表 3中詳述,向21.6 uL DMA中添加22.0 uL 水或具有所指示之pH之50 mM琥珀酸鈉緩衝液、含有1 v/v% DMA之20 mM水性亞硫酸氫鈉儲備液(3.0 uL)、及14.5 mM D1的DMA溶液(3.4 uL)。使按體積計含有50% DMA之所得反應混合物在25℃下反應6 h。藉由UPLC-MS分析反應產物。觀察之二磺基、順丁烯二醯亞胺-磺基、亞胺-磺基、及未磺化D1產物之相對豐度示出於
表 3中。
表 3.
| 琥珀酸鈉緩衝液pH | 亞硫酸氫鈉(總當量) | D1反應產物(%) | |||||
| 反應 | 二磺基 | 順丁烯二醯亞胺-磺基 | 亞胺-磺基 | 未磺化 | 剩餘之總反應性順丁烯二醯亞胺 | ||
| 1 | 3.5 | 1.2 | 0.8 | 0.5 | 86.9 | 11.8 | 98.7 |
| 2 | 4.0 | 1.2 | 4.8 | 2.9 | 70.0 | 22.8 | 92.8 |
| 3 | 僅水 | 1.2 | 2.8 | 1.8 | 75.8 | 19.6 | 95.4 |
類似地,如
表 4中詳述,向47.6 uL DMA中添加55.6 uL水或pH 4.75 50 mM琥珀酸鈉緩衝液、含有1 v/v% DMA之20 mM水性亞硫酸氫鈉儲備液(6.9 uL)、及8.4 mM D1的DMA溶液(14.9 uL)。使按體積計含有50% DMA之所得反應混合物在25℃下反應24 h。藉由UPLC-MS分析反應產物(參見圖2)。觀察之二磺基、順丁烯二醯亞胺-磺基、亞胺-磺基、及未磺化DGN549-C產物之相對豐度指示於
表 4中。
表 4.
| 琥珀酸鈉緩衝液pH | 亞硫酸氫鈉(總當量) | D1反應產物(%) | |||||
| 反應 | 二磺基 | 順丁烯二醯亞胺-磺基 | 亞胺-磺基 | 未磺化 | 剩餘之總反應性順丁烯二醯亞胺 | ||
| 1 | 4.75 | 1.1 | 9.8 | 40.7 | 13.4 | 36.1 | 49.5 |
| 3 | 僅水 | 1.1 | 1.5 | 0.9 | 73.8 | 23.8 | 97.6 |
在另一實驗中,如
表 5中詳述,向24.6 uL DMA中添加指示體積之水、指示體積之20 mM水性亞硫酸氫鈉儲備液。此等溶液之pH指示於
表 5中。向此等混合物中添加於11.2 mM D1的DMA溶液(5.4 uL)。使按體積計含有50% DMA之所得反應混合物在25℃下反應1至2 h。藉由UPLC-MS分析反應產物。觀察之二磺基、順丁烯二醯亞胺-磺基、亞胺-磺基、及未磺化D1產物之相對豐度指示於
表 5中。
表 5
「-」意指未藉由UPLC觀察到。
實例 6. 抗體 - 細胞毒性劑結合物之製備
| 水(uL) | 亞硫酸氫鈉儲備液 | 觀察之反應pH | DGN549-C反應產物(%) | |||||||
| 反應 | 總當量 | 儲備液濃度(mM) | 添加之體積(uL) | 二磺基 | 順丁烯二醯亞胺-磺基 | 亞胺-磺基 | 未磺化 | 剩餘之總反應性順丁烯二醯亞胺 | ||
| 1 | 21.0 | 3.0 | 20 | 9.0 | 4.2 | 6.9 | - | 90.9 | 2.2 | 93.1 |
| 2 | 15.0 | 5.0 | 20 | 15.0 | 4.2 | 20.5 | - | 78.0 | 1.5 | 79.5 |
隨後將根據實例2製備之磺化反應混合物(240 mL, 3.5當量)引入至50 mM磷酸鈉pH 6.0溶液,該溶液含有10 g具有經還原C442工程改造半胱胺酸殘基之抗CD123抗體。在2 mg/mL抗體及15 v/v% DMA之最終濃度下,使結合反應在25℃下進行18 h。反應產物之SEC分析得到DAR (藥物與抗體比率)為1.9且%HMW (高分子量物質之百分比)為4.4%對比3.7% (在結合之前)的ADC。
亦根據上文所述之類似程序製備具有兩種具有經還原C442工程改造半胱胺酸殘基之其他人源化單株抗體之結合物。
實例 7.
帶有順丁烯二醯亞胺基團之含亞胺 PBD 二聚物之選擇性磺化
以下列順序向21.2 µL 50 mM琥珀酸鈉pH 3.3緩衝劑中添加:20 µL DMA、3.8 µL 20 mM亞硫酸氫鈉水性儲備液及5.0 µL 10.0 mM塔立林之DMA溶液。就塔立林而言,此對應於1.5當量亞硫酸氫鹽。使按體積計含有50% DMA之所得反應混合物在25℃下反應4 h。藉由UPLC-MS分析反應產物。觀察到之亞胺二磺基、總亞胺單磺基、未磺化及總順丁烯二醯亞胺-磺基產物之相對豐度係如表
6中所指示進行確定。ESI-MS:塔立林之計算值(C
60H
65N
8O
12 +) [M+H]
+1089.4716,實驗值1089.4716;亞胺單磺化塔立林之計算值(C
60H
65N
8O
15S
-) [M-H]
-1169.4296,實驗值1169.4345;亞胺二磺化塔立林之計算值(C
60H
67N
8O
18S
2 -) [M-H]
-1251.4020,實驗值1251.4053。最終反應混合物之代表性層析圖(在330 nm下之吸光度)顯示於圖3中。經識別之反應產物之結構係
表 6.
實例 8. 帶有順丁烯二醯亞胺基團之含亞胺 IGN 二聚物之選擇性磺化
| 琥珀酸鈉緩衝液(uL) | 亞硫酸氫鈉儲備液 | 塔立林反應產物(%) | |||||||
| 反應 | 總當量 (相對於酬載(payload)) | 儲備液濃度(mM) | 添加之體積(uL) | 亞胺二磺基 | 總亞胺單磺基 | 總順丁烯二醯亞胺-磺基物種 | 未磺化 | 剩餘之總反應性順丁烯二醯亞胺 | |
| 塔立林 | 21.2 | 1.5 | 20 | 3.8 | 57.3 | 39.0 | <1 | 3.7 | >99.0 |
如
表 7中指出,以下列順序向所需體積的50 mM琥珀酸鈉pH 3.3緩衝液中添加:DMA (21.2 uL)、所需體積20 mM亞硫酸氫鈉水性儲備液及13.2 mM D5的DMA溶液(3.8 uL)。使按體積計含有50% DMA之所得反應混合物在25℃下反應4 h。藉由UPLC-MS分析反應產物。觀察到之亞胺二磺基、亞胺單磺基、未磺化及總順丁烯二醯亞胺-磺化產物之相對豐度係如表
7中所指示進行確定。ESI-MS:D5之計算值(C
60H
60N
9O
12 +) [M+H]
+1098.4356,實驗值1098.4351;亞胺單磺化D5之計算值(C
60H
60N
9O
15S
-) [M-H]
-1178.3935,實驗值1178.4006;亞胺二磺化D5之計算值(C
60H
62N
9O
18S
2 -) [M-H]
-1260.3660,實驗值1260.3704;亞胺二磺化順丁烯二醯亞胺磺化D5之計算值(C
60H
64N
9O
21S
3 -) [M-2H]
2-z=2 670.6653,實驗值670.6693。以2.0及2.5當量亞硫酸氫鹽之最終反應混合物之代表性層析圖(在330 nm下之吸光度)顯示於圖4A及4B中。經識別之反應產物之結構顯示如下。
表 7
| 琥珀酸鈉緩衝液(uL) | 亞硫酸氫鈉儲備液 | IGN148-mal反應產物(%) | |||||||
| 反應 | 總當量 (相對於酬載) | 儲備液濃度(mM) | 添加之體積(uL) | 亞胺二磺基 | 亞胺單磺基 | 總順丁烯二醯亞胺-磺基物種 | 未磺化 | 剩餘之總反應性順丁烯二醯亞胺 | |
| 1 | 21.2 | 1.5 | 20 | 3.8 | 41.9 | 46.9 | 1.4 | 9.7 | 98.6 |
| 2 | 20.0 | 2.0 | 20 | 5.0 | 76.0 | 20.3 | 1.9 | 1.8 | 98.1 |
| 3 | 18.7 | 2.5 | 20 | 6.3 | 83.3 | 6.7 | 10.0 | - | 90.0 |
圖1顯示含亞胺細胞毒性劑D1與亞硫酸氫鈉之反應混合物在pH 3.3下的UPLC層析圖。
圖2顯示含亞胺細胞毒性劑D1與亞硫酸氫鈉之反應混合物在pH 4.75下的UPLC層析圖。
圖3顯示含PBD亞胺細胞毒性劑塔立林(talirine)與亞硫酸氫鈉之反應混合物的UPLC層析圖。
圖4A及4B顯示含亞胺細胞毒性劑D5與2.0 (圖4A)或2.5 (圖4B)當量亞硫酸氫鈉之反應混合物的UPLC層析圖。
<![CDATA[<110> 美商伊繆諾金公司(IMMUNOGEN, INC.)]]>
<![CDATA[<120> 苯二氮平衍生物之選擇性磺化]]>
<![CDATA[<130> 128037-03863]]>
<![CDATA[<140> TW 106140599]]>
<![CDATA[<141> 2017-11-22]]>
<![CDATA[<150> 62/425,761]]>
<![CDATA[<151> 2016-11-23]]>
<![CDATA[<160> 27 ]]>
<![CDATA[<170> PatentIn version 3.5]]>
<![CDATA[<210> 1]]>
<![CDATA[<211> 4]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 1]]>
Ala Leu Ala Leu
1
<![CDATA[<210> 2]]>
<![CDATA[<211> 4]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<220>]]>
<![CDATA[<221> MOD_RES]]>
<![CDATA[<222> (1)..(1)]]>
<![CDATA[<223> β-Ala]]>
<![CDATA[<400> 2]]>
Xaa Leu Ala Leu
1
<![CDATA[<210> 3]]>
<![CDATA[<211> 4]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 3]]>
Gly Phe Leu Gly
1
<![CDATA[<210> 4]]>
<![CDATA[<211> 5]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 4]]>
Gly Tyr Phe Met Asn
1 5
<![CDATA[<210> 5]]>
<![CDATA[<211> 23]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<220>]]>
<![CDATA[<221> MOD_RES]]>
<![CDATA[<222> (14)..(14)]]>
<![CDATA[<223> Lys, Gln, His 或 Arg]]>
<![CDATA[<220>]]>
<![CDATA[<221> MOD_RES]]>
<![CDATA[<222> (18)..(18)]]>
<![CDATA[<223> Gln, His, Asn 或 Arg]]>
<![CDATA[<220>]]>
<![CDATA[<221> MOD_RES]]>
<![CDATA[<222> (21)..(21)]]>
<![CDATA[<223> Gly, Glu, Thr, Ser, Ala 或 Val]]>
<![CDATA[<400> 5]]>
Arg Ile His Pro Tyr Asp Gly Asp Thr Phe Tyr Asn Gln Xaa Ala Ala
1 5 10 15
Phe Xaa Ala Ala Xaa Ala Ala
20
<![CDATA[<210> 6]]>
<![CDATA[<211> 9]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 6]]>
Tyr Asp Gly Ser Arg Ala Met Asp Tyr
1 5
<![CDATA[<210> 7]]>
<![CDATA[<211> 15]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 7]]>
Lys Ala Ser Gln Ser Val Ser Phe Ala Gly Thr Ser Leu Met His
1 5 10 15
<![CDATA[<210> 8]]>
<![CDATA[<211> 7]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 8]]>
Arg Ala Ser Asn Leu Glu Ala
1 5
<![CDATA[<210> 9]]>
<![CDATA[<211> 9]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 9]]>
Gln Gln Ser Arg Glu Tyr Pro Tyr Thr
1 5
<![CDATA[<210> 10]]>
<![CDATA[<211> 17]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 10]]>
Arg Ile His Pro Tyr Asp Gly Asp Thr Phe Tyr Asn Gln Lys Phe Gln
1 5 10 15
Gly
<![CDATA[<210> 11]]>
<![CDATA[<211> 447]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 11]]>
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Phe Met Asn Trp Val Lys Gln Ser Pro Gly Gln Ser Leu Glu Trp Ile
35 40 45
Gly Arg Ile His Pro Tyr Asp Gly Asp Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr Ala His
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Phe Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Tyr Asp Gly Ser Arg Ala Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Cys Leu Ser Pro Gly
435 440 445
<![CDATA[<210> 12]]>
<![CDATA[<211> 218]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 12]]>
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Pro Ala Ile Ile Ser Cys Lys Ala Ser Gln Ser Val Ser Phe Ala
20 25 30
Gly Thr Ser Leu Met His Trp Tyr His Gln Lys Pro Gly Gln Gln Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ala Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Lys Thr Asp Phe Thr Leu Asn Ile Ser
65 70 75 80
Pro Val Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<![CDATA[<210> 13]]>
<![CDATA[<211> 218]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 13]]>
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Pro Ala Ile Ile Ser Cys Lys Ala Ser Gln Ser Val Ser Phe Ala
20 25 30
Gly Thr Ser Leu Met His Trp Tyr His Gln Lys Pro Gly Gln Gln Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ala Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Lys Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Pro Val Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<![CDATA[<210> 14]]>
<![CDATA[<211> 118]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 14]]>
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Phe Met Asn Trp Val Lys Gln Ser Pro Gly Gln Ser Leu Glu Trp Ile
35 40 45
Gly Arg Ile His Pro Tyr Asp Gly Asp Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr Ala His
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Phe Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Tyr Asp Gly Ser Arg Ala Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<![CDATA[<210> 15]]>
<![CDATA[<211> 112]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 15]]>
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Pro Ala Ile Ile Ser Cys Lys Ala Ser Gln Ser Val Ser Phe Ala
20 25 30
Gly Thr Ser Leu Met His Trp Tyr His Gln Lys Pro Gly Gln Gln Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ala Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Lys Thr Asp Phe Thr Leu Asn Ile Ser
65 70 75 80
Pro Val Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
<![CDATA[<210> 16]]>
<![CDATA[<211> 112]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 16]]>
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Pro Ala Ile Ile Ser Cys Lys Ala Ser Gln Ser Val Ser Phe Ala
20 25 30
Gly Thr Ser Leu Met His Trp Tyr His Gln Lys Pro Gly Gln Gln Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ala Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Lys Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Pro Val Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Arg
85 90 95
Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
<![CDATA[<210> 17]]>
<![CDATA[<211> 5]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 17]]>
Ser Ser Ile Met His
1 5
<![CDATA[<210> 18]]>
<![CDATA[<211> 17]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 18]]>
Tyr Ile Lys Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<![CDATA[<210> 19]]>
<![CDATA[<211> 12]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 19]]>
Glu Gly Gly Asn Asp Tyr Tyr Asp Thr Met Asp Tyr
1 5 10
<![CDATA[<210> 20]]>
<![CDATA[<211> 11]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 20]]>
Arg Ala Ser Gln Asp Ile Asn Ser Tyr Leu Ser
1 5 10
<![CDATA[<210> 21]]>
<![CDATA[<211> 7]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 21]]>
Arg Val Asn Arg Leu Val Asp
1 5
<![CDATA[<210> 22]]>
<![CDATA[<211> 9]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 22]]>
Leu Gln Tyr Asp Ala Phe Pro Tyr Thr
1 5
<![CDATA[<210> 23]]>
<![CDATA[<211> 121]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<220>]]>
<![CDATA[<221> MOD_RES]]>
<![CDATA[<222> (2)..(2)]]>
<![CDATA[<223> 任何胺基酸]]>
<![CDATA[<400> 23]]>
Gln Xaa Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ser Ser
20 25 30
Ile Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Ser Asp Arg Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly Asn Asp Tyr Tyr Asp Thr Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<![CDATA[<210> 24]]>
<![CDATA[<211> 108]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 24]]>
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Val Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Ala Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<![CDATA[<210> 25]]>
<![CDATA[<211> 450]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 25]]>
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ser Ser
20 25 30
Ile Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Ser Asp Arg Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly Asn Asp Tyr Tyr Asp Thr Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Cys Leu Ser
435 440 445
Pro Gly
450
<![CDATA[<210> 26]]>
<![CDATA[<211> 214]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<400> 26]]>
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Val Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Ala Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<![CDATA[<210> 27]]>
<![CDATA[<211> 4]]>
<![CDATA[<212> PRT]]>
<![CDATA[<213> 人工序列]]>
<![CDATA[<220>]]>
<![CDATA[<223> 人工序列之描述:合成肽]]>
<![CDATA[<220>]]>
<![CDATA[<221> MOD_RES]]>
<![CDATA[<222> (1)..(1)]]>
<![CDATA[<223> β-Ala]]>
<![CDATA[<400> 27]]>
Xaa Gly Gly Gly
1
Claims (20)
- 一種製備細胞結合劑-細胞毒性劑結合物之方法,其包含以下步驟:(a)使由下式表示之含亞胺細胞毒性劑或其醫藥學上可接受之鹽中亞胺部分:
- 如請求項1之方法,其中步驟(a)之該反應係在pH 2.9至4.0下進行。
- 如請求項1之方法,其中步驟(a)之該反應係在pH 2.9至3.7下進行。
- 如請求項1之方法,其中步驟(a)之該反應係在pH 3.1至3.5下進行。
- 如請求項1之方法,其中步驟(a)之該反應係在pH 3.2至3.4下進行。
- 如請求項1之方法,其中步驟(a)之該反應係在pH 3.3下進行。
- 如請求項1之方法,其中步驟(a)之該反應係在緩衝溶液之存在下進行。
- 如請求項7之方法,其中該緩衝溶液係檸檬酸鹽緩衝液、乙酸鹽緩衝液、琥珀酸鹽緩衝液、及磷酸鹽緩衝液。
- 一種製備細胞結合劑-細胞毒性劑結合物之方法,其包含以下步驟:(a)使由下式表示之含亞胺細胞毒性劑或其醫藥學上可接受之鹽中亞胺部分:
- 如請求項1之方法,其中(i)使0.5至5當量該亞硫酸氫鹽或0.25至2.5當量該偏亞硫酸氫鹽與1當量該含亞胺細胞毒性劑反應;(ii)使0.8至2.0當量該亞硫酸氫鹽或0.4至1.0當量該偏亞硫酸氫鹽與1當量該含亞胺細胞毒性劑反應;(iii)使1.1至1.6當量該亞硫酸氫鹽或0.55至0.8當量該偏亞硫酸氫鹽與1當量該含亞胺細胞毒性劑反應;或(iv)使1.4當量該亞硫酸氫鹽或0.7當量該偏亞硫酸氫鹽與1當量該含亞胺細胞毒性劑反應。
- 如請求項1之方法,其中步驟(a)之該反應係(i)在pH 2.9至3.7下進行,且使1.0至1.8當量該亞硫酸氫鹽或0.5至0.9當量該偏亞硫酸氫鹽與1當量該含亞胺細胞毒性劑反應;(ii)在pH 3.1至3.5下進行,且使1.1至1.6當量該亞硫酸氫鹽或0.55至0.8當量該偏亞硫酸氫鹽與1當量該含亞胺細胞毒性劑反應;或(iii)在pH 3.3下進行,且使1.4當量該亞硫酸氫鹽或0.7當量該偏亞硫酸氫鹽與1當量該含亞胺細胞毒性劑反應。
- 如請求項1之方法,其中步驟(a)之該反應係於有機溶劑及水之混合物中進行。
- 如請求項12之方法,其中步驟(a)之該反應係於二甲基乙醯胺(DMA)及水之混合物中進行。
- 如請求項1之方法,其中在步驟(a)中,使該含亞胺細胞毒性劑與亞硫酸氫鈉或偏亞硫酸氫鈉反應。
- 如請求項1之方法,其中該經修飾細胞毒性劑在步驟(b)中與該細胞結合劑反應之前係未純化。
- 如請求項1之方法,其中步驟(b)之該反應係在pH 4至9下進行。
- 如請求項1之方法,其中步驟(b)之該反應係在pH 5至8.5下進行。
- 如請求項1之方法,其中步驟(b)之該反應係在pH 5.5至6.5下進行。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662425761P | 2016-11-23 | 2016-11-23 | |
| US62/425,761 | 2016-11-23 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| TW202235109A TW202235109A (zh) | 2022-09-16 |
| TWI845890B true TWI845890B (zh) | 2024-06-21 |
Family
ID=60655118
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW111103323A TWI845890B (zh) | 2016-11-23 | 2017-11-22 | 苯二氮平衍生物之選擇性磺化 |
| TW106140599A TWI755450B (zh) | 2016-11-23 | 2017-11-22 | 苯二氮平衍生物之選擇性磺化 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW106140599A TWI755450B (zh) | 2016-11-23 | 2017-11-22 | 苯二氮平衍生物之選擇性磺化 |
Country Status (11)
| Country | Link |
|---|---|
| US (5) | US10287256B2 (zh) |
| EP (1) | EP3544983A2 (zh) |
| JP (2) | JP7203729B2 (zh) |
| KR (2) | KR20230133935A (zh) |
| CN (2) | CN110392685B (zh) |
| AU (2) | AU2017363237B2 (zh) |
| CA (1) | CA3044391A1 (zh) |
| IL (2) | IL266743B (zh) |
| MA (1) | MA46887A (zh) |
| TW (2) | TWI845890B (zh) |
| WO (1) | WO2018098258A2 (zh) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3769787A1 (en) * | 2015-06-29 | 2021-01-27 | ImmunoGen, Inc. | Conjugates of cysteine engineered antibodies |
| ES2887273T3 (es) | 2015-06-29 | 2021-12-22 | Immunogen Inc | Anticuerpos anti-CD123 y conjugados y derivados de los mismos |
| TWI845890B (zh) * | 2016-11-23 | 2024-06-21 | 美商伊繆諾金公司 | 苯二氮平衍生物之選擇性磺化 |
| US20200157228A1 (en) * | 2018-10-30 | 2020-05-21 | Immunogen, Inc. | Methods of treatment using anti-cd123 immunoconjugates |
| WO2020092344A1 (en) * | 2018-10-31 | 2020-05-07 | Health Research, Inc. | Combination treatment with anti-cd123 antibody drug conjugate and parp inhibitor |
| US11833214B2 (en) | 2019-03-21 | 2023-12-05 | Immunogen, Inc. | Methods of preparing cell-binding agent-drug conjugates |
| CA3137454A1 (en) | 2019-04-29 | 2020-11-05 | Immunogen, Inc. | Therapeutic combinations comprising anti-cd123 immunoconjugates |
| US20220306751A1 (en) | 2019-09-13 | 2022-09-29 | Mythic Therapeutics, Inc. | Antigen-binding protein constructs and uses thereof |
| CN113189184B (zh) * | 2021-04-28 | 2022-09-09 | 浙江大学 | 含有半胱氨酸的毛细管凝胶电泳样品缓冲液 |
| KR20250031149A (ko) | 2022-06-30 | 2025-03-06 | 도레이 카부시키가이샤 | 암의 치료 및/또는 예방용 의약 조성물 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012112708A1 (en) * | 2011-02-15 | 2012-08-23 | Immunogen, Inc. | Cytotoxic benzodiazepine derivatives and methods of preparation |
| WO2015028850A1 (en) * | 2013-09-02 | 2015-03-05 | Hangzhou Dac Biotech Co., Ltd | Novel cytotoxic agents for conjugation of drugs to cell binding molecule |
| TW201613929A (en) * | 2014-09-03 | 2016-04-16 | Immunogen Inc | Cytotoxic benzodiazepine derivatives |
| TWI755450B (zh) * | 2016-11-23 | 2022-02-21 | 美商伊繆諾金公司 | 苯二氮平衍生物之選擇性磺化 |
Family Cites Families (45)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5208020A (en) | 1989-10-25 | 1993-05-04 | Immunogen Inc. | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| ES2149768T3 (es) | 1992-03-25 | 2000-11-16 | Immunogen Inc | Conjugados de agentes enlazantes de celulas derivados de cc-1065. |
| GB9422383D0 (en) | 1994-11-05 | 1995-01-04 | Wellcome Found | Antibodies |
| ES2276708T3 (es) | 1999-11-24 | 2007-07-01 | Immunogen, Inc. | Agentes citotoxicos que comprenden taxanos y su uso terapeutico. |
| US6441163B1 (en) | 2001-05-31 | 2002-08-27 | Immunogen, Inc. | Methods for preparation of cytotoxic conjugates of maytansinoids and cell binding agents |
| US6716821B2 (en) | 2001-12-21 | 2004-04-06 | Immunogen Inc. | Cytotoxic agents bearing a reactive polyethylene glycol moiety, cytotoxic conjugates comprising polyethylene glycol linking groups, and methods of making and using the same |
| US6756397B2 (en) | 2002-04-05 | 2004-06-29 | Immunogen, Inc. | Prodrugs of CC-1065 analogs |
| CN100522955C (zh) | 2002-08-02 | 2009-08-05 | 伊缪诺金公司 | 含有新型强效紫杉烷的细胞毒性剂及其治疗用途 |
| JP2006500364A (ja) | 2002-08-16 | 2006-01-05 | イムノージェン インコーポレーテッド | 高い反応性と溶解度を有する架橋剤および小分子薬物の標的化送達用コンジュゲートの調製におけるそれらの使用 |
| BR0316101A (pt) | 2002-11-07 | 2005-09-27 | Immunogen Inc | Anticorpos anticd33 e processo para tratamento de leucemia melóide aguda usando os mesmos |
| US8088387B2 (en) | 2003-10-10 | 2012-01-03 | Immunogen Inc. | Method of targeting specific cell populations using cell-binding agent maytansinoid conjugates linked via a non-cleavable linker, said conjugates, and methods of making said conjugates |
| US7276497B2 (en) | 2003-05-20 | 2007-10-02 | Immunogen Inc. | Cytotoxic agents comprising new maytansinoids |
| AU2005218642B2 (en) | 2004-03-02 | 2011-04-28 | Seagen Inc. | Partially loaded antibodies and methods of their conjugation |
| KR20120064120A (ko) | 2004-06-01 | 2012-06-18 | 제넨테크, 인크. | 항체 약물 접합체 및 방법 |
| KR101270829B1 (ko) | 2004-09-23 | 2013-06-07 | 제넨테크, 인크. | 시스테인 유전자조작 항체 및 접합체 |
| EP1817341A2 (en) | 2004-11-29 | 2007-08-15 | Seattle Genetics, Inc. | Engineered antibodies and immunoconjugates |
| PL1879901T3 (pl) | 2005-04-21 | 2010-06-30 | Medimmune Ltd | Pirolobenzodiazepiny |
| US8008453B2 (en) | 2005-08-12 | 2011-08-30 | Amgen Inc. | Modified Fc molecules |
| ES2567402T3 (es) | 2006-05-30 | 2016-04-22 | Genentech, Inc. | Anticuerpos anti CD22, sus inmunoconjugados y usos de los mismos |
| WO2008119353A1 (en) | 2007-03-29 | 2008-10-09 | Genmab A/S | Bispecific antibodies and methods for production thereof |
| PL2019104T3 (pl) | 2007-07-19 | 2014-03-31 | Sanofi Sa | Środki cytotoksyczne obejmujące nowe pochodne tomaymycyny i ich zastosowanie terapeutyczne |
| KR20200058590A (ko) | 2008-04-30 | 2020-05-27 | 이뮤노젠 아이엔씨 | 가교제 및 그 용도 |
| EP2276506A4 (en) | 2008-04-30 | 2014-05-07 | Immunogen Inc | EFFICIENT CONJUGATES AND HYDROPHILIC BINDER |
| GB0819095D0 (en) | 2008-10-17 | 2008-11-26 | Spirogen Ltd | Pyrrolobenzodiazepines |
| CN102365021B (zh) | 2009-02-05 | 2015-07-15 | 伊缪诺金公司 | 新型苯并二氮杂*衍生物 |
| AU2010270979B2 (en) | 2009-06-22 | 2015-04-23 | Medimmune, Llc | Engineered Fc regions for site-specific conjugation |
| WO2011092838A1 (ja) | 2010-01-29 | 2011-08-04 | 株式会社フォーサイド・ドット・コム | コンテンツ共有システム、およびコンテンツ共有方法 |
| CN103037900B (zh) | 2010-02-24 | 2016-04-06 | 伊缪诺金公司 | 叶酸受体1抗体与免疫缀合物以及其用途 |
| SG183542A1 (en) | 2010-03-12 | 2012-10-30 | Immunogen Inc | Cd37-binding molecules and immunoconjugates thereof |
| US8697688B2 (en) | 2010-04-15 | 2014-04-15 | Seattle Genetics Inc. | Pyrrolobenzodiazepines used to treat proliferative diseases |
| DK2560993T3 (da) | 2010-04-20 | 2024-10-14 | Genmab As | Heterodimeric antibody fc-containing proteins and methods for production thereof |
| CN103298489A (zh) | 2010-10-29 | 2013-09-11 | 伊缪诺金公司 | 新型egfr结合分子及其免疫偶联物 |
| CN105399831A (zh) | 2010-10-29 | 2016-03-16 | 伊缪诺金公司 | 非拮抗性egfr结合分子及其免疫偶联物 |
| WO2013177481A1 (en) | 2012-05-25 | 2013-11-28 | Immunogen, Inc. | Benzodiazepines and conjugates thereof |
| JP6494533B2 (ja) | 2013-02-28 | 2019-04-03 | イミュノジェン・インコーポレーテッド | 細胞結合剤及び細胞毒性剤としてのマイタンシノイドを含む複合体 |
| WO2014134457A2 (en) | 2013-02-28 | 2014-09-04 | Immunogen, Inc. | Conjugates comprising cell-binding agents and cytotoxic agents |
| WO2014134486A2 (en) | 2013-02-28 | 2014-09-04 | Immunogen, Inc. | Conjugates comprising cell-binding agents and cytotoxic agents |
| WO2015196089A1 (en) | 2014-06-20 | 2015-12-23 | Bioalliance C.V. | Anti-cd22 antibody-drug conjugates and methods of using thereof |
| SG11201610620UA (en) | 2014-06-20 | 2017-01-27 | Bioalliance Cv | Anti-folate receptor aplha (fra) antibody-drug conjugates and methods of using thereof |
| CN106999604B (zh) | 2014-09-02 | 2021-08-03 | 伊缪诺金公司 | 用于配制抗体药物缀合物组合物的方法 |
| EP3189057A1 (en) | 2014-09-03 | 2017-07-12 | ImmunoGen, Inc. | Cytotoxic benzodiazepine derivatives |
| MA41645A (fr) | 2015-03-04 | 2018-01-09 | Abbvie Stemcentrx Llc | Anticorps issus de génie génétique spécifiques au site et méthodes d'utilisation |
| ES2887273T3 (es) | 2015-06-29 | 2021-12-22 | Immunogen Inc | Anticuerpos anti-CD123 y conjugados y derivados de los mismos |
| EP3769787A1 (en) | 2015-06-29 | 2021-01-27 | ImmunoGen, Inc. | Conjugates of cysteine engineered antibodies |
| MX2018009487A (es) | 2016-02-05 | 2019-01-31 | Millennium Pharm Inc | Conjugados de anticuerpo y fármaco dirigidos contra gcc. |
-
2017
- 2017-11-22 TW TW111103323A patent/TWI845890B/zh not_active IP Right Cessation
- 2017-11-22 EP EP17812176.0A patent/EP3544983A2/en not_active Withdrawn
- 2017-11-22 JP JP2019527831A patent/JP7203729B2/ja active Active
- 2017-11-22 TW TW106140599A patent/TWI755450B/zh not_active IP Right Cessation
- 2017-11-22 WO PCT/US2017/062989 patent/WO2018098258A2/en not_active Ceased
- 2017-11-22 AU AU2017363237A patent/AU2017363237B2/en not_active Ceased
- 2017-11-22 CA CA3044391A patent/CA3044391A1/en active Pending
- 2017-11-22 KR KR1020237030171A patent/KR20230133935A/ko not_active Ceased
- 2017-11-22 KR KR1020197017971A patent/KR102576550B1/ko active Active
- 2017-11-22 CN CN201780084278.3A patent/CN110392685B/zh not_active Expired - Fee Related
- 2017-11-22 US US15/820,648 patent/US10287256B2/en active Active
- 2017-11-22 CN CN202310731029.6A patent/CN116813690A/zh active Pending
- 2017-11-22 MA MA046887A patent/MA46887A/fr unknown
-
2019
- 2019-03-26 US US16/364,801 patent/US10494348B2/en active Active
- 2019-05-20 IL IL266743A patent/IL266743B/en unknown
- 2019-10-30 US US16/669,121 patent/US10822313B2/en active Active
-
2020
- 2020-09-17 US US17/023,545 patent/US11572349B2/en active Active
-
2022
- 2022-03-22 IL IL291597A patent/IL291597A/en unknown
- 2022-06-15 AU AU2022204163A patent/AU2022204163B2/en not_active Expired - Fee Related
- 2022-12-26 JP JP2022207896A patent/JP2023036842A/ja active Pending
- 2022-12-30 US US18/091,653 patent/US20230391733A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012112708A1 (en) * | 2011-02-15 | 2012-08-23 | Immunogen, Inc. | Cytotoxic benzodiazepine derivatives and methods of preparation |
| WO2015028850A1 (en) * | 2013-09-02 | 2015-03-05 | Hangzhou Dac Biotech Co., Ltd | Novel cytotoxic agents for conjugation of drugs to cell binding molecule |
| TW201613929A (en) * | 2014-09-03 | 2016-04-16 | Immunogen Inc | Cytotoxic benzodiazepine derivatives |
| TWI755450B (zh) * | 2016-11-23 | 2022-02-21 | 美商伊繆諾金公司 | 苯二氮平衍生物之選擇性磺化 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI845890B (zh) | 苯二氮平衍生物之選擇性磺化 | |
| RU2733740C2 (ru) | Конъюгаты сконструированных антител с цистеиновыми заменами | |
| TWI862991B (zh) | 具有自分解肽連接子之類美登素衍生物及其結合物 | |
| CN107580604A (zh) | 包含细胞结合剂和细胞毒性剂的缀合物 | |
| TWI827575B (zh) | 苯二氮平衍生物 | |
| RU2773881C2 (ru) | Селективное сульфирование производных бензодиазепина | |
| RU2834224C1 (ru) | Конъюгаты сконструированных антител с цистеиновыми заменами |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | Annulment or lapse of patent due to non-payment of fees |