KR101390523B1 - Novel compounds and organic electro luminescence device using the same - Google Patents
Novel compounds and organic electro luminescence device using the same Download PDFInfo
- Publication number
- KR101390523B1 KR101390523B1 KR1020110131297A KR20110131297A KR101390523B1 KR 101390523 B1 KR101390523 B1 KR 101390523B1 KR 1020110131297 A KR1020110131297 A KR 1020110131297A KR 20110131297 A KR20110131297 A KR 20110131297A KR 101390523 B1 KR101390523 B1 KR 101390523B1
- Authority
- KR
- South Korea
- Prior art keywords
- group
- compound
- groups
- aryl
- same
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D221/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00
- C07D221/02—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00 condensed with carbocyclic rings or ring systems
- C07D221/04—Ortho- or peri-condensed ring systems
- C07D221/18—Ring systems of four or more rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/36—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D265/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom and one oxygen atom as the only ring hetero atoms
- C07D265/28—1,4-Oxazines; Hydrogenated 1,4-oxazines
- C07D265/34—1,4-Oxazines; Hydrogenated 1,4-oxazines condensed with carbocyclic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D279/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom and one sulfur atom as the only ring hetero atoms
- C07D279/10—1,4-Thiazines; Hydrogenated 1,4-thiazines
- C07D279/14—1,4-Thiazines; Hydrogenated 1,4-thiazines condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D335/00—Heterocyclic compounds containing six-membered rings having one sulfur atom as the only ring hetero atom
- C07D335/04—Heterocyclic compounds containing six-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/06—Luminescent materials, e.g. electroluminescent or chemiluminescent containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/656—Aromatic compounds comprising a hetero atom comprising two or more different heteroatoms per ring
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
본 발명은 신규 화합물 및 이를 이용한 유기 전계 발광 소자에 관한 것으로, 구체적으로는 인덴계 화합물과 축합 헤테로환 모이어티가 연결된 기본 골격에 여러 치환체가 결합된 화합물과 상기 화합물을 유기 전계 발광 소자에 적용하는 것이다. 이와 같은 본 발명은 효율, 수명 및 안정성 등이 향상된 유기 전계 발광 소자를 제공할 수 있다.The present invention relates to a novel compound and an organic electroluminescent device using the same. More specifically, the present invention relates to a compound in which various substituents are bonded to a basic skeleton in which an indene compound and a condensed heterocyclic moiety are connected to each other, will be. The present invention can provide an organic electroluminescent device with improved efficiency, lifetime, and stability.
Description
본 발명은 신규 화합물 및 이를 포함하는 유기 전계 발광 소자에 관한 것으로, 보다 구체적으로는 유기 전계 발광 소자의 유기물층에 사용되는 화합물에 관한 것이다.TECHNICAL FIELD The present invention relates to a novel compound and an organic electroluminescent device including the same and more particularly to a compound used in an organic material layer of an organic electroluminescent device.
1950년대 Bernanose의 유기 박막 발광 관측을 시점으로 하여, 1965년 안트라센 단결정을 이용한 청색 전기발광으로 이어진 유기 전계 발광(electroluminescent, EL) 소자에 대한 연구는 1987년 탕(Tang)에 의하여 정공층과 발광층의 기능층으로 나눈 적층 구조의 유기 전계 발광 소자가 제시되었다. 이후 유기 전계 발광 소자는 소자의 효율 및 수명을 향상시키기 위하여 소자 내 특징적인 유기물 층을 도입하는 형태로 발전해왔다.A study on the electroluminescent (EL) devices that led to the blue electroluminescence using the anthracene single crystal in 1965 based on the observation of the organic thin film emission of the Bernanose in the 1950s was carried out by Tang in 1987, An organic electroluminescent device having a laminated structure divided by functional layers has been proposed. In order to improve the efficiency and lifetime of the organic electroluminescent device, the organic electroluminescent device has been developed to introduce characteristic organic layers in the device.
유기 전계 발광 소자는 두 전극 사이에 전압을 걸어 주면 양극에서 정공이, 음극에서 전자가 유기물층으로 주입되어, 주입된 정공과 전자가 만나 엑시톤(exciton)이 형성되며, 형성된 엑시톤이 바닥상태로 떨어질 때 빛이 나게 된다. 유기물층으로 사용되는 물질은 기능에 따라, 발광 물질, 정공 주입 물질, 정공 수송 물질, 전자 수송 물질, 전자 주입 물질 등으로 분류될 수 있다.In the organic electroluminescent device, when a voltage is applied between the two electrodes, holes are injected from the anode and electrons from the cathode are injected into the organic layer, and the injected holes and electrons meet to form an exciton. When the exciton formed drops to a ground state The light comes out. The material used as the organic material layer may be classified into a light emitting material, a hole injecting material, a hole transporting material, an electron transporting material, and an electron injecting material depending on functions.
발광 물질은 발광색에 따라 청색, 녹색, 적색 발광 물질과 보다 나은 천연색을 구현하기 위해 필요한 노란색 및 주황색 발광 물질로 구분될 수 있다. 또한, 색순도의 증가와 에너지 전이를 통한 발광 효율을 증가시키기 위하여, 발광 물질로서 호스트/도판트 계를 사용할 수 있다.The luminescent material can be classified into blue, green and red luminescent materials according to luminescent colors and yellow and orange luminescent materials necessary for realizing better natural colors. Further, in order to increase the color purity and to increase the luminous efficiency through energy transfer, a host / dopant system can be used as a luminescent material.
도판트 물질은 유기 물질을 사용하는 형광 도판트와 Ir, Pt 등의 중원자(heavy atoms)가 포함된 금속 착체 화합물을 사용하는 인광 도판트로 나눌 수 있다. 인광 도판트의 개발은 이론적으로 형광 도판트에 비해 4배까지 발광 효율을 향상 시킬 수 있어 인광 도판트 뿐만 아니라 인광 호스트에 대해서도 연구되고 있다.The dopant material can be divided into a fluorescent dopant using an organic material and a phosphorescent dopant using a metal complex compound containing heavy atoms such as Ir and Pt. The development of the phosphorescent dopant can theoretically improve the luminous efficiency up to 4 times as compared with the fluorescent dopant, so that the phosphorescent dopant as well as the phosphorescent host have been studied.
현재까지 정공 수송층. 정공 차단층, 전자 수송층으로 사용되는 물질로는 NPB, BCP, Alq3 등이 널리 알려져 있으며, 발광 물질로는 안트라센 유도체들이 사용되고 있다. 특히 발광 물질 중 효율 향상 측면에서 큰 장점을 가지고 있는 Firpic, Ir(ppy)3, (acac)Ir(btp)2 등과 같은 Ir을 포함하는 금속 착체 화합물은 blue, green, red 인광 도판트 재료로, CBP는 인광 호스트 재료로 사용되고 있다.Up to now, the hole transport layer. NPB, BCP, Alq 3 and the like are widely known as materials used as a hole blocking layer and an electron transporting layer, and an anthracene derivative is used as a luminescent material. In particular, metal complex compounds containing Ir such as Firpic, Ir (ppy) 3 , (acac) Ir (btp) 2 and the like having great advantages in terms of efficiency improvement of light emitting materials are blue, green, red phosphorescent dopant materials, CBP is used as a phosphorescent host material.
그러나 종래의 발광 물질들은 발광 특성이 양호하나, 유리전이온도가 낮고 열적 안정성이 매우 좋지 않아 유기 전계 발광 소자의 수명 측면에서 만족할만한 수준이 되지 못하기 때문에 성능이 우수한 발광 물질의 개발이 요구되고 있다.However, since conventional luminescent materials have good luminescence characteristics, they have low glass transition temperature and are not very satisfactory in terms of the lifetime of the organic electroluminescent devices because of their poor thermal stability, development of luminescent materials having excellent performance is required .
본 발명은 상기한 문제점을 해결하기 위해, 유기 전계 발광 소자의 효율, 수명 및 안정성 등을 향상시킬 수 있는 신규 화합물 및 상기 화합물을 이용한 유기 전계 발광 소자를 제공하는 것을 목적으로 한다.The present invention has been made to solve the above problems and it is an object of the present invention to provide a novel compound capable of improving the efficiency, lifetime and stability of the organic electroluminescent device and an organic electroluminescent device using the compound.
상기한 목적을 달성하기 위해, 본 발명은 하기 화학식 1로 표시되는 화합물을 제공한다.In order to achieve the above object, the present invention provides a compound represented by the following general formula (1).
[화학식 1] [Chemical Formula 1]
상기 화학식 1에서,In Formula 1,
X 및 Y는 서로 같거나 다르고, CR3R4, O, S, NR5, SiR6R7로 이루어진 군에서 선택되며, 단, X 및 Y가 모두 CR3R4인 경우는 제외되고;X and Y are the same or different and are selected from the group consisting of CR 3 R 4 , O, S, NR 5 , and SiR 6 R 7 except when X and Y are both CR 3 R 4 ;
R1 내지 R7는 서로 같거나 다르고, 수소, 중수소, 할로겐, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아미노기, C6~C40의 디아릴아미노기, C6~C40의 아릴알킬기, C3~C40의 시클로알킬기, C6~C40의 아릴실릴기 및 C3~C40의 헤테로시클로알킬기로 이루어진 군에서 선택되며;R 1 to R 7 are the same or different from each other and represent hydrogen, deuterium, halogen, C 1 to C 40 alkyl, C 2 to C 40 alkenyl, C 2 to C 40 alkynyl, C 6 to C 40 aryl Group, a C 5 to C 40 heteroaryl group, a C 6 to C 40 aryloxy group, a C 1 to C 40 alkyloxy group, a C 6 to C 40 arylamino group, a C 6 to C 40 diarylamino group , A C 6 to C 40 arylalkyl group, a C 3 to C 40 cycloalkyl group, a C 6 to C 40 arylsilyl group, and a C 3 to C 40 heterocycloalkyl group;
Ar1 내지 Ar3는 서로 같거나 다르고, 수소, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C3~C40의 시클로알킬기, C3~C40의 헤테로시클로알킬기, C6~C40의 아릴기, C5~C60의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C40의 아릴옥시기, C6~C40의 아릴실릴기 및 C6~C40의 아릴아민기로 이루어진 군에서 선택되고; Ar 1 to Ar 3 are the same or different from each other, hydrogen, deuterium, halogen, cyano group, C 1 ~ C 40 alkyl group, C 3 ~ C 40 cycloalkyl group, C 3 ~ C 40 heterocycloalkyl group, C 6 ~ of C 6 to C 40 aryloxy groups, C 6 to C 40 arylsilyl groups and C 6 to C 40 aryl groups, C 5 to C 60 heteroaryl groups, C 1 to C 40 alkyloxy groups, C 6 to C 40 aryloxy groups, 40 < / RTI > arylamine groups;
a, b 및 c는 0 내지 4의 정수이다.a, b and c are an integer of 0 to 4;
여기서, 상기 R1 내지 R7는 수소, 중수소, 할로겐, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아미노기, C6~C40의 디아릴아미노기, C6~C40의 아릴알킬기, C3~C40의 시클로알킬기, C6~C40의 아릴실릴기 및 C3~C40의 헤테로시클로알킬기로 이루어진 군에서 선택된 치환기로 치환되거나, 비치환될 수 있다.Wherein R 1 to R 7 are independently selected from the group consisting of hydrogen, deuterium, halogen, C 1 to C 40 alkyl, C 2 to C 40 alkenyl, C 2 to C 40 alkynyl, C 6 to C 40 aryl, A C 6 to C 40 heteroaryl group, a C 6 to C 40 aryloxy group, a C 1 to C 40 alkyloxy group, a C 6 to C 40 arylamino group, a C 6 to C 40 diarylamino group, a C Which may be unsubstituted or substituted with a substituent selected from the group consisting of an aryl group, a C 6 to C 40 arylalkyl group, a C 3 to C 40 cycloalkyl group, a C 6 to C 40 arylsilyl group, and a C 3 to C 40 heterocycloalkyl group have.
또한, 상기 Ar1 내지 Ar3인 C1~C40의 알킬기 및 C1~C40의 알킬옥시기는 직쇄 또는 분지쇄일 수 있으며, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기 및 C6~C40의 아릴아민기는 융합 또는 비융합된 것일 수 있다.The C 1 to C 40 alkyl groups and C 1 to C 40 alkyloxy groups represented by Ar 1 to Ar 3 may be linear or branched, and include C 6 to C 40 aryl groups, C 5 to C 40 heteroaryl Group, a C 6 to C 40 aryloxy group and a C 6 to C 40 arylamine group may be fused or unfused.
또, 상기 Ar1 내지 Ar3는 인접한 기와 융합하여 고리를 형성할 수도 있다.In addition, Ar 1 to Ar 3 may be fused with adjacent groups to form a ring.
한편, 본 발명은 하기 화학식 2 내지 4로 표시되는 화합물로 이루어진 군에서 선택된 화합물도 제공한다.The present invention also provides compounds selected from the group consisting of compounds represented by the following formulas (2) to (4).
[화학식 2] (2)
[화학식 3] (3)
[화학식 4] [Chemical Formula 4]
상기 화학식 2 내지 4에서,In the above Chemical Formulas 2 to 4,
X, Y, R1 내지 R7, Ar1 내지 Ar3 및 a, b, c에 대해서는 상기 화학식 1로 표시되는 화합물에서 정의된 바와 동일하며,X, Y, R 1 to R 7 , Ar 1 to Ar 3 And a, b and c are the same as defined in the compound represented by the formula (1)
X' 및 Y'는 서로 같거나 다르고, CR3''R4'. O, S, NR5' 및 SiR6'R7'로 이루어진 군에서 선택되며, 단, X' 및 Y'가 모두 CR3'R4'인 경우는 제외되고;X 'and Y' are the same or different from each other, and CR 3 "R 4 '. O, S, NR 5 'and SiR 6 ' R 7 ', with the proviso that X' and Y 'are not CR 3 ' R 4 ';
R1' 내지 R7'는 서로 같거나 다르고, 수소, 중수소, 할로겐, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아미노기, C6~C40의 디아릴아미노기, C6~C40의 아릴알킬기, C3~C40의 시클로알킬기, C6~C40의 아릴실릴기 및 C3~C40의 헤테로시클로알킬기로 이루어진 군에서 선택되며;R 1 ' To R 7 'are the same or different from each other and represent hydrogen, deuterium, halogen, a C 1 to C 40 alkyl group, a C 2 to C 40 alkenyl group, a C 2 to C 40 alkynyl group, a C 6 to C 40 aryl group , A C 5 to C 40 heteroaryl group, a C 6 to C 40 aryloxy group, a C 1 to C 40 alkyloxy group, a C 6 to C 40 arylamino group, a C 6 to C 40 diarylamino group, A C 6 to C 40 arylalkyl group, a C 3 to C 40 cycloalkyl group, a C 6 to C 40 arylsilyl group, and a C 3 to C 40 heterocycloalkyl group;
Ar1' 내지 Ar3'는 서로 같거나 다르고, 수소, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C3~C40의 시클로알킬기, C3~C40의 헤테로시클로알킬기, C6~C40의 아릴기, C5~C60의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C40의 아릴옥시기, C6~C40의 아릴실릴기 및 C6~C40의 아릴아민기로 이루어진 군에서 선택되고;Ar 1 'to Ar 3 ' are the same or different from each other and represent hydrogen, deuterium, halogen, cyano, C 1 to C 40 alkyl, C 3 to C 40 cycloalkyl, C 3 to C 40 heterocycloalkyl, C an aryl group of 6 ~ C 40, C 5 ~ heteroaryl group of C 60, C 1 ~ C 40 alkyloxy group of, C aryloxy of 6 ~ C 40, C 6 ~ C 40 aryl silyl group, and a C 6 of ~ C 40 is selected from the group consisting of an aryl amine;
a', b' 및 c'는 0 내지 4의 정수이다.a ', b' and c 'are an integer of 0 to 4;
이때, 상기 R1' 내지 R7' 또한 R1 내지 R7과 같이 상기에서 설명한 치환기로 치환될 수 있다.Here, R 1 'to R 7 ' may also be substituted with the substituents described above as R 1 to R 7 .
또한, 상기 Ar1' 내지 상기 Ar3'는 C1~C40의 알킬기 및 C1~C40의 알킬옥시기는 직쇄 또는 분지쇄일 수 있으며, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기 및 C6~C40의 아릴아민기는 융합 또는 비융합된 것일 수 있다.In the above Ar 1 'to Ar 3 ', the C 1 to C 40 alkyl group and the C 1 to C 40 alkyloxy group may be linear or branched, and include C 6 to C 40 aryl groups, C 5 to C 40 a heteroaryl group, C 6 ~ C 40 aryloxy and C 6 ~ C 40 arylamine groups may be fused or non-fused.
또, 상기 Ar1' 내지 Ar3'도 인접한 기와 융합하여 고리를 형성할 수 있다.In addition, Ar 1 'to Ar 3 ' may be fused with adjacent groups to form a ring.
한편, 본 발명은, 양극, 음극, 및 상기 양극과 음극 사이에 개재(介在)된 1층 이상의 유기물층을 포함하는 유기 전계 발광 소자에 있어서, 상기 유기물층 중 적어도 하나는 상기 화학식 1 내지 4로 표시되는 화합물 중 어느 하나를 포함하는 유기물층인 것을 특징으로 하는 유기 전계 발광 소자를 제공한다.On the other hand, the present invention is an organic electroluminescent device comprising an anode, a cathode, and one or more organic layers sandwiched between the anode and the cathode, wherein at least one of the organic layers is represented by the general formulas And the organic compound layer is an organic compound layer containing any one of the compounds.
여기서, 상기 유기물층은 발광층, 정공수송층 또는 전자수송층일 수 있다.Here, the organic material layer may be a light emitting layer, a hole transporting layer, or an electron transporting layer.
본 발명의 화학식 1 내지 4로 표시되는 화합물 중 어느 하나를 유기 전계 발광 소자의 발광 물질로 사용할 경우, 종래의 발광 물질에 비해 유기 전계 발광 소자의 효율(발광 효율 및 전령 효율), 수명, 휘도 및 구동전압 등을 향상시킬 수 있다. 따라서, 본 발명은 풀 칼라 유기 EL 패널의 성능 및 수명을 향상시킬 수 있다.When one of the compounds represented by the general formulas (1) to (4) of the present invention is used as a light emitting material of an organic electroluminescent device, the efficiency (luminous efficiency and messenger efficiency), lifetime, The driving voltage and the like can be improved. Therefore, the present invention can improve the performance and lifetime of the full color organic EL panel.
이하, 본 발명을 상세히 설명한다.
Hereinafter, the present invention will be described in detail.
1, 신규 화합물1, a novel compound
본 발명에 따른 신규 화합물은 인덴계 화합물과 축합(fused) 헤테로환 모이어티가 연결되어 기본 골격을 이루며, 다양한 치환체가 결합된 화합물로 상기 화학식 1(이하, '화학식Ⅰ'이라 함)로 표시된다. 이러한, 본 발명의 화합물Ⅰ은 다양한 치환체(상기 화학식 1에서 R1, R2 및 Ar1 내지 Ar3)가 결합되어 에너지 레벨이 조절됨으로써 종래의 유기 발광 소자용 재료(예를 들어, CBP(4,4-dicarbazolybiphenyl))보다 높은 분자량을 가지며, 넓은 에너지 밴드갭을 나타내는 것이 특징이다.The novel compound according to the present invention is a compound in which an indene compound and a fused heterocyclic moiety are linked to form a basic skeleton and various substituents are bonded thereto, and is represented by the formula 1 (hereinafter referred to as a 'formula I') . The compound I of the present invention can be prepared by mixing various substituents (R 1 , R 2 and Ar 1 to Ar 3 in the above formula (1)) to control the energy level so that a conventional organic light emitting device material (for example, CBP , 4-dicarbazolybiphenyl), and exhibits a wide energy bandgap.
구체적으로, 본 발명의 화합물Ⅰ에 있어서, 헤테로환 모이어티가 페노티아진(phenothiazine, 화학식 1에서 X나 Y 중 하나가 NH이고 다른 하나가 S인 화합물), 페녹사진(phenoxazine, 화학식 1에서 X나 Y 중 하나가 NH이고 다른 하나가 O인 화합물), 아크리딘(arridine, 화학식 1에서 X나 Y 중 하나가 NH이고 다른 하나가 CH2인 화합물), 페나자실린(phenazasiline, 화학식 1에서 X나 Y 중 하나가 NH이고 다른 하나가 SiH2인 화합물)일 경우 다양한 치환체의 도입이 용이하며, 도입된 치환체에 의해 삼중항 에너지 레벨(Triplet energy state)이 안정하게 형성되어 에너지 레벨을 조절할 수 있다.Specifically, in the compound I of the present invention, the heterocyclic moiety is phenothiazine (a compound in which one of X and Y is NH and the other is S), phenoxazine (X in Formula 1) Or a compound wherein Y is NH and the other is O, arridine (a compound wherein one of X and Y is NH and the other is CH 2 ), phenazasiline (compound of formula 1) When one of X and Y is NH and the other is SiH 2 ), various substituents can be easily introduced, and the triplet energy state can be stably formed by the introduced substituent to control the energy level have.
또한, 다양한 치환체가 도입된 본 발명의 화합물Ⅰ은 분자량이 유의적으로 증대됨으로써, 유리전이온도가 향상되고 이로 인해 종래 재료들에 비해 높은 열적 안정성을 가질 수 있다.In addition, the compound I of the present invention in which various substituents have been introduced has a significantly increased molecular weight, thereby improving the glass transition temperature and thus having higher thermal stability than conventional materials.
따라서, 본 발명의 화합물Ⅰ을 유기 전계 발광 소자의 재료로 사용할 경우 소자의 인광특성뿐만 아니라, 전자 및/또는 정공 수송 능력, 발광효율, 구동전압, 수명 특성 등이 개선될 수 있다. 이때, 본 발명의 화합물Ⅰ은 유기 전계 발광 소자의 유기물층의 재료, 바람직하게는 발광층, 정공수송층 또는 전자수송층의 재료, 보다 바람직하게는 발광층의 호스트 재료로 사용될 수 있다.Therefore, when Compound I of the present invention is used as a material for an organic electroluminescent device, not only the phosphorescence characteristics of the device, but also the electron and / or hole transporting ability, luminous efficiency, driving voltage and lifetime characteristics can be improved. At this time, the compound I of the present invention can be used as a material of an organic material layer of an organic electroluminescent device, preferably a material of a light emitting layer, a hole transporting layer or an electron transporting layer, more preferably a host material of a light emitting layer.
이러한, 본 발명의 화합물Ⅰ의 치환체인 R1 내지 R7 및 Ar1 내지 Ar3의 예로 하기와 같은 예(S1~S138)를 들 수 있지만, 이에 한정되는 것은 아니다.Examples of such substituents R 1 to R 7 and Ar 1 to Ar 3 of the compound I of the present invention include, but are not limited to, the following examples (S1 to S138).
상기한 본 발명의 화합물Ⅰ은 하기 화학식 C-1 내지 화학식 C-11로 표시되는 화합물로 이루어진 군에서 선택되는 것이 바람직하나, 이에 한정되는 것은 아니다.The compound I of the present invention is preferably selected from the group consisting of compounds represented by the following formulas C-1 to C-11, but is not limited thereto.
상기 화학식 C-1 내지 C-11에서,In the above formulas C-1 to C-11,
R1 내지 R7, Ar1 내지 Ar3 및 a, b, c에 대한 정의는 상기 화합물Ⅰ에서 정의된 바와 동일하다.The definitions of R 1 to R 7 , Ar 1 to Ar 3, and a, b, and c are the same as those defined in the above-mentioned compound I.
한편, 유기 전계 발광 소자의 효율 및 수명 특성 등을 고려할 때 상기 화학식 C-1 내지 C-11에서 R1 및 R2는 서로 동일하며, 메틸기 또는 페닐기인 것이 바람직하다. 또한, 상기 화학식 C-1 내지 C-11에서 R3 및 R4도 서로 동일하며, 메틸기 또는 페닐기인 것이 바람직하다. 또, 상기 화학식 C-1 내지 C-11에서 R5는 C6~C40의 아릴기 또는 C5~C40의 헤테로아릴기인 것이 바람직하다.Meanwhile, considering the efficiency and lifetime characteristics of the organic electroluminescent device, R 1 and R 2 in the formulas (C-1) to (C-11) are preferably the same and are preferably a methyl group or a phenyl group. In the above formulas C-1 to C-11, R 3 and R 4 are also the same and preferably a methyl group or a phenyl group. In the above formulas C-1 to C-11, it is preferable that R 5 is a C 6 to C 40 aryl group or a C 5 to C 40 heteroaryl group.
이와 같은 상기 화학식 C-1 내지 C-11로 표시되는 화합물은 하기와 같은 방법으로 합성될 수 있다.The compounds represented by the above Formulas C-1 to C-11 can be synthesized as follows.
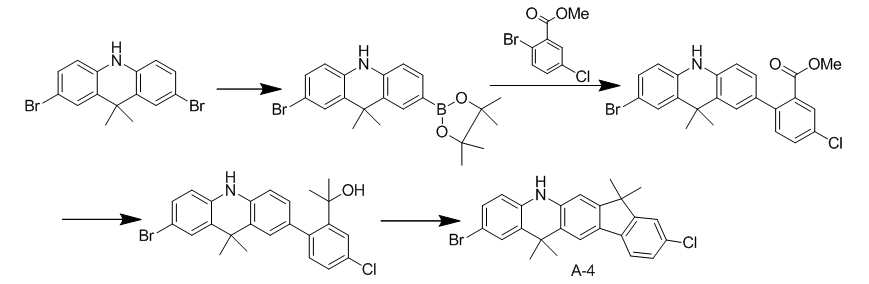
A. 화학식 C-1로 표시되는 화합물의 예로 화합물 A-1 내지 A-4 합성A. Examples of the compound represented by the formula C-1 include compounds A-1 to A-4
A-1) 화합물 A-1의 합성A-1) Synthesis of Compound A-1
질소기류 하에서 2-bromo-9,9-dimethyl-9,10-dihydroacridine 40.2g(0.128mol), 4,4,4',4',5,5,5',5'-octamethyl-2,2'-bi(1,3,2-dioxaborolane) 48.58g(0.191mol), Pd(dppf)Cl2 5.2g(5mol%), KOAc 37.55g(0.383mol), DMF 500ml를 넣고 130℃에서 12h 교반한 후 반응을 종결시키고, 에틸아세테이트로 추출하여 MgSO4로 수분을 제거한다. 용매를 제거한 반응물은 컬럼크로마토그래피 (Hexane:EA = 10:1 (v/v))를 이용하여 9,9-dimethyl-2-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-9,10-dihydroacridine 18.53g(0.051mol)(수율 40 %)을 획득한다.(0.128 mol) of 2-bromo-9,9-dimethyl-9,10-dihydroacridine and 4,4,4 ', 4', 5,5,5 ', 5'-octamethyl-2,2 , 5.25 g (5 mol%) of Pd (dppf) Cl 2 , 37.55 g (0.383 mol) of KOAc and 500 ml of DMF were placed and stirred at 130 ° C for 12 hours The reaction is terminated, extracted with ethyl acetate and the water is removed with MgSO 4 . The solvent was removed and the residue was purified by column chromatography (Hexane: EA = 10: 1 (v / v)) to obtain 9,9-dimethyl- 2- (4,4,5,5-tetramethyl- dioxaborolan-2-yl) -9,10-dihydroacridine (0.051 mol) (yield 40%).
질소기류 하에서 methyl 2-bromobenzoate 8.72g(0.040mol), 9,9-dimethyl-2-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-9,10-dihydroacridine 18.53g(0.051mol), 4.75g(118.8mmol)의 NaOH과 200 ml/100 ml의 THF/H2O를 넣고 교반한다. 40℃에서 2.29g(5 mol%)의 Pd(PPh3)4를 넣고 80℃에서 12시간 동안 교반한다. 반응 종결 후 메틸렌클로라이드로 추출하고 MgSO4를 넣고 필터한다. 필터된 유기층의 용매를 제거한 후 컬럼 크로마토그래피 (Hexane:EA = 3:1 (v/v))를 이용하여 methyl 2-(9,9-dimethyl-9,10-dihydroacridin-2-yl)benzoate 13.21g (35.7mmol)(수율 70%)을 획득한다.8.72 g (0.040 mol) of methyl 2-bromobenzoate, 9,9-dimethyl-2- (4,4,5,5-tetramethyl-1,3,2-dioxaborolan- 18.53 g (0.051 mol) of dihydroacridine, 4.75 g (118.8 mmol) of NaOH and 200 ml / 100 ml of THF / H 2 O are added and stirred. At 40 ℃ into the Pd (PPh 3) 4 of 2.29g (5 mol%) and stirred at 80 ℃ for 12 hours. After completion of the reaction, the reaction mixture is extracted with methylene chloride, and the mixture is filtered with MgSO 4 . After removing the solvent of the filtered organic layer, methyl 2- (9,9-dimethyl-9,10-dihydroacridin-2-yl) benzoate 13.21 (3H) was obtained by column chromatography (Hexane: EA = 3: 1 g (35.7 mmol) (yield 70%).
methyl 2-(9,9-dimethyl-9,10-dihydroacridin-2-yl)benzoate 13.21g (35.7mmol)을 진공 분위기 하에서 아르곤으로 채운 후 테트라하이드로퓨란 1L를 넣고 -75℃에서 10분간 교반한다. MeLi(1.6M in hexane) 100mL(0.16mmol)를 첨가하고 -75℃에서 10분 동안 교반한 후, 상온에서 3시간 동안 교반한다. 반응이 종결되면 증류수와 에틸아세테이트로 추출한다. 유기층을 MgSO4로 건조 시킨 다음 용매를 제거한 후 헥산과 에틸아세테이트로 컬럼 분리하여 2-(2-(9,9-dimethyl-9,10-dihydroacridin-2-yl)phenyl)propan-2-ol 11.23g (30.3mmol)(수율 85 %)를 획득한다.13.21 g (35.7 mmol) of methyl 2- (9,9-dimethyl-9,10-dihydroacridin-2-yl) benzoate was charged with argon in a vacuum atmosphere, followed by the addition of 1 L of tetrahydrofuran and stirring at -75 ° C for 10 minutes. 100 mL (0.16 mmol) MeLi (1.6 M in hexane) was added, and the mixture was stirred at -75 째 C for 10 minutes and then at room temperature for 3 hours. When the reaction is complete, extract with distilled water and ethyl acetate. The organic layer was dried over MgSO 4 and then the solvent was removed. The organic layer was separated by column using hexane and ethyl acetate to give 2- (9,9-dimethyl-9,10-dihydroacridin-2-yl) phenylpropan- g (30.3 mmol) (yield 85%).
2-(2-(9,9-dimethyl-9,10-dihydroacridin-2-yl)phenyl)propan-2-ol 11.23g(30.3mmol)을 플라스크에 넣고 AcOH 300mL를 넣은 후, 0℃에서 10분간 교반한다. H3PO4 400mL를 첨가하고 상온에서 1시간 동안 교반한 후, 반응이 종결되면 NaOH로 중화시키고 증류수와 에틸아세테이트로 추출한다. 유기층을 MgSO4로 건조 시킨 다음 용매를 제거한 후 헥산과 에틸아세테이트로 컬럼 분리하여 화합물 A-1인 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 7.92g(22.5mmol) (수율 74 %)를 합성한다.11.23 g (30.3 mmol) of 2- (9,9-dimethyl-9,10-dihydroacridin-2-yl) phenylpropan-2-ol was placed in a flask, 300 mL of AcOH was added, Lt; / RTI > After adding 400 mL of H 3 PO 4 and stirring at room temperature for 1 hour, the reaction is neutralized with NaOH and extracted with distilled water and ethyl acetate. The organic layer was dried over MgSO 4 and the solvent was removed. The solvent was removed by column separation using hexane and ethyl acetate to obtain 7,7,13,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b ] acridine (yield: 74%).
1H-NMR: δ 1.72 (s, 12H), 4.00(s, 1H), 6.67(s, 1H), 6.73-6.75(d, 2H), 7.02-7.05(t, 2H), 7.28-7.38 (t, 2H), 7.46(s, 1H) 7.55-7.60(d, 2H) 1 H-NMR: δ 1.72 ( s, 12H), 4.00 (s, 1H), 6.67 (s, 1H), 6.73-6.75 (d, 2H), 7.02-7.05 (t, 2H), 7.28-7.38 (t , 2H), 7.46 (s, 1 H) 7.55 - 7.60 (d, 2 H)
Elemental Analysis: C, 88.57; H, 7.12; N, 4.30 [M+] : 324Elemental Analysis: C, 88.57; H, 7.12; N, 4.30 [M < + >]: 324
A-2) 화합물 A-2의 합성A-2) Synthesis of Compound A-2
상기 화합물 A-1의 합성에서 2-bromo-9,9-dimethyl-9,10-dihydroacridine 대신 2,7-dibromo-9,9-dimethyl-9,10-dihydroacridine을 사용한 것을 제외하고는 동일한 방법으로 합성한다.Except that 2,7-dibromo-9,9-dimethyl-9,10-dihydroacridine was used instead of 2-bromo-9,9-dimethyl-9,10-dihydroacridine in the synthesis of the compound A-1. Synthesized.
A-3) 화합물 A-3의 합성A-3) Synthesis of Compound A-3
상기 화합물 A-1의 합성에서 methyl 2-bromobenzoate 대신 methyl 2-bromo-5-chlorobenzoate을 사용한 것을 제외하고는 동일한 방법으로 합성한다.The synthesis was carried out in the same manner except that methyl 2-bromo-5-chlorobenzoate was used instead of methyl 2-bromobenzoate in the synthesis of the compound A-1.
A-4) 화합물 A-4의 합성A-4) Synthesis of Compound A-4
상기 A-1의 합성에서 2-bromo-9,9-dimethyl-9,10-dihydroacridine 대신 2,7-dibromo-9,9-dimethyl-9,10-dihydroacridine을 사용하고, methyl 2-bromobenzoate 대신 methyl 2-bromo-5-chlorobenzoate를 사용한 것을 제외하고는 동일한 방법으로 합성한다.
In the synthesis of A-1 above, 2,7-dibromo-9,9-dimethyl-9,10-dihydroacridine was used instead of 2-bromo-9,9-dimethyl-9,10-dihydroacridine, and methyl 2-bromobenzoate 2-bromo-5-chlorobenzoate.
B. 화학식 C-2로 표시되는 화합물의 예로 화합물 B-1 내지 B-4 합성B. Examples of the compound represented by the formula C-2 include compounds B-1 to B-4
B-1) 화합물 B-1의 합성B-1) Synthesis of Compound B-1
상기 화합물 A-1의 합성에서 2-bromo-9,9-dimethyl-9,10-dihydroacridine 대신 3-bromo-9,9-dimethyl-9,10-dihydroacridine를 사용한 것을 제외하고는 동일한 방법으로 합성한다.Except that 3-bromo-9,9-dimethyl-9,10-dihydroacridine was used in place of 2-bromo-9,9-dimethyl-9,10-dihydroacridine in the synthesis of Compound A-1 .
B-2) 화합물 B-2의 합성B-2) Synthesis of Compound B-2
상기 화합물 A-2의 합성에서 2,7-dibromo-9,9-dimethyl-9,10-dihydroacridine 대신 3,6-dibromo-9,9-dimethyl-9,10-dihydroacridine를 사용한 것을 제외하고는 동일한 방법으로 합성한다.Except that 3,6-dibromo-9,9-dimethyl-9,10-dihydroacridine was used instead of 2,7-dibromo-9,9-dimethyl-9,10-dihydroacridine in the synthesis of Compound A- .
B-3) 화합물 B-3의 합성B-3) Synthesis of Compound B-3
상기 화합물 A-3의 합성에서 2-bromo-9,9-dimethyl-9,10-dihydroacridine 대신 3-bromo-9,9-dimethyl-9,10-dihydroacridine을 사용한 것을 제외하고는 동일한 방법으로 합성한다.Except that 3-bromo-9,9-dimethyl-9,10-dihydroacridine was used instead of 2-bromo-9,9-dimethyl-9,10-dihydroacridine in the synthesis of Compound A-3 .
B-4) 화합물 B-4의 합성B-4) Synthesis of Compound B-4
상기 화합물 A-4의 합성에서 2,7-dibromo-9,9,10,10-tetramethyl-9,10-dihydroanthracene 대신 3,6-dibromo-9,9-dimethyl-9,10-dihydroacridine를 사용하고, methyl 2-bromobenzoate 대신 methyl 2-bromo-5-chlorobenzoate를 사용한 것을 제외하고는 동일한 방법으로 합성한다.
3,6-dibromo-9,9-dimethyl-9,10-dihydroacridine was used instead of 2,7-dibromo-9,9,10,10-tetramethyl-9,10-dihydroanthracene in the synthesis of Compound A- , methyl 2-bromo-5-chlorobenzoate instead of methyl 2-bromobenzoate.
C. 화학식 C-3 내지 C-11로 표시되는 화합물 합성C. Synthesis of Compound Represented by Formulas C-3 to C-11
상기 화합물 A-1의 합성에서 2-bromo-9,9-dimethyl-9,10-dihydroacridine 대신 하기 표 1의 화합물을 사용한 것을 제외하고는 동일한 방법을 적용하여 화학식 C-3 내지 C-11에 해당되는 화합물을 얻을 수 있다.C-3 to C-11 were obtained by the same method except that 2-bromo-9,9-dimethyl-9,10-dihydroacridine was used in the synthesis of the compound A-1, ≪ / RTI >
상기에 제시된 화합물 이외에 본 발명은 상기 합성방법을 참조하여 화학식 C-1 내지 C-11로 표시되는 여러 화합물들을 합성할 수 있다. 이러한 본 발명의 화학식 C-1 내지 C-11로 표시되는 화합물의 예(구체적으로는 화학식 C-1의 예)로 하기 화합물들(C1~C112)을 들 수 있지만, 이에 한정되지는 않는다.In addition to the compounds shown above, the present invention can synthesize various compounds represented by the formulas C-1 to C-11 with reference to the above synthesis method. Examples of the compounds represented by formulas C-1 to C-11 of the present invention (specifically, examples of formula C-1) include, but are not limited to, the following compounds (C1 to C112).
한편, 본 발명에 따른 신규 화합물은 상기 화합물Ⅰ이 대칭 또는 비대칭으로 결합된 화합물일 수 있다. 즉, 본 발명에 따른 신규 화합물은 하기 화학식 2 내지 4로 표시되는 화합물로 이루어진 군에서 선택될 수 있다. 구체적으로, 화학식 2로 표시되는 화합물(이하, '화합물Ⅱ'라 함)은 화합물Ⅰ의 헤테로환 모이어티측끼리 결합된 것이고, 화학식 3으로 표시되는 화합물(이하, '화합물Ⅲ'이라 함)은 화합물Ⅰ의 헤테로환 모이어티측과 인덴계 화합물측이 결합된 것이고, 화학식 4로 표시되는 화합물(이하, '화합물Ⅳ'라 함)은 화합물Ⅰ의 인덴계 화합물측끼리 결합된 것이다.On the other hand, the novel compound according to the present invention may be a compound in which the compound I is bonded symmetrically or asymmetrically. That is, the novel compounds according to the present invention can be selected from the group consisting of compounds represented by the following formulas (2) to (4). Specifically, a compound represented by the formula (2) (hereinafter referred to as a 'compound II') is a compound in which the heterocyclic moieties of the compound I are bonded together, and the compound represented by the formula (3) (Hereinafter referred to as "compound IV") is a compound bonded to the indene compound side of Compound I, and the compound represented by Formula 4 (hereinafter referred to as Compound IV) is bonded to the indene compound side.
[화학식 2] (2)
[화학식 3] (3)
[화학식 4] [Chemical Formula 4]
상기 화학식 2 내지 4에서,In the above Chemical Formulas 2 to 4,
X, Y, R1 내지 R7, Ar1 내지 Ar3 및 a, b, c에 대해서는 상기 화학식 1로 표시되는 화합물에서 정의된 바와 동일하며,X, Y, R 1 to R 7 , Ar 1 to Ar 3 And a, b and c are the same as defined in the compound represented by the formula (1)
X' 및 Y'는 서로 같거나 다르고, CR3'R4'. O, S, NR5' 및 SiR6'R7'로 이루어진 군에서 선택되며, 단, X' 및 Y'가 모두 CR3'R4'인 경우는 제외되고;X 'and Y' are the same or different from each other, and CR 3 'R 4 '. O, S, NR 5 'and SiR 6 ' R 7 ', with the proviso that X' and Y 'are not CR 3 ' R 4 ';
R1' 내지 R7'는 서로 같거나 다르고, 수소, 중수소, 할로겐, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아미노기, C6~C40의 디아릴아미노기, C6~C40의 아릴알킬기, C3~C40의 시클로알킬기, C6~C40의 아릴실릴기 및 C3~C40의 헤테로시클로알킬기로 이루어진 군에서 선택되며;R 1 ' To R 7 'are the same or different from each other and represent hydrogen, deuterium, halogen, a C 1 to C 40 alkyl group, a C 2 to C 40 alkenyl group, a C 2 to C 40 alkynyl group, a C 6 to C 40 aryl group , A C 5 to C 40 heteroaryl group, a C 6 to C 40 aryloxy group, a C 1 to C 40 alkyloxy group, a C 6 to C 40 arylamino group, a C 6 to C 40 diarylamino group, A C 6 to C 40 arylalkyl group, a C 3 to C 40 cycloalkyl group, a C 6 to C 40 arylsilyl group, and a C 3 to C 40 heterocycloalkyl group;
Ar1' 내지 Ar3'는 서로 같거나 다르고, 수소, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C3~C40의 시클로알킬기, C3~C40의 헤테로시클로알킬기, C6~C40의 아릴기, C5~C60의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C40의 아릴옥시기, C6~C40의 아릴실릴기 및 C6~C40의 아릴아민기로 이루어진 군에서 선택되고;Ar 1 'to Ar 3 ' are the same or different from each other and represent hydrogen, deuterium, halogen, cyano, C 1 to C 40 alkyl, C 3 to C 40 cycloalkyl, C 3 to C 40 heterocycloalkyl, C an aryl group of 6 ~ C 40, C 5 ~ heteroaryl group of C 60, C 1 ~ C 40 alkyloxy group of, C aryloxy of 6 ~ C 40, C 6 ~ C 40 aryl silyl group, and a C 6 of ~ C 40 is selected from the group consisting of an aryl amine;
a', b' 및 c'는 0 내지 4의 정수이다.a ', b' and c 'are an integer of 0 to 4;
이러한 본 발명의 화합물Ⅱ 내지 Ⅳ는 상기 화합물Ⅰ을 기본단위로 포함하고 있기 때문에 화합물Ⅱ 내지 Ⅳ 중 어느 하나를 유기 전계 발광 소자의 재료로 사용할 경우에도 소자의 인광특성뿐만 아니라, 전자 및/또는 정공 수송 능력, 발광효율, 구동전압, 수명 특성 등이 개선될 수 있다. 이때, 본 발명의 화합물Ⅱ 내지 Ⅳ도 유기 전계 발광 소자의 유기물층의 재료, 바람직하게는 발광층, 정공수송층 또는 전자수송층의 재료, 보다 바람직하게는 발광층의 호스트 재료로 사용될 수 있다.Since the compounds II to IV of the present invention contain the compound I as a basic unit, even when any one of the compounds II to IV is used as the material of the organic electroluminescence device, the phosphorescence property of the device, as well as the electron and / Transporting ability, luminous efficiency, driving voltage, lifetime characteristics and the like can be improved. At this time, the compounds II to IV of the present invention can also be used as a material of an organic material layer of an organic electroluminescent device, preferably a material of a light emitting layer, a hole transporting layer or an electron transporting layer, more preferably a host material of a light emitting layer.
한편, 유기 전계 발광 소자의 효율 및 수명 특성 등을 고려할 때 상기 화합물Ⅱ 내지 Ⅳ에서 R1 및 R2는 서로 동일하며 메틸기 또는 페닐기이고, R1' 및 R2' 역시 서로 동일하며 메틸기 또는 페닐기인 것이 바람직하다. 또한, 상기 화합물Ⅱ 내지 Ⅳ에서 R3 및 R4는 서로 동일하며 메틸기 또는 페닐기이고, R3' 및 R4' 역시 서로 동일하며 메틸기 또는 페닐기인 것이 바람직하다. 여기서, R1 및 R2는 R1' 및 R2'와 서로 같거나 다를 수 있으며, R3 및 R4 또한 R3' 및 R4'와 서로 같거나 다를 수 있다. 또, 상기 화합물Ⅱ 내지 Ⅳ에서 R5 및 R5'는 C6~C40의 아릴기 또는 C5~C40의 헤테로아릴기인 것이 바람직하며, 서로 같거나 다를 수 있다.Considering the efficiency and lifetime characteristics of the organic electroluminescent device, R 1 and R 2 in the compounds II to IV are the same as each other and are a methyl group or a phenyl group, and R 1 'and R 2 ' are also the same and are a methyl group or a phenyl group . R 3 and R 4 in the compounds II to IV are the same as each other and are a methyl group or a phenyl group, and R 3 'and R 4 ' are also the same and are preferably a methyl group or a phenyl group. Here, R 1 and R 2 may be the same as or different from R 1 'and R 2 ', and R 3 and R 4 may also be the same as or different from R 3 'and R 4 '. In addition, in the compounds II to IV, R 5 and R 5 'are preferably a C 6 to C 40 aryl group or a C 5 to C 40 heteroaryl group, and they may be the same or different.
이러한 본 발명의 화합물Ⅱ 내지 Ⅳ는 상기 화합물Ⅰ의 합성과정(화학식 C-1 내지 C-11로 표시되는 화합물의 합성과정)을 참조하여 합성할 수 있는 것으로, 하기와 같은 화합물들(C113~C118)을 예로 들 수 있지만, 이에 한정되는 것은 아니다.The compounds II to IV of the present invention can be synthesized with reference to the synthesis process of the compound I (the process of synthesizing the compounds represented by the formulas C-1 to C-11), and the following compounds (C113 to C118 ), But the present invention is not limited thereto.
2. 유기 2. Organic 전계Field 발광 소자 Light emitting element
본 발명은 양극, 음극, 및 상기 양극과 음극 사이에 개재(介在)된 1층 이상의 유기물층을 포함하는 유기 전계 발광 소자를 제공하는데, 이때, 상기 1층 이상의 유기물층 중 적어도 하나는 상기 화학식 1 내지 4로 표시되는 화합물 중 어느 하나를 포함하는 유기물층인 것을 특징으로 한다.The present invention provides an organic electroluminescent device comprising a cathode, a cathode, and at least one organic layer sandwiched between the anode and the cathode, wherein at least one of the one or more organic layers is a compound represented by any one of formulas Is an organic material layer containing any one of the compounds represented by the following formulas.
본 발명의 화학식 1 내지 4로 표시되는 화합물 중 어느 하나의 화합물을 포함하는 유기물층은 정공주입층, 정공수송층, 발광층, 전자수송층 및 전자주입층 중 어느 하나 이상일 수 있다. 구체적으로, 상기 유기물층은 정공수송층, 발광층 또는 전자수송층인 것이 바람직하며, 발광층인 것이 더욱 바람직하다.The organic material layer containing any one of the compounds represented by the general formulas (1) to (4) of the present invention may be any one or more of a hole injecting layer, a hole transporting layer, a light emitting layer, an electron transporting layer and an electron injecting layer. Specifically, the organic material layer is preferably a hole transporting layer, a light emitting layer, or an electron transporting layer, more preferably a light emitting layer.
본 발명에 따른 유기 전계 발광 소자의 발광층은 호스트 재료를 함유할 수 있는데, 이때, 호스트 재료로 상기 화학식 1 내지 4로 표시되는 화합물 중 어느 하나를 사용할 수 있는 것이다. 이와 같이 발광층이 상기 화학식 1 내지 4로 표시되는 화합물 중 어느 하나를 함유할 경우 정공 수송 능력이 증가되어 발광층에서 정공과 전자의 결합력이 높아지기 때문에 효율(발광효율 및 전력효율), 수명, 휘도 및 구동전압 등이 우수한 유기 전계 발광 소자를 제공할 수 있다.The light emitting layer of the organic electroluminescent device according to the present invention may contain a host material. In this case, any one of the compounds represented by the above formulas 1 to 4 may be used as a host material. When the light emitting layer contains any one of the compounds represented by Chemical Formulas 1 to 4 as described above, the hole transporting ability is increased, and the bonding force between holes and electrons in the light emitting layer is increased. Therefore, efficiency (luminous efficiency and power efficiency), lifetime, It is possible to provide an organic electroluminescent device excellent in voltage and the like.
또한, 본 발명에 따른 유기 전계 발광 소자의 정공수송층은 상기 화학식 1 내지 4로 표시되는 화합물 중 어느 하나를 포함할 때 정공수송 능력이 우수해져 유기 전계 발광 소자의 특성을 향상시킬 수 있다. 여기서, 상기 화학식 1 내지 4로 표시되는 화합물 중 어느 하나가 정공수송층에 포함될 경우에는 화학식 1 내지 4의 Ar1, Ar1', Ar3 또는 Ar3'는 C6~C40의 아릴아민기인 것이 바람직하다.In addition, when the hole transport layer of the organic electroluminescent device according to the present invention includes any one of the compounds represented by the general formulas (1) to (4), the hole transporting ability is improved and the characteristics of the organic electroluminescent device can be improved. When any one of the compounds represented by Chemical Formulas 1 to 4 is included in the hole transporting layer, Ar 1 , Ar 1 ', and Ar 3 in Chemical Formulas 1 to 4 Or Ar 3 'is preferably a C 6 to C 40 arylamine group.
이러한 본 발명의 유기 전계 발광 소자의 구조는 특별히 한정되지 않으나, 비제한적인 예로 기판, 양극, 정공주입층, 정공수송층, 발광층, 전자수송층 및 음극이 순차적으로 적층된 구조로 이루어질 수 있다. 여기서, 전자수송층 위에는 전자주입층이 추가로 적층될 수도 있다. 또한, 본 발명에 따른 유기 전계 발광 소자는 양극, 1층 이상의 유기물층 및 음극이 순차적으로 적층된 구조뿐만 아니라, 전극과 유기물층 계면에 절연층 또는 접착층이 삽입된 구조로 이루어질 수 있다.The structure of the organic electroluminescent device of the present invention is not particularly limited, but may be a structure in which a substrate, an anode, a hole injecting layer, a hole transporting layer, a light emitting layer, an electron transporting layer, and a cathode are sequentially stacked. Here, the electron injection layer may be further stacked on the electron transporting layer. The organic electroluminescent device according to the present invention may have a structure in which an anode, one or more organic layers and an anode are sequentially stacked, and an insulating layer or an adhesive layer is interposed between the electrodes and the organic layer.
한편, 본 발명에 따른 유기 전계 발광 소자에 포함되는 양극으로 사용 가능한 물질은 특별히 한정되지 않으나, 비제한적인 예로 바나듐, 크롬, 구리, 아연, 금과 같은 금속 또는 이들의 합금; 아연산화물, 인듐산화물, 인듐 주석 산화물(ITO), 인듐 아연 산화물(IZO)과 같은 금속 산화물; ZnO:Al 또는 SnO2:Sb와 같은 금속과 산화물의 조합; 폴리티오펜, 폴리(3-메틸티오펜), 폴리[3,4-(에틸렌-1,2-디옥시)티오펜](PEDT), 폴리피롤 또는 폴리아닐린과 같은 전도성 고분자; 및 카본블랙 등을 사용할 수 있다.Examples of the material usable as the anode included in the organic electroluminescent device according to the present invention include, but are not limited to, metals such as vanadium, chromium, copper, zinc and gold or alloys thereof; Metal oxides such as zinc oxide, indium oxide, indium tin oxide (ITO), and indium zinc oxide (IZO); ZnO: Al or SnO 2: a combination of a metal and an oxide such as Sb; Conductive polymers such as polythiophene, poly (3-methylthiophene), poly [3,4- (ethylene-1,2-dioxy) thiophene] (PEDT), polypyrrole or polyaniline; And carbon black.
또한, 본 발명에 따른 유기 전계 발광 소자에 포함되는 음극으로 사용 가능한 물질은 특별히 한정되지 않으나, 비제한적인 예로 마그네슘, 칼슘, 나트륨, 칼륨, 타이타늄, 인듐, 이트륨, 리튬, 가돌리늄, 알루미늄, 은, 주석, 또는 납과 같은 금속 또는 이들의 합금; 및 LiF/Al 또는 LiO2/Al과 같은 다층 구조 물질 등을 사용할 수 있다.Examples of materials usable as a cathode included in the organic electroluminescent device according to the present invention include, but are not limited to, magnesium, calcium, sodium, potassium, titanium, indium, yttrium, lithium, gadolinium, Tin, or lead, or alloys thereof; And a multilayer structure material such as LiF / Al or LiO 2 / Al.
또, 본 발명에 따른 유기 전계 발광 소자에 포함되는 유기물층은 상기 화학식 1 내지 4로 표시되는 화합물 중 어느 하나의 화합물을 발광층, 정공수송층 또는 전자수송층에 사용하는 것을 제외하고는 당업계에 공지된 물질로 이루어질 수 있다.The organic material layer included in the organic electroluminescent device according to the present invention may be a material known in the art except for using any one of the compounds represented by Chemical Formulas 1 to 4 in the light emitting layer, the hole transporting layer, or the electron transporting layer. ≪ / RTI >
본 발명에 따른 유기 전계 발광 소자에 포함되는 기판으로 사용 가능한 물질은 특별히 한정되지 않으나, 비제한적인 예로 실리콘 웨이퍼, 석영, 유리판, 금속판, 플라스틱 필름 및 시트 등이 사용될 수 있다. Materials that can be used as the substrate included in the organic electroluminescent device according to the present invention are not particularly limited, but examples thereof include silicon wafers, quartz, glass plates, metal plates, plastic films and sheets.
이와 같은 본 발명의 유기 전계 발광 소자는 당업계에 공지된 방법으로 제조될 수 있으며, 이때, 유기물층에 포함되는 발광층은 진공 증착법이나 용액 도포법으로 제조될 수 있다. 여기서, 용액 도포법의 예로는 스핀 코팅, 딥코팅, 닥터 블레이딩, 잉크젯 프린팅 또는 열 전사법 등이 있으나, 이들에 한정되지 않는다.
The organic electroluminescent device of the present invention may be manufactured by a method known in the art, and the luminescent layer included in the organic material layer may be prepared by a vacuum evaporation method or a solution coating method. Examples of the solution coating method include, but are not limited to, spin coating, dip coating, doctor blading, inkjet printing, and thermal transfer.
이하 본 발명을 실시예를 통하여 상세히 설명하면 다음과 같다. 단, 하기 실시예는 본 발명을 예시하는 것일 뿐 본 발명이 하기 실시예에 의해 한정되는 것은 아니다.
Hereinafter, the present invention will be described in detail with reference to examples. However, the following examples are for illustrative purposes only and are not intended to limit the scope of the present invention.
[[ 합성예Synthetic example 1] 화합물 1의 합성 1] Synthesis of Compound 1
질소 하에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 8.125g(25.0mmol)과 2-bromo-1-phenyl-1H-benzo[d]imidazole 8.16g(30.0mmol), Pd2(dba)3 0.69g(0.75mmol), P(t-bu)3 1.22ml(2.52mmol), NaO(t-bu) 6.05g(63.01mmol)을 넣고 Toluene을 첨가 한 뒤 24시간 환류 교반하였다. 반응 종료 후 디클로로메탄으로 추출 및 MgSO4로 유기층을 건조시켰다. 실리카겔 필터 후에 Hexane:Mc 3:2 (v/v)으로 컬럼하여 화합물 1인 7,7,13,13-tetramethyl-5-(1-phenyl-1H-benzo[d]imidazol-2-yl)-7,13-dihydro-5H-indeno[1,2-b]acridine 5.81g(11.2mmol)(수율 45%)을 획득하였다.1-phenyl-1H-benzo [d] thiophene was obtained under nitrogen atmosphere by the same procedure as in Example 1 except that 8.125 g (25.0 mmol) of 7,7,13,13-tetramethyl-7,13-dihydro- 1.25 ml (2.50 mmol) of imidazole, 0.69 g (0.75 mmol) of Pd 2 (dba) 3 , 1.22 ml (2.52 mmol) of P (t-bu) 3 and 6.05 g (63.01 mmol) of NaO And the mixture was stirred under reflux for 24 hours. After completion of the reaction, the mixture was extracted with dichloromethane and the organic layer was dried over MgSO 4 . After silica gel filtration, the column was subjected to column chromatography with Hexane: Mc 3: 2 (v / v) to obtain Compound 1, 7,7,13,13-tetramethyl- 5- (1-phenyl-1H- benzo [d] imidazol- (11.2 mmol) (yield 45%) of 7,13-dihydro-5H-indeno [1,2-b] acridine.
Elemental Analysis: C, 85.85; H, 6.04; N, 8.12 [M+] : 516
Elemental Analysis: C, 85.85; H, 6.04; N, 8.12 [M < + >]: 516
[[ 합성예Synthetic example 2] 화합물 2의 합성 2] Synthesis of Compound 2
합성예 1에서 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 3-bromoquinoline을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Except that 3-bromoquinoline was used instead of 2-bromo-1-phenyl-1H-benzo [d] imidazole in Synthesis Example 1.
Elemental Analysis: C, 87.57; H, 6.24; N, 6.19 [M+] : 451
Elemental Analysis: C, 87.57; H, 6.24; N, 6.19 [M < + >]: 451
[[ 합성예Synthetic example 3] 화합물 3의 합성 3] Synthesis of Compound 3
합성예 1에서 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 2-bromo-4,6-diphenylpyridine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Synthesis Example 1 was repeated except that 2-bromo-4,6-diphenylpyridine was used instead of 2-bromo-1-phenyl-1H-benzo [d] imidazole.
Elemental Analysis: C, 88.77; H, 6.18; N, 5.05 [M+] : 553
Elemental Analysis: C, 88.77; H, 6.18; N, 5.05 [M < + >]: 553
[[ 합성예Synthetic example 4] 화합물 4의 합성 4] Synthesis of Compound 4
합성예 1에서 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 2-bromo-4,6-diphenyl-1,3,5-triazine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Except that 2-bromo-4,6-diphenyl-1,3,5-triazine was used instead of 2-bromo-1-phenyl-1H-benzo [d] imidazole in Synthesis Example 1 .
Elemental Analysis: C, 84.14; H, 5.79; N, 10.06 [M+] : 555
Elemental Analysis: C, 84.14; H, 5.79; N, 10.06 [M < + >]: 555
[[ 합성예Synthetic example 5] 화합물 5의 합성 5] Synthesis of Compound 5
합성예 1에서 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 3-bromo-9-phenyl-9H-carbazole을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Except that 3-bromo-9-phenyl-9H-carbazole was used instead of 2-bromo-1-phenyl-1H-benzo [d] imidazole in Synthesis Example 1.
Elemental Analysis: C, 89.01; H, 6.05; N, 4.94 [M+] : 565
Elemental Analysis: C, 89.01; H, 6.05; N, 4.94 [M < + >]: 565
[[ 합성예Synthetic example 6] 화합물 6의 합성 6] Synthesis of Compound 6
합성예 1에서 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 4-bromo-N,N-diphenylaniline을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Except that 4-bromo-N, N-diphenylaniline was used instead of 2-bromo-1-phenyl-1H-benzo [d] imidazole in Synthesis Example 1.
Elemental Analysis: C, 88.69; H, 6.38; N, 4.93 [M+] : 567
Elemental Analysis: C, 88.69; H, 6.38; N, 4.93 [M < + >]: 567
[[ 합성예Synthetic example 7] 화합물 7의 합성 7] Synthesis of Compound 7
합성예 1에서 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 2-bromo-5-phenylpyridine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Except that 2-bromo-5-phenylpyridine was used instead of 2-bromo-1-phenyl-1H-benzo [d] imidazole in Synthesis Example 1.
Elemental Analysis: C, 87.83; H, 6.32; N, 5.85 [M+] : 477
Elemental Analysis: C, 87.83; H, 6.32; N, 5.85 [M < + >]: 477
[[ 합성예Synthetic example 8] 화합물 8의 합성 8] Synthesis of Compound 8
합성예 1에서 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 2'-bromo-3,4'-bipyridine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Except that 2'-bromo-3,4'-bipyridine was used instead of 2-bromo-1-phenyl-1H-benzo [d] imidazole in Synthesis Example 1.
Elemental Analysis: C, 85.14; H, 6.09; N, 8.76 [M+] : 478
Elemental Analysis: C, 85.14; H, 6.09; N, 8.76 [M < + >]: 478
[[ 합성예Synthetic example 9] 화합물 9의 합성 9] Synthesis of Compound 9
합성예 1에서 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 9-(4-bromophenyl)-9H-carbazole을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Except that 9- (4-bromophenyl) -9H-carbazole was used instead of 2-bromo-1-phenyl-1H-benzo [d] imidazole in Synthesis Example 1.
Elemental Analysis: C, 89.01; H, 6.05; N, 4.94 [M+] : 565
Elemental Analysis: C, 89.01; H, 6.05; N, 4.94 [M < + >]: 565
[[ 합성예Synthetic example 10] 화합물 10의 합성 10] Synthesis of Compound 10
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 2-bromo-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine를 사용하고, 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 2-bromo-4,6-diphenylpyridine를 사용하는 것을 제외하고는 동일한 방법을 이용하여 2-bromo-5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine을 합성하였다.In Synthesis Example 1, 2-bromo-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2- except that 2-bromo-4,6-diphenylpyridine was used instead of 2-bromo-1-phenyl-1H-benzo [d] imidazole 2-yl) -7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine Were synthesized.
합성된 2-bromo-5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 7.71g(12.2mmol), 9-phenyl-3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-9H-carbazole 6.3g(1당량), tetrakis(triphenylphosphine)palladium(0) 0.7g(5 mol %), potassium carbonate 5g(3당량)을 1,4-dioxane 61ml, H2O 18ml와 함께 250ml 둥근 플라스크에 넣고 질소 상태하에서 3시간 동안 환류 교반 시켰다. 반응 종료 후, 반응액을 Celite를 통해 Filter한 다음, 컬럼 크로마토그래피를 통하여 7.76g (9.76mmol)(수득율:80%)의 화합물 10을 합성하였다. A solution of the synthesized 2-bromo-5- (4,6-diphenylpyridin-2-yl) -7,7,13,13-tetramethyl-7,13-dihydro- 6.3 g (1 eq.) Of tetrakis (triphenylphosphine) palladium (1 eq.), 9.2 g (5 mol%) and 5 g (3 eq.) Of potassium carbonate were placed in a 250 ml round-bottomed flask together with 61 ml of 1,4-dioxane and 18 ml of H 2 O and refluxed under nitrogen for 3 hours. After completion of the reaction, the reaction solution was filtered through Celite, and then 7.76 g (9.76 mmol) (yield: 80%) of Compound 10 was synthesized by column chromatography.
Elemental Analysis: C, 89.02; H, 5.70; N, 5.28 [M]+: 794
Elemental Analysis: C, 89.02; H, 5.70; N, 5.28 [M] < + >: 794
[[ 합성예Synthetic example 11] 화합물 11의 합성 11] Synthesis of Compound 11
질소기류 하에서 2-bromo-5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 8.09g(12.8mmol), 4,4,4',4',5,5, 5',5'-octamethyl-2,2'-bi(1,3,2-dioxaborolane) 4.86g(19.1mmol), Pd(dppf)Cl2 0.52 g(5mol%), KOAc 3.75g(38.3mmol), DMF 50ml를 넣고 130℃에서 12h 교반한 후 반응을 종결시키고, 에틸아세테이트로 추출하여 MgSO4로 수분을 제거하였다. 용매를 제거한 반응물은 컬럼크로마토그래피(Hexane:EA = 10:1 (v/v))를 이용하여 5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-2-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-7,13-dihydro-5H-indeno[1,2-b]acridine 3.48g(5.12mol)(수율 40 %)을 획득하였다. To a solution of 8.09 g of 2-bromo-5- (4,6-diphenylpyridin-2-yl) -7,7,13,13-tetramethyl-7,13- dihydro-5H- indeno [ (12.8 mmol), 4,4,4 ', 4', 5,5,5 ', 5'-octamethyl-2,2'-bi (1,3,2-dioxaborolane), Pd (dppf) Cl 2 , 3.75 g (38.3 mmol) of KOAc and 50 ml of DMF were added. The mixture was stirred at 130 ° C for 12 hours, and the reaction was terminated. The reaction mixture was extracted with ethyl acetate and the water was removed with MgSO 4 . The solvent was removed and the residue was purified by column chromatography (Hexane: EA = 10: 1 (v / v)) to give 5- (4,6-diphenylpyridin-2-yl) -7,7,13,13-tetramethyl- - (4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl) -7,13-dihydro-5H- indeno [1,2- b] acridine 40%).
합성된 5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-2-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-7,13-dihydro-5H-indeno[1,2-b]acridine 3.48g(5.12mol), 2-bromo-5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 3.24g(1당량), tetrakis(triphenylphosphine)palladium(0) 0.35g(5 mol %), potassium carbonate 2.5g(3당량)을 1,4-dioxane 35ml, H2O 9ml와 함께 250ml 둥근 플라스크에 넣고 질소 상태하에서 3시간 동안 환류 교반시켰다. 반응 종료 후, 반응액을 Celite를 통해 Filter한 다음, 컬럼 크로마토그래피를 통하여 4.54g(4.10mmol)(수득율 : 80%)의 화합물 11을 합성하였다.Synthesis of 5- (4,6-diphenylpyridin-2-yl) -7,7,13,13-tetramethyl-2- (4,4,5,5-tetramethyl-1,3,2-dioxaborolan- ), 7,13-dihydro-5H-indeno [1,2-b] acridine, 3.48 g (5.12 mol), 2-bromo-5- (4,6-diphenylpyridin- 3.24 g (1 equivalent) of tetrakis (triphenylphosphine) palladium (0), 0.35 g (5 mol%) of potassium carbonate, 2.5 g (3 mol) of 13-tetramethyl-7,13-dihydro- Equivalent) were placed in a 250 ml round-bottomed flask together with 35 ml of 1,4-dioxane and 9 ml of H 2 O, and the mixture was stirred under reflux for 3 hours under a nitrogen atmosphere. After completion of the reaction, the reaction solution was filtered through Celite, and then 4.54 g (4.10 mmol) (yield: 80%) of Compound 11 was synthesized by column chromatography.
Elemental Analysis: C, 88.93; H, 6.01; N, 5.06 [M+]: 1105
Elemental Analysis: C, 88.93; H, 6.01; N, 5.06 [M < + >]: 1105
[[ 합성예Synthetic example 12] 화합물 12의 합성 12] Synthesis of Compound 12
합성예 4에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 9-chloro-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 을 사용한 것을 제외하고 동일한 방법을 이용하여 합성하였다.9-chloro-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine was used in place of 7,7,13,13- dihydro-5H-indeno [1,2-b] acridine was used as the starting material.
이후, 이를 이용하여 합성예 10에서 9-phenyl-3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-9H-carbazole 대신 9-(4-(pyridin-2-yl)phenyl)-3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-9H-carbazole을 사용한 것을 제외하고 동일한 방법을 이용하여 화합물 12를 합성하였다.9- (4- (pyridin-2-yl) -9H-carbazole was used in place of 9-phenyl-3- (4,4,5,5-tetramethyl-1,3,2-dioxaborolan- -2-yl) phenyl) -3- (4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl) -9H-carbazole. Were synthesized.
Elemental Analysis: C, 85.10; H, 5.30; N, 9.60 [M+]: 873
Elemental Analysis: C, 85.10; H, 5.30; N, 9.60 [M < + >]: 873
[[ 합성예Synthetic example 13] 화합물 13의 합성 13] Synthesis of Compound 13
합성예 12에서 9-(4-(pyridin-2-yl)phenyl)-3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-9H-carbazole 대신 합성예 11의 중간체인 5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-2-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-7,13-dihydro-5H-indeno[1,2-b]acridine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Synthesis instead of 9- (4- (pyridin-2-yl) phenyl) -3- (4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2- (4,6-diphenylpyridin-2-yl) -7,7,13,13-tetramethyl-2- (4,4,5,5-tetramethyl-1,3,2-dioxaborolan- 2-yl) -7,13-dihydro-5H-indeno [1,2-b] acridine was used as the starting material.
Elemental Analysis: C, 86.61; H, 5.81; N, 7.58 [M+]: 1107
Elemental Analysis: C, 86.61; H, 5.81; N, 7.58 [M < + >]: 1107
[[ 합성예Synthetic example 14] 화합물 14의 합성 14] Synthesis of Compound 14
합성예 11에서 2-bromo-5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 9-chloro-5-(4,6-diphenyl-1,3,5-triazin-2-yl)-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Instead of 2-bromo-5- (4,6-diphenylpyridin-2-yl) -7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2- b] acridine in Synthesis Example 11 9-chloro-5- (4,6-diphenyl-1,3,5-triazin-2-yl) -7,7,13,13-tetramethyl-7,13- dihydro-5H- indeno [ b] acridine was used as the starting material.
Elemental Analysis: C, 84.29; H, 5.62; N, 10.08 [M+]: 1109
Elemental Analysis: C, 84.29; H, 5.62; N, 10.08 [M < + >]: 1109
[[ 합성예Synthetic example 15] 화합물 15의 합성 15] Synthesis of compound 15
합성예 10에서 2-bromo-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 2-bromo-10-chloro-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 을 사용한 것을 제외하고는 동일한 방법을 이용하여 10-chloro-5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-2-(9-phenyl-9H-carbazol-3-yl)-7,13-dihydro-5H-indeno[1,2-b]acridine을 합성하였다.Bromo-10-chloro-7,7,13,13-dihydro-5H-indeno [1,2-b] acridine was used in place of 2-bromo-7,7,13,13-tetramethyl- 5-chloro-5- (4,6-diphenylpyridin-2-yl) - 1, 3-dicarboxylic acid dihydrochloride was prepared using the same procedure except that 13-tetramethyl-7,13-dihydro- Synthesis of 7,7,13,13-tetramethyl-2- (9-phenyl-9H-carbazol-3-yl) -7,13-dihydro-5H-indeno [1,2-b] acridine.
NaH 0.47g(19.6mmol)을 질소 하에서 25ml DMF 에 넣어 교반하였다. 여기에 DMF 100ml에 녹인 9H-carbazole 1.32g(7.85mmol)을 천천히 첨가하고 1시간 가량 교반하였다. 이어서 DMF 100ml에 녹인 10-chloro-5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-2-(9-phenyl-9H-carbazol-3-yl)-7,13-dihydro-5H-indeno[1,2-b]acridine 13.0g(15.7mmol)을 천천히 첨가하고 12시간 동안 교반하였다.0.47 g (19.6 mmol) of NaH was added to 25 ml of DMF under nitrogen and the mixture was stirred. 1.32 g (7.85 mmol) of 9H-carbazole dissolved in 100 ml of DMF was slowly added thereto, followed by stirring for about 1 hour. Then, 10-chloro-5- (4,6-diphenylpyridin-2-yl) -7,7,13,13-tetramethyl-2- (9- , 13-dihydro-5H-indeno [1,2-b] acridine (13.0 g, 15.7 mmol) was slowly added thereto and stirred for 12 hours.
반응 종료 후 혼합물을 실리카 필터하고 물과 메탄올로 Washing후에 용매를 제거하여 3.39g(3.53mmol)(수율 45%)의 화합물 15를 합성하였다.After completion of the reaction, the mixture was filtered through silica, washed with water and methanol, and then the solvent was removed to obtain 3.39 g (3.53 mmol) (yield 45%) of Compound 15.
Elemental Analysis: C, 88.72; H, 5.45; N, 5.83 [M+]: 959
Elemental Analysis: C, 88.72; H, 5.45; N, 5.83 [M < + >]: 959
[[ 합성예Synthetic example 16] 화합물 16의 합성 16] Synthesis of Compound 16
합성예 15에서 2-bromo-4,6-diphenylpyridine 대신 bromobenzene를 사용하고, 9H-carbazole 대신 diphenylamine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다. Synthesis Example 15 was synthesized using bromobenzene instead of 2-bromo-4,6-diphenylpyridine and diphenylamine instead of 9H-carbazole.
Elemental Analysis: C, 88.74; H, 6.08; N, 5.17 [M+]: 810
Elemental Analysis: C, 88.74; H, 6.08; N, 5.17 [M < + >]: 810
[[ 합성예Synthetic example 17] 화합물 17의 합성 17] Synthesis of Compound 17
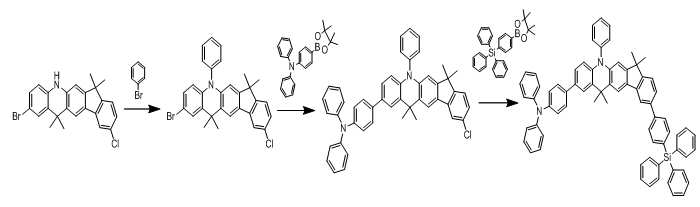
합성예 16에서 diphenylamine 대신 triphenyl(4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl)silane을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다. Synthesis Example 16 was synthesized in the same manner except that triphenyl (4- (4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl) phenyl) silane was used instead of diphenylamine.
Elemental Analysis: C, 88.30; H, 5.97; N, 2.86; Si, 2.87 [M+]: 977
Elemental Analysis: C, 88.30; H, 5.97; N, 2.86; Si, 2.87 [M < + >]: 977
[[ 합성예Synthetic example 18] 화합물 18의 합성 18] Synthesis of compound 18
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 상기 화합물 B-1을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다. Except that Compound B-1 was used instead of 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine in Synthesis Example 1 .
Elemental Analysis: C, 85.85; H, 6.04; N, 8.12 [M+] : 516
Elemental Analysis: C, 85.85; H, 6.04; N, 8.12 [M < + >]: 516
[[ 합성예Synthetic example 19] 화합물 19의 합성 19] Synthesis of Compound 19
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 상기 화합물 B-1를 사용하고, 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 3-bromoquinoline을 사용한 것을 제외하고 동일한 방법을 이용하여 합성하였다. The compound B-1 was used instead of 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine in Synthesis Example 1, and 2-bromo- -benzo [d] imidazole was used instead of 3-bromoquinoline.
Elemental Analysis: C, 87.57; H, 6.24; N, 6.19 [M+] : 451
Elemental Analysis: C, 87.57; H, 6.24; N, 6.19 [M < + >]: 451
[[ 합성예Synthetic example 20] 화합물 20의 합성 20] Synthesis of Compound 20
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 상기 화합물 B-1를 사용하고 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 2-bromo-4,6-diphenylpyridine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다. The compound B-1 was used instead of 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine in Synthesis Example 1 and 2-bromo- benzo [d] imidazole was used instead of 2-bromo-4,6-diphenylpyridine.
Elemental Analysis: C, 88.77; H, 6.18; N, 5.05 [M+] : 553Elemental Analysis: C, 88.77; H, 6.18; N, 5.05 [M < + >]: 553
[[ 합성예Synthetic example 21] 화합물 21의 합성 21] Synthesis of Compound 21
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 상기 화합물 B-1를 사용하고, 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 2-bromo-4,6-diphenyl-1,3,5-triazine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다. The compound B-1 was used instead of 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine in Synthesis Example 1, and 2-bromo- -benzo [d] imidazole was used instead of 2-bromo-4,6-diphenyl-1,3,5-triazine.
Elemental Analysis: C, 84.14; H, 5.79; N, 10.06 [M+] : 555
Elemental Analysis: C, 84.14; H, 5.79; N, 10.06 [M < + >]: 555
[[ 합성예Synthetic example 22] 화합물 22의 합성 22] Synthesis of Compound 22
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 상기 화합물 B-1를 사용하고, 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 3-bromo-9-phenyl-9H-carbazole을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다. The compound B-1 was used instead of 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine in Synthesis Example 1, and 2-bromo- -benzo [d] imidazole was used instead of 3-bromo-9-phenyl-9H-carbazole.
Elemental Analysis: C, 89.01; H, 6.05; N, 4.94 [M+] : 565
Elemental Analysis: C, 89.01; H, 6.05; N, 4.94 [M < + >]: 565
[[ 합성예Synthetic example 23] 화합물 23의 합성 23] Synthesis of Compound 23
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 상기 화합물 B-1를 사용하고, 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 4-bromo-N,N-diphenylaniline을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다. The compound B-1 was used instead of 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine in Synthesis Example 1, and 2-bromo- -benzo [d] imidazole was used instead of 4-bromo-N, N-diphenylaniline.
Elemental Analysis: C, 88.69; H, 6.38; N, 4.93 [M+] : 567
Elemental Analysis: C, 88.69; H, 6.38; N, 4.93 [M < + >]: 567
[[ 합성예Synthetic example 24] 화합물 24의 합성 24] Synthesis of Compound 24
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 상기 화합물 B-1를 사용하고, 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 2-bromo-5-phenylpyridine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.The compound B-1 was used instead of 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine in Synthesis Example 1, and 2-bromo- -benzo [d] imidazole was used instead of 2-bromo-5-phenylpyridine.
Elemental Analysis: C, 87.83; H, 6.32; N, 5.85 [M+] : 477
Elemental Analysis: C, 87.83; H, 6.32; N, 5.85 [M < + >]: 477
[[ 합성예Synthetic example 25] 화합물 25의 합성 25] Synthesis of Compound 25
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 상기 화합물 B-1를 사용하고, 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 2'-bromo-3,4'-bipyridine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.The compound B-1 was used instead of 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine in Synthesis Example 1, and 2-bromo- -benzo [d] imidazole was used instead of 2'-bromo-3,4'-bipyridine.
Elemental Analysis: C, 85.14; H, 6.09; N, 8.76 [M+] : 478
Elemental Analysis: C, 85.14; H, 6.09; N, 8.76 [M < + >]: 478
[[ 합성예Synthetic example 26] 화합물 26의 합성 26] Synthesis of Compound 26
합성예 1에서 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 상기 화합물 B-1를 사용하고, 2-bromo-1-phenyl-1H-benzo[d]imidazole 대신 9-(4-bromophenyl)-9H-carbazole을 사용한 것을 제외하고 동일한 방법을 이용하여 합성하였다.The compound B-1 was used instead of 7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine in Synthesis Example 1, and 2-bromo- -benzo [d] imidazole was used instead of 9- (4-bromophenyl) -9H-carbazole.
Elemental Analysis: C, 89.01; H, 6.05; N, 4.94 [M+] : 565
Elemental Analysis: C, 89.01; H, 6.05; N, 4.94 [M < + >]: 565
[[ 합성예Synthetic example 27] 화합물 27의 합성 27] Synthesis of Compound 27
합성예 10에서 상기 화합물 A-2 대신 상기 화합물 B-2을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Synthesis Example 10 was synthesized in the same manner except that Compound B-2 was used instead of Compound A-2.
Elemental Analysis: C, 89.02; H, 5.70; N, 5.28 [M]+: 794
Elemental Analysis: C, 89.02; H, 5.70; N, 5.28 [M] < + >: 794
[[ 합성예Synthetic example 28] 화합물 28의 합성 28] Synthesis of compound 28
합성예 11에서 2-bromo-5-(4,6-diphenylpyridin-2-yl)-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 2-bromo-5-(4,6-diphenylpyridin-2-yl)-11,11,13,13-tetramethyl-11,13-dihydro-5H-indeno[2,1-b]acridine을 사용한 것을 제외하고는 동일한 방법으로 합성하였다.Instead of 2-bromo-5- (4,6-diphenylpyridin-2-yl) -7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2- b] acridine in Synthesis Example 11 Except that 2-bromo-5- (4,6-diphenylpyridin-2-yl) -11,11,13,13-tetramethyl-11,13-dihydro-5H-indeno [2,1- Were synthesized in the same manner.
Elemental Analysis: C, 88.93; H, 6.01; N, 5.06 [M+]: 1105
Elemental Analysis: C, 88.93; H, 6.01; N, 5.06 [M < + >]: 1105
[[ 합성예Synthetic example 29] 화합물 29의 합성 29] Synthesis of Compound 29
합성예 12에서 상기 화합물 A-3 대신 상기 화합물 B-3을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Synthesis Example 12 was synthesized in the same manner except that Compound B-3 was used instead of Compound A-3.
Elemental Analysis: C, 85.10; H, 5.30; N, 9.60 [M+]: 873
Elemental Analysis: C, 85.10; H, 5.30; N, 9.60 [M < + >]: 873
[[ 합성예Synthetic example 30] 화합물 30의 합성 30] Synthesis of Compound 30
합성예 13에서 상기 화합물 A-3 대신 상기 화합물 B-3을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Synthesis Example 13 was synthesized in the same manner except that Compound B-3 was used instead of Compound A-3.
Elemental Analysis: C, 86.61; H, 5.81; N, 7.58 [M+]: 1107
Elemental Analysis: C, 86.61; H, 5.81; N, 7.58 [M < + >]: 1107
[[ 합성예Synthetic example 31] 화합물 31의 합성 31] Synthesis of Compound 31
합성예 14에서 상기 화합물 A-3 대신 상기 화합물 B-3을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Synthesis Example 14 was synthesized in the same manner except that Compound B-3 was used instead of Compound A-3.
Elemental Analysis: C, 84.29; H, 5.62; N, 10.08 [M+]: 1109
Elemental Analysis: C, 84.29; H, 5.62; N, 10.08 [M < + >]: 1109
[[ 합성예Synthetic example 32] 화합물 32의 합성 32] Synthesis of Compound 32
합성예 15에서 상기 화합물 A-4 대신 상기 화합물 B-4를 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Synthesis Example 15 was synthesized in the same manner except that Compound B-4 was used instead of Compound A-4.
Elemental Analysis: C, 88.72; H, 5.45; N, 5.83 [M+]: 959
Elemental Analysis: C, 88.72; H, 5.45; N, 5.83 [M < + >]: 959
[[ 합성예Synthetic example 33] 화합물 33의 합성 33] Synthesis of Compound 33
합성예 16에서 상기 화합물 A-4 대신 상기 화합물 B-4를 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Synthesis Example 16 was synthesized in the same manner except that Compound B-4 was used instead of Compound A-4.
Elemental Analysis: C, 88.74; H, 6.08; N, 5.17 [M+]: 810
Elemental Analysis: C, 88.74; H, 6.08; N, 5.17 [M < + >]: 810
[[ 합성예Synthetic example 34] 화합물 34의 합성 34] Synthesis of Compound 34
합성예 17에서 상기 화합물 A-4 대신 상기 화합물 B-4를 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Synthesis Example 17 was synthesized in the same manner except that Compound B-4 was used instead of Compound A-4.
Elemental Analysis: C, 88.30; H, 5.97; N, 2.86; Si, 2.87 [M+]: 977
Elemental Analysis: C, 88.30; H, 5.97; N, 2.86; Si, 2.87 [M < + >]: 977
[[ 합성예Synthetic example 35] 화합물 35의 합성 35] Synthesis of Compound 35
합성예 34에서 상기 화합물 B-4 대신 3-bromo-8-chloro-11,11-dimethyl-11,13-dihydro-5H-indeno[1,2-b]phenazine를 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.The same procedure was followed except that 3-bromo-8-chloro-11,11-dimethyl-11,13-dihydro-5H-indeno [1,2-b] phenazine was used instead of the compound B-4 in Synthesis Example 34 Respectively.
Elemental Analysis: C, 87.87; H, 5.62; N, 6.51 [M+]: 859
Elemental Analysis: C, 87.87; H, 5.62; N, 6.51 [M < + >]: 859
[[ 합성예Synthetic example 36] 화합물 36의 합성 36] Synthesis of Compound 36
합성예 10에서 2-bromo-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 3-bromo-11,11-dimethyl-11,13-dihydro-5H-indeno[1,2-b]phenazine, 2-bromo-4,6-diphenylpyridine 대신 2-bromonaphthalene을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Bromo-11,11-dimethyl-11,13-dihydro-5H-indeno [1,2-b] acridine was used in place of 2-bromo-7,7,13,13-tetramethyl- dihydro-5H-indeno [1,2-b] phenazine and 2-bromo-4,6-diphenylpyridine instead of 2-bromonaphthalene.
Elemental Analysis: C, 89.48; H, 5.22; N, 5.31 [M+]: 790
Elemental Analysis: C, 89.48; H, 5.22; N, 5.31 [M < + >]: 790
[[ 합성예Synthetic example 37] 화합물 37의 합성 37] Synthesis of Compound 37
합성예 10에서 2-bromo-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 3-bromo-11,11-dimethyl-11,13-dihydroindeno[2,1-b]phenoxazine를 사용하고, 2-bromo-4,6-diphenylpyridine 대신 2-(3-bromophenyl)pyridine를 사용하며, 9-phenyl-3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-9H-carbazole 대신 9-(4,6-diphenyl-1,3,5-triazin-2-yl)-3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-9H-carbazole을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.Bromo-11,11-dimethyl-11,13-dihydro-5H-indeno [1,2-b] acridine was used in place of 2-bromo-7,7,13,13-tetramethyl- (3-bromophenyl) pyridine was used instead of 2-bromo-4,6-diphenylpyridine and 9-phenyl-3- (4,4,5,5- (4,6-diphenyl-1,3,5-triazin-2-yl) -3- (4,4,5-tetramethyl-1,3,2-dioxaborolan- 5-tetramethyl-1,3,2-dioxaborolan-2-yl) -9H-carbazole.
Elemental Analysis: C, 83.47; H, 4.75; N, 9.90; O, 1.88 [M+]: 847
Elemental Analysis: C, 83.47; H, 4.75; N, 9.90; O, 1.88 [M < + >]: 847
[[ 합성예Synthetic example 38] 화합물 38의 합성 38] Synthesis of Compound 38
합성예 37에서 3-bromo-11,11-dimethyl-11,13-dihydroindeno[2,1-b]phenoxazine 대신 3-bromo-11,11-dimethyl-11,13-dihydroindeno[2,1-b]phenothiazine를 사용하고, 2-(3-bromophenyl)pyridine 대신 2,2'-(5-bromo-1,3-phenylene)dipyridine을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.3-bromo-11,11-dimethyl-11,13-dihydroindeno [2,1-b] pyridine was used instead of 3-bromo-11,11-dimethyl-11,13-dihydroindeno [ phenothiazine was used and 2,2 '- (5-bromo-1,3-phenylene) dipyridine was used instead of 2- (3-bromophenyl) pyridine.
Elemental Analysis: C, 81.59; H, 4.60; N, 10.41; S, 3.40 [M+]: 940
Elemental Analysis: C, 81.59; H, 4.60; N, 10.41; S, 3.40 [M < + >]: 940
[[ 합성예Synthetic example 39] 화합물 39의 합성 39] Synthesis of Compound 39
합성예 12에서 9-chloro-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno[1,2-b]acridine 대신 9-chloro-7,7,13,13-tetramethyl-7,13-dihydro-5H-benzo[b]fluoreno[3,2-e][1,4]azasiline을 사용한 것을 제외하고는 동일한 방법을 이용하여 합성하였다.9-chloro-7,7,13,13-tetramethyl-7,13-dihydro-5H-indeno [1,2-b] acridine was used in place of 9-chloro-7,7,13,13- 7,13-dihydro-5H-benzo [b] fluoreno [3,2-e] [1,4] azasiline.
Elemental Analysis: C, 84.53; H, 5.32; N, 7.25; Si, 2.91 [M+]: 964
Elemental Analysis: C, 84.53; H, 5.32; N, 7.25; Si, 2.91 [M < + >]: 964
[[ 실시예Example 1 내지 39] 유기 1 to 39] Organic 전계Field 발광 소자의 제조 Manufacturing of light emitting device
합성예 1 내지 39에서 합성된 화합물을 고순도 승화정제를 한 후, 이들 화합물을 각각 사용하여 아래의 과정에 따라 녹색 유기 전계 발광 소자를 제작하였다.The compounds synthesized in Synthesis Examples 1 to 39 were subjected to high-purity sublimation purification and each of these compounds was used to prepare a green organic electroluminescent device according to the following procedure.
ITO (Indium tin oxide)가 1500A 두께로 박막 코팅된 유리 기판을 증류수 초음파로 세척하였다. 증류수 세척이 끝나면 이소프로필 알코올, 아세톤, 메탄올 등의 용제로 초음파 세척을 하고 건조시킨 후 UV OZONE 세정기 (Power sonic 405, 화신테크)로 이송시킨 다음 UV를 이용하여 상기 기판을 5분간 세정한 후 진공 증착기로 기판을 이송하였다.The glass substrate coated with ITO (Indium tin oxide) thin film with thickness of 1500A was washed with distilled water ultrasonic wave. After the distilled water was washed, it was ultrasonically washed with a solvent such as isopropyl alcohol, acetone, methanol, dried, and then transferred to a UV OZONE cleaner (Power Sonic 405, Hoshin Tech). Then, the substrate was cleaned using UV for 5 minutes, The substrate was transferred to an evaporator.
이렇게 준비된 ITO 투명 전극 위에 m-MTDATA(60nm)/TCTA(80nm)/합성예 1 내지 39의 화합물을 각각 적용 + 10% Ir(ppy)3(300nm)/BCP(10nm)/Alq3(30nm)/LiF(1nm)/Al(200 nm) 의 구조를 가지는 유기 전계 발광 소자를 제조하였다. + 10% Ir (ppy) 3 (300 nm) / BCP (10 nm) / Alq 3 (30 nm) were respectively applied to the ITO transparent electrode prepared above, m-MTDATA (60 nm) / TCTA / LiF (1 nm) / Al (200 nm).
이때, m-MTDATA, TCTA, Ir(ppy)3 및 BCP의 구조는 하기와 같다.At this time, the structures of m-MTDATA, TCTA, Ir (ppy) 3 and BCP are as follows.
[[ 비교예Comparative Example ] 유기 ] Organic 전계Field 발광 소자의 제조 Manufacturing of light emitting device
발광층 형성시 합성예 1 내지 39에서 합성된 화합물 대신 하기 구조를 가지는 CBP를 발광호스트 물질로 사용한 것을 제외하고는, 상기 실시예 1 내지 39와 동일한 방법으로 유기 전계 발광 소자를 제작하였다.An organic electroluminescent device was fabricated in the same manner as in Examples 1 to 39 except that CBP having the following structure was used as a light emitting host material in place of the compound synthesized in Synthesis Examples 1 to 39 in the formation of a light emitting layer.
[[ 평가예Evaluation example ]]
실시예 1 내지 39 및 비교예에서 제조된 유기 전계 발광 소자에 대하여 구동전압, 전류효율 및 발광 피크를 측정하고, 그 결과를 하기 표 2에 나타내었다.The driving voltage, current efficiency and emission peak were measured for the organic electroluminescent devices manufactured in Examples 1 to 39 and Comparative Examples, and the results are shown in Table 2 below.
전압(V)Driving
Voltage (V)
(nm)EL peak
(nm)
(cd/A)Current efficiency
(cd / A)
상기 표2의 결과로부터 알 수 있는 바와 같이, 본 발명에 따른 화합물을 녹색 유기 전계 발광 소자의 발광층으로 사용하였을 경우(실시예 1 내지 39) 종래 CBP를 사용한 녹색 유기 전계 발광 소자(비교예)와 대비하여 볼 때 효율 및 구동전압면에서 보다 우수한 성능을 나타내는 것을 확인할 수 있다.As can be seen from the results shown in Table 2, when the compound according to the present invention was used as a light emitting layer of a green organic electroluminescent device (Examples 1 to 39), a green organic electroluminescent device using a conventional CBP (Comparative Example) It can be seen that it shows superior performance in terms of efficiency and driving voltage.
Claims (12)
상기 화학식 C-1 내지 C-6에서,
R1 내지 R4, R6 및 R7는 서로 같거나 다르고, 수소, 중수소, 할로겐, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아미노기, C6~C40의 디아릴아미노기, C6~C40의 아릴알킬기, C3~C40의 시클로알킬기, C6~C40의 아릴실릴기 및 C3~C40의 헤테로시클로알킬기로 이루어진 군에서 선택되며,
R5는 C6~C40의 아릴기이고,
Ar1 내지 Ar3는 서로 같거나 다르고, 수소, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C3~C40의 시클로알킬기, C3~C40의 헤테로시클로알킬기, C6~C40의 아릴기, C5~C60의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C40의 아릴옥시기, C6~C40의 아릴실릴기 및 C6~C40의 아릴아민기로 이루어진 군에서 선택되며, 인접한 기와 융합하여 고리를 형성할 수 있고,
a, b 및 c는 0 내지 4의 정수이며,
상기 화학식 C-7 내지 C-11에서,
R1 내지 R4, R6 및 R7는 서로 같거나 다르고, 수소, 중수소, 할로겐, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아미노기, C6~C40의 디아릴아미노기, C6~C40의 아릴알킬기, C3~C40의 시클로알킬기, C6~C40의 아릴실릴기 및 C3~C40의 헤테로시클로알킬기로 이루어진 군에서 선택되며,
Ar1 내지 Ar3는 서로 같거나 다르고, 수소, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C3~C40의 시클로알킬기, C3~C40의 헤테로시클로알킬기, C6~C40의 아릴기, C5~C60의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C40의 아릴옥시기, C6~C40의 아릴실릴기 및 C6~C40의 아릴아민기로 이루어진 군에서 선택되고, 인접한 기와 융합하여 고리를 형성할 수 있으며,
a, b 및 c는 0 내지 4의 정수이다.A compound selected from the group consisting of compounds represented by the following formulas C-1 to C-11:
In the above formulas C-1 to C-6,
R 1 to R 4 , R 6 and R 7 are the same or different and each represents hydrogen, deuterium, halogen, C 1 to C 40 alkyl, C 2 to C 40 alkenyl, C 2 to C 40 alkynyl, C 6 ~ C 40 aryl group, C 5 ~ C 40 heteroaryl group, C 6 ~ C 40 of the aryloxy group, C 1 ~ C 40 alkyloxy group of, C 6 ~ C 40 aryl group, C 6 ~ of C 40 of the diarylamino group, is selected from the group consisting of a heterocycloalkyl group of C 6 ~ C 40 aryl group, C 3 ~ C 40 cycloalkyl group, C 6 ~ C 40 aryl silyl group and C 3 ~ C 40 of ,
R 5 is a C 6 to C 40 aryl group,
Ar 1 to Ar 3 are the same or different from each other, hydrogen, deuterium, halogen, cyano group, C 1 ~ C 40 alkyl group, C 3 ~ C 40 cycloalkyl group, C 3 ~ C 40 heterocycloalkyl group, C 6 ~ of C 6 to C 40 aryloxy groups, C 6 to C 40 arylsilyl groups and C 6 to C 40 aryl groups, C 5 to C 60 heteroaryl groups, C 1 to C 40 alkyloxy groups, C 6 to C 40 aryloxy groups, An arylamine group having 1 to 40 carbon atoms, and may be fused with adjacent groups to form a ring,
a, b and c are integers of 0 to 4,
In the above formulas C-7 to C-11,
R 1 to R 4 , R 6 and R 7 are the same or different and each represents hydrogen, deuterium, halogen, C 1 to C 40 alkyl, C 2 to C 40 alkenyl, C 2 to C 40 alkynyl, C 6 ~ C 40 aryl group, C 5 ~ C 40 heteroaryl group, C 6 ~ C 40 of the aryloxy group, C 1 ~ C 40 alkyloxy group of, C 6 ~ C 40 aryl group, C 6 ~ of C 40 of the diarylamino group, is selected from the group consisting of a heterocycloalkyl group of C 6 ~ C 40 aryl group, C 3 ~ C 40 cycloalkyl group, C 6 ~ C 40 aryl silyl group and C 3 ~ C 40 of ,
Ar 1 to Ar 3 are the same or different from each other, hydrogen, deuterium, halogen, cyano group, C 1 ~ C 40 alkyl group, C 3 ~ C 40 cycloalkyl group, C 3 ~ C 40 heterocycloalkyl group, C 6 ~ of C 6 to C 40 aryloxy groups, C 6 to C 40 arylsilyl groups and C 6 to C 40 aryl groups, C 5 to C 60 heteroaryl groups, C 1 to C 40 alkyloxy groups, C 6 to C 40 aryloxy groups, An arylamine group having 1 to 40 carbon atoms, and may be fused with an adjacent group to form a ring,
a, b and c are an integer of 0 to 4;
상기 R1 및 R2는 서로 동일하며, 메틸기 또는 페닐기인 것을 특징으로 하는 화합물.The method according to claim 1,
Wherein R 1 and R 2 are the same as each other and are a methyl group or a phenyl group.
상기 R3 및 R4는 서로 동일하며, 메틸기 또는 페닐기인 것을 특징으로 하는 화합물.The method according to claim 1,
Wherein R 3 and R 4 are the same as each other and are a methyl group or a phenyl group.
[화학식 2]
[화학식 3]
[화학식 4]
상기 화학식 2 내지 4에서,
X 및 Y는 서로 같거나 다르고, CR3R4, O, S, NR5, SiR6R7로 이루어진 군에서 선택되며, 단, X 및 Y가 모두 CR3R4인 경우는 제외되고,
R1 내지 R4, R6 및 R7는 서로 같거나 다르고, 수소, 중수소, 할로겐, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아미노기, C6~C40의 디아릴아미노기, C6~C40의 아릴알킬기, C3~C40의 시클로알킬기, C6~C40의 아릴실릴기 및 C3~C40의 헤테로시클로알킬기로 이루어진 군에서 선택되며,
R5는 C6~C40의 아릴기이고,
Ar1 내지 Ar3는 서로 같거나 다르고, 수소, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C3~C40의 시클로알킬기, C3~C40의 헤테로시클로알킬기, C6~C40의 아릴기, C5~C60의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C40의 아릴옥시기, C6~C40의 아릴실릴기 및 C6~C40의 아릴아민기로 이루어진 군에서 선택되며, 인접한 기와 융합하여 고리를 형성할 수 있고,
a, b 및 c는 0 내지 4의 정수이며,
X' 및 Y'는 서로 같거나 다르고, CR3'R4'. O, S, NR5' 및 SiR6'R7'로 이루어진 군에서 선택되며, 단, X' 및 Y'가 모두 CR3'R4'인 경우는 제외되고,
R1' 내지 R4', R6' 및 R7'는 서로 같거나 다르고, 수소, 중수소, 할로겐, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, C5~C40의 헤테로아릴기, C6~C40의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아미노기, C6~C40의 디아릴아미노기, C6~C40의 아릴알킬기, C3~C40의 시클로알킬기, C6~C40의 아릴실릴기 및 C3~C40의 헤테로시클로알킬기로 이루어진 군에서 선택되며,
R5' 는 C6~C40의 아릴기이고,
Ar1' 내지 Ar3'는 서로 같거나 다르고, 수소, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C3~C40의 시클로알킬기, C3~C40의 헤테로시클로알킬기, C6~C40의 아릴기, C5~C60의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C40의 아릴옥시기, C6~C40의 아릴실릴기 및 C6~C40의 아릴아민기로 이루어진 군에서 선택되며, 인접한 기와 융합하여 고리를 형성할 수 있고,
a', b' 및 c'는 0 내지 4의 정수이다.A compound selected from the group consisting of compounds represented by the following formulas (2) to (4):
(2)
(3)
[Chemical Formula 4]
In the above Chemical Formulas 2 to 4,
X and Y are the same or different and are selected from the group consisting of CR 3 R 4 , O, S, NR 5 and SiR 6 R 7 except that when X and Y are both CR 3 R 4 ,
R 1 to R 4 , R 6 and R 7 are the same or different and each represents hydrogen, deuterium, halogen, C 1 to C 40 alkyl, C 2 to C 40 alkenyl, C 2 to C 40 alkynyl, C 6 ~ C 40 aryl group, C 5 ~ C 40 heteroaryl group, C 6 ~ C 40 of the aryloxy group, C 1 ~ C 40 alkyloxy group of, C 6 ~ C 40 aryl group, C 6 ~ of C 40 of the diarylamino group, is selected from the group consisting of a heterocycloalkyl group of C 6 ~ C 40 aryl group, C 3 ~ C 40 cycloalkyl group, C 6 ~ C 40 aryl silyl group and C 3 ~ C 40 of ,
R 5 is a C 6 to C 40 aryl group,
Ar 1 to Ar 3 are the same or different from each other, hydrogen, deuterium, halogen, cyano group, C 1 ~ C 40 alkyl group, C 3 ~ C 40 cycloalkyl group, C 3 ~ C 40 heterocycloalkyl group, C 6 ~ of C 6 to C 40 aryloxy groups, C 6 to C 40 arylsilyl groups and C 6 to C 40 aryl groups, C 5 to C 60 heteroaryl groups, C 1 to C 40 alkyloxy groups, C 6 to C 40 aryloxy groups, An arylamine group having 1 to 40 carbon atoms, and may be fused with adjacent groups to form a ring,
a, b and c are integers of 0 to 4,
X 'and Y' are the same or different from each other, and CR 3 'R 4 '. O, S, NR 5 'and SiR 6 ' R 7 ', with the exception that when X' and Y 'are both CR 3 ' R 4 '
R 1 'to R 4 ', R 6 'and R 7 ' are the same or different and represent hydrogen, deuterium, halogen, C 1 to C 40 alkyl, C 2 to C 40 alkenyl, C 2 to C 40 A C 6 to C 40 aryl group, a C 5 to C 40 heteroaryl group, a C 6 to C 40 aryloxy group, a C 1 to C 40 alkyloxy group, a C 6 to C 40 arylamino group , consisting of a heterocycloalkyl group of C 6 ~ C 40 of the diarylamino group, C 6 ~ C 40 aryl group, C 3 ~ C 40 cycloalkyl group, C 6 ~ C 40 aryl silyl group and C 3 ~ C 40 of ≪ / RTI >
R 5 'is a C 6 to C 40 aryl group,
Ar 1 'to Ar 3 ' are the same or different from each other and represent hydrogen, deuterium, halogen, cyano, C 1 to C 40 alkyl, C 3 to C 40 cycloalkyl, C 3 to C 40 heterocycloalkyl, C an aryl group of 6 ~ C 40, C 5 ~ heteroaryl group of C 60, C 1 ~ C 40 alkyloxy group of, C aryloxy of 6 ~ C 40, C 6 ~ C 40 aryl silyl group, and a C 6 of To C 40 arylamine groups, and may be fused with adjacent groups to form a ring,
a ', b' and c 'are an integer of 0 to 4;
상기 R1 및 R2는 서로 동일하며,
상기 R1'및 R2'는 서로 동일하고,
상기 R1, R2, R1'및 R2'는 메틸기 또는 페닐기인 것을 특징으로 하는 화합물.The method according to claim 6,
The R 1 And R < 2 > are the same as each other,
Wherein R 1 'and R 2 ' are the same as each other,
Wherein R 1 , R 2 , R 1 'and R 2 ' are a methyl group or a phenyl group.
상기 R3 및 R4는 서로 동일하며,
상기 R3' 및 R4'는 서로 동일하고,
상기 R3, R4, R3' 및 R4'는 메틸기 또는 페닐기인 것을 특징으로 하는 화합물.The method according to claim 6,
The R 3 And R < 4 > are the same as each other,
R 3 'and R 4 ' are the same as each other,
Wherein R 3 , R 4 , R 3 'and R 4 ' are a methyl group or a phenyl group.
상기 유기물층 중 적어도 하나는 제1항, 제3항, 제4항, 제6항 내지 제8항 중 어느 한 항에 따른 화합물을 포함하는 유기물층인 것을 특징으로 하는 유기 전계 발광 소자.1. An organic electroluminescent device comprising an anode, a cathode, and at least one organic material layer interposed between the anode and the cathode,
Wherein at least one of the organic material layers is an organic material layer including a compound according to any one of claims 1, 3, 4, 6 to 8.
상기 화합물을 포함하는 유기물층은 발광층인 것을 특징으로 하는 유기 전계 발광 소자.11. The method of claim 10,
Wherein the organic compound layer containing the compound is a light emitting layer.
상기 화합물을 포함하는 유기물층은 정공 수송층인 것을 특징으로 하는 유기 전계 발광 소자.11. The method of claim 10,
Wherein the organic compound layer containing the compound is a hole transport layer.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020110131297A KR101390523B1 (en) | 2011-12-08 | 2011-12-08 | Novel compounds and organic electro luminescence device using the same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020110131297A KR101390523B1 (en) | 2011-12-08 | 2011-12-08 | Novel compounds and organic electro luminescence device using the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20130064601A KR20130064601A (en) | 2013-06-18 |
| KR101390523B1 true KR101390523B1 (en) | 2014-05-07 |
Family
ID=48861517
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020110131297A Expired - Fee Related KR101390523B1 (en) | 2011-12-08 | 2011-12-08 | Novel compounds and organic electro luminescence device using the same |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR101390523B1 (en) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20130118269A (en) * | 2012-04-19 | 2013-10-29 | 에스에프씨 주식회사 | Aromatic compound and organoelectroluminescent device comprising the compound |
| KR102058262B1 (en) * | 2012-09-03 | 2019-12-20 | 호도가야 가가쿠 고교 가부시키가이샤 | Compound having indeno acridan ring structure, and organic electroluminescence |
| WO2014112360A1 (en) * | 2013-01-17 | 2014-07-24 | 保土谷化学工業株式会社 | Compound having indeno acridan ring structure, and organic electroluminescent element |
| KR102317448B1 (en) | 2014-07-17 | 2021-10-28 | 삼성디스플레이 주식회사 | Condensed-cyclic compound and organic light-emitting device including the same |
| CN105968045B (en) * | 2016-07-20 | 2018-12-25 | 长春海谱润斯科技有限公司 | A kind of nitrogen-containing heterocycle analog derivative and its preparation method and application |
| KR102075732B1 (en) * | 2017-09-12 | 2020-02-10 | 주식회사 엘지화학 | Novel hetero-cyclic compound and organic light emitting device comprising the same |
| WO2019054634A1 (en) * | 2017-09-12 | 2019-03-21 | 주식회사 엘지화학 | Novel heterocyclic compound and organic light-emitting device using same |
| KR102103506B1 (en) * | 2017-10-18 | 2020-04-22 | 주식회사 엘지화학 | Novel hetero-cyclic compound and organic light emitting device comprising the same |
| WO2019078462A1 (en) * | 2017-10-18 | 2019-04-25 | 주식회사 엘지화학 | Novel heterocyclic compound and organic light-emitting device using same |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011000455A1 (en) * | 2009-06-30 | 2011-01-06 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
-
2011
- 2011-12-08 KR KR1020110131297A patent/KR101390523B1/en not_active Expired - Fee Related
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011000455A1 (en) * | 2009-06-30 | 2011-01-06 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20130064601A (en) | 2013-06-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101390523B1 (en) | Novel compounds and organic electro luminescence device using the same | |
| KR101452578B1 (en) | Novel compounds and organic electro luminescence device using the same | |
| KR102263822B1 (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR101298397B1 (en) | Organic lightemitting compound and organic electroluminescent device using the same | |
| KR101601356B1 (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR20150047858A (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR102508486B1 (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR101729372B1 (en) | Organic compound and organic electroluminescent device comprising the same | |
| KR101571592B1 (en) | Organic compound and organic electroluminescent device comprising the same | |
| KR101561338B1 (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR20150008678A (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR102530095B1 (en) | Organic light-emitting compound and organic electroluminescent device using the same | |
| KR102559589B1 (en) | Organic compound and organic electroluminescent device including the same | |
| KR20150053027A (en) | Organic light-emitting compound and organic electroluminescent device using the same | |
| KR101585303B1 (en) | Organic lightingemitting compound and organic electroluminescent device using the same | |
| KR101667443B1 (en) | Organic compound and organic electroluminescent device comprising the same | |
| KR20150098977A (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR101390616B1 (en) | Novel compounds and organic electro luminescence device using the same | |
| KR101548040B1 (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR101577099B1 (en) | Organic compound and organic electroluminescent device comprising the same | |
| KR101759439B1 (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR102692891B1 (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR101561340B1 (en) | Organic compound and organic electroluminescent device comprising the same | |
| KR20150086107A (en) | Organic compounds and organic electro luminescence device comprising the same | |
| KR102620860B1 (en) | Organic light-emitting compound and organic electroluminescent device using the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| FPAY | Annual fee payment |
Payment date: 20170424 Year of fee payment: 4 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| LAPS | Lapse due to unpaid annual fee | ||
| PC1903 | Unpaid annual fee |
St.27 status event code: A-4-4-U10-U13-oth-PC1903 Not in force date: 20180424 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE |
|
| PC1903 | Unpaid annual fee |
St.27 status event code: N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 20180424 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R13-asn-PN2301 St.27 status event code: A-5-5-R10-R11-asn-PN2301 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |