JP2017171627A - Aqueous solution and object treatment method - Google Patents
Aqueous solution and object treatment method Download PDFInfo
- Publication number
- JP2017171627A JP2017171627A JP2016061517A JP2016061517A JP2017171627A JP 2017171627 A JP2017171627 A JP 2017171627A JP 2016061517 A JP2016061517 A JP 2016061517A JP 2016061517 A JP2016061517 A JP 2016061517A JP 2017171627 A JP2017171627 A JP 2017171627A
- Authority
- JP
- Japan
- Prior art keywords
- aqueous solution
- liquid sample
- solution
- hydrogen peroxide
- acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Apparatus For Disinfection Or Sterilisation (AREA)
- Water Treatment By Electricity Or Magnetism (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
Abstract
【課題】高い活性を有し、簡単に利用可能な水溶液を提供する。【解決手段】水溶液は、主たる成分として、亜硝酸イオンと、過酸化水素と、pHが6以上8以下の範囲に緩衝性を有し、濃度が0.5mM以上100mM以下の緩衝成分とを含有し、pHが6以上8以下である。【選択図】図1AAn object of the present invention is to provide an aqueous solution that has high activity and can be easily used. The aqueous solution contains, as main components, nitrite ions, hydrogen peroxide, and a buffering component having a buffering property in a pH range of 6 to 8 and a concentration of 0.5 mM to 100 mM. and pH is 6 or more and 8 or less. [Selection drawing] Fig. 1A
Description
本開示は、水溶液及び当該水溶液を用いた対象物処理方法に関する。 The present disclosure relates to an aqueous solution and an object processing method using the aqueous solution.
従来、薬剤、機能水又はアルコールなどを用いて、除殺菌又は有機物の分解などが行われている。薬剤としては、例えば、グルタール又は次亜塩素酸ソーダなどを用いることができる。しかしながら、これらの薬剤には、特有の刺激臭があり、また、人体、環境への有害性及び残留性が高い。機能水としては、次亜塩素酸水又はオゾン水などを用いることができる。これらの機能水及びアルコールは、有害性、残留性は低いものの、塩素臭、オゾン臭又はアルコール臭などの特有の臭いを発する。また、アルコールは、ウイルスなどへの殺菌性が弱い。 Conventionally, sterilization or decomposition of organic substances has been performed using chemicals, functional water, alcohol, or the like. As the drug, for example, glutar or sodium hypochlorite can be used. However, these drugs have a peculiar irritating odor, and are highly harmful to humans and the environment and have a high persistence. As functional water, hypochlorous acid water or ozone water can be used. Although these functional waters and alcohols are less harmful and persistent, they emit a characteristic odor such as chlorine odor, ozone odor or alcohol odor. Alcohol is weakly bactericidal against viruses.
一方で、生体内では、無臭で強力な活性を有するペルオキシ亜硝酸によって殺菌が行われている。具体的には、スーパーオキシドディスムターゼ(Superoxide dismutase;SOD)、一酸化窒素合成酵素(Nitric Oxide Synthase;NOS)などの酵素から産生されたスーパーオキサイドとNOラジカルとが結合することにより、ペルオキシ亜硝酸を発生させている。無臭で強力な活性を有するペルオキシ亜硝酸の性質を調べる科学的な研究が各種行われている(例えば、非特許文献1及び2を参照)。
On the other hand, in a living body, sterilization is performed by peroxynitrous acid having no odor and strong activity. Specifically, superoxide dismutase (SOD), nitric oxide synthase (Nitric Oxide Synthase; NOS) and the like are combined with superoxide and NO radicals to bind peroxynitrite. Is generated. Various scientific studies have been conducted to examine the properties of peroxynitrite having odorless and strong activity (see, for example,
しかしながら、非特許文献1では、このような反応が酸性下では極めて早く進行することが記載されている。また、非特許文献2に記載された方法では、生成した溶液を凍結保存する必要がある。このため、利用機会及び利用環境が限定され、除殺菌の利用したいときに利用したい目的で利用することが難しい。
However, Non-Patent
そこで、本開示は、高い活性を有し、簡単に利用可能な水溶液及び当該水溶液を用いた対象物処理方法を提供する。 Therefore, the present disclosure provides an aqueous solution that has high activity and can be easily used, and an object processing method using the aqueous solution.
上記課題を解決するため、本開示の一態様に係る水溶液は、主たる成分として、亜硝酸イオンと、過酸化水素と、pHが6以上8以下の範囲に緩衝性を有し、濃度が0.5mM以上100mM以下の緩衝成分とを含有し、pHが6以上8以下である。 In order to solve the above problems, an aqueous solution according to one embodiment of the present disclosure has, as main components, nitrite ions, hydrogen peroxide, buffering in a pH range of 6 to 8, and a concentration of 0. A buffer component of 5 mM or more and 100 mM or less, and a pH of 6 or more and 8 or less.
また、例えば、本開示の一態様に係る対象物処理方法は、主たる成分として、亜硝酸イオンと、過酸化水素とを含有し、pHが6以上8以下である水溶液を準備するステップと、前記水溶液のpHを6より小さく、又は8より大きく調整するステップと、前記水溶液を対象物に接触させるステップとを含む。 For example, the object processing method according to an aspect of the present disclosure includes preparing an aqueous solution containing nitrite ions and hydrogen peroxide as main components and having a pH of 6 or more and 8 or less, Adjusting the pH of the aqueous solution to be less than 6 or greater than 8, and bringing the aqueous solution into contact with an object.
本開示によれば、高い活性を有し、簡単に利用可能な水溶液及び当該水溶液を用いた対象物処理方法を提供することができる。 According to the present disclosure, it is possible to provide an aqueous solution that has high activity and can be easily used, and an object processing method using the aqueous solution.
(本開示の基礎となった知見)
亜硝酸イオン(NO2 −)を含む溶液と、過酸化水素(H2O2)を含む溶液とを混合し、混合溶液の液性を酸性にすることで、ペルオキシ亜硝酸(ONOOH)が発生する。具体的には、以下の(式1)で示す反応が起きている。
(Knowledge that became the basis of this disclosure)
Peroxynitrite (ONOHH) is generated by mixing a solution containing nitrite ion (NO 2 − ) with a solution containing hydrogen peroxide (H 2 O 2 ) to make the mixed solution acidic. To do. Specifically, the reaction shown by the following (Formula 1) has occurred.
(式1) NO2 −+H2O2+H+(酸性) → ONOOH+H2O (Formula 1) NO 2 − + H 2 O 2 + H + (acidic) → ONOOH + H 2 O
ペルオキシ亜硝酸は、対象物と接触した場合に、強い酸化若しくは水酸化反応、又は、ニトロソ化若しくはニトロ化反応を行うことで、除殺菌作用、及び、有機物の分解作用を起こすことができる。このとき、刺激臭などの臭いは発生させない。酸性下で、対象物が存在しない場合には、ペルオキシ亜硝酸は、構造異性体である硝酸に速やかに変化し、活性が失われるので、残留性が低い。 When peroxynitrous acid is brought into contact with an object, a strong oxidization or hydroxylation reaction, or a nitrosation or nitration reaction can be performed to cause a disinfection action and an organic substance decomposition action. At this time, no odor such as irritating odor is generated. In the absence of an object under acidic conditions, peroxynitrous acid is rapidly changed to nitric acid, which is a structural isomer, and its activity is lost, so its persistence is low.
また、混合溶液の液性をアルカリ性にすることで、混合溶液に含まれる過酸化水素が活性となる。過酸化水素は、対象物と接触した場合に、除殺菌作用、及び、有機物の分解作用を起こすことができる。このとき、刺激臭などの臭いは発生させない。アルカリ性下で、対象物が存在しない場合には、過酸化水素の分解が進行し、活性は低下する。 Further, by making the liquid property of the mixed solution alkaline, hydrogen peroxide contained in the mixed solution becomes active. Hydrogen peroxide can cause a disinfection action and an organic substance decomposition action when in contact with an object. At this time, no odor such as irritating odor is generated. In the absence of an object under alkaline conditions, the decomposition of hydrogen peroxide proceeds and the activity decreases.
亜硝酸イオンは、単独では不安定であり、通常、亜硝酸ナトリウム、亜硝酸カリウム、亜硝酸リチウムなどのアルカリ金属、又は、アルカリ土類金属などを用いた亜硝酸塩の水溶液において安定である。このような亜硝酸塩の水溶液はpH9程度のアルカリ性であるため、過酸化水素の分解反応が徐々に進行する。 Nitrite ions are unstable by themselves and are usually stable in an aqueous solution of nitrite using an alkali metal such as sodium nitrite, potassium nitrite, or lithium nitrite, or an alkaline earth metal. Since such an aqueous solution of nitrite is alkaline with a pH of about 9, the decomposition reaction of hydrogen peroxide proceeds gradually.
以上のことから、本開示の一態様に係る水溶液は、主たる成分として、亜硝酸イオンと、過酸化水素と、pHが6以上8以下の範囲に緩衝性を有し、濃度が0.5mM以上100mM以下の緩衝成分とを含有し、pHが6以上8以下である。 From the above, the aqueous solution according to one embodiment of the present disclosure has, as main components, nitrite ions, hydrogen peroxide, and buffering in a pH range of 6 to 8, and a concentration of 0.5 mM or more. The buffer component is 100 mM or less, and the pH is 6 or more and 8 or less.
これにより、液性を中性に保つことで、水溶液を安定に保管することができる。また、必要に応じて水溶液を酸性化又はアルカリ性化することで、高い活性を有するペルオキシ亜硝酸を生成し、又は、過酸化水素を活性化させることができる。このように、簡単に水溶液を除殺菌又は有機物の分解などに利用することができる。また、ペルオキシ亜硝酸は、刺激臭などの臭いを発生させず、活性は速やかに失われるので、残留性が低い。このため、環境に与える影響が少ない。 Thereby, aqueous solution can be stably stored by keeping liquidity neutral. Moreover, peroxynitrous acid with high activity can be produced | generated or hydrogen peroxide can be activated by acidifying or alkalizing aqueous solution as needed. In this way, the aqueous solution can be easily used for sterilization or decomposition of organic substances. In addition, peroxynitrous acid does not generate odors such as irritating odors, and its activity is quickly lost, so its persistence is low. For this reason, there is little influence on an environment.
また、本態様に係る水溶液は、pHが6以上8以下の範囲に緩衝性を有する緩衝成分を含んでいるので、pHを中性の範囲で安定させることができる。これにより、pHの調整(酸性化又はアルカリ性化)、又は、保管時の取り扱いが容易になる。 Moreover, since the aqueous solution which concerns on this aspect contains the buffer component which has buffering property in pH 6-8, pH can be stabilized in neutral range. This facilitates pH adjustment (acidification or alkalinization) or handling during storage.
例えば、緩衝性がない(又は弱い)場合、保管中又は対象物との接触時に、水溶液の液性が意図せず変化してしまい、活性が失われてしまう恐れがある。逆に、緩衝性が強すぎる場合、水溶液を酸性化又はアルカリ性化しようとしたときに、大量の酸又はアルカリを必要とする。本態様に係る水溶液では、緩衝成分の濃度が0.5mM以上100mM以下であるので、適切な緩衝性を有する。したがって、pHの調整(酸性化又はアルカリ性化)、又は、保管時の取り扱いが一層容易になる。 For example, when there is no (or weak) buffering property, the liquidity of the aqueous solution may change unintentionally during storage or contact with an object, and the activity may be lost. On the other hand, if the buffering property is too strong, a large amount of acid or alkali is required when the aqueous solution is acidified or alkalized. In the aqueous solution which concerns on this aspect, since the density | concentration of a buffer component is 0.5 mM or more and 100 mM or less, it has suitable buffer property. Therefore, pH adjustment (acidification or alkalinization) or handling during storage becomes easier.
また、例えば、本開示の一態様に係る水溶液は、さらに、硝酸イオンを含有してもよい。 For example, the aqueous solution which concerns on 1 aspect of this indication may contain a nitrate ion further.
これにより、水溶液を中性に保つことができる。 Thereby, the aqueous solution can be kept neutral.
また、例えば、前記緩衝成分は、リン酸であってもよい。 For example, the buffer component may be phosphoric acid.
これにより、pHの調整(酸性化又はアルカリ性化)、又は、保管時の取り扱いが一層容易になる。 As a result, pH adjustment (acidification or alkalinization) or handling during storage becomes easier.
また、例えば、前記緩衝成分の濃度は、1mM以上10mM以下であってもよい。 For example, the concentration of the buffer component may be 1 mM or more and 10 mM or less.
これにより、pHの調整(酸性化又はアルカリ性化)、又は、保管時の取り扱いが極めて容易になる。 Thereby, pH adjustment (acidification or alkalinization) or handling during storage becomes extremely easy.
また、例えば、本開示の一態様に係る対象物処理方法は、主たる成分として、亜硝酸イオンと、過酸化水素とを含有し、pHが6以上8以下である水溶液を準備するステップと、前記水溶液のpHを6より小さく、又は8より大きく調整するステップと、前記水溶液を対象物に接触させるステップとを含む。 For example, the object processing method according to an aspect of the present disclosure includes preparing an aqueous solution containing nitrite ions and hydrogen peroxide as main components and having a pH of 6 or more and 8 or less, Adjusting the pH of the aqueous solution to be less than 6 or greater than 8, and bringing the aqueous solution into contact with an object.
これにより、水溶液を酸性化又はアルカリ性化することで、高い活性を有するペルオキシ亜硝酸を生成し、又は、過酸化水素を活性化させることができる。したがって、簡単に水溶液を除殺菌又は有機物の分解などに利用することができる。 Thereby, peroxynitrous acid which has high activity can be produced | generated, or hydrogen peroxide can be activated by acidifying or making alkaline aqueous solution. Therefore, the aqueous solution can be easily used for sterilization or decomposition of organic substances.
また、例えば、前記調整するステップは、前記接触させるステップの後に行われてもよい。 For example, the adjusting step may be performed after the contacting step.
これにより、水溶液を対象物に接触させた後に水溶液のpHを調整するので、水溶液の活性が高められると直ちに対象物に作用することができる。したがって、対象物の分解などを効率良く行うことができる。 As a result, the pH of the aqueous solution is adjusted after the aqueous solution is brought into contact with the object, so that when the activity of the aqueous solution is increased, it can act on the object immediately. Accordingly, it is possible to efficiently decompose the object.
また、例えば、前記接触させるステップは、前記調整するステップの後に行われてもよい。 Further, for example, the contacting step may be performed after the adjusting step.
これにより、活性を高めた後に水溶液を対象物に接触させるので、水溶液と対象物との反応を制御することができる。例えば、水溶液と対象物との反応速度などを調整することができる。 Thereby, after increasing activity, since aqueous solution is made to contact a target object, reaction with aqueous solution and a target object can be controlled. For example, the reaction rate between the aqueous solution and the object can be adjusted.
また、例えば、前記調整するステップでは、(i)酸、塩基若しくは塩、(ii)酸、塩基若しくは塩の少なくとも1つを含む溶液、(iii)溶解して酸若しくは塩基となる気体若しくは固体、又は、(iv)当該気体若しくは当該液体又は固体を発生する生物を含む溶液、を前記水溶液に添加することで、前記水溶液のpHを調整してもよい。 Further, for example, in the adjusting step, (i) an acid, a base or a salt, (ii) a solution containing at least one of an acid, a base or a salt, (iii) a gas or a solid which dissolves into an acid or a base, Alternatively, (iv) the pH of the aqueous solution may be adjusted by adding the gas, the liquid, or a solution containing a living organism that generates a solid to the aqueous solution.
これにより、水溶液のpHを容易に調整することができる。具体的には、pHを調整するための材料として、多くの材料の中から選択することができる。例えば、安価な材料を選択することができ、コストを削減することができる。 Thereby, pH of aqueous solution can be adjusted easily. Specifically, the material for adjusting the pH can be selected from many materials. For example, an inexpensive material can be selected, and the cost can be reduced.
また、例えば、前記調整するステップでは、前記水溶液を電気分解することで、前記水溶液のpHを調整してもよい。 For example, in the step of adjusting, the pH of the aqueous solution may be adjusted by electrolyzing the aqueous solution.
これにより、薬剤などの添加を行わずに水溶液のpHを調整することができる。このように、水溶液のpHの調整方法には特に限定されないので、例えば、対象物に適した手法でpHを調整することができる。 Thereby, pH of aqueous solution can be adjusted, without adding a chemical | medical agent etc. Thus, since it is not specifically limited to the adjustment method of pH of aqueous solution, For example, pH can be adjusted with the method suitable for a target object.
また、例えば、前記水溶液は、さらに、pHが6以上8以下の範囲に緩衝性を有し、濃度が0.5mM以上100mM以下の緩衝成分を含有してもよい。 In addition, for example, the aqueous solution may further include a buffer component having a pH in the range of 6 to 8 and a concentration of 0.5 mM to 100 mM.
これにより、pHを中性の範囲で安定させることができるので、pHの調整(酸性化又はアルカリ性化)、又は、保管時の取り扱いが容易になる。 Thereby, since pH can be stabilized in the neutral range, pH adjustment (acidification or alkalinization) or handling during storage becomes easy.
以下では、実施の形態について、図面を参照しながら具体的に説明する。 Hereinafter, embodiments will be specifically described with reference to the drawings.
なお、以下で説明する実施の形態は、いずれも包括的又は具体的な例を示すものである。以下の実施の形態で示される数値、形状、材料、構成要素、構成要素の配置位置及び接続形態、ステップ、ステップの順序などは、一例であり、本開示を限定する主旨ではない。また、以下の実施の形態における構成要素のうち、最上位概念を示す独立請求項に記載されていない構成要素については、任意の構成要素として説明される。 It should be noted that each of the embodiments described below shows a comprehensive or specific example. Numerical values, shapes, materials, components, arrangement positions and connection forms of components, steps, order of steps, and the like shown in the following embodiments are merely examples, and are not intended to limit the present disclosure. In addition, among the constituent elements in the following embodiments, constituent elements that are not described in the independent claims indicating the highest concept are described as optional constituent elements.
また、各図は、模式図であり、必ずしも厳密に図示されたものではない。したがって、例えば、各図において縮尺などは必ずしも一致しない。また、各図において、実質的に同一の構成については同一の符号を付しており、重複する説明は省略又は簡略化する。 Each figure is a mimetic diagram and is not necessarily illustrated strictly. Therefore, for example, the scales and the like do not necessarily match in each drawing. Moreover, in each figure, the same code | symbol is attached | subjected about the substantially same structure, The overlapping description is abbreviate | omitted or simplified.
また、本明細書において、「中性」とは、pH(水素イオン指数)が6以上8以下であることを意味する。「アルカリ性」とはpHが8より大きいことを意味する。「酸性」とは、pHが6より小さいことを意味する。 In the present specification, “neutral” means that the pH (hydrogen ion index) is 6 or more and 8 or less. “Alkaline” means that the pH is greater than 8. “Acid” means that the pH is less than 6.
「中性化」とは、「中性」にすること、すなわち、pHを6以上8以下にすることを意味する。「アルカリ性化」とは、「アルカリ性」にすること、すなわち、pHを8より大きくすることを意味する。「酸性化」とは、「酸性」にすること、すなわち、pHを6より小さくすることを意味する。 “Neutralization” means “neutralization”, that is, pH is 6 or more and 8 or less. “Alkalinization” means making it “alkaline”, that is, making the pH higher than 8. “Acidification” means making it “acidic”, that is, making the pH lower than 6.
(実施の形態1)
[1.水溶液]
まず、本実施の形態に係る水溶液について説明する。
(Embodiment 1)
[1. Aqueous solution]
First, the aqueous solution according to the present embodiment will be described.
本実施の形態に係る水溶液は、主たる成分として、亜硝酸イオン(NO2 −)と、過酸化水素(H2O2)と、緩衝成分とを含有する水溶液であり、pHが6以上8以下である。具体的には、水溶液は、亜硝酸イオンを含む第1溶液と、過酸化水素を含む第2溶液と、緩衝成分を含む第3溶液とが混合された混合溶液である。なお、主たる成分とは、水溶液中の亜硝酸イオン、過酸化水素及び緩衝成分を除く物質に対して、10倍以上の濃度を有する成分であることを意味する。 The aqueous solution according to the present embodiment is an aqueous solution containing nitrite ions (NO 2 − ), hydrogen peroxide (H 2 O 2 ), and a buffer component as main components, and has a pH of 6 or more and 8 or less. It is. Specifically, the aqueous solution is a mixed solution in which a first solution containing nitrite ions, a second solution containing hydrogen peroxide, and a third solution containing a buffer component are mixed. The main component means a component having a concentration of 10 times or more with respect to substances other than nitrite ions, hydrogen peroxide and buffer components in the aqueous solution.
亜硝酸イオンを含む第1溶液は、例えば、亜硝酸ナトリウム(NaNO2)などの亜硝酸塩を含む水溶液である。亜硝酸塩は、例えば、アルカリ金属又はアルカリ土類金属を用いた亜硝酸塩であり、具体的には、亜硝酸カリウム、亜硝酸リチウムなどでもよい。 The first solution containing nitrite ions is an aqueous solution containing a nitrite such as sodium nitrite (NaNO 2 ), for example. The nitrite is, for example, a nitrite using an alkali metal or an alkaline earth metal, and specifically, potassium nitrite, lithium nitrite, or the like may be used.
過酸化水素を含む第2溶液は、例えば、過酸化水素を含む水溶液(過酸化水素水)である。 The second solution containing hydrogen peroxide is, for example, an aqueous solution containing hydrogen peroxide (hydrogen peroxide solution).
緩衝成分を含む第3溶液は、例えば、リン酸(H3PO4)などの緩衝成分を含む水溶液である。緩衝成分は、リン酸に限らず、トリス・塩酸、HEPES、EDTA、クエン酸/クエン酸ナトリウムなど、又は、これらに酢酸(CH3COOH)、ホウ酸(H3BO3)などの成分を加えた広域緩衝液であってもよい。 The third solution containing a buffer component is an aqueous solution containing a buffer component such as phosphoric acid (H 3 PO 4 ). Buffer components are not limited to phosphoric acid, but include components such as tris / hydrochloric acid, HEPES, EDTA, citric acid / sodium citrate, or acetic acid (CH 3 COOH) and boric acid (H 3 BO 3 ). Or a wide range buffer.
緩衝成分は、pHが6以上8以下の範囲に緩衝性を有する。すなわち、緩衝成分は、中性に緩衝性を有する。緩衝成分を含む水溶液に少量の酸又は塩基を添加したとしても、pHはほとんど変化しないので、当該水溶液を中性で安定して保管することができる。 The buffer component has a buffering property in a pH range of 6 to 8. That is, the buffer component is neutrally buffered. Even if a small amount of acid or base is added to an aqueous solution containing a buffer component, the pH hardly changes, so that the aqueous solution can be stored neutrally and stably.
緩衝成分の濃度は、0.5mM以上100mM以下である。好ましくは、緩衝成分の濃度は、1mM以上10mM以下である。より好ましくは、緩衝成分の濃度は、5mM以上10mM以下である。これにより、水溶液のpHを調整(酸性化又はアルカリ性化)する際に、必要以上に多くの酸又は塩基を必要としないで済む。したがって、簡単に水溶液の液性を変化させることができ、簡単に水溶液の活性を発揮させることができる。 The concentration of the buffer component is 0.5 mM or more and 100 mM or less. Preferably, the concentration of the buffer component is 1 mM or more and 10 mM or less. More preferably, the concentration of the buffer component is 5 mM or more and 10 mM or less. This eliminates the need for more acid or base than necessary when adjusting the pH of the aqueous solution (acidification or alkalinization). Therefore, the liquidity of the aqueous solution can be easily changed, and the activity of the aqueous solution can be easily exhibited.
本実施の形態では、水溶液に含まれる亜硝酸イオンの濃度及び過酸化水素の濃度は、特に限定されないが、例えば、100mM以下である。これにより、水溶液を除殺菌又は有機物の分解などに簡単に用いることができる。 In this Embodiment, although the density | concentration of the nitrite ion contained in aqueous solution and the density | concentration of hydrogen peroxide are not specifically limited, For example, it is 100 mM or less. Thereby, the aqueous solution can be easily used for sterilization or decomposition of organic substances.
例えば、亜硝酸イオン及び過酸化水素のいずれも濃度が高すぎる場合、水溶液(混合溶液)が中性に保たれていたとしても、反応が徐々に進行する。このため、水溶液の長期間の保管には適さない。また、水溶液を酸性化してペルオキシ亜硝酸を発生させた場合、ペルオキシ亜硝酸は反応後に硝酸に変化する。このため、水溶液が強酸性になるので、反応速度の調整が難しくなる。 For example, when the concentrations of both nitrite ions and hydrogen peroxide are too high, the reaction gradually proceeds even if the aqueous solution (mixed solution) is kept neutral. For this reason, it is not suitable for long-term storage of aqueous solution. In addition, when peroxynitrite is generated by acidifying the aqueous solution, the peroxynitrite changes to nitric acid after the reaction. For this reason, since aqueous solution becomes strong acidity, adjustment of reaction rate becomes difficult.
また、上述した(式1)で示すように、当モルの亜硝酸イオン及び過酸化水素から、当モルのペルオキシ亜硝酸が発生する。このため、亜硝酸イオンのモル濃度と過酸化水素のモル濃度とは、略同じであればよい。 Further, as shown in the above (Formula 1), equimolar peroxynitrite is generated from equimolar nitrite ions and hydrogen peroxide. For this reason, the molar concentration of nitrite ions and the molar concentration of hydrogen peroxide may be substantially the same.
本実施の形態では、水溶液中の亜硝酸イオンに対する過酸化水素の含有モル濃度の比率(=過酸化水素/亜硝酸イオン)は、0.5より大きく、2より小さい範囲にある。好ましくは、当該比率は、0.75より大きく、1.25より小さい範囲にある。 In the present embodiment, the ratio of the molar concentration of hydrogen peroxide to nitrite ions in the aqueous solution (= hydrogen peroxide / nitrite ions) is in the range of more than 0.5 and less than 2. Preferably, the ratio is in a range greater than 0.75 and less than 1.25.
水溶液に含まれる過酸化水素は、長期間の保管により分解されて減少する。このため、予め過酸化水素のモル濃度を亜硝酸イオンのモル濃度より大きくしておくことで、長期間の保管後においても高い活性を実現することができる。 Hydrogen peroxide contained in the aqueous solution is decomposed and reduced by long-term storage. For this reason, high activity can be realized even after long-term storage by making the molar concentration of hydrogen peroxide larger than the molar concentration of nitrite ions in advance.
また、酸性下ではペルオキシ亜硝酸は短寿命であり、対象物に作用する時間が短い。このため、予め亜硝酸イオンのモル濃度を過酸化水素のモル濃度より大きくしておくことで、ペルオキシ亜硝酸による作用が終わった後に残留する亜硝酸を利用して、酸性下で弱い殺菌又は防腐などを行うことができる。 In addition, peroxynitrous acid has a short life under acidic conditions, and the time for acting on the object is short. For this reason, by making the molar concentration of nitrite ions larger than the molar concentration of hydrogen peroxide in advance, nitrite remaining after the action of peroxynitrous acid is used, and weak sterilization or preserving under acidic conditions. And so on.
なお、本実施の形態では、中性の緩衝成分を含む第3溶液を混合することで、水溶液を中性化したが、これに限らない。緩衝成分の代わりに、又は、緩衝成分に加えて、硝酸イオンを加えてもよい。すなわち、水溶液は、硝酸イオンを含有してもよい。また、本実施の形態に係る水溶液は、緩衝成分を含有していなくてもよい。 In the present embodiment, the aqueous solution is neutralized by mixing the third solution containing a neutral buffer component. However, the present invention is not limited to this. Nitrate ions may be added instead of or in addition to the buffer component. That is, the aqueous solution may contain nitrate ions. Moreover, the aqueous solution which concerns on this Embodiment does not need to contain the buffer component.
[2.水溶液の活性(分解力)]
本発明者は、本実施の形態に係る水溶液の活性の高さ(分解力)を確認するため、数種類の液体サンプル(実施例及び比較例)を作製し、作製した液体サンプルを用いてインディゴカーミンの分解試験を行った。
[2. Activity of aqueous solution (decomposition power)]
In order to confirm the high activity (decomposition power) of the aqueous solution according to the present embodiment, the present inventor produced several types of liquid samples (Examples and Comparative Examples), and indigo carmine using the produced liquid samples. The decomposition test was conducted.
インディゴカーミンは、610nmの波長の光に対して吸収極大を有する。すなわち、液体サンプル中にインディゴカーミンが存在している場合には、610nmの波長の光が吸収されるので、当該波長の光に対する液体サンプルの吸光度は大きい値になる。一方で、液体サンプルに含まれるインディゴカーミンが分解されて減少した場合には、610nmの波長の光は吸収されないので、当該波長の光に対する液体サンプルの吸光度は小さい値になる。したがって、液体サンプルとインディゴカーミンとを混合したときの吸光度の時間変化を、液体サンプルの活性の高さ(分解力)の指標として用いることができる。 Indigo carmine has an absorption maximum for light having a wavelength of 610 nm. That is, when indigo carmine is present in the liquid sample, light having a wavelength of 610 nm is absorbed, and thus the absorbance of the liquid sample with respect to light having the wavelength becomes a large value. On the other hand, when the indigo carmine contained in the liquid sample is decomposed and decreased, light with a wavelength of 610 nm is not absorbed, and thus the absorbance of the liquid sample with respect to the light with the wavelength becomes a small value. Therefore, the time change of the absorbance when the liquid sample and indigo carmine are mixed can be used as an index of the activity level (decomposition power) of the liquid sample.
そこで、分光測定器を用いて、インディゴカーミンを混合した液体サンプルにおける、610nmの波長の光に対する吸光度の時間変化を測定した。なお、以下の各試験において、インディゴカーミンの初期濃度は、10mg/Lである。 Then, the time change of the light absorbency with respect to the light of a wavelength of 610 nm in the liquid sample which mixed indigo carmine was measured using the spectrometer. In each of the following tests, the initial concentration of indigo carmine is 10 mg / L.
[2−1.実施例]
実施例に係る液体サンプルAについて説明する。液体サンプルAは、亜硝酸イオン、過酸化水素及び緩衝成分(リン酸)を含む中性の水溶液(混合溶液)である。
[2-1. Example]
The liquid sample A according to the example will be described. The liquid sample A is a neutral aqueous solution (mixed solution) containing nitrite ions, hydrogen peroxide, and a buffer component (phosphoric acid).
まず、pHが7.2で1Mのリン酸緩衝液を調製(準備)した。具体的には、このリン酸緩衝液は、リン酸二水素ナトリウム二水和物(NaH2PO4・2H2O)44.0gと、リン酸水素ナトリウム(NaHPO4)30.2gとを混合し、超純水で500mLにメスアップすることで生成した。 First, a 1M phosphate buffer having a pH of 7.2 was prepared (prepared). Specifically, this phosphate buffer is a mixture of 44.0 g of sodium dihydrogen phosphate dihydrate (NaH 2 PO 4 .2H 2 O) and 30.2 g of sodium hydrogen phosphate (NaHPO 4 ). And was made up to 500 mL with ultrapure water.
7.14mMの亜硝酸ナトリウム液14.85mLに、150μLの上記pH7.2で1Mのリン酸緩衝液を添加し、亜硝酸溶液を生成した。さらに、上記pH7.2で1Mのリン酸緩衝液を超純水で100倍希釈した10mMのリン酸緩衝液15mLに、30%過酸化水素水5μLを添加することで、過酸化水素溶液を生成した。これらの亜硝酸溶液と過酸化水素溶液とを当量で混合することにより、実施例に係る水溶液(すなわち、液体サンプルA)を作製した。
To 14.85 mL of the 7.14 mM sodium nitrite solution, 150 μL of 1 M phosphate buffer at pH 7.2 was added to form a nitrite solution. Furthermore, a hydrogen peroxide solution is produced by adding 5 μL of 30% aqueous hydrogen peroxide to 15 mL of 10 mM phosphate buffer obtained by diluting 1M phosphate buffer at pH 7.2 with
[2−2.比較例1]
次に、比較例1に係る液体サンプルBについて説明する。液体サンプルBは、亜硝酸イオン及び緩衝成分(リン酸)を含む中性の水溶液(混合溶液)である。
[2-2. Comparative Example 1]
Next, the liquid sample B according to Comparative Example 1 will be described. The liquid sample B is a neutral aqueous solution (mixed solution) containing nitrite ions and a buffer component (phosphoric acid).
実施例に係る液体サンプルAの作製に用いた亜硝酸溶液を、上記10mMのリン酸緩衝液で2倍に希釈することで、pHが7.2の亜硝酸ナトリウム溶液を比較例1に係る液体サンプルBとして作製した。 By diluting the nitrous acid solution used for the preparation of the liquid sample A according to the example with the 10 mM phosphate buffer twice, the sodium nitrite solution having a pH of 7.2 is changed to the liquid according to the comparative example 1. Sample B was prepared.
[2−3.比較例2]
次に、比較例2に係る液体サンプルCについて説明する。液体サンプルCは、過酸化水素及び緩衝成分(リン酸)を含む中性の水溶液(混合溶液)である。
[2-3. Comparative Example 2]
Next, the liquid sample C according to Comparative Example 2 will be described. The liquid sample C is a neutral aqueous solution (mixed solution) containing hydrogen peroxide and a buffer component (phosphoric acid).
実施例に係る液体サンプルAの作製に用いた過酸化水素溶液を、上記10mMのリン酸緩衝液で2倍に希釈することで、pHが7.2の過酸化水素溶液を比較例2に係る液体サンプルCとして作製した。 By diluting the hydrogen peroxide solution used for the preparation of the liquid sample A according to the example with the 10 mM phosphate buffer solution twice, the hydrogen peroxide solution with a pH of 7.2 is related to the comparative example 2. A liquid sample C was prepared.
[2−4.試験結果]
上記の液体サンプルA〜Cの各々を中性化(中性で維持)し、酸性化し、又は、アルカリ性化することで、インディゴカーミンの分解試験を行った。なお、酸性化は、硫酸(4.5N)を添加することで行った。アルカリ性化は、水酸化ナトリウム水溶液(4.5N)を添加することで行った。具体的な添加量は、以下の表1に示す通りである。
[2-4. Test results]
Each of the above liquid samples A to C was neutralized (maintained neutral), acidified, or alkalized to perform an indigo carmine decomposition test. In addition, acidification was performed by adding sulfuric acid (4.5N). Alkalinization was performed by adding an aqueous sodium hydroxide solution (4.5 N). Specific addition amounts are as shown in Table 1 below.
図1A〜図1Cはそれぞれ、実施例、比較例1及び比較例2に係る水溶液によるインディゴカーミンの分解試験の結果を示す図である。 1A to 1C are diagrams showing the results of indigo carmine decomposition tests using aqueous solutions according to Examples, Comparative Examples 1 and 2, respectively.
[2−4−1.中性]
図1A〜図1Cに示すように、液体サンプルA〜Cのいずれにおいても、中性では、吸光度は、時間の経過とともにほとんど低下していない。つまり、実施例に係る液体サンプルAは、中性で安定していることが分かる。
[2-4-1. neutral]
As shown in FIGS. 1A to 1C, in any of the liquid samples A to C, the absorbance hardly decreases with the passage of time in the neutral state. That is, it can be seen that the liquid sample A according to the example is neutral and stable.
[2−4−2.酸性化]
実施例に係る液体サンプルAを酸性化した場合、図1Aに示すように、時間の経過とともに吸光度が急激に低下した。液体サンプルAは、ペルオキシ亜硝酸を発生し、インディゴカーミンを分解していると考えられる。
[2-4-2. Acidification]
When the liquid sample A according to the example was acidified, as shown in FIG. 1A, the absorbance rapidly decreased with time. Liquid sample A is considered to generate peroxynitrous acid and decompose indigo carmine.
比較例1に係る液体サンプルBを酸性化した場合、図1Bに示すように、時間の経過とともに吸光度が低下している。しかしながら、実施例に係る液体サンプルAと比較して、吸光度の低下の度合い(グラフの傾き)は緩やかであり、分解速度が遅いことが分かる。したがって、液体サンプルAと液体サンプルBとでは、インディゴカーミンの分解に寄与している物質が異なっていると考えられる。具体的には、液体サンプルBでは、ペルオキシ亜硝酸ではなく、亜硝酸イオンがインディゴカーミンを分解していると考えられる。亜硝酸イオンの分解力は、ペルオキシ亜硝酸の10分の1程度である。 When the liquid sample B which concerns on the comparative example 1 is acidified, as FIG. 1B shows, the light absorbency is falling with progress of time. However, as compared with the liquid sample A according to the example, it can be seen that the degree of decrease in absorbance (gradient of the graph) is gentle and the decomposition rate is slow. Therefore, it is considered that the liquid sample A and the liquid sample B are different in substances that contribute to the decomposition of indigo carmine. Specifically, in the liquid sample B, it is considered that not nitrous acid but nitrite ions decompose indigo carmine. The decomposition power of nitrite ions is about one-tenth that of peroxynitrite.
比較例2に係る液体サンプルCを酸性化した場合、図1Cに示すように、中性の場合と同様に、時間の経過とともにほとんど低下していない。 When the liquid sample C which concerns on the comparative example 2 is acidified, as shown to FIG. 1C, it is hardly falling with progress of time similarly to the neutral case.
[2−4−3.アルカリ性化]
実施例及び比較例2に係る液体サンプルA及び液体サンプルCの各々をアルカリ性化した場合、図1A及び図1Cに示すように、時間の経過とともに吸光度が低下した。各々の低下の度合いは、略同じである。すなわち、アルカリ性化した液体サンプルAとアルカリ性化した液体サンプルBとは、分解力が略同じであることが分かる。
[2-4-3. Alkaline]
When each of the liquid sample A and the liquid sample C according to Example and Comparative Example 2 was made alkaline, the absorbance decreased with time as shown in FIGS. 1A and 1C. The degree of each decrease is substantially the same. That is, it can be seen that the alkalinized liquid sample A and the alkalinized liquid sample B have substantially the same decomposition power.
なお、実施例に係る液体サンプルAにインディゴカーミンを添加しなかった場合、アルカリ性化したときに過酸化水素の濃度は低下したが、亜硝酸濃度の減少及び硝酸濃度の上昇は殆ど見られなかった。したがって、実施例に係る液体サンプルAでは、過酸化水素が活性となって、インディゴカーミンが分解されていると考えられる。 In addition, when no indigo carmine was added to the liquid sample A according to the example, the concentration of hydrogen peroxide decreased when alkalized, but almost no decrease in nitrite concentration and increase in nitric acid concentration were observed. . Therefore, in the liquid sample A according to the example, it is considered that hydrogen peroxide is activated and indigo carmine is decomposed.
比較例1に係る液体サンプルBをアルカリ性化した場合、図1Bに示すように、時間の経過とともにほとんど低下していない。 When the liquid sample B according to Comparative Example 1 is made alkaline, as shown in FIG. 1B, it hardly decreases with the passage of time.
[3.ペルオキシ亜硝酸の確認試験(質量分析)]
以上のように、実施例に係る液体サンプルAでは、酸性化された場合にはペルオキシ亜硝酸が発生することで極めて高い分解力を発揮し、アルカリ性化された場合には過酸化水素が活性化することで高い分解力を発揮すると考えられる。以下では、液体サンプルAを酸性化した場合に、ペルオキシ亜硝酸が発生していることを確認するために行った実験結果について説明する。
[3. Peroxynitrite confirmation test (mass spectrometry)]
As described above, in the liquid sample A according to the embodiment, when acidified, peroxynitrous acid is generated to exhibit extremely high decomposing power, and when alkalized, hydrogen peroxide is activated. By doing so, it is thought that high resolution power is demonstrated. Below, when the liquid sample A is acidified, the experimental result performed in order to confirm that peroxy nitrous acid has generate | occur | produced is demonstrated.
まず、フェノール(C6H5OH)を超純水に溶解し、10000mg/Lの濃度のフェノール溶液を準備した。さらに、実施例に係る液体サンプルA及び比較例1に係る液体サンプルBの各々に、フェノール溶液を体積比100:1(=液体サンプルA又はB:フェノール)で添加することで、フェノールの濃度が100mg/Lになるように調製した。 First, phenol (C 6 H 5 OH) was dissolved in ultrapure water to prepare a phenol solution having a concentration of 10,000 mg / L. Furthermore, by adding a phenol solution at a volume ratio of 100: 1 (= liquid sample A or B: phenol) to each of the liquid sample A according to the example and the liquid sample B according to comparative example 1, the concentration of phenol is increased. It was prepared to be 100 mg / L.
さらに、各々の溶液に、上述したインディゴカーミンの分解試験における酸性化と同様の条件で硫酸を添加した。硫酸の添加から200秒後に同量の水酸化ナトリウムを添加することで、各溶液を中和した。このように、フェノール溶液を混合し、酸性化後に中和された液体サンプルA及び液体サンプルBをそれぞれ、液体サンプルD及び液体サンプルEとする。
Furthermore, sulfuric acid was added to each solution under the same conditions as the acidification in the above-described decomposition test of indigo carmine. Each solution was neutralized by adding the same amount of
以下では、液体サンプルD及び液体サンプルEの各々に含まれる生成物を質量分析法によって分析した。分析結果を図2A〜図3Bに示す。 Below, the product contained in each of liquid sample D and liquid sample E was analyzed by mass spectrometry. The analysis results are shown in FIGS. 2A to 3B.
ペルオキシ亜硝酸が発生している場合、フェノールとペルオキシ亜硝酸とが反応し、フェノールのメタ位又はパラ位に、ペルオキシ亜硝酸(ONOOH)の−O−N=O又は−OHが付加される。したがって、フェノールのメタ位又はパラ位に−O−N=Oが付加された物質と、フェノールのメタ位又はパラ位に−OHが付加された物質の両方が生成されたことが確認された場合、ペルオキシ亜硝酸が発生していることが分かる。 When peroxynitrous acid is generated, phenol and peroxynitrous acid react with each other, and —O—N═O or —OH of peroxynitrous acid (ONOOH) is added to the meta position or para position of phenol. Therefore, when it was confirmed that both a substance in which —O—N═O was added to the meta or para position of phenol and a substance in which —OH was added to the meta or para position of phenol were generated. It can be seen that peroxynitrite is generated.
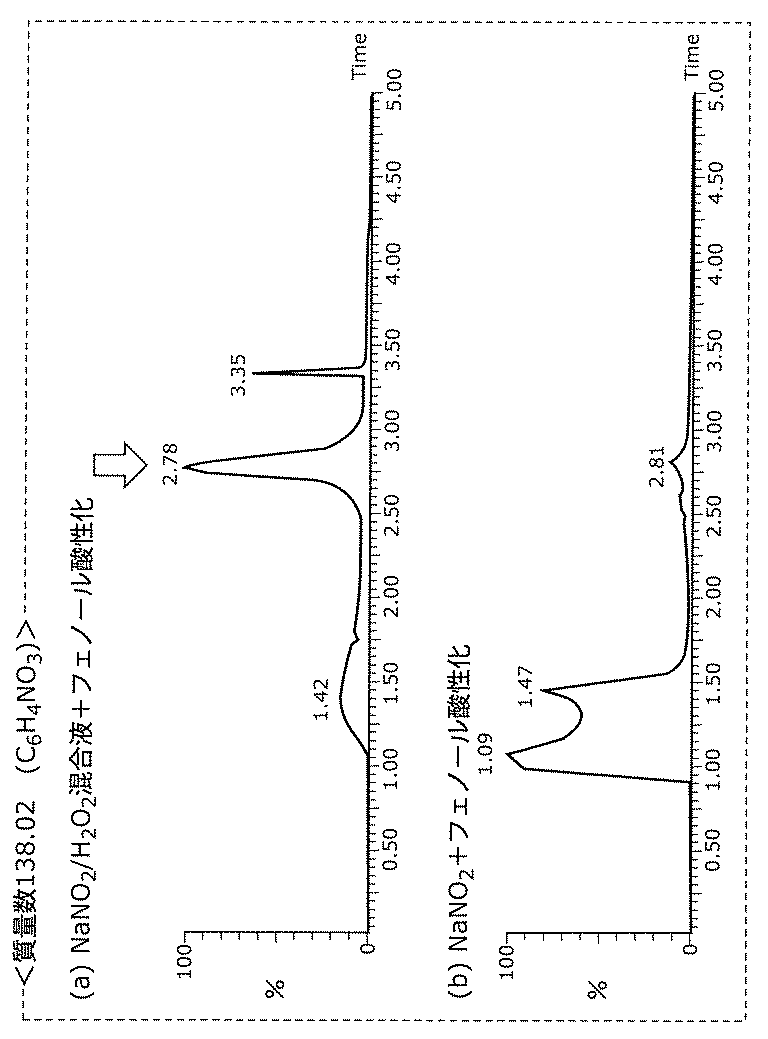
図2Aは、液体サンプルD及び液体サンプルEの各々に含まれる質量数138.02(C6H4NO3)の物質を飛行時間型質量分析(Time Of Flight Mass Spectrometry;TOF−MS)法で分析した結果を示す図である。図2Bは、図2Aで示す質量数138.02の物質をタンデム質量分析法で分析した分析結果を示す図である。 FIG. 2A shows a time of flight mass spectrometry (TOF-MS) method for substances having a mass number of 138.02 (C 6 H 4 NO 3 ) contained in each of liquid sample D and liquid sample E. It is a figure which shows the result of having analyzed. FIG. 2B is a diagram showing an analysis result obtained by analyzing the substance with a mass number of 138.02 shown in FIG. 2A by tandem mass spectrometry.
図3Aは、液体サンプルD及び液体サンプルEの各々に含まれる質量数109.03(C6H5O2)の物質を飛行時間型質量分析(TOF−MS)法で分析した結果を示す図である。図3Bは、図3Aで示す質量数109.03の物質をタンデム質量分析法で分析した分析結果を示す図である。 FIG. 3A is a diagram illustrating a result of analyzing a substance having a mass number of 109.03 (C 6 H 5 O 2 ) contained in each of the liquid sample D and the liquid sample E by a time-of-flight mass spectrometry (TOF-MS) method. It is. FIG. 3B is a diagram showing an analysis result obtained by analyzing the substance having a mass number of 109.03 shown in FIG. 3A by tandem mass spectrometry.
なお、タンデム質量分析法は、以下の条件で行った。 Tandem mass spectrometry was performed under the following conditions.
<液体クロマトグラフ>UPLC H-Class
分析カラム:ACQUITY UPLC(登録商標) BEH C18 1.7μm(2.1mmID×100mm)
溶離液A:純水
溶離液B:アセトニトリル
カラムオーブン温度:40℃
<質量分析計>SYNAPT G2-Si
測定モード:ESI(Electrospray Ionization)
極性:ネガティブ
測定質量範囲:m/z=50〜1000
MSMS電圧:15〜30V
<Liquid chromatograph> UPLC H-Class
Analytical column: ACQUITY UPLC (registered trademark) BEH C18 1.7μm (2.1mmID × 100mm)
Eluent A: Pure water Eluent B: Acetonitrile Column oven temperature: 40 ° C
<Mass spectrometer> SYNAPT G2-Si
Measurement mode: ESI (Electrospray Ionization)
Polarity: Negative Measurement mass range: m / z = 50-1000
MSMS voltage: 15-30V
図2Aの(a)及び図3Aの(a)に示すように、液体サンプルDからは、質量数138.02及び109.03に特徴的な物質の生成が確認された。具体的には、図2Aの(a)に示す質量数138.02の、時刻が2.78のピークに対応する第1物質と、図3Aの(a)に示す質量数109.02の、時刻が1.76のピークに対応する第2物質とが生成されていることが確認された。 As shown in (a) of FIG. 2A and (a) of FIG. 3A, production of a characteristic substance with mass numbers of 138.02 and 109.03 was confirmed from the liquid sample D. Specifically, a first substance corresponding to a peak at a time of 2.78 having a mass number of 138.02 shown in FIG. 2A (a), and a mass number of 109.02 shown in FIG. It was confirmed that the 2nd substance corresponding to the peak of time 1.76 was generated.
図2Bは、上記の第1物質をタンデム質量分析法で分析した結果を示している。図2Bに示すように、質量数(質量電荷比(m/z))が138.02の物質のフラグメントとして、質量数が108.2及び92.03の物質が検出されている。138.02からの各々の差は、約30と約36とであり、それぞれが−N=O及び−O−N=Oの分子量に相当する。したがって、第1物質は、フェノールのパラ位又はメタ位の炭素原子に−O−N=Oが付加した物質であることが確認された。 FIG. 2B shows the result of analyzing the first substance by tandem mass spectrometry. As shown in FIG. 2B, substances having mass numbers of 108.2 and 92.03 are detected as fragments of substances having a mass number (mass-to-charge ratio (m / z)) of 138.02. Each difference from 138.02 is about 30 and about 36, which correspond to molecular weights of -N = O and -O-N = O, respectively. Therefore, it was confirmed that the first substance was a substance in which —O—N═O was added to the carbon atom at the para or meta position of phenol.
図3Bは、上記の第2物質をタンデム質量分析法で分析した結果を示している。図3Bに示すように、質量数が109.03のフラグメントとして、質量数が91.02の物質が検出されている。109.03からの差は、約18であり、−OHの分子量に略一致する。したがって、第2物質は、フェノールのパラ位又はメタ位の炭素原子に−OHが付加した物質であった付加した物質であることが確認された。 FIG. 3B shows the result of analyzing the second substance by tandem mass spectrometry. As shown in FIG. 3B, a substance with a mass number of 91.02 is detected as a fragment with a mass number of 109.03. The difference from 109.03 is about 18, which roughly corresponds to the molecular weight of -OH. Therefore, it was confirmed that the second substance was an added substance that was a substance in which —OH was added to a carbon atom at the para or meta position of phenol.
以上のことから、液体サンプルDからは、フェノールのパラ位又はメタ位の炭素原子に−O−N=Oが付加した物質と、フェノールのパラ位又はメタ位の炭素原子に−OHが付加した物質の両方が生成されていることが確認されたので、液体サンプルDでは、ペルオキシ亜硝酸が発生していたことが確認された。 From the above, from the liquid sample D, a substance in which —O—N═O was added to a carbon atom at the para or meta position of phenol, and —OH was added to a carbon atom in the para or meta position of phenol. Since it was confirmed that both substances were produced, it was confirmed that peroxynitrite was generated in the liquid sample D.
なお、図2Aの(b)に示すように、液体サンプルEからは、時刻が2.78のピークは見られなかった。すなわち、液体サンプルEでは、フェノールのパラ位又はメタ位の炭素原子に−O−N=Oが付加した物質が含まれていないことが確認された。 As shown in FIG. 2A (b), the liquid sample E did not show a peak at time 2.78. In other words, it was confirmed that the liquid sample E does not contain a substance in which —O—N═O is added to the para-position or meta-position carbon atom of phenol.
また、図3Aの(b)に示すように、液体サンプルEからは、保持時間が1.76のピークが見られなかった。すなわち、液体サンプルEでは、フェノールのパラ位又はメタ位の炭素原子に−OHが付加した物質が含まれていないことが確認された。 Further, as shown in FIG. 3A (b), the liquid sample E did not show a peak with a retention time of 1.76. That is, it was confirmed that the liquid sample E does not contain a substance in which —OH is added to the carbon atom at the para or meta position of phenol.
以上のことから、液体サンプルEでは、ペルオキシ亜硝酸が発生していないことが確認された。 From the above, it was confirmed that no peroxynitrite was generated in the liquid sample E.
なお、亜硝酸と過酸化水素との混合溶液(液体サンプルA)にフェノールを添加せずに酸性化した場合、亜硝酸及び過酸化水素の濃度が低下し、硝酸の濃度が上昇した。 When acidification was performed without adding phenol to a mixed solution of nitrous acid and hydrogen peroxide (liquid sample A), the concentrations of nitrous acid and hydrogen peroxide decreased, and the concentration of nitric acid increased.
[4.pHに対する活性(分解力)の変化]
次に、亜硝酸イオンと過酸化水素とを含む水溶液(混合溶液)のpHを変化させたときの水溶液の分解力の変化を調べるため、数種類の液体サンプル(実施例)を作製し、作製した液体サンプルを用いてインディゴカーミンの分解試験を行った。
[4. Change in activity (degradability) against pH]
Next, several types of liquid samples (Examples) were prepared and manufactured in order to investigate changes in the decomposition power of the aqueous solution when the pH of the aqueous solution (mixed solution) containing nitrite ions and hydrogen peroxide was changed. A decomposition test of indigo carmine was performed using a liquid sample.
[4−1.液体サンプル]
以下では、作製した16種類の液体サンプルI〜XVIについて説明する。
[4-1. Liquid sample]
Below, 16 types of produced liquid samples I-XVI are demonstrated.
(I) NaNO2+H2O2+硝酸、pH=7.02
液体サンプルIは、200mMの亜硝酸ナトリウム水溶液(NaNO2水溶液)と200mMの過酸化水素水溶液(H2O2水溶液)とが混合された、pHが7.02の水溶液である。具体的には、超純水2.375mLに、200mMのNaNO2水溶液を62.5μLと200mMのH2O2水溶液を62.5μLとを混合し、さらに、1mMの硝酸水溶液を1μL添加することにより、液体サンプルIを作製した。
(I) NaNO 2 + H 2 O 2 + Nitric acid, pH = 7.02
The liquid sample I is an aqueous solution having a pH of 7.02 in which a 200 mM sodium nitrite aqueous solution (NaNO 2 aqueous solution) and a 200 mM hydrogen peroxide aqueous solution (H 2 O 2 aqueous solution) are mixed. Specifically, 62.5 μL of 200 mM NaNO 2 aqueous solution and 62.5 μL of 200 mM H 2 O 2 aqueous solution are mixed with 2.375 mL of ultrapure water, and 1 μL of 1 mM nitric acid aqueous solution is further added. Thus, a liquid sample I was prepared.
(II) NaNO2+H2O2+リン酸緩衝液、pH=7.25
液体サンプルIIは、200mMのNaNO2水溶液と200mMのH2O2水溶液と100mMのリン酸緩衝液とが混合された、pHが7.25の水溶液である。具体的には、まず、NaH2PO4・2H2OとNaHPO4とを用いて、pHが7.25で、100mMのリン酸緩衝液を5mL調整した。当該リン酸緩衝液に、42.5mLの超純水を添加し、上記200mMのNaNO2水溶液を1.25mLと、上記200mMのH2O2水溶液を1.25mLとを混合することにより、液体サンプルIIを作製した。
(II) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 7.25
The liquid sample II is an aqueous solution having a pH of 7.25 in which a 200 mM NaNO 2 aqueous solution, a 200 mM H 2 O 2 aqueous solution, and a 100 mM phosphate buffer are mixed. Specifically, first, using NaH 2 PO 4 .2H 2 O and NaHPO 4 , 5 mL of a 100 mM phosphate buffer solution having a pH of 7.25 was adjusted. By adding 42.5 mL of ultrapure water to the phosphate buffer and mixing 1.25 mL of the 200 mM NaNO 2 aqueous solution and 1.25 mL of the 200 mM H 2 O 2 aqueous solution, Sample II was made.
(III)NaNO2+H2O2+リン酸緩衝液、pH=2
液体サンプルIIIは、液体サンプルIIが酸性化されたpH2の水溶液である。具体的には、2.5mLの液体サンプルIIに、2000mg/Lのインディゴカーミン水溶液を12.5μL混合し、10μLの4.5NのH2SO4液を混合することにより、液体サンプルIIIを作製した。
(III) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 2
Liquid sample III is a
(IV) NaNO2+H2O2+リン酸緩衝液、pH=2.5
液体サンプルIVは、液体サンプルIIが酸性化されたpHが2.5の水溶液である。上記H2SO4液の添加量が6μLである点を除いて、液体サンプルIIIと同様にして、液体サンプルIVを作製した。
(IV) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 2.5
The liquid sample IV is an aqueous solution having a pH of 2.5 obtained by acidifying the liquid sample II. A liquid sample IV was prepared in the same manner as the liquid sample III except that the amount of the H 2 SO 4 solution added was 6 μL.
(V) NaNO2+H2O2+リン酸緩衝液、pH=3
液体サンプルVは、液体サンプルIIが酸性化されたpHが3の水溶液である。上記H2SO4液の添加量が5μLである点を除いて、液体サンプルIIIと同様にして、液体サンプルVを作製した。
(V) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 3
The liquid sample V is an aqueous solution having a pH of 3 obtained by acidifying the liquid sample II. A liquid sample V was prepared in the same manner as the liquid sample III except that the amount of the H 2 SO 4 liquid added was 5 μL.
(VI) NaNO2+H2O2+リン酸緩衝液、pH=6
液体サンプルVIは、液体サンプルIIが酸性化されたpHが6の水溶液である。上記H2SO4液の添加量が2.5μLである点を除いて、液体サンプルIIIと同様にして、液体サンプルVIを作製した。
(VI) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 6
The liquid sample VI is an aqueous solution having a pH of 6 obtained by acidifying the liquid sample II. A liquid sample VI was prepared in the same manner as the liquid sample III except that the amount of the H 2 SO 4 liquid added was 2.5 μL.
(VII)NaNO2+H2O2+リン酸緩衝液、pH=8
液体サンプルVIIは、液体サンプルIIが中性化されたpHが8の水溶液である。上記H2SO4の代わりに、4.5NのNaOHを1.5μL混合することにより、液体サンプルVIIを作製した。
(VII) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 8
The liquid sample VII is an aqueous solution having a pH of 8 in which the liquid sample II is neutralized. Instead of H 2 SO 4 , liquid sample VII was prepared by mixing 1.5 μL of 4.5 N NaOH.
(VIII)NaNO2+H2O2+リン酸緩衝液、pH=8.5
液体サンプルVIIIは、液体サンプルIIがアルカリ性化されたpHが8.5の水溶液である。上記H2SO4の代わりに、4.5NのNaOHを2μL混合することにより、液体サンプルVIIIを作製した。
(VIII) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 8.5
The liquid sample VIII is an aqueous solution having a pH of 8.5 obtained by alkalizing the liquid sample II. Instead of H 2 SO 4 , liquid sample VIII was prepared by mixing 2 μL of 4.5 N NaOH.
(IX) NaNO2+H2O2+リン酸緩衝液、pH=11
液体サンプルIXは、液体サンプルIIがアルカリ性化されたpHが11の水溶液である。上記H2SO4の代わりに、4.5NのNaOHを4μL混合することにより、液体サンプルIXを作製した。
(IX) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 11
The liquid sample IX is an aqueous solution having a pH of 11 obtained by alkalizing the liquid sample II. Instead of H 2 SO 4 , liquid sample IX was prepared by mixing 4 μL of 4.5 N NaOH.
(X) NaNO2+H2O2+リン酸緩衝液、pH=11.5
液体サンプルXは、液体サンプルIIがアルカリ性化されたpHが11.5の水溶液である。上記H2SO4の代わりに、4.5NのNaOHを7.5μL混合することにより、液体サンプルXを作製した。
(X) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 11.5
The liquid sample X is an aqueous solution having a pH of 11.5 obtained by alkalizing the liquid sample II. Instead of H 2 SO 4 , liquid sample X was prepared by mixing 7.5 μL of 4.5 N NaOH.
(XI) NaNO2+H2O2+リン酸緩衝液、pH=12
液体サンプルXIは、液体サンプルIIがアルカリ性化されたpHが12の水溶液である。上記H2SO4の代わりに、4.5NのNaOHを14μL混合することにより、液体サンプルXIを作製した。
(XI) NaNO 2 + H 2 O 2 + phosphate buffer, pH = 12
The liquid sample XI is an aqueous solution having a pH of 12 obtained by alkalizing the liquid sample II. A liquid sample XI was prepared by mixing 14 μL of 4.5 N NaOH instead of H 2 SO 4 .
(XII)NaNO2+H2O2+酢酸緩衝液、pH=4
液体サンプルXIIは、液体サンプルIと酢酸緩衝液とが混合された、pHが4の水溶液である。具体的には、まず、酢酸(CH3COOH)と超純水とを混合することで、2Mの酢酸水溶液を作製し、当該酢酸水溶液1mLあたり60μLで4.5NのNaOHを混合することにより、pHが4の酢酸緩衝液を調整した。2.2mLの液体サンプルIに、インディゴカーミン水溶液11μLと酢酸緩衝液11μLとを混合することにより、液体サンプルXIIを作製した。
(XII) NaNO 2 + H 2 O 2 + acetic acid buffer, pH = 4
The liquid sample XII is an aqueous solution having a pH of 4 in which the liquid sample I and an acetate buffer are mixed. Specifically, first, acetic acid (CH 3 COOH) and ultrapure water are mixed to prepare a 2M acetic acid aqueous solution, and by mixing 4.5 N NaOH at 60 μL per 1 mL of the acetic acid aqueous solution, A
(XIII)NaNO2+H2O2+酢酸緩衝液、pH=5
液体サンプルXIIIは、液体サンプルIと酢酸緩衝液とが混合された、pHが5の水溶液である。上記NaOHの添加量が1mLあたり280μLである点を除いて、液体サンプルXIIと同様にして、液体サンプルXIIIを作製した。
(XIII) NaNO 2 + H 2 O 2 + acetic acid buffer, pH = 5
The liquid sample XIII is an aqueous solution having a pH of 5 in which the liquid sample I and an acetate buffer are mixed. A liquid sample XIII was prepared in the same manner as the liquid sample XII except that the amount of NaOH added was 280 μL per mL.
(XIV)NaNO2+H2O2+酢酸緩衝液、pH=5.5
液体サンプルXIVは、液体サンプルIと酢酸緩衝液とが混合された、pHが5.5の水溶液である。上記NaOHの添加量が1mLあたり380μLである点を除いて、液体サンプルXIIと同様にして、液体サンプルXIVを作製した。
(XIV) NaNO 2 + H 2 O 2 + acetic acid buffer, pH = 5.5
The liquid sample XIV is an aqueous solution having a pH of 5.5, in which the liquid sample I and an acetate buffer are mixed. A liquid sample XIV was produced in the same manner as the liquid sample XII except that the amount of NaOH added was 380 μL per mL.
(XV) NaNO2+H2O2+ホウ酸緩衝液、pH=9
液体サンプルXVは、液体サンプルIとホウ酸緩衝液とが混合された、pHが9の水溶液である。具体的には、まず、ホウ酸(H3BO3)と超純水とを混合することで、0.5Mのホウ酸水溶液を作製し、当該ホウ酸水溶液1mLに対して40μLの比率で4.5NのNaOHを混合することにより、pHが9のホウ酸緩衝液を作製した。2.2mLの液体サンプルIに、インディゴカーミン水溶液11μLとホウ酸緩衝液44μLとを混合することにより、液体サンプルXVを作製した。
(XV) NaNO 2 + H 2 O 2 + borate buffer, pH = 9
The liquid sample XV is an aqueous solution having a pH of 9 in which the liquid sample I and a borate buffer are mixed. Specifically, first, boric acid (H 3 BO 3 ) and ultrapure water are mixed to prepare a 0.5 M boric acid aqueous solution, and a ratio of 40 μL with respect to 1 mL of the boric acid aqueous solution. A borate buffer with a pH of 9 was made by mixing 5N NaOH. Liquid sample XV was prepared by mixing 11 μL of indigo carmine aqueous solution and 44 μL of borate buffer solution with 2.2 mL of liquid sample I.
(XVI)NaNO2+H2O2+ホウ酸緩衝液、pH=10
液体サンプルXVIは、液体サンプルIとホウ酸緩衝液とが混合された、pHが10の水溶液である。上記NaOHの添加量が1mLあたり90μLである点を除いて、液体サンプルXVと同様にして、液体サンプルXVIを作製した。
(XVI) NaNO 2 + H 2 O 2 + borate buffer, pH = 10
The liquid sample XVI is an aqueous solution having a pH of 10 in which the liquid sample I and a borate buffer are mixed. A liquid sample XVI was prepared in the same manner as the liquid sample XV, except that the amount of NaOH added was 90 μL per mL.
[4−2.試験結果]
以上の16種類の液体サンプルI〜XVIを用いたインディゴカーミンの分解試験の結果を図4A及び図4Bに示す。図4Aは、実施例に係る水溶液を酸性化した場合のインディゴカーミンの分解試験の結果を示す図である。図4Bは、実施例に係る水溶液をアルカリ性化した場合のインディゴカーミンの分解試験の結果を示す図である。図4A及び図4Bにおいて、横軸は分解時間であり、縦軸は吸光度を示している。なお、横軸の分解時間は、I、II、XII〜XVIでは溶液にインディゴカーミンを添加した時点、及び、III〜XIでは液体のpHを変化させた時点からの時間である。
[4-2. Test results]
The results of the indigo carmine degradation test using the above 16 types of liquid samples I to XVI are shown in FIGS. 4A and 4B. FIG. 4: A is a figure which shows the result of the decomposition | disassembly test of indigo carmine at the time of acidifying the aqueous solution which concerns on an Example. FIG. 4B is a diagram illustrating a result of an indigo carmine decomposition test when the aqueous solution according to the example is alkalized. 4A and 4B, the horizontal axis represents the decomposition time, and the vertical axis represents the absorbance. The decomposition time on the horizontal axis is the time from when indigo carmine is added to the solution for I, II, and XII to XVI, and from the time when the pH of the liquid is changed for III to XI.
図4Aには、中性の液体サンプルI及びVIと、酸性の液体サンプルIII〜V及びXII〜XIVとの各々の吸光度の時間変化を示している。図4Aから分かるように、中性の液体サンプルI及びVIでは、吸光度は分解時間に対して略一定であり、インディゴカーミンがほとんど分解されていないことが分かる。 In FIG. 4A, the time change of each light absorbency of neutral liquid samples I and VI and acidic liquid samples III-V and XII-XIV is shown. As can be seen from FIG. 4A, in the neutral liquid samples I and VI, the absorbance is substantially constant with respect to the decomposition time, and it can be seen that indigo carmine is hardly decomposed.
一方で、酸性の液体サンプルIII〜V及びXII〜XIVでは、吸光度は分解時間が経過するにつれて低下している。具体的には、pHが小さい程、吸光度の低下の割合が大きく、インディゴカーミンの分解速度が速いことが分かる。特に、pHが4以下の液体サンプルXII及びIII〜Vでは、急激に吸光度が低下していることから、インディゴカーミンの分解は急速に進んだことが分かる。 On the other hand, in the acidic liquid samples III to V and XII to XIV, the absorbance decreases as the decomposition time elapses. Specifically, it can be seen that the smaller the pH, the greater the rate of decrease in absorbance and the faster the decomposition rate of indigo carmine. In particular, in the liquid samples XII and III to V having a pH of 4 or less, it can be seen that the decomposition of indigo carmine progressed rapidly because the absorbance decreased rapidly.
以上のことから、亜硝酸イオンと過酸化水素とを混合した水溶液を酸性化することで、当該水溶液が高い分解力を発揮することが確認された。このとき、緩衝成分は、リン酸及び酢酸のいずれでもよく、特に限定されないことも確認できる。 From the above, it was confirmed that the aqueous solution exhibits high decomposing power by acidifying an aqueous solution in which nitrite ions and hydrogen peroxide are mixed. At this time, the buffer component may be either phosphoric acid or acetic acid, and it can be confirmed that there is no particular limitation.
図4Bには、中性の液体サンプルI、II及びVIIと、アルカリ性の液体サンプルVII〜XI、XV及びXVIとの各々の吸光度の時間変化を示している。図4Bから分かるように、中性の液体サンプルI、II及びVIIでは、吸光度は分解時間に対して略一定であり、インディゴカーミンが分解されていないことが分かる。なお、pHが8の液体サンプルVIIでは、吸光度が僅かに低下しており、インディゴカーミンの分解が緩やかに進行していることが確認された。 FIG. 4B shows changes in absorbance of the neutral liquid samples I, II and VII and the alkaline liquid samples VII to XI, XV and XVI over time. As can be seen from FIG. 4B, in the neutral liquid samples I, II, and VII, it can be seen that the absorbance is substantially constant with respect to the decomposition time, and indigo carmine is not decomposed. In the liquid sample VII having a pH of 8, the absorbance was slightly decreased, and it was confirmed that the decomposition of indigo carmine was slowly progressing.
一方で、アルカリ性の液体サンプルVII〜XI、XV及びXVIでは、吸光度は分解時間が経過するにつれて低下している。具体的には、pHが大きい程、吸光度の低下の割合が大きく、インディゴカーミンの分解速度が速いことが分かる。特に、pHが11以上の液体サンプルIX〜XIでは、急激に吸光度が低下していることから、インディゴカーミンの分解は急速に進んだことが分かる。 On the other hand, in the alkaline liquid samples VII to XI, XV, and XVI, the absorbance decreases as the decomposition time elapses. Specifically, it can be seen that the greater the pH, the greater the rate of decrease in absorbance and the faster the decomposition rate of indigo carmine. In particular, in the liquid samples IX to XI having a pH of 11 or more, it can be seen that the decomposition of indigo carmine progressed rapidly since the absorbance decreased rapidly.
以上のことから、亜硝酸イオンと過酸化水素とを混合した水溶液をアルカリ性化することで、当該水溶液が高い分解力を発揮することが確認された。このとき、緩衝成分は、リン酸及びホウ酸のいずれでもよく、特に限定されないことも確認できる。 From the above, it was confirmed that the aqueous solution exhibits high decomposing power by making the aqueous solution obtained by mixing nitrite ions and hydrogen peroxide alkaline. At this time, the buffer component may be either phosphoric acid or boric acid, and it can be confirmed that there is no particular limitation.
図5Aは、実施例に係る水溶液のpHとインディゴカーミンの分解率(分解速度)との関係を示す図である。図5Bは、図5Aに示す分解率を説明するための図である。 FIG. 5A is a graph showing the relationship between the pH of the aqueous solution according to the example and the decomposition rate (decomposition rate) of indigo carmine. FIG. 5B is a diagram for explaining the decomposition rate shown in FIG. 5A.
インディゴカーミンの分解率(分解速度)は、インディゴカーミンの濃度の時間変化で示される。具体的には、図5Bに示すように、分解開始後15秒の時点での吸光度曲線の傾き(すなわち、吸光度の変化率)をインディゴカーミンの濃度の時間変化(すなわち、分解率)に変換した。より具体的には、吸光度曲線の傾きに、インディゴカーミンの濃度に対する吸光度の検量線から算出した係数(2.72ppm/abs)を乗ずることにより、濃度の時間変化を算出した。なお、pHが2より小さい、又は、12より大きい範囲では、分解速度が速すぎたために正確な測定ができなかった。 The degradation rate (degradation rate) of indigo carmine is indicated by the change over time in the concentration of indigo carmine. Specifically, as shown in FIG. 5B, the slope of the absorbance curve (that is, the rate of change in absorbance) at the point of 15 seconds after the start of degradation was converted to the time change in the concentration of indigo carmine (ie, the rate of degradation). . More specifically, the change with time in concentration was calculated by multiplying the slope of the absorbance curve by a coefficient (2.72 ppm / abs) calculated from a calibration curve of absorbance with respect to the concentration of indigo carmine. In addition, in the range where pH is less than 2 or more than 12, accurate measurement was not possible because the decomposition rate was too high.
図5Aに示すように、pHが6より小さい、又は、9より大きい範囲の液体サンプルでは、分解率が0より大きくなっている。特に、pHが4より小さい、又は、10より大きい範囲の液体サンプルでは、分解率が大きく、当該液体サンプルは、十分に高い分解能力を有していることが分かる。 As shown in FIG. 5A, the degradation rate is larger than 0 in the liquid sample whose pH is smaller than 6 or larger than 9. In particular, a liquid sample having a pH of less than 4 or greater than 10 has a high decomposition rate, and it can be seen that the liquid sample has a sufficiently high decomposition ability.
また、図4A及び図4Bに示したように、pHが5、5.5、8及び8.5の場合においても、インディゴカーミンが分解されたことを確認できた。また、pHが6の場合も図4Aに示すように、僅かではあるがインディゴカーミンの分解が進んでいる。以上のことから、本実施の形態に係る水溶液のpHを6より小さく、又は、8より大きく調整することで、当該水溶液が高い活性(分解力)を発揮することができる。 Further, as shown in FIGS. 4A and 4B, it was confirmed that indigo carmine was decomposed even when the pH was 5, 5.5, 8, and 8.5. In addition, even when the pH is 6, as shown in FIG. 4A, the decomposition of indigo carmine is proceeding, albeit slightly. From the above, by adjusting the pH of the aqueous solution according to the present embodiment to be smaller than 6 or larger than 8, the aqueous solution can exhibit high activity (decomposition power).
[5.保管可能性]
続いて、本実施の形態に係る水溶液の保管可能性について説明する。
[5. Storage possibility]
Then, the storage possibility of the aqueous solution which concerns on this Embodiment is demonstrated.
本発明者は、本実施の形態に係る水溶液の保管可能性を確認するため、数種類の液体サンプルを作製し、10日間、常温で放置した。液体サンプルの作製直後と10日間放置後とにおける亜硝酸イオンの濃度をイオンクロマトグラフィーによって測定し、かつ、過酸化水素の濃度の変化を比色法で測定した。表2に測定結果を示す。 In order to confirm the storage possibility of the aqueous solution according to the present embodiment, the present inventor prepared several types of liquid samples and left them at room temperature for 10 days. The concentration of nitrite ion immediately after the preparation of the liquid sample and after standing for 10 days was measured by ion chromatography, and the change in the concentration of hydrogen peroxide was measured by a colorimetric method. Table 2 shows the measurement results.
まず、200mMのNaNO2水溶液と200mMのH2O2水溶液と超純水とを混合することで、100mMのNaNO2水溶液と100mMのH2O2水溶液との混合溶液(a)を作製した。当該混合溶液を超純水で10倍又は100倍希釈することで、それぞれ10mMのNaNO2水溶液と10mMのH2O2水溶液との混合溶液(b)と、1mMのNaNO2水溶液と1mMのH2O2水溶液との混合溶液(c)とを作製した。
First, a mixed solution (a) of a 100 mM NaNO 2 aqueous solution and a 100 mM H 2 O 2 aqueous solution was prepared by mixing a 200 mM NaNO 2 aqueous solution, a 200 mM H 2 O 2 aqueous solution, and ultrapure water. By diluting the
さらに、混合溶液(a)〜(c)の各々に、pHが7.2で1Mのリン酸緩衝液を体積比100:1(=混合溶液(a)〜(c):リン酸緩衝液)で混合することで、混合溶液(d)〜(e)を作製した。すなわち、混合溶液(d)は、100mMのNaNO2水溶液と100mMのH2O2水溶液とリン酸緩衝液との混合溶液である。混合溶液(e)は、10mMのNaNO2水溶液と10mMのH2O2水溶液とリン酸緩衝液との混合溶液である。混合溶液(f)は、1mMのNaNO2水溶液と1mMのH2O2水溶液とリン酸緩衝液との混合溶液である。 Furthermore, 1M phosphate buffer having a pH of 7.2 is added to each of the mixed solutions (a) to (c) at a volume ratio of 100: 1 (= mixed solution (a) to (c): phosphate buffer). Were mixed to prepare mixed solutions (d) to (e). That is, the mixed solution (d) is a mixed solution of a 100 mM NaNO 2 aqueous solution, a 100 mM H 2 O 2 aqueous solution, and a phosphate buffer. The mixed solution (e) is a mixed solution of a 10 mM NaNO 2 aqueous solution, a 10 mM H 2 O 2 aqueous solution, and a phosphate buffer. The mixed solution (f) is a mixed solution of a 1 mM NaNO 2 aqueous solution, a 1 mM H 2 O 2 aqueous solution, and a phosphate buffer.
表2において、pHは、混合溶液の作製直後のpHである。NO2 −初期値比は、混合溶液の作製直後に対する10日間の放置後のNO2 −の濃度の比を示している。H2O2初期値比についても同様である。 In Table 2, the pH is the pH immediately after preparation of the mixed solution. NO 2 - initial value ratio, NO 2 after standing for 10 days for immediately after the production of the mixed solution - represents the ratio of the concentrations. The same applies to the H 2 O 2 initial value ratio.
表2に示すように、リン酸緩衝液を混合していない混合溶液(a)〜(c)では、亜硝酸イオンが増加し、過酸化水素が75%以下に減少していることが分かる。上述した通り、当モルの亜硝酸イオン及び過酸化水素から当モルのペルオキシ亜硝酸が生成されるので、過酸化水素の濃度が減少することにより、生成されるペルオキシ亜硝酸の量も減少する。このため、作製直後に比べて酸性化又はアルカリ性化した際の混合溶液の活性が低下する。 As shown in Table 2, it can be seen that in the mixed solutions (a) to (c) in which the phosphate buffer was not mixed, nitrite ions increased and hydrogen peroxide decreased to 75% or less. As described above, since equimolar peroxynitrite is produced from equimolar nitrite ions and hydrogen peroxide, decreasing the concentration of hydrogen peroxide also reduces the amount of peroxynitrite produced. For this reason, compared with immediately after preparation, the activity of the mixed solution when acidified or alkalized is lowered.
一方で、リン酸緩衝液を混合して中性化した混合溶液(d)〜(f)では、過酸化水素が若干減少してはいるものの、85%以上の濃度を保っている。また、亜硝酸イオンについても増加又は減少が見られるが、90%以上の濃度を保っている。このように、リン酸緩衝液を加えない場合に比べて、亜硝酸イオンの減少を十分に抑制することができていることが分かる。 On the other hand, in the mixed solutions (d) to (f) neutralized by mixing the phosphate buffer, the concentration of 85% or more is maintained although the hydrogen peroxide is slightly decreased. Moreover, although the increase or decrease is seen also about nitrite ion, the density | concentration of 90% or more is maintained. Thus, it turns out that the reduction | decrease of nitrite ion can fully be suppressed compared with the case where a phosphate buffer solution is not added.
以上のことから、リン酸緩衝液などの緩衝成分を加えて中性化することで、亜硝酸イオンと過酸化水素とを含む混合溶液を長期間保管することができる。保管された水溶液は、除菌などの目的に使用する際に、水溶液のpHを調整することで、酸化力を発揮させることができる。 From the above, a mixed solution containing nitrite ions and hydrogen peroxide can be stored for a long period of time by adding a buffer component such as a phosphate buffer to neutralize it. When the stored aqueous solution is used for the purpose of sterilization or the like, the oxidizing power can be exhibited by adjusting the pH of the aqueous solution.
[6.除菌試験]
以下では、本発明者が、本実施の形態に係る水溶液を用いて行った除菌試験について説明する。表3に、試験結果を示す。除菌試験は、上述した液体サンプルA〜Cを用いて行った。
[6. Disinfection test]
Hereinafter, a sterilization test performed by the inventor using the aqueous solution according to the present embodiment will be described. Table 3 shows the test results. The sterilization test was performed using the liquid samples A to C described above.
除菌試験について説明する。まず、試料水に所定量の大腸菌を混合して、104cfuとなるように調整された菌液を生成した。試料水は、表3に示す通りである。 The sterilization test will be described. First, a predetermined amount of Escherichia coli was mixed with sample water to produce a bacterial solution adjusted to 10 4 cfu. The sample water is as shown in Table 3.
スパイラルプレーターを用いて標準寒天培地上に1mLの菌液を散布した後、所定時間毎に反応停止処理を行った。具体的には、10秒、30秒、60秒、120秒、300秒、600秒、30分、1時間毎に反応停止処理を行った。反応停止処理は、試料水が酸性又はアルカリ性の場合は、中和処理(塩基又は酸を2.33μL添加)を行った。 After spraying 1 mL of the bacterial solution on the standard agar medium using a spiral plater, the reaction was stopped every predetermined time. Specifically, the reaction stop process was performed every 10 seconds, 30 seconds, 60 seconds, 120 seconds, 300 seconds, 600 seconds, 30 minutes, and 1 hour. When the sample water was acidic or alkaline, the reaction stop treatment was neutralized (added 2.33 μL of base or acid).
反応停止処理の後、恒温槽(30℃)を用いて16時間培養した。その後、コロニーカウンタを用いて菌数をカウントした。 After the reaction termination treatment, the cells were cultured for 16 hours using a thermostatic bath (30 ° C.). Thereafter, the number of bacteria was counted using a colony counter.
表3に示すように、亜硝酸と過酸化水素との混合緩衝液(液体サンプルA)を酸性化した場合、除菌時間が約10秒であった。これに対して、亜硝酸のみを含有する緩衝液(液体サンプルB)を酸性化した場合、除菌時間が約2.5分であった。したがって、液体サンプルAの方が、除菌効果が高いことが分かる。なお、除菌時間とは、菌液と接触後に、生菌率が1%になるまでの時間として測定した。 As shown in Table 3, when the mixed buffer solution (liquid sample A) of nitrous acid and hydrogen peroxide was acidified, the sterilization time was about 10 seconds. On the other hand, when the buffer solution (liquid sample B) containing only nitrous acid was acidified, the sterilization time was about 2.5 minutes. Therefore, it can be seen that the liquid sample A has a higher sterilization effect. The sterilization time was measured as the time until the viable cell rate reached 1% after contact with the bacterial solution.
また、亜硝酸と過酸化水素との混合緩衝液(液体サンプルA)をアルカリ性化した場合、除菌時間は約5分であった。これに対して、過酸化水素のみを含有する緩衝液(液体サンプルC)をアルカリ性化した場合、除菌時間が約8分であった。したがって、液体サンプルAと液体サンプルCとでは、アルカリ性化する場合には、除菌時間がいずれも10分以下であり、略同等の除菌力を有することが分かる。なお、大腸菌に対してはpHが酸性、アルカリ性となるだけでも除菌効果があるが上記のような構成とすることにより、より短時間で除菌を行うことができる。 Further, when the mixed buffer solution of nitrous acid and hydrogen peroxide (liquid sample A) was made alkaline, the sterilization time was about 5 minutes. On the other hand, when the buffer solution containing only hydrogen peroxide (liquid sample C) was made alkaline, the sterilization time was about 8 minutes. Therefore, it can be seen that when the liquid sample A and the liquid sample C are made alkaline, the sterilization time is 10 minutes or less, and they have substantially the same sterilization power. In addition, although E. coli has a sterilizing effect even if the pH becomes acidic or alkaline, it can be sterilized in a shorter time by using the above-described configuration.
これに対して、中性の液体サンプルA〜Cのいずれも、1時間経過後において生菌率が1%に達することがなく、除菌を行うことができなかった。 On the other hand, all of the neutral liquid samples A to C did not reach 1% after 1 hour, and could not be sterilized.
以上のように、本実施の形態に係る亜硝酸イオン、過酸化水素及び緩衝成分を含有する水溶液は、酸性化又はアルカリ性化された場合に、除菌に利用することができることが分かる。また、この結果は、他の実験で生成した液体サンプルの場合でも同様に除菌に利用できることを示唆している。 As described above, it can be seen that the aqueous solution containing nitrite ions, hydrogen peroxide, and a buffer component according to the present embodiment can be used for sterilization when acidified or alkalinized. In addition, this result suggests that liquid samples produced in other experiments can be used for sterilization as well.
(実施の形態2)
以下では、実施の形態2に係る対象物処理装置及びその動作(すなわち、対象物処理方法)について説明する。
(Embodiment 2)
Below, the target object processing apparatus which concerns on
[1.構成]
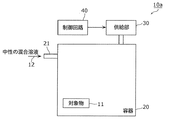
図6は、本実施の形態に係る対象物処理装置10の構成を示す図である。本実施の形態に係る対象物処理装置は、上記の実施の形態1に係る水溶液(亜硝酸イオン、過酸化水素及び緩衝成分の混合溶液)を利用して、菌などの対象物11を処理する装置である。
[1. Constitution]
FIG. 6 is a diagram showing a configuration of the
対象物11は、実施の形態1によって分解(又は、死滅)される物質である。具体的には、対象物11は、有機物、微生物又は細菌である。
The
図6に示すように、対象物処理装置10は、容器20と、供給部30と、制御回路40と、接触部50とを備える。以下では、対象物処理装置10を構成する各構成要素について、詳細に説明する。
As illustrated in FIG. 6, the
[1−1.容器]
容器20は、液体を収容するための容器である。容器20には、液体を供給するための供給口21と、液体を排出するための排出口22とが設けられている。
[1-1. container]
The
容器20は、例えば、酸又はアルカリに耐性を有する材料から形成される。例えば、容器20は、ポリ塩化ビニル、テトラフルオロエチレン(PFA)などの樹脂材料、ステンレスなどの金属材料、又は、セラミックなどから形成される。容器20の大きさ及び形状は、特に限定されない。
The
排出口22には、開閉自在なバルブ23が設けられている。本実施の形態では、バルブ23は、制御回路40によって開閉が制御される。なお、バルブ23は、ユーザによって手動で開閉されてもよい。また、供給口21にも同様のバルブが設けられていてもよい。
The
本実施の形態では、供給口21を介して、上記の実施の形態1に係る中性の混合溶液12が容器20内に入れられる。中性の混合溶液12は、主たる成分として、亜硝酸イオン、過酸化水素及び緩衝成分を含有する、pHが6以上8以下の水溶液である。緩衝成分は、pHが6以上8以下の範囲に緩衝性を有する物質であり、例えば、リン酸である。
In the present embodiment, the neutral
実施の形態1で説明したように、中性の混合溶液12は保管が可能であるので、容器20内で一定の期間保管することもできる。すなわち、容器20は、混合溶液12の保管容器として利用してもよい。
As described in
[1−2.供給部]
供給部30は、容器20内の液体のpHを調整するためのpH調整物質を、容器20内に供給する。供給部30は、例えば、制御回路40からの指示に基づいて、所定のタイミングで所定量のpH調整物質を容器20内に供給する。供給部30は、pH調整物質として、例えば酸、塩基又は塩を含む溶液を容器20内に供給することで、容器20に貯められる混合溶液12のpHを調整する。
[1-2. Supply section]
The
供給部30は、例えば、pH調整物質を収容するための容器と、当該容器に接続され、容器20にpH調整物質を供給するためのポンプ及び/又はバルブを備える。例えば、制御回路40がポンプを制御することで、pH調整物質が収容された容器と、中性の混合溶液12が収容された容器20との圧力差が調整される。また、制御回路40がバルブの開閉動作を制御することで、供給部30は、所定のタイミングでpH調整物質を容器20内に供給する。
The
本実施の形態では、pH調整物質は、(i)酸、塩基若しくは塩、(ii)酸、塩基若しくは塩の少なくとも1つを含む溶液、(iii)溶解して酸若しくは塩基となる気体若しくは固体、又は、(iv)当該気体若しくは当該液体又は固体を発生する生物を含む溶液である。具体的には、pH調整物質は、硫酸(H2SO4)、硝酸(HNO3)などの酸、水酸化ナトリウム(NaOH)、アンモニア(NH3)水溶液などの塩基、又は、硫酸アルミニウム(Al2(SO4)3)、塩化マグネシウム(MgCl2)などの塩である。 In the present embodiment, the pH adjusting substance is (i) an acid, a base or a salt, (ii) a solution containing at least one of an acid, a base or a salt, (iii) a gas or a solid which dissolves into an acid or a base Or (iv) a solution containing an organism that generates the gas or the liquid or solid. Specifically, the pH adjusting substance may be an acid such as sulfuric acid (H 2 SO 4 ) or nitric acid (HNO 3 ), a base such as an aqueous solution of sodium hydroxide (NaOH) or ammonia (NH 3 ), or aluminum sulfate (Al 2 (SO 4 ) 3 ) and magnesium chloride (MgCl 2 ).
[1−3.制御回路]
制御回路40は、供給部30を制御する。具体的には、制御回路40は、供給部30から容器20に供給するpH調整物質の供給量及び供給タイミングを制御する。
[1-3. Control circuit]
The
本実施の形態では、制御回路40は、容器20内に中性の混合溶液12が入れられている場合に、供給部30にpH調整物質を容器20内に供給させる。これにより、例えば、容器20内で中性の混合溶液12とpH調整物質とが混合されて、混合溶液12のpHが調整される。例えばpHが6より小さく、又は、8より大きく調整された混合溶液13が排出口22を介して外部に排出され、対象物11と接触する。上記の実施の形態1で示したように、酸性化又はアルカリ性化された混合溶液13は、高い活性(分解力)を有するので、対象物11を分解することができる。
In the present embodiment, the
本実施の形態では、制御回路40は、さらに、排出口22に設けられたバルブ23の開閉を制御する。具体的には、容器20内で中性の混合溶液12が酸性化又はアルカリ性化された後に、制御回路40は、バルブ23を開けることで、酸性化又はアルカリ性化された混合溶液13を接触部50に供給する。
In the present embodiment, the
制御回路40は、例えば、プログラムが格納された不揮発性メモリと、プログラムを実行するプロセッサとを備える。制御回路40は、さらに、プログラムを実行するための一時的な記憶領域である揮発性メモリと、入出力ポートとを備えてもよい。制御回路40は、例えば、マイコン(マイクロコントローラ又はマイクロコンピュータ)である。
The
[1−4.接触部]
接触部50は、容器20内でpHが調整された混合溶液13を対象物11に接触させるための部分である。本実施の形態では、接触部50は、容器20の排出口22にバルブ23を介して接続されている。
[1-4. Contact part]
The
接触部50は、例えば、対象物11を入れる容器である。排出口22を介して混合溶液13が接触部50内に入れられることで、混合溶液13を対象物11に接触させることができる。なお、接触部50は、スプレーなどの噴出器でもよい。この場合、接触部50は、混合溶液13を対象物11に向けて噴出することで、混合溶液13を対象物11に接触させることができる。
The
接触部50は、例えば、対象物11を含む物体に混合溶液13を接触させる。対象物11を含む物体は、例えば、食器類などの生活用品、医療機器、又は、浴室の床若しくは窓ガラスなどの建材である。あるいは、対象物11を含む物体は、虫歯菌若しくは歯周病菌などを対象物11として含む人体の口腔、又は、腐敗菌などを対象物11として含む食品若しくは動植物などである。
The
[2.動作(対象物処理方法)]
続いて、本実施の形態に係る対象物処理装置10の動作(すなわち、対象物処理方法)について、図7を用いて説明する。図7は、本実施の形態に係る対象物処理装置10の動作を示すフローチャートである。
[2. Operation (object processing method)]
Subsequently, the operation (that is, the object processing method) of the
まず、亜硝酸イオン及び過酸化水素を含む中性の水溶液を準備する(S10)。具体的には、図6に示す混合溶液12を準備する。ここで、混合溶液12を準備するとは、混合溶液12を生成するだけでなく、混合溶液12を調達する意味も含んでいる。本実施の形態では、混合溶液12の準備として、供給口21を介して混合溶液12を容器20内に入れる。
First, a neutral aqueous solution containing nitrite ions and hydrogen peroxide is prepared (S10). Specifically, a
次に、準備した水溶液のpHを6より小さく、又は、8より大きく調整する(S12)。具体的には、制御回路40が供給部30を制御することで、pH調整物質を容器20内に供給する。これにより、容器20内で混合溶液12とpH調整物質とを混合させることにより、混合溶液12のpHを6より小さく(酸性化)、又は、8より大きく(アルカリ性化)調整する。
Next, the pH of the prepared aqueous solution is adjusted to be smaller than 6 or larger than 8 (S12). Specifically, the
なお、混合溶液12のpHを調整する程度は、例えば、調整後の混合溶液13に要求される酸化力に応じて決定される。例えば、より強い酸化力が必要な場合には、pHがより小さくなるように、供給部30から多量の酸を供給してもよい。あるいは、弱い酸化力が必要な場合には、pHが中性に近い値になるように、供給部30から少量の酸又は塩基などを供給してもよい。pH調整物質の種類及び供給量は、例えば、対象物11の種類によって決定されてもよい。
In addition, the grade which adjusts the pH of the
次に、pHを調整した後の水溶液を対象物11に接触させる(S14)。具体的には、制御回路40がバルブ23を開けることで、酸性化又はアルカリ性化された混合溶液13を接触部50に供給する。これにより、接触部50内で混合溶液13と対象物11とが接触し、対象物11の分解が行われる。
Next, the aqueous solution after adjusting the pH is brought into contact with the object 11 (S14). Specifically, the
以上のように、本実施の形態では、対象物11に接触させるステップS14は、pHを調整するステップS12の後に行われる。これにより、活性を高めた後の混合溶液13を対象物11に接触させるので、混合溶液13と対象物11との反応を制御することができる。例えば、混合溶液13と対象物11との反応速度などを調整することができる。
As mentioned above, in this Embodiment, step S14 made to contact the
なお、本実施の形態では、pH調整物質を供給することで、中性の混合溶液のpHを調整する例について説明したが、これに限らない。例えば、中性の混合溶液を電気分解することで、水溶液のpHを調整してもよい。例えば、図6に示す対象物処理装置10は、容器20内に配置された一対の電極対と、当該電極対間に電圧を印加するための電源とを備えてもよい。
In the present embodiment, an example in which the pH of a neutral mixed solution is adjusted by supplying a pH adjusting substance has been described, but the present invention is not limited thereto. For example, the pH of the aqueous solution may be adjusted by electrolyzing a neutral mixed solution. For example, the
また、本実施の形態では、供給口21から混合溶液12を容器20内に供給したが、容器20内で混合溶液12を生成してもよい。具体的には、供給口21などから亜硝酸イオンを含む第1溶液と、過酸化水素を含む第2溶液と、緩衝成分を含む第3溶液とを容器20内に供給し、容器20内で混合することで混合溶液12を生成してもよい。
Moreover, in this Embodiment, although the
(変形例)
以下では、上記の実施の形態2の変形例について説明する。
(Modification)
Below, the modification of said
図8は、本変形例に係る対象物処理装置10aの構成を示す図である。図8に示すように、本変形例に係る対象物処理装置10aでは、容器20内に対象物11が入れられている点が相違する。すなわち、対象物処理装置10aは、排出口22及び接触部50を備えていなくてもよい。以下では、上記の実施の形態2との相違点を中心に説明し、同じ点については、説明を省略又は簡略化する。
FIG. 8 is a diagram showing the configuration of the
本変形例では、容器20内に対象物11が入れられる。したがって、中性の混合溶液12のpHが調整する前に、混合溶液12と対象物11とが接触する。なお、対象物11は、例えば、混合溶液12に混合されて供給口21から容器20内に入れられる。あるいは、供給部30が対象物11を容器20内に入れてもよい。
In the present modification, the
図9は、本変形例に係る対象物処理装置10aの動作(対象物処理方法)を示すフローチャートである。図9に示すように、中性の水溶液(具体的には混合溶液12)を準備する工程は、実施の形態2と同様である。
FIG. 9 is a flowchart showing the operation (object processing method) of the
本変形例では、準備した水溶液を対象物11に接触させる(S22)。具体的には、容器20内で混合溶液12と対象物11とを接触させる。
In this modification, the prepared aqueous solution is brought into contact with the object 11 (S22). Specifically, the
次に、接触後の水溶液のpHを6より小さく、又は、8より大きく調整する(S24)。具体的には、制御回路40が供給部30を制御することで、pH調整物質を容器20内に供給する。これにより、容器20内で、対象物11と接触した混合溶液12とpH調整物質とを混合させることにより、混合溶液12のpHを6より小さく(酸性化)、又は、8より大きく(アルカリ性化)調整する。
Next, the pH of the aqueous solution after contact is adjusted to be smaller than 6 or larger than 8 (S24). Specifically, the
以上のように、本実施の形態では、混合溶液12のpHを調整するステップS24は、対象物11に接触させるステップS22の後に行われる。これにより、混合溶液12を対象物11に接触させた後に混合溶液12のpHを調整するので、混合溶液12の活性が高められると直ちに対象物11に作用することができる。したがって、対象物11の分解などを効率良く行うことができる。
As mentioned above, in this Embodiment, step S24 which adjusts pH of the
(他の実施の形態)
以上、1つ又は複数の態様に係る水溶液及び対象物処理方法について、実施の形態に基づいて説明したが、本開示は、これらの実施の形態に限定されるものではない。本開示の主旨を逸脱しない限り、当業者が思いつく各種変形を本実施の形態に施したもの、及び、異なる実施の形態における構成要素を組み合わせて構築される形態も、本開示の範囲内に含まれる。
(Other embodiments)
As mentioned above, although the aqueous solution and the target object processing method which concern on one or some aspect were demonstrated based on embodiment, this indication is not limited to these embodiment. Unless it deviates from the main point of this indication, the form which carried out various deformation | transformation which those skilled in the art thought to this embodiment, and the structure constructed | assembled combining the component in different embodiment is also included in the scope of this indication. It is.
例えば、上記の実施の形態2では、亜硝酸イオン、過酸化水素及び緩衝成分を含む混合溶液12のpHを6より小さく、又は、8より大きく調整したが、これに限らない。混合溶液12のpHを5より小さく、又は、9より大きく調整してもよい。また、混合溶液12は、緩衝成分を含んでいなくてもよい。例えば、混合溶液12を長期間保存しない場合などでは、緩衝成分を含まない混合溶液12を酸性化又はアルカリ性化することで、混合溶液12を酸性化又はアルカリ性化した際の活性を高め、対象物11を分解することができる。緩衝成分を含まない場合には、少量の酸又は塩基を添加するだけで、混合溶液12のpHを大きく調整することができる。
For example, in
また、例えば、上記の実施の形態では、薬剤を含む溶液を混合することで、亜硝酸イオン、過酸化水素及び緩衝成分を含む水溶液を生成したが、これに限らない。例えば、水道水などの液体をプラズマ処理することで、過酸化水素又は亜硝酸イオンなどを発生させた液体を用いてもよい。あるいは、ダイアモンド電極を用いた電解によって過酸化水素を発生させた溶液に亜硝酸塩を添加した液体を用いてもよい。あるいは、硝酸を含む溶液から硝酸還元菌によって亜硝酸を発生させた後に過酸化水素水を加えた液体を用いてもよい。つまり、亜硝酸イオンを含む第1溶液、過酸化水素を含む第2溶液、緩衝成分を含む第3溶液の各々の生成方法(準備方法)については、特に限定されない。 Further, for example, in the above-described embodiment, an aqueous solution containing nitrite ions, hydrogen peroxide, and a buffer component is generated by mixing a solution containing a drug. However, the present invention is not limited to this. For example, a liquid in which hydrogen peroxide or nitrite ions are generated by plasma treatment of a liquid such as tap water may be used. Alternatively, a liquid obtained by adding nitrite to a solution in which hydrogen peroxide is generated by electrolysis using a diamond electrode may be used. Alternatively, a liquid in which hydrogen peroxide is added after nitrous acid is generated by nitrate-reducing bacteria from a solution containing nitric acid may be used. That is, there are no particular limitations on the method (preparation method) for generating each of the first solution containing nitrite ions, the second solution containing hydrogen peroxide, and the third solution containing a buffer component.
また、上記の各実施の形態は、特許請求の範囲又はその均等の範囲において種々の変更、置き換え、付加、省略などを行うことができる。 Each of the above-described embodiments can be variously changed, replaced, added, omitted, etc. within the scope of the claims or an equivalent scope thereof.
本開示は、高い活性を有し、簡単に利用可能な水溶液、及び、当該水溶液を用いた対象物処理方法として利用でき、例えば、有機物の分解処理、微生物若しくは細菌などの除殺菌などに利用することができる。 The present disclosure can be used as an aqueous solution that has high activity and can be easily used, and a method for treating an object using the aqueous solution. For example, it can be used for organic substance decomposition treatment, sterilization of microorganisms, bacteria, and the like. be able to.
10、10a 対象物処理装置
11 対象物
12、13 混合溶液
20 容器
21 供給口
22 排出口
23 バルブ
30 供給部
40 制御回路
50 接触部
10, 10a
Claims (10)
pHが6以上8以下である
水溶液。 The main components include nitrite ions, hydrogen peroxide, and buffer components having a pH in the range of 6 to 8 and a concentration of 0.5 mM to 100 mM.
An aqueous solution having a pH of 6 or more and 8 or less.
請求項1に記載の水溶液。 The aqueous solution according to claim 1, further comprising nitrate ions.
請求項1又は2に記載の水溶液。 The aqueous solution according to claim 1 or 2, wherein the buffer component is phosphoric acid.
請求項1〜3のいずれか1項に記載の水溶液。 The aqueous solution according to claim 1, wherein a concentration of the buffer component is 1 mM or more and 10 mM or less.
前記水溶液のpHを6より小さく、又は8より大きく調整するステップと、
前記水溶液を対象物に接触させるステップとを含む
対象物処理方法。 Preparing an aqueous solution containing nitrite ions and hydrogen peroxide as main components and having a pH of 6 or more and 8 or less;
Adjusting the pH of the aqueous solution to be less than 6 or greater than 8.
Contacting the object with the aqueous solution.
請求項5に記載の対象物処理方法。 The object processing method according to claim 5, wherein the adjusting step is performed after the contacting step.
請求項5に記載の対象物処理方法。 The object processing method according to claim 5, wherein the contacting step is performed after the adjusting step.
請求項5〜7のいずれか1項に記載の対象物処理方法。 In the adjusting step, (i) an acid, a base or a salt, (ii) a solution containing at least one of an acid, a base or a salt, (iii) a gas or a solid which dissolves into an acid or a base, or (iv) The object processing method according to any one of claims 5 to 7, wherein the pH of the aqueous solution is adjusted by adding a solution containing a living organism that generates the gas or the liquid or a solid to the aqueous solution.
請求項5〜7のいずれか1項に記載の対象物処理方法。 The object processing method according to any one of claims 5 to 7, wherein in the adjusting step, the pH of the aqueous solution is adjusted by electrolyzing the aqueous solution.
請求項5〜9のいずれか1項に記載の対象物処理方法。 The object according to any one of claims 5 to 9, wherein the aqueous solution further has a buffering property in a pH range of 6 to 8, and contains a buffer component having a concentration of 0.5 mM to 100 mM. Processing method.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016061517A JP2017171627A (en) | 2016-03-25 | 2016-03-25 | Aqueous solution and object treatment method |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016061517A JP2017171627A (en) | 2016-03-25 | 2016-03-25 | Aqueous solution and object treatment method |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2017171627A true JP2017171627A (en) | 2017-09-28 |
Family
ID=59971788
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016061517A Pending JP2017171627A (en) | 2016-03-25 | 2016-03-25 | Aqueous solution and object treatment method |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2017171627A (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112118873A (en) * | 2018-05-18 | 2020-12-22 | 莱布尼茨等离子体科学和技术研究所 | Disinfection method using disinfectant formed in situ by reaction of H2O2 and NO2- |
-
2016
- 2016-03-25 JP JP2016061517A patent/JP2017171627A/en active Pending
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112118873A (en) * | 2018-05-18 | 2020-12-22 | 莱布尼茨等离子体科学和技术研究所 | Disinfection method using disinfectant formed in situ by reaction of H2O2 and NO2- |
| JP2021524315A (en) * | 2018-05-18 | 2021-09-13 | ライプニッツ−インスティトゥート フュール プラズマフォルシュング ウント テヒノロギー エー.ファウ. | Disinfection method using a disinfectant formed on the spot by the reaction of H2O2 and NO2- |
| CN112118873B (en) * | 2018-05-18 | 2023-12-05 | 莱布尼茨等离子体科学和技术研究所 | Disinfection method using disinfectants formed in situ through the reaction of H2O2 and NO2- |
| JP7417546B2 (en) | 2018-05-18 | 2024-01-18 | ライプニッツ-インスティトゥート フュール プラズマフォルシュング ウント テヒノロギー エー.ファウ. | Disinfection method using a disinfectant formed in situ by the reaction of H2O2 and NO2- |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Smet et al. | Inactivation of single strains of Listeria monocytogenes and Salmonella typhimurium planktonic cells biofilms with plasma activated liquids | |
| Mai-Prochnow et al. | Interactions of plasma-activated water with biofilms: inactivation, dispersal effects and mechanisms of action | |
| Julák et al. | The persistent microbicidal effect in water exposed to the corona discharge | |
| Lukes et al. | Aqueous-phase chemistry and bactericidal effects from an air discharge plasma in contact with water: evidence for the formation of peroxynitrite through a pseudo-second-order post-discharge reaction of H2O2 and HNO2 | |
| Dhakal et al. | Effects of spark dielectric barrier discharge plasma on water sterilization and seed germination | |
| Pavlovich et al. | Quantification of air plasma chemistry for surface disinfection | |
| Pavlovich et al. | Ozone correlates with antibacterial effects from indirect air dielectric barrier discharge treatment of water | |
| JP6087029B2 (en) | Sterilization method, sterilization preparation, and sterilization liquid production apparatus | |
| Darmanin et al. | Generation of plasma functionalized water: Antimicrobial assessment and impact on seed germination | |
| US20150373985A1 (en) | Electrolytic System and Method for Generating Biocides Having an Electron Deficient Carrier Fluid and Chlorine Dioxide | |
| JP2017001020A (en) | Liquid treatment method, object treatment method, liquid treatment device, object treatment device and plasma treatment liquid | |
| JP7233925B2 (en) | Method for producing chlorous acid water using as raw material obtained by electrolyzing salt | |
| Suwal et al. | Mechanism characterization of bacterial inactivation of atmospheric air plasma gas and activated water using bioluminescence technology | |
| JP2016023134A (en) | Electrolysis system and method for generating biocide containing electron-deficient carrier fluid and chlorine dioxide | |
| CN104150558A (en) | Method for preparing activated water through micro plasma | |
| KR102742477B1 (en) | Disinfection method using a disinfectant formed on site by the reaction of H2O2 and NO2- | |
| Vassileva et al. | Results from the research of water catholyte with nascent (Atomic) hydrogen | |
| Cayemitte et al. | Study of the electro-activation process of calcium lactate, calcium ascorbate solutions, and their equimolar mixture: assessment of their physicochemical properties | |
| JP2017171627A (en) | Aqueous solution and object treatment method | |
| JP2017001021A (en) | Liquid treatment method, object treatment method, liquid treatment device and plasma treatment liquid | |
| Ke et al. | Potassium iodide potentiates bacterial killing by helium atmospheric pressure plasma jet | |
| JP2014148526A (en) | Method for producing disinfectant antiseptic solution | |
| JP2007031374A (en) | Method for producing germicidal disinfectant solution | |
| Rothwell et al. | The Antimicrobial Efficacy Of Plasma Activated Water Is Modulated By Reactor Design And Water Composition | |
| JP6240632B2 (en) | Manufacturing method of disinfectant |