-
Technisches Gebiet
-
Die vorliegende Offenbarung betrifft eine organische elektrolumineszierende Verbindung und eine organische elektrolumineszierende Vorrichtung.
-
Stand der Technik
-
Eine elektrolumineszierende Vorrichtung (EL-Vorrichtung) ist eine selbstlichtemittierende Anzeigevorrichtung, die insofern Vorteile aufweist, als sie einen weiteren Betrachtungswinkel, ein größeres Kontrastverhältnis und eine schnellere Ansprechzeit bereitstellt. Die erste organische EL-Vorrichtung wurde von Eastman Kodak im Jahre 1987 unter Verwendung von kleinen aromatischen Diaminmolekülen und Aluminiumkomplexen als Materialien zur Bildung einer lichtemittierenden Schicht entwickelt (siehe Appl. Phys. Lett. 51, 913, 1987).
-
Eine organische elektrolumineszierende Vorrichtung weist eine mehrschichtige Struktur mit einer Lochinjektionsschicht, einer Lochtransportschicht, einer lichtemittierenden Schicht, einer Elektronentransportschicht und einer Elektroneninjektionsschicht usw. zur Erhöhung von Effizienz und Stabilität auf. Die Auswahl der in der Lochtransportschicht usw. enthaltenen Verbindungen ist als eines der Mittel zur Verbesserung der Eigenschaften der Vorrichtung, wie Lochtransporteffizienz zur lichtemittierenden Schicht, Lichtausbeute und Lebensdauer, erkannt worden.
-
Zur Verbesserung der Lichtausbeute, Treiberspannung und/oder Lebensdauer sind verschiedene Materialien oder Konzepte für eine Lochtransportschicht einer organischen elektrolumineszierenden Vorrichtung vorgeschlagen worden, die jedoch in der praktischen Anwendung nicht zufriedenstellend waren. Demgemäß besteht anhaltender Bedarf an der Entwicklung einer organischen elektrolumineszierenden Vorrichtung mit verbesserter Leistungsfähigkeit, wie verbesserten Treiberspannungs-, Lichtausbeute-, Leistungseffizienz- und/oder Lebensdauereigenschaften im Vergleich zu zuvor offenbarten organischen elektrolumineszierenden Vorrichtungen.
-
Unterdessen offenbaren die
japanische Offenlegungsschrift Nr. 2023-021983 und die internationale Veröffentlichung Nr. 2015/061198 usw. eine Aminverbindung, offenbaren aber nicht, dass die Strukturen der in der ersten Lochtransportschicht, der zweiten Lochtransportschicht und der dritten Lochtransportschicht der organischen elektrolumineszierenden Vorrichtung gemäß der vorliegenden Offenbarung enthaltenen Verbindungen jeweils verschieden sind und die zweite Lochtransportschicht eine Verbindung mit einer Fluorenamin-, Benzofluorenamin- oder Naphthofluorenamin-Struktur umfasst. Daher besteht anhaltender Bedarf an der Verbesserung der Leistungsfähigkeit von OLEDs.
-
Offenbarung der Erfindung
-
Technische Aufgabe
-
Ziel der vorliegenden Offenbarung ist erstens die Bereitstellung einer organischen elektrolumineszierenden Verbindung, mit der eine organische elektrolumineszierende Vorrichtung mit verbesserter Treiberspannung und/oder Stromeffizienz hergestellt werden kann, und zweitens die Bereitstellung einer organischen elektrolumineszierenden Vorrichtung mit verbesserter Treiberspannung und/oder Stromeffizienz.
-
Lösung der Aufgabe
-
Als Ergebnis intensiver Studien zur Lösung der technischen Aufgaben wurde im Zuge der vorliegenden Erfindung festgestellt, dass das obige Ziel erreicht werden kann durch eine organische elektrolumineszierende Vorrichtung, umfassend eine erste Elektrode; eine der ersten Elektrode zugewandte zweite Elektrode; eine Struktur, in der eine Lochinjektionsschicht, eine erste Lochtransportschicht, eine zweite Lochtransportschicht, eine dritte Lochtransportschicht und eine lichtemittierende Schicht aufeinanderfolgend zwischen der ersten Elektrode und der zweiten Elektrode gestapelt sind, wobei die Strukturen der in der ersten Lochtransportschicht, der zweiten Lochtransportschicht und der dritten Lochtransportschicht enthaltenen Verbindungen jeweils verschieden sind; wobei die zweite Lochtransportschicht eine Verbindung mit einer Fluorenamin-, Benzofluorenamin- oder Naphthofluorenamin-Struktur umfasst.
-
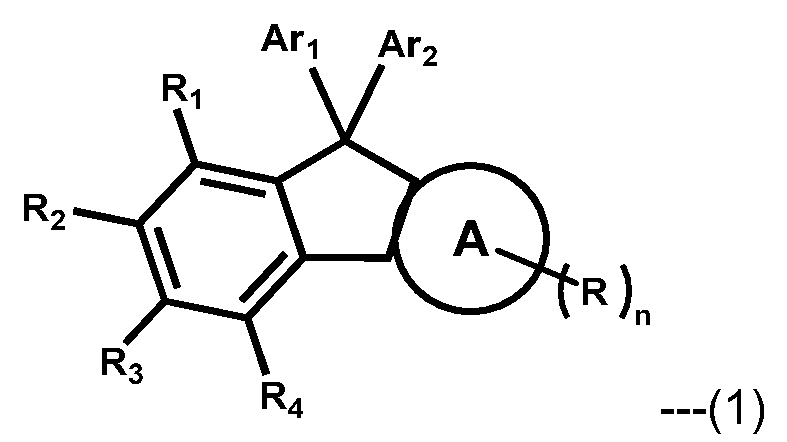
Außerdem wurde im Zuge der vorliegenden Erfindung festgestellt, dass das obige Ziel durch eine organische elektrolumineszierende Verbindung, die durch die folgende Formel 1 wiedergegeben wird, erreicht werden kann.
-
Dabei gilt, dass in Formel 1
-
Ring A für ein substituiertes oder unsubstituiertes Benzol, ein substituiertes oder unsubstituiertes Naphthalin oder ein substituiertes oder unsubstituiertes Phenanthren steht;
-
Ar1 und Ar2 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C2-C30)-Alkyl stehen;
-
R und R1 bis R4 jeweils unabhängig für Wasserstoff, Deuterium, Halogen, Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy stehen oder mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein können; mit der Maßgabe, dass mindestens eines von R und R1 bis R4 durch -L1-NAr3Ar4 wiedergegeben wird;
-
L1 für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C6-C30)-Arylen oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroarylen steht;
-
Ar3 und Ar4 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C6-C30)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl stehen;
-
n für eine ganze Zahl von 1 bis 8 steht, dann, wenn n eine Mehrzahl ist, jedes von n gleich oder voneinander verschieden sein kann.
-
Außerdem wurde im Zuge der vorliegenden Erfindung festgestellt, dass das obige Ziel durch eine organische elektrolumineszierende Verbindung, die durch die folgende Formel 3 wiedergegeben wird, erreicht werden kann.
-
Dabei gilt, dass in Formel 3 mindestens eines von R
a bis R
j durch die folgende Formel 3-1 wiedergegeben wird;
-
Dabei gilt, dass in Formel 3 und Formel 3-1
-
R
a bis R
m jeweils unabhängig für Wasserstoff, Deuterium, Halogen, Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl stehen;
für die Bindung zwischen Formel 3 und Formel 3-1 steht;
-
L6 bis L8 jeweils unabhängig für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C6-C30)-Arylen oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroarylen stehen;
-
Ar8 für ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl steht;
-
k und /jeweils unabhängig für eine ganze Zahl von 1 bis 5 stehen, m für eine ganze Zahl von 1 bis 3 steht;
-
dann, wenn k bis m für eine ganze Zahl mit einem Wert von 2 oder mehr stehen, jedes von Rk bis Rm gleich oder voneinander verschieden sein kann.
-
Vorteilhafte Effekte der Erfindung
-
Eine organische elektrolumineszierende Vorrichtung mit verbesserter Treiberspannung und/oder Stromeffizienz kann durch Verwendung der organischen elektrolumineszierenden Verbindung der vorliegenden Offenbarung bereitgestellt werden.
-
Kurze Beschreibung der Figuren
-
- 1 und 2 veranschaulichen repräsentative Formeln für die organische elektrolumineszierende Verbindung gemäß der vorliegenden Offenbarung.
-
Ausführungsform der Erfindung
-
Im Folgenden wird die vorliegende Offenbarung ausführlich beschrieben. Die folgende Beschreibung soll jedoch die vorliegende Offenbarung erläutern und den Schutzbereich der vorliegenden Offenbarung in keiner Weise einschränken.
-
Die vorliegende Offenbarung betrifft eine organische elektrolumineszierende Vorrichtung, umfassend eine erste Elektrode; eine der ersten Elektrode zugewandte zweite Elektrode; eine Struktur, in der eine Lochinjektionsschicht, eine erste Lochtransportschicht, eine zweite Lochtransportschicht, eine dritte Lochtransportschicht und eine lichtemittierende Schicht aufeinanderfolgend zwischen der ersten Elektrode und der zweiten Elektrode gestapelt sind, wobei die Strukturen der in der ersten Lochtransportschicht, der zweiten Lochtransportschicht und der dritten Lochtransportschicht enthaltenen Verbindungen jeweils verschieden sind; wobei die zweite Lochtransportschicht eine Verbindung mit einer Fluorenamin-, Benzofluorenamin- oder Naphthofluorenamin-Struktur umfasst.
-
Der Begriff „organische elektrolumineszierende Verbindung“ bedeutet in der vorliegenden Offenbarung eine Verbindung, die in einer organischen elektrolumineszierenden Vorrichtung verwendet werden kann und je nach Bedarf in einer beliebigen Schicht, aus der eine organische elektrolumineszierende Vorrichtung aufgebaut ist, enthalten sein kann.
-
Der Begriff „ein organisches elektrolumineszierendes Material“ bedeutet in der vorliegenden Offenbarung ein Material, das in einer organischen elektrolumineszierenden Vorrichtung verwendet werden kann und mindestens eine Verbindung umfassen kann. Das organische elektrolumineszierende Material kann je nach Bedarf in einer beliebigen Schicht, aus der eine organische elektrolumineszierende Vorrichtung aufgebaut ist, enthalten sein. Beispielsweise kann es sich bei dem organischen elektrolumineszierenden Material um ein Lochinjektionsmaterial, ein Lochtransportmaterial, ein Lochhilfsmaterial, ein lichtemittierendes Hilfsmaterial, ein Elektronenblockiermaterial, ein lichtemittierendes Material (das ein Wirtsmaterial und ein Dotierstoffmaterial enthält), ein Elektronenpuffermaterial, ein Lochblockiermaterial, ein Elektronentransportmaterial, ein Elektroneninjektionsmaterial usw. handeln. Das Lochtransferzonenmaterial kann mindestens eines aus der Gruppe bestehend aus einem Lochtransportmaterial, einem Lochinjektionsmaterial, einem Elektronenblockiermaterial, einem Lochhilfsmaterial und einem lichtemittierenden Hilfsmaterial sein.
-
Ein organisches elektrolumineszierendes Material der vorliegenden Offenbarung kann mindestens eine durch obige Formel 1 wiedergegebene Verbindung umfassen. Die Verbindung der Formel 1 kann in mindestens einer der Schichten, aus der eine organische elektrolumineszierende Vorrichtung aufgebaut ist, enthalten sein, ist aber nicht darauf beschränkt und kann in mindestens einer Schicht unter den Schichten, aus denen die Lochtransferzone aufgebaut ist, enthalten sein. Wenn die Verbindung der Formel 1 in einer Lochtransferschicht, einer Lochhilfsschicht, einer Elektronenblockierschicht, einer lichtemittierenden Schicht oder einer lichtemittierenden Hilfsschicht enthalten ist, kann sie als Lochtransportmaterial, Lochhilfsmaterial, Elektronenblockiermaterial, Wirtsmaterial oder lichtemittierendes Material enthalten sein.
-
Unter dem Begriff „eine Elektronentransportzone“ ist in der vorliegenden Offenbarung ein Bereich zu verstehen, in dem sich Elektronen zwischen der lichtemittierenden Schicht und der Kathode bewegen. Beispielsweise kann sie eine Lochblockierschicht, eine Elektronentransportschicht und/oder eine Elektroneninjektionsschicht, vorzugsweise eine Elektronentransportschicht und/oder eine Elektroneninjektionsschicht, enthalten. Die Lochblockierschicht dient dazu, beim Treiben der organischen elektrolumineszierenden Vorrichtung den Durchgang von Löchern durch die lichtemittierende Schicht und das Einfließen in die Kathode zu verhindern.
-
Der Begriff „Lochtransportzone“ bedeutet in der vorliegenden Offenbarung eine Region, in der sich Löcher zwischen einer ersten Elektrode und einer lichtemittierenden Schicht bewegen, und kann beispielsweise eine Lochinjektionsschicht, eine Lochtransportschicht, eine Lochhilfsschicht, eine lichtemittierende Hilfsschicht und/oder eine Elektronenblockierschicht umfassen. Die Lochinjektionsschicht, die Lochtransportschicht, die Lochhilfsschicht, die lichtemittierende Hilfsschicht und die Elektronenblockierschicht können jeweils eine einzelne Schicht oder mehrere Schichten, wobei zwei oder mehr Schichten oder drei oder mehr Schichten gestapelt sind, sein. Gemäß einer Ausführungsform der vorliegenden Offenbarung kann die Lochtransportzone eine erste Lochtransportschicht und eine zweite Lochtransportschicht umfassen und kann ferner eine dritte Lochtransportschicht umfassen. Die zweite Lochtransportschicht und die dritte Lochtransportschicht können mindestens eine von mehreren Lochtransportschichten sein und können eine Lochhilfsschicht, eine lichtemittierende Hilfsschicht und/oder eine Elektronenblockierschicht umfassen. Außerdem kann gemäß einer weiteren Ausführungsform der vorliegenden Offenbarung die Lochtransportzone eine erste Lochtransportschicht und eine zweite Lochtransportschicht umfassen, wobei die erste Lochtransportschicht zwischen einer ersten Elektrode und einer lichtemittierenden Schicht angeordnet sein kann, die zweite Lochtransportschicht zwischen der ersten Lochtransportschicht und der lichtemittierenden Schicht angeordnet sein kann und die zweite Lochtransportschicht eine Schicht sein kann, die als eine Lochtransportschicht, eine lichtemittierende Hilfsschicht, eine Lochhilfsschicht und/oder eine Elektronenblockierschicht dient. Gemäß einer anderen Ausführungsform der vorliegenden Offenbarung kann die Lochtransportzone eine erste Lochtransportschicht, eine zweite Lochtransportschicht und eine dritte Lochtransportschicht umfassen, wobei die erste Lochtransportschicht zwischen einer ersten Elektrode und einer lichtemittierenden Schicht angeordnet sein kann, die zweite Lochtransportschicht zwischen der ersten Lochtransportschicht und der lichtemittierenden Schicht angeordnet sein kann, die dritte Lochtransportschicht zwischen der zweiten Lochtransportschicht und der lichtemittierenden Schicht angeordnet sein kann und die dritte Lochtransportschicht eine Schicht sein kann, die als Lochtransportschicht, lichtemittierende Hilfsschicht, Lochhilfsschicht und/oder Elektronenblockierschicht dient.
-
Hier soll sich der Begriff „(C1-C30)-Alkyl“ auf ein lineares oder verzweigtes Alkyl mit 1 bis 30 Kohlenstoffatomen, aus denen eine Kette aufgebaut ist, beziehen, wobei die Zahl von Kohlenstoffatomen vorzugsweise 1 bis 20 und weiter bevorzugt 1 bis 10 beträgt. Das obige Alkyl kann Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl, tert-Butyl, sec-Butyl usw. einschließen. Der Begriff „(C2-C30)-Alkenyl“ soll sich in der vorliegenden Offenbarung auf ein lineares oder verzweigtes Alkenyl mit 2 bis 30 Kohlenstoffatomen, aus denen die Kette aufgebaut ist, beziehen, wobei die Zahl von Kohlenstoffatomen vorzugsweise 2 bis 20 und weiter bevorzugt 2 bis 10 beträgt. Das obige Alkenyl kann Vinyl, 1-Propenyl, 2-Propenyl, 1-Butenyl, 2-Butenyl, 3-Butenyl, 2-Methylbut-2-enyl usw. einschließen. Der Begriff „(C2-C30)-Alkinyl“ soll sich in der vorliegenden Offenbarung auf ein lineares oder verzweigtes Alkinyl mit 2 bis 30 Kohlenstoffatomen, aus denen die Kette aufgebaut ist, beziehen, wobei die Zahl von Kohlenstoffatomen vorzugsweise 2 bis 20 und weiter bevorzugt 2 bis 10 beträgt. Das obige Alkinyl kann Ethinyl, 1-Propinyl, 2-Propinyl, 1-Butinyl, 2-Butinyl, 3-Butinyl, 1-Methylpent-2-inyl usw. einschließen. Der Begriff „(C3-C30)-Cycloalkyl“ soll sich auf einen mono- oder polycyclischen Kohlenwasserstoff mit 3 bis 30 Ringgerüst-Kohlenstoffatomen beziehen, wobei die Zahl von Kohlenstoffatomen vorzugsweise 3 bis 20 und weiter bevorzugt 3 bis 7 beträgt. Das obige Cycloalkyl kann Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl usw. einschließen. Der Begriff „(3- bis 7-gliedriges) Heterocycloalkyl“ soll sich in der vorliegenden Offenbarung auf ein Cycloalkyl mit 3 bis 7, vorzugsweise 5 bis 7, Ringgerüstatomen, die mindestens ein Heteroatom ausgewählt aus der Gruppe bestehend aus B, N, O, S, Si und P einschließen, vorzugsweise mindestens ein Heteroatom ausgewählt aus der Gruppe bestehend aus O, S und N, beziehen. Das obige Heterocycloalkyl kann Tetrahydrofuran, Pyrrolidin, Thiolan, Tetrahydropyran usw. einschließen. Der Begriff „(C6-C30)-Aryl(en)“ und „(C6-C30)-Aren“ soll sich in der vorliegenden Offenbarung auf einen monocyclischen oder anellierten Ringrest, der von einem aromatischen Kohlenwasserstoff mit 6 bis 30 Ringgerüst-Kohlenstoffatomen abgeleitet ist und teilweise gesättigt sein kann, beziehen. Die Zahl der Ringgerüst-Kohlenstoffatome beträgt vorzugsweise 6 bis 25, weiter bevorzugt 6 bis 18. Das obige Aryl(en) kann eine Spirostruktur umfassen. Das obige Aryl kann Phenyl, Biphenyl, Terphenyl, Naphthyl, Binaphthyl, Phenylnaphthyl, Naphthylphenyl, Phenylterphenyl, Fluorenyl, Phenylfluorenyl, Diphenylfluorenyl, Dimethylfluorenyl, Benzofluorenyl, Dibenzofluorenyl, Phenanthrenyl, Phenylphenanthrenyl, Anthracenyl, Indenyl, Triphenylenyl, Pyrenyl, Tetracenyl, Perylenyl, Chrysenyl, Naphthacenyl, Fluoranthenyl, Spirobifluorenyl usw. einschließen. Insbesondere kann das Aryl Phenyl, 1-Naphthyl, 2-Naphthyl, 1-Anthryl, 2-Anthryl, 9-Anthryl, Benzanthryl, 1-Phenanthryl, 2-Phenanthryl, 3-Phenanthryl, 4-Phenanthryl, 9-Phenanthryl, Naphthacenyl, Pyrenyl, 1-Chrysenyl, 2-Chrysenyl, 3-Chrysenyl, 4-Chrysenyl, 5-Chrysenyl, 6-Chrysenyl, Benzo[c]phenanthryl, Benzo[g]chrysenyl, 1-Triphenylenyl, 2-Triphenylenyl, 3-Triphenylenyl, 4-Triphenylenyl, 1-Fluorenyl, 2-Fluorenyl, 3-Fluorenyl, 4-Fluorenyl, 9-Fluorenyl, Benzo[a]fluorenyl, Benzo[b]fluorenyl, Benzo[c]fluorenyl, Dibenzofluorenyl, 2-Biphenylyl, 3-Biphenylyl, 4-Biphenylyl, o-Terphenyl, m-Terphenyl-4-yl, m-Terphenyl-3-yl, m-Terphenyl-2-yl, p-Terphenyl-4-yl, p-Terphenyl-3-yl, p-Terphenyl-2-yl, m-Quaterphenyl, 3-Fluoranthenyl, 4-Fluoranthenyl, 8-Fluoranthenyl, 9-Fluoranthenyl, Benzofluoranthenyl, o-Tolyl, m-Tolyl, p-Tolyl, 2,3-Xylyl, 3,4-Xylyl, 2,5-Xylyl, Mesityl, o-Cumenyl, m-Cumenyl, p-Cumenyl, p-tert-Butylphenyl, p-(2-Phenylpropyl)phenyl, 4'-Methylbiphenylyl, 4"-tert-Butyl-p-terphenyl-4-yl, 9,9-Dimethyl-1-fluorenyl, 9,9-Dimethyl-2-fluorenyl, 9,9-Dimethyl-3-fluorenyl, 9,9-Dimethyl-4-fluorenyl, 9,9-Diphenyl-1-fluorenyl, 9,9-Diphenyl-2-fluorenyl, 9,9-Diphenyl-3-fluorenyl, 9,9-Diphenyl-4-fluorenyl, 11,11-Dimethyl-1-benzo[a]fluorenyl, 11,11-Dimethyl-2-benzo[a]fluorenyl, 11,11-Dimethyl-3-benzo[a]fluorenyl, 11,11-Dimethyl-4-benzo[a]fluorenyl, 11,11-Dimethyl-5-benzo[a]fluorenyl, 11,11-Dimethyl-6-benzo[a]fluorenyl, 11,11-Dimethyl-7-benzo[a]fluorenyl, 11,11-Dimethyl-8-benzo[a]fluorenyl, 11,11-Dimethyl-9-benzo[a]fluorenyl, 11,11-Dimethyl-10-benzo[a]fluorenyl, 11,11-Dimethyl-1-benzo[b]fluorenyl, 11,11-Dimethyl-2-benzo[b]fluorenyl, 11,11-Dimethyl-3-benzo[b]fluorenyl, 11,11-Dimethyl-4-benzo[b]fluorenyl, 11,11-Dimethyl-5-benzo[b]fluorenyl, 11,11-Dimethyl-6-benzo[b]fluorenyl, 11,11-Dimethyl-7-benzo[b]fluorenyl, 11,11-Dimethyl-8-benzo[b]fluorenyl, 11,11-Dimethyl-9-benzo[b]fluorenyl, 11,11-Dimethyl-10-benzo[b]fluorenyl, 11,11-Dimethyl-1-benzo[c]fluorenyl, 11,11-Dimethyl-2-benzo[c]fluorenyl, 11, 11-Dimethyl-3-benzo[c]fluorenyl, 11,11-Dimethyl-4-benzo[c]fluorenyl, 11, 11-Dimethyl-5-benzo[c]fluorenyl, 11,11-Dimethyl-6-benzo[c]fluorenyl, 11,11-Dimethyl-7-benzo[c]fluorenyl, 11,11-Dimethyl-8-benzo[c]fluorenyl, 11,11-Dimethyl-9-benzo[c]fluorenyl, 11,11-Dimethyl-10-benzo[c]fluorenyl, 11,11-Diphenyl-1-benzo[a]fluorenyl, 11,11-Diphenyl-2-benzo[a]fluorenyl, 11,11-Diphenyl-3-benzo[a]fluorenyl, 11,11-Diphenyl-4-benzo[a]fluorenyl, 11,11-Diphenyl-5-benzo[a]fluorenyl, 11,11-Diphenyl-6-benzo[a]fluorenyl, 11,11-Diphenyl-7-benzo[a]fluorenyl, 11,11-Diphenyl-8-benzo[a]fluorenyl, 11,11-Diphenyl-9-benzo[a]fluorenyl, 11,11-Diphenyl-10-benzo[a]fluorenyl, 11,11-Diphenyl-1-benzo[b]fluorenyl, 11,11-Diphenyl-2-benzo[b]fluorenyl, 11,11-Diphenyl-3-benzo[b]fluorenyl, 11,11-Diphenyl-4-benzo[b]fluorenyl, 11,11-Diphenyl-5-benzo[b]fluorenyl, 11,11-Diphenyl-6-benzo[b]fluorenyl, 11,11-Diphenyl-7-benzo[b]fluorenyl, 11,11-Diphenyl-8-benzo[b]fluorenyl, 11,11-Diphenyl-9-benzo[b]fluorenyl, 11,11-Diphenyl-10-benzo[b]fluorenyl, 11,11-Diphenyl-1-benzo[c]fluorenyl, 11,11-Diphenyl-2-benzo[c]fluorenyl, 11,11-Diphenyl-3-benzo[c]fluorenyl, 11,11-Diphenyl-4-benzo[c]fluorenyl, 11,11-Diphenyl-5-benzo[c]fluorenyl, 11,11-Diphenyl-6-benzo[c]fluorenyl, 11,11-Diphenyl-7-benzo[c]fluorenyl, 11,11-Diphenyl-8-benzo[c]fluorenyl, 11,11-Diphenyl-9-benzo[c]fluorenyl, 11,11-Diphenyl-10-benzo[c]fluorenyl, 9,9,10,10-Tetramethyl-9,10-dihydro-1-phenanthrenyl, 9,9,10,10-Tetramethyl-9,10-dihydro-2-phenanthrenyl, 9,9,10,10-Tetramethyl-9,10-dihydro-3-phenanthrenyl, 9,9,10,10-Tetramethyl-9,10-dihydro-4-phenanthrenyl usw. einschließen.
-
Der Begriff „(3- bis 30-gliedriges) Heteroaryl(en)“ und „(3- bis 30-gliedriges) Heteroaren“ soll sich in der vorliegenden Offenbarung auf eine Aryl(en)gruppe mit 3 bis 30 Ringgerüstatomen und mindestens einem Heteroatom aus der Gruppe bestehend aus B, N, O, S, Si, P, Se, Te und Ge beziehen. Die Zahl der Heteroatome beträgt vorzugsweise 1 bis 4. Das obige Heteroaryl(en) kann ein monocyclischer Ring oder ein anellierter Ring, der mit mindestens einem Benzolring kondensiert ist, sein; es kann teilweise gesättigt sein. Außerdem kann es sich bei dem obigen Heteroaryl(en) um ein durch Verknüpfen mindestens einer Heteroaryl- oder Arylgruppe mit einer Heteroaryl(en)gruppe über eine oder mehrere Einfachbindungen gebildetes Heteroaryl(en) handeln, und es kann eine Spirostruktur umfassen. Das obige Heteroaryl kann ein Heteroaryl vom Typ monocyclischer Ring wie Furyl, Thiophenyl, Pyrrolyl, Imidazolyl, Pyrazolyl, Thiazolyl, Thiadiazolyl, Isothiazolyl, Isoxazolyl, Oxazolyl, Oxadiazolyl, Triazinyl, Tetrazinyl, Triazolyl, Tetrazolyl, Furazanyl, Pyridyl, Pyrazinyl, Pyrimidinyl, Pyridazinyl usw. und ein Heteroaryl vom Typ anellierter Ring wie Benzofuranyl, Benzothiophenyl, Isobenzofuranyl, Dibenzofuranyl, Benzophenanthrofuranyl, Dibenzothiophenyl, Benzimidazolyl, Benzothiazolyl, Benzoisothiazolyl, Benzophenanthrothiophenyl, Benzoisoxazolyl, Benzoxazolyl, Phenanthrooxazolyl, Phenanthrothiazolyl, Isoindolyl, Indolyl, Benzoindolyl, Indazolyl, Benzothiadiazolyl, Chinolyl, Isochinolyl, Cinnolyl, Chinazolinyl, Benzochinazolinyl, Chinoxalinyl, Benzochinoxalinyl, Naphthyridinyl, Carbazolyl, Benzocarbazolyl, Dibenzocarbazolyl, Phenoxazinyl, Phenothiazinyl, Phenanthridinyl, Benzodioxolyl, Dihydroacridinyl usw. einschließen. Spezieller kann das Heteroaryl 1-Pyrrolyl, 2-Pyrrolyl, 3-Pyrrolyl, Pyrazinyl, 2-Pyridyl, 2-Pyrimidinyl, 4-Pyrimidinyl, 5-Pyrimidinyl, 6-Pyrimidinyl, 1,2,3-Triazin-4-yl, 1,2,4-Triazin-3-yl, 1,3,5-Triazin-2-yl, 1-Imidazolyl, 2-Imidazolyl, 1-Pyrazolyl, 1-Indolidinyl, 2-Indolidinyl, 3-Indolidinyl, 5-Indolidinyl, 6-Indolidinyl, 7-Indolidinyl, 8-Indolidinyl, 2-Imidazopyridyl, 3-Imidazopyridyl, 5-Imidazopyridyl, 6-Imidazopyridyl, 7-Imidazopyridyl, 8-Imidazopyridyl, 3-Pyridyl, 4-Pyridinyl, 1-Indolyl, 2-Indolyl, 3-Indolyl, 4-Indolyl, 5-Indolyl, 6-Indolyl, 7-Indolyl, 1-Isoindolyl, 2-Isoindolyl, 3-Isoindolyl, 4-Isoindolyl, 5-Isoindolyl, 6-Isoindolyl, 7-Isoindolyl, 2-Furyl, 3-Furyl, 2-Benzofuranyl, 3-Benzofuranyl, 4-Benzofuranyl, 5-Benzofuranyl, 6-Benzofuranyl, 7-Benzofuranyl, 1-Isobenzofuranyl, 3-Isobenzofuranyl, 4-Isobenzofuranyl, 5-Isobenzofuranyl, 6-Isobenzofuranyl, 7-Isobenzofuranyl, 2-Chinolyl, 3-Chinolyl, 4-Chinolyl, 5-Chinolyl, 6-Chinolyl, 7-Chinolyl, 8-Chinolyl, 1-Isochinolyl, 3-Isochinolyl, 4-Isochinolyl, 5-Isochinolyl, 6-Isochinolyl, 7-Isochinolyl, 8-Isochinolyl, 2-Chinoxalinyl, 5-Chinoxalinyl, 6-Chinoxalinyl, 1-Carbazolyl, 2-Carbazolyl, 3-Carbazolyl, 4-Carbazolyl, 9-Carbazolyl, Azacarbazolyl-1-yl, Azacarbazolyl-2-yl, Azacarbazolyl-3-yl, Azacarbazolyl-4-yl, Azacarbazolyl-5-yl, Azacarbazolyl-6-yl, Azacarbazolyl-7-yl, Azacarbazolyl-8-yl, Azacarbazolyl-9-yl, 1-Phenanthridinyl, 2-Phenanthridinyl, 3-Phenanthridinyl, 4-Phenanthridinyl, 6-Phenanthridinyl, 7-Phenanthridinyl, 8-Phenanthridinyl, 9-Phenanthridinyl, 10-Phenanthridinyl, 1-Acridinyl, 2-Acridinyl, 3-Acridinyl, 4-Acridinyl, 9-Acridinyl, 2-Oxazolyl, 4-Oxazolyl, 5-Oxazolyl, 2-Oxadiazolyl, 5-Oxadiazolyl, 3-Furazanyl, 2-Thienyl, 3-Thienyl, 2-Methylpyrrol-1-yl, 2-Methylpyrrol-3-yl, 2-Methylpyrrol-4-yl, 2-Methylpyrrol-5-yl, 3-Methylpyrrol-1-yl, 3-Methylpyrrol-2-yl, 3-Methylpyrrol-4-yl, 3-Methylpyrrol-5-yl, 2-tert-Butylpyrrol-4-yl, 3-(2-Phenylpropyl)pyrrol-1-yl, 2-Methyl-1-indolyl, 4-Methyl-1-indolyl, 2-Methyl-3-indolyl, 4-Methyl-3-indolyl, 2-tert-Butyl-1-indolyl, 4-tert-Butyl-1-indolyl, 2-tert-Butyl-3-indolyl, 4-tert-Butyl-3-indolyl, 1-Dibenzofuranyl, 2-Dibenzofuranyl, 3-Dibenzofuranyl, 4-Dibenzofuranyl, 1-Dibenzothiophenyl, 2-Dibenzothiophenyl, 3-Dibenzothiophenyl, 4-Dibenzothiophenyl, 1-Naphtho-[1,2-b]-benzofuranyl, 2-Naphtho-[1,2-b]-benzofuranyl, 3-Naphtho-[1,2-b]-benzofuranyl, 4-Naphtho-[1,2-b]-benzofuranyl, 5-Naphtho-[1,2-b]-benzofuranyl, 6-Naphtho-[1,2-b]-benzofuranyl, 7-Naphtho-[1,2-b]-benzofuranyl, 8-Naphtho-[1,2-b]-benzofuranyl, 9-Naphtho-[1,2-b]-benzofuranyl, 10-Naphtho-[1,2-b]-benzofuranyl, 1-Naphtho-[2,3-b]-benzofuranyl, 2-Naphtho-[2,3-b]-benzofuranyl, 3-Naphtho-[2,3-b]-benzofuranyl, 4-Naphtho-[2,3-b]-benzofuranyl, 5-Naphtho-[2,3-b]-benzofuranyl, 6-Naphtho-[2,3-b]-benzofuranyl, 7-Naphtho-[2,3-b]-benzofuranyl, 8-Naphtho-[2,3-b]-benzofuranyl, 9-Naphtho-[2,3-b]-benzofuranyl, 10-Naphtho-[2,3-b]-benzofuranyl, 1-Naphtho-[2,1-b]-benzofuranyl, 2-Naphtho-[2,1-b]-benzofuranyl, 3-Naphtho-[2,1-b]-benzofuranyl, 4-Naphtho-[2,1-b]-benzofuranyl, 5-Naphtho-[2,1-b]-benzofuranyl, 6-Naphtho-[2,1-b]-benzofuranyl, 7-Naphtho-[2,1-b]-benzofuranyl, 8-Naphtho-[2,1-b]-benzofuranyl, 9-Naphtho-[2,1-b]-benzofuranyl, 10-Naphtho-[2,1-b]-benzofuranyl, 1-Naphtho-[1,2-b]-benzothiophenyl, 2-Naphtho-[1,2-b]-benzothiophenyl, 3-Naphtho-[1,2-b]-benzothiophenyl, 4-Naphtho-[1,2-b]-benzothiophenyl, 5-Naphtho-[1,2-b]-benzothiophenyl, 6-Naphtho-[1,2-b]-benzothiophenyl, 7-Naphtho-[1,2-b]-benzothiophenyl, 8-Naphtho-[1,2-b]-benzothiophenyl, 9-Naphtho-[1,2-b]-benzothiophenyl, 10-Naphtho-[1,2-b]-benzothiophenyl, 1-Naphtho-[2,3-b]-benzothiophenyl, 2-Naphtho-[2,3-b]-benzothiophenyl, 3-Naphtho-[2,3-b]-benzothiophenyl, 4-Naphtho-[2,3-b]-benzothiophenyl, 5-Naphtho-[2,3-b]-benzothiophenyl, 1-Naphtho-[2,1-b]-benzothiophenyl, 2-Naphtho-[2,1-b]-benzothiophenyl, 3-Naphtho-[2,1-b]-benzothiophenyl, 4-Naphtho-[2,1-b]-benzothiophenyl, 5-Naphtho-[2,1-b]-benzothiophenyl, 6-Naphtho-[2,1-b]-benzothiophenyl, 7-Naphtho-[2, 1-5]-benzothiophenyl, 8-Naphtho-[2,1-b]-benzothiophenyl, 9-Naphtho-[2,1-b]-benzothiophenyl, 10-Naphtho-[2,1-b]-benzothiophenyl, 2-Benzofuro[3,2-d]pyrimidinyl, 6-Benzofuro[3,2-d]pyrimidinyl, 7-Benzofuro[3,2-d]pyrimidinyl, 8-Benzofuro[3,2-d]pyrimidinyl, 9-Benzofuro[3,2-d]pyrimidinyl, 2-Benzothio[3,2-d]pyrimidinyl, 6-Benzothio[3,2-d]pyrimidinyl, 7-Benzothio[3,2-d]pyrimidinyl, 8-Benzothio[3,2-d]pyrimidinyl, 9-Benzothio[3,2-d]pyrimidinyl, 2-Benzofuro[3,2-d]pyrazinyl, 6-Benzofuro[3,2-d]pyrazinyl, 7-Benzofuro[3,2-d]pyrazinyl, 8-Benzofuro[3,2-d]pyrazinyl, 9-Benzofuro[3,2-d]pyrazinyl, 2-Benzothio[3,2-d]pyrazinyl, 6-Benzothio[3,2-d]pyrazinyl, 7-Benzothio[3,2-d]pyrazinyl, 8-Benzothio[3,2-d]pyrazinyl, 9-Benzothio[3,2-d]pyrazinyl, 1-Silafluorenyl, 2-Silafluorenyl, 3-Silafluorenyl, 4-Silafluorenyl, 1-Germafluorenyl, 2-Germafluorenyl, 3-Germafluorenyl, 4-Germafluorenyl, 1-Dibenzoselenophenyl, 2-Dibenzoselenophenyl, 3-Dibenzoselenophenyl, 4-Dibenzoselenophenyl usw. einschließen. Außerdem kann „Heteroaryl(en)“ in ein Heteroaryl(en) mit Elektroneneigenschaften und ein Heteroaryl(en) mit Locheigenschaften eingeteilt werden. Ein Heteroaryl(en) mit Elektroneneigenschaften ist ein Substituent, der im zugrunde liegenden Kern relativ elektronenreich ist, beispielsweise ein substituiertes oder unsubstituiertes Pyridinyl, ein substituiertes oder unsubstituiertes Pyrimidinyl, ein substituiertes oder unsubstituiertes Triazinyl, ein substituiertes oder unsubstituiertes Chinazolinyl, ein substituiertes oder unsubstituiertes Chinoxalinyl oder ein substituiertes oder unsubstituiertes Chinolyl usw. Ein Heteroaryl(en) mit Locheigenschaften ist ein Substituent, der im zugrunde liegenden Kern relativ elektronenarm ist, beispielsweise ein substituiertes oder unsubstituiertes Carbazolyl, ein substituiertes oder unsubstituiertes Dibenzofuranyl, ein substituiertes oder unsubstituiertes Dibenzothiophenyl usw. In der vorliegenden Offenbarung schließt der Begriff „Halogen“ F, Cl, Br und I ein.
-
Außerdem sind „ortho-“ („o-“), „meta-“ („m-)“ und „para“ („p-“) Präfixe, die jeweils die relativen Positionen von Substituenten wiedergeben. Das Präfix „ortho-“ zeigt an, dass zwei Substituenten einander benachbart sind, und beispielsweise wird dann, wenn zwei Substituenten in einem Benzolderivat die Positionen 1 und 2 besetzen, dies als eine „ortho-“-Konfiguration bezeichnet. Das Präfix „meta-“ zeigt an, dass zwei Substituenten in den Positionen 1 und 3 stehen, und beispielsweise wird dann, wenn zwei Substituenten in einem Benzolderivat die Positionen 1 und 3 besetzen, dies als eine „meta-“-Konfiguration bezeichnet. Das Präfix „para-“ zeigt an, dass zwei Substituenten in den Positionen 1 und 4 stehen, und beispielsweise wird dann, wenn zwei Substituenten in einem Benzolderivat die Positionen 1 und 4 besetzen, dies als eine „para-“-Konfiguration bezeichnet.
-
Hier bedeutet „substituiert“ in dem Ausdruck „substituiert oder unsubstituiert“, dass ein Wasserstoffatom in einer bestimmten funktionellen Gruppe durch ein anderes Atom oder eine andere funktionelle Gruppe, d. h. einen Substituenten, ersetzt ist. Sofern nicht anders angegeben, kann der Substituent Wasserstoff an einer Position ersetzen, an der der Substituent ohne Einschränkung substituiert werden kann, und wenn zwei oder mehr Wasserstoffatome in einer bestimmten funktionellen Gruppe jeweils durch einen Substituenten ersetzt sind, kann jeder Substituent gleich oder voneinander verschieden sein. Die maximale Zahl von Substituenten, die für eine bestimmte funktionelle Gruppe substituiert sein können, kann die gesamte Zahl von Valenzen sein, die für jedes die funktionelle Gruppe bildende Atom substituiert sein können. Hier handelt es sich bei dem substituierten Alkyl, dem substituierten Alkenyl, dem substituierten Aryl(en), dem substituierten Heteroaryl(en), dem substituierten Cycloalkyl und dem substituierten Alkoxy jeweils unabhängig um mindestens eines aus der Gruppe bestehend aus Deuterium; einem Halogen; einem Cyano; einem Carboxyl; einem Nitro; einem Hydroxy; einem Phosphinoxid; einem (C1-C30)-Alkyl; einem Halogen-(C1-C30)-alkyl; einem (C2-C30)-Alkenyl; einem (C2-C30)-Alkinyl; einem (C1-C30)-Alkoxy; einem(C1-C30)-Alkylthio; einem (C3-C30)-Cycloalkyl; einem (C3-C30)-Cycloalkenyl; einem (3- bis 7-gliedrigen) Heterocycloalkyl; einem (C6-C30)-Aryloxy; einem (C6-C30)-Arylthio; einem (C6-C30)-Aryl, das unsubstituiert oder durch eines oder mehrere von (C1-C30)-Alkyl und/oder von Di-(C6-C30)-arylamino substituiert ist; einem (3- bis 30-gliedrigen) Heteroaryl, das unsubstituiert oder durch eines oder mehrere von (C6-C30)-Aryl substituiert ist; einem oder mehreren Tri-(C1-C30)-alkylsilyl; einem oder mehreren Tri-(C6-C30)-arylsilyl; einem oder mehreren Di-(C1-C30)-alkyl-(C6-C30)-arylsilyl; einem oder mehreren (C1-C30)-Alkyldi-(C6-C30)-arylsilyl; einer anellierten Ringgruppe aus einem oder mehreren aliphatischen (C3-C30)-Ringen und einem oder mehreren aromatischen (C6-C30)-Ringen; einem Amino; einem Mono- oder Di-(C1-C30)-alkylamino; einem Mono- oder Di-(C2-C30)-alkenylamino; einem Mono- oder Di-(C6-C30)-arylamino, das unsubstituiert oder durch ein (C1-C30)-Alkyl substituiert ist; einem Mono- oder Di-(3- bis 30-gliedrigen)-heteroarylamino; einem (C1-C30)-Alkyl-(C2-C30)-alkenylamino; einem (C1-C30)-Alkyl-(C6-C30)-arylamino; einem (C1-C30)-Alkyl-(3- bis 30-gliedrigen)-heteroarylamino; einem (C2-C30)-Alkenyl-(C6-C30)-arylamino; einem (C2-C30)-Alkenyl-(3- bis 30-gliedrigen)-heteroarylamino; einem (C6-C30)-Aryl-(3- bis 30-gliedrigen)-heteroarylamino; einem (C1-C30)-Alkylcarbonyl; einem (C1-C30)-Alkoxycarbonyl; einem (C6-C30)-Arylcarbonyl; einem Di-(C6-C30)-arylboronyl; einem Di-(C1-C30)-alkylboronyl; einem (C1-C30)-Alkyl-(C6-C30)-arylboronyl; einem (C6-C30)-Aryl-(C1-C30)-alkyl und einem (C1-C30)-Alkyl-(C6-C30)-aryl. Gemäß einer Ausführungsform der vorliegenden Offenbarung kann es sich bei dem Substituenten bzw. den Substituenten jeweils unabhängig um Deuterium; ein (C1-C30)-Alkyl; ein (C3-C30)-Cycloalkyl; ein (C3-C30)-Cycloalkenyl; ein (3- bis 7-gliedriges) Heterocycloalkyl; ein (C6-C30)-Aryl, das unsubstituiert oder durch ein oder mehrere (C1-C30)-Alkyl und/oder ein oder mehrere Di-(C6-C30)-arylamino substituiert ist; ein (3- bis 30-gliedriges) Heteroaryl, das unsubstituiert oder durch ein oder mehrere (C6-C30)-Aryl substituiert ist; eine anellierte Ringgruppe aus einem oder mehreren aliphatischen (C3-C30)-Ringen und einem oder mehreren aromatischen (C6-C30)-Ringen; ein Amino; ein Mono- oder Di-(C1-C30)-alkylamino; ein Mono- oder Di-(C2-C30)-alkenylamino; ein Mono- oder Di-(C6-C30)-arylamino, das unsubstituiert oder durch ein (C1-C30)-Alkyl substituiert ist; ein Mono- oder Di-(3- bis 30-gliedriges)-heteroarylamino; ein (C1-C30)-Alkyl-(C2-C30-)alkenylamino; ein (C1-C30)-Alkyl-(C6-C30)-arylamino; ein (C1-C30)-Alkyl-(3- bis 30-gliedriges)-heteroarylamino; ein (C2-C30)-Alkenyl-(C6-C30)-arylamino; ein (C2-C30)-Alkenyl-(3- bis 30-gliedriges)-heteroarylamino; ein (C6-C30)-Aryl-(3- bis 30-gliedriges)-heteroarylamino; ein (C6-C30)-Aryl-(C1-C30)-alkyl und ein (C1-C30)-Alkyl-(C6-C30)-aryl handeln. Gemäß einer anderen Ausführungsform der vorliegenden Offenbarung kann es sich bei dem Substituenten bzw. den Substituenten jeweils unabhängig um Deuterium; ein (C1-C20)-Alkyl; ein (C3-C20)-Cycloalkyl; ein (3-bis 7-gliedriges) Heterocycloalkyl; ein (C6-C20)-Aryl, das unsubstituiert oder durch ein oder mehrere (C1-C30)-Alkyl und/oder ein oder mehrere Di-(C6-C30)-arylamino substituiert ist; ein (3- bis 20-gliedriges) Heteroaryl, das unsubstituiert oder durch ein oder mehrere (C6-C30)-Aryl substituiert ist; eine anellierte Ringgruppe aus einem oder mehreren aliphatischen (C3-C30)-Ringen und einem oder mehreren aromatischen (C6-C30)-Ringen; ein Mono- oder Di-(C6-C20)-arylamino, das unsubstituiert oder durch ein (C1-C30)-Alkyl substituiert ist; ein Mono- oder Di-(3- bis 20-gliedriges)-heteroarylamino; ein (C1-C20)-Alkyl-(C6-C20)-arylamino; ein (C1-C20)-Alkyl-(3- bis 20-gliedriges)-heteroarylamino; ein (C2-C20)-Alkenyl-(C6-C20)-arylamino; ein (C2-C20)-Alkenyl-(3- bis 20-gliedriges)-heteroarylamino; ein (C6-C20)-Aryl-(3- bis 20-gliedriges)-heteroarylamino; ein (C6-C30)-Aryl-(C1-C30)-alkyl und ein (C1-C30)-Alkyl-(C6-C30)-aryl handeln. Beispielsweise kann es sich bei dem Substituenten bzw. den Substituenten jeweils unabhängig um mindestens einen aus der Gruppe bestehend aus Deuterium, einem Methyl, einem Naphthyl, einem Phenanthrenyl, einem Dibenzofuranyl, einem Phenyl, das unsubstituiert oder durch Deuterium substituiert ist, einem Phenanthrylen, einem Dimethylfluorenyl, einem Benzonaphthofuranyl, einem Benzonaphthothiophenyl, einem Phenyldimethylfluorenylamino und einem Adamantyl handeln.
-
Wenn in der vorliegenden Offenbarung ein Substituent in der chemischen Formel oder der Verbindungsstruktur nicht angegeben ist, kann dies bedeuten, dass alle möglichen Positionen für die Substituenten Wasserstoff oder Deuterium sind. Das heißt im Fall von Deuterium, dass es ein Isotop von Wasserstoff ist und es sich bei einigen Wasserstoffatomen um das Isotop Deuterium handeln kann und in diesem Fall der Deuteriumgehalt 0 % bis 100 % betragen kann. Wenn in der vorliegenden Offenbarung in Fällen, in denen ein Substituent in der chemischen Formel oder Verbindungsstruktur nicht angegeben ist, der Substituent nicht explizit ausgeschlossen ist, wie 0 % Deuterium, 100 % Wasserstoff, und alle Substituenten Wasserstoff sind, können Wasserstoff und Deuterium in einer Verbindung gemischt verwendet werden. Das Deuterium ist eines der Isotope von Wasserstoff und ist ein Element mit einem Deuteron, das aus einem Proton und einem Neutron besteht, als Kern. Es kann als Wasserstoff-2 wiedergegeben werden, dessen Elementsymbol auch als D oder 2H geschrieben werden kann. Die Isotope sind Atome mit der gleichen Ordnungszahl (Z), aber verschiedenen Massenzahlen (A) und können auch als Elemente mit der gleichen Zahl von Protonen, aber verschiedenen Zahlen von Neutronen interpretiert werden.
-
In der vorliegenden Offenbarung bezieht sich „eine Kombination davon“ auf eine Kombination von einem oder mehreren Elementen aus der entsprechenden Liste unter Bildung einer bekannten oder chemisch stabilen Anordnung, die für den Fachmann aus der entsprechenden Liste vorstellbar ist. Beispielsweise können Alkyl und Deuterium unter Bildung einer teilweise oder vollständig deuterierten Alkylgruppe kombiniert werden; Halogen und Alkyl können unter Bildung eines halogenierten Alkylsubstituenten kombiniert werden; und Halogen, Alkyl und Aryl können unter Bildung eines halogenierten Arylalkyls kombiniert werden. Beispielsweise enthält eine bevorzugte Kombination von Substituenten bis zu 50 Atome, bei denen es sich nicht um Wasserstoff oder Deuterium handelt, oder bis zu 40 Atome, bei denen es sich nicht um Wasserstoff oder Deuterium handelt, oder bis zu 30 Atome, bei denen es sich nicht um Wasserstoff oder Deuterium handelt, oder in vielen Fällen kann eine bevorzugte Kombination von Substituenten bis zu 20 Atome, bei denen es sich nicht um Wasserstoff oder Deuterium handelt, umfassen.
-
Im Folgenden wird eine organische elektrolumineszierende Vorrichtung ausführlicher beschrieben.
-
Gemäß einer Ausführungsform der vorliegenden Offenbarung wird eine organische elektrolumineszierende Vorrichtung bereitgestellt, die eine erste Elektrode; eine der ersten Elektrode zugewandte zweite Elektrode; eine Struktur, in der eine Lochinjektionsschicht, eine erste Lochtransportschicht, eine zweite Lochtransportschicht, eine dritte Lochtransportschicht und eine lichtemittierende Schicht aufeinanderfolgend zwischen der ersten Elektrode und der zweiten Elektrode gestapelt sind, umfasst. Insbesondere sind in der organischen elektrolumineszierenden Vorrichtung gemäß einer Ausführungsform der vorliegenden Offenbarung die Strukturen der in der ersten Lochtransportschicht, der zweiten Lochtransportschicht und der dritten Lochtransportschicht enthaltenen Verbindungen jeweils verschieden; und die zweite Lochtransportschicht umfasst eine Verbindung mit einer Fluorenamin-, Benzofluorenamin- oder Naphthofluorenamin-Struktur.
-
Die Verbindung mit einer Fluorenamin-, Benzofluorenamin- oder Naphthofluorenamin-Struktur kann durch die folgende Formel 1 wiedergegeben werden.
-
Dabei gilt, dass in Formel 1
-
Ring A für ein substituiertes oder unsubstituiertes Benzol, ein substituiertes oder unsubstituiertes Naphthalin oder ein substituiertes oder unsubstituiertes Phenanthren steht;
-
Ar1 und Ar2 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C30)-Aryl stehen oder miteinander zu einem oder mehreren Ringen verknüpft sein können;
-
R und R1 bis R4 jeweils unabhängig für Wasserstoff, Deuterium, Halogen, Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy stehen oder mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein können; mit der Maßgabe, dass mindestens eines von R und R1 bis R4 durch -L1-NAr3Ar4 wiedergegeben wird;
-
L1 für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C6-C30)-Arylen oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroarylen steht;
-
Ar3 und Ar4 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C6-C30)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl stehen;
-
n für eine ganze Zahl von 1 bis 8 steht, dann, wenn n eine Mehrzahl ist, jedes von n gleich oder voneinander verschieden sein kann.
-
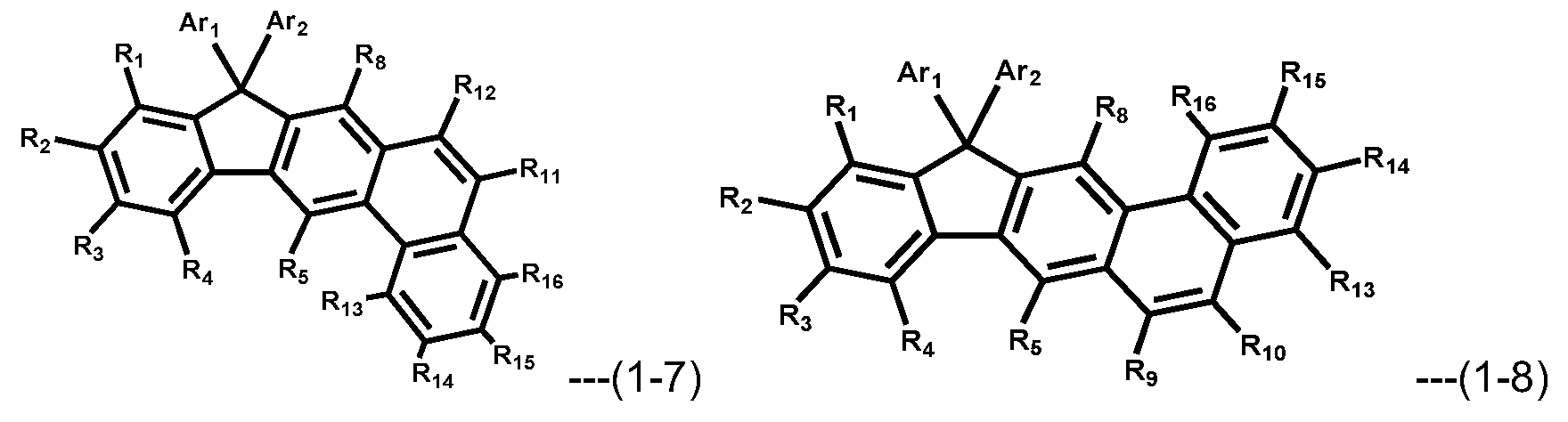
Gemäß einer Ausführungsform der vorliegenden Erfindung kann die durch die Formel 1 wiedergegebene Verbindung durch eine der folgenden Formeln 1-1 bis 1-11 wiedergegeben werden.
-
Dabei gilt, dass in den Formeln 1-1 bis 1-11
-
Ar1 und Ar2 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C30)-Aryl stehen oder miteinander zu einem oder mehreren Ringen verknüpft sein können. Gemäß einer Ausführungsform der vorliegenden Offenbarung können Ar1 und Ar2 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C1-C20)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C20)-Aryl stehen oder miteinander zu einem oder mehreren anellierten Ringen verknüpft sein. Gemäß einer anderen Ausführungsform der vorliegenden Offenbarung können Ar1 und Ar2 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C1-C10)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C10)-Aryl stehen oder miteinander zu einem oder mehreren anellierten Ringen verknüpft sein. Beispielsweise können Ar1 und Ar2 jeweils unabhängig für ein Methyl, ein Ethyl, ein Propyl, ein Butyl, ein Pentyl, ein Hexyl, ein Heptyl, ein Octyl oder ein Phenyl stehen oder zu einem (C13)-Aryl verknüpft sein, und diese können durch mindestens ein Deuterium substituiert sein.
-
R1 bis R16 stehen jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy oder können mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein; mit der Maßgabe, dass mindestens eines von R1 bis R16 durch -L1-NAr3Ar4 wiedergegeben wird. Gemäß einer Ausführungsform der vorliegenden Offenbarung können R1 bis R16 jeweils unabhängig für Wasserstoff, Deuterium, ein substituiertes oder unsubstituiertes (C1-C20)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C20)-Aryl stehen oder mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein; mit der Maßgabe, dass mindestens eines von R1 bis R16 durch -L1-NAr3Ar4 wiedergegeben wird. Beispielsweise können R1 bis R16 jeweils unabhängig für Wasserstoff, Deuterium, ein Phenyl, das unsubstituiert oder durch Deuterium substituiert ist, oder -L1-NAr3Ar4 stehen.
-
L1 steht für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C6-C30)-Arylen oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroarylen. Gemäß einer Ausführungsform der vorliegenden Offenbarung kann L1 für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C6-C25)-Arylen oder ein substituiertes oder unsubstituiertes (3- bis 25-gliedriges) Heteroarylen stehen. Beispielsweise kann L1 für eine Einfachbindung, ein Phenylen oder Phenanthrenylen stehen, und diese können durch mindestens ein Deuterium substituiert sein.
-
Ar3 und Ar4 stehen jeweils unabhängig für ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl. Gemäß einer Ausführungsform der vorliegenden Offenbarung stehen Ar3 und Ar4 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C6-C30)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 25-gliedriges) Heteroaryl. Beispielsweise können Ar3 und Ar4 jeweils unabhängig für ein Benzonaphthofuranyl; ein Benzonaphthothiophenyl; ein Biphenyl, das unsubstituiert oder durch ein Methyl substituiert ist; ein Dibenzofuranyl; ein Dibenzothiophenyl; ein Dimethylfluorenyl, das unsubstituiert oder durch ein Phenyl substituiert ist; ein Diethylfluorenyl; ein Diphenylfluorenyl; ein Dipropylfluorenyl; ein Dibutylfluorenyl; ein Dipentylfluorenyl; ein Dihexylfluorenyl; ein Diheptylfluorenyl; ein Dioctylfluorenyl; ein Dimethylbenzofluorenyl, das unsubstituiert oder durch ein Phenyl substituiert ist; ein Diethylbenzofluorenyl; ein Diphenylbenzofluorenyl, das unsubstituiert oder durch ein Phenyl substituiert ist; ein Phenanthrenyl, das unsubstituiert oder durch ein Naphthyl, ein Phenyl, das unsubstituiert oder durch Deuterium substituiert ist, ein Dibenzofuranyl oder ein Phenyldimethylfluorenylamino substituiert ist; ein Phenyl, das unsubstituiert oder durch ein Naphthyl, ein Benzonaphthofuranyl, ein Benzonaphthothiophenyl oder ein Methyl substituiert ist; ein Naphthyl; ein Quaterphenyl; ein o-Terphenyl; ein m-Terphenyl; ein p-Terphenyl oder ein Carbazolyl, das unsubstituiert oder durch ein Phenyl, das unsubstituiert oder durch ein Methyl oder Adamantyl substituiert ist, ein Naphthyl, das unsubstituiert oder durch ein Methyl substituiert ist, oder Biphenyl substituiert ist; stehen; und diese können durch mindestens ein Deuterium substituiert sein..
-
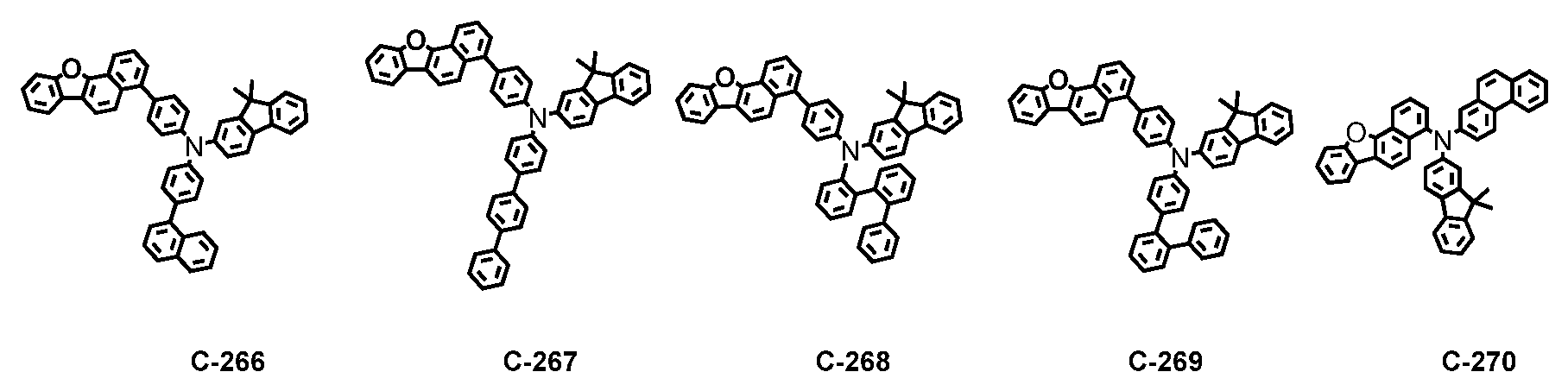
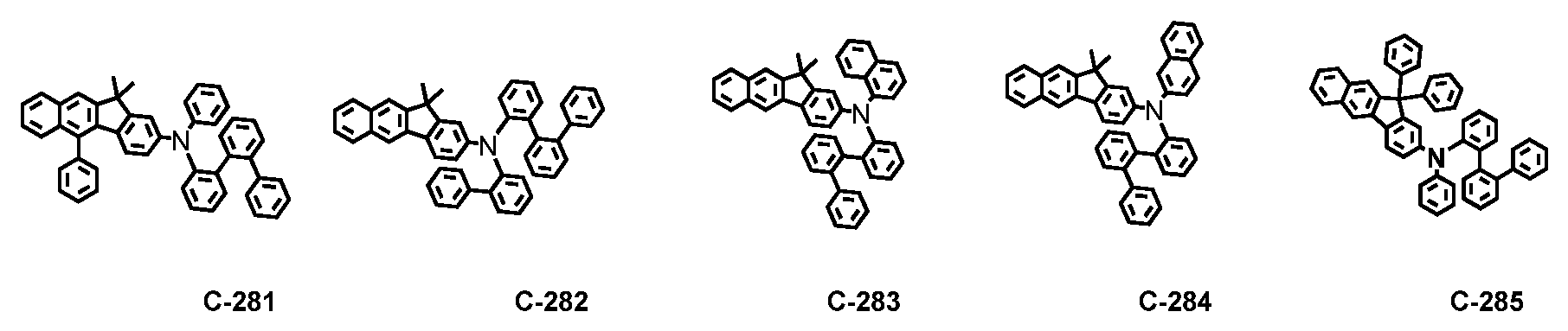
Die durch Formel 1 wiedergegebene Verbindung kann mindestens eine sein, die aus den folgenden Verbindungen ausgewählt ist, ist aber nicht darauf beschränkt.
-
In den obigen Verbindungen steht Dn dafür, dass n Wasserstoffatome durch Deuterium ersetzt sind, und n für eine ganze Zahl mit einem Wert von 1 oder mehr steht, wobei es sich um eine ganze Zahl mit einem Wert von 1 bis zur maximalen Zahl von Wasserstoffatomen in der Verbindung handelt.
-
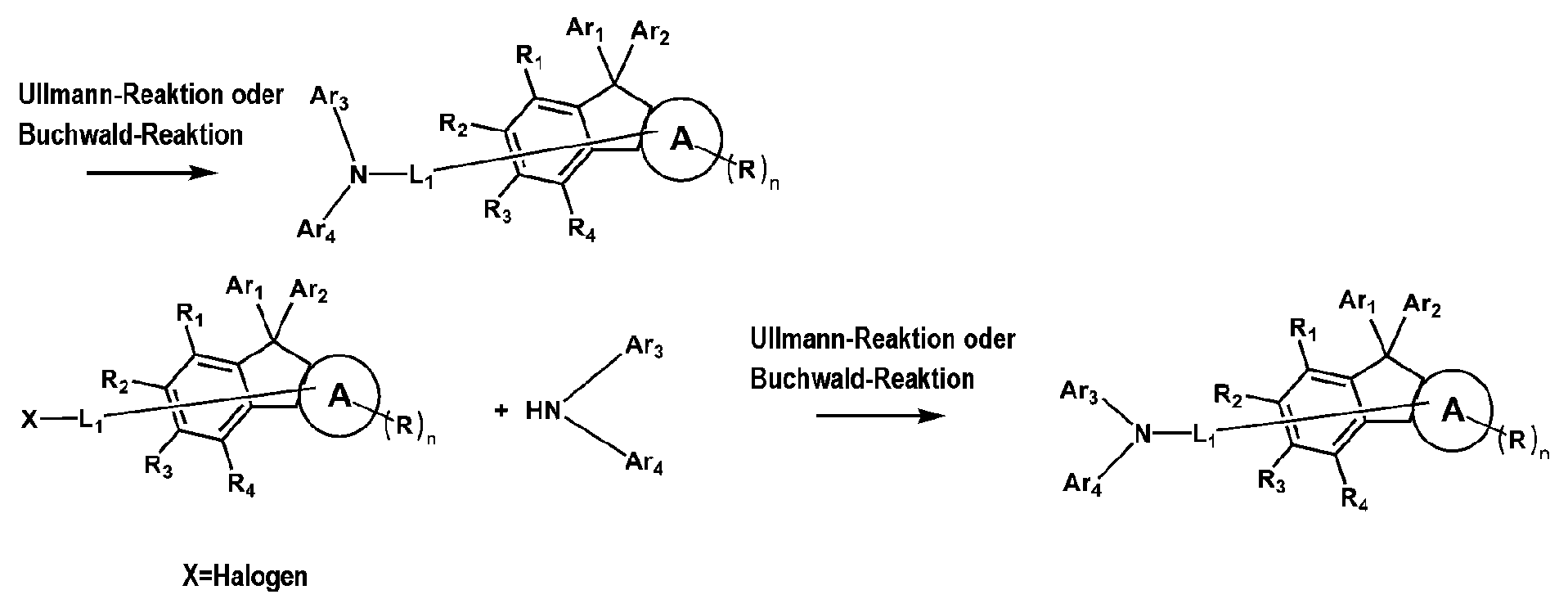
Beispiele für das Herstellungsverfahren für die durch Formel 1 oder Formel 1-1 bis 1-11 wiedergegebenen Verbindung gemäß der vorliegenden Offenbarung sind in dem folgenden Reaktionsschema 1 und den folgenden Reaktionsschemata 1-1 bis 1-4 gezeigt, aber nicht darauf beschränkt. Sie kann nach dem Fachmann bekannten Syntheseverfahren hergestellt werden.
-
In den obigen Reaktionsschemata sind R und n wie in Formel 1 definiert und sind R1 bis R12, L1 und Ar1 bis Ar4 wie in jeder der Formel 1-1 bis 1-11 definiert.
-
Wenngleich oben veranschaulichende Synthesebeispiele der durch die Formeln 1-1 bis 1-11 wiedergegebenen Verbindung beschrieben werden, ist es für den Fachmann leicht ersichtlich, dass sie alle auf einer Buchwald-Hartwig-Kreuzkupplungsreaktion, einer N-Arylierungsreaktion, einer H-Mont-vermittelten Veretherungsreaktion, einer Miyaura-Borylierungsreaktion, einer Suzuki-Kreuzkupplungsreaktion, einer intramolekularen säureinduzierten Cyclisierungsreaktion, einer Pd(II)-katalysierten oxidativen Cyclisierungsreaktion, einer Grignard-Reaktion, einer Heck-Reaktion, einer Cyclodehydratisierungsreaktion, einer SN1-Substitutionsreaktion, einer SN2-Substitutionsreaktion, einer phosphinvermittelten reduktiven Cyclisierungsreaktion usw. basieren und die obige Reaktion selbst dann abläuft, wenn Substituenten, die in den Formeln 1-1 bis 1-11 definiert, aber in dem spezifischen Synthesebeispiel nicht angegeben sind, gebunden sind.
-
In der organischen elektrolumineszierenden Vorrichtung emittiert die lichtemittierende Schicht eine beliebige Farbe von blau, grün oder rot, mit der Maßgabe, dass dann, wenn die lichtemittierende Schicht die blaue oder grüne Farbe emittiert, der Fall ausgeschlossen ist, dass R2 oder R7 von Formel 1-1 -L1-NAr3Ar4 ist.
-
In der organischen elektrolumineszierenden Vorrichtung umfasst die dritte Lochtransportschicht die durch die folgende Formel 2 wiedergegebene Verbindung.
-
Dabei gilt, dass in Formel 2
-
L2 bis L4 jeweils unabhängig für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C1-C30)-Alkylen, ein substituiertes oder unsubstituiertes (C6-C30)-Arylen, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroarylen oder ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkylen stehen. Gemäß einer Ausführungsform der vorliegenden Offenbarung können L2 bis L4 jeweils unabhängig für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C5-C25)-Alkylen oder ein substituiertes oder unsubstituiertes (C6-C25)-Arylen stehen. Gemäß einer anderen Ausführungsform der vorliegenden Offenbarung können L2 bis L4 jeweils unabhängig für eine Einfachbindung oder ein substituiertes oder unsubstituiertes (C6-C25)-Arylen stehen. Beispielsweise können L2 bis L4 jeweils unabhängig für eine Einfachbindung, ein Phenylen, das unsubstituiert oder durch Deuterium substituiert ist, ein Biphenylen, ein Terphenylen oder ein Naphthylen stehen, und diese können durch mindestens ein Deuterium substituiert sein.
-
Ar5 bis Ar7 stehen jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy, ein substituiertes oder unsubstituiertes Tri-(C1-C30)-alkylsilyl, ein substituiertes oder unsubstituiertes Di-(C1-C30)-alkyl-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyldi-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Tri-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Mono- oder Di-(C1-C30)-alkylamino, ein substituiertes oder unsubstituiertes Mono- oder Di-(C6-C30)-arylamino oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl-(C6-C30)-arylamino. Gemäß einer Ausführungsform der vorliegenden Offenbarung können Ar5 bis Ar7 jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C25)-Alkyl, ein substituiertes oder unsubstituiertes (C6-C25)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 25-gliedriges) Heteroaryl, ein substituiertes oder unsubstituiertes (C3-C25)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C1-C25)-Alkoxy, ein substituiertes oder unsubstituiertes Tri-(C1-C25)-alkylsilyl, ein substituiertes oder unsubstituiertes Di-(C1-C25)-alkyl-(C6-C25)-arylsilyl, ein substituiertes oder unsubstituiertes Tri-(C6-C25)-arylsilyl stehen. Beispielsweise können Ar5 bis Ar7 jeweils unabhängig für ein Phenyl, ein Biphenyl, ein Naphthyl, ein Dibenzofuranyl, ein Dibenzothiophenyl, ein Dibenzoselenophenyl, ein Benzonaphthofuranyl, ein Benzonaphthothiophenyl, ein Dimethylfluorenyl, ein Diethylfluorenyl, ein Diphenylfluorenyl, ein Diphenylbenzofluorenyl, ein Spirobifluorenyl, ein Carbazolyl, das unsubstituiert oder durch ein Phenyl oder ein Naphthyl substituiert ist, ein Phenanthrenyl, das unsubstituiert oder durch ein Phenyl oder ein Naphthyl substituiert ist, ein o-Terphenyl, ein m-Terphenyl, ein p-Terphenyl, ein Adamantyl oder eine beliebige der Formeln 2-1 bis 2-6 stehen, und diese können durch mindestens ein Deuterium substituiert sein.
-
Mit der Maßgabe, dass der Fall, bei dem L2 bis L4 alle Einfachbindungen sind und Ar5 bis Ar7 alle Wasserstoff sind, ausgeschlossen ist.
-
In der organischen elektrolumineszierenden Vorrichtung wird das Ar
5 in Formel 2 durch eine der folgenden Formeln 2-1 bis 2-6 wiedergegeben.
-
Dabei gilt, dass in den Formeln 2-1 bis 2-6
-
L5 für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C1-C30)-Alkylen, ein substituiertes oder unsubstituiertes (C6-C30)-Arylen, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroarylen oder ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkylen steht. Gemäß einer Ausführungsform der vorliegenden Offenbarung kann L5 für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C1-C30)-Alkylen oder ein substituiertes oder unsubstituiertes (C6-C30)-Arylen stehen. Gemäß einer anderen Ausführungsform der vorliegenden Offenbarung kann L5 für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C1-C20)-Alkylen oder ein substituiertes oder unsubstituiertes (C6-C20)-Arylen stehen. Beispielsweise kann L5 für eine Einfachbindung oder ein Phenylen stehen, und diese können durch mindestens ein Deuterium substituiert sein.
-
Ar8 ist mit L2 von Formel 2 verknüpft oder steht für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy, ein substituiertes oder unsubstituiertes Tri-(C1-C30)-alkylsilyl, ein substituiertes oder unsubstituiertes Di-(C1-C30)-alkyl-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyldi-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Tri-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Mono- oder Di-(C1-C30)-alkylamino, ein substituiertes oder unsubstituiertes Mono- oder Di-(C6-C30)-arylamino oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl-(C6-C30)-arylamino. Gemäß einer Ausführungsform der vorliegenden Offenbarung kann Ar8 mit L2 von Formel 2 verknüpft sein oder für Wasserstoff, Deuterium, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C30)-Aryl stehen. Gemäß einer anderen Ausführungsform der vorliegenden Offenbarung kann Ar8 mit L2 von Formel 2 verknüpft sein oder für Wasserstoff, ein substituiertes oder unsubstituiertes (C1-C20)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C20)-Aryl stehen. Beispielsweise kann Ar8 mit L2 von Formel 2 verknüpft sein oder für ein Phenyl oder ein Naphthyl stehen, und diese können durch mindestens ein Deuterium substituiert sein.
-
R17 bis R68 sind mit L2 von Formel 2 verknüpft oder stehen jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy, ein substituiertes oder unsubstituiertes Tri-(C1-C30)-alkylsilyl, ein substituiertes oder unsubstituiertes Di-(C1-C30)-alkyl-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyldi-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Tri-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Mono- oder Di-(C1-C30)-alkylamino, ein substituiertes oder unsubstituiertes Mono- oder Di-(C6-C30)-arylamino oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl-(C6-C30)-arylamino oder können mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein. Gemäß einer Ausführungsform der vorliegenden Offenbarung können R17 bis R68 mit L2 von Formel 2 verknüpft sein oder jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy stehen oder mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein. Gemäß einer anderen Ausführungsform der vorliegenden Offenbarung können R17 bis R68 mit L2 von Formel 2 verknüpft sein oder jeweils unabhängig für Wasserstoff, Deuterium, ein substituiertes oder unsubstituiertes (C6-C25)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 25-gliedriges) Heteroaryl stehen. Beispielsweise können R17 bis R68 mit L2 von Formel 2 verknüpft sein oder jeweils unabhängig für Wasserstoff, Deuterium, ein Phenyl oder ein Naphthyl stehen.
-
Mit der Maßgabe, dass mindestens eines von Ar8 und R17 bis R68 mit L2 von Formel 2 verknüpft ist.
-
In der organischen elektrolumineszierenden Vorrichtung wird Formel 2-3 durch eine der folgenden Formeln 2-3-a bis 2-3-c wiedergegeben oder Formel 2-4 durch eine der folgenden Formeln 2-4-a bis 2-4-c wiedergegeben.
-
In den Formeln 2-3-a bis 2-3-c und den Formeln 2-4-a bis 2-4-c sind R35 bis R50 wie in den Formeln 2-1 bis 2-6 definiert.
-
R69 bis R72 sind mit L2 von Formel 2 verknüpft oder stehen jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy, ein substituiertes oder unsubstituiertes Tri-(C1-C30)-alkylsilyl, ein substituiertes oder unsubstituiertes Di-(C1-C30)-alkyl-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyldi-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Tri-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Mono- oder Di-(C1-C30)-alkylamino, ein substituiertes oder unsubstituiertes Mono- oder Di-(C6-C30)-arylamino oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl-(C6-C30)-arylamino oder können mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein. Gemäß einer Ausführungsform der vorliegenden Offenbarung können R69 bis R72 mit L2 von Formel 2 verknüpft sein oder jeweils unabhängig für Wasserstoff, Deuterium, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl stehen. Beispielsweise können R69 bis R72 mit L2 von Formel 2 verknüpft sein und jeweils unabhängig für Wasserstoff stehen.
-
Mit der Maßgabe, dass mindestens eines von R35 bis R50 und R69 bis R72 mit L2 von Formel 2 verknüpft ist.
-
Die durch Formel 2 wiedergegebene Verbindung kann mindestens eine sein, die aus den folgenden Verbindungen ausgewählt ist, ist aber nicht darauf beschränkt.
-
In den obigen Verbindungen steht Dn dafür, dass n Wasserstoffatome durch Deuterium ersetzt sind, und n für eine ganze Zahl mit einem Wert von 1 oder mehr steht, wobei es sich um eine ganze Zahl mit einem Wert von 1 bis zur maximalen Zahl von Wasserstoffatomen in der Verbindung handelt.
-
Die durch Formel 2 wiedergegebene Verbindung gemäß der vorliegenden Offenbarung kann durch Bezugnahme auf dem Fachmann bekannte Syntheseverfahren, beispielsweise die in der koreanischen Patentanmeldung Nr.
2015-0066202 (veröffentlicht am 16. Juni 2015), der koreanischen Patentanmeldung Nr.
2015-0076129 (veröffentlicht am 6. Juli 2015), der koreanischen Patentanmeldung Nr.
2017-0043439 (veröffentlicht am 21. April 2017), der koreanischen Patentanmeldung Nr.
2019-0090695 (veröffentlicht am 2. August 2019), der koreanischen Patentanmeldung Nr.
2020-0004257 (veröffentlicht am 13. Januar 2020), der koreanischen Patentanmeldung Nr.
2020-0018275 (veröffentlicht am 19. Februar 2020) und der koreanischen Patentanmeldung Nr.
2020-0090091 (veröffentlicht am 28. Juli 2020) usw. offenbarten Verfahren, synthetisiert werden, die aber nicht darauf beschränkt sind.
-
In der organischen elektrolumineszierenden Vorrichtung umfasst die lichtemittierende Schicht eine lichtemittierende Schicht, die rotes Licht emittiert.
-
Im Folgenden wird eine organische elektrolumineszierende Verbindung gemäß einer Ausführungsform der vorliegenden Offenbarung ausführlicher beschrieben.
-
Die vorliegende Offenbarung stellt eine organische elektrolumineszierende Verbindung bereit, die durch die folgende Formel 1 wiedergegeben wird.
-
Dabei gilt, dass in Formel 1
-
Ring A für ein substituiertes oder unsubstituiertes Benzol, ein substituiertes oder unsubstituiertes Naphthalin oder ein substituiertes oder unsubstituiertes Phenanthren steht;
-
Ar1 und Ar2 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C2-C30)-Alkyl stehen;
-
R und R1 bis R4 jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy stehen oder mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein können; mit der Maßgabe, dass mindestens eines von R und R1 bis R4 durch -L1-NAr3Ar4 wiedergegeben wird;
-
L1 für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C6-C30)-Arylen oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroarylen steht;
-
Ar3 und Ar4 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C6-C30)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl stehen;
-
n für eine ganze Zahl von 1 bis 8 steht, dann, wenn n eine Mehrzahl ist, jedes von n gleich oder voneinander verschieden sein kann.
-
Formel 1 kann durch eine der folgenden Formeln 1-1 bis 1-11 wiedergegeben werden.
-
Dabei gilt, dass in den Formeln 1-1 bis 1-11
-
Ar1 und Ar2 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C2-C30)-Alkyl stehen. Gemäß einer Ausführungsform der vorliegenden Offenbarung können Ar1 und Ar2 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C2-C20)-Alkyl stehen. Gemäß einer anderen Ausführungsform der vorliegenden Offenbarung können Ar1 und Ar2 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C2-C10)-Alkyl stehen. Beispielsweise können Ar1 und Ar2 jeweils unabhängig für ein Methyl, ein Ethyl, ein Propyl, ein Butyl, ein Pentyl, ein Hexyl, ein Heptyl oder ein Octyl stehen, und diese können durch mindestens ein Deuterium substituiert sein.
-
R1 bis R16 stehen jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy oder können mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein; mit der Maßgabe, dass mindestens eines von R1 bis R16 durch -L1-NAr3Ar4 wiedergegeben wird. Gemäß einer Ausführungsform der vorliegenden Offenbarung stehen R1 bis R16 jeweils unabhängig für Wasserstoff, Deuterium, ein substituiertes oder unsubstituiertes (C1-C20)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C20)-Aryl oder können mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren Ringen verknüpft sein; mit der Maßgabe, dass mindestens eines von R1 bis R16 durch -L1-NAr3Ar4 wiedergegeben wird. Beispielsweise stehen R1 bis R16 jeweils unabhängig für Wasserstoff, Deuterium oder -L1-NAr3Ar4.
-
L1 steht für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C6-C30)-Arylen oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroarylen. Gemäß einer Ausführungsform der vorliegenden Offenbarung kann L1 für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C6-C25)-Arylen oder ein substituiertes oder unsubstituiertes (3- bis 25-gliedriges) Heteroarylen stehen. Beispielsweise kann L1 für eine Einfachbindung oder ein Phenylen stehen.
-
Ar3 und Ar4 stehen jeweils unabhängig für ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl. Gemäß einer Ausführungsform der vorliegenden Offenbarung können Ar3 und Ar4 jeweils unabhängig für ein substituiertes oder unsubstituiertes (C6-C30)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 25-gliedriges) Heteroaryl stehen. Beispielsweise können Ar3 und Ar4 jeweils unabhängig für ein Benzonaphthofuranyl; ein Benzonaphthothiophenyl; ein Biphenyl; ein Dibenzofuranyl; ein Dibenzothiophenyl; ein Dimethylfluorenyl; ein Diethylfluorenyl; ein Diphenylfluorenyl; ein Dimethylbenzofluorenyl; ein Diethylbenzofluorenyl; ein Dipropylfluorenyl; ein Dibutylfluorenyl; ein Dipentylfluorenyl; ein Dihexylfluorenyl; ein Diheptylfluorenyl; ein Dioctylfluorenyl; ein Diphenylbenzofluorenyl; ein Naphthyl; ein Phenanthrenyl, das unsubstituiert oder durch ein Naphthyl, ein Phenyl, ein Phenyl, das durch Deuterium substituiert ist, ein Dibenzofuranyl oder ein Phenyldimethylfluorenylamino substituiert ist; ein Phenyl, das unsubstituiert oder durch ein Methyl, ein Naphthyl, ein Benzonaphthofuranyl oder ein Benzonaphthothiophenyl substituiert ist; ein Quaterphenyl; ein o-Terphenyl oder ein p-Terphenyl stehen, und diese können durch mindestens ein Deuterium substituiert sein.
-
Ar
3 in Formel 1 wird durch eine der folgenden Formeln wiedergegeben.
-
In den obigen Formeln gilt, dass
X für O, S, NR73 oder CR74R75 steht. Beispielsweise kann X für O, S oder CR74R75 stehen.
-
R' und R73 bis R75 stehen jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy, ein substituiertes oder unsubstituiertes Tri-(C1-C30)-alkylsilyl, ein substituiertes oder unsubstituiertes Di-(C1-C30)-alkyl-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyldi-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Tri-(C6-C30)-arylsilyl, ein substituiertes oder unsubstituiertes Mono- oder Di-(C1-C30)-alkylamino, ein substituiertes oder unsubstituiertes Mono- oder Di-(C6-C30)-arylamino oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl-(C6-C30)-arylamino oder können mit einem oder mehreren benachbarten Substituenten zu einem oder mehreren substituierten oder unsubstituierten (3- bis 30-gliedrigen) monocyclischen oder polycyclischen Ringen verknüpft sein. Gemäß einer Ausführungsform der vorliegenden Offenbarung stehen R' und R73 bis R75 jeweils unabhängig für Wasserstoff, Deuterium, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C30)-Aryl. Gemäß einer anderen Ausführungsform der vorliegenden Offenbarung können R' und R73 bis R75 jeweils unabhängig für Wasserstoff, Deuterium, ein substituiertes oder unsubstituiertes (C1-C20)-Alkyl oder ein substituiertes oder unsubstituiertes (C6-C20)-Aryl stehen. Beispielsweise können R' und R73 bis R75 jeweils unabhängig für Wasserstoff; Deuterium; ein Methyl, das unsubstituiert oder durch Deuterium substituiert ist; ein Ethyl, das unsubstituiert oder durch Deuterium substituiert ist; ein Propyl, das unsubstituiert oder durch Deuterium substituiert ist; ein Butyl, das unsubstituiert oder durch Deuterium substituiert ist; ein Pentyl, das unsubstituiert oder durch Deuterium substituiert ist; ein Hexyl, das unsubstituiert oder durch Deuterium substituiert ist, ein Heptyl, das unsubstituiert oder durch Deuterium substituiert ist; ein Octyl, das unsubstituiert oder durch Deuterium substituiert ist; oder ein Phenyl, das unsubstituiert oder durch Deuterium substituiert ist, stehen.
-
In jeder Formel ist ein beliebiges von R' mit L1 von Formel 1 verknüpft.
-
In jeder Formel stehen a und b jeweils unabhängig für eine ganze Zahl von 1 bis 4, stehen c und d jeweils unabhängig für eine ganze Zahl von 1 bis 6, steht e für eine ganze Zahl von 1 bis 10 und kann dann, wenn a bis e für eine ganze Zahl mit einem Wert von 2 oder mehr stehen, jedes von R' gleich oder voneinander verschieden sein.
-
Die durch Formel 1 wiedergegebene Verbindung kann mindestens eine sein, die aus den folgenden Verbindungen ausgewählt ist, ist aber nicht darauf beschränkt.
-
Wobei in den obigen Verbindungen Dn dafür steht, dass n Wasserstoffatome durch Deuterium ersetzt sind, und n für eine ganze Zahl mit einem Wert von 1 oder mehr steht, wobei es sich um eine ganze Zahl mit einem Wert von 1 bis zur maximalen Zahl von Wasserstoffatomen in der Verbindung handelt.
-
Die organische elektrolumineszierende Vorrichtung gemäß einer Ausführungsform der vorliegenden Offenbarung kann die durch Formel 1 wiedergegebene organische elektrolumineszierende Verbindung umfassen.
-
Außerdem stellt die vorliegende Offenbarung die organische elektrolumineszierende Verbindung bereit, die durch die folgende Formel 3 wiedergegeben wird.
-
Dabei gilt, dass in Formel 3 mindestens eines von R
a bis R
j durch die folgende Formel 3-1 wiedergegeben wird.
-
Dabei gilt, dass in Formel 3 und Formel 3-1
-
R
a bis R
m jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein Cyano, ein substituiertes oder unsubstituiertes (C1-C30)-Alkyl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl stehen. Gemäß einer Ausführungsform der vorliegenden Offenbarung können R
a bis R
m jeweils unabhängig für Wasserstoff, Deuterium, ein substituiertes oder unsubstituiertes (C6-C20)-Aryl oder ein substituiertes oder unsubstituiertes (3- bis 20-gliedriges) Heteroaryl stehen. Beispielsweise können R
a bis R
m jeweils unabhängig für Wasserstoff, Deuterium, ein Phenyl, das unsubstituiert oder durch Deuterium substituiert ist, ein Naphthyl, ein Biphenyl, das unsubstituiert oder durch Deuterium substituiert ist oder ein m-Terphenyl, das unsubstituiert oder durch Deuterium substituiert ist, stehen.
steht für die Bindung zwischen Formel 3 und Formel 3-1.
-
L6 bis L8 stehen jeweils unabhängig für eine Einfachbindung, ein substituiertes oder unsubstituiertes (C6-C30)-Arylen oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroarylen. Gemäß einer Ausführungsform der vorliegenden Offenbarung können L6 bis L8 jeweils unabhängig für eine Einfachbindung oder ein substituiertes oder unsubstituiertes (C6-C20)-Arylen stehen. Beispielsweise können L6 bis L8 jeweils unabhängig für eine Einfachbindung, ein Phenylen, das unsubstituiert oder durch Deuterium substituiert ist, ein Naphthylen, ein Biphenylenylen, das unsubstituiert oder durch Deuterium substituiert ist, oder ein m-Terphenylen, das unsubstituiert oder durch Deuterium substituiert ist, stehen.
-
Ar8 steht für ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl oder ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl. Gemäß einer Ausführungsform der vorliegenden Offenbarung kann Ar8 für ein substituiertes oder unsubstituiertes (C6-C20)-Aryl, ein substituiertes oder unsubstituiertes (C3-C20)-Cycloalkyl oder ein substituiertes oder unsubstituiertes (3- bis 20-gliedriges) Heteroaryl stehen. Beispielsweise kann Ar8 für ein Phenyl, das unsubstituiert oder durch Deuterium oder ein Naphthyl substituiert ist, ein Biphenyl, das unsubstituiert oder durch Deuterium substituiert ist, ein Naphthyl, ein Dibenzofuranyl, ein Dibenzothiophenyl, ein Dimethylfluorenyl, ein Diphenylfluorenyl, ein Dibenzoselenophenyl, ein Spirobifluorenyl, ein o-Terphenyl, ein m-Terphenyl oder ein Adamantyl stehen.
-
k und l stehen jeweils unabhängig für eine ganze Zahl von 1 bis 5, und m steht für eine ganze Zahl von 1 bis 3. Beispielsweise können k und l jeweils unabhängig für eine ganze Zahl mit einem Wert von 5 stehen, und m für eine ganze Zahl mit einem Wert von 3 stehen.
-
Dann, wenn k bis m für eine ganze Zahl mit einem Wert von 2 oder mehr stehen, kann jedes von Rk bis Rm gleich oder voneinander verschieden sein.
-
Gemäß einer Ausführungsform der vorliegenden Erfindung kann die durch Formel 3-1 wiedergegebene Verbindung durch eine der folgenden Formeln 3-1a bis 3-1f wiedergegeben werden.
-
Dabei gilt, dass in den Formeln 3-1a bis 3-1f
für eine an Formel 3 gebundene Verknüpfungsgruppe steht;
L
6 bis L
8, Ar
8 und R
k bis R
m wie in Formel 3 und Formel 3-1 definiert sind;
k und /jeweils unabhängig für eine ganze Zahl von 1 bis 5 stehen, m für eine ganze Zahl von 1 bis 3 steht;
und dann, wenn k bis m für eine ganze Zahl mit einem Wert von 2 oder mehr stehen, jedes von R
k bis R
m gleich oder voneinander verschieden sein kann.
-
Die durch Formel 3 wiedergegebene Verbindung kann mindestens eine sein, die aus den folgenden Verbindungen ausgewählt ist, ist aber nicht darauf beschränkt.
-
Wobei in den obigen Verbindungen Dn dafür steht, dass n Wasserstoffatome durch Deuterium ersetzt sind, und n für eine ganze Zahl mit einem Wert von 1 oder mehr steht, wobei es sich um eine ganze Zahl mit einem Wert von 1 bis zur maximalen Zahl von Wasserstoffatomen in der Verbindung handelt.
-
Beispiele für das Herstellungsverfahren für die durch Formel 3 wiedergegebene Verbindung gemäß der vorliegenden Offenbarung sind in dem folgenden Reaktionsschema 2 und dem folgenden Reaktionsschema 3 gezeigt, aber nicht darauf beschränkt. Eine derartige Verbindung kann nach dem Fachmann bekannten Syntheseverfahren hergestellt werden.
-
In dem obigen Reaktionsschema 2 und dem obigen Reaktionsschema 3 sind Ra bis Rm, L6 bis L8, Ar8 und k bis m wie in Formel 3 und Formel 3-1 definiert.
-
Die organische elektrolumineszierende Vorrichtung gemäß der vorliegenden Offenbarung kann die durch Formel 3 wiedergegebene organische elektrolumineszierende Verbindung umfassen.
-
Die lichtemittierende Schicht kann einen oder mehrere Wirte und einen oder mehrere Dotierstoffe enthalten. Gegebenenfalls kann die lichtemittierende Schicht ein Co-Wirtsmaterial, d. h. mehrere Wirtsmaterialien, enthalten. Bei dem in der vorliegenden Erfindung verwendeten Wirt kann es sich um eine phosphoreszierende Wirtsverbindung oder fluoreszierende Wirtsverbindung handeln, und diese Wirtsverbindungen unterliegen keinen besonderen Beschränkungen darauf.
-
Gemäß einer Ausführungsform der vorliegenden Offenbarung kann die Dotierungskonzentration der Dotierstoffverbindung, bezogen auf die Wirtsverbindung der lichtemittierenden Schicht, weniger als 20 Gew.-% betragen. Der in der organischen elektrolumineszierenden Vorrichtung der vorliegenden Offenbarung enthaltene Dotierstoff kann mindestens ein phosphoreszierender oder fluoreszierender Dotierstoff sein und ist vorzugsweise ein phosphoreszierender Dotierstoff. Die auf die organische elektrolumineszierende Vorrichtung der vorliegenden Offenbarung angewendeten phosphoreszierenden Dotierstoffmaterialien unterliegen keinen besonderen Einschränkungen, aber es kann sich dabei um eine metallierte Komplexverbindung eines Metallatoms, das aus Iridium (Ir), Osmium (Os), Kupfer (Cu) und Platin (Pt) ausgewählt ist, und vorzugsweise eine ortho-metallierte Komplexverbindung eines Metallatoms, das aus Iridium (Ir), Osmium (Os), Kupfer (Cu) und Platin (Pt) ausgewählt ist, und weiter bevorzugt eine ortho-metallierte Iridium-Komplexverbindung handeln.
-
Bei dem in der organischen elektrolumineszierenden Vorrichtung der vorliegenden Offenbarung enthaltenen Dotierstoff kann es sich um eine durch die folgende Formel 101 wiedergegebene Verbindung handeln, er ist aber nicht darauf beschränkt.
-
Dabei gilt, dass in Formel 101
-
L aus einer der folgenden Strukturen 1 bis 3 ausgewählt ist:
-
R100 bis R103 jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein (C1-C30)-Alkyl, das unsubstituiert oder durch Deuterium und/oder ein oder mehrere Halogene substituiert ist, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein Cyano, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy stehen oder mit einem benachbarten Substituenten zu einem oder mehreren Ringen, z. B. einem substituierten oder unsubstituierten Chinolin, Benzofuropyridin, Benzothienopyridin, Indenopyridin, Benzofurochinolin, Benzothienochinolin oder Indenochinolin, zusammen mit Pyridin verknüpft sein können;
-
R104 bis R107 jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein (C1-C30)-Alkyl, das unsubstituiert oder durch Deuterium und/oder ein oder mehrere Halogene substituiert ist, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl, ein substituiertes oder unsubstituiertes (C6-C30)-Aryl, ein substituiertes oder unsubstituiertes (3- bis 30-gliedriges) Heteroaryl, ein Cyano oder ein substituiertes oder unsubstituiertes (C1-C30)-Alkoxy stehen oder mit einem benachbarten Substituenten zu einem oder mehreren substituierten oder unsubstituierten Ringen, z. B. einem substituierten oder unsubstituierten Naphthalin, Fluoren, Dibenzothiophen, Dibenzofuran, Indenopyridin, Benzofuropyridin oder Benzothienopyridin, zusammen mit Benzol verknüpft sein können;
-
R201 bis R220 jeweils unabhängig für Wasserstoff, Deuterium, ein Halogen, ein (C1-C30)-Alkyl, das unsubstituiert oder durch Deuterium und/oder ein oder mehrere Halogene substituiert ist, ein substituiertes oder unsubstituiertes (C3-C30)-Cycloalkyl oder ein substituiertes oder unsubstituiertes (C6-C30)-Aryl stehen oder mit einem benachbarten Substituenten zu einem oder mehreren substituierten oder unsubstituierten Ringen verknüpft sein können; und
s für eine ganze Zahl von 1 bis 3 steht.
-
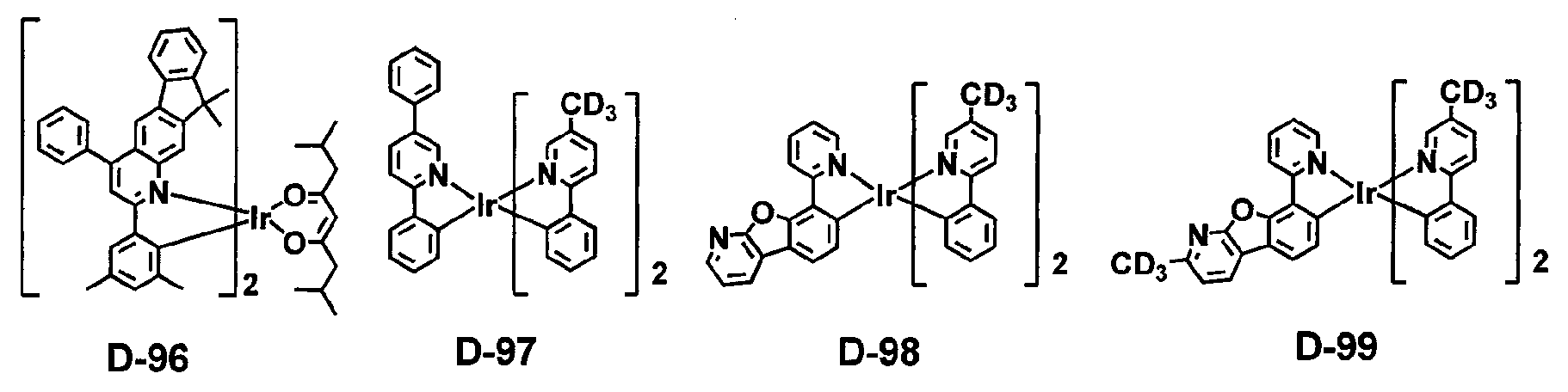
Die spezifischen Beispiele für die Dotierstoffverbindung sind wie folgt, aber nicht darauf beschränkt.
-
Die organische elektrolumineszierende Vorrichtung gemäß der vorliegenden Offenbarung umfasst eine Anode; eine Kathode und mindestens eine organische Schicht zwischen der Anode und der Kathode. Die organische Schicht umfasst eine lichtemittierende Schicht und kann ferner mindestens eine Schicht umfassen, die aus beliebigen der folgenden ausgewählt ist: einer Lochinjektionsschicht, einer Lochtransportschicht, einer Lochhilfsschicht, einer lichtemittierenden Hilfsschicht, einer Elektronentransportschicht, einer Elektronenpufferschicht, einer Elektroneninjektionsschicht, einer Zwischenschicht, einer Lochblockierschicht und einer Elektronenblockierschicht. Jede der Schichten kann ferner in Form von mehreren Schichten ausgeführt sein.
-
Die Anode und die Kathode können jeweils aus einem transparenten leitfähigen Material oder einem transflektiven oder reflektiven leitfähigen Material ausgebildet sein. In Abhängigkeit von dem Typ von Material, aus dem die Anode und die Kathode ausgebildet sind, kann die organische elektrolumineszierende Vorrichtung vom Oberseitenlichtemissionstyp, Unterseitenlichtemissionstyp oder Doppelseitenlichtemissionstyp sein. Außerdem kann die Lochinjektionsschicht ferner mit einem oder mehreren p-Dotierstoffen dotiert sein und die Elektroneninjektionsschicht ferner mit einem oder mehreren n-Dotierstoffen dotiert sein.
-
In der organischen Schicht kann ferner mindestens eine Verbindung aus der Gruppe bestehend aus Verbindungen auf Arylamin-Basis und Verbindungen auf Styrylarylamin-Basis enthalten sein. Außerdem kann die Schicht aus organischem Material ferner mindestens ein Metall aus der Gruppe bestehend aus Metallen der Gruppe 1, Metallen der Gruppe 2, Übergangsmetallen der 4. Periode, Übergangsmetallen der 5. Periode, Lanthaniden und organischen Metallen der d-Übergangselemente des Periodensystems oder mindestens eine Komplexverbindung, die das Metall umfasst, umfassen.
-
Außerdem kann die organische elektrolumineszierende Vorrichtung der vorliegenden Offenbarung dadurch, dass sie neben der Verbindung der vorliegenden Offenbarung ferner mindestens eine lichtemittierende Schicht, die eine blaue, rote oder grüne lichtemittierende Verbindung, die in der Technik bekannt ist, umfasst, weißes Licht emittieren. Außerdem kann sie gegebenenfalls ferner eine gelbes oder orangefarbenes Licht emittierende Schicht umfassen.
-
In der organischen elektrolumineszierenden Vorrichtung der vorliegenden Offenbarung ist vorzugsweise mindestens eine aus einer Chalcogenidschicht, einer Metallhalogenidschicht und einer Metalloxidschicht ausgewählte Schicht (die im Folgenden als eine „Oberflächenschicht“ bezeichnet wird) auf mindestens einer Innenoberflächen eines Paars von Elektroden angeordnet. Im Einzelnen ist eine Schicht aus Chalcogenid (einschließlich eines Oxids) von Silicium und Aluminium vorzugsweise auf eine Anodenoberfläche einer Seite der Schicht aus einem elektrolumineszierenden Medium angeordnet und eine Metallhalogenidschicht oder eine Metalloxidschicht vorzugsweise auf einer Kathodenoberfläche einer Seite der Schicht aus elektrolumineszierendem Medium angeordnet. Durch die Oberflächenschicht kann Treibstabilisierung der organischen elektrolumineszierenden Vorrichtung erhalten werden. Bevorzugte Beispiele für das Chalcogenid sind u. a. SiOX (1≤X≤2), AlOX (1≤X≤1,5), SiON, SiAlON usw.; bevorzugte Beispiele für das Metallhalogenid sind u. a. LiF, MgF2, CaF2, ein Seltenerdmetallfluorid usw., und bevorzugte Beispiele für das Metalloxid sind u. a. Cs2O, Li2O, MgO, SrO, BaO, CaO usw.
-
Zwischen einer Anode und einer lichtemittierenden Schicht kann eine Lochinjektionsschicht, eine Lochtransportschicht, eine Elektronenblockierschicht oder eine Kombination davon verwendet werden. Die Lochinjektionsschicht kann zur Erniedrigung der Lochinjektionsbarriere (oder Lochinjektionsspannung) von der Anode zur Lochtransportschicht oder Elektronenblockierschicht mehrschichtig ausgebildet sein, wobei in jeder der mehreren Schichten zwei Verbindungen gleichzeitig verwendet werden können. Die Lochtransportschicht oder die Elektronenblockierschicht kann mehrschichtig sein.
-
Zwischen einer lichtemittierenden Schicht und einer Kathode kann eine Elektronenpufferschicht, eine Lochblockierschicht, eine Elektronentransportschicht, eine Elektroneninjektionsschicht oder eine Kombination davon verwendet werden. Die Elektronenpufferschicht kann mehrschichtig sein, um die Elektroneninjektion zu steuern und Grenzflächeneigenschaften zwischen der lichtemittierenden Schicht und der Elektroneninjektionsschicht zu verbessern, wobei in jeder der mehreren Schichten zwei Verbindungen gleichzeitig verwendet werden können. Die Lochblockierschicht oder die Elektronentransportschicht kann mehrschichtig sein, wobei in jeder der mehreren Schichten mehrere Verbindungen verwendet werden können.
-
Eine lichtemittierende Hilfsschicht kann eine Schicht sein, die zwischen einer Anode und einer lichtemittierenden Schicht oder zwischen einer Kathode und einer lichtemittierenden Schicht angeordnet ist. Bei Anordnung zwischen der Anode und der lichtemittierenden Schicht kann die lichtemittierende Hilfsschicht zur Förderung der Lochinjektion und/oder des Lochtransports oder zur Blockierung des Überfließens von Elektronen verwendet werden. Bei Anordnung zwischen der Katode und der lichtemittierenden Schicht kann die lichtemittierende Hilfsschicht zur Förderung der Elektroneninjektion und/oder des Elektronentransports oder zur Blockierung des Überfließens von Löchern verwendet werden. Außerdem kann die Lochhilfsschicht zwischen der Lochtransportschicht (oder Lochinjektionsschicht) und der lichtemittierenden Schicht angeordnet sein und kann eine Wirkung des Ermöglichens oder Blockierens der Lochtransportrate (oder Lochinjektionsrate) zeigen und kann demgemäß die Ladungsbalance einstellen. Außerdem kann die Elektronenblockierschicht zwischen der Lochtransportschicht (oder Lochinjektionsschicht) und der lichtemittierenden Schicht angeordnet sein und das Überfließen von Elektronen aus der lichtemittierenden Schicht blockieren und die Exzitonen in der lichtemittierenden Schicht beschränken, um eine Lichtleckage zu verhindern. Wenn eine organische elektrolumineszierende Vorrichtung zwei oder mehr Lochtransportschichten enthält, kann die Lochtransportschicht, die ferner enthalten ist, als Lochhilfsschicht oder Elektronenblockierschicht verwendet werden. Die lichtemittierende Hilfsschicht, die Lochhilfsschicht oder die Elektronenblockierschicht können die Wirkung haben, die Effizienz und/oder die Lebensdauer der organischen elektrolumineszierenden Vorrichtung zu verbessern.
-
Außerdem kann in einer organischen elektrolumineszierenden Vorrichtung der vorliegenden Offenbarung eine gemischte Region aus einer Elektronentransportverbindung und einem reduktiven Dotierstoff oder eine gemischte Region aus einer Lochtransportverbindung und einem oxidativen Dotierstoff auf mindestens einer Oberfläche eines Paars von Elektroden angeordnet sein. In diesem Fall wird die Elektronentransportverbindung zu einem Anion reduziert, wodurch es leichter wird, Elektronen aus dem gemischten Bereich in das lichtemittierende Medium zu injizieren und zu transportieren. Des Weiteren wird die Lochtransportverbindung zu einem Kation oxidiert, wodurch es leichter wird, Löcher aus dem gemischten Bereich in das lichtemittierende Medium zu injizieren und zu transportieren. Zu den bevorzugten oxidativen Dotierstoffen gehören verschiedene Lewis-Säure- und -Akzeptor-Verbindungen, und zu den bevorzugten reduktiven Dotierstoffen gehören Alkalimetalle, Alkalimetallverbindungen, Erdalkalimetalle, Seltenerdmetalle und Mischungen davon. Außerdem kann durch Verwendung der Schicht aus reduktivem Dotierstoff als Ladungserzeugungsschicht eine organische elektrolumineszierende Vorrichtung hergestellt werden, die mindestens zwei lichtemittierende Schichten aufweist und weißes Licht emittiert.
-
Eine organische elektrolumineszierende Vorrichtung kann gemäß der vorliegenden Offenbarung eine organische elektrolumineszierende Vorrichtung mit einer Tandemstruktur sein. Im Fall der organischen elektrolumineszierenden Tandemvorrichtung kann gemäß einer Ausführungsform eine einzige lichtemittierende Einheit (lichtemittierender Teil) in einer Struktur, in der zwei oder mehr Einheiten durch eine Ladungserzeugungsschicht verbunden sind, ausgebildet sein. Die organische elektrolumineszierende Vorrichtung kann eine Mehrzahl von zwei oder mehr lichtemittierenden Einheiten, beispielsweise eine Mehrzahl von drei oder mehr lichtemittierenden Einheiten, mit einer ersten Elektrode und einer zweiten Elektrode, die auf einem Substrat einander gegenüberliegen, und eine lichtemittierende Schicht, die zwischen der ersten Elektrode und der zweiten Elektrode angeordnet ist und Licht in einem spezifischen Wellenlängenbereich emittiert, enthalten. Sie kann mehrere lichtemittierende Einheiten enthalten, und jede der lichtemittierenden Einheiten kann eine Lochtransportzone, eine lichtemittierende Schicht und eine Elektronentransportzone enthalten, die Lochtransportzone kann eine Lochinjektionsschicht und eine Lochtransportschicht enthalten, und die Elektronentransportzone kann eine Elektronentransportschicht und eine Elektroneninjektionsschicht enthalten. Gemäß einer Ausführungsform der vorliegenden Offenbarung können in der lichtemittierenden Einheit drei oder mehr lichtemittierende Schichten enthalten sein. Mehrere lichtemittierende Einheiten können die gleiche Farbe oder verschiedene Farben emittieren. Zusätzlich kann eine lichtemittierende Einheit eine oder mehrere lichtemittierende Schichten enthalten, und die mehreren lichtemittierenden Schichten können lichtemittierende Schichten der gleichen Farbe oder verschiedener Farben sein. Sie kann eine oder mehrere Ladungserzeugungsschichten enthalten, die sich zwischen jeder lichtemittierenden Einheit befinden. Die Ladungserzeugungsschicht bezieht sich auf eine Schicht, in der beim Anlegen einer Spannung Löcher und Elektronen erzeugt werden. Bei Vorliegen von drei oder mehr lichtemittierenden Einheiten kann sich zwischen jeder lichtemittierenden Einheit eine Ladungserzeugungsschicht befinden. Dabei können die mehreren Ladungserzeugungsschichten gleich oder voneinander verschieden sein. Durch Anordnen der ladungserzeugenden Schicht zwischen lichtemittierenden Einheiten wird die Stromeffizienz in jeder lichtemittierenden Einheit erhöht, und Ladungen können problemlos verteilt werden. Im Einzelnen wird die Ladungserzeugungsschicht zwischen zwei benachbarten Stapeln bereitgestellt und kann dazu dienen, eine organische elektrolumineszierende Tandemvorrichtung unter Verwendung von nur einem Paar von Anoden und Kathoden ohne eine separate interne Elektrode zwischen den Stapeln zu treiben.
-
Die Ladungserzeugungsschicht kann aus einer Ladungserzeugungsschicht vom n-Typ und einer Ladungserzeugungsschicht vom p-Typ bestehen, und die Ladungserzeugungsschicht vom n-Typ kann mit einem Alkalimetall, einem Erdalkalimetall oder einer Verbindung eines Alkalimetalls und eines Erdalkalimetalls dotiert sein. Das Alkalimetall kann eines aus der Gruppe bestehend aus Li, Na, K, Rb, Cs, Fr, Yb und Kombinationen davon umfassen, und das Erdalkalimetall kann eines aus der Gruppe bestehend aus Be, Mg, Ca, Sr, Ba, Ra und Kombinationen davon umfassen. Die Ladungserzeugungsschicht vom p-Typ kann aus einem Metall oder einem organischen Material, das mit einem Dotierstoff vom p-Typ dotiert ist, bestehen. Beispielsweise kann das Metall aus einer oder zwei oder mehr Legierungen aus der Gruppe bestehend aus Al, Cu, Fe, Pb, Zn, Au, Pt, W, In, Mo, Ni und Ti bestehen. Zusätzlich können gemeinhin verwendete Materialien als Dotierstoff vom p-Typ und in dem p-Typ-dotierten organischen Material verwendete Wirtsmaterialien verwendet werden.
-
Das organische elektrolumineszierende Material gemäß einer Ausführungsform der vorliegenden Offenbarung kann als lichtemittierendes Material für eine weiße organische lichtemittierende Vorrichtung verwendet werden. Die weiße organische lichtemittierende Vorrichtung ist in verschiedenen Strukturen vorgeschlagen worden, wie einer Methode mit Seite-an-Seite-Anordnung, einer Methode mit Stapelungsanordnung oder einer Methode mit einem Farbumwandlungsmaterial (Color Conversion Material, CCM) usw., gemäß der Anordnung von rotes (R), grünes (G) oder gelblich-grünes (YG) und blaues (B) Licht emittierenden Einheiten. Außerdem kann das organische elektrolumineszierende Material gemäß einer Ausführungsform der vorliegenden Offenbarung auch in einer organischen elektrolumineszierenden Vorrichtung, die einen Quantenpunkt (Quantum Dot, QD) umfasst, verwendet werden.
-
Zur Bildung jeder Schicht der organischen elektrolumineszierenden Vorrichtung der vorliegenden Offenbarung können Trockenfilmbildungsverfahren wie Vakuumverdampfung, Sputtern, Plasma, lonenplattierungsverfahren usw. oder Nassfilmbildungsverfahren wie Tintenstrahldruck, Düsendruck, Spritzbeschichten, Aufschleudern, Tauchbeschichten, Fluten usw. verwendet werden. Bei der Bildung einer Schicht aus der ersten Wirtsverbindung und der zweiten Wirtsverbindung der vorliegenden Offenbarung wird Coabscheidung oder Mischabscheidung durchgeführt.
-
Bei Verwendung eines Nassfilmbildungsverfahrens kann durch Lösen oder Diffundieren von jede Schicht bildenden Materialien in einem geeigneten Lösungsmittel wie Ethanol, Chloroform, Tetrahydrofuran, Dioxan usw. ein dünner Film gebildet werden. Bei dem Lösungsmittel kann es sich um ein beliebiges Lösungsmittel handeln, in dem die jede Schicht bildenden Materialien gelöst oder diffundiert werden können und bei dem es keine Probleme hinsichtlich der Filmbildungsfähigkeit gibt.
-
Außerdem ist es möglich, unter Verwendung der organischen elektrolumineszierenden Vorrichtung der vorliegenden Offenbarung ein Anzeigesystem, z. B. ein Anzeigesystem für Smartphones, Tablets, Notebooks, PCs, Fernseher oder Autos, oder ein Beleuchtungssystem, z. B. ein Außen- oder Innenbeleuchtungssystem, herzustellen.
-
Im Folgenden werden das Herstellungsverfahren der Verbindung der vorliegenden Offenbarung, deren Eigenschaften und die Treiberspannung und die Lichtausbeute der organischen elektrolumineszierenden Vorrichtung (OLED), die eine organische elektrolumineszierende Verbindung gemäß der vorliegenden Offenbarung umfasst, unter Bezugnahme auf die repräsentativen Verbindungen der vorliegenden Offenbarung ausführlich erklärt. Die folgenden Beispiele beschreiben jedoch lediglich die Eigenschaften der Verbindung gemäß der vorliegenden Offenbarung und der OLED, die sie umfasst, und die vorliegende Offenbarung ist nicht auf die folgenden Beispiele beschränkt.
-
Im Folgenden wird das Herstellungsverfahren der Wirtsmaterialien gemäß der vorliegenden Offenbarung unter Bezugnahme auf das Syntheseverfahren einer repräsentativen Verbindung oder Zwischenverbindung erklärt, um die vorliegende Offenbarung im Detail zu verstehen.
-
In einen Kolben wurden Verbindung 1-1 (CAS: 373390-07-9) (10,5 g, 33,5 mmol), Verbindung 1-2 (CAS: 2408008-08-0) (10,0 g, 37,2 mmol), Tris(dibenzylidenaceton)dipalladium(0) (1,70 g, 1,86 mmol), Tri-t-butylphosphin (1,84 ml, 3,72 mmol, 50%ige Lösung in Toluol), Natrium-t-butoxid (7,15 g, 74,4 mmol) und 186 ml Toluol gegeben und 2 Stunden am Rückfluss erhitzt. Die Reaktionslösung wurde auf Raumtemperatur abgekühlt, am Rotationsverdampfer vom Lösungsmittel befreit und dann durch Säulenchromatographie gereinigt, was eine weiße feste Verbindung, C-86 (11,5 g, Ausbeute: 57 %) ergab.
-
In einen Kolben wurden Verbindung 1-1 (CAS: 373390-07-9) (11,2 g, 35,6 mmol), Verbindung 1-3 (CAS: 2305687-93-6) (10,0 g, 39,6 mmol), Tris(dibenzylidenaceton)dipalladium(0) (1,81 g, 1,98 mmol), Tri-t-butylphosphin (1,95 ml, 3,96 mmol, 50%ige Lösung in Toluol), Natrium-t-butoxid (7,61 g, 79,1 mmol) und 198 ml Toluol gegeben und 2 Stunden am Rückfluss erhitzt. Die Reaktionslösung wurde auf Raumtemperatur abgekühlt, am Rotationsverdampfer vom Lösungsmittel befreit und dann durch Säulenchromatographie gereinigt, was eine weiße feste Verbindung, C-111 (5,2 g, Ausbeute: 28 %) ergab.
-
In einen Kolben wurden Verbindung 1-1 (CAS: 373390-07-9) (10,0 g, 32,0 mmol), Verbindung 1-4 (CAS: 2397634-76-1) (9,7 g, 35,0 mmol), Tris(dibenzylidenaceton)dipalladium(0) (1,5 g, 1,60 mmol), Tri-t-butylphosphin (1,58 ml, 3,20 mmol, 50%ige Lösung in Toluol), Natrium-t-butoxid (6,15 g, 64,0 mmol) und 160 ml Toluol gegeben und 1 Stunde am Rückfluss erhitzt. Die Reaktionslösung wurde auf Raumtemperatur abgekühlt, am Rotationsverdampfer vom Lösungsmittel befreit und dann durch Säulenchromatographie gereinigt, was eine weiße feste Verbindung, C-1 (8,9 g, Ausbeute: 50 %) ergab.
-
In einen Kolben wurden Verbindung 1-1 (CAS: 373390-07-9) (8,0 g, 26,0 mmol), Verbindung 1-5 (CAS: 2412522-09-7) (12,3 g, 31,0 mmol), Tris(dibenzylidenaceton)dipalladium(0) (1,20 g, 1,30 mmol), Tri-t-butylphosphin (1,30 ml, 2,60 mmol, 50%ige Lösung in Toluol), Natrium-t-butoxid (4,9 g, 52,0 mmol) und 130 ml Toluol gegeben und 1 Stunde am Rückfluss erhitzt. Die Reaktionslösung wurde auf Raumtemperatur abgekühlt, am Rotationsverdampfer vom Lösungsmittel befreit und dann durch Säulenchromatographie gereinigt, was eine weiße feste Verbindung, C-36 (15,4 g, Ausbeute: 89 %) ergab.
| | HOMO | LUMO | Triplettenergie | Fp. (°C) | Tg (°C) |
| C-86 | -4,900 | -1,325 | 2,427 | 265 | 100 |
| C-111 | -4,883 | -1,198 | 2,481 | 204 | 90 |
| C-1 | -4,809 | -1,230 | 2,503 | 322 | 106 |
| C-36 | -4,775 | -1,257 | 2,369 | 266 | 127 |
-
In einen Kolben wurden Verbindung 1-6 (CAS: 1776936-11-8) (3,0 g, 9,33 mmol), Verbindung 1-7 (CAS: 1198396-39-2) (4,2 g, 13,1 mmol), Tris(dibenzylidenaceton)dipalladium(0) (0,43 g, 0,47 mmol), Tri-t-butylphosphin (0,45 ml, 0,93 mmol, 50%ige Lösung in Toluol), Natrium-t-butoxid (1,35 g, 14,0 mmol) und 48 ml Toluol gegeben und 1 Stunde am Rückfluss erhitzt. Die Reaktionslösung wurde auf Raumtemperatur abgekühlt, am Rotationsverdampfer vom Lösungsmittel befreit und dann durch Säulenchromatographie gereinigt, was eine weiße feste Verbindung, C-279 (5,3 g, Ausbeute: 98 %) ergab.
| | HOMO | LUMO | Triplettenergie | Fp. (°C) | Tg (°C) |
| C-279 | -4,848 | -1,177 | 2,419 | 234 | 106 |
-
Vorrichtungsbeispiel 1: Herstellung einer rotes Licht emittierenden OLED gemäß der vorliegenden Offenbarung
-
Es wurde eine OLED gemäß der vorliegenden Offenbarung hergestellt. Zunächst wurde eine transparente dünne Elektrodenschicht aus Indiumzinnoxid (ITO) (10 Ω/sq) auf einem Glassubstrat für eine OLED (GEOMATEC CO., LTD., Japan) nacheinander einer Ultraschallwäsche mit Aceton und Isopropylalkohol unterworfen und dann in Isopropylalkohol aufbewahrt. Das ITO-Substrat wurde auf einem Substrathalter einer Vakuumdampfabscheidungsapparatur befestigt. Die in Tabelle 2 gezeigt Verbindung HI-1 wurde als erste Lochinjektionsverbindung in eine Zelle der Vakuumdampfabscheidungsapparatur eingebracht, und die in Tabelle 2 gezeigte Verbindung HT-1 wurde als erste Lochtransportverbindung in eine andere Zelle eingebracht. Die beiden Materialien wurden mit verschiedenen Raten verdampft, und die erste Lochinjektionsverbindung wurde in einer Dotierungsmenge von 3 Gew.-%, bezogen auf die Gesamtmenge der ersten Lochinjektionsverbindung und der ersten Lochtransportverbindung, abgeschieden, um eine erste Lochinjektionsschicht mit einer Dicke von 10 nm zu bilden. Anschließend wurde Verbindung HT-1 auf der ersten Lochinjektionsschicht abgeschieden, um eine erste Lochtransportschicht mit einer Dicke von 90 nm zu bilden. Als Nächstes wurde die in Tabelle 2 gezeigte Verbindung C-86 als zweite Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine zweite Lochtransportschicht mit einer Dicke von 55 nm auf der ersten Lochtransportschicht abgeschieden wurde. Als Nächstes wurde die in Tabelle 2 gezeigte Verbindung H-31 als dritte Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine dritte Lochtransportschicht mit einer Dicke von 5 nm auf der zweiten Lochtransportschicht abgeschieden wurde. Nach der Bildung der Lochinjektionsschicht und der Lochtransportschichten wurde eine lichtemittierende Schicht wie folgt darauf abgeschieden: Verbindung A-1 und Verbindung B-1 wurden als Wirte für die lichtemittierende Schicht in zwei Zellen der Vakuumdampfabscheidungsapparatur eingetragen, und die Verbindung A-1 und die Verbindung B-1 wurden mit einer Rate von 1:1 verdampft. Nach Eintragen von Verbindung D-39 in eine andere Zelle als Dotierstoff wurde der Dotierstoff dann in einer Dotierungsmenge von 2 Gew.-%, bezogen auf die Gesamtmenge der Wirte und des Dotierstoffs, abgeschieden, um eine lichtemittierende Schicht mit einer Dicke von 40 nm auf der dritten Lochtransportschicht zu bilden. Anschließend wurde Verbindung B-2 bis zu einer Dicke von 5 nm als Elektronenpuffermaterial auf der lichtemittierenden Schicht abgeschieden. Dann wurden Verbindung ET-1 und Verbindung EI-1 in einem Gewichtsverhältnis von 5:5 als Elektronentransportschicht dotiert und bis zu einer Dicke von 30 nm abgeschieden. Nach der Abscheidung von Verbindung EI-1 als Elektroneninjektionsschicht mit einer Dicke von 2 nm auf der Elektronentransportschicht wurde unter Verwendung einer weiteren Vakuumdampfabscheidungsapparatur eine Al-Kathode mit einer Dicke von 80 nm auf der Elektroneninjektionsschicht abgeschieden, was eine OLED ergab.
-
Vorrichtungsbeispiele 2 und 3: Herstellung von rotes Licht emittierenden OLEDs gemäß der vorliegenden Offenbarung
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 1 hergestellt, außer dass die in Tabelle 2 gezeigten Verbindungen C-111 und C-1 in der zweiten Lochtransportschicht als zweite Lochtransportverbindungen anstelle von Verbindung C-86 verwendet wurden.
-
Vorrichtungsbeispiel 4: Herstellung einer rotes Licht emittierenden OLED gemäß der vorliegenden Offenbarung
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 1 hergestellt, außer dass die in Tabelle 2 gezeigte Verbindung C-36 in der zweiten Lochtransportschicht als zweite Lochtransportverbindung anstelle von Verbindung C-86 verwendet wurde und die in Tabelle 2 gezeigte Verbindung H-1 in der dritten Lochtransportschicht als dritte Lochtransportverbindung anstelle von Verbindung H-31 verwendet wurde.
-
Vergleichsbeispiel 1: Herstellung einer rotes Licht emittierenden OLED, die nicht der vorliegenden Offenbarung entspricht
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 1 hergestellt, außer dass eine einzige Verbindung H-31 mit 60 nm abgeschieden wurde, statt jede Verbindung in der zweiten und dritten Lochtransportschicht zu verwenden.
-
Vergleichsbeispiel 2: Herstellung einer rotes Licht emittierenden OLED, die nicht der vorliegenden Offenbarung entspricht
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 1 hergestellt, außer dass eine einzige Verbindung H-1 mit 60 nm abgeschieden wurde, statt jede Verbindung in der zweiten und dritten Lochtransportschicht zu verwenden.
-
Die Treiberspannung, die Stromeffizienz und die CIE-Farbkoordinaten bei einer Leuchtdichte von 1000 Nits für die OLED-Vorrichtungen der Vorrichtungsbeispiele 1 bis 4 und der Vergleichsbeispiele 1 und 2, die wie oben beschrieben hergestellt wurden, wurden gemessen, und die Ergebnisse sind in der folgenden Tabelle 1 gezeigt. [Tabelle 1]
| | Zweite Lochtransportschicht | Dritte Lochtransportschicht | Treiberspannung (V) | Stromeffizienz (cd/A) | CIE-Farbkoordinaten (x, y) |
| Vorrichtungsbeispiel 1 | C-86 | H-31 | 3,4 | 30,1 | (0,661,0,339) |
| Vorrichtungsbeispiel 2 | C-111 | H-31 | 3,8 | 32,2 | (0,661,0,339) |
| Vorrichtungsbeispiel 3 | C-1 | H-31 | 2,9 | 31,8 | (0,661,0,339) |
| Vergleichsbeispiel 1 | H-31 | 5,6 | 28,6 | (0,661,0,339) |
| Vorrichtungsbeispiel 4 | C-36 | H-1 | 2,7 | 30,2 | (0,661,0,338) |
| Vergleichsbeispiel 2 | H-1 | 4,6 | 29,1 | (0,661,0,339) |
-
Aus obiger Tabelle 1 ist ersichtlich, dass die OLEDs gemäß der vorliegenden Offenbarung eine niedrige Treiberspannung und eine hohe Stromeffizienz im Vergleich zu den OLEDs, bei denen die herkömmliche Verbindung in der zweiten und dritten Lochtransportschicht verwendet wird, aufweisen.
-
Die in den Vorrichtungsbeispielen 1 bis 4 und den Vergleichsbeispielen 1 und 2 verwendeten Verbindungen sind in nachstehender Tabelle 2 gezeigt. [Tabelle 2]
| Lochinjektionsschicht/ Lochtransportschicht | |
| Lichtemittierende Schicht | |
| Elektronenpufferschicht/ Elektronentransportschicht/Elektroneninjektionsschicht | |
-
Vorrichtungsbeispiel 5: Herstellung einer rotes Licht emittierenden OLED gemäß der vorliegenden Offenbarung
-
Es wurde eine OLED gemäß der vorliegenden Offenbarung hergestellt. Zunächst wurde eine transparente dünne Elektrodenschicht aus Indiumzinnoxid (ITO) (10 Ω/sq) auf einem Glassubstrat für eine OLED (GEOMATEC CO., LTD., Japan) nacheinander einer Ultraschallwäsche mit Aceton und Isopropylalkohol unterworfen und dann in Isopropylalkohol aufbewahrt. Das ITO-Substrat wurde auf einem Substrathalter einer Vakuumdampfabscheidungsapparatur befestigt. Die in Tabelle 4 gezeigte Verbindung HI-1 wurde als erste Lochinjektionsverbindung in eine Zelle der Vakuumdampfabscheidungsapparatur eingebracht, und die in Tabelle 4 gezeigte Verbindung HT-2 wurde als erste Lochtransportverbindung in eine andere Zelle eingebracht. Die beiden Materialien wurden mit verschiedenen Raten verdampft, und die erste Lochinjektionsverbindung wurde in einer Dotierungsmenge von 5 Gew.-%, bezogen auf die Gesamtmenge der ersten Lochinjektionsverbindung und der ersten Lochtransportverbindung, abgeschieden, um eine erste Lochinjektionsschicht mit einer Dicke von 10 nm zu bilden. Anschließend wurde Verbindung HT-2 auf der ersten Lochinjektionsschicht abgeschieden, um eine erste Lochtransportschicht mit einer Dicke von 90 nm zu bilden. Als Nächstes wurde die in Tabelle 4 gezeigte Verbindung C-279 als zweite Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine zweite Lochtransportschicht mit einer Dicke von 60 nm auf der ersten Lochtransportschicht abgeschieden wurde. Als Nächstes wurde die in Tabelle 4 gezeigte Verbindung H-56 als dritte Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine dritte Lochtransportschicht mit einer Dicke von 7,5 nm auf der zweiten Lochtransportschicht abgeschieden wurde. Nach der Bildung der Lochinjektionsschicht und der Lochtransportschichten wurde eine lichtemittierende Schicht wie folgt darauf abgeschieden: Verbindung A-2 und Verbindung B-1 wurden als Wirte für die lichtemittierende Schicht in zwei Zellen der Vakuumdampfabscheidungsapparatur eingetragen, und die Verbindung A-2 und die Verbindung B-1 wurden mit einer Rate von 1:1 verdampft. Nach Eintragen von Verbindung D-39 in eine andere Zelle als Dotierstoff wurde der Dotierstoff dann in einer Dotierungsmenge von 2 Gew.-%, bezogen auf die Gesamtmenge der Wirte und des Dotierstoffs, abgeschieden, um eine lichtemittierende Schicht mit einer Dicke von 36 nm auf der dritten Lochtransportschicht zu bilden. Anschließend wurde Verbindung B-3 bis zu einer Dicke von 5 nm als Elektronenpuffermaterial auf der lichtemittierenden Schicht abgeschieden. Dann wurden Verbindung ET-2 und Verbindung EI-1 in einem Gewichtsverhältnis von 2:1 als Elektronentransportschicht dotiert und bis zu einer Dicke von 25 nm abgeschieden. Nach der Abscheidung von Verbindung EI-1 als Elektroneninjektionsschicht mit einer Dicke von 2 nm auf der Elektronentransportschicht wurde unter Verwendung einer weiteren Vakuumdampfabscheidungsapparatur eine Al-Kathode mit einer Dicke von 80 nm auf der Elektroneninjektionsschicht abgeschieden, was eine OLED ergab.
-
Vorrichtungsbeispiel 6: Herstellung einer rotes Licht emittierenden OLED gemäß der vorliegenden Offenbarung
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 5 hergestellt, außer dass die in Tabelle 4 gezeigte Verbindung A-3 in der lichtemittierenden Schicht als lichtemittierende Verbindung anstelle von Verbindung A-2 verwendet wurde.
-
Vergleichsbeispiel 3: Herstellung einer rotes Licht emittierenden OLED, die nicht der vorliegenden Offenbarung entspricht
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 5 hergestellt, außer dass eine einzige Verbindung H-56 mit 67,5 nm abgeschieden wurde, statt jede Verbindung in der zweiten und dritten Lochtransportschicht zu verwenden.
-
Vergleichsbeispiel 4: Herstellung einer rotes Licht emittierenden OLED, die nicht der vorliegenden Offenbarung entspricht
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 5 hergestellt, außer dass eine einzige Verbindung H-56 bei 67,5 nm abgeschieden wurde, statt jede Verbindung in der zweiten und dritten Lochtransportschicht zu verwenden, und die in Tabelle 4 gezeigte Verbindung A-3 in der lichtemittierenden Schicht als lichtemittierende Verbindung anstelle von Verbindung A-2 verwendet wurde.
-
Die Treiberspannung, die Stromeffizienz und die CIE-Farbkoordinaten bei einer Leuchtdichte von 1000 Nits für die OLED-Vorrichtungen der Vorrichtungsbeispiele 5 und 6 und der Vergleichsbeispiele 3 und 4, die wie oben beschrieben hergestellt wurden, wurden gemessen, und die Ergebnisse sind in der folgenden Tabelle 3 gezeigt. [Tabelle 3]
| | Zweite Lochtransportschicht | Dritte Lochtransportschicht | Lichtemittierender Wirt | Treiberspannung (V) | Stromeffizienz (cd/A) | CIE-Farbkoordinaten (x, y) |
| Vorrichtungsbeispiel 5 | C-279 | H-56 | A-2:B-1 | 2,9 | 29,2 | (0,661,0,338) |
| Vergleichsbeispiel 3 | H-56 | A-2:B-1 | 3,9 | 28,4 | (0,662,0,338) |
| Vorrichtungsbeispiel 6 | C-279 | H-56 | A-3:B-1 | 2,9 | 28,6 | (0,661,0,338) |
| Vergleichsbeispiel 4 | H-56 | A-3:B-1 | 3,9 | 27,6 | (0,662,0,338) |
-
Aus obiger Tabelle 3 ist ersichtlich, dass die OLEDs gemäß der vorliegenden Offenbarung eine niedrige Treiberspannung und eine hohe Stromeffizienz im Vergleich zu den OLEDs, bei denen die herkömmliche Verbindung in der zweiten und dritten Lochtransportschicht verwendet wird, aufweisen.
-
Die in den Vorrichtungsbeispielen 5 und 6 und den Vergleichsbeispielen 3 und 4 verwendeten Verbindungen sind in nachstehender Tabelle 4 gezeigt. [Tabelle 4]
| Lochinjektionsschicht/Lochtransportschicht | |
| Lichtemittierende Schicht | |
| Elektronenpufferschicht/Elektronentransportschicht/Elektroneninjektionsschicht | |
| | |
-
Vorrichtungsbeispiel 7: Herstellung einer rotes Licht emittierenden OLED gemäß der vorliegenden Offenbarung
-
Es wurde eine OLED gemäß der vorliegenden Offenbarung hergestellt. Zunächst wurde eine transparente dünne Elektrodenschicht aus Indiumzinnoxid (ITO) (10 Ω/sq) auf einem Glassubstrat für eine OLED (GEOMATEC CO., LTD., Japan) nacheinander einer Ultraschallwäsche mit Aceton und Isopropylalkohol unterworfen und dann in Isopropylalkohol aufbewahrt. Das ITO-Substrat wurde auf einem Substrathalter einer Vakuumdampfabscheidungsapparatur befestigt. Die in Tabelle 6 gezeigt Verbindung HI-1 wurde als erste Lochinjektionsverbindung in eine Zelle der Vakuumdampfabscheidungsapparatur eingebracht, und die in Tabelle 6 gezeigt Verbindung HT-1 wurde als erste Lochtransportverbindung in eine andere Zelle eingebracht. Die beiden Materialien wurden mit verschiedenen Raten verdampft, und die erste Lochinjektionsverbindung wurde in einer Dotierungsmenge von 3 Gew.-%, bezogen auf die Gesamtmenge der ersten Lochinjektionsverbindung und der ersten Lochtransportverbindung, abgeschieden, um eine erste Lochinjektionsschicht mit einer Dicke von 10 nm zu bilden. Anschließend wurde Verbindung HT-1 auf der ersten Lochinjektionsschicht abgeschieden, um eine erste Lochtransportschicht mit einer Dicke von 90 nm zu bilden. Als Nächstes wurde die in Tabelle 6 gezeigte Verbindung C-1 als zweite Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine zweite Lochtransportschicht mit einer Dicke von 55 nm auf der ersten Lochtransportschicht abgeschieden wurde. Als Nächstes wurde die in Tabelle 6 gezeigte Verbindung H-13 als dritte Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine dritte Lochtransportschicht mit einer Dicke von 5 nm auf der zweiten Lochtransportschicht abgeschieden wurde. Nach der Bildung der Lochinjektionsschicht und der Lochtransportschichten wurde eine lichtemittierende Schicht wie folgt darauf abgeschieden: Verbindung A-1 und Verbindung B-1 wurden als Wirte für die lichtemittierende Schicht in zwei Zellen der Vakuumdampfabscheidungsapparatur eingetragen, und die Verbindung A-1 und die Verbindung B-1 wurden mit einer Rate von 4:6 verdampft. Nach Eintragen von Verbindung D-39 in eine andere Zelle als Dotierstoff wurde der Dotierstoff dann in einer Dotierungsmenge von 2 Gew.-%, bezogen auf die Gesamtmenge der Wirte und des Dotierstoffs, abgeschieden, um eine lichtemittierende Schicht mit einer Dicke von 40 nm auf der dritten Lochtransportschicht zu bilden. Anschließend wurde Verbindung B-2 bis zu einer Dicke von 5 nm als Elektronenpuffermaterial auf der lichtemittierenden Schicht abgeschieden. Dann wurden Verbindung ET-1 und Verbindung EI-1 in einem Gewichtsverhältnis von 5:5 als Elektronentransportschicht dotiert und bis zu einer Dicke von 30 nm abgeschieden. Nach der Abscheidung von Verbindung EI-1 als Elektroneninjektionsschicht mit einer Dicke von 2 nm auf der Elektronentransportschicht wurde unter Verwendung einer weiteren Vakuumdampfabscheidungsapparatur eine Al-Kathode mit einer Dicke von 80 nm auf der Elektroneninjektionsschicht abgeschieden, was eine OLED ergab.
-
Vorrichtungsbeispiele 8 und 9: Herstellung von rotes Licht emittierenden OLEDs gemäß der vorliegenden Offenbarung
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 7 hergestellt, außer dass jede in Tabelle 5 gezeigte Verbindung H-5 und H-114 in der dritten Lochtransportschicht als dritte Lochtransportverbindung anstelle von Verbindung H-13 verwendet wurde.
-
Die Treiberspannung, die Stromeffizienz und die CIE-Farbkoordinaten bei einer Leuchtdichte von 1000 Nits für die OLED-Vorrichtungen der Vorrichtungsbeispiele 7 bis 9, die wie oben beschrieben hergestellt wurden, wurden gemessen, und die Ergebnisse sind in der folgenden Tabelle 5 gezeigt. [Tabelle 5]
| | Zweite Lochtransportschicht | Dritte Lochtransportschicht | Treiberspannung (V) | Stromeffizienz (cd/A) | CIE-Farbkoordinaten (x, y) |
| Vorrichtungsbeispiel 7 | C-1 | H-13 | 2,8 | 33,4 | (0,657,0,342) |
| Vorrichtungsbeispiel 8 | C-1 | H-5 | 2,8 | 32,6 | (0,659,0,340) |
| Vorrichtungsbeispiel 9 | C-1 | H-114 | 2,8 | 33,2 | (0,658,0,341) |
-
Aus obiger Tabelle 5 ist ersichtlich, dass die OLEDs gemäß der vorliegenden Offenbarung eine niedrige Treiberspannung und eine hohe Stromeffizienz aufweisen.
-
Die in den Vorrichtungsbeispielen 7 bis 9 verwendeten Verbindungen sind in nachstehender Tabelle 6 gezeigt. [Tabelle 6]
| Lochinjektionsschicht/Lochtransportschicht | |
| Lichtemittierende Schicht | |
| Elektronenpufferschicht/ Elektronentransportschicht/ Elektroneninjektionsschicht | |
-
Vorrichtungsbeispiel 10: Herstellung einer rotes Licht emittierenden OLED gemäß der vorliegenden Offenbarung
-
Es wurde eine OLED gemäß der vorliegenden Offenbarung hergestellt. Zunächst wurde eine transparente dünne Elektrodenschicht aus Indiumzinnoxid (ITO) (10 Ω/sq) auf einem Glassubstrat für eine OLED (GEOMATEC CO., LTD., Japan) nacheinander einer Ultraschallwäsche mit Aceton und Isopropylalkohol unterworfen und dann in Isopropylalkohol aufbewahrt. Das ITO-Substrat wurde auf einem Substrathalter einer Vakuumdampfabscheidungsapparatur befestigt. Die in Tabelle 8 gezeigt Verbindung HI-1 wurde als erste Lochinjektionsverbindung in eine Zelle der Vakuumdampfabscheidungsapparatur eingebracht, und die in Tabelle 8 gezeigte Verbindung HT-1 wurde als erste Lochtransportverbindung in eine andere Zelle eingebracht. Die beiden Materialien wurden mit verschiedenen Raten verdampft, und die erste Lochinjektionsverbindung wurde in einer Dotierungsmenge von 3 Gew.-%, bezogen auf die Gesamtmenge der ersten Lochinjektionsverbindung und der ersten Lochtransportverbindung, abgeschieden, um eine erste Lochinjektionsschicht mit einer Dicke von 10 nm zu bilden. Anschließend wurde Verbindung HT-1 auf der ersten Lochinjektionsschicht abgeschieden, um eine erste Lochtransportschicht mit einer Dicke von 90 nm zu bilden. Als Nächstes wurde die in Tabelle 8 gezeigte Verbindung C-351 als zweite Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine zweite Lochtransportschicht mit einer Dicke von 55 nm auf der ersten Lochtransportschicht abgeschieden wurde. Als Nächstes wurde die in Tabelle 8 gezeigte Verbindung H-5 als dritte Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine dritte Lochtransportschicht mit einer Dicke von 5 nm auf der zweiten Lochtransportschicht abgeschieden wurde. Nach der Bildung der Lochinjektionsschicht und der Lochtransportschichten wurde eine lichtemittierende Schicht wie folgt darauf abgeschieden: Verbindung A-1 und Verbindung B-1 wurden als Wirte für die lichtemittierende Schicht in zwei Zellen der Vakuumdampfabscheidungsapparatur eingetragen, und die Verbindung A-1 und die Verbindung B-1 wurden mit einer Rate von 1:1 verdampft. Nach Eintragen von Verbindung D-39 in eine andere Zelle als Dotierstoff wurde der Dotierstoff dann in einer Dotierungsmenge von 2 Gew.-%, bezogen auf die Gesamtmenge der Wirte und des Dotierstoffs, abgeschieden, um eine lichtemittierende Schicht mit einer Dicke von 40 nm auf der dritten Lochtransportschicht zu bilden. Anschließend wurde Verbindung B-2 bis zu einer Dicke von 5 nm als Elektronenpuffermaterial auf der lichtemittierenden Schicht abgeschieden. Dann wurden Verbindung ET-1 und Verbindung EI-1 in einem Gewichtsverhältnis von 5:5 als Elektronentransportschicht dotiert und bis zu einer Dicke von 30 nm abgeschieden. Nach der Abscheidung von Verbindung EI-1 als Elektroneninjektionsschicht mit einer Dicke von 2 nm auf der Elektronentransportschicht wurde unter Verwendung einer weiteren Vakuumdampfabscheidungsapparatur eine Al-Kathode mit einer Dicke von 80 nm auf der Elektroneninjektionsschicht abgeschieden, was eine OLED ergab.
-
Vorrichtungsbeispiele 11 und 12: Herstellung von rotes Licht emittierenden OLEDs gemäß der vorliegenden Offenbarung
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 10 hergestellt, außer dass jede in Tabelle 7 gezeigte Verbindung C-164 und C-163 in der zweiten Lochtransportschicht als zweite Lochtransportverbindung anstelle von Verbindung C-351 verwendet wurde.
-
Die Treiberspannung, die Stromeffizienz und die CIE-Farbkoordinaten bei einer Leuchtdichte von 1000 Nits für die OLED-Vorrichtungen der Vorrichtungsbeispiele 10 bis 12, die wie oben beschrieben hergestellt wurden, wurden gemessen, und die Ergebnisse sind in der folgenden Tabelle 7 gezeigt. [Tabelle 7]
| | Zweite Lochtransportschicht | Dritte Lochtransportschicht | Treiberspannung (V) | Stromeffizienz (cd/A) | CIE-Farbkoordinaten (x, y) |
| Vorrichtungsbeispiel 10 | C-351 | H-5 | 2,9 | 32,5 | (0,660,0,339) |
| Vorrichtungsbeispiel 11 | C-164 | H-5 | 2,9 | 31,3 | (0,660,0,339) |
| Vorrichtungsbeispiel 12 | C-163 | H-5 | 2,7 | 31,7 | (0,660,0,339) |
-
Aus obiger Tabelle 7 ist ersichtlich, dass die OLEDs gemäß der vorliegenden Offenbarung eine niedrige Treiberspannung und eine hohe Stromeffizienz aufweisen.
-
Die in den Vorrichtungsbeispielen 10 bis 12 verwendeten Verbindungen sind in nachstehender Tabelle 8 gezeigt. [Tabelle 8]
| Lochinjektionsschicht/ Lochtransportschicht | |
| Lichtemittierende Schicht | |
| Elektronenpufferschicht/ Elektronentransportschicht/Elektroneninjektionsschicht | |
-
Vorrichtungsbeispiel 13: Herstellung einer rotes Licht emittierenden OLED gemäß der vorliegenden Offenbarung
-
Es wurde eine OLED gemäß der vorliegenden Offenbarung hergestellt. Zunächst wurde eine transparente dünne Elektrodenschicht aus Indiumzinnoxid (ITO) (10 Ω/sq) auf einem Glassubstrat für eine OLED (GEOMATEC CO., LTD., Japan) nacheinander einer Ultraschallwäsche mit Aceton und Isopropylalkohol unterworfen und dann in Isopropylalkohol aufbewahrt. Das ITO-Substrat wurde auf einem Substrathalter einer Vakuumdampfabscheidungsapparatur befestigt. Die in Tabelle 10 gezeigt Verbindung HI-1 wurde als erste Lochinjektionsverbindung in eine Zelle der Vakuumdampfabscheidungsapparatur eingebracht, und die in Tabelle 10 gezeigte Verbindung HT-2 wurde als erste Lochtransportverbindung in eine andere Zelle eingebracht. Die beiden Materialien wurden mit verschiedenen Raten verdampft, und die erste Lochinjektionsverbindung wurde in einer Dotierungsmenge von 5 Gew.-%, bezogen auf die Gesamtmenge der ersten Lochinjektionsverbindung und der ersten Lochtransportverbindung, abgeschieden, um eine erste Lochinjektionsschicht mit einer Dicke von 10 nm zu bilden. Anschließend wurde Verbindung HT-2 auf der ersten Lochinjektionsschicht abgeschieden, um eine erste Lochtransportschicht mit einer Dicke von 90 nm zu bilden. Als Nächstes wurde die in Tabelle 10 gezeigte Verbindung C-272 als zweite Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine zweite Lochtransportschicht mit einer Dicke von 60 nm auf der ersten Lochtransportschicht abgeschieden wurde. Als Nächstes wurde die in Tabelle 10 gezeigte Verbindung H-56 als dritte Lochtransportverbindung in eine andere Zelle der Vakuumdampfabscheidungsapparatur eingebracht und durch Anlegen eines elektrischen Stroms an die Zelle verdampft, wodurch eine dritte Lochtransportschicht mit einer Dicke von 7,5 nm auf der zweiten Lochtransportschicht abgeschieden wurde. Nach der Bildung der Lochinjektionsschicht und der Lochtransportschichten wurde eine lichtemittierende Schicht wie folgt darauf abgeschieden: Verbindung A-2 und Verbindung B-1 wurden als Wirte für die lichtemittierende Schicht in zwei Zellen der Vakuumdampfabscheidungsapparatur eingetragen, und die Verbindung A-2 und die Verbindung B-1 wurden mit einer Rate von 1:1 verdampft. Nach Eintragen von Verbindung D-39 in eine andere Zelle als Dotierstoff wurde der Dotierstoff dann in einer Dotierungsmenge von 2 Gew.-%, bezogen auf die Gesamtmenge der Wirte und des Dotierstoffs, abgeschieden, um eine lichtemittierende Schicht mit einer Dicke von 36 nm auf der dritten Lochtransportschicht zu bilden. Anschließend wurde Verbindung B-3 bis zu einer Dicke von 5 nm als Elektronenpuffermaterial auf der lichtemittierenden Schicht abgeschieden. Dann wurden Verbindung ET-2 und Verbindung EI-1 in einem Gewichtsverhältnis von 2:1 als Elektronentransportschicht dotiert und bis zu einer Dicke von 25 nm abgeschieden. Nach der Abscheidung von Verbindung EI-1 als Elektroneninjektionsschicht mit einer Dicke von 2 nm auf der Elektronentransportschicht wurde unter Verwendung einer weiteren Vakuumdampfabscheidungsapparatur eine Al-Kathode mit einer Dicke von 80 nm auf der Elektroneninjektionsschicht abgeschieden, was eine OLED ergab.
-
Vorrichtungsbeispiele 14 bis 23: Herstellung von rotes Licht emittierenden OLEDs gemäß der vorliegenden Offenbarung
-
Eine OLED wurde auf die gleiche Weise wie in Vorrichtungsbeispiel 13 hergestellt, außer dass jede in Tabelle 9 gezeigte Verbindung in der zweiten Lochtransportschicht als zweite Lochtransportverbindung anstelle von Verbindung C-272 verwendet wurde.
-
Die Treiberspannung, die Stromeffizienz und die CIE-Farbkoordinaten bei einer Leuchtdichte von 1000 Nits für die OLED-Vorrichtungen der Vorrichtungsbeispiele 10 bis 12, die wie oben beschrieben hergestellt wurden, wurden gemessen, und die Ergebnisse sind in der folgenden Tabelle 9 gezeigt. [Tabelle 9]
| | Zweite Lochtransportschicht | Dritte Lochtransportschicht | Lichtemittierender Wirt | Treiberspannung (V) | Stromeffizienz (cd/A) | CIE-Farbkoordinaten (x, y) |
| Vorrichtungsbeispiel 13 | C-272 | H-56 | A-2:B-1 | 3,0 | 29,5 | (0,662,0,338) |
| Vorrichtungsbeispiel 14 | C-347 | H-56 | A-2:B-1 | 3,2 | 29,4 | (0,662,0,337) |
| Vorrichtungsbeispiel 15 | C-11 | H-56 | A-2:B-1 | 2,9 | 30,0 | (0,662,0,338) |
| Vorrichtungsbeispiel 16 | C-257 | H-56 | A-2:B-1 | 3,0 | 30,6 | (0,661,0,338) |
| Vorrichtungsbeispiel 17 | C-252 | H-56 | A-2:B-1 | 2,9 | 29,6 | (0,662,0,338) |
| Vorrichtungsbeispiel 18 | C-18 | H-56 | A-2:B-1 | 3,0 | 30,9 | (0,662,0,338) |
| Vorrichtungsbeispiel 19 | C-381 | H-56 | A-2:B-1 | 2,9 | 30,6 | (0,662,0,338) |
| Vorrichtungsbeispiel 20 | C-382 | H-56 | A-2:B-1 | 2,9 | 31,3 | (0,662,0,338) |
| Vorrichtungsbeispiel 21 | C-383 | H-56 | A-2:B-1 | 2,8 | 29,5 | (0,662,0,338) |
| Vorrichtungsbeispiel 22 | C-384 | H-56 | A-2:B-1 | 2,9 | 30,2 | (0,662,0,338) |
| Vorrichtungsbeispiel 23 | C-385 | H-56 | A-2:B-1 | 2,9 | 30,8 | (0,661,0,338) |
-
Aus obiger Tabelle 9 ist ersichtlich, dass die OLEDs gemäß der vorliegenden Offenbarung eine niedrigere Treiberspannung und eine hohe Stromeffizienz aufweisen.
-
Die in den Vorrichtungsbeispielen 13 bis 23 verwendeten Verbindungen sind in nachstehender Tabelle 10 gezeigt. [Tabelle 10]
| Lochinjektionsschicht/ Lochtransportschicht | |
| | |
| Lichtemittierende Schicht | |
| Elektronenpufferschicht/ Elektronentransportschicht/Elektroneninjektionsschicht | |
| | |
-
ZITATE ENTHALTEN IN DER BESCHREIBUNG
-
Diese Liste der vom Anmelder aufgeführten Dokumente wurde automatisiert erzeugt und ist ausschließlich zur besseren Information des Lesers aufgenommen. Die Liste ist nicht Bestandteil der deutschen Patent- bzw. Gebrauchsmusteranmeldung. Das DPMA übernimmt keinerlei Haftung für etwaige Fehler oder Auslassungen.
-
Zitierte Patentliteratur
-
- JP 2023-021983 [0005]
- KR 2015-0066202 [0074]
- KR 2015-0076129 [0074]
- KR 2017-0043439 [0074]
- KR 2019-0090695 [0074]
- KR 2020-0004257 [0074]
- KR 2020-0018275 [0074]
- KR 2020-0090091 [0074]
-
Zitierte Nicht-Patentliteratur
-
- Appl. Phys. Lett. 51, 913, 1987 [0002]